文档内容
1.菜谱中记载:河虾不宜与西红柿同食。主要原因是河虾中含有+5价砷,西红柿中含有
比较多的维生素C,两者同食时会生成有毒的+3价砷。下列说法正确的是( )
A.在该反应中维生素C作氧化剂
B.由上述信息可推知砒霜(As O)有毒
2 3
C.因为河虾中含有砷元素,所以不能食用
D.上述反应中河虾中的+5价砷被氧化
2.碲(Te)广泛用于彩色玻璃和陶瓷。工业上用精炼铜的阳极泥(含有质量分数为 8%的
TeO 、少量Ag、Au)为原料制备单质碲的一种工艺流程如下(已知TeO 微溶于水,易溶于强
2 2
酸和强碱),下列有关说法不正确的是( )
A.将阳极泥研磨、反应适当加热都有利于提高“碱浸”的速率和效率
B.“碱浸”时发生主要反应的离子方程式为TeO +2OH-===TeO+HO
2 2
C.“沉碲”时为使碲元素沉淀充分,应加入过量的硫酸
D.若提取过程碲元素的回收率为90%,则处理1 kg这种阳极泥最少需通入标准状况下SO
2
20.16 L
3.纯磷酸可通过市售85%磷酸溶液减压蒸馏除水、结晶除杂得到。制备纯磷酸的实验装置
如图所示(夹持装置略)。已知:纯磷酸熔点为42 ℃,磷酸纯化过程需要严格控制温度和水
分,温度低于21 ℃易形成杂质2HPO ·H O(熔点为30 ℃),高于100 ℃则发生分子间脱水
3 4 2
生成焦磷酸等。
下列说法错误的是( )
A.装置m不能用球形冷凝管代替
B.实验选用水浴加热的目的包括使溶液受热均匀
C.磷酸过滤时需要控制温度低于20 ℃
D.磷酸中少量的水极难除去的原因是磷酸与水形成分子间氢键
4.一种处理强酸性高浓度砷(AsO)、Cu2+废液并回收As O 和海绵铜等的工艺流程如图:
2 3下列说法正确的是( )
A.试剂X可以是FeO
B.加入NaHSO 发生反应后溶液的酸性增强
3
C.加入HO 的主要目的是将过量NaHSO 氧化成NaSO
2 2 3 2 4
D.达标废液中含有的溶质主要为NaSO
2 4
5.硒是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。粗硒经过下
列流程可获得亚硒酸钠(Na SeO)。请回答下列问题:
2 3
(1)硒与硫是同主族的相邻元素,NaSeO 中硒的化合价为______,硒元素在周期表中的位置
2 3
为________________。
(2)已知在氧化器中粗硒转化为 SeO ,则搅拌槽中发生主要反应的离子方程式为
2
_______________________________________________________________________________
_______________________________________________________________________________
。
(3)由滤液获取 NaSeO·5H O 晶体的操作为__________________、过滤、洗涤。
2 3 2
NaSeO·5H O 脱 水 制 取 NaSeO 时 , 须 在 真 空 箱 中 进 行 , 原 因 是
2 3 2 2 3
___________________________________
_______________________________________________________________________________
。
(4)吸入人体内的O 有2%转化为氧化性极强的“活性氧(O)”,它能加速人体衰老,被称为
2
“生命杀手”。服用亚硒酸钠(Na SeO)能消除人体内的活性氧(O)。由此判断下列说法正确
2 3
的是________(填字母)。
A.活性氧发生氧化反应
B.NaSeO 具有氧化性
2 3
C.NaSeO 在反应中作还原剂
2 3D.活性氧化合价升高
(5)硒酸(H SeO)是中强酸,水溶液中的电离方程式为HSeO===H++HSeO,HSeOH++
2 4 2 4
SeO。25 ℃时,1 mol·L-1的 HSeO 溶液中,HSeO 的电离度为 α,则其电离常数 K=
2 4
__________(用含α的计算式表示,忽略水的电离)。
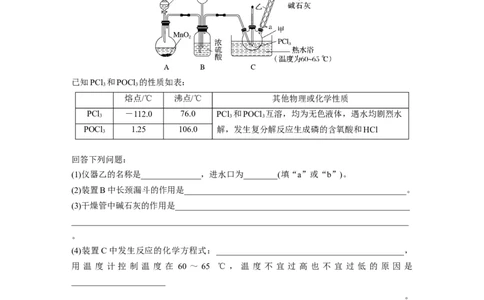
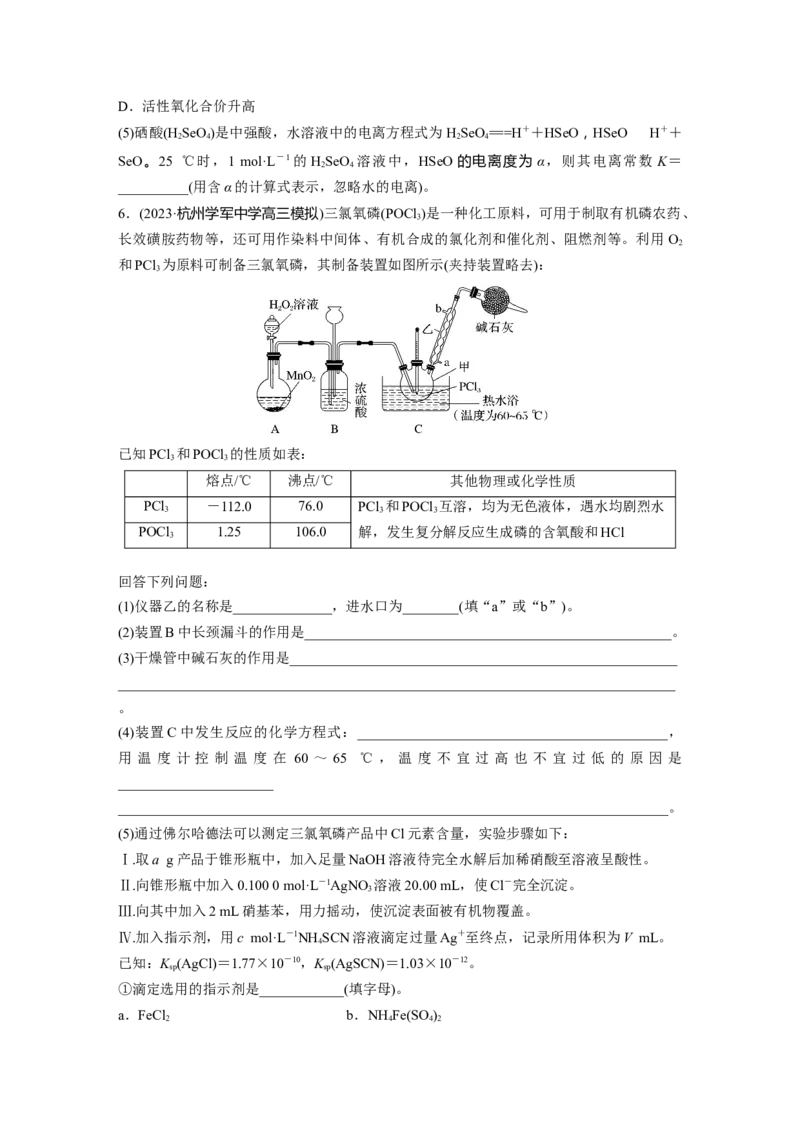
6.(2023·杭州学军中学高三模拟)三氯氧磷(POCl )是一种化工原料,可用于制取有机磷农药、
3
长效磺胺药物等,还可用作染料中间体、有机合成的氯化剂和催化剂、阻燃剂等。利用 O
2
和PCl 为原料可制备三氯氧磷,其制备装置如图所示(夹持装置略去):
3
已知PCl 和POCl 的性质如表:
3 3
熔点/℃ 沸点/℃ 其他物理或化学性质
PCl -112.0 76.0 PCl 和POCl 互溶,均为无色液体,遇水均剧烈水
3 3 3
POCl 1.25 106.0 解,发生复分解反应生成磷的含氧酸和HCl
3
回答下列问题:
(1)仪器乙的名称是______________,进水口为________(填“a”或“b”)。
(2)装置B中长颈漏斗的作用是____________________________________________________。
(3)干燥管中碱石灰的作用是_______________________________________________________
_______________________________________________________________________________
。
(4)装置C中发生反应的化学方程式:____________________________________________,
用 温 度 计 控 制 温 度 在 60 ~ 65 ℃ , 温 度 不 宜 过 高 也 不 宜 过 低 的 原 因 是
______________________
______________________________________________________________________________。
(5)通过佛尔哈德法可以测定三氯氧磷产品中Cl元素含量,实验步骤如下:
Ⅰ.取a g产品于锥形瓶中,加入足量NaOH溶液待完全水解后加稀硝酸至溶液呈酸性。
Ⅱ.向锥形瓶中加入0.100 0 mol·L-1AgNO 溶液20.00 mL,使Cl-完全沉淀。
3
Ⅲ.向其中加入2 mL硝基苯,用力摇动,使沉淀表面被有机物覆盖。
Ⅳ.加入指示剂,用c mol·L-1NH SCN溶液滴定过量Ag+至终点,记录所用体积为V mL。
4
已知:K (AgCl)=1.77×10-10,K (AgSCN)=1.03×10-12。
sp sp
①滴定选用的指示剂是____________(填字母)。
a.FeCl b.NH Fe(SO )
2 4 4 2c.淀粉 d.甲基橙
②实验过程中加入硝基苯的目的是_________________________________________________
_______________________________________________________________________________
。
③所测Cl元素含量为_____________________________________________________(列出表
达式)。
7.NaSbF (六氟锑酸钠)是光化学反应的催化剂。我国科学家开发一种以锑矿(主要含
6
Sb O、Sb S,还含少量Sb O、Fe O、CuO等)为原料制备NaSbF 的工艺流程如图所示。
2 3 2 3 2 5 2 3 6
已知:① Sb 的氧化物及氢氧化物的性质与 Al 的类似,Sb S 溶于 NaOH 浓溶液;
2 3
②NaSbO ·3H O难溶于水,NaSbF 易溶于水;③常温下,K (CuS)=6.0×10-36。
3 2 6 sp
回答下列问题:
(1)NaSbF 的组成元素中第一电离能最大的是______(填元素符号)。
6
(2)“碱浸”前,先将锑矿粉碎过筛的目的是____________________________________。
(3)“除杂”时生成CuS的化学方程式为____________________________________________
_______________________________________________________________________________
,
“除杂”结束后溶液中c(S2-)=1×10-6mol·L-1,此时溶液中c(Cu2+)=____________mol·L-
1。
(4)“转化”中HO 与NaSbO 溶液发生反应,该反应中氧化剂与还原剂的物质的量之比为
2 2 2
__________;分离出NaSbO ·3H O的操作是________(填名称);“转化”时适当加热可提高
3 2
反应速率,但是温度过高,转化效率降低,其主要原因是_____________________________
_______________________________________________________________________________
。
(5)“氟化”中加入氢氟酸,“氟化”不能使用陶瓷容器,其主要原因是_________________
_______________________________________________________________________________
。