文档内容
第2讲 物质的分离、提纯与检验
【2020·备考】
最新考纲:1.掌握常见物质分离与提纯的常用方法。2.掌握常见离子的检验方法。
核心素养:1.科学探究与创新意识:认识科学探究是进行科学解释和发现、创造和
应用的科学实践活动;能发现和提出有探究价值的问题,从问题和假设出发,确定
物质的分离和提纯以及检验探究方案,进行科学探究;善于合作,敢于质疑,勇于
创新。
2.科学精神与社会责任:在物质分离与提纯的方案设计中,要具有环境保护和合理
开发、利用资源的意识;能关心并积极参与和化学有关的社会热点问题的讨论,有
社会责任感,敢于参与力所能及的决策和实践活动。
考点一 物质的分离和提纯
(频数:★★★ 难度:★★☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 物
质的分离与提纯是高频考点,在一卷和二卷都有所涉及,应掌握常见分离装置及
使用注意事项,常见物质分离、提纯方法,能设计相关分离、提纯方案,另外一些创
新型的分离、提纯装置也应加以关注。
1.分离、提纯的含义
2.物质分离与提纯的实验装置
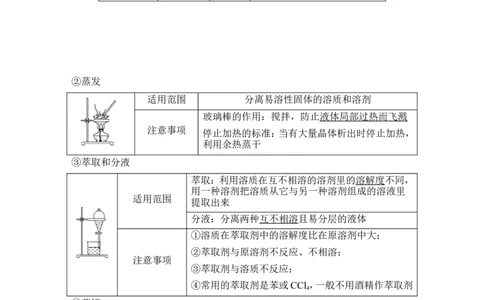
(1)常规实验装置①过滤
适用范围 把不溶性固体与液体进行分离
一贴 滤纸紧贴漏斗内壁
滤纸上缘低于漏斗口
二低
液面低于滤纸上缘
注意事项
烧杯紧靠玻璃棒
三靠 玻璃棒下端紧靠三层滤纸处
漏斗下端紧靠烧杯内壁
②蒸发
适用范围 分离易溶性固体的溶质和溶剂
玻璃棒的作用:搅拌,防止液体局部过热而飞溅
注意事项
停止加热的标准:当有大量晶体析出时停止加热,
利用余热蒸干
③萃取和分液
萃取:利用溶质在互不相溶的溶剂里的溶解度不同,
用一种溶剂把溶质从它与另一种溶剂组成的溶液里
适用范围
提取出来
分液:分离两种互不相溶且易分层的液体
①溶质在萃取剂中的溶解度比在原溶剂中大;
②萃取剂与原溶剂不反应、不相溶;
注意事项
③萃取剂与溶质不反应;
④常用的萃取剂是苯或CCl ,一般不用酒精作萃取剂
4
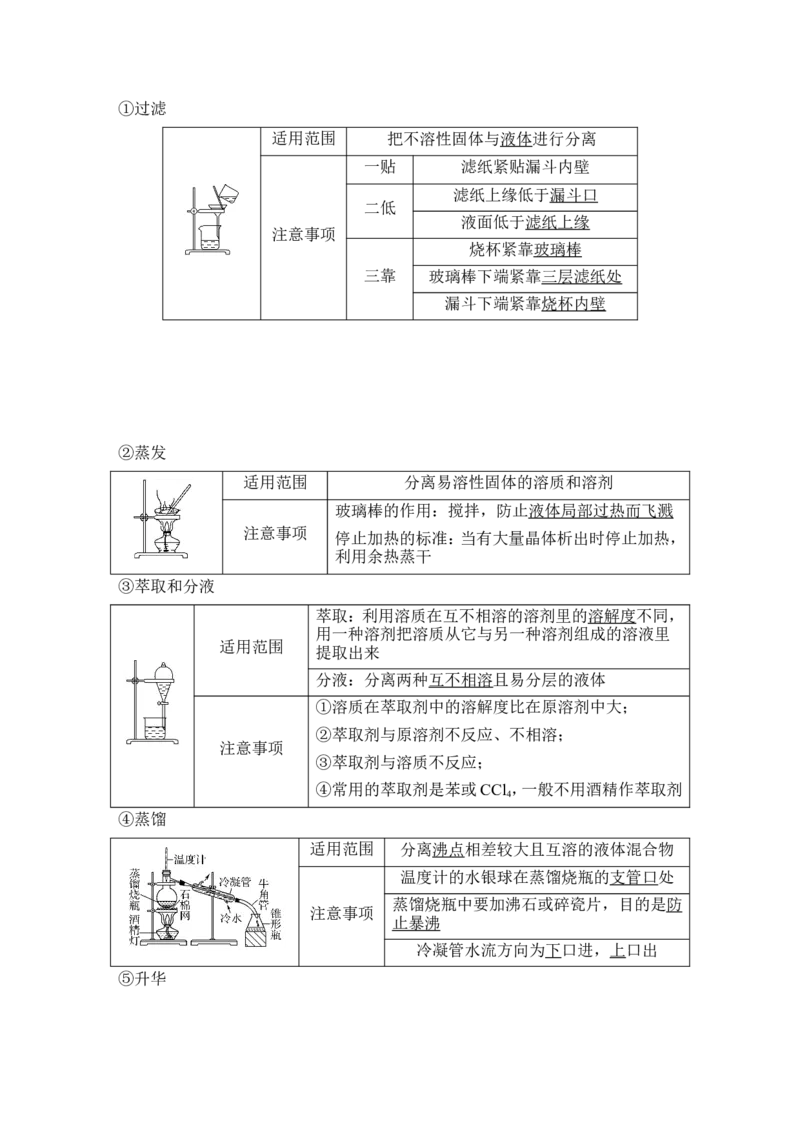
④蒸馏
适用范围 分离沸点相差较大且互溶的液体混合物
温度计的水银球在蒸馏烧瓶的支管口处
蒸馏烧瓶中要加沸石或碎瓷片,目的是防
注意事项
止暴沸
冷凝管水流方向为下口进,上口出
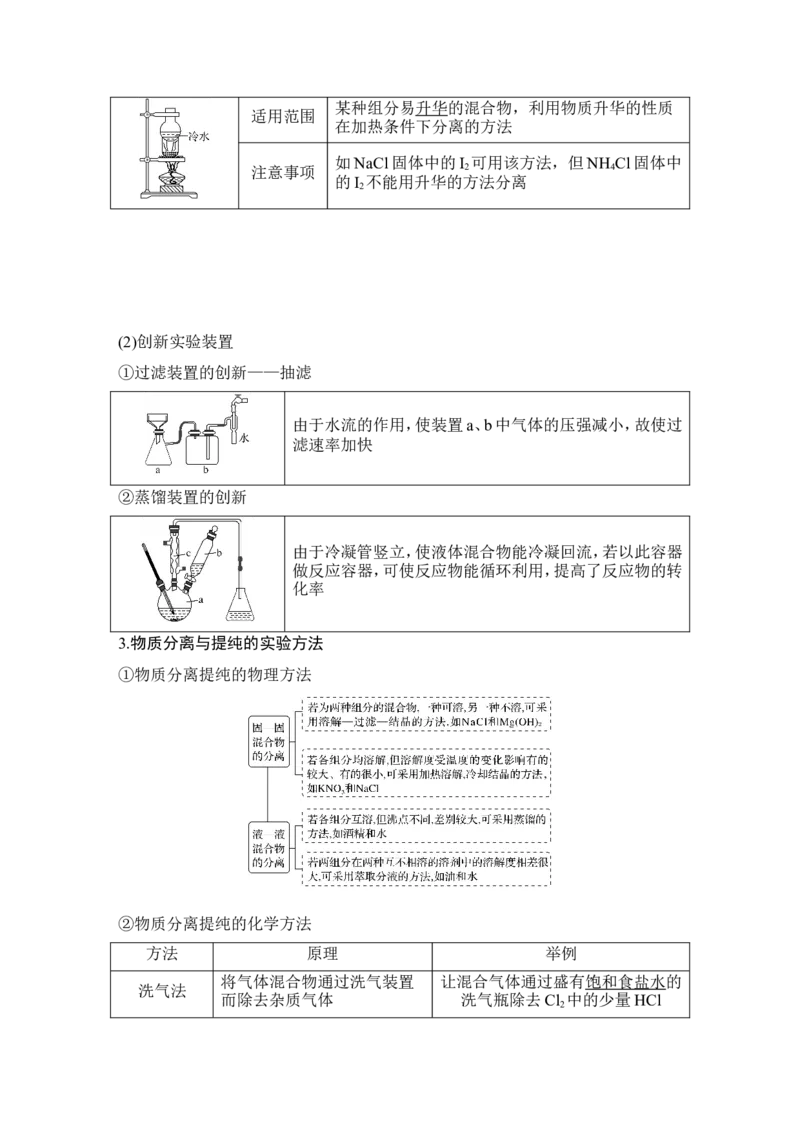
⑤升华某种组分易升华的混合物,利用物质升华的性质
适用范围
在加热条件下分离的方法
如NaCl固体中的I 可用该方法,但NH Cl固体中
注意事项 2 4
的I 不能用升华的方法分离
2
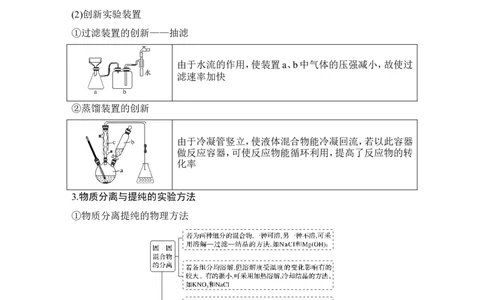
(2)创新实验装置
①过滤装置的创新——抽滤
由于水流的作用,使装置a、b中气体的压强减小,故使过
滤速率加快
②蒸馏装置的创新
由于冷凝管竖立,使液体混合物能冷凝回流,若以此容器
做反应容器,可使反应物能循环利用,提高了反应物的转
化率
3.物质分离与提纯的实验方法
①物质分离提纯的物理方法
②物质分离提纯的化学方法
方法 原理 举例
将气体混合物通过洗气装置 让混合气体通过盛有饱和食盐水的
洗气法
而除去杂质气体 洗气瓶除去Cl 中的少量HCl
2Cl-、SO、CO及能形成弱碱的金属
沉淀法 将杂质离子转化为沉淀 阳离子可加入适当的沉淀剂,使离
子生成沉淀,过滤除去
CO、HCO、SO、HSO、NH等与H+
气化法 将杂质离子转化为气体
或OH-反应生成气体除去
用加热法除去固体混合物中
热分解法 除去NaCl中的NH Cl
易分解的物质 4
酸碱溶解法 利用酸或碱将杂质溶解除去 用 盐 酸 除去SiO 中的CaCO
2 3
用酸性KMnO 溶液除去CO 中
氧化还原法 利用氧化还原反应除去杂质 4 2
SO
2
可用 CuO 、 Cu(OH) 等除去CuCl 溶
水解法 利用水解反应除去杂质 2 2
液中的FeCl
3
电解精炼铜,将含杂质的粗铜作阳
利用电解原理分离和提纯物
电解法 极、精铜作阴极,电解液为含铜离
质
子的溶液
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)(全国新课标卷)除去Cu粉中混有CuO的实验操作是加入稀硝酸溶解、过滤、洗
涤、干燥(×)
(2)(全国新课标卷)将Cl 与HCl的混合气体通过饱和食盐水可得到纯净的Cl (×)
2 2
(3)( 全国新课标卷)用CCl 萃取碘水中的I 的实验操作是先从分液漏斗下口放出
4 2
有机层,后从上口倒出水层(√)
(4)(海南化学)过滤操作中,漏斗的尖端应接触烧杯内壁(√)
(5)(天津理综)将气体通入澄清石灰水,溶液变浑浊,证明原气体是CO (×)
2
2.分离提纯装置判断
(1)(天津理综)图A是蒸馏时的接收装置(×)
(2)(安徽理综)用图B完成苯萃取碘水中I ,分出水层后的操作(×)
2
(3)(全国新课标卷)用图C装置除去粗盐溶液中不溶物(×)
(4)( 全国新课标卷)用图D装置除去CO气体中的CO 气体(×)
2
(5)(江苏化学)用图E装置蒸干NH Cl饱和溶液制备NH Cl晶体(×)
4 4
(6)(天津化学)用图F装置从KI和I 的固体混合物中回收I (×)
2 23.(教材实验探究)教材“实验1-1”探究
(1)除去粗盐中的 Ca2+、Mg2+、SO 杂质离子,应依次加入(写试剂化学
式)__________________________________________________________________。
(2)过滤时所用到的玻璃仪器为__________________________________________。
(3)蒸发时,能否将母液蒸干后,再停止加热。_____________________________
_____________________________________________________________________
。
答案 (1)BaCl 、NaOH、Na CO 或BaCl 、Na CO 、NaOH或NaOH、BaCl 、Na CO
2 2 3 2 2 3 2 2 3
(2)烧杯、漏斗、玻璃棒
(3)不能,如果将母液蒸干后,再停止加热,蒸发皿的余热会使析出的晶体受热不均
而飞溅,造成食盐损失和实验事故
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.(2018·山东名校联盟期末联考)《炼丹秘诀》中的“抽汞法”有如下叙述:“朱砂
不计多少。入沙锅中以炭屑填平锅口,剪蛎壳板如锅大密钻小窍盖之,却将空沙锅
一个与前锅二口相合,铁丝固济(包括有用铁丝缠和用盐泥固济二法),地下掘一穴
安埋空锅,锻炼之后候冷取出,大概银朱一两只有真汞三钱。 ”文中涉及的操作
方法是( )
A.蒸馏 B.升华
C.干馏 D.萃取解析 意思为“向一沙锅中放入一定量的朱砂,用炭屑填平锅口,剪与锅一般大
蛎壳板,在上面钻许多小孔,盖在锅上,再将一空沙锅与该锅的口密合,再用铁丝
等固定密封,在地上挖一洞,将空锅放在洞口上,加热锻烧,冷却后可以得到汞”。
即通过加热反应产生的汞蒸气冷却后得纯净汞。
答案 A
2.下列物质中杂质(括号内为杂质)的检验试剂、除杂试剂和除杂方法都正确的是(
)
选项 物质及其杂质 检验试剂 除杂试剂 除杂方法
A HCl(Cl ) 湿润的淀粉KI试纸 饱和食盐水 洗气
2
B C H OH(H O) 无水硫酸铜粉末 生石灰 蒸馏
2 5 2
饱和碳酸钠
C CO (SO ) 品红溶液 洗气
2 2 溶液
D NH Cl(I ) 淀粉溶液 无 加热
4 2
解析 HCl极易溶于水,饱和食盐水能除去Cl 中的HCl气体,A错误。生石灰与
2
水反应生成氢氧化钙,与乙醇的沸点相差较大,再通过蒸馏可得乙醇,B正确。饱
和碳酸钠溶液与SO 、CO 均能反应,可以选择酸性高锰酸钾溶液除去 CO 中的
2 2 2
SO ,C错误。碘受热易升华,NH Cl受热分解成NH 和HCl,遇冷又结合成NH Cl
2 4 3 4
固体,加热不能除去NH Cl中的I ,D错误。
4 2
答案 B
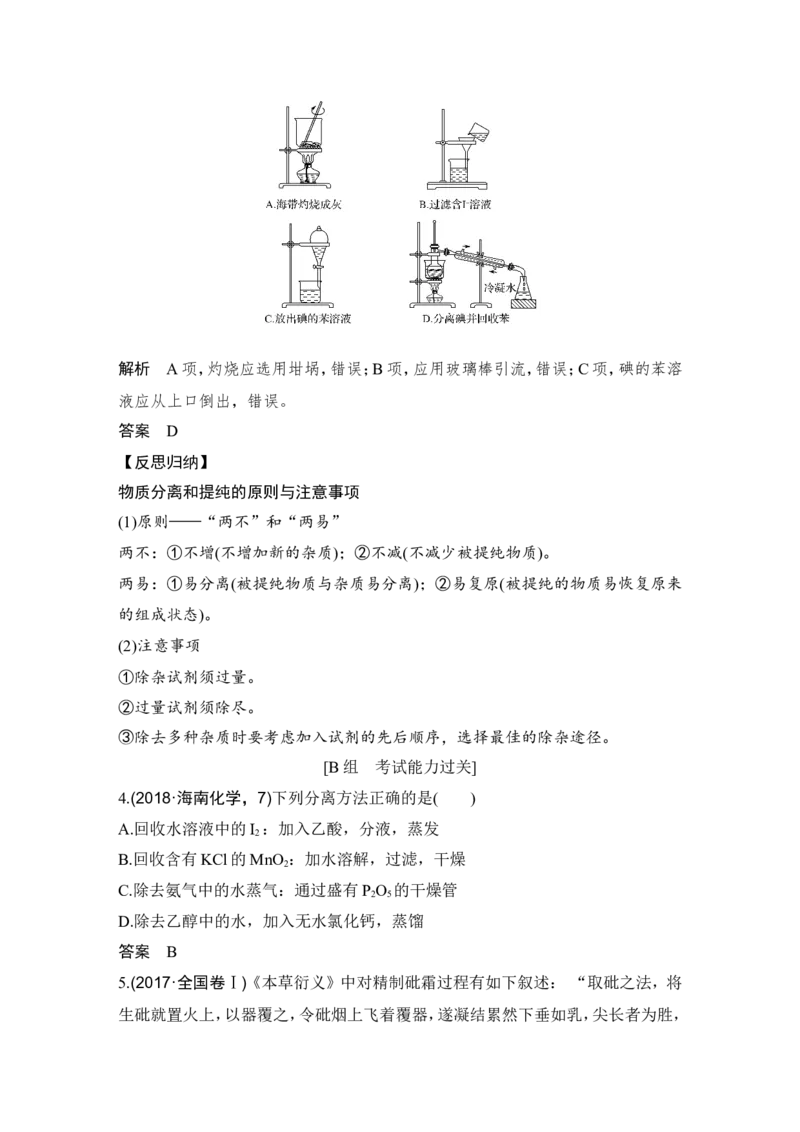
3.从海带中提取碘要经过灼烧、浸取、过滤、氧化、萃取、分液、蒸馏等操作,下列对
应的装置合理、操作规范的是( )解析 A项,灼烧应选用坩埚,错误;B项,应用玻璃棒引流,错误;C项,碘的苯溶
液应从上口倒出,错误。
答案 D
【反思归纳】
物质分离和提纯的原则与注意事项
(1)原则——“两不”和“两易”
两不:①不增(不增加新的杂质);②不减(不减少被提纯物质)。
两易:①易分离(被提纯物质与杂质易分离);②易复原(被提纯的物质易恢复原来
的组成状态)。
(2)注意事项
①除杂试剂须过量。
②过量试剂须除尽。
③除去多种杂质时要考虑加入试剂的先后顺序,选择最佳的除杂途径。
[B组 考试能力过关]
4.(2018·海南化学,7)下列分离方法正确的是( )
A.回收水溶液中的I :加入乙酸,分液,蒸发
2
B.回收含有KCl的MnO :加水溶解,过滤,干燥
2
C.除去氨气中的水蒸气:通过盛有P O 的干燥管
2 5
D.除去乙醇中的水,加入无水氯化钙,蒸馏
答案 B
5.(2017·全国卷Ⅰ)《本草衍义》中对精制砒霜过程有如下叙述: “取砒之法,将
生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之。”文中涉及的操作方法是( )
A.蒸馏 B.升华 C.干馏 D.萃取
解析 “令砒烟上飞着覆器”“凝结”说明该操作为升华。
答案 B
6.(2015·全国卷Ⅰ)下列实验中,所采取的分离方法与对应原理都正确的是( )
选项 目的 分离方法 原理
A 分离溶于水的碘 乙醇萃取 碘在乙醇中的溶解度较大
乙酸乙酯和乙醇的密度不
B 分离乙酸乙酯和乙醇 分液
同
除去KNO 固体中混杂的 NaCl在水中的溶解度很
C 3 重结晶
NaCl 大
丁醇与乙醚的沸点相差较
D 除去丁醇中的乙醚 蒸馏
大
解析 乙醇与水互溶,不能用作萃取剂,A项错;乙醇和乙酸乙酯互溶,不能用分
液方法分离,B项错;除去KNO 中NaCl杂质是利用二者在不同温度下溶解度变
3
化差别很大,使用重结晶法,C项错;分离两种沸点差别较大的互溶液体,一般使
用蒸馏操作,D项正确。
答案 D
7.(2014·全国卷)下列除杂方案错误的是( )
选项 被提纯的物质 杂质 除杂试剂 除杂方法
NaOH溶液、浓
A CO(g) CO (g) 洗气
2 H SO
2 4
B NH Cl(aq) Fe3+(aq) NaOH溶液 过滤
4
饱和食盐水、浓
C Cl (g) HCl(g) 洗气
2 H SO
2 4
D Na CO (s) NaHCO (s) - 灼烧
2 3 3
解析 A项,NaOH溶液吸收CO ,浓H SO 除去水蒸气,且两种试剂都不与CO
2 2 4
反应,正确;B项,NaOH溶液不仅能与Fe3+反应,还能与NH反应,且还能引入杂
质,错误;C项,饱和食盐水可以除去HCl,浓H SO 可以除去水蒸气,正确;D项,
2 4
灼烧能使NaHCO 固体分解生成Na CO ,正确。
3 2 3
答案 B考点二 离子的检验与推断
(频数:★★☆ 难度:☆☆☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 本
考点在高考中主要考查:(1)常见离子(或物质)的检验方法。(2)离子推断。特别是有
干扰离子时,某些离子的检验更是考查重点,复习时要加以关注。
1.离子检验的三种方法
(1)沉淀法
离子 试剂 现象 反应原理(离子方程式)
AgCl(白色)、 Ag++Cl-===AgCl↓、
稀HNO 和
Cl-、Br-、I- 3 AgBr(淡黄色)、 Ag++Br-===AgBr↓、
AgNO 溶液
3 AgI(黄色) Ag++I-===AgI↓
稀盐酸和BaCl
SO 2 白色沉淀 Ba2++SO==BaSO ↓
溶液 4
Fe2++2OH-===
白色沉淀→灰绿色
Fe2+ NaOH溶液
沉淀→红褐色沉淀 Fe(OH) 2 ↓、4Fe(OH) 2 +
O +2H O===4Fe(OH)
2 2 3
3Fe2++2[Fe(CN) ]3-
K [Fe(CN) ] 溶液 蓝色沉淀 6
3 6 === Fe [Fe(CN) ] ↓
3 6 2
Fe3++3OH-===
Fe3+ NaOH溶液 红褐色沉淀
Fe(OH) ↓
3
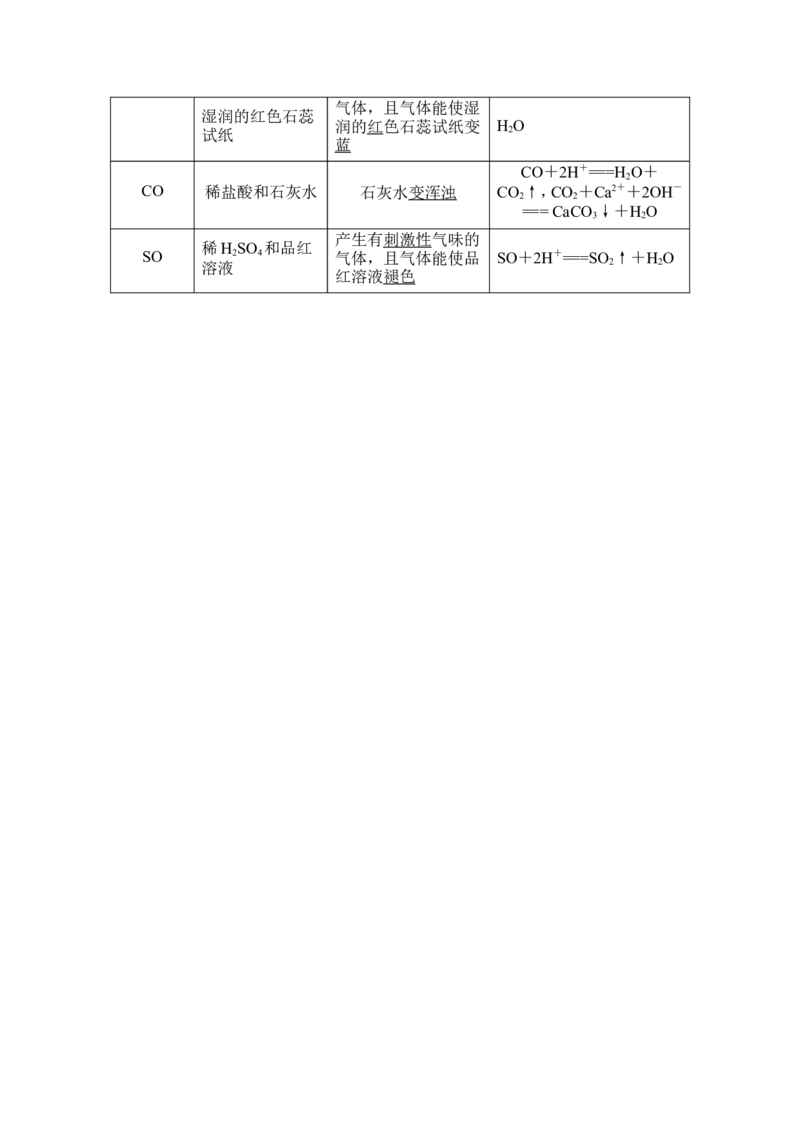
(2)气体法
离子 试剂 现象 反应原理(离子方程式)
NH 浓NaOH溶液和 产生有刺激性气味的 NH+OH-=====NH ↑+
3气体,且气体能使湿
湿润的红色石蕊
润的红色石蕊试纸变 H O
试纸 2
蓝
CO+2H+===H O+
2
CO 稀盐酸和石灰水 石灰水变浑浊 CO ↑,CO +Ca2++2OH-
2 2
=== CaCO ↓+H O
3 2
产生有刺激性气味的
稀H SO 和品红
SO 2 4 气体,且气体能使品 SO+2H+===SO ↑+H O
溶液 2 2
红溶液褪色(3)显色法
离子 试剂 现象 反应原理(离子方程式)
I- 氯水、淀粉溶液 溶液变蓝色 2I-+Cl ===2Cl-+I
2 2
先加KSCN溶液
2Fe2++Cl ===2Fe3++2Cl-,
Fe2+ KSCN溶液和氯水 无变化,滴加氯 2
Fe3++3SCN-===Fe(SCN)
水后变红色 3
Fe3+ KSCN溶液 红色 Fe3++3SCN-===Fe(SCN)
3
火焰分别呈黄 K+要透过蓝色钴玻璃观察焰
Na+、K+ Pt(Fe)丝和稀盐酸
色、紫色 色
2.排除三种离子检验的“干扰”
(1)SO的检验
①检验方法
②排除干扰
Ag+的干扰 先用盐酸酸化,能防止Ag+干扰
因为BaCO 、BaSO 也是白色沉淀,与BaSO 白色沉淀不
3 3 4
CO、SO的干扰 同的是这些沉淀能溶于盐酸中,因此检验SO时,必须先
用盐酸酸化(不能用HNO 、H SO 酸化)
3 2 4
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
所用的钡盐不能用Ba(NO ) 溶液,因为在酸性条件下,SO、HSO会被溶液中的
3 2
NO(H+)氧化成SO,从而得出错误结论。
(2)CO的检验
①检验方法②排除干扰
若被检液中不含CO而含有HCO,则加入CaCl (或BaCl )溶液时
2 2
HCO的干扰 不会产生白色沉淀,故可用BaCl (或CaCl )不能用Ba(OH) [或
2 2 2
Ca(OH) ]
2
因为CaSO 与CaCO 一样,也是白色沉淀,且CaSO 也能与盐酸
3 3 3
SO的干扰 反应产生使澄清石灰水变浑浊的气体(SO ),但SO 是有刺激性
2 2
气味的气体,故可用无色无味来排除SO的干扰
(3)Fe2+的检验
①溶液中只含Fe2+:可用KSCN溶液和氯水检验,不考虑干扰问题。
②溶液中含Fe2+、Fe3+,不含Cl-时,可加入酸性KMnO 溶液,溶液褪色,说明溶
4
液中含有Fe2+,不能用KSCN溶液和氯水,原因是Fe3+形成干扰。
③溶液中含有Fe2+、Fe3+、Cl-时,加入K [Fe(CN) ](铁氰化钾)溶液,生成蓝色沉淀,
3 6
不能用酸性KMnO 溶液,原因是Cl-也能使酸性KMnO 溶液褪色,Cl-能形成干
4 4
扰。
3.离子推断中的基本原则
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”(1)加入稀盐酸酸化的BaCl 溶液,出现白色沉淀,则溶液中可能有SO或Ag+(√)
2
(2)加入CaCl 溶液,有白色沉淀生成,溶液中一定存在CO(×)
2
(3)滴入硝酸酸化的BaCl 溶液,产生白色沉淀,溶液中一定存在SO(×)
2
(4)加入稀硫酸,产生使品红褪色的无色有刺激性气味的气体,则溶液中一定存在
SO(×)
(5)某溶液的焰色反应呈黄色,则溶液中一定有钠元素,不能确定是否有钾元素(√)
2.[教材改编题](RJ必修1·P 3改编)下列鉴别方法可行的是( )
10
A.滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口检验溶液中是否含有NH
B.用Ba(NO ) 溶液鉴别Cl-、SO和CO
3 2
C.通入少量Cl 后,溶液变为棕黄色,再加入淀粉溶液后,溶液变蓝,说明有I-
2
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,说明有Ca2+
答案 C
3.(思维探究)怎样检验溶液中既有Cl-,又有SO?
答案 向试液中,先加足量的Ba(NO ) 溶液,生成白色沉淀,过滤后,再向滤液中
3 2
加入AgNO 溶液,仍有白色沉淀,且白色沉淀不溶于稀HNO 。
3 3
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.(2018·安徽省“江淮十校”高三第一次联考)下列关于离子检验的说法正确的是
( )
A.检验溶液中是否含有Ba2+:取少量待测液,向其中加入少量稀硫酸,若有白色沉
淀产生,则溶液中含有Ba2+
B.检验用硫酸亚铁制得的硫酸铁中是否含有硫酸亚铁,可选用的试剂是酸性
KMnO 溶液
4
C.检验溶液中是否含有CO:取少量待测液,向其中加入适量稀盐酸,观察是否有
大量气泡产生
D.在未知溶液中滴加BaCl 溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未
2
知溶液中存在SO或SO解析 A.如果溶液中含有Ca2+、Ag+等,向其中加入少量稀硫酸,会有硫酸钙、硫
酸银等白色沉淀产生,所以不能确定溶液中含有Ba2+,故A错误;B.硫酸亚铁可将
KMnO 还原而使酸性KMnO 溶液褪色,故B正确;C.HCO、SO、HSO也可遇稀盐
4 4
酸产生大量气泡,故C错误;D.也可能存在Ag+,产生氯化银白色沉淀,故D错误。
答案 B
2.(2018·郑州模拟)某化学兴趣小组在课外活动中,对某一份溶液成分(已知不含其
他还原性离子)进行了检测,其中三次检测结果如下表所示:
检测序号 溶液中检测出的离子组合
第一次 KCl、K SO 、Na CO 、NaCl
2 4 2 3
第二次 KCl、AlCl 、Na SO 、K CO
3 2 4 2 3
第三次 Na SO 、KCl、K CO 、NaCl
2 4 2 3
则下列说法合理的是( )
A.三次检测结果都正确
B.该溶液中的阳离子无法判断
C.为了检验SO,应先加过量稀硝酸后再滴加Ba(NO ) 溶液,观察是否有沉淀现象
3 2
D.为了确定是否存在CO,可以向其中滴加CaCl 溶液,观察是否有沉淀现象
2
解析 Al3+与CO不能大量共存于溶液中,第二次检测结果不正确,A项错误;因
第一次、第三次检测中均有CO,阳离子均只有K+、Na+,故溶液中的阳离子可以
确定,B项错误;CO也能与Ba2+结合形成沉淀,先加过量稀硝酸可排除CO的干
扰,再加Ba(NO ) 溶液来检验SO,C项正确;CaSO 也可沉淀出来,D项错误。
3 2 4
答案 C
3.某同学为检验溶液中是否含有常见的几种无机离子,进行了如图所示的实验操
作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得到
的正确结论是( )
A.原溶液中一定含有SO B.原溶液中一定含有NH
C.原溶液中一定含有Cl- D.原溶液中一定含有Fe3+
解析 原溶液中加入Ba(NO ) 和HCl生成白色沉淀,原溶液中可能存在SO、SO
3 2
或Ag+,A错误;因检验过程中产生的气体能使湿润的红色石蕊试纸变蓝,说明原溶液中一定含有NH,B正确;加AgNO 溶液产生白色沉淀,可能是加入的HCl引
3
起的,C错误;加入KSCN溶液得到红色溶液,Fe3+可能是由原溶液中的Fe2+被H
+、NO氧化而来的,故原溶液中不一定含有Fe3+,D错误。
答案 B
【思维建模】
无色溶液中离子检验的一般思路
[B组 考试能力过关]
4.(2018·海南化学,4)下列化合物中,能与Na CO 溶液反应生成沉淀且沉淀可溶
2 3
于NaOH溶液的是( )
A.MgCl B.Ca(NO )
2 3 2
C.FeSO D.AlCl
4 3
答案 D
5.(2016·课标全国Ⅱ,12)某白色粉末由两种物质组成,为鉴别其成分进行如下实
验:
①取少量样品加入足量水仍有部分固体未溶解;再加入足量稀盐酸,有气泡产生,
固体全部溶解;
②取少量样品加入足量稀硫酸有气泡产生,振荡后仍有固体存在。
该白色粉末可能为( )A.NaHCO 、Al(OH) B.AgCl、NaHCO
3 3 3
C.Na SO 、BaCO D.Na CO 、CuSO
2 3 3 2 3 4
解析 A项,NaHCO 、Al(OH) 中加入足量稀硫酸有气泡产生,生成硫酸钠、硫酸
3 3
铝、二氧化碳和水,最终无固体存在,错误;B项,AgCl不溶于酸,固体不能全部溶
解,错误;C项,亚硫酸钠和碳酸钡加入水,碳酸钡不溶于水使部分固体不溶解,加
入稀盐酸,碳酸钡与盐酸反应生成氯化钡、二氧化碳和水,固体全部溶解,再将样
品加入足量稀硫酸,稀硫酸和碳酸钡反应生成硫酸钡沉淀、二氧化碳和水,正确;
D项,Na CO 、CuSO 中加入足量稀硫酸,振荡后无固体存在,错误。
2 3 4
答案 C
6.(2016·四川理综,2)根据下列实验操作和现象得出的结论正确的是( )
选项 实验操作 现象 结论
将某溶液与稀盐酸反应产
A 石灰水变浑浊 该溶液中一定含有CO
生的气体通入澄清石灰水
常温下,将铁片浸入足量 常温下,铁与浓硫酸一定
B 铁片不溶解
浓硫酸中 没有发生化学反应
向某食盐溶液中滴加淀粉 该食盐中一定没有添加
C 溶液颜色不变
溶液 KIO
3
向苯酚钠溶液中滴加乙酸 相同条件下,乙酸的酸性
D 溶液变浑浊
溶液 一定比苯酚强
解析 A项,能使澄清石灰水变浑浊的气体有SO 或CO ,因此溶液中可能含有
2 2
CO、HCO、HSO、SO中的一种或几种,错误;B项,发生钝化,即在铁表面生成一层
致密的氧化物薄膜,阻止进一步被氧化,发生了化学变化,错误;C项,淀粉遇I 溶
2
液才变蓝,要检验KIO ,需要先将IO转化为I ,错误;D项,苯酚钠与乙酸反应生
3 2
成苯酚,说明乙酸的酸性强于苯酚,正确。
答案 D
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\分层课时作业.TIF" \* MERGEFORMATINET[A级 全员必做题]
1.(2018·烟台期末)清初《泉州府志》物产条载: “初,人不知盖泥法,元时南安有
黄长者为宅煮糖,宅垣忽坏,去土而糖白,后人遂效之。 ”文中“盖泥法”的原
理与下列相同的是( )
A.活性炭净水 B.用漂白粉漂白织物
C.除去KNO 中的NaCl D.除去河水中泥沙
3
解析 文中“去土而糖白”是指固体土吸附糖色,所以文中“盖泥法”的原理与
活性炭净水相同,故选A项。
答案 A
2.(2018·山东烟台会诊,8)中国传统文化对人类文明贡献巨大。下列各文献中所记
载的古代化学研究过程或成果不涉及分离提纯操作的是( )
A《. 本草纲目》: “(烧酒)自元时创始,其法用浓酒和糟入甑,蒸令气上,用器盛露
滴。”
B.《齐民要术》: “凡酿酒失所味者,或初好后动未压者,皆宜廻作醋。 ”
C.《开宝本草》: “(消石)所在山泽,冬月地上有霜扫取,以水淋汁,后乃煎炼而
成。”
D《. 天工开物》: “草木之实,其中蕴藏膏液,而不能自流,假媒水火,凭藉木石,
而后倾注而出焉。”
解析 A项,描述的是酒的蒸馏,涉及分离提纯操作;B项,酒精在醋酸菌的作用
下氧化可以转化成醋酸和水,涉及化学反应但没有涉及分离提纯操作;C项,包含
溶解、蒸发结晶,涉及分离提纯操作;D项,榨油或加热使油脂从果实中分离出来,
涉及分离提纯操作。
答案 B
3.为提纯下列物质(括号内为杂质),选用的试剂或分离方法错误的是( )
选项 物质 试剂 分离方法
A 硝酸钾(氯化钠) 蒸馏水 降温结晶
B 二氧化碳(氯化氢) 饱和NaHCO 溶液 洗气
3
C 甲烷(乙烯) 酸性高锰酸钾溶液 洗气
D 乙醇(水) 生石灰 蒸馏解析 KNO 的溶解度受温度影响较大,而NaCl的溶解度受温度影响较小,可加
3
蒸馏水溶解固体,再通过蒸发浓缩、降温结晶的方法,获得纯净的KNO 固体,A
3
项正确;HCl与饱和 NaHCO 溶液反应生成二氧化碳,B项正确;乙烯被酸性
3
KMnO 溶液氧化生成CO ,使甲烷中混入CO 气体,C项错误;加入的生石灰能与
4 2 2
水反应生成Ca(OH) ,消耗掉部分水,再通过蒸馏获得乙醇,D项正确。
2
答案 C
4.下列装置所示的分离、提纯方法和物质的溶解性无关的是( )
解析 洗气法、冷却结晶、萃取及分液都与物质的溶解性有关,而蒸馏法分离液体
混合物是利用各液体组分的沸点不同,与物质的溶解性无关。
答案 C
5.(2018·沈阳质量监测)下列检验方法不合理的是( )
选项 实验 检验方法
向沸水中滴加5~6滴饱和FeCl 溶
3
A 液,继续煮沸至溶液呈红褐色,停 用激光笔照射烧杯中的液体
止加热,得Fe(OH) 胶体
3
B 证明溶液中存在NH
滴加浓NaOH溶液,加热,将湿
润的红色石蕊试纸置于试管口,试纸变蓝
分别取少量溶液,滴加BaCl 溶
C 区分AgNO 溶液和Al (SO ) 溶液 2
3 2 4 3 液
用CCl 充分萃取,将红纸条分
D 证明氯水中起漂白作用的不是Cl 4
2 别浸入分层后的溶液中
解析 胶体的制备和检验方法均正确,A项不符合题意;铵根离子的检验方法正
确,B项不符合题意;向硝酸银溶液中加入氯化钡溶液生成氯化银白色沉淀,向硫
酸铝溶液中加入氯化钡溶液生成硫酸钡白色沉淀,二者现象相同,不能区分,C项
符合题意;此方法能够证明Cl 没有漂白性,D项不符合题意。
2
答案 C
6.下列说法不正确的是( )
A.葡萄糖溶液和乙酸可用新制氢氧化铜鉴别
B.植物油和矿物油可用热的饱和碳酸钠溶液鉴别
C.甲苯和乙醇可用酸性高锰酸钾溶液鉴别
D.乙醇、苯、四氯化碳既可用燃烧法鉴别,又可用水鉴别
解析 葡萄糖溶液与新制氢氧化铜在加热条件下反应产生砖红色沉淀,新制氢氧
化铜与乙酸发生中和反应,溶液变蓝,A项正确;矿物油不溶于热的饱和碳酸钠溶
液而出现分层,但热的饱和碳酸钠溶液会使植物油水解而使油层变少,B项正确;
甲苯和乙醇都能使酸性高锰酸钾溶液褪色,不能鉴别,C项错误;乙醇燃烧产生淡
蓝色火焰且无烟,苯燃烧时火焰明亮且有浓烟,四氯化碳不能燃烧,所以可以用燃
烧法鉴别三者,由于乙醇易溶于水,苯不溶于水且密度比水小,四氯化碳不溶于水
且密度比水大,所以用水也可以鉴别三者,D项正确。
答案 C
7.下表中根据实验操作和现象所得出的结论正确的是( )
选项 实验操作 实验现象 结论
蘸有浓氨水的玻璃棒靠近浓X
A 有白烟产生 X一定是HCl
溶液
溶液先变蓝 氯气先表现氧化性,后
B 将Cl 持续通入淀粉KI溶液中
2 色,后褪色 表现漂白性
向强酸性溶液Y中加入
只有白色沉淀 Y中一定含有SO,一
C Ba(NO ) 溶液,静置后再加入铁
3 2 产生 定不含Fe2+
氰化钾溶液
D 将无色气体X通入品红溶液 开始时品红溶 X中一定含有SO 2液褪色,加热
中,然后加热
后又恢复红色
解析 能与氨气反应产生白烟的有浓盐酸、浓硝酸等,A项错误;将Cl 持续通入
2
淀粉KI溶液中,先将I-氧化为I ,然后将I 氧化为IO,整个过程只表现出氧化性,
2 2
B项错误;酸性条件下NO具有强氧化性,能把溶液Y中的Fe2+氧化成Fe3+,加入
铁氰化钾溶液时不产生蓝色沉淀,故溶液Y中可能含有Fe2+,C项错误;能使品红
溶液褪色,加热后又恢复红色的气体只能为SO ,D项正确。
2
答案 D
8.[2018·广东佛山教学质量检测(二)]超临界状态下的CO 流体溶解性与有机溶剂
2
相似,可提取中药材的有效成份,工艺流程如下。
下列说法中错误的是( )
A.浸泡时加入乙醇有利于中草药有效成分的浸出
B.高温条件下更有利于超临界CO 流体萃取
2
C.升温、减压的目的是实现CO 与产品分离
2
D.超临界CO 流体萃取中药材具有无溶剂残留、绿色环保等优点
2
解析 高温条件下,二氧化碳为气态,而萃取是利用超临界状态下的CO 流体,故
2
高温条件下不利于超临界CO 流体萃取,B项错误。
2
答案 B
9.某化学兴趣小组从含有KI、KNO 等成分的工业废水中回收I 和KNO ,其流程
3 2 3
如下:
下列说法正确的是( )
A.步骤1中有机相应从分液漏斗下端放出,无机相从上口倒出
B.步骤2使用的玻璃仪器有蒸馏烧瓶、酒精灯、牛角管、球形冷凝管、锥形瓶C.步骤3可在装置 中完成
D.步骤4中,将溶液蒸发至只剩少量水时,用余热将晶体蒸干
解析 步骤1为萃取分液操作,苯的密度比水小,故有机相应从分液漏斗上口倒
出,A错误;步骤2为蒸馏,应选用直形冷凝管,球形冷凝管一般用于冷凝回流,B
错误;步骤3为升华,用图中装置能较好地控制温度,C正确;步骤4为蒸发结晶,
由于KNO 的溶解度随温度变化比较大,应采用蒸发浓缩、冷却结晶的方法,因此
3
加热至有少量晶体出现就可停止加热,D错误。
答案 C
10.我国青海查尔汗盐湖蕴藏着丰富的食盐资源。经分析知道,该湖水中含有高浓
度的Na+、K+、Mg2+及Cl-等。利用盐湖水可得到某些物质。其主要工业流程如下:
请根据上述流程,回答下列问题:
(1)利用湖水得到晶体(A)的方法是________结晶法(填“降温”或“蒸发”)。
(2) 操 作 Ⅰ 的 名 称 为 ________ , 此 操 作 适 用 于 分 离
_____________________________________________________________________
_____________________________________________________________________
。
(3)本流程中分别采用条件 1 和条件 2 获得不同晶体,所以依据的物理量是
________。
a.摩尔质量 B.溶解度
c.溶解性 D.熔、沸点
(4)检验钾肥中是否含有Na+的实验方法是________,若含有Na+,能观察到的现
象是________。若需得到高纯度的钾肥,可以采用的提纯方法为________。
解析 (1)天然湖水应采用蒸发的方法使溶质结晶。(2)不溶性固体和液体混合物的
分离,应用过滤的方法。(3)由流程图可知,条件1和条件2温度不同,是利用物质在不同温度下的溶解度的大小不同而进行分离的。(4)检验Na+、K+等应用焰色反
应。
答案 (1)蒸发 (2)过滤 不溶性固体和液体混合物 (3)b (4)焰色反应 火焰
呈黄色 重结晶法
11.(2016·海南)某废催化剂含58.2%的SiO 、21.0%的ZnO、4.5%的ZnS和12.8%的
2
CuS。某同学用15.0 g该废催化剂为原料,回收其中的锌和铜。采用的实验方案如
下:
回答下列问题:
(1)在下列装置中,第一次浸出必须用________,第二次浸出应选用________。(填
标号)
(2)第二次浸出时,向盛有滤液1的反应器中加入稀硫酸,后滴入过氧化氢溶液。若
顺序相反,会造成________。滤渣2的主要成分是________。
(3)浓缩硫酸锌、硫酸铜溶液使用的器皿名称是________。
(4)某同学在实验完成之后,得到1.5 g CuSO ·5H O,则铜的回收率为________。
4 2
解析 (1)根据题给化学工艺流程知第一次浸出发生反应 ZnO+H SO ===ZnSO
2 4 4
+H O、ZnS+H SO ===ZnSO +H S↑,有有毒气体H S生成,必须用氢氧化钠溶
2 2 4 4 2 2
液进行尾气处理,选 D 装置,第二次浸出时发生反应:CuS+H O +
2 2
H SO ===CuSO +S+2H O,不产生有毒气体,可选用A装置。(2)第二次浸出时,
2 4 4 2
向盛有滤液1的反应器中加入稀硫酸,后滴入过氧化氢溶液。若顺序相反,会造成
H O 与固体颗粒接触分解。滤渣2的主要成分是二氧化硅。(3)浓缩硫酸锌、硫酸铜
2 2
溶液使用的器皿名称是蒸发皿。(4)15.0 g废催化剂中含有铜的物质的量为 15.0
g×12.8%÷96 g/mol=0.02 mol,1.5 g CuSO ·5H O 中铜的物质的量为 1.5 g÷250
4 2
g/mol=0.006 mol,则铜的回收率为0.006 mol/0.02 mol×100%=30%。答案 (1)D A (2)H O 与固体颗粒接触分解 SiO
2 2 2
(3)蒸发皿 (4)30%
[B级 拔高选做题]
12.(2019·晋豫省际大联考,7)过碳酸钠是过氧化氢与碳酸钠通过反应得到的一种
固体物质,具有双氧水的性质,主要用作漂白剂、氧化剂、去污剂、清洗剂以及杀菌
剂,一种制备过碳酸钠的工艺如下。
下列说法中正确的是( )
A.过碳酸钠是混合物
B.为了加快反应速率,应该在高温下进行反应,再冷却析出更多过碳酸钠
C.稳定剂使碱性溶液转化为酸性溶液,让过碳酸钠更稳定
D.操作a应该是过滤、洗涤
解析 过碳酸钠是具有确定化学组成的化合物,A项错误。高温会使过氧化氢分
解而无法得到过碳酸钠,B项错误。稳定剂是硫酸镁和硅酸钠,都不能使溶液显酸
性,C项错误。反应后,经冷却结晶、过滤、洗涤、干燥就可得到产品,D项正确。
答案 D
13.(2019·广东江门高考模拟,10)实验室在 500 ℃时隔绝空气加热硫酸亚铁铵
[(NH ) Fe(SO ) ]至分解完全并确定分解产物成分的装置如图所示(已知分解的固
4 2 4 2
体产物可能有FeO、Fe O 和Fe O ,气体产物可能有NH 、N 、H O、SO 和SO )。下
2 3 3 4 3 2 2 3 2
列说法中正确的是( )
A.装置②用于检验分解产物中是否有水蒸气生成,试剂X最好选用碱石灰
B.装置③用于检验分解产物中是否有SO 气体生成并除去SO 和NH
3 3 3
C.取①中固体残留物与稀硫酸反应并滴加KSCN溶液,溶液变红色,则残留物一定为Fe O
2 3
D.装置④用于检验分解产物中是否有SO 气体生成,装置⑤用于收集生成的NH
2 3
和N
2
解析 装置②的作用是检验产物中是否有水蒸气生成,故试剂X应为无水硫酸铜
A项错误;装置③用于检验产物中是否有SO 气体生成,若存在则装置③中会产生
3
白色沉淀,并可用盐酸除去NH ,B项正确;取①中固体残留物与稀硫酸反应并滴
3
加KSCN溶液,溶液变红色,则①中固体残留物中也可能含有Fe O ,不一定有
3 4
Fe O ,C项错误;氨气极易溶于水,若分解产物中有NH ,则氨气被装置③吸收,
2 3 3
装置⑤不可能收集到氨气,D项错误。
答案 B
14.(2016·全国卷Ⅲ,26)过氧化钙微溶于水,溶于酸,可用作分析试剂、医用防腐剂、
消毒剂。以下是一种制备过氧化钙的实验方法。回答下列问题:
(一)碳酸钙的制备
(1)步骤①加入氨水的目的是___________________________________________。
小火煮沸的作用是使沉淀颗粒长大,有利于________。(2)右图是某学生的过滤操作示意图,其操作不规范的是________(填标号)。
a.漏斗末端颈尖未紧靠烧杯壁
b.玻璃棒用作引流
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(二)过氧化钙的制备
CaCO ――→滤液――→――→白色结晶
3
(3)步骤②的具体操作为逐滴加入稀盐酸,至溶液中尚存有少量固体,此时溶液呈
________性(填“酸”、“碱”或“中”)。将溶液煮沸,趁热过滤。将溶液煮沸的作
用是____________________________。
(4)步骤③中反应的化学方程式为_______________________________________,
该反应需要在冰浴下进行,原因是_______________________________________。
(5)将过滤得到的白色结晶依次使用蒸馏水、乙醇洗涤,使用乙醇洗涤的目的是
________。
(6)制备过氧化钙的另一种方法是:将石灰石煅烧后,直接加入双氧水反应,过滤后
可得到过氧化钙产品。该工艺方法的优点是____________________________,
产品的缺点是________________________________________________________。
解析 (1)反应混合液中盐酸过量,加入氨水可以中和盐酸,调节溶液的pH使Fe3
+转化为Fe(OH) 沉淀而除去。小火煮沸的作用是使沉淀颗粒长大,有利于过滤分
3
离。(2)a项,漏斗末端颈尖未紧靠烧杯壁,容易造成溶液飞溅,错误;b项,玻璃棒
用作引流,正确;c项,将滤纸湿润,使其紧贴漏斗壁,防止有气泡,正确;d项,滤
纸边缘应低于漏斗口,错误;e项,用玻璃棒在漏斗中轻轻搅动容易划破滤纸,错误。
(3)步骤②中逐滴加入稀盐酸,至溶液中尚存有少量固体,此时溶液中含有大量的
CO ,溶液呈酸性,而CaO 溶于酸,故应将溶液煮沸以除去溶解的CO 气体。(4)根
2 2 2
据题意可知反应物为CaCl 、H O 、NH ·H O,产物为CaO 、NH Cl和H O,则反应
2 2 2 3 2 2 4 2
的化学方程式为CaCl +2NH ·H O+H O ===CaO ↓+2NH Cl+2H O,由于H O
2 3 2 2 2 2 4 2 2 2
在高温下易分解,所以反应应在冰浴中进行。(5)由于乙醇与水互溶且易挥发,所以
使用乙醇洗涤去除晶体表面的水分。(6)制备过氧化钙的另一种方法将石灰石煅烧
后,直接加入双氧水反应,过滤后可得到过氧化钙产品。该工艺方法的优点是:工艺简单,操作方便,产品的缺点是:没有除杂净化工艺,所制得产品纯度低。
答案 (1)调节溶液pH使Fe(OH) 沉淀 过滤分离 (2)ade
3
(3)酸 除去溶液中的CO
2
(4)CaCl +2NH ·H O+H O ===CaO ↓+2NH Cl+2H O 或 CaCl +2NH ·H O+
2 3 2 2 2 2 4 2 2 3 2
H O +6H O===CaO ·8H O↓+2NH Cl 温度过高时双氧水易分解
2 2 2 2 2 4
(5)去除晶体表面水分
(6)工艺简单,操作方便 纯度较低