文档内容
南阳一中 2023 届高三第一次阶段性考试
化学试题
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Fe-56
第Ⅰ卷(选择题)
一、单选题
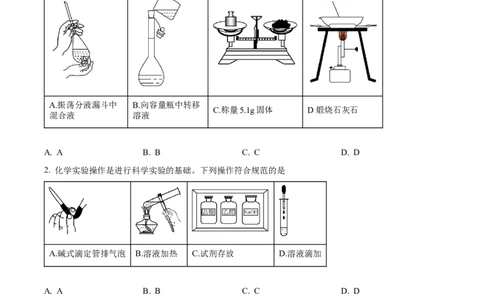
1. 下列对装置或仪器的使用或操作规范的是
.
A.振荡分液漏斗中 B.向容量瓶中转移
C.称量5.1g固体 D煅烧石灰石
混合液 溶液
A. A B. B C. C D. D
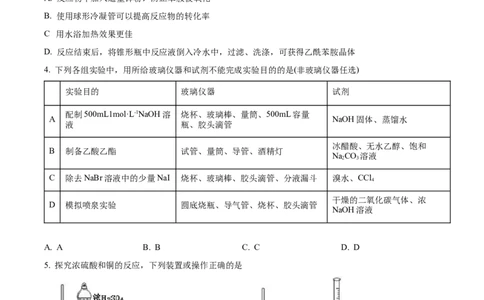
2. 化学实验操作是进行科学实验的基础。下列操作符合规范的是
A.碱式滴定管排气泡 B.溶液加热 C.试剂存放 D.溶液滴加
A. A B. B C. C D. D
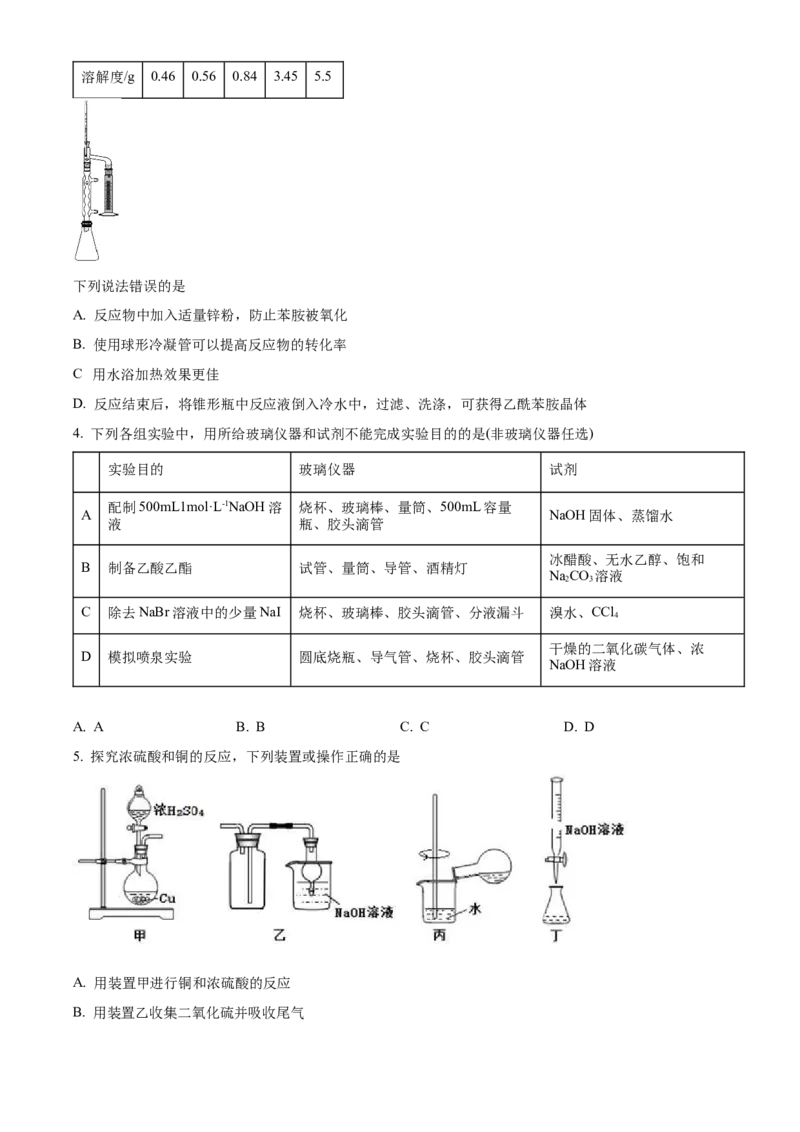
3. 乙酰苯胺 可用作止痛剂、退热剂,制备装置如图所示。反应原理为:
。已知苯胺可溶于水,沸点 ,接触空气
易被氧化;冰醋酸的沸点为 。乙酰苯胺的溶解度如下表:
温度/ 20 25 50 80 100
下载最新免费模拟卷,到公众号:一枚试卷君溶解度/g 0.46 0.56 0.84 3.45 5.5
下列说法错误的是
A. 反应物中加入适量锌粉,防止苯胺被氧化
B. 使用球形冷凝管可以提高反应物的转化率
.
C 用水浴加热效果更佳
D. 反应结束后,将锥形瓶中反应液倒入冷水中,过滤、洗涤,可获得乙酰苯胺晶体
4. 下列各组实验中,用所给玻璃仪器和试剂不能完成实验目的的是(非玻璃仪器任选)
实验目的 玻璃仪器 试剂
配制500mL1mol·L-1NaOH溶 烧杯、玻璃棒、量筒、500mL容量
A NaOH固体、蒸馏水
液 瓶、胶头滴管
冰醋酸、无水乙醇、饱和
B 制备乙酸乙酯 试管、量筒、导管、酒精灯
NaCO 溶液
2 3
C 除去NaBr溶液中的少量NaI 烧杯、玻璃棒、胶头滴管、分液漏斗 溴水、CCl
4
干燥的二氧化碳气体、浓
D 模拟喷泉实验 圆底烧瓶、导气管、烧杯、胶头滴管
NaOH溶液
A. A B. B C. C D. D
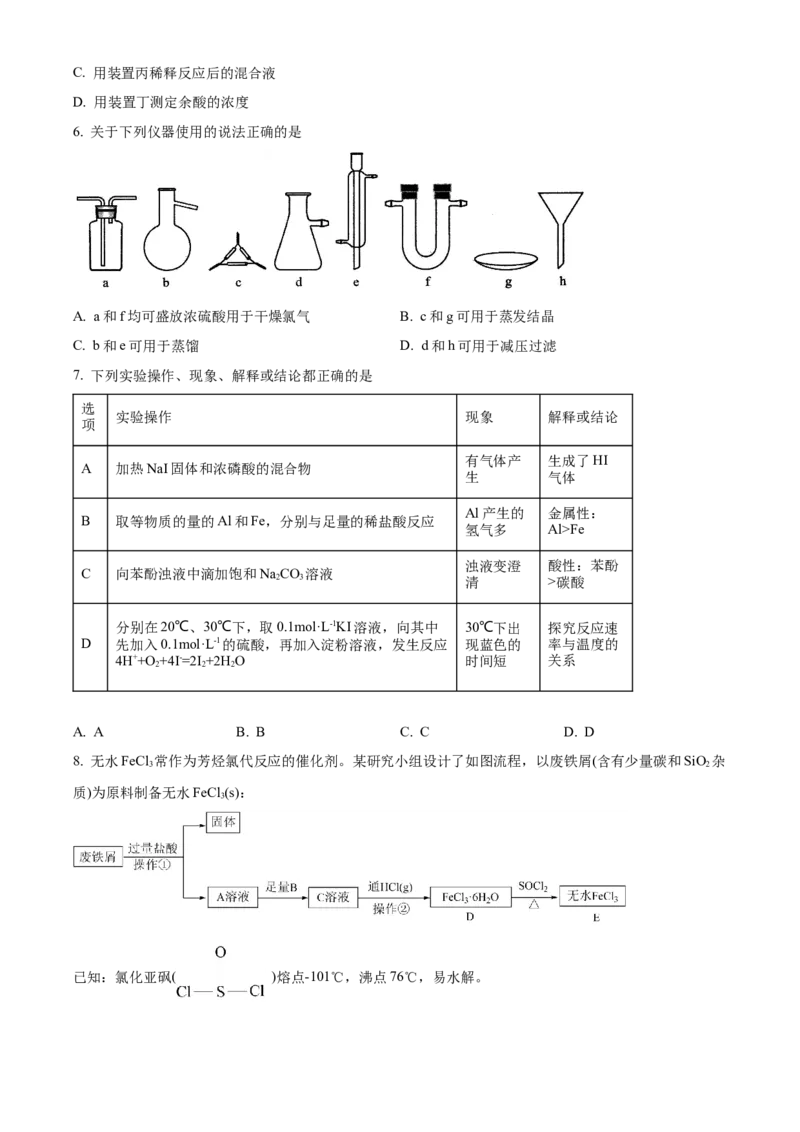
5. 探究浓硫酸和铜的反应,下列装置或操作正确的是
A. 用装置甲进行铜和浓硫酸的反应
B. 用装置乙收集二氧化硫并吸收尾气C. 用装置丙稀释反应后的混合液
D. 用装置丁测定余酸的浓度
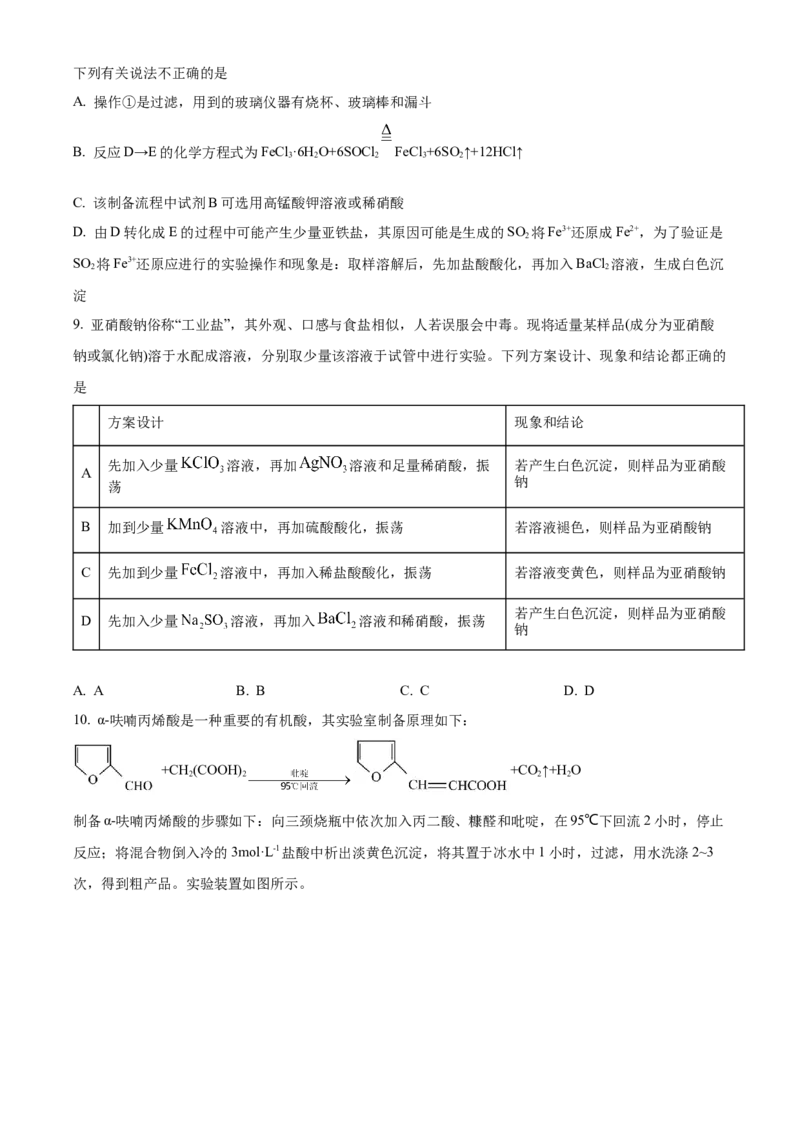
6. 关于下列仪器使用的说法正确的是
A. a和f均可盛放浓硫酸用于干燥氯气 B. c和g可用于蒸发结晶
C. b和e可用于蒸馏 D. d和h可用于减压过滤
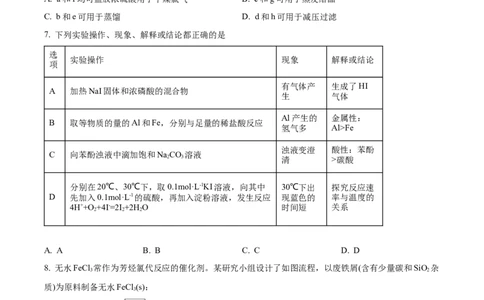
7. 下列实验操作、现象、解释或结论都正确的是
选
实验操作 现象 解释或结论
项
有气体产 生成了HI
A 加热NaI固体和浓磷酸的混合物
生 气体
Al产生的 金属性:
B 取等物质的量的Al和Fe,分别与足量的稀盐酸反应
氢气多 Al>Fe
浊液变澄 酸性:苯酚
C 向苯酚浊液中滴加饱和NaCO 溶液
2 3 清 >碳酸
分别在20℃、30℃下,取0.1mol·L-1KI溶液,向其中 30℃下出 探究反应速
D 先加入0.1mol·L-1的硫酸,再加入淀粉溶液,发生反应 现蓝色的 率与温度的
4H++O +4I-=2I +2H O 时间短 关系
2 2 2
A. A B. B C. C D. D
8. 无水FeCl 常作为芳烃氯代反应的催化剂。某研究小组设计了如图流程,以废铁屑(含有少量碳和SiO 杂
3 2
质)为原料制备无水FeCl (s):
3
已知:氯化亚砜( )熔点-101℃,沸点76℃,易水解。下列有关说法不正确的是
A. 操作①是过滤,用到的玻璃仪器有烧杯、玻璃棒和漏斗
B. 反应D→E的化学方程式为FeCl ·6H O+6SOCl FeCl +6SO↑+12HCl↑
3 2 2 3 2
C. 该制备流程中试剂B可选用高锰酸钾溶液或稀硝酸
D. 由D转化成E的过程中可能产生少量亚铁盐,其原因可能是生成的SO 将Fe3+还原成Fe2+,为了验证是
2
SO 将Fe3+还原应进行的实验操作和现象是:取样溶解后,先加盐酸酸化,再加入BaCl 溶液,生成白色沉
2 2
淀
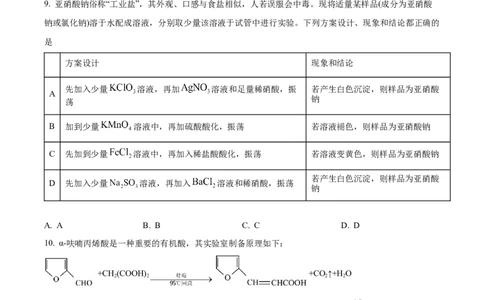
9. 亚硝酸钠俗称“工业盐”,其外观、口感与食盐相似,人若误服会中毒。现将适量某样品(成分为亚硝酸
钠或氯化钠)溶于水配成溶液,分别取少量该溶液于试管中进行实验。下列方案设计、现象和结论都正确的
是
方案设计 现象和结论
先加入少量 溶液,再加 溶液和足量稀硝酸,振 若产生白色沉淀,则样品为亚硝酸
A
钠
荡
B 加到少量 溶液中,再加硫酸酸化,振荡 若溶液褪色,则样品为亚硝酸钠
C 先加到少量 溶液中,再加入稀盐酸酸化,振荡 若溶液变黄色,则样品为亚硝酸钠
若产生白色沉淀,则样品为亚硝酸
D 先加入少量 溶液,再加入 溶液和稀硝酸,振荡
钠
A. A B. B C. C D. D
10. α-呋喃丙烯酸是一种重要的有机酸,其实验室制备原理如下:
+CH (COOH) +CO ↑+H O
2 2 2 2
制备α-呋喃丙烯酸的步骤如下:向三颈烧瓶中依次加入丙二酸、糠醛和吡啶,在95℃下回流2小时,停止
反应;将混合物倒入冷的3mol·L-1盐酸中析出淡黄色沉淀,将其置于冰水中1小时,过滤,用水洗涤2~3
次,得到粗产品。实验装置如图所示。下列说法正确的是
A. 仪器A的a口为进水口
B. 不产生气泡时表明三颈烧瓶中反应已完成
C. 冷的盐酸和冰水的主要作用是提高晶体纯度
D. 过滤后洗涤时,向漏斗中注满蒸馏水并不断搅拌
11. 在我国,粉煤灰排放量是仅次于尼矿的工业固废。粉煤灰的主要组成为 、 ,含少量 、
CaO等,可利用酸碱联合法回收粉煤灰中 和 ,回收流程如下图所示。
已知:低温拜尔法反应原理之一为 、
。下列说法错误的是
A. 水浸后,溶液进行蒸发浓缩、冷却结晶、过滤、洗涤得到粗硫酸铝晶体
B. 滤渣的主要成分为
C. 还原焙烧的主要反应为
D. 低温拜尔法所得滤液不可循环利用
12. 氧化锆是一种高级耐火材料,氧化钇主要用作制造微波用磁性材料。一种利用玻璃窑炉替换下的锆废砖(主要成分ZrO、YO、CaO等)提纯氧化锆和氧化钇的工艺流程如下:
2 2 3
下列说法正确的是
A. “酸化”是锆废砖粉和硫酸在硫酸铵催化作用下进行的焙烧反应,硫酸适宜用盐酸代替
B. “中和1”发生反应的离子方程式为Zr4+ +4OH- =Zr(OH) ↓
4
C. 实验室模拟“焙烧”时使用的硅酸盐仪器只有烧杯和酒精灯
D. 滤液2可以处理后返回“酸化”使用,实现循环
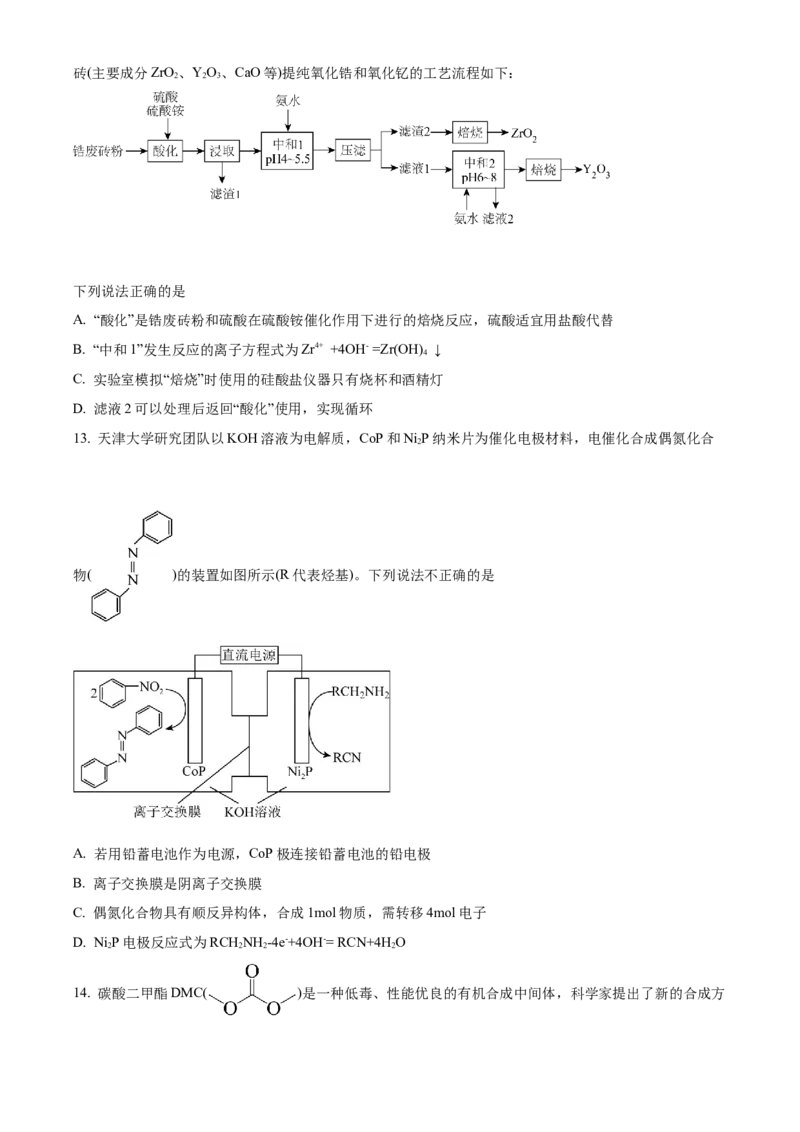
13. 天津大学研究团队以KOH溶液为电解质,CoP和Ni P纳米片为催化电极材料,电催化合成偶氮化合
2
物( )的装置如图所示(R代表烃基)。下列说法不正确的是
A. 若用铅蓄电池作为电源,CoP极连接铅蓄电池的铅电极
B. 离子交换膜是阴离子交换膜
C. 偶氮化合物具有顺反异构体,合成1mol物质,需转移4mol电子
D. Ni P电极反应式为RCHNH -4e-+4OH-= RCN+4HO
2 2 2 2
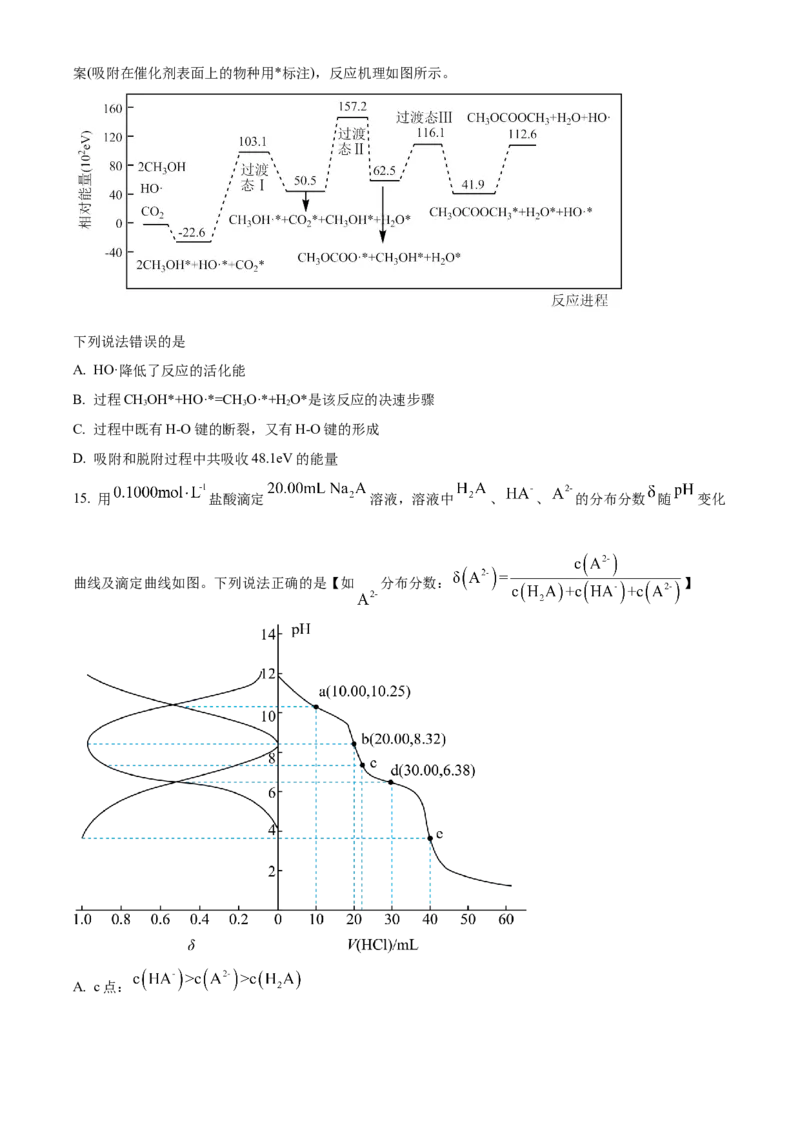
14. 碳酸二甲酯DMC( )是一种低毒、性能优良的有机合成中间体,科学家提出了新的合成方案(吸附在催化剂表面上的物种用*标注),反应机理如图所示。
下列说法错误的是
A. HO·降低了反应的活化能
B. 过程CHOH*+HO·*=CH O·*+HO*是该反应的决速步骤
3 3 2
C. 过程中既有H-O键的断裂,又有H-O键的形成
D. 吸附和脱附过程中共吸收48.1eV的能量
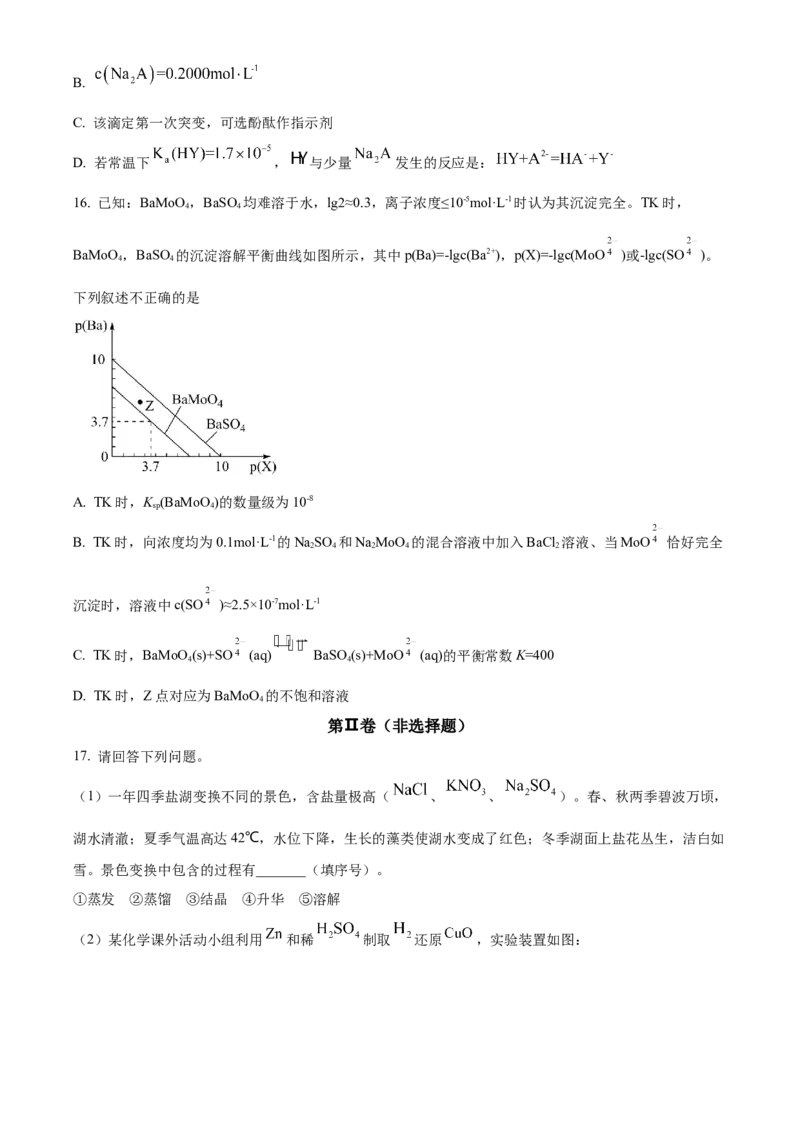
15. 用 盐酸滴定 溶液,溶液中 、 、 的分布分数 随 变化
曲线及滴定曲线如图。下列说法正确的是【如 分布分数: 】
A. c点:B.
C. 该滴定第一次突变,可选酚酞作指示剂
D. 若常温下 , 与少量 发生的反应是:
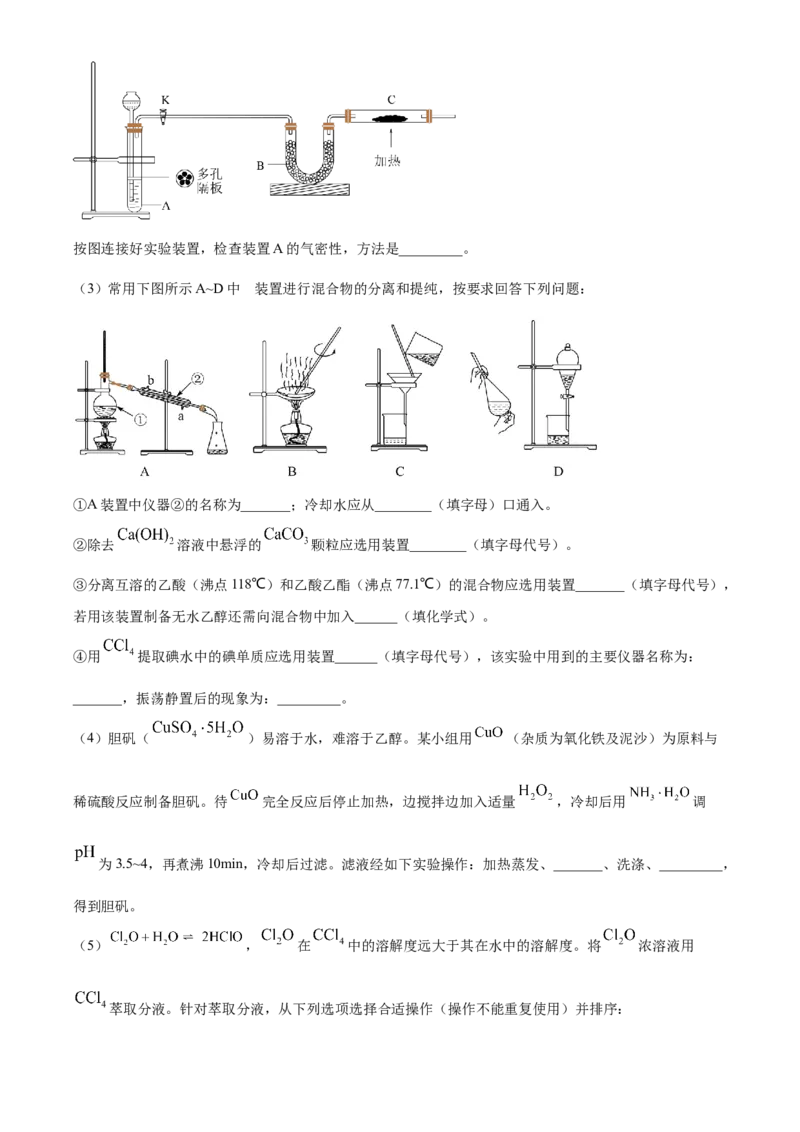
16. 已知:BaMoO,BaSO 均难溶于水,lg2≈0.3,离子浓度≤10-5mol·L-1时认为其沉淀完全。TK时,
4 4
BaMoO,BaSO 的沉淀溶解平衡曲线如图所示,其中p(Ba)=-lgc(Ba2+),p(X)=-lgc(MoO )或-lgc(SO )。
4 4
下列叙述不正确的是
A. TK时,K (BaMoO )的数量级为10-8
sp 4
B. TK时,向浓度均为0.1mol·L-1的NaSO 和NaMoO 的混合溶液中加入BaCl 溶液、当MoO 恰好完全
2 4 2 4 2
沉淀时,溶液中c(SO )≈2.5×10-7mol·L-1
C. TK时,BaMoO(s)+SO (aq) BaSO(s)+MoO (aq)的平衡常数K=400
4 4
D. TK时,Z点对应为BaMoO 的不饱和溶液
4
第Ⅱ卷(非选择题)
17. 请回答下列问题。
(1)一年四季盐湖变换不同的景色,含盐量极高( 、 、 )。春、秋两季碧波万顷,
湖水清澈;夏季气温高达42℃,水位下降,生长的藻类使湖水变成了红色;冬季湖面上盐花丛生,洁白如
雪。景色变换中包含的过程有_______(填序号)。
①蒸发 ②蒸馏 ③结晶 ④升华 ⑤溶解
(2)某化学课外活动小组利用 和稀 制取 还原 ,实验装置如图:按图连接好实验装置,检查装置A的气密性,方法是_________。
的
(3)常用下图所示A~D中 装置进行混合物的分离和提纯,按要求回答下列问题:
①A装置中仪器②的名称为_______;冷却水应从________(填字母)口通入。
②除去 溶液中悬浮的 颗粒应选用装置________(填字母代号)。
③分离互溶的乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合物应选用装置_______(填字母代号),
若用该装置制备无水乙醇还需向混合物中加入______(填化学式)。
④用 提取碘水中的碘单质应选用装置______(填字母代号),该实验中用到的主要仪器名称为:
_______,振荡静置后的现象为:_________。
(4)胆矾( )易溶于水,难溶于乙醇。某小组用 (杂质为氧化铁及泥沙)为原料与
稀硫酸反应制备胆矾。待 完全反应后停止加热,边搅拌边加入适量 ,冷却后用 调
为3.5~4,再煮沸10min,冷却后过滤。滤液经如下实验操作:加热蒸发、_______、洗涤、_________,
得到胆矾。
(5) , 在 中的溶解度远大于其在水中的溶解度。将 浓溶液用
萃取分液。针对萃取分液,从下列选项选择合适操作(操作不能重复使用)并排序:c→_______→e→_______。
a.检查旋塞、玻璃塞处是否漏水
b.将溶液和 转入分液漏斗
c.涂凡士林
d.旋开旋塞放气
e.倒转分液漏斗,小心振摇
f.经几次振摇并放气后,将分液漏斗置于铁架台上静置
g.打开旋塞,向锥形瓶放出下层液体
18. 摩尔盐 是一种常见的复盐。以下是摩尔盐的制备流程。请回答相关问题。
取适量的废铁屑于锥形瓶 加入15 mL 3molL' 在滤液中加入一定量的
中,加15mL10% ,水浴加 固体,加热浓
→ →
溶液,小火加热煮沸 热至反应完成,趁 缩,冷却结晶,抽滤并洗
2min,分离并洗涤 热抽滤 涤
步骤1:铁屑的净化 步骤2: 步骤3:摩尔盐的制备
(1)步骤2的名称应为_______。
(2)抽滤装置如图所示。和普通过滤相比,抽滤的优点是______。
(3)加热浓缩时所用到的主要仪器中属于硅酸盐材质的有酒精灯、玻璃棒和_________。
(4)生成摩尔盐的反应方程式为_______。
(5)步骤3中将滤液加热浓缩至______即停止加热,这样做的原因是_________。
(6)步骤3抽滤后用乙醇洗涤后再用滤纸吸干。用乙醇洗涤的原因是________。
(7) 含量是影响产品品质的关键指标。定量测定方法是:取1.00g产品于烧杯中,加入适量盐酸溶解,
并加入3滴 溶液,定容至50mL,取溶液置于比色管中,与标准色阶进行目视比色,确定产品级别。可以根据颜色确定产品级别的原理是_______。
(8)取30.00g所制得的固体于小烧杯中,加入适量稀硫酸,溶解后在250 mL容量瓶中定容。取25.00 mL
于锥形瓶中,用0.1 的 ,溶液滴定至终点。平行操作三次,消耗 溶液的平均体
积为16.00 mL。此样品中 含量为_______%(保留小数点后1位)。导致该测定结果与理论值有偏差
的可能原因是_______。
A.配溶液定容时俯视刻度线
B.取摩尔盐溶液的滴定管没有润洗
C.取待测液的锥形瓶洗净后未干燥
D.摩尔盐的结晶水数量不足
19. 丙烯(C H)是石油化工行业重要的有机原料之一,主要用于生产聚丙烯、二氯丙烷、异丙醇等产品。回
3 6
答下列问题:
(1)丙烷脱氢制备丙烯。由图可得C H(g)=C H(g)+H(g) ΔH=_______kJ·mol-1。
3 8 3 6 2
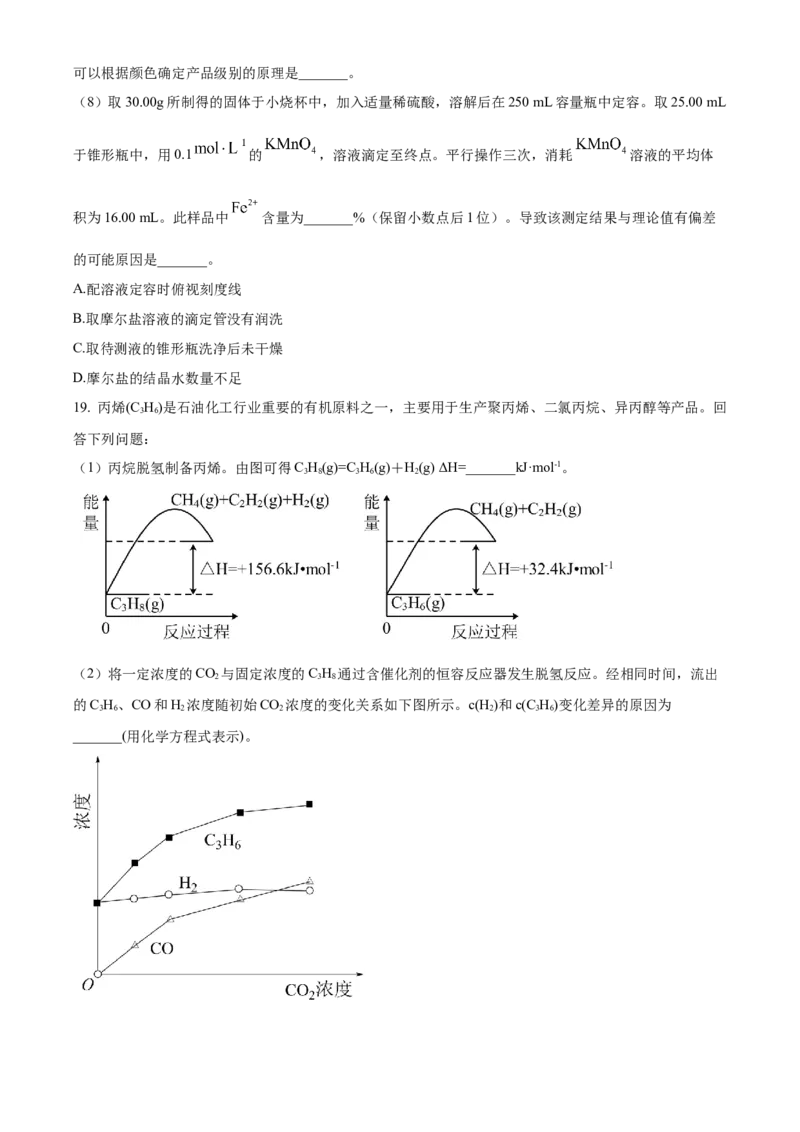
(2)将一定浓度的CO 与固定浓度的C H 通过含催化剂的恒容反应器发生脱氢反应。经相同时间,流出
2 3 8
的C H、CO和H 浓度随初始CO 浓度的变化关系如下图所示。c(H)和c(C H)变化差异的原因为
3 6 2 2 2 3 6
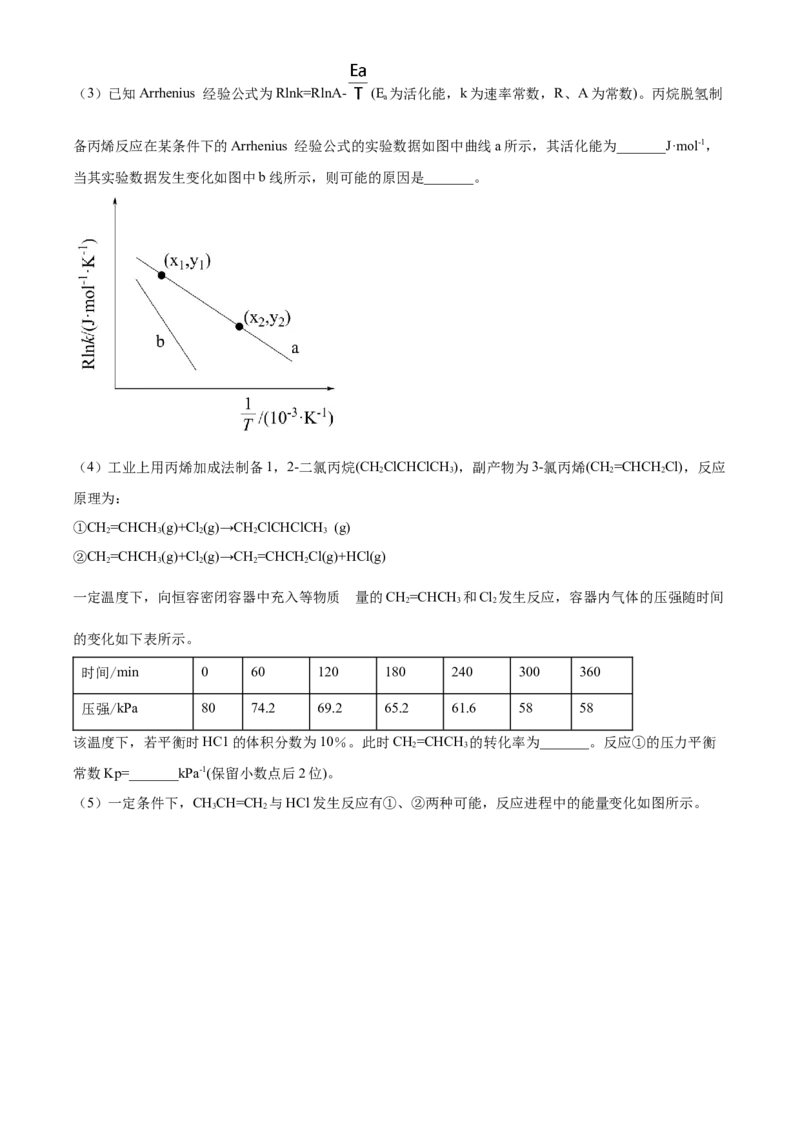
_______(用化学方程式表示)。(3)已知Arrhenius 经验公式为Rlnk=RlnA- (E 为活化能,k为速率常数,R、A为常数)。丙烷脱氢制
a
备丙烯反应在某条件下的Arrhenius 经验公式的实验数据如图中曲线a所示,其活化能为_______J·mol-1,
当其实验数据发生变化如图中b线所示,则可能的原因是_______。
(4)工业上用丙烯加成法制备1,2-二氯丙烷(CHClCHClCH ),副产物为3-氯丙烯(CH=CHCHCl),反应
2 3 2 2
原理为:
①CH=CHCH(g)+Cl (g)→CH ClCHClCH (g)
2 3 2 2 3
②CH=CHCH(g)+Cl (g)→CH =CHCHCl(g)+HCl(g)
2 3 2 2 2
的
一定温度下,向恒容密闭容器中充入等物质 量的CH=CHCH 和Cl 发生反应,容器内气体的压强随时间
2 3 2
的变化如下表所示。
时间/min 0 60 120 180 240 300 360
压强/kPa 80 74.2 69.2 65.2 61.6 58 58
该温度下,若平衡时HC1的体积分数为10%。此时CH=CHCH 的转化率为_______。反应①的压力平衡
2 3
常数Kp=_______kPa-1(保留小数点后2位)。
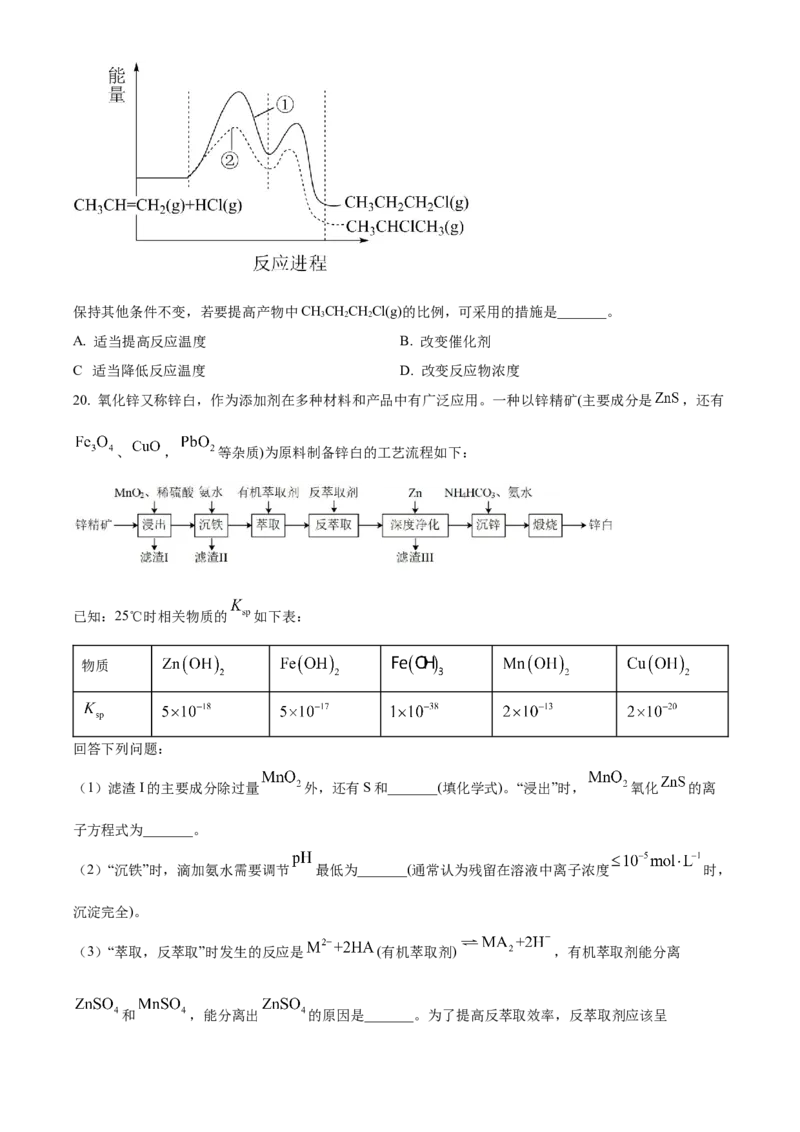
(5)一定条件下,CHCH=CH 与HCl发生反应有①、②两种可能,反应进程中的能量变化如图所示。
3 2保持其他条件不变,若要提高产物中CHCHCHCl(g)的比例,可采用的措施是_______。
3 2 2
A. 适当提高反应温度 B. 改变催化剂
.
C 适当降低反应温度 D. 改变反应物浓度
20. 氧化锌又称锌白,作为添加剂在多种材料和产品中有广泛应用。一种以锌精矿(主要成分是 ,还有
、 , 等杂质)为原料制备锌白的工艺流程如下:
已知:25℃时相关物质的 如下表:
物质
回答下列问题:
(1)滤渣I的主要成分除过量 外,还有S和_______(填化学式)。“浸出”时, 氧化 的离
子方程式为_______。
(2)“沉铁”时,滴加氨水需要调节 最低为_______(通常认为残留在溶液中离子浓度 时,
沉淀完全)。
(3)“萃取,反萃取”时发生的反应是 (有机萃取剂) ,有机萃取剂能分离
和 ,能分离出 的原因是_______。为了提高反萃取效率,反萃取剂应该呈_______(填“酸”“碱”或“中”)性。
(4)“深度净化”中加 的目的是_______。
(5)①“沉锌”时,充分反应,过滤,洗涤得到碱式碳酸锌[ ],其反应的离子方程式
为_______,检验沉淀洗涤干净的方法是_______。
②为测定碱式碳酸锌[ ]的组成,称取一定量的碱式碳酸锌,充分加热分解,产生的
气体依次通过足量浓硫酸和碱石灰,分别增重0.72g和0.88g,则该碱式碳酸锌的化学式为_______。下载最新免费模拟卷,到公众号:一枚试卷君