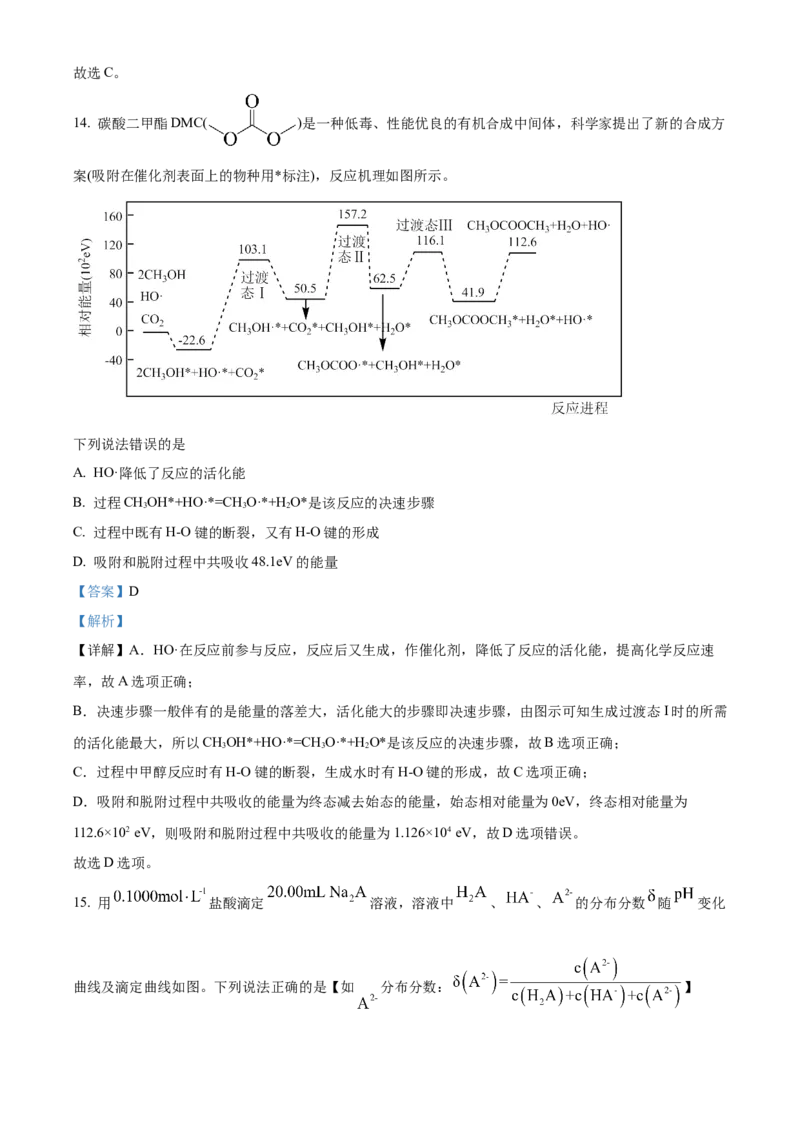
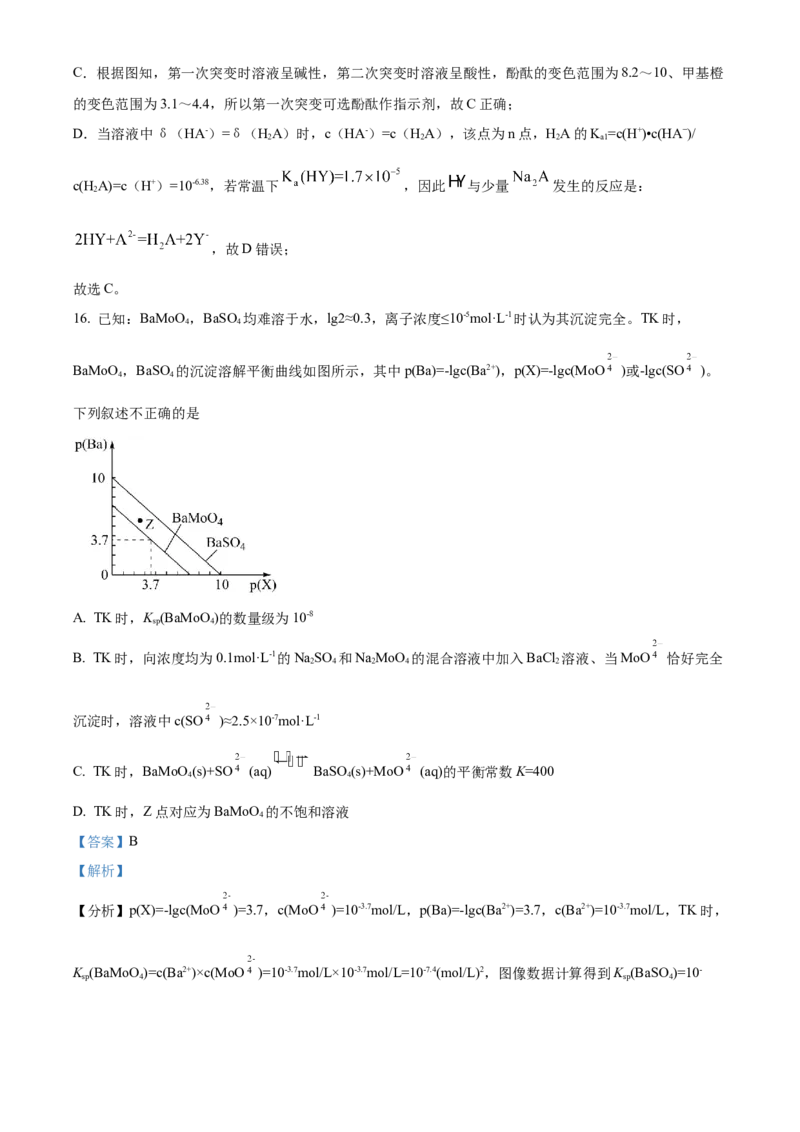
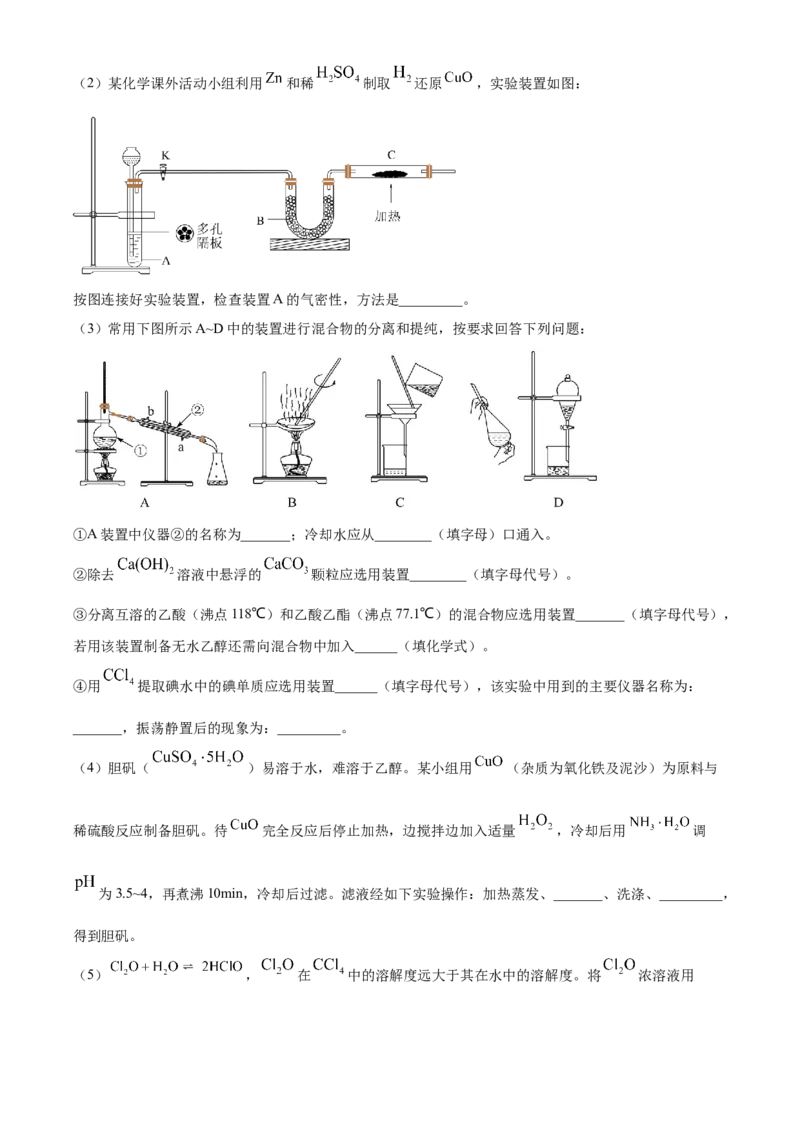
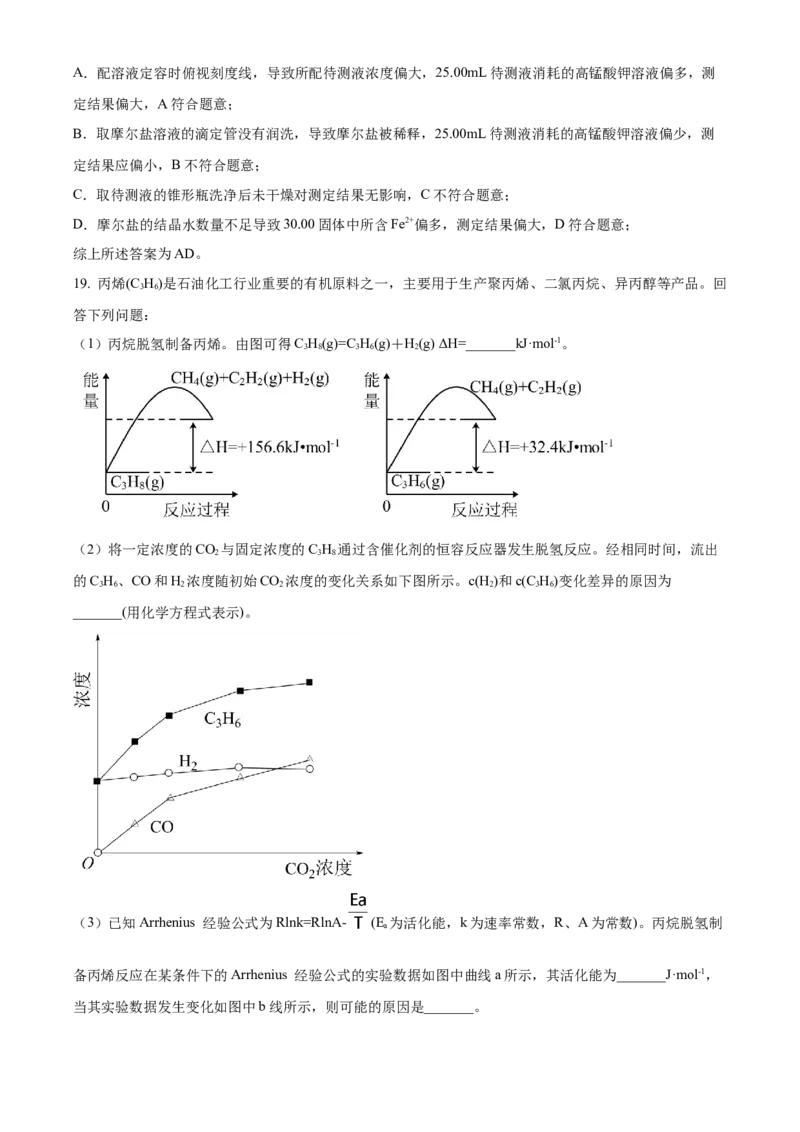
文档内容
南阳一中 2023 届高三第一次阶段性考试
化学试题
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Fe-56
第Ⅰ卷(选择题)
一、单选题
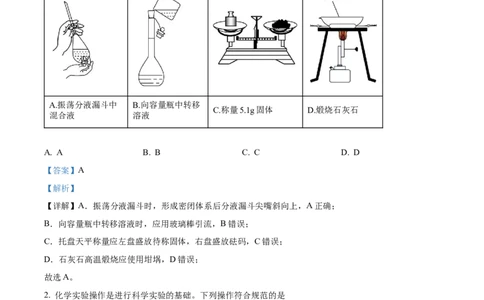
1. 下列对装置或仪器的使用或操作规范的是
A.振荡分液漏斗中 B.向容量瓶中转移
C.称量5.1g固体 D.煅烧石灰石
混合液 溶液
A. A B. B C. C D. D
【答案】A
【解析】
【详解】A.振荡分液漏斗时,形成密闭体系后分液漏斗尖嘴斜向上,A正确;
B.向容量瓶中转移溶液时,应用玻璃棒引流,B错误;
C.托盘天平称量应左盘盛放待称固体,右盘盛放砝码,C错误;
D.石灰石高温煅烧应使用坩埚,D错误;
故选A。
2. 化学实验操作是进行科学实验的基础。下列操作符合规范的是
A.碱式滴定管排气泡 B.溶液加热 C.试剂存放 D.溶液滴加
A. A B. B C. C D. D
下载最新免费模拟卷,到公众号:一枚试卷君【答案】A
【解析】
【详解】A.碱式滴定管排气泡时,把橡皮管向上弯曲,出口上斜,轻轻挤压玻璃珠附近的橡皮管可以使
溶液从尖嘴涌出,气泡即可随之排出,A符合规范;
B.用试管加热溶液时,试管夹应夹在距离管口的 处,B不符合规范;
C.实验室中,盐酸和NaOH要分开存放,有机物和无机物要分开存放,C不符合规范;
D.用滴管滴加溶液时,滴管不能伸入试管内部,应悬空滴加,D不符合规范;
故选A。
3. 乙酰苯胺 可用作止痛剂、退热剂,制备装置如图所示。反应原理为:
。已知苯胺可溶于水,沸点 ,接触空气
易被氧化;冰醋酸的沸点为 。乙酰苯胺的溶解度如下表:
温度/ 20 25 50 80 100
溶解度/g 0.46 0.56 0.84 3.45 5.5
下列说法错误的是
A. 反应物中加入适量锌粉,防止苯胺被氧化
B. 使用球形冷凝管可以提高反应物的转化率
C. 用水浴加热效果更佳
D. 反应结束后,将锥形瓶中反应液倒入冷水中,过滤、洗涤,可获得乙酰苯胺晶体
【答案】C
【解析】
【详解】A.由于苯胺接触空气易被氧化,反应物中加入适量锌粉,锌粉可与酸反应生成氢气,形成氢气环境,从而防止苯胺被氧化,故A正确;
B.球形冷凝管内管曲面多,可使蒸气与冷凝液充分进行热量交换,可使更多蒸发出去的有机物冷凝为液
态回流,减小反应物蒸发损失,使反应充分进行,可以提高反应物的转化率,故B正确;
C.由题中信息可知,制取乙酰苯胺 的反应温度为105 ,大于水的沸点,所以该反
应不能使用水浴加热,故C错误;
D.由题中信息可知,反应物苯胺、乙酸均溶于水,产物乙酰苯胺在20 时溶解度很小,所以,反应结束
后,将锥形瓶中反应液倒入冷水中,乙酰苯胺为沉淀,过滤、洗涤,可获得乙酰苯胺晶体,故D正确;
答案为C。
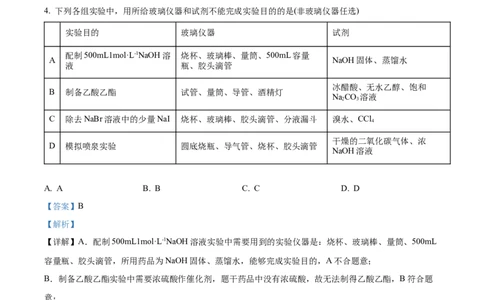
4. 下列各组实验中,用所给玻璃仪器和试剂不能完成实验目的的是(非玻璃仪器任选)
实验目的 玻璃仪器 试剂
配制500mL1mol·L-1NaOH溶 烧杯、玻璃棒、量筒、500mL容量
A NaOH固体、蒸馏水
液 瓶、胶头滴管
冰醋酸、无水乙醇、饱和
B 制备乙酸乙酯 试管、量筒、导管、酒精灯
NaCO 溶液
2 3
C 除去NaBr溶液中的少量NaI 烧杯、玻璃棒、胶头滴管、分液漏斗 溴水、CCl
4
干燥的二氧化碳气体、浓
D 模拟喷泉实验 圆底烧瓶、导气管、烧杯、胶头滴管
NaOH溶液
A. A B. B C. C D. D
【答案】B
【解析】
【详解】A.配制500mL1mol·L-1NaOH溶液实验中需要用到的实验仪器是:烧杯、玻璃棒、量筒、500mL
容量瓶、胶头滴管,所用药品为NaOH固体、蒸馏水,能够完成实验目的,A不合题意;
B.制备乙酸乙酯实验中需要浓硫酸作催化剂,题干药品中没有浓硫酸,故无法制得乙酸乙酯,B符合题
意;
C.除去NaBr溶液中的少量NaI,可以向混合溶液中加入适当过量的Br 水,发生反应:
2
2NaI+Br =2NaBr+I ,然后再用CCl 萃取出I 和过量的Br ,故实验仪器要烧杯、玻璃棒、胶头滴管、分液
2 2 4 2 2
漏斗,可以达到实验目的,C不合题意;
D.由于CO+2NaOH=Na CO+H O,可以使盛满CO 的圆底烧瓶中气体压强快速减小,形成喷泉,故用圆
2 2 3 2 2
底烧瓶收集满一瓶CO,用圆底烧瓶、导气管、烧杯、胶头滴管连接实验装置,可以形成喷泉,D不合题
2
意;
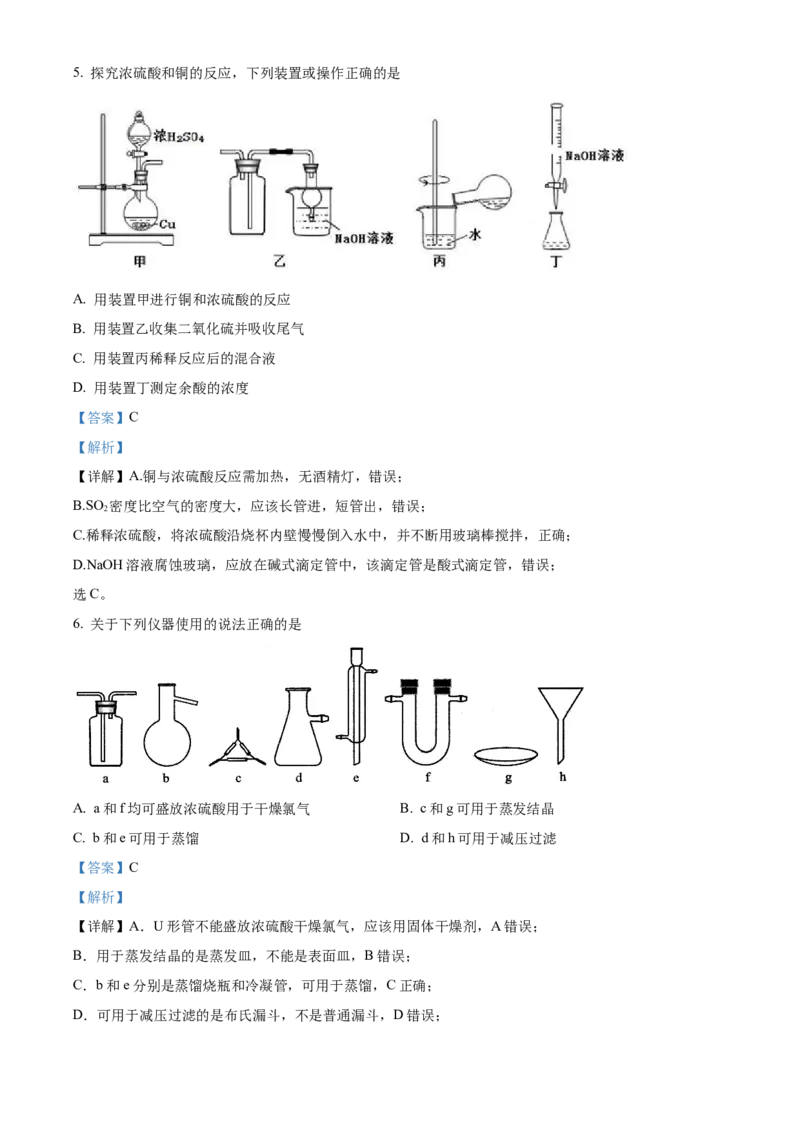
故答案为:B。5. 探究浓硫酸和铜的反应,下列装置或操作正确的是
A. 用装置甲进行铜和浓硫酸的反应
B. 用装置乙收集二氧化硫并吸收尾气
C. 用装置丙稀释反应后的混合液
D. 用装置丁测定余酸的浓度
【答案】C
【解析】
【详解】A.铜与浓硫酸反应需加热,无酒精灯,错误;
B.SO 密度比空气的密度大,应该长管进,短管出,错误;
2
C.稀释浓硫酸,将浓硫酸沿烧杯内壁慢慢倒入水中,并不断用玻璃棒搅拌,正确;
D.NaOH溶液腐蚀玻璃,应放在碱式滴定管中,该滴定管是酸式滴定管,错误;
选C。
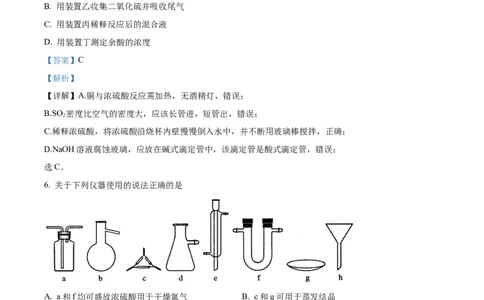
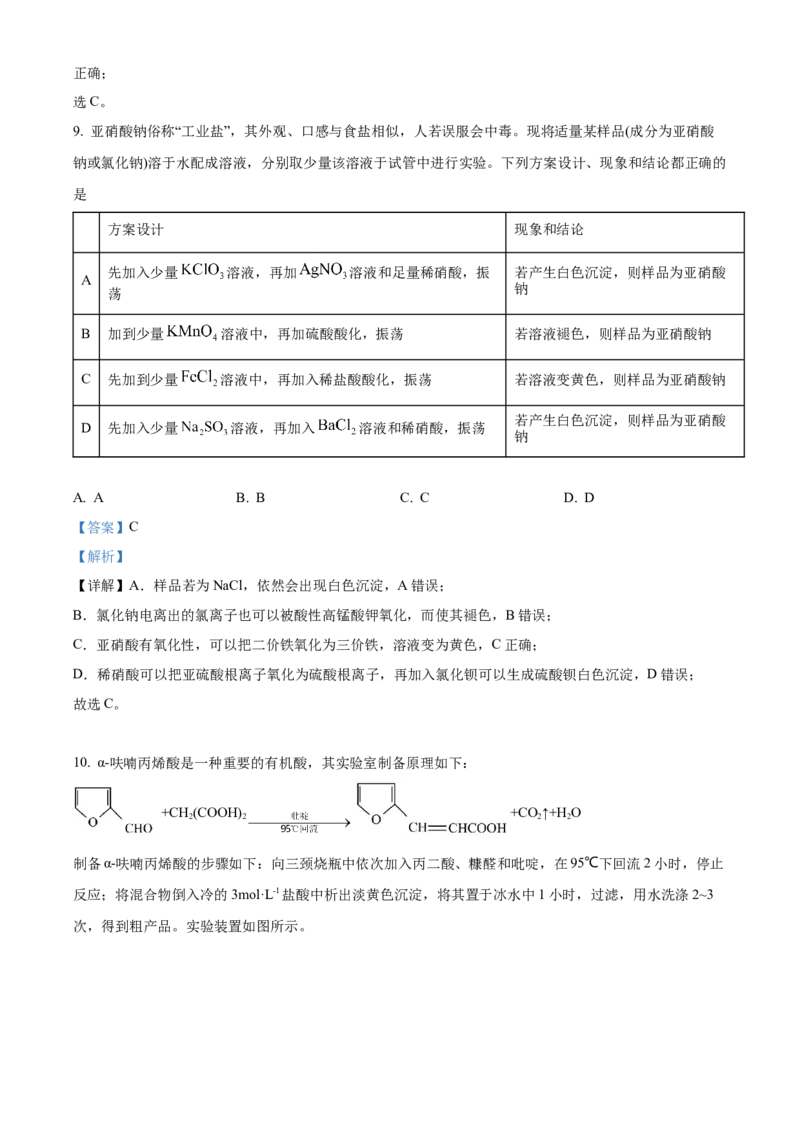
6. 关于下列仪器使用的说法正确的是
A. a和f均可盛放浓硫酸用于干燥氯气 B. c和g可用于蒸发结晶
C. b和e可用于蒸馏 D. d和h可用于减压过滤
【答案】C
【解析】
【详解】A.U形管不能盛放浓硫酸干燥氯气,应该用固体干燥剂,A错误;
B.用于蒸发结晶的是蒸发皿,不能是表面皿,B错误;
C.b和e分别是蒸馏烧瓶和冷凝管,可用于蒸馏,C正确;
D.可用于减压过滤的是布氏漏斗,不是普通漏斗,D错误;答案选C。
7. 下列实验操作、现象、解释或结论都正确的是
选
实验操作 现象 解释或结论
项
有气体产 生成了HI
A 加热NaI固体和浓磷酸的混合物
生 气体
Al产生的 金属性:
B 取等物质的量的Al和Fe,分别与足量的稀盐酸反应
氢气多 Al>Fe
浊液变澄 酸性:苯酚
C 向苯酚浊液中滴加饱和NaCO 溶液
2 3 清 >碳酸
分别在20℃、30℃下,取0.1mol·L-1KI溶液,向其中 30℃下出 探究反应速
D 先加入0.1mol·L-1的硫酸,再加入淀粉溶液,发生反应 现蓝色的 率与温度的
4H++O +4I-=2I +2H O 时间短 关系
2 2 2
A. A B. B C. C D. D
【答案】A
【解析】
【详解】A.加热NaI固体和浓磷酸的混合物,由于HI氢易挥发,浓磷酸不易挥发,会有HI气体生成,
故A正确;
的
B.取等物质 量的Al和Fe,分别与足量的稀盐酸反应, Al产生的氢气多, 说明Al失去的电子数多,
但金属性与失去电子数多少无关,不能比较Al、Fe的金属性,故B错误;
C.向苯酚浊液中滴加饱和NaCO 溶液,反应生成苯酚钠、碳酸氢钠,浊液变澄清,说明酸性:苯酚>碳
2 3
酸氢根,故C错误;
D.若先加硫酸,先发生反应4H++O +4I-=2I +2H O,在20℃、30℃都会反应生成碘,加入淀粉都会变蓝,
2 2 2
应先加入淀粉,再加硫酸进行反应,故D错误;
答案选A。
8. 无水FeCl 常作为芳烃氯代反应的催化剂。某研究小组设计了如图流程,以废铁屑(含有少量碳和SiO 杂
3 2
质)为原料制备无水FeCl (s):
3已知:氯化亚砜( )熔点-101℃,沸点76℃,易水解。
下列有关说法不正确的是
A. 操作①是过滤,用到的玻璃仪器有烧杯、玻璃棒和漏斗
B. 反应D→E的化学方程式为FeCl ·6H O+6SOCl FeCl +6SO↑+12HCl↑
3 2 2 3 2
C. 该制备流程中试剂B可选用高锰酸钾溶液或稀硝酸
D. 由D转化成E的过程中可能产生少量亚铁盐,其原因可能是生成的SO 将Fe3+还原成Fe2+,为了验证是
2
SO 将Fe3+还原应进行的实验操作和现象是:取样溶解后,先加盐酸酸化,再加入BaCl 溶液,生成白色沉
2 2
淀
【答案】C
【解析】
【分析】由流程可知:废铁屑(含有少量碳和 杂质)加入盐酸,铁粉与盐酸反应生成氯化亚铁,过滤除
去少量碳和 杂质,A(氯化亚铁)加入氧化剂B生成C(氯化铁),通入HCl蒸发结晶生成 ,
通入 ,生成 。
【详解】A.操作①是过滤,过滤用到的玻璃仪器有烧杯、玻璃棒和漏斗,故A正确;
B.根据已知信息氯化亚砜( )熔点-101℃,沸点76℃,易水解, 与 反应
生成 的化学方程式为 ,故B正确;
C.该流程中试剂B的作用是将 氧化成 ,酸性高锰酸钾溶液或稀硝酸都可以将 氧化成 ,
但都会引入新杂质,为了不引入新杂质,试剂B应选用氯水或 ,故C错误;
D.由D→E的化学方程式可知反应中生成的二氧化硫可将氯化铁还原为氯化亚铁,若是 作还原剂,
则氧化产物为硫酸盐,故若加盐酸酸化,再加 溶液,产生白色沉淀,则是二氧化硫作还原剂,故D正确;
选C。
9. 亚硝酸钠俗称“工业盐”,其外观、口感与食盐相似,人若误服会中毒。现将适量某样品(成分为亚硝酸
钠或氯化钠)溶于水配成溶液,分别取少量该溶液于试管中进行实验。下列方案设计、现象和结论都正确的
是
方案设计 现象和结论
先加入少量 溶液,再加 溶液和足量稀硝酸,振 若产生白色沉淀,则样品为亚硝酸
A
钠
荡
B 加到少量 溶液中,再加硫酸酸化,振荡 若溶液褪色,则样品为亚硝酸钠
C 先加到少量 溶液中,再加入稀盐酸酸化,振荡 若溶液变黄色,则样品为亚硝酸钠
若产生白色沉淀,则样品为亚硝酸
D 先加入少量 溶液,再加入 溶液和稀硝酸,振荡
钠
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.样品若为NaCl,依然会出现白色沉淀,A错误;
B.氯化钠电离出的氯离子也可以被酸性高锰酸钾氧化,而使其褪色,B错误;
C.亚硝酸有氧化性,可以把二价铁氧化为三价铁,溶液变为黄色,C正确;
D.稀硝酸可以把亚硫酸根离子氧化为硫酸根离子,再加入氯化钡可以生成硫酸钡白色沉淀,D错误;
故选C。
10. α-呋喃丙烯酸是一种重要的有机酸,其实验室制备原理如下:
+CH (COOH) +CO ↑+H O
2 2 2 2
制备α-呋喃丙烯酸的步骤如下:向三颈烧瓶中依次加入丙二酸、糠醛和吡啶,在95℃下回流2小时,停止
反应;将混合物倒入冷的3mol·L-1盐酸中析出淡黄色沉淀,将其置于冰水中1小时,过滤,用水洗涤2~3
次,得到粗产品。实验装置如图所示。下列说法正确 的是
A. 仪器A的a口为进水口
B. 不产生气泡时表明三颈烧瓶中反应已完成
C. 冷的盐酸和冰水的主要作用是提高晶体纯度
.
D 过滤后洗涤时,向漏斗中注满蒸馏水并不断搅拌
【答案】B
【解析】
【详解】A.仪器A为冷凝管,冷水应从下端流入,上口流出,故a口为出水口,故A错误;
B.由于反应中有 生成,会产生气泡,当不产生气泡时表明三颈烧瓶中反应已完成,故B正确;
C.冷的盐酸和冰水的主要作用是析出晶体,提高产率,故C错误;
D.洗涤时操作为:向漏斗中注满蒸馏水浸没固体,静置待水自然流下,重复 次,故D错误;
故答案为B。
11. 在我国,粉煤灰排放量是仅次于尼矿的工业固废。粉煤灰的主要组成为 、 ,含少量 、
CaO等,可利用酸碱联合法回收粉煤灰中 和 ,回收流程如下图所示。
已知:低温拜尔法反应原理之一为 、。下列说法错误的是
A. 水浸后,溶液进行蒸发浓缩、冷却结晶、过滤、洗涤得到粗硫酸铝晶体
B. 滤渣的主要成分为
C. 还原焙烧的主要反应为
D. 低温拜尔法所得滤液不可循环利用
【答案】D
【解析】
【分析】由题给流程可知,加入硫酸溶液熟化时,氧化铝、氧化铁溶于硫酸溶液得到可溶性硫酸盐,氧化
钙与硫酸溶液反应得到微溶的硫酸钙,二氧化硅不与硫酸溶液反应,水浸、过滤得到含有二氧化硅、少量
的硫酸钙的滤渣和含有可溶性硫酸盐的滤液;滤液经结晶、脱水得到硫酸盐晶体,硫酸盐与碳粉高温条件
下,焙烧得到粗氧化铝,向粗氧化铝中加入氢氧化钠溶液,将氧化铝转化为偏铝酸钠,过滤得到偏铝酸钠
溶液;偏铝酸钠溶液发生低温拜尔法反应后,过滤得到含有氢氧化钠的滤液和冶金级氧化铝,滤液可以重
新溶解粗氧化铝而循环使用;向滤渣中加入氢氧化钠溶液浸出得到硅酸钠溶液。
【详解】A.由分析可知,水浸后,滤液经蒸发浓缩、冷却结晶、过滤、洗涤得到含有硫酸铁晶体的粗硫
酸铝晶体,故A正确;
B.由分析可知,滤渣中二氧化硅、少量的硫酸钙,主要成分为二氧化硅,故B正确;
C.由分析可知,还原焙烧发生的主要反应为硫酸铝与碳高温下反应生成氧化铝、二氧化碳和二氧化硫,
反应的化学方程式为 ,故C正确;
D.由分析可知,偏铝酸钠溶液发生低温拜尔法反应后,过滤得到含有氢氧化钠的滤液和冶金级氧化铝,
滤液可以重新溶解粗氧化铝而循环使用,故D错误;
故选D。
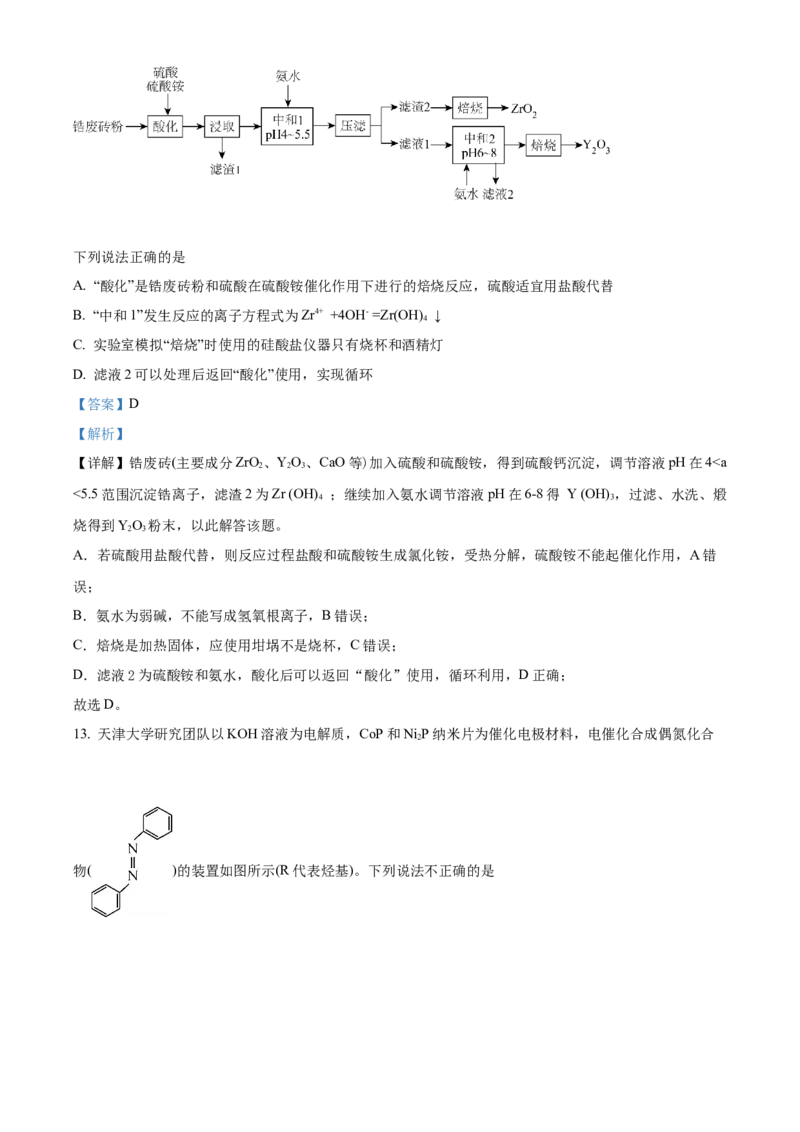
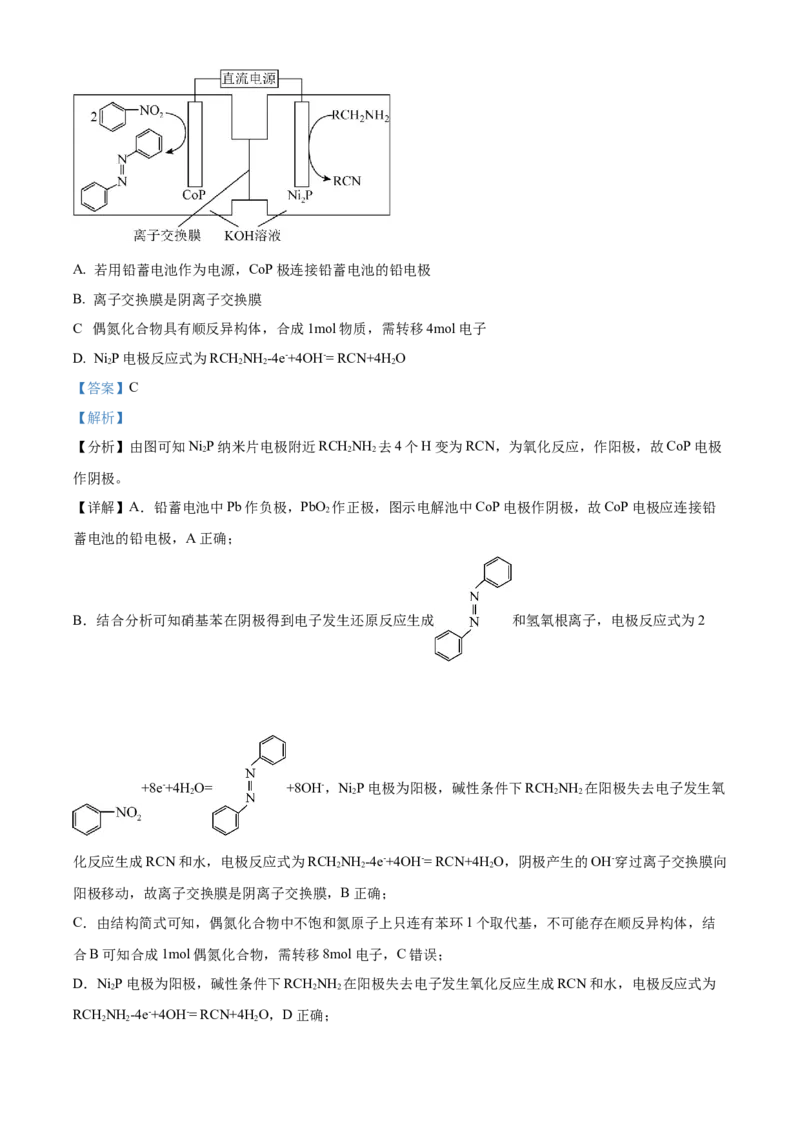
12. 氧化锆是一种高级耐火材料,氧化钇主要用作制造微波用磁性材料。一种利用玻璃窑炉替换下的锆废
砖(主要成分ZrO、YO、CaO等)提纯氧化锆和氧化钇的工艺流程如下:
2 2 3下列说法正确的是
A. “酸化”是锆废砖粉和硫酸在硫酸铵催化作用下进行的焙烧反应,硫酸适宜用盐酸代替
B. “中和1”发生反应的离子方程式为Zr4+ +4OH- =Zr(OH) ↓
4
C. 实验室模拟“焙烧”时使用的硅酸盐仪器只有烧杯和酒精灯
D. 滤液2可以处理后返回“酸化”使用,实现循环
【答案】D
【解析】
【详解】锆废砖(主要成分ZrO、YO、CaO等)加入硫酸和硫酸铵,得到硫酸钙沉淀,调节溶液pH在4