文档内容
红河州2023届高中毕业生第二次复习统一检测
理科综合(化学)参考答案及评分标准
一、选择题
题号 7 8 9 10 11 12 13
答案 C D A C B B D
7.【答案】C
【解析】C.喷油漆、涂油脂保护金属是物理方法,但金属表面钝化,是金属防护的化
学方法,故C错误。
8.【答案】D
【解析】A.配制 450mL0.02mol·L-1的 FeSO 溶液,要用 500ml 容量瓶,需要 2.78g
4
FeSO ·7H O,故A错误;
4 2
B.标况下SO 不是气体,故B错误。
3
C.先检验SO 再检验SO ,b、c装置中的试剂分别为BaCl 、品红溶液溶液,
3 2 2
故C错误。
9.【答案】A
【解析】A.左旋布洛芬与右旋布洛芬属于手性异构体,故A正确;
B.修饰产物中的-NH 中的N原子采取sp3杂化,故B错误;
2
C.与苯环相连接的碳原子上有氢原子,可被酸性KMnO 氧化,故C错误;
4
D.产物虚线内多于10个原子在同一平面上,故D错误。
10.【答案】C
【解析】根据已知条件推出:X是H,Y是N,Z是O,R是Na,W是P,L是S。
A.元素第一电离能应为Y>Z,即N>O,故A错误;
B.元素电负性应为:WS>P,即最简单
气态氢化物的稳定性为HO>HS>PH,故C正确;
2 2 3
D.简单离子半径应为W>L>Y>Z>R>X,即P3->S2->N3->O2->Na+>H+,故D错误。
11.【答案】B
【解析】A.向1mL浓度均为0.1mol·L-1的CuSO 和ZnSO 混合溶液中加入3mL等浓度
4 4
的 NaS 溶 液 , NaS 溶 液 过 量 , 产 生 黑 色 沉 淀 , 不 能 说 明
2 2
K (ZnS)>K (CuS),故A错误;
sp sp
B.NH 极易溶于水,在稀溶液中加入稀NaOH溶液,生成的氨水浓度小,不
3
加热NH 不会挥发出来,故B正确;
3
C.将乙醇与浓硫酸加热至140℃,主要发生乙醇分子间的脱水生成乙醚,反应
产生的气体通入酸性高锰酸钾溶液,溶液紫色褪去,不能证明乙醇发生了
消去反应生成了乙烯气体,因为加热时挥发出的乙醇、乙烯、副反应生成
的SO 都能使酸性 KMnO 溶液褪色,故C错误;
2 4
D.在试管中加入2mL 5%CuSO 溶液,滴加5滴10% NaOH溶液,硫酸铜溶液
4
过量,不会出现砖红色沉淀,故D错误。
12.【答案】B
【解析】钒液流电池是以+4、+5价态的钒氧离子溶液作为阳极的活性物质,以+2、+3
价态的钒离子溶液作为阴极的活性物质,分别储存在各自的电解液储罐中。充
理科综合(化学)参考答案及评分标准·第1页(共4页)
学科网(北京)股份有限公司放电过程中,主要是依靠电解液中H+在离子膜上的定向移动形成电流回路,根
据放电时b电极电极反应式为:V2+-e- =V3+,当生成2mol V3+时,电路中共转移
电子数为2N 。电池阳极反应:VO2+ + H O -e- = VO + + 2H+ ,阴极反应:V3+ +
A 2 2
e- = V2+,电池总反应为:VO + + V2+ + 2H+ VO2+ +V3+ + HO,故A、C
2 2
正确,B错误;全钒液流电池仅存在钒离子之间的反应,作为水性电解液不产
生有害物质,安全性高,故D正确。
13.【答案】D
【解析】 pH=-lgc(H+),所以随 pH 升高直线减小的是 lgc(H+),则直线升高的是
lgc(OH-),而pH升高时,HA会与氢氧根发生反应HA+OH-=H O+A-,所以开
2
始几乎不变,后续随pH增大而减少的是lgc(HA),随pH增大而增加,后续
几乎不变的是lgc(A-)。
A.据图可知O点处lgc(H+)=lgc(OH-),即c(H+)=c(OH-),溶液呈中性,温度为
25℃,所以pH=7,故A正确;
B.K (HA)= ,据图可知N点处c(A-)=c(HA),pH=4.74,即
a
c(H+)=10-4.74mol/L,所以K (HA)=10-4.74,数量级为10-5,故B正确;
a
C.该体系中c(HA)+c(A-)=0.1 mol·L-1,即c(A-)=0.1mol/L-c(HA),c(HA)=
= ,解得c(HA)=0.1c (H+)/[K +c
a
(H+)]mol·L-1,故C正确;
D.据图可知M点处c(A-)=c(H+),故D错误。
二、非选择题
27.(15分,除特殊标注外,每空2分)
(1)AlPO (1分)
4
(2)2Fe2+ + H O + 2H+ == 2Fe3+ + 2H O Fe3+催化HO 分解
2 2 2 2 2
(3)4
(4)加热浓缩(1分) 冷却结晶(1分)
(5)提高氟的利用率(答案合理即可)
(6)6 MgSiF MgF + SiF↑
6 2 4
【解析】
(2)Fe3+催化HO 分解,HO 的实际使用量远大于理论量。
2 2 2 2
(5)由信息可知,SiF 与水反应生成HSiF,与MgO反应生成MgSiF ,提高氟的利用率。
4 2 6 6
(6)由热重曲线分析,结合结晶水合物热重曲线变化规律可知,起点到A为失去x个结晶
水,剩余固体为MgSiF ,则:
4
MgSiF ·xHO MgSiF + xHO↑
6 2 6 2
166 18x
33.2g (54.8-33.2)g
x=6
B点组成为MgSiF ,由流程分析可知,MgSiF 分解生成SiF 且C点固体物质为镁的氟
6 6 4
理科综合(化学)参考答案及评分标准·第2页(共4页)
学科网(北京)股份有限公司化物,则根据Mg原子守恒可得n(Mg)=54.8/274mol=0.2mol,n(F)=(12.4-24×0.2)/
19=0.4mol,n(Mg):n(F)=1:2,C点固体组成为MgF ,化学方程式为MgSiF MgF +
2 6 2
SiF↑。
4
28.(14分,除特殊标注外,每空2分)
(1)球形冷凝管(1分) ab→ef→ij
(2)2MnO - + 10Cl- + 16H+ = 2Mn2+ + 5Cl↑ + 8HO
4 2 2
(3)SnCl + (x +2)HO = SnO ·xHO + 4HCl
4 2 2 2
(4)蒸馏(1分)
(5)将剩余的Cl 及产生的SnCl 蒸汽赶入后续装置收集和吸收
2 4
(6)① ZnSn N
3
②
29.(14分,除特殊标注外,每空2分)
(1) +40.8
(2)①选择性 ②B、C
(3)①增加CO可使反应Ⅱ逆向进行,增大CO 和H 的浓度,提高乙醇的产率。(答到
2 2
增大压强不给分,一定要提到增加CO可使反应Ⅱ逆向进行才给分)
②d/tV mol/(L·min)
③ (5-2a-c-d )c/(ab)(其他合理答案也可以得分)
(4)k /k
正 逆
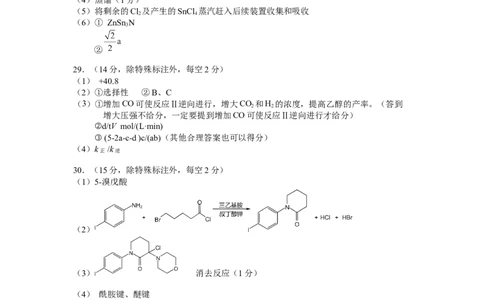
30.(15分,除特殊标注外,每空2分)
(1)5-溴戊酸
(2)
(3) 消去反应(1分)
(4) 酰胺键、醚键
(5)12 (1分)
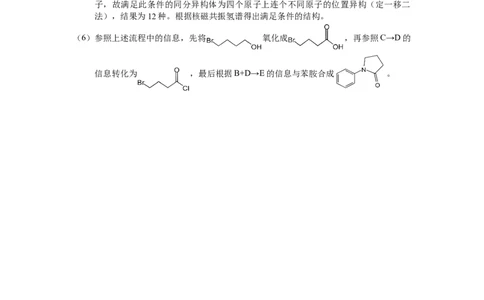
(6)
(3分,合理答案即可给分)
理科综合(化学)参考答案及评分标准·第3页(共4页)
学科网(北京)股份有限公司【解析】
(1)取代羧酸的命名以羧酸为母体,溴原子为取代基进行命名。
(2)根据流程信息可知,此反应为取代反应,由B和D生成E的同时有HCl、HBr产生。
(3)F生成H涉及两步反应,已知第一步的反应类型为取代反应,则F分子中的一个氯原
子被氮原子取代,根据H分子结构中未含氯原子而多出了碳碳双键,则第二步的反
应为脱去HCl的消去反应。
(4)根据I的结构简式得到含有的含氧官能团为酰胺键和醚键。
(5)根据C的分子结构结合不饱和度推知,分子中必须含有甲酸酯结构(-OOCH)和溴原
子,故满足此条件的同分异构体为四个原子上连个不同原子的位置异构(定一移二
法),结果为12种。根据核磁共振氢谱得出满足条件的结构。
(6)参照上述流程中的信息,先将 氧化成 ,再参照C→D的
信息转化为 ,最后根据B+D→E的信息与苯胺合成 。
理科综合(化学)参考答案及评分标准·第4页(共4页)
学科网(北京)股份有限公司理科综合(化学)参考答案及评分标准·第5页(共4页)
学科网(北京)股份有限公司