文档内容
考向 25 弱电解质的电离平衡
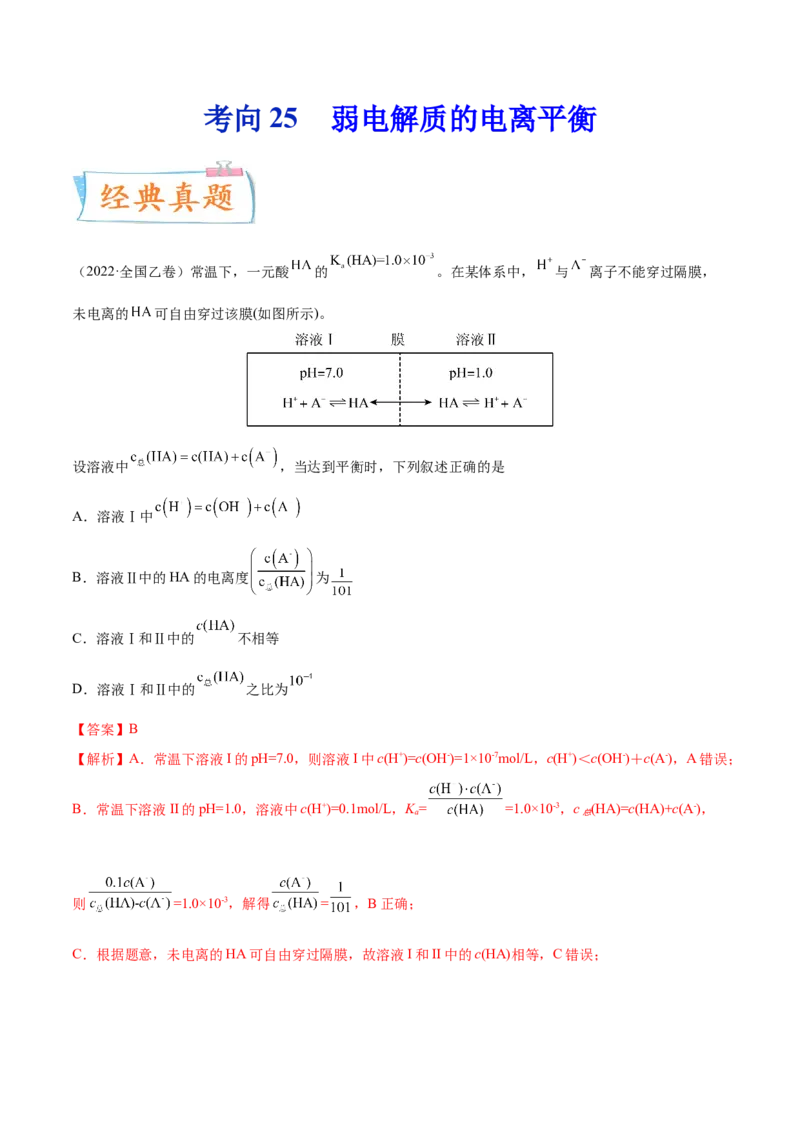
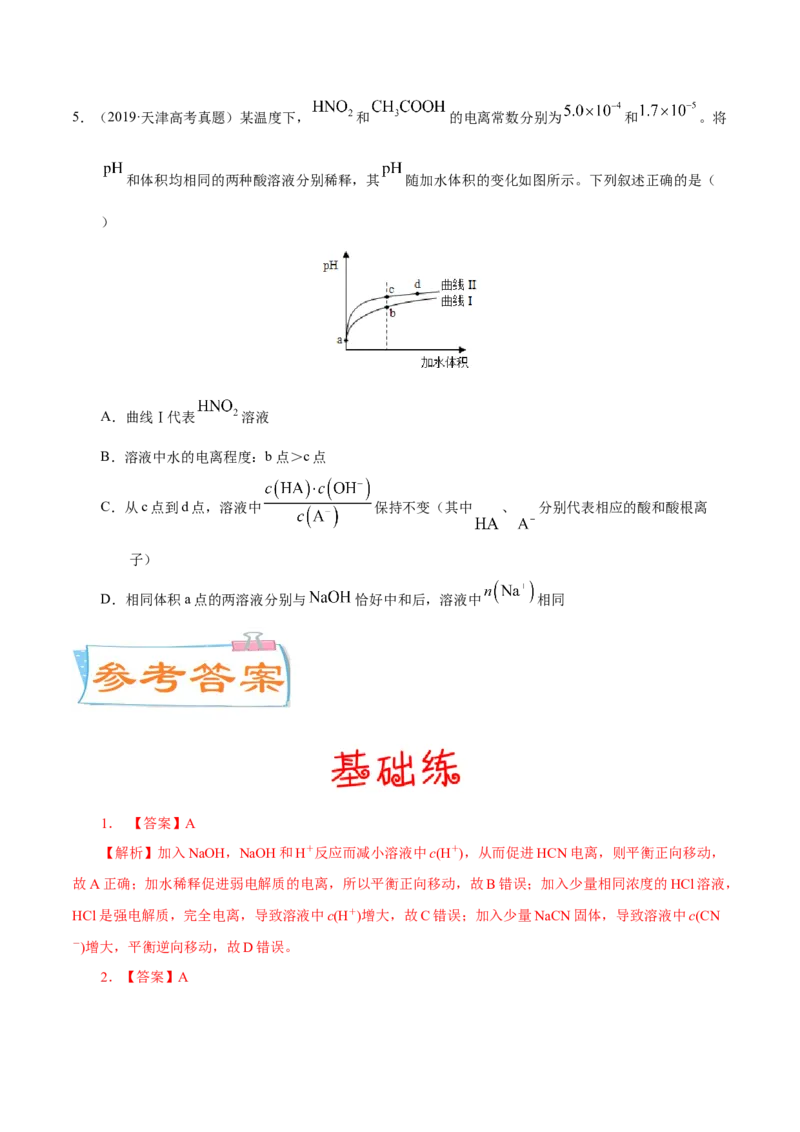
(2022·全国乙卷)常温下,一元酸 的 。在某体系中, 与 离子不能穿过隔膜,
未电离的 可自由穿过该膜(如图所示)。
设溶液中 ,当达到平衡时,下列叙述正确的是
A.溶液Ⅰ中
B.溶液Ⅱ中的HA的电离度 为
C.溶液Ⅰ和Ⅱ中的 不相等
D.溶液Ⅰ和Ⅱ中的 之比为
【答案】B
【解析】A.常温下溶液I的pH=7.0,则溶液I中c(H+)=c(OH-)=1×10-7mol/L,c(H+)<c(OH-)+c(A-),A错误;
B.常温下溶液II的pH=1.0,溶液中c(H+)=0.1mol/L,K = =1.0×10-3,c (HA)=c(HA)+c(A-),
a 总
则 =1.0×10-3,解得 = ,B正确;
C.根据题意,未电离的HA可自由穿过隔膜,故溶液I和II中的c(HA)相等,C错误;D.常温下溶液I的pH=7.0,溶液I中c(H+)=1×10-7mol/L,K = =1.0×10-3,c (HA)=c(HA)
a 总
+c(A-), =1.0×10-3,溶液I中c (HA)=(104+1)c(HA),溶液II的pH=1.0,溶液II中
总
c(H+)=0.1mol/L,K = =1.0×10-3,c (HA)=c(HA)+c(A-), =1.0×10-3,溶液II
a 总
中c (HA)=1.01c(HA),未电离的HA可自由穿过隔膜,故溶液I和II中的c(HA)相等,溶液I和II中c
总 总
(HA)之比为[(104+1)c(HA)]∶[1.01c(HA)]=(104+1)∶1.01≈104,D错误;
答案选B。知识点一 弱电解质的电离平衡
1.强、弱电解质
(1)定义与物质类别
(2)电离方程式的书写——“强等号,弱可逆,多元弱酸分步离”
①强电解质:如HSO :HSO == =2H + + SO_ 。
2 4 2 4
②弱电解质
a.一元弱酸,如CHCOOH:CHCOOHCH COO - + H + 。
3 3 3
b.多元弱酸,分步电离,分步书写且第一步电离程度远大于第二步电离程度,如HCO:
2 3
HCO H + + HCO_ 、 HCO H + + CO 。
2 3
c.多元弱碱,分步电离,一步书写,如Fe(OH) :Fe(OH) Fe 3 + + 3OH - 。
3 3
③酸式盐
a.强酸的酸式盐,如NaHSO 在水溶液中:
4
NaHSO == =Na + + H + + SO ;熔融时: NaHSO === Na + + HSO 。
4 4
b.弱酸的酸式盐:“强中有弱”,如NaHCO :
3
NaHCO == =Na + + HCO 、 HCO H + + CO 。
3
[名师点拨] (1)中学阶段常见的六大强酸是指HCl、HSO 、HNO、HBr、HI、HClO,其他一般是中
2 4 3 4
强酸或弱酸。
(2)中学阶段常见的四大强碱是指NaOH、KOH、Ca(OH) 、Ba(OH) ,其他一般是中强碱或弱碱。
2 2
2.弱电解质的电离平衡
(1)电离平衡的建立在一定条件(如温度、浓度等)下,当弱电解质分子电离成离子的速率和离子结合成弱电解质分子的速
率相等时,电离过程就达到平衡状态,即电离平衡。平衡建立过程如图所示:
(2)外因对电离平衡的影响
①浓度:在一定温度下,同一弱电解质溶液,浓度越小,越易电离。
②温度:温度越高,电离程度越大。
③相同离子:加入与弱电解质具有相同离子的电解质时,可使电离平衡向结合成弱电解质分子的方向
移动。
④化学反应:加入能与弱电解质电离出的离子反应的物质时,可使电离平衡向电离方向移动。
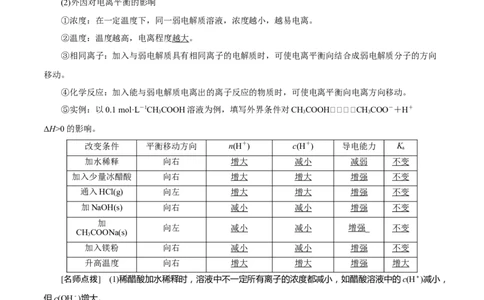
⑤实例:以0.1 mol·L-1CHCOOH溶液为例,填写外界条件对CHCOOHCH COO-+H+
3 3 3
ΔH>0的影响。
改变条件 平衡移动方向 n(H+) c(H+) 导电能力 K
a
加水稀释 向右 增大 减小 减弱 不变
加入少量冰醋酸 向右 增大 增大 增强 不变
通入HCl(g) 向左 增大 增大 增强 不变
加NaOH(s) 向右 减小 减小 增强 不变
加
向左 减小 减小 增强_ 不变
CHCOONa(s)
3
加入镁粉 向右 减小 减小 增强 不变
升高温度 向右 增大 增大 增强 增大
[名师点拨] (1)稀醋酸加水稀释时,溶液中不一定所有离子的浓度都减小,如醋酸溶液中的c(H+)减小,
但c(OH-)增大。
(2)电离平衡右移,电解质分子的浓度不一定减小,如稀醋酸中加入冰醋酸。
(3)电离平衡右移,离子的浓度不一定增大,电离程度也不一定增大,如增大弱电解质的浓度,使电离
平衡向右移动,但电离程度减小。
3.电解质溶液的导电能力与溶液中离子的关系
电解质溶液导电能力取决于自由移动离子的浓度和离子所带电荷数,自由移动离子的浓度越大、离子
所带电荷数越多,导电能力越强。
比较对象 导电性 原因同浓度的氢氧化钠溶液与氨 氢氧化钠是强电解质,完全电离;
氢氧化钠溶液大于氨水溶液
水溶液 一水合氨是弱电解质,部分电离
HC O 的K =5.9×10-2
2 2 4 a1
同浓度的醋酸溶液与草酸溶
醋酸溶液小于草酸溶液 CHCOOH的K=1.79×10-5
液 3 a
电离常数:HC O>CHCOOH
2 2 4 3
氢氧化钠极稀溶液与0.1 氢氧化钠极稀溶液小于 0.1 氢氧化钠极稀溶液的离子浓度小于
mol·L-1氨水溶液 mol·L-1氨水溶液 0.1 mol·L-1氨水溶液的离子浓度
4.判断弱电解质的三个思维角度
角度一:弱电解质的定义,即弱电解质不能完全电离。
(1)测定一定浓度的HA溶液的pH。
(2)与同浓度盐酸比较导电性。
(3)与同浓度的盐酸比较和锌反应的快慢。
角度二:弱电解质溶液中存在电离平衡,条件改变,平衡移动。
(1)从一定pH的HA溶液稀释前后pH的变化判断。
(2)从升高温度后pH的变化判断。
(3)从等体积、等pH的HA溶液与盐酸分别与过量的锌反应生成H 的量判断。
2
角度三:弱电解质形成的盐类能水解。如判断CHCOOH为弱酸可用下面两个现象:
3
(1)配制某浓度的醋酸钠溶液,向其中加入几滴酚酞溶液。现象:溶液变为浅红色。
(2)用玻璃棒蘸取一定浓度的醋酸钠溶液滴在pH试纸上,测其pH。现象:pH>7。
知识点二 电离平衡常数
1.电离常数
(1)概念:在一定条件下,弱电解质在达到电离平衡时,溶液中电离所生成的各种离子浓度的乘积与溶
液中未电离的分子浓度的比值是一个常数,这个常数叫做电离平衡常数,又称电离常数,用K(弱酸用K,
a
弱碱用K )表示。
b
(2)表达式
一元弱酸HA 一元弱碱BOH
电离方程式 HAH++A- BOHB++OH-
电离常数表
K= K =
达式 a b
(3)意义
相同条件下,K值越大,表示该弱电解质越易电离,所对应酸或碱的酸性或碱性相对越强。
(4)特点①电离常数只与温度有关,与电解质的浓度、酸碱性无关,由于电离过程是吸热的,故温度升高,K
增大。
②多元弱酸是分步电离的,各级电离常数的大小关系是K K ……所以其酸性主要取决于第一步电离。
1 2
(5)电离常数的四大应用 ≫
①判断弱酸(或弱碱)的相对强弱,电离常数越大,酸性(或碱性)越强。
②判断盐溶液的酸性(或碱性)强弱
电离常数越大,对应盐的水解程度越小,盐溶液的碱性(或酸性)越弱。
③判断反应能否发生或者判断产物是否正确
通过强酸制弱酸来判断。如HCO:K =4.2×10-7,K =5.6×10-11,苯酚(C HOH):K=1.3×10-10,
2 3 a1 a2 6 5 a
向苯酚钠(C HONa)溶液中通入的CO 不论是少量还是过量,其化学方程式均为C H ONa + CO +
6 5 2 6 5 2
H O == =C H OH + NaHCO 。
2 6 5 3
④判断溶液微粒浓度比值的变化
利用温度不变,电离常数不变来判断。
如把0.1 mol·L-1CHCOOH溶液加水稀释,==,稀释时,c(H+)减小,K 不变,则变大。
3 a
2.电离度
(1)概念
电离度是在一定条件下的弱电解质在溶液中达到电离平衡时,已经电离的电解质分子数占原电解质分
子总数的百分数。
(2)表示方法
α=×100%
也可表示为α=×100%
(3)影响因素
升高温度,电离平衡向右移动,电离度增大;降低温度,电离平衡向左移
温度的影响
动,电离度减小
当弱电解质溶液浓度增大时,电离度减小;当弱电解质溶液浓度减小时,电
浓度的影响
离度增大
[名师点拨] (1)浓度为c mol·L-1的一元弱酸(HA)溶液中,c(H+)=c·α=。
(2)浓度为c mol·L-1的一元弱碱(BOH)溶液中,c(OH-)=c·α=。
(3)一元弱酸(HA)溶液中电离度与电离常数的关系为K=c·α2或α= 。
a1.在0.1 mol·L-1的HCN溶液中存在如下电离平衡:HCNH++CN-。对该平衡,下列叙述正
确的是( )
A.加入少量NaOH固体,平衡正向移动
B.加水,平衡逆向移动
C.滴加少量0.1 mol·L-1 HCl溶液,溶液中c(H+)减小
D.加入少量NaCN固体,平衡正向移动
2.在25 ℃时,用蒸馏水稀释1 mol·L-1氨水至0.01 mol·L-1,随溶液的稀释,下列各项中始终保持增
大趋势的是( )
A. B.
C. D.c(OH-)
3.下列有关水电离情况的说法正确的是( )
A.25 ℃,pH=12的烧碱溶液与pH=12的纯碱溶液,水的电离程度相同
B.其他条件不变,CHCOOH溶液在加水稀释过程中,一定变小
3
C.其他条件不变,稀释氢氧化钠溶液,水的电离程度减小
D.其他条件不变,温度升高,水的电离程度增大,K 增大
W
4.已知次磷酸(H PO )为一元酸,欲证明它是弱电解质,下列操作方法不正确的是( )
3 2
A.用物质的量浓度相同的NaCl溶液和NaH PO 溶液进行导电性实验,比较灯泡的亮度
2 2
B.用一定浓度的NaOH溶液分别滴定等体积、等pH的盐酸和次磷酸溶液,比较消耗碱液的体积
C.加热滴有酚酞试液的NaH PO 溶液,溶液颜色变深
2 2
D.常温下,稀释0.1 mol·L-1次磷酸溶液至原溶液体积的100倍,测得pH在4~5之间
5.已知下面三个数据:7.2×10-4、4.6×10-4、4.9×10-10分别是下列有关三种酸的电离常数(25 ℃)。若
已知下列反应可以发生:NaCN+HNO===HCN+NaNO 、NaCN+HF===HCN+NaF、NaNO +
2 2 2
HF===HNO +NaF。由此可判断下列叙述不正确的是( )
2
A.K(HF)=7.2×10-4
B.K(HNO)=4.9×10-10
2
C.根据两个反应即可得出一元弱酸的强弱顺序:HF>HNO>HCN
2
D.K(HCN)HNO>HCN,所以亚硝酸的电离平衡常数为4.6×10-4,故B错误。
2
1.【答案】C
【详解】A.氯化铵促进水电离,pH=5的NH4Cl溶液由水电离出的c(H+)为10-5mol•L-1;醋酸抑制水电
离,pH=5的醋酸溶液由水电离出的c(H+)为10-9mol•L-1,故A错误;
B.醋酸是弱酸,常温下,将pH=3的醋酸和pH=11的NaOH溶液等体积混合后,醋酸有剩余,溶液呈酸
性,pH<7,故B错误;
2
C.c(H+)︰c(OH-)=1︰l012的溶液呈碱性,Na+、I-、NO3、SO4 相互之间不反应,能大量共存,故C正
确;D.0.1mol•L-1Na2CO3溶液和0.1mol•L-1NaHSO4溶液等体积混合,反应生成NaHCO3、Na2SO4,根据电
2 2
荷守恒,c(Na+)+c(H+)=2c(CO3 )+2c(SO4 )+c(HCO3)+c(OH-),故D错误;
选C。
2. 【答案】B
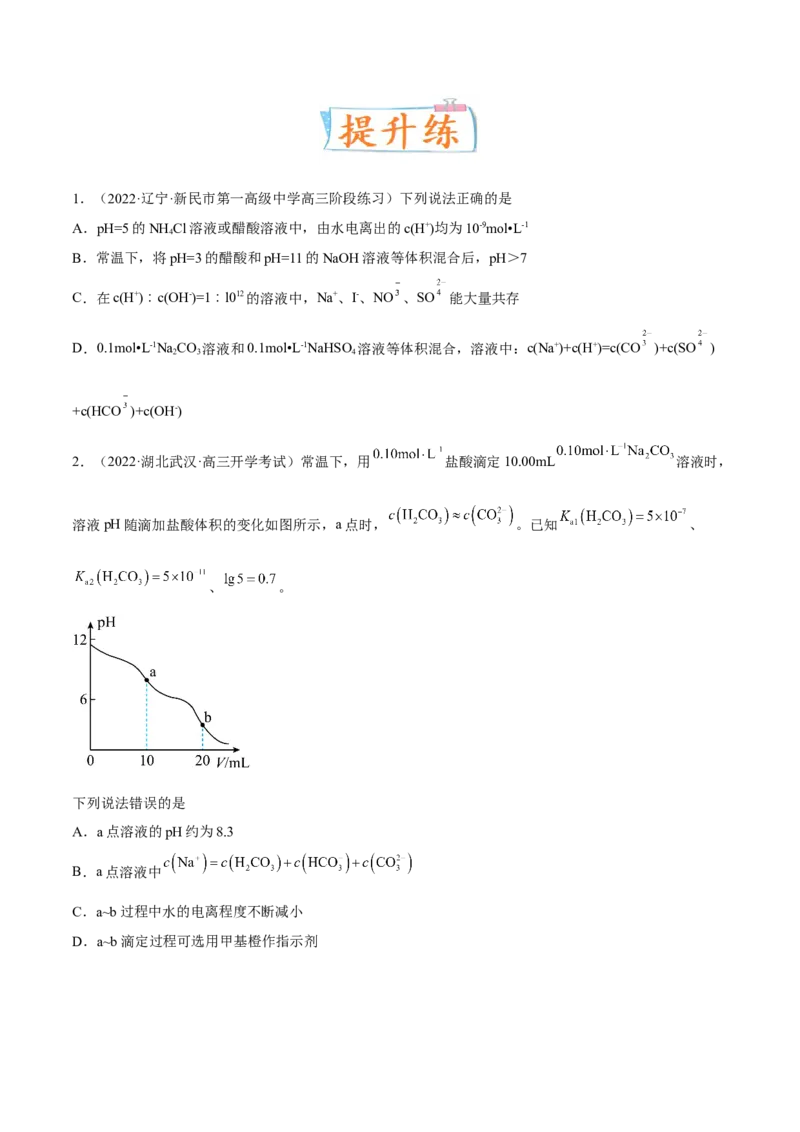
【分析】常温下,用0.10molL1
盐酸滴定10.00mL
0.10molL1Na
2
CO
3溶液时,则a点恰好反应得到碳酸
氢钠溶液,b点碳酸氢钠与盐酸恰好反应生成氯化钠、二氧化碳和水。
c(CO2-)c2(H+)
K a1 K a2 = c(H 3 CO ) cH CO c CO2
【详解】A.按电离平衡常数的定义, 2 3 ,已知a点时, 2 3 3 。
K H CO 5107 K H CO 51011 lg50.7 510751011=c2(H+) c(H+)=5109
a1 2 3 、 a2 2 3 、 ,则 ,则 ,
则a点溶液的pH约为8.3,A正确;
c Na 2cH CO 2c HCO 2c CO2
B.据分析、结合物料守恒可知, a点溶液中 2 3 3 3 ,B错误;
C. a~b过程为碳酸氢钠与盐酸恰好反应生成氯化钠、二氧化碳和水,碳酸氢钠溶液因电离大于水解促进
水的电离,酸溶液抑制水的电离,故a~b过程水的电离程度不断减小,C正确;
D.a点溶液呈弱碱性、b点呈弱酸性,故a~b滴定过程可选用在弱酸性范围内变色的甲基橙作指示剂,D
正确;
答案选B。
3. 【答案】D
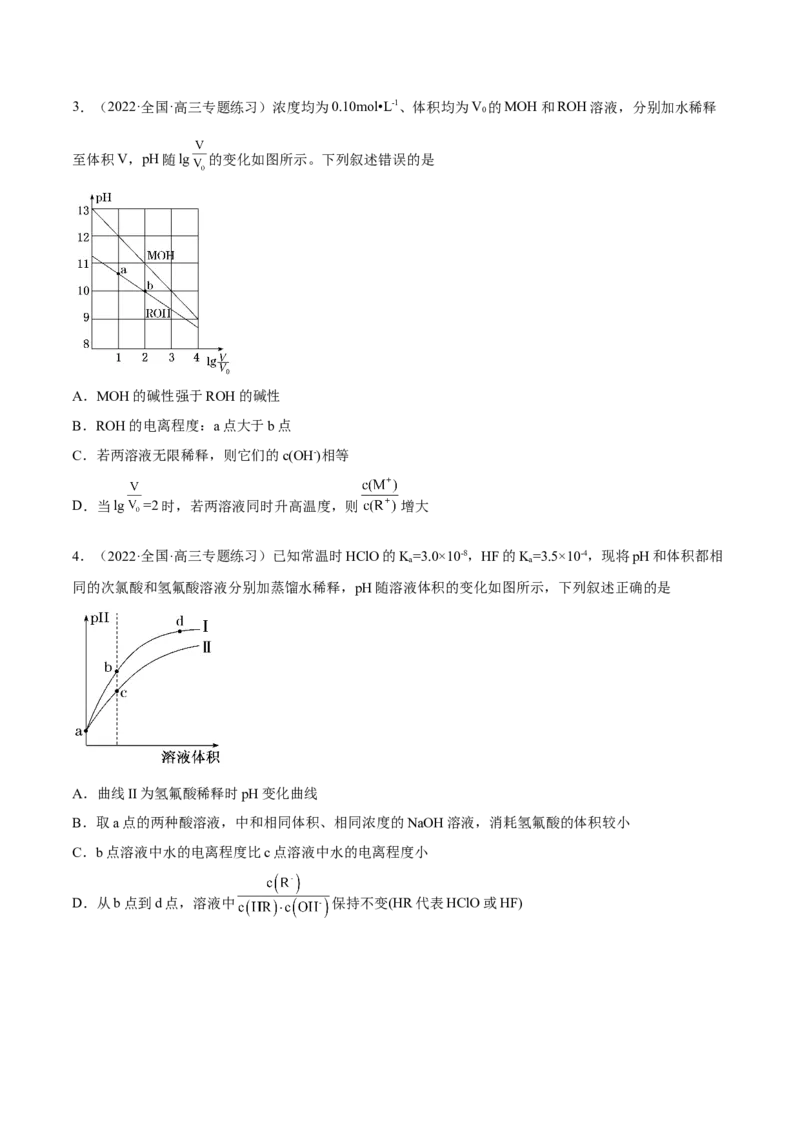
【详解】A.由图像分析可知,浓度为0.10mol•L-1的MOH溶液,在稀释前pH为13,说明MOH完全电
离,则MOH为强碱,而ROH的pH<13,说明ROH没有完全电离,ROH为弱碱。MOH的碱性强于ROH
的碱性,A正确;
V
V
B.曲线的横坐标lg 0 越大,表示加水稀释体积越大,由曲线可以看出b点的稀释程度大于a点,弱碱
ROH存在电离平衡:ROH噲垐�� R++OH-,溶液越稀,弱电解质电离程度越大,故ROH的电离程度:b点
大于a点,B正确;
C.若两溶液无限稀释,则溶液的pH接近于7,故两溶液的c(OH-)相等,C正确;V
V
D.当lg 0 =2时,溶液V=100V0,溶液稀释100倍,由于MOH发生完全电离,升高温度,c(M+)不变,
c(M+)
ROH存在电离平衡:ROH噲垐�� R++OH-,升高温度促进电离平衡向电离方向移动,c(R+)增大,故 c(R+)
减小,D错误。
故选D。
4.【答案】D
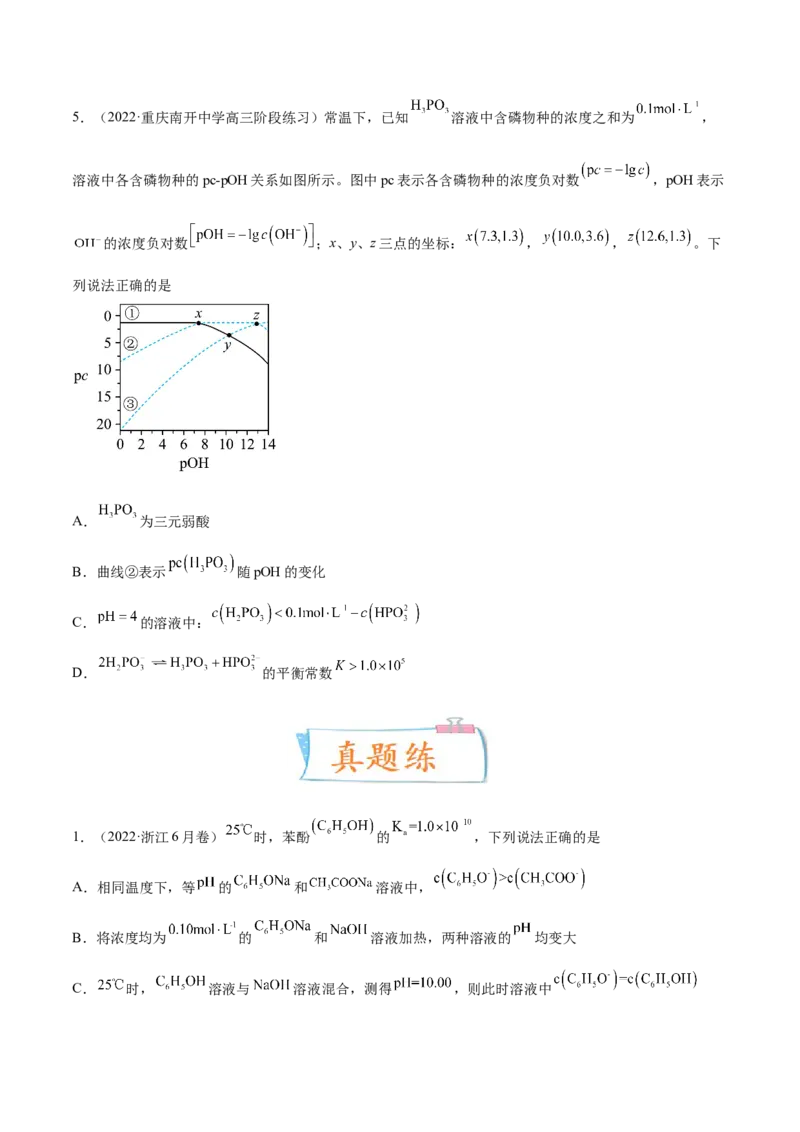
【详解】A.酸性越强,加水稀释时溶液pH变化越大,HF酸性强于HClO,加水稀释时pH变化大,所以
曲线Ⅰ代表HF稀释时pH变化曲线,A错误;
B.pH相同的两种酸,越弱的酸其浓度越大,消耗的NaOH溶液体积更多,HClO酸性弱于HF,所以中和
相同体积、相同浓度的NaOH溶液,消耗HClO的体积较小,B错误;
C.酸越弱,电离出H+趋势越小,对水的电离抑制程度越低,所以b点溶液中水的电离程度比c点溶液中
水的电离程度大,C错误;
c
R-
c
R-
K K
cHRc OH- cHR
c(H
w
) K
a
D.溶液中 = = w ,Ka和Kw只随温度的改变而改变,所以从b点到d点,
c
R-
cHRc OH-
溶液中 保持不变,D正确;
故选D。
5. 【答案】C
H PO
【详解】A.图像中含P物质只有3种,说明 3 3为二元弱酸,选项A错误;
pcH PO pc H PO pc HPO2
B.曲线③表示 3 3 ,曲线②表示 2 3 ,曲线①表示 3 ,选项B错误;
pH4 pOH10 p HPO2 pcH PO cH PO =c HPO2-
C. 即 ,由图可知,此时, c 3 3 3 ,即 3 3 3 ,而
cH
3
PO
3
+c H
2
PO
3
- +c HPO
3
2- 0.1molL1
,故
c H
2
PO
3
- =0.1mol×L-1-2c HPO
3
2-
,
c H PO- <0.1mol×L-1-c HPO2-
2 3 3 ,选项C正确;D.由 H 3 PO 3 ⇌ H 2 PO 3 -+H+ 减去 H 2 PO 3 - ⇌ HPO 3 2-+H+ ,可得 H 3 PO 3 +HPO 3 2- ⇌ 2H 2 PO 3 - 的平衡常数
K 10-1.4
K= a1 = =105.3>1×105
K a2 10-6.7 ,故 2H 2 PO 3 - ⇌ H 3 PO 3 +HPO 3 2- 的平衡常数K<1.0×105 ,选项D错误;
答案选C。
1. 【答案】C
【解析】A.醋酸的酸性大于苯酚,则醋酸根离子的水解程度较小,则相同温度下,等pH的C HONa和
6 5
CHCOONa溶液中c(C HO-)7的溶液不一定呈碱性;溶液酸碱性与溶液中氢离子、氢氧根离
子浓度有关,当c(H+)