文档内容
考向 26 水的电离和溶液的 pH
(2022浙江1月)已知25℃时二元酸HA的K =1.3×10-7,K =7.1×10-15。下列说法正确的是
2 a1 a2
A.在等浓度的NaA、NaHA溶液中,水的电离程度前者小于后者
2
B.向0.1mol·L-1的HA溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,则HA的电离度为0.013%
2 2
C.向HA溶液中加入NaOH溶液至pH=11,则c(A2-)>c(HA-)
2
D.取pH=a的HA溶液10mL,加蒸馏水稀释至100mL,则该溶液pH=a+1
2
【答案】B
【详解】A.在等浓度的NaA、NaHA溶液中,A2-的水解程度大于HA-,水的电离程度前者大于后者,故
2
A错误;B.溶液中c(H+)=10-3mol/L,HA电离程度较小,溶液中c(HA)≈0.1mol/L,K =
2 2 a1
,c(HA-)=1.3×10-5mol/L,c(HA-)≈c(HA) ,则HA的电离度
2 电离 2
0.013%,故B正确;C.向HA溶液中加入NaOH溶液至pH=11,
2
,则c(A2-)1×10-7 mol·L-1。
4.水电离出的c (H+)或c (OH-)的计算
水 水
(1)当抑制水的电离时(如酸或碱溶液)
在溶液中c(H+)、c(OH-)较小的数值是水电离出来的。如下表:
溶液(25 ℃) 水电离出来的
pH=2的盐酸 10-2 10 - 12 10 - 12
pH=13的NaOH溶液 10-13 10 - 1 10 - 13
(2)当促进水的电离时(如盐的水解)
在溶液中c(H+)、c(OH-)较大的数值是水电离出来的。如下表:
水电离出来的
溶液(25 ℃)
pH=5的NH Cl溶液 10-5 10 - 9 10 - 5
4
pH=10的NaCO 溶液 10-10 10 - 4 10 - 4
2 3
[名师点拨] 室温下,水电离的c(H+)或c(OH-)的计算方法
(1)中性溶液:c(OH-)=c(H+)=10-7 mol·L-1
(2)酸溶液
酸溶液中,H+来源于酸的电离和水的电离,而OH-只来源于水的电离。
(3)碱溶液
碱溶液中,OH-来源于碱的电离和水的电离,而H+只来源于水的电离。
(4)盐溶液
水解呈酸性或碱性的盐溶液中,H+和OH-均来源于水的电离。
知识点二 溶液的酸碱性
1.溶液的酸碱性
溶液的酸碱性取决于溶液中c(H+)和c(OH-)的相对大小
c(H+)>c(OH-) 溶液呈 性,常温下 pH 7
c(H+)=c(OH-) 溶液呈 性,常温下 pH =
c(H+)<c(OH-) 溶液呈 性,常温下 pH 7
[名师点拨] (1)溶液中c(H+)越大,c(OH-)越小,溶液的酸性越强,碱性越弱;溶液中c(H+)越小,
c(OH-)越大,溶液的碱性越强,酸性越弱。(2)pH=7或c(H+)=10-7mol·L-1的溶液不一定呈中性,因水的电离与温度有关,常温时,pH=7的溶
液呈中性,100 ℃时,pH=6的溶液呈中性。
2.溶液的pH及其测量
(1)定义式:pH=-lg c(H+)。
(2)溶液的酸碱性与pH的关系(常温下)
(3)测量方法
①pH试纸法:把小片试纸放在一洁净的玻璃片或表面皿上,用玻璃棒蘸取待测溶液点在干燥的pH试
纸的中央,试纸变色后,与标准比色卡对照即可确定溶液的pH。
②pH计测量法。
[名师点拨] (1)pH试纸使用前不能用蒸馏水润湿,否则待测液因被稀释可能产生误差。
(2)广泛pH试纸只能测出整数值,使用范围为0~14。
3.溶液pH的计算方法
(1)单一溶液pH的计算
强酸溶液:如HA,设浓度为c mol·L-1,c(H+)=nc mol·L-1,pH=-lg c(H+)=-lg(nc)。
n
强碱溶液(25 ℃):如B(OH) ,设浓度为c mol·L-1,c(H+)= mol·L-1,pH=-lg c(H+)=14+lg(nc)。
n
(2)混合溶液pH的计算
①两种强酸混合:直接求出c (H+),再据此求pH。
混
c (H+)=
混
②两种强碱混合:先求出c (OH-),再根据K 求出c(H+) ,最后求pH。
混 W 混
c (OH-)=。
混
③强酸、强碱混合:先判断哪种物质过量,再由下式求出溶液中H+或OH-的浓度,最后求pH。
c (H+)或c (OH-)=。
混 混
④将强酸、强碱溶液以某体积之比混合,若混合液呈中性,pH +pH =14-lg,现举例如下:
酸 碱
V ∶V c(H+)∶c(OH-) pH +pH
酸 碱 酸 碱
10 ∶ 1 1∶10 15
1∶1 1∶1 14
1 ∶ 10 10∶1 13[名师点拨] 速判混合溶液酸碱性的方法
(1)等浓度等体积一元酸与一元碱溶液的混合——“谁强显谁性,同强显中性”。
(2)常温下,等体积、pH之和等于14的一强一弱酸与碱混合溶液——“谁弱谁过量,谁弱显谁性”。
(3)强酸、强碱等体积混合(常温下)
①pH之和等于14呈中性;
②pH之和小于14呈酸性;
③pH之和大于14呈碱性。
知识点三 酸、碱中和滴定
1.实验原理
(1)原理:利用酸碱中和反应,用已知浓度的酸(或碱)来测定未知浓度的碱(或酸)的实验方法。以标准
HCl溶液滴定待测的NaOH溶液,待测的NaOH溶液的物质的量浓度为c(NaOH)=。
(2)关键
①准确测定参加反应的酸、碱溶液的体积。
②选取适当的指示剂,准确判断滴定终点。
2.实验用品
(1)仪器
图(A)是酸式滴定管,图(B)是碱式滴定管,滴定管夹、铁架台、锥形瓶。
(2)试剂
标准液、待测液、指示剂、蒸馏水。
(3)滴定管
①构造:“0”刻度线在上方,尖嘴部分无刻度。
②精确度:读数可估计到 0.01 mL。
③洗涤:先用蒸馏水洗涤,再用待装液润洗。
④排泡:酸、碱式滴定管中的液体在滴定前均要排出尖嘴中的气泡。[名师点拨] (1)酸性KMnO 溶液只能盛装在酸性滴定管中,不能盛装在碱式滴定管中,原因是
4
KMnO 能腐蚀橡胶。
4
(2)由于滴定管尖嘴处无刻度,故将滴定管中的液体全部放出时,放出的液体体积比理论值要大。
(3)碱式滴定管排气泡的方法:
3.指示剂
(1)常用酸碱指示剂及变色范围
指示剂 变色的pH范围
石蕊 <5.0红色 5.0~8.0紫色 >8.0蓝色
甲基橙 <3.1红色 3.1~4.4橙色 >4.4黄色
酚酞 <8.2无色 8.2~10.0粉红色 >10.0红色
(2)指示剂选择的基本原则
①酸碱中和滴定中一般不用石蕊作指示剂,因其颜色变化不明显。
②滴定终点为碱性时,用酚酞作指示剂,例如用NaOH溶液滴定醋酸。
③滴定终点为酸性时,用甲基橙作指示剂,例如用盐酸滴定氨水。
④强酸滴定强碱一般用酚酞,但用甲基橙也可以。
⑤并不是所有的滴定都需使用指示剂,如氧化还原滴定中,用标准的酸性KMnO 溶液滴定HC O 溶
4 2 2 4
液时,可利用KMnO 溶液本身颜色的变化来判断滴定终点。
4
[名师点拨] 判断滴定终点的答题模板
当滴入最后一滴标准溶液时,溶液由×××色变成×××色 ,且半分钟内溶液颜色不发生变化,表明到达
滴定终点。
例如,(1)用a mol·L-1 HCl溶液滴定未知浓度的NaOH溶液,若用酚酞作指示剂,达到滴定终点的现
象:滴入最后一滴盐酸,溶液由红色变为无色,且半分钟内不恢复红色;
若用甲基橙作指示剂,达到滴定终点的现象:滴入最后一滴盐酸,溶液由黄色变为橙色,且半分钟内
不恢复黄色。
(2)用标准碘溶液滴定溶有SO 的水溶液,以测定水中SO 的含量,应选用淀粉溶液作指示剂,达到滴
2 2
定终点的现象:滴入最后一滴碘溶液,溶液由无色变为蓝色,且半分钟内不褪色。
4.实验操作(以酚酞作指示剂,用标准盐酸滴定待测NaOH溶液为例)
(1)滴定前的准备
(2)滴定
(3)终点判断
待滴入最后一滴标准液,溶液由红色变为无色,且在半分钟内不恢复原来的颜色,即为滴定终点,记
录标准液的体积。
(4)数据处理
按上述操作重复2~3次,求出用去标准盐酸体积的平均值,根据c(NaOH)=计算。
5.酸碱中和滴定中常见误差分析
以标准盐酸溶液滴定未知浓度的NaOH溶液(酚酞作指示剂)为例,常见的因操作不正确而引起的误差:
步骤 操作 V(标准) c(待测)
酸式滴定管未用标准溶液润洗 变大 偏高
碱式滴定管未用待测溶液润洗 ①变小 ②偏低
洗涤
锥形瓶用待测溶液润洗 ③变大 ④偏高
锥形瓶洗净后还留有蒸馏水 ⑤不变 ⑥无影响
放出碱液的滴定管开始有气泡,
取液 ⑦变小 ⑧偏低
放出液体后气泡消失
酸式滴定管滴定前有气泡,滴定
⑨变大 ⑩偏高
终点时气泡消失
滴定 振荡锥形瓶时部分液体溅出 ⑪变小 ⑫偏低
部分酸液滴到锥形瓶外 ⑬变大 ⑭偏高
溶液颜色较浅时滴入酸液过快, ⑮变大 ⑯偏高停止滴定后反加一滴NaOH溶液
无变化
酸式滴定管滴定前读数正确,滴
⑰变小 ⑱偏低
定后俯视读数(或前仰后俯)
读数
酸式滴定管滴定前读数正确,滴
⑲变大 ⑳偏高
定后仰视读数(或前俯后仰)
[名师点拨] 图解量器的读数方法
(1)平视读数
实验室中用量筒、移液管或滴定管量取一定体积的液体,读取液体体积时,视线应与凹液面最低点保
持水平,视线与刻度的交点即为读数(即凹液面定视线,视线定读数)。
(2)俯视和仰视(如图b和图c)
俯视和仰视的误差,要结合具体仪器进行分析,不同量器的刻度顺序不同,如量筒刻度从下到上逐渐
增大,滴定管刻度从下到上逐渐减小。
①如图b,当用量筒测量液体的体积时,由于俯视视线向下倾斜,寻找切点的位置在凹液面的上侧,
读数高于正确的刻度线位置,即读数偏大。
②如图c,当用滴定管测量液体的体积时,由于仰视视线向上倾斜,寻找切点的位置在液面的下侧,
因滴定管刻度顺序与量筒不同,仰视读数偏大。
6.图示强酸与强碱滴定过程中pH曲线
(以0.100 0 mol·L-1NaOH溶液滴定20.00 mL 0.100 0 mol·L-1盐酸为例)
[名师点拨] (1)酸碱恰好中和(即滴定终点)时溶液不一定呈中性,最终溶液的酸碱性取决于生成盐的
性质,强酸强碱盐的溶液呈中性,强碱弱酸盐的溶液呈碱性,强酸弱碱盐的溶液呈酸性。(2)滴定终点是通过指示剂颜色的变化来控制停止滴定的“点”,滴定终点与恰好反应越吻合,测定的
误差越小。
1.用标准盐酸溶液滴定未知浓度的氢氧化钠溶液,用甲基橙作指示剂,下列说法正确的是( )
A.可以用石蕊代替指示剂
B.滴定前用待测液润洗锥形瓶
C.若氢氧化钠溶液吸收少量CO,不影响滴定结果
2
D.当锥形瓶内溶液由橙色变为红色,且半分钟内不褪色,即达到滴定终点
2.室温下,下列叙述正确的是( )
A.pH=2的盐酸与pH=12的氨水等体积混合后pH>7
B.pH=4的盐酸稀释至10倍后pH>5
C.0.2 mol·L-1的醋酸与等体积水混合后pH=1
D.100 ℃纯水的pH=6,所以水在100 ℃时呈酸性
3.常温下,下列说法不正确的是( )
A.pH=11的氨水、NaOH溶液中,水电离产生的c(H+)相同
B.pH=3的HCl溶液与pH=11的氨水等体积混合,混合后溶液的pH小于7
C.pH=3的盐酸、CHCOOH溶液中,c(Cl-)=c(CHCOO-)
3 3
D.往10 mL pH=3的盐酸中分别加入pH=11的氨水、NaOH溶液至中性,消耗氨水的体积小
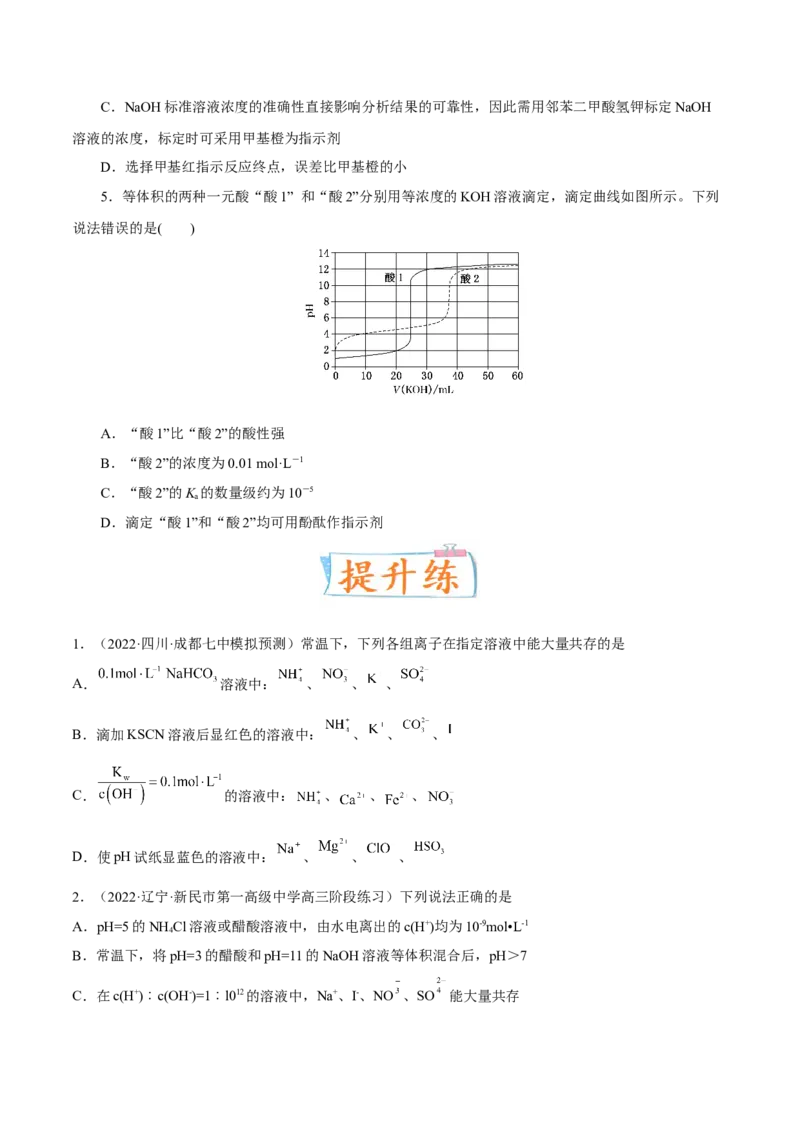
4.室温下,向20.00 mL 0.100 0 mol·L-1盐酸中滴加0.100 0 mol·L-1NaOH溶液,溶液的pH随NaOH溶
液体积的变化如图。已知lg 5=0.7,下列说法不正确的是( )
A.NaOH与盐酸恰好完全反应时,溶液pH=7
B.V(NaOH)=30.00 mL时,溶液pH=12.3C.NaOH标准溶液浓度的准确性直接影响分析结果的可靠性,因此需用邻苯二甲酸氢钾标定NaOH
溶液的浓度,标定时可采用甲基橙为指示剂
D.选择甲基红指示反应终点,误差比甲基橙的小
5.等体积的两种一元酸“酸1” 和“酸2”分别用等浓度的KOH溶液滴定,滴定曲线如图所示。下列
说法错误的是( )
A.“酸1”比“酸2”的酸性强
B.“酸2”的浓度为0.01 mol·L-1
C.“酸2”的K 的数量级约为10-5
a
D.滴定“酸1”和“酸2”均可用酚酞作指示剂
1.(2022·四川·成都七中模拟预测)常温下,下列各组离子在指定溶液中能大量共存的是
A. 溶液中: 、 、 、
B.滴加KSCN溶液后显红色的溶液中: 、 、 、
C. 的溶液中: 、 、 、
D.使pH试纸显蓝色的溶液中: 、 、 、
2.(2022·辽宁·新民市第一高级中学高三阶段练习)下列说法正确的是
A.pH=5的NH Cl溶液或醋酸溶液中,由水电离出的c(H+)均为10-9mol•L-1
4
B.常温下,将pH=3的醋酸和pH=11的NaOH溶液等体积混合后,pH>7
C.在c(H+)︰c(OH-)=1︰l012的溶液中,Na+、I-、NO 、SO 能大量共存D.0.1mol•L-1NaCO 溶液和0.1mol•L-1NaHSO 溶液等体积混合,溶液中:c(Na+)+c(H+)=c(CO )+c(SO )
2 3 4
+c(HCO )+c(OH-)
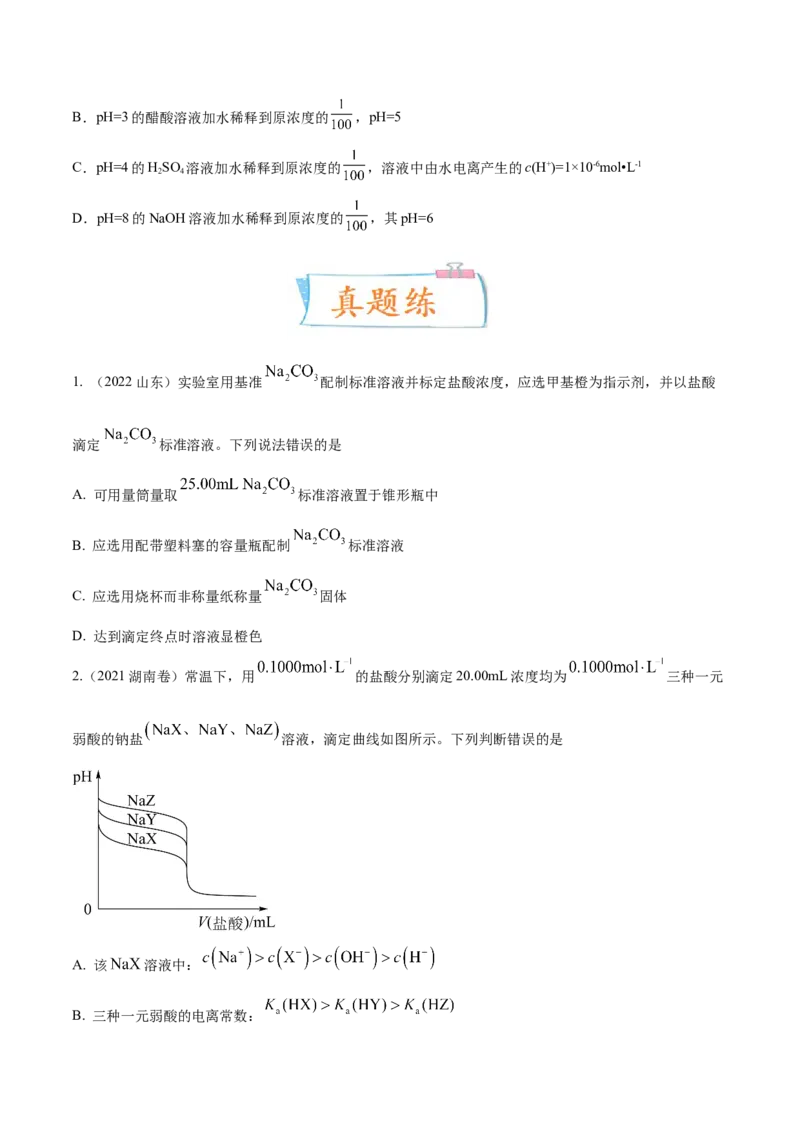
3.(2022·江西·会昌县第五中学高三阶段练习)在烧杯中对 溶液先升温,后降温,溶液
的 与温度关系如图所示。下列说法正确的是
A.a,d点溶液的 不同原因可能是水的离子积不同
B. 段 减小的原因是升温抑制了 水解
C. 时 的 数量级为
D.a点溶液中, 大于
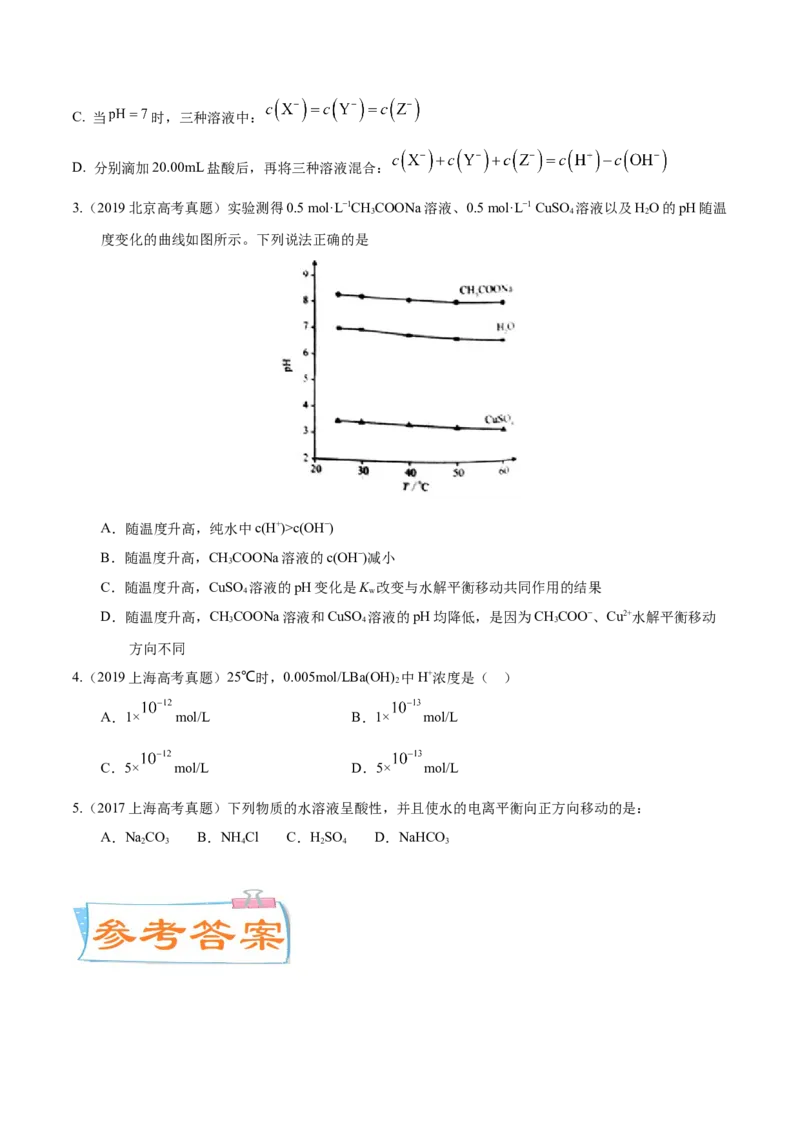
4.(2022·全国·高三专题练习)若往20mL0.01mol•L-1CHCOOH溶液中逐滴加入一定浓度的烧碱溶液,测
3
得混合溶液的温度变化如图所示,下列有关说法不正确的是
A.c点时,水的电离程度最大,溶液呈碱性
B.若b点混合溶液显酸性,则2c(Na+)=c(CH COO-)+c(CH COOH)
3 3
C.混合溶液中水的电离程度:b>c>d
D.由图可知,该反应的中和热保持不变
5.(2022·全国·高三专题练习)常温下,关于溶液稀释的说法正确的是
A.将1L0.1mol•L-1的Ba(OH) 溶液加水到体积为2L,pH=13
2B.pH=3的醋酸溶液加水稀释到原浓度的 ,pH=5
C.pH=4的HSO 溶液加水稀释到原浓度的 ,溶液中由水电离产生的c(H+)=1×10-6mol•L-1
2 4
D.pH=8的NaOH溶液加水稀释到原浓度的 ,其pH=6
1. (2022山东)实验室用基准 配制标准溶液并标定盐酸浓度,应选甲基橙为指示剂,并以盐酸
滴定 标准溶液。下列说法错误的是
A. 可用量筒量取 标准溶液置于锥形瓶中
B. 应选用配带塑料塞的容量瓶配制 标准溶液
C. 应选用烧杯而非称量纸称量 固体
D. 达到滴定终点时溶液显橙色
2.(2021湖南卷)常温下,用 的盐酸分别滴定20.00mL浓度均为 三种一元
弱酸的钠盐 溶液,滴定曲线如图所示。下列判断错误的是
A. 该 溶液中:
B. 三种一元弱酸的电离常数:C. 当 时,三种溶液中:
D. 分别滴加20.00mL盐酸后,再将三种溶液混合:
3.(2019北京高考真题)实验测得0.5 mol·L−1CHCOONa溶液、0.5 mol·L−1 CuSO 溶液以及HO的pH随温
3 4 2
度变化的曲线如图所示。下列说法正确的是
A.随温度升高,纯水中c(H+)>c(OH−)
B.随温度升高,CHCOONa溶液的c(OH−)减小
3
C.随温度升高,CuSO 溶液的pH变化是K 改变与水解平衡移动共同作用的结果
4 w
D.随温度升高,CHCOONa溶液和CuSO 溶液的pH均降低,是因为CHCOO−、Cu2+水解平衡移动
3 4 3
方向不同
4.(2019上海高考真题)25℃时,0.005mol/LBa(OH) 中H+浓度是( )
2
A.1× mol/L B.1× mol/L
C.5× mol/L D.5× mol/L
5.(2017上海高考真题)下列物质的水溶液呈酸性,并且使水的电离平衡向正方向移动的是:
A.NaCO B.NH Cl C.HSO D.NaHCO
2 3 4 2 4 31. 【答案】C
【解析】A项,石蕊颜色变化不明显,不符合要求,错误;B项,滴定前用待测液洗涤锥形瓶,导致
n(NaOH)增大,盐酸消耗的量偏大,滴定结果偏大,错误;C项,若NaOH溶液吸收少量CO,发生的反
2
应为CO+2NaOH===Na CO+HO,再滴入盐酸,盐酸先和剩余的OH-反应,H++OH-===H O,再与
2 2 3 2 2
CO反应,CO+2H+===H O+CO↑,存在关系:2OH-~CO~2H+,因此消耗HCl的物质的量始终等于
2 2
NaOH的物质的量,故氢氧化钠溶液吸收少量CO,不影响测定结果,正确;D项,该实验滴定终点为锥
2
形瓶内溶液颜色由黄色变为橙色,且半分钟内不褪色,即为滴定终点,如果变为红色说明盐酸已经过量,
错误。
2. 【答案】A
【解析】pH=2的盐酸与pH=12的氨水,氨水的物质的量浓度大于盐酸的物质的量浓度,所以两种
溶液等体积混合后所得溶液显碱性,故A正确;pH=4的盐酸,c(H+)=1×10-4 mol·L-1,稀释10倍,c(H
+)=1×10-5 mol·L-1,溶液pH=5,故B错误;醋酸溶液中存在电离平衡,加水稀释促进其电离,与等体
积水混合后pH>1,故C错误;加热促进水的电离,氢离子和氢氧根离子浓度都同等程度增大,纯水始终
显中性,故D错误。
3. 【答案】B
【解析】碱抑制水的电离,pH=11的氨水、NaOH溶液中氢氧根离子浓度相等,则二者抑制水电离的
程度相等,故A正确;pH=3的HCl溶液与pH=11的氨水等体积混合,氨水过量,溶液显碱性,混合后
溶液的pH大于7,故B错误;盐酸、CHCOOH溶液中,分别存在电荷守恒:c(H+)=c(Cl-)+c(OH-)、
3
c(H+)=c(CHCOO-)+c(OH-),都是pH=3的溶液,则c(H+)相等,c(OH-)也是相等的,所以c(Cl-)=
3
c(CHCOO-),故C正确;pH=11的氨水、NaOH溶液,c(NH ·H O)>10-3 mol·L-1,c(NaOH)=10-3
3 3 2
mol·L-1,中和等量的盐酸,消耗氨水的体积小,故D正确。
4. 【答案】C
【解析】 盐酸与NaOH溶液浓度相同,加入30.00 mL NaOH溶液时,NaOH过量,则反应后溶液中
NaOH的浓度为c(NaOH)= mol·L-1=0.02 mol·L-1,c(H+)= mol·L-1=5×10-13 mol·L-1,pH=-lg(5×10-
13)=12.3,用邻苯二甲酸氢钾标定NaOH溶液的浓度,滴定终点溶液呈碱性,应该选用酚酞作指示剂,指
示剂的变色范围与pH突变范围越靠近,误差越小,故甲基红指示反应终点,误差比甲基橙的小。
5. 【答案】B【解析】由图示可知,滴定达终点时,酸2消耗KOH溶液的体积大,说明c(酸2)>c(酸1),而起始时
的pH:酸2>酸1,则“酸1”比“酸2”的酸性强,故A正确;酸2为弱酸,起始时c(H+)=0.01 mol·L-1,
则酸2的起始浓度大于0.01 mol·L-1,故B错误;酸2滴定一半时,c(酸2)≈c(酸2的酸根离子),此时溶液
pH介于4~5之间,则酸2的K≈c(H+),其数量级约为10-5,C正确;滴定终点时,酸1和酸2的pH与酚
a
酞的变色范围接近或重叠,所以二者均可用酚酞作指示剂,故D正确。
1.A
【详解】A.各种离子之间互不反应,都不与NaHCO 反应,在溶液中能够大量共存,故A正确;
3
B.滴加 KSCN 溶液显红色的溶液中存在铁离子,Fe3+、I-之间发生氧化还原反应,在溶液中不能大量共
存,故B错误;
C. 溶液呈酸性,S2-、 在酸性条件下发生氧化还原反应,在溶液中不能大
量共存,故C错误;
D.使pH试纸显蓝色的溶液中存在大量OH-,Mg2+与OH-、ClO-、 反应,ClO-、 之间发生氧化
还原反应, 与OH-反应,在溶液中不能大量共存,故D错误;
故选:A。
2.C
【详解】A.氯化铵促进水电离,pH=5的NH Cl溶液由水电离出的c(H+)为10-5mol•L-1;醋酸抑制水电离,
4
pH=5的醋酸溶液由水电离出的c(H+)为10-9mol•L-1,故A错误;
B.醋酸是弱酸,常温下,将pH=3的醋酸和pH=11的NaOH溶液等体积混合后,醋酸有剩余,溶液呈酸
性,pH<7,故B错误;
C.c(H+)︰c(OH-)=1︰l012的溶液呈碱性,Na+、I-、NO 、SO 相互之间不反应,能大量共存,故C正确;
D.0.1mol•L-1NaCO 溶液和0.1mol•L-1NaHSO 溶液等体积混合,反应生成NaHCO 、NaSO ,根据电荷守
2 3 4 3 2 4
恒,c(Na+)+c(H+)=2c(CO )+2c(SO )+c(HCO )+c(OH-),故D错误;
选C。3.C
【详解】A. 点、 点对应的温度相同,水的离子积相等,升温过程中,部分 被氧化,故 点溶液
大于 点, 越大,溶液 越大,A项错误;
B. 段表示升温, 水解是吸热反应,升温,一方面促进 水解,另一方面促进水的电离, 降
低的主要原因可能是水的离子积增大,B项错误;
C.根据 点溶液 计算: , ,C项正确;
D.常温下, ,由上面C项计算结果可知 ,电离平衡常数 ,则 ,则
,所以 ,D项错误;
故选:C。
4.C
【详解】A.c点时,CHCOOH和NaOH恰好完全反应,得到CHCOONa溶液,由于CHCOO-水解,溶
3 3 3
液呈碱性,且水的电离程度最大,A项正确;
B.b点时,反应得到等物质的量浓度的CHCOOH、CHCOONa的混合溶液,根据物料守恒,2c(Na+)=
3 3
c(CHCOOH)+c(CH COO-),B项正确;
3 3
C.b点为等物质的量浓度的CHCOOH、CHCOONa的混合溶液,c点为CHCOONa溶液,d点为等物质
3 3 3
的量浓度的NaOH、CHCOONa的混合溶液,故c点水的电离程度最大,C项错误;
3
D.中和热与酸碱的用量无关,中和热保持不变,D项正确;
故答案选C。
5.A
【详解】A.c(OH-)=0.2mol·L-1,稀释1倍后c(OH-)=0.1mol·L-1,c(H+)= =10-13mol·L-1,pH=-
lgc(H+)=13,A正确;
B.醋酸是弱酸,pH=3的醋酸中c(H+)=10-3mol/L,稀释100倍后,由于溶液中有大量未电离的醋酸分子在
稀释时发生电离,故醋酸溶液的pH<5,B错误;C.硫酸是强酸,pH=4的醋酸中c(H+)=10-4mol/L,稀释100倍后,HSO 溶液的c(H+)=10-6mol/L,故
2 4
pH=6,水电离的c(H+) =c(OH-) = =10-8mol·L-1,C错误;
水 水
D.常温下,pH=8的NaOH溶液稀释100倍后,仍是碱性溶液,pH不可能小于7,D错误;
故选A。
1. 【答案】A
【分析】选甲基橙为指示剂,并以盐酸滴定NaCO 标准溶液,则应将NaCO 标准溶液置于锥形瓶中,将
2 3 2 3
待测盐酸置于酸式滴定管中,滴定终点时溶液由黄色变为橙色。
【详解】A.量筒的精确度不高,不可用量简量取NaCO 标准溶液,应该用碱式滴定管或移液管量取
2 3
25.00 mL Na CO 标准溶液置于锥形瓶中,A说法错误;
2 3
B.NaCO 溶液显碱性,盛放NaCO 溶液的容器不能用玻璃塞,以防碱性溶液腐蚀玻璃产生有粘性的硅酸
2 3 2 3
钠溶液而将瓶塞粘住,故应选用配带塑料塞的容量瓶配制NaCO 标准溶液,B说法正确;
2 3
C.NaCO 有吸水性且有一定的腐蚀性,故应选用烧杯而非称量纸称量NaCO 固体,C说法正确;
2 3 2 3
D.NaCO 溶液显碱性,甲基橙滴入NaCO 溶液中显黄色,当滴入最后一滴盐酸时,溶液由黄色突变为橙
2 3 2 3
色且半分钟之内不变色即为滴定终点,故达到滴定终点时溶液显橙色,D说法正确;
综上所述,本题选A。
2. 【答案】C
【分析】由图可知,没有加入盐酸时,NaX、NaY、NaZ溶液的pH依次增大,则HX、HY、HZ三种一元
弱酸的酸性依次减弱。
【详解】A.NaX为强碱弱酸盐,在溶液中水解使溶液呈碱性,则溶液中离子浓度的大小顺序为c(Na+)>
c(X-)>c(OH-)>c(H+),故A正确;
B.弱酸的酸性越弱,电离常数越小,由分析可知,HX、HY、HZ三种一元弱酸的酸性依次减弱,则三种
一元弱酸的电离常数的大小顺序为K(HX)>K (HY)>K(HZ),故B正确;
a a a
C.当溶液pH为7时,酸越弱,向盐溶液中加入盐酸的体积越大,酸根离子的浓度越小,则三种盐溶液中
酸根的浓度大小顺序为c(X-)>c(Y-)>c(Z-),故C错误;D.向三种盐溶液中分别滴加20.00mL盐酸,三种盐都完全反应,溶液中钠离子浓度等于氯离子浓度,将
三种溶液混合后溶液中存在电荷守恒关系c(Na+)+ c(H+)= c(X-)+c(Y-)+c(Z-)+ c(Cl-)+ c(OH-),由c(Na+)=
c(Cl-)可得:c(X-)+c(Y-)+c(Z-)= c(H+)—c(OH-),故D正确;
故选C。
3.【答案】C
【解析】水的电离为吸热过程,升高温度,促进水的电离;盐类水解为吸热过程,升高温度促进盐类水解,
据此解题;A.水的电离为吸热过程,升高温度,平衡向着电离方向移动,水中c(H+).c(OH-)=Kw增大,故
pH减小,但c(H+)=c(OH-),不符合题意;B.水的电离为吸热过程,升高温度,促进水的电离,所以
c(OH-)增大,醋酸根水解为吸热过程,CHCOOH-+H O CHCOOH+OH-,升高温度促进盐类水解,所以
3 2 3
c(OH-)增大,不符合题意;C.升高温度,促进水的电离,(H+)增大;升高温度,促进铜离子水解Cu2+
+2H O Cu(OH) +2H+,(H+)增大,两者共同作用使pH发生变化,符合题意;D.盐类水解为吸热过程,
2 2
升高温度促进盐类水解,不符合题意;综上所述,本题应选C。
4.【答案】A
【解析】溶液中的氢氧根离子浓度为0.01mol/L,根据水的离子积常数计算,氢离子浓度为
mol/L。故选A 。
5.【答案】B
【解析】A.NaCO 是强碱弱酸盐,碳酸根离子水解导致溶液呈碱性,促进水电离,错误;B.氯化铵是
2 3
强酸弱碱盐,铵根离子水解,溶液显酸性,促进水的电离,正确;C.硫酸完全电离生成氢离子而导致溶
液中c(H+)增大,溶液显酸性,抑制水的电离,错误;D.碳酸氢钠是强碱弱酸酸式盐,碳酸氢根离子水解
程度大于电离程度,溶液显碱性,促进水的电离,错误;故选B。