文档内容
考向 27 盐类的水解
(2022·湖南卷)甲基丙烯酸甲酯是合成有机玻璃的单体。
旧法合成的反应:
新法合成的反应:
下列说法错误的是(阿伏加德罗常数的值为 )
A. 的电子式为
B.新法没有副产物产生,原子利用率高
C. 的 溶液中 的微粒数小于
D. 的作用是降低反应的活化能,使活化分子数目增多,百分数不变
【答案】D
【解析】A.氢氰酸为共价化合物,结构式为H—C≡N,电子式为 ,故A正确;
B.由方程式可知,新法合成甲基丙烯酸甲酯的反应为没有副产物生成,原子利用率为100的化合反应,
故B正确;
C.硫酸氢铵是强酸弱碱的酸式盐,铵根离子在溶液中会发生水解反应,所以1L0.05mol/L的硫酸氢铵溶液
中铵根离子的数目小于0.05mol/L×1L×N mol—1=0.05N ,故C正确;
A A
D.由方程式可知,钯为新法合成甲基丙烯酸甲酯的催化剂,能降低反应的活化能,使活化分子的数目和
百分数都增大,故D错误;
故选D。知识点一 盐类的水解及影响因素
1.盐类的水解
2.盐类的水解规律实例:下列盐溶液:①CuSO ②KNO ③NaCO ④(NH )SO ⑤NaHCO ⑥CHCOONa
4 3 2 3 4 2 4 3 3
溶液呈酸性的是:____①④____;
溶液呈碱性的是:____③⑤⑥__;
溶液呈中性的是:______②____。
[名师点拨] (1)盐类发生水解反应后,其水溶液往往呈酸性或碱性, 但也有特殊情况,如
CHCOONH 溶液呈中性。
3 4
(2)多元弱酸的酸式盐溶液呈酸碱性取决于酸式酸根离子的电离程度和水解程度的相对大小。如
NaHCO 溶液中HCO的水解>电离,故溶液呈碱性;NaHSO 溶液中HSO的电离>水解,故溶液呈酸性。
3 3
(3)能发生相互促进的水解反应的盐溶液的酸碱性,取决于弱酸、弱碱的相对强弱,如NH F溶液呈酸
4
性,是因为HF的电离常数大于NH ·H O的电离常数。
3 2
3.水解离子方程式的书写
(1)多元弱酸盐水解:分步进行,以第一步为主。
如NaCO 水解的离子方程式:
2 3
CO + H OHCO + OH - , HCO + H OHCO + OH - 。
2 2 2 3
(2)多元弱碱盐水解:方程式一步完成。
如FeCl 水解的离子方程式:
3
Fe 3 + + 3H OFe(OH) + 3H + 。
2 3
(3)阴、阳离子相互促进水解:水解程度较大,书写时要用“===”“↑”“↓”等。
如NaHCO 与AlCl 溶液混合反应的离子方程式:
3 3
Al 3 + + 3HCO == =Al(OH) ↓ + 3CO ↑。
3 2
[名师点拨] (1)盐类的水解是微弱的,书写用“”不标“↑”和“↓”。
(2)多元弱酸根分步书写,水的化学计量数始终是1,以第一步为主,一般只写第一步水解方程式。
(3)Al3+(或Fe3+)与CO、HCO、S2-、HSO、AlO发生相互促进的水解反应,水解程度较大,进行完全,
书写时要用“===” “↑” “↓”。
(4)NH与CHCOO-、HCO、CO等在水解时相互促进,其水解程度比单一离子的水解程度大,但仍然
3
水解程度比较弱,不能进行完全,在书写水解方程式时用“”。
4.影响盐类水解平衡的因素(1)内因:形成盐的酸或碱越弱,其盐就越易水解。如水解程度:NaCONaSO ,NaCONaHCO 。
2 3 2 3 2 3 3
(2)外因
(3)以FeCl 水解为例[Fe3++3HOFe(OH) +3H+],填写外界条件对水解平衡的影响。
3 2 3
条件 移动方向 H+数 pH 现象
升温 向右 增多 减小 颜色变深
通入HCl(g) 向左 增多 减小 颜色变浅
加HO 向右 增多 增大 颜色变浅
2
加NaHCO 向右 减少 增大 生成红褐色沉淀,放出气体
3
[名师点拨] (1)相同条件下的水解程度:
①正盐>相应的酸式盐,如CO>HCO。
②水解相互促进的盐>单独水解的盐>水解相互抑制的盐。如NH的水解程度:(NH )CO>(NH )SO
4 2 3 4 2 4
>(NH )Fe(SO )。
4 2 4 2
(2)稀释溶液时,盐溶液被稀释后浓度越小,水解程度越大,但由于溶液体积的增大是主要的,故水解
产生的H+或OH-的浓度是减小的,则溶液酸性(或碱性)越弱。
(3)向CHCOONa溶液中加入少量冰醋酸,并不会与CHCOONa溶液水解产生的OH-反应,使平衡向
3 3
水解方向移动,主要原因是体系中c(CHCOOH)增大,会使平衡CHCOO-+HOCHCOOH+OH-
3 3 2 3
左移。
5.水解常数及应用
(1)含义:盐类水解的平衡常数,称为水解常数,用K 表示。
h
(2)表达式
①对于A-+HOHA+OH-,
2
K =;
h
②对于B++HOBOH+H+,K =。
2 h
(3)意义和影响因素
①K 越大,表示相应盐的水解程度越大;
h
②K 只受温度的影响,升高温度,K 值增大。
h h
(4)与电离常数的关系
①强碱弱酸盐:K =;
h
②强酸弱碱盐:K =。
h
(5)水解常数的应用
①计算盐溶液中c(H+)或c(OH-)
a.对于A-+HOHA+OH-
2起始 c 0 0
平衡c-c(HA) c(HA) c(OH-)
K =≈,
h
c(OH-)=。
b.同理对于B++HOBOH+H+,
2
c(H+)=。
②判断盐溶液的酸碱性和微粒浓度的大小
a.单一溶液
ⅰ.如一定浓度的NaHCO 溶液,K =4.4×10-7,K =5.6×10-11,K ==≈2.27×10-8>K ,HCO的水
3 a1 a2 h a2
解程度大于其电离程度,溶液呈碱性,c(OH-)>c(H+),c(H CO)>c(CO)。
2 3
ⅱ.又如一定浓度的NaHSO 溶液,K =1.54×10-2,K =1.2×10-7,K ==≈6.5×10-13<K ,HSO的
3 a1 a2 h a2
水解程度小于其电离程度,溶液呈酸性,c(H+)>c(OH-),c(SO)>c(H SO )。
2 3
ⅲ.再如一定浓度的CHCOONH 溶液,由于K(CHCOOH)=1.75×10-5≈K (NH ·H O)=1.71×10-5,则
3 4 a 3 b 3 2
CHCOO-与NH的水解常数近似相等,二者水解程度相同,CHCOONH 溶液呈中性,c(CHCOO-)=
3 3 4 3
c(NH)。
b.混合溶液
ⅰ.如物质的量浓度相等的CHCOOH和CHCOONa混合溶液,K(CHCOOH)=1.75×10-5,K ==
3 3 a 3 h
≈5.7×10-10c(OH
a 3 3 3
-),c(CHCOO-)>c(Na+)>c(CHCOOH)。
3 3
ⅱ.又如物质的量浓度相等的HCN和NaCN混合溶液,K(HCN)=4.9×10-10,K ==≈2.0×10-5>
a h
K(HCN),CN-的水解程度大于HCN的电离程度,溶液呈碱性,c(OH-)>c(H+),c(HCN)>c(Na+)>c(CN
a
-)。
知识点二 盐类水解的应用
1.盐类水解的“十二”大应用
应用 举例
FeCl 溶液显酸性,原因是 Fe 3 + +
判断溶液的酸碱性 3
3HOFe(OH) +3H+
2 3
等物质的量浓度的NaX、NaY、NaZ三种盐溶液的
判断酸性强弱
pH分别为8、9、10,则酸性: HX > HY > HZ
配制CuSO 溶液时,加入少量硫酸,防止Cu2+水
4
配制或贮存易水解的盐溶液 解;配制FeCl 溶液,加入少量盐酸;贮存NaCO
3 2 3
溶液、NaSiO 溶液不能用带磨口玻璃塞的试剂瓶
2 3
制取Fe(OH) 胶体的离子方程式: Fe 3 + +
胶体的制取 3
3H O ===== Fe(OH) ( 胶体 ) + 3H +
2 3成分为NaHCO 与Al (SO ),发生的反应为 Al 3 + +
泡沫灭火器原理 3 2 4 3
3HCO == =Al(OH) ↓ + 3CO ↑
3 2
明矾可作净水剂,原理为 Al 3 + +
作净水剂
3HOAl(OH) ( 胶体 ) + 3H +
2 3
化肥的施用 铵态氮肥与草木灰不得混用
除锈剂 NH Cl与ZnCl 溶液可作焊接时的除锈剂
4 2
Fe3+与CO不能大量共存: 2Fe 3 + + 3CO +
判断离子能否共存
3H O == =2Fe(OH) ↓ + 3CO ↑
2 3 2
热的纯碱溶液清洗油污,加热能促进CO的水解,
去油污
溶液中c(OH-)增大,油脂的皂化反应进行得彻底
TiO 的制备:TiCl +(x+2)H O(过量)
2 4 2
制备无机物
TiO·xHO+4HCl;TiO·xHO=====TiO+xHO
2 2 2 2 2 2
用MgO[或Mg(OH) 或MgCO ]调节溶液pH,除去
2 3
MgCl 溶液中的Fe3+杂质Fe3++
2
混合盐溶液的除杂与提纯 3H 2 OFe(OH) 3 +3H+
MgO+2H+===Mg2++HO,从而将Fe3+转化成
2
Fe(OH) 沉淀
3
2.盐溶液蒸干时所得产物的判断
(1)盐溶液水解生成难挥发性酸时,蒸干后一般得原物质,如CuSO (aq)蒸干得CuSO (s)。
4 4
(2)盐溶液水解生成易挥发性酸时,蒸干灼烧后一般得到对应的氧化物,如AlCl (aq)蒸干得Al(OH) ,
3 3
灼烧得Al O。
2 3
(3)考虑盐受热时是否分解。
原物质 蒸干灼烧后固体物质
Ca(HCO ) CaCO 或CaO
3 2 3
NaHCO NaCO
3 2 3
KMnO KMnO 和MnO
4 2 4 2
NH Cl 分解为NH 和HCl,无固体物质存在
4 3
(4)还原性盐在蒸干时会被O 氧化。如NaSO (aq)蒸干得NaSO (s)。
2 2 3 2 4
知识点三 电解质溶液中的粒子浓度关系
1.理解两大平衡,树立微弱意识
(1)电离平衡——建立电离过程是微弱的意识
弱电解质(弱酸、弱碱、水)的电离是微弱的,且水的电离能力远远小于弱酸和弱碱的电离能力。如在
稀醋酸溶液中存在:CHCOOHCH COO-+H+,HOOH-+H+,溶液中粒子浓度由大到小的
3 3 2
顺序:c(CHCOOH)>c(H+)>c(CHCOO-)>c(OH-)。
3 3
(2)水解平衡——建立水解过程是微弱的意识弱酸根离子或弱碱阳离子的水解是微弱的,但水的电离程度远远小于盐的水解程度。如稀的
CHCOONa溶液中存在:CHCOONa===CH COO-+Na+,CHCOO-+HOCHCOOH+OH-,
3 3 3 3 2 3
HOH++OH-,溶液中,c(Na+)>c(CHCOO-)>c(OH-)>c(CHCOOH)>c(H+)。
2 3 3
2.巧用守恒思想,明确定量关系
(1)电荷守恒
电解质溶液中所有阳离子所带正电荷总数与所有阴离子所带负电荷总数相等。
如NaHCO 溶液中电荷守恒:
3
c(Na+)+c(H+)=c(HCO)+c(OH-)+2c(CO)。
(2)物料守恒
电解质溶液中由于电离或水解因素,离子会发生变化变成其他离子或分子,但离子或分子中某种特定
元素原子的总数不变,符合原子守恒。
如NaHCO 溶液中,n(Na+)∶n(C原子)=1∶1,因HCO水解:HCO+HOHCO3+OH-以及
3 2 2
HCO电离:HCOH++CO,C元素的存在形式有3种,即HCO、HCO、CO,由n(Na+)∶n(C原
2 3
子)=1∶1,得c(Na+)=c(HCO)+c(CO)+c(H CO)。
2 3
(3)质子守恒
电解质溶液中分子或离子得到或失去质子(H+)的物质的量相等。例如,
①在NaCO 溶液中:
2 3
质子守恒:c(OH-)=c(H+)+c(HCO)+2c(H CO)。
2 3
②在NaHCO 溶液中:
3
质子守恒:c(H+)+c(H CO)=c(OH-)+c(CO)。
2 3
另外,质子守恒式可以由电荷守恒式和物料守恒式推导得出。
以KHS溶液为例,电荷守恒式为c(K+)+c(H+)=c(OH-)+c(HS-)+2c(S2-)①,物料守恒式为c(K+)=
c(HS-)+c(S2-)+c(H S)②,由①-②消去没有参与变化的K+得质子守恒式:c(H+)+c(H S)=c(OH-)+
2 2
c(S2-)。
3.明确三大类型,熟知解题流程类型一 单一溶液中的粒子浓度关系
[典题示例1] 0.1 mol·L-1 Na S溶液中各粒子浓度的关系
2
(1)大小关系:____________________________________________________________;
(2)物料守恒:__________________________________________________________;
(3)电荷守恒:___________________________________________________________;
(4)质子守恒:___________________________________________________________。
[解析] NaS===2Na++S2-(完全电离),
2
S2-+HOHS-+OH-(主要),
2
HS-+HOHS+OH-(次要),
2 2
HOH++OH-(极微弱)。
2
[答案] (1)c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+)
(2)c(Na+)=2[c(S2-)+c(HS-)+c(H S)]
2
(3)c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-)
(4)c(OH-)=c(H+)+c(HS-)+2(H S)
2
[典题示例2] 0.1 mol·L-1 NaHSO 溶液中各粒子浓度关系
3
(1)大小关系:____________________________________________________________;
(2)物料守恒:_____________________________________________________________;
(3)电荷守恒:________________________________________________________;
(4)质子守恒:_________________________________________________________。
[解析] NaHSO===Na++HSO(完全电离),
3
HSOH++SO(主要),
HSO+HOHSO +OH-(次要),
2 2 3
HOH++OH-(极微弱)。
2
[答案] (1)c(Na+)>c(HSO)>c(H+)>c(SO)>c(OH-)
(2)c(Na+)=c(HSO)+c(SO)+c(H SO )
2 3
(3)c(Na+)+c(H+)=c(OH-)+c(HSO)+2c(SO)
(4)c(H+)+c(H SO )=c(OH-)+c(SO)
2 3
类型二 混合溶液中粒子浓度关系
[典题示例3] 浓度均为0.1 mol·L-1 NH Cl和氨水的混合溶液中粒子浓度关系
4
(1)电荷守恒:____________________________________________________________。
(2)物料守恒:_____________________________________________________________。
(3)质子守恒:_____________________________________________________________。(4)大小关系:____________________________________________________________。
[解析] NH Cl===NH+Cl-(完全电离),
4
NH ·H ONH+OH-(主要,混合液呈碱性),
3 2
NH+HONH ·H O+H+(次要),
2 3 2
HOH++OH-(极微弱)。
2
[答案] (1)c(NH)+c(H+)=c(Cl-)+c(OH-)
(2)c(NH)+c(NH ·H O)=2c(Cl-)
3 2
(3)c(NH)+2c(H+)=c(NH ·H O)+2c(OH-)
3 2
(4)c(NH)>c(Cl-)>c(NH ·H O)>c(OH-)>c(H+)
3 2
[典题示例4] 浓度均为0.1 mol·L-1 CHCOONa和CHCOOH的混合溶液中粒子浓度关系
3 3
(1)电荷守恒:_____________________________________________________________。
(2)物料守恒:____________________________________________________________。
(3)质子守恒:_____________________________________________________________。
(4)大小关系:_____________________________________________________________。
[解析] CHCOONa===CH COO-+Na+(完全电离),
3 3
CHCOOHCH COO-+H+(主要,混合液呈酸性),
3 3
CHCOO-+HOCHCOOH+OH-(次要),
3 2 3
HOH++OH-(极微弱)。
2
[答案] (1)c(Na+)+c(H+)=c(CHCOO-)+c(OH-)
3
(2)c(CHCOO-)+c(CHCOOH)=2c(Na+)
3 3
(3)c(CHCOOH)+2c(H+)=c(CHCOO-)+2c(OH-)
3 3
(4)c(CHCOO-)>c(Na+)>c(CHCOOH)>c(H+)>c(OH-)
3 3
[典题示例5] 浓度均为0.1 mol·L-1 Na CO 和NaHCO 的混合溶液中粒子浓度关系
2 3 3
(1)电荷守恒:___________________________________________________________。
(2)物料守恒:_____________________________________________________________。
(3)质子守恒:_____________________________________________________________。
(4)大小关系:_____________________________________________________________。
[解析] NaCO===2Na++CO(完全电离),
2 3
NaHCO ===Na++HCO(完全电离),
3
CO+HOHCO+OH-(主要,CO的水解程度大于HCO的水解程度),
2
HCO+HOHCO+OH-(次要),
2 2 3
HCOH++CO(微弱),HOH++OH-(极微弱)。
2
[答案] (1)c(Na+)+c(H+)=c(OH-)+c(HCO)+2c(CO)
(2)2c(Na+)=3[c(CO)+c(HCO)+c(H CO)]
2 3
(3)2c(OH-)+c(CO)=2c(H+)+c(HCO)+3c(H CO)
2 3
(4)c(Na+)>c(HCO)>c(CO)>c(OH-)>c(H+)
类型三 不同溶液中同一离子浓度大小的比较
[解题流程]
[典题示例6] 25 ℃时,相同物质的量浓度的下列溶液中:①NH Cl、②CHCOONH、③NH HSO 、
4 3 4 4 4
④(NH )SO 、⑤(NH )Fe(SO ),c(NH)由大到小的顺序为_____________。
4 2 4 4 2 4 2
[解析] 分析流程为
分组―――――――――――→
[答案] ⑤>④>③>①>②
1.下列物质在水溶液中不发生水解的是( )
A.NaF B.NaHS
C.NaNO D.NaClO
3
2.《本草纲目》中对白矾之用有如下叙述:“吐利风热之痰涎,取其酸苦涌泄也;治诸血痛,脱
肛……取其酸涩而收也……”下列说法正确的是( )A.治血痛的原因是利用了胶体的吸附作用
B.白矾溶于水后微粒浓度排序:c(H O)>c(SO)>c(Al3+)>c(K+)>c(H+)>c(OH-)
2
C.白矾和氯化铁均可用作水处理剂,均可以杀菌消毒
D.白矾常用于油条中作膨化剂的原理是:Al3++3HCO===Al(OH) ↓+3CO↑
3 2
3.要使0.1 mol·L-1 KSO 溶液中的c(SO)更接近0.1 mol·L-1,可以采取的措施是( )
2 3
A.通入SO B.加入SO
2 3
C.加热 D.加入适量KOH固体
4.0.5 mol·L-1 CHCOONa溶液和水的pH随温度的变化如图所示。下列分析错误的是( )
3
A.25 ℃,CHCOONa溶液的pH=8.2,显碱性
3
B.60 ℃,HO中c(H+)=1×10-6.5mol·L-1,呈中性
2
C.60 ℃,CHCOONa溶液中c(OH-)=1×10-5.1mol·L-1
3
D.升高温度,CHCOONa溶液水解程度和pH都减小
3
5.25 ℃时,浓度均为0.1 mol·L-1的几种溶液的pH如表:
③CHCOONH 溶
溶液 ①CHCOONa溶液 ②NaHCO 溶液 3 4
3 3 液
pH 8.88 8.33 7.00
下列说法不正确的是( )
A.①中,c(Na+)=c(CHCOO-)+c(CHCOOH)
3 3
B.由①②可知,CHCOO-的水解程度大于HCO的水解程度
3
C.③中,c(CHCOO-)=c(NH)<0.1 mol·L-1
3
D.推测25 ℃,0.1 mol·L-1NH HCO 溶液的pH<8.33
4 3
1.(2022·湖南永州·一模)下列离子方程式书写错误的是
A.向明矾溶液中加入少量氢氧化钡溶液:2Al3++3 +3Ba2++6OH-=2Al(OH) ↓+3BaSO ↓
3 4B.澄清石灰水中通入过量的二氧化碳:CO+OH-=HCO
2
C.氢氧化镁固体溶解于氯化铵溶液:Mg(OH) +2H+=Mg2++2H O
2 2
D.SO 使酸性KMnO 溶液褪色:5SO +2H O+2 =5 +4H++2Mn2+
2 4 2 2
2.(2022·河北沧州·高三开学考试)对下列粒子组在溶液中能否大量共存的判断和分析错误的是
选项 粒子组 判断和分析
A H+、Na+、SO 、NO 能大量共存,粒子间不发生反应
B HO、SO 、Na+、K+ 不能共存,能发生反应:HO+SO =SO +H O
2 2 2 2 2
不能大量共存,能发生反应:HCO +Al3+=3OH-
C HCO 、Al3+、K+、Cl-
+Al(CO)↓
2 3 3
D K+、H+、Br-、Fe3+ 能大量共存,粒子间不反应
3.(2022·辽宁·新民市第一高级中学高三阶段练习)在给定条件下,下列物质之间不能实现转化的是
①HS S SO
2 3
②Si SiO HSiO
2 2 3
③饱和NaCl(aq) NaHCO NaCO
3 2 3
④Al AlCl (aq) 无水AlCl
3 3
⑤Fe FeCl Fe(OH)
2 3
A.①③⑤ B.②③④ C.②④⑤ D.①②④
4.(2022·江苏省如东高级中学高三开学考试)室温下,通过下列实验探究NaC O 溶液的性质。下列说
2 2 4
法不正确的是
已知:25℃时K (H C O)=5.9×10-2,K (H C O)=6.4×10-5。
a1 2 2 4 a2 2 2 4
实
实验操作和现象
验
1 用pH计测得0.0100mol·L-1NaC O 溶液pH为8.60
2 2 4
2 向0.0100mol·L-1NaC O 溶液中滴加稀盐酸至溶液pH=7
2 2 4
3 向0.0100mol·L-1NaC O 溶液中滴加等浓度、等体积稀盐酸
2 2 44 向0.0100mol·L-1NaC O 溶液中加入足量稀硫酸酸化后,再滴加KMnO 溶液,溶液紫红色褪去
2 2 4 4
A.实验1溶液中存在:c(OH-)=c(H+)+2c(H C O)+c(HC O )
2 2 4 2
B.实验2溶液中存在:c(Na+)=c((HC O )+2c(C O )
2 2
C.实验3溶液中存在:c(HC O )>c(C O )>c(H C O)
2 2 2 2 4
D.实验4中滴加KMnO 溶液所发生的离子方程式为:5HC O+2MnO +6H+=10CO ↑+2Mn2++8H O
4 2 2 4 2 2
5.(2022·全国·高三专题练习)室温下,将两种浓度均为0.10mol·L-1的溶液等体积混合,若溶液混合引起
的体积变化可忽略,下列各混合溶液中微粒物质的量浓度关系正确的是
A.NaHCO -Na CO 混合溶液(pH=10.30):c(Na+)>c( )>c( )>c(OH-)
3 2 3
B.氨水-NH Cl混合溶液(pH=9.25):c( )+c(H+)=c(NH·H O)+c(OH-)
4 3 2
C.CHCOOH-CHCOONa混合溶液(pH=4.76):c(Na+)>c(CH COOH)>c(CH COO-)>c(H+)
3 3 3 3
D.HC O-NaHC O 混合溶液(pH=1.68,HC O 为二元弱酸):c(H+)+c(H C O)=c(Na+)+c( )+c(OH-)
2 2 4 2 4 2 2 4 2 2 4
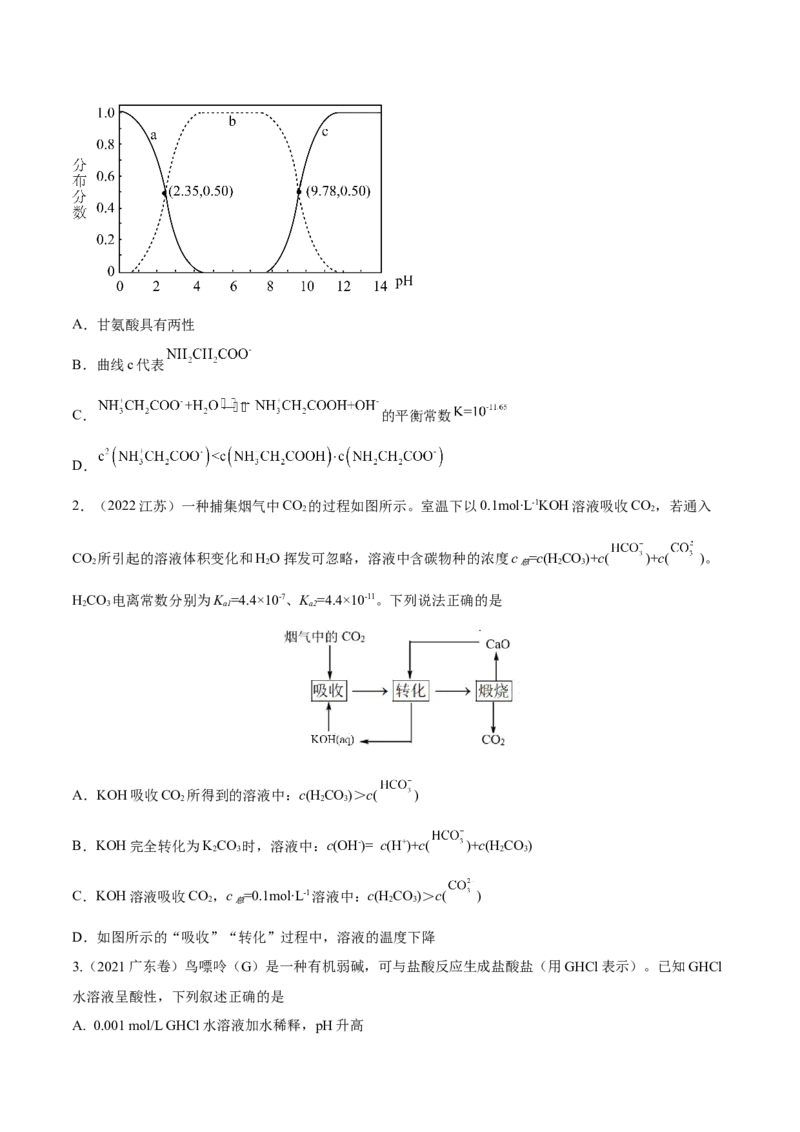
1.(2022辽宁)甘氨酸 是人体必需氨基酸之一、在 时, 、
和 的分布分数【如 】与溶液 关系如图。
下列说法错误的是A.甘氨酸具有两性
B.曲线c代表
C. 的平衡常数
D.
2.(2022江苏)一种捕集烟气中CO 的过程如图所示。室温下以0.1mol∙L-1KOH溶液吸收CO,若通入
2 2
CO 所引起的溶液体积变化和HO挥发可忽略,溶液中含碳物种的浓度c =c(H CO)+c( )+c( )。
2 2 总 2 3
HCO 电离常数分别为K =4.4×10-7、K =4.4×10-11。下列说法正确的是
2 3 a1 a2
A.KOH吸收CO 所得到的溶液中:c(H CO)>c( )
2 2 3
B.KOH完全转化为KCO 时,溶液中:c(OH-)= c(H+)+c( )+c(H CO)
2 3 2 3
C.KOH溶液吸收CO,c =0.1mol∙L-1溶液中:c(H CO)>c( )
2 总 2 3
D.如图所示的“吸收”“转化”过程中,溶液的温度下降
3.(2021广东卷)鸟嘌呤(G)是一种有机弱碱,可与盐酸反应生成盐酸盐(用GHCl表示)。已知GHCl
水溶液呈酸性,下列叙述正确的是
A. 0.001 mol/L GHCl水溶液加水稀释,pH升高B. 0.001 mol/L GHCl水溶液的pH=3
C. GHCl 在水中的电离方程式为:GHCl = G + HCl
D. GHCl 水溶液中:c(OH—) + c(Cl—) = c(GH+)+ c(G)
4.(2020·天津高考真题)常温下,下列有关电解质溶液的说法错误的是
A.相同浓度的 HCOONa和NaF两溶液,前者的pH较大,则
B.相同浓度的CHCOOH和CHCOONa两溶液等体积混合后pH约为4.7,则溶液中
3 3
C.FeS溶于稀硫酸,而CuS不溶于稀硫酸,则
D.在 溶液中,
5.(2019·上海高考真题)常温下0.1mol/L①CHCOOH、②NaOH、③CHCOONa,下列叙述正确的是(
3 3
)
A.①中[CHCOOH]>[CH COO-]>[H+]>[OH-]
3 3
B.①②等体积混合后,醋酸根离子浓度小于③的二分之一
C.①③等体积混合以后,溶液呈酸性,则(Na+)>(CH COO-)>(H+)
3
D.①②等体积混合以后,水的电离程度比①③等体积混合的电离程度小
1.【答案】C
【解析】A项中的F-,B项中的HS-,D项中的ClO-都是弱酸根离子,易水解。
2.【答案】D
【解析】白矾中的铝离子水解生成氢氧化铝胶体,治血痛的原因是利用了胶体的聚沉,不是吸附作用,
故A错误;白矾是硫酸铝钾晶体,KAl(SO )·12H O,其水溶液中因铝离子水解而显酸性,铝离子减少,微
4 2 2
粒浓度排序:c(H O)>c(SO)>c(K+)>c(Al3+)>c(H+)>c(OH-),故B错误;白矾和氯化铁水溶液均可水解
2
生成胶体,具有吸附作用,可以净水,但无强氧化性,不能杀菌消毒,故C错误;白矾常用于油条中作膨化剂是利用铝离子和小苏打中的碳酸氢根离子发生相互促进的水解反应生成二氧化碳气体,Al3++
3HCO===Al(OH) ↓+3CO↑,故D正确。
3 2
3.【答案】D
【解析】向KSO 溶液中通入SO 发生反应生成KHSO,导致溶液中c(SO)减小,不可能更接近0.1
2 3 2 3
mol·L-1,故A错误;加入的SO 能与水反应生成硫酸,硫酸会与KSO 发生反应生成二氧化硫、硫酸钾和
3 2 3
水,导致溶液中c(SO)减小,不可能更接近0.1 mol·L-1,故B错误;盐类的水解反应属于吸热反应,加热
促进SO水解平衡正向移动,导致溶液中c(SO)减小,不可能更接近0.1 mol·L-1,故C错误;加入适量
KOH固体,使SO的水解平衡逆向移动,c(SO)更接近0.1 mol·L-1,故D正确。
4.【答案】D
【解析】根据图示信息得知25 ℃时,CHCOONa溶液的pH是8.2,大于7,溶液显碱性,故A正确;
3
根据图示信息得知60 ℃水的pH=6.5,c(H+)=1×10-6.5 mol·L-1,无论什么温度下,水都是呈中性的,
故B正确;根据图示得知60 ℃时K =10-13,60 ℃,CHCOONa溶液中c(OH-)= mol·L-1=1×10-5.1
W 3
mol·L-1,故C正确;升高温度促进盐的水解,CHCOONa溶液水解程度增大,故D错误。
3
5.【答案】B
【解析】CHCOONa溶液中,物料关系为c(Na+)=c(CHCOO-)+c(CHCOOH),故A正确;由于
3 3 3
HCO既存在电离平衡,又存在水解平衡,不能根据①②溶液的pH判断醋酸和碳酸的酸性强弱,实际上酸
性:醋酸>碳酸,所以HCO的水解程度大于CHCOO-的水解程度,故B错误;CHCOONH 溶液的pH=
3 3 4
7.00,但CHCOO-和NH相互促进水解,则c(CHCOO-)=c(NH)<0.1 mol·L-1,故C正确;0.1 mol·L-
3 3
1NaHCO 溶液的pH=8.33,0.1 mol·L-1NH HCO 溶液相当于在0.1 mol·L-1NaHCO 溶液中加入等物质的量
3 4 3 3
的NH Cl固体,由于NH Cl水解显酸性,导致所得溶液的碱性减弱,即0.1 mol·L-1NH HCO 溶液的pH<
4 4 4 3
8.33,故D正确。
1.【答案】C
【详解】A.向明矾溶液中加入少量氢氧化钡溶液,铝离子、硫酸根离子过量,钡离子、氢氧根离子完全
反应生产氢氧化铝沉淀、硫酸钡沉淀:2Al3++3 +3Ba2++6OH-=2Al(OH) ↓+3BaSO ↓,A正确;
3 4
B.澄清石灰水中通入过量的二氧化碳生成可溶性碳酸氢钙溶液:CO+OH-=HCO ,B正确;
2C.氢氧化镁固体溶解于氯化铵溶液,是铵根离子水解生成的氢离子与氢氧化镁反应,故反应生成一水合
氨:Mg(OH) +2NH =Mg2++2NH∙H O;C错误;
2 3 2
D.SO 使酸性KMnO 溶液褪色是发生氧化还原反应生成硫酸根离子和锰离子:5SO +2H O+2 =5
2 4 2 2
+4H++2Mn2+,D正确;
故选C。
2.【答案】C
【详解】A.四种离子相互之间不反应,能共存,故A正确;
B.过氧化氢具有强氧化性,会和亚硫酸根离子发生氧化还原反应,HO+SO =SO +H O,故B正确;
2 2 2
C.碳酸氢根离子与铝离子发生双水解生成氢氧化铝沉淀和二氧化碳,3HCO +Al3+=3CO ↑+Al(OH) ↓,故
2 3
C错误 ;
D.四种离子相互之间不反应,能共存,,故D正确;
故选C。
3.【答案】D
【详解】①HS不充分燃烧生成S和水,S和氧气反应不能直接生成SO ;②Si在空气中点燃可以生成
2 3
SiO,SiO 不能和水反应生成HSiO;③饱和NaCl溶液中先通入氨气,再通入CO,可以生成溶解度较小
2 2 2 3 2
的NaHCO ,NaHCO 固体加热分解,可以得到NaCO,两步反应都可以实现转化;④Al和盐酸可以生成
3 3 2 3
AlCl 和氢气,AlCl 溶液中存在着Al3+的水解,水解生成的HCl挥发,所以直接加热AlCl 溶液不能得到无
3 3 3
水AlCl ,可以在氯化氢气流中加热;⑤铁和盐酸可以生成FeCl ,FeCl 和NaOH溶液反应生成Fe(OH) ,
3 2 2 2
Fe(OH) 容易被空气中的氧气氧化为Fe(OH) ,都可以实现转化,故选D。
2 3
4.【答案】B
【详解】A.实验1溶液 溶液中,根据质子守恒可知,该溶液中存在:
,A正确;B.向0.0100mol·L-1NaC O 溶液中滴加稀盐酸至溶液pH=7,则 ,又根据电荷守恒可得
2 2 4
,故c(Na+)=c((HC O )+2c(C O )+c(Cl-),B错误;
2 2
C.向 溶液中滴加等浓度等体积稀盐酸,则发生反应:
NaC O+HCl=NaHC O+NaCl,由题干信息 , 可知,Kh =
2 2 4 2 4 2
<Ka,即实验3溶液反应后显酸性,即电离大于水解,故实验3溶液中存在:c(HC O
2 2
)>c(C O )>c(H C O),C正确;
2 2 2 4
D.向 溶液中加入足量稀硫酸,即将NaC O 转化为HC O,HC O 为弱酸,在离
2 2 4 2 2 4 2 2 4
子方程式书写时不能拆,再滴加 溶液,溶液紫红色褪去,则实验4溶液中 参与反应的离子
方程式为: ,D正确;
故答案为:B。
5.【答案】D
【详解】A.浓度均为0.10 mol·L-1的NaHCO NaCO 的混合溶液中, 的水解程度大于 的水解程
3 2 3
度,所以溶液中c(Na+)>c( )>c( )>c(OH-),A错误;
B.浓度均为0.10 mol·L-1的氨水NH Cl混合溶液的pH=9.25,说明NH ·H O的电离程度大于 的水解程
4 3 2
度,溶液中c(NH ·H O)<c(Cl-),根据电荷守恒,溶液中c( )+c(H+)=c(Cl-)+c(OH-),可知c( )+
3 2
c(H+)>c(NH·H O)+c(OH-),B错误;
3 2
C.浓度均为0.10 mol·L-1的CHCOOHCHCOONa混合溶液的pH=4.76,说明CHCOOH的电离程度大于
3 3 3
CHCOO-的水解程度,则溶液中c(CHCOO-)>c(Na+)>c(CH COOH)>c(H+),C错误;
3 3 3D.浓度均为0.10 mol·L-1的HC ONaHC O 混合溶液的pH=1.68,根据电荷守恒有c(Na+)+c(H+)=c(OH-)
2 2 4 2 4
+c( )+2c( ),根据物料守恒有2c(Na+)=c( )+c(HC O)+c( ),联立上述两式得c(H
2 2 4
+)+c(HC O)=c(Na+)+c( )+c(OH-),D正确。
2 2 4
故选D。
11.【答案】D
【详解】
A. 中存在 和-COOH,所以溶液既有酸性又有碱性,故A正确;
B.氨基具有碱性,在酸性较强时会结合氢离子,羧基具有酸性,在碱性较强时与氢氧根离子反应,故曲
线a表示 的分布分数随溶液pH的变化,曲b表示
的分布分数随溶液pH的变化,曲线c表示 的分布分数随溶液pH的变化,故
B正确;
C. 的平衡常数 , 时,根
据a,b曲线交点坐标 可知, 时, ,则
,故C正确;
D.由C项分析可知, ,根据b,c曲线交点坐标坐标 分析可得电
离平衡 的电离常数为K= ,
1,则 ,即
,故D错误;
故答案选D。
2.【答案】C
【详解】
A.KOH吸收CO 所得到的溶液,若为KCO 溶液,则 主要发生第一步水解,溶液中:c(H CO)<c(
2 2 3 2 3
),若为KHCO 溶液,则 发生水解的程度很小,溶液中:c(H CO)<c( ),A不正确;
3 2 3
B.KOH完全转化为KCO 时,依据电荷守恒,溶液中:c(K+)+ c(H+)=c(OH-)+ +c( )+2c( ),依据
2 3
物料守恒,溶液中:c(K+)=2[c( )+c( )+c(H CO)],则c(OH-)= c(H+)+c( )+2c(H CO),B不正
2 3 2 3
确;
C.KOH溶液吸收CO,c(KOH)=0.1mol∙L-1,c =0.1mol∙L-1,则溶液为KHCO 溶液, K = =
2 总 3 h2
≈2.3×10-8>K =4.4×10-11,表明 以水解为主,所以溶液中:c(H CO)>c( ),C正确;
a2 2 3
D.如图所示的“吸收”“转化”过程中,发生反应为:CO+2KOH=K CO+H O、
2 2 3 2
KCO+CaO+H O=CaCO ↓+2KOH(若生成KHCO 或KCO 与KHCO 的混合物,则原理相同),二式相加得:
2 3 2 3 3 2 3 3
CO+CaO=CaCO ↓,该反应放热,溶液的温度升高,D不正确;
2 3
故选C。
3.【答案】A
【解析】
A、0.001 mol/L GHCl水溶液呈酸性,加水稀释之后酸性降低,所以pH升高,A正确;
B、GHCl为强酸弱碱盐,水解使溶液显酸性,因为水解存在水解平衡,所以0.001 mol/L GHCl的pH > 3,
B错误;
C、GHCl为强酸弱碱盐,在水中的电离方程式为GHCl =GH+ +C1-,C错误;
D、由电荷守恒可知,GHCl水溶液中存在c(OH-) +c(Cl- )= c(GH+)+ c(H+),D错误。故答案为A。
4.【答案】A
【解析】A.HCOONa和NaF的浓度相同,HCOONa溶液的pH较大,说明HCOO-的水解程度较大,根
据越弱越水解,因此甲酸的电离平衡常数较小,即K(HCOOH)<K(HF),错误;B.相同浓度的
a a
CHCOOH和CHCOONa两溶液等体积混合后pH约为4.7,此时溶液呈酸性,氢离子浓度大于氢氧根浓度,
3 3
说明溶液中醋酸电离程度大于水解程度,则醋酸根浓度大于钠离子浓度,则溶液中c(CHCOO-)>c(Na+)>
3
c(H+)>c(OH-),正确;C.CuS的溶解度较小,将CuS投入到稀硫酸溶液中,CuS溶解平衡电离出的S2−不
足以与H+发生反应,而将FeS投入到稀硫酸后可以得到HS气体,说明K (FeS)>K (CuS),正确;D.根
2 sp sp
据溶液中的物料守恒定律,1 mol∙L−1 Na S溶液中所有含S元素的粒子的总物质的量的浓度为1 mol∙L−1,即
2
c(S2−)+c(HS-)+c(H S)=1 mol∙L−1,正确;综上所述,答案为A。
2
5.【答案】B
【解析】A.CHCOOH溶液中的H+来自醋酸分子的电离和水的电离,所以
3
[CHCOOH]>[H+]>[CH COO-]>[OH-],错误;B.①②等体积混合后恰好反应生成CHCOONa,体积大约为
3 3 3
原来的2倍,如果CHCOO-不水解,浓度约为原来的1/2,CHCOONa为弱酸强碱盐,越稀越水解,
3 3
CHCOO- +H O CHCOOH+OH-,水解平衡向正向移动,因此CHCOO-浓度小于原来的1/2,正确;
3 2 3 3
C.①③等体积混合以后,溶液呈酸性,说明CHCOOH的电离程度大于CHCOO- 的水解程度,因此
3 3
(CHCOO-)>(Na+)>(H+),错误;D.①②等体积混合以后恰好反应生成CHCOONa,CHCOO- 的水解促进
3 3 3
水的电离,①③等体积混合,CHCOOH电离产生的H+抑制水的电离,因此总体上看①②等体积混合后水
3
的电离程度比①③等体积混和后水的电离程度大,错误;答案选B。