文档内容
考向 28 沉淀溶解平衡
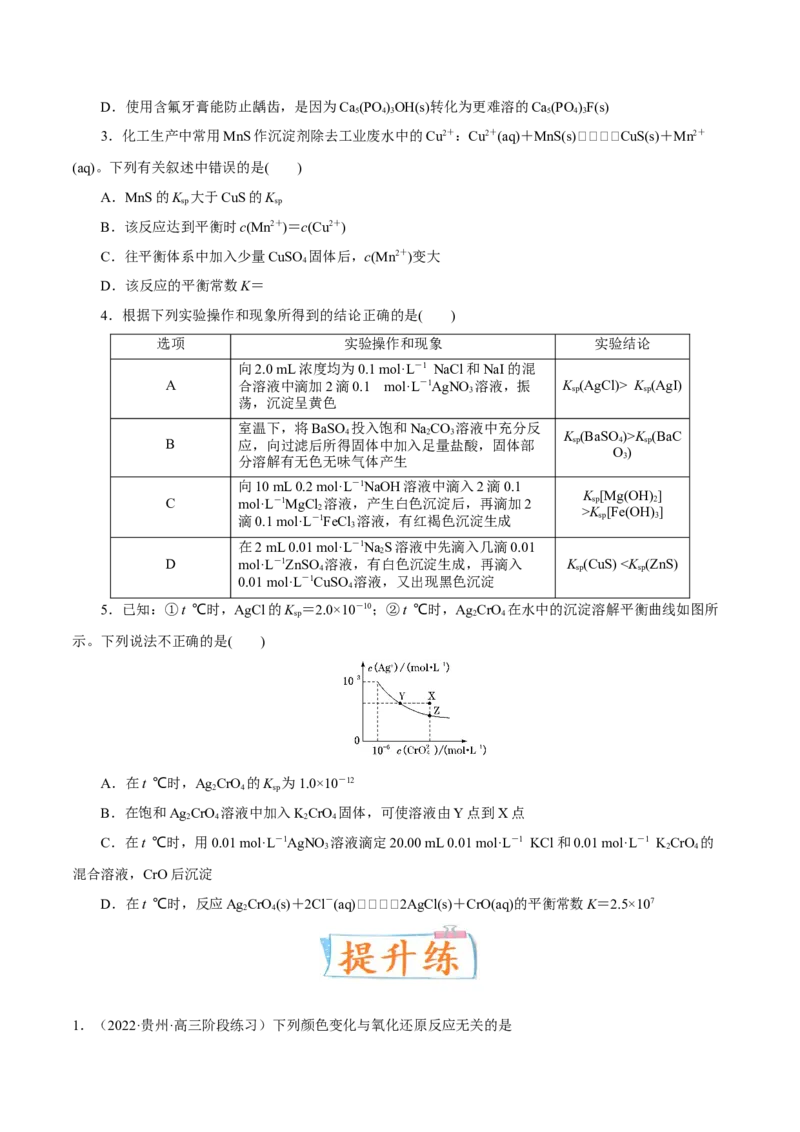
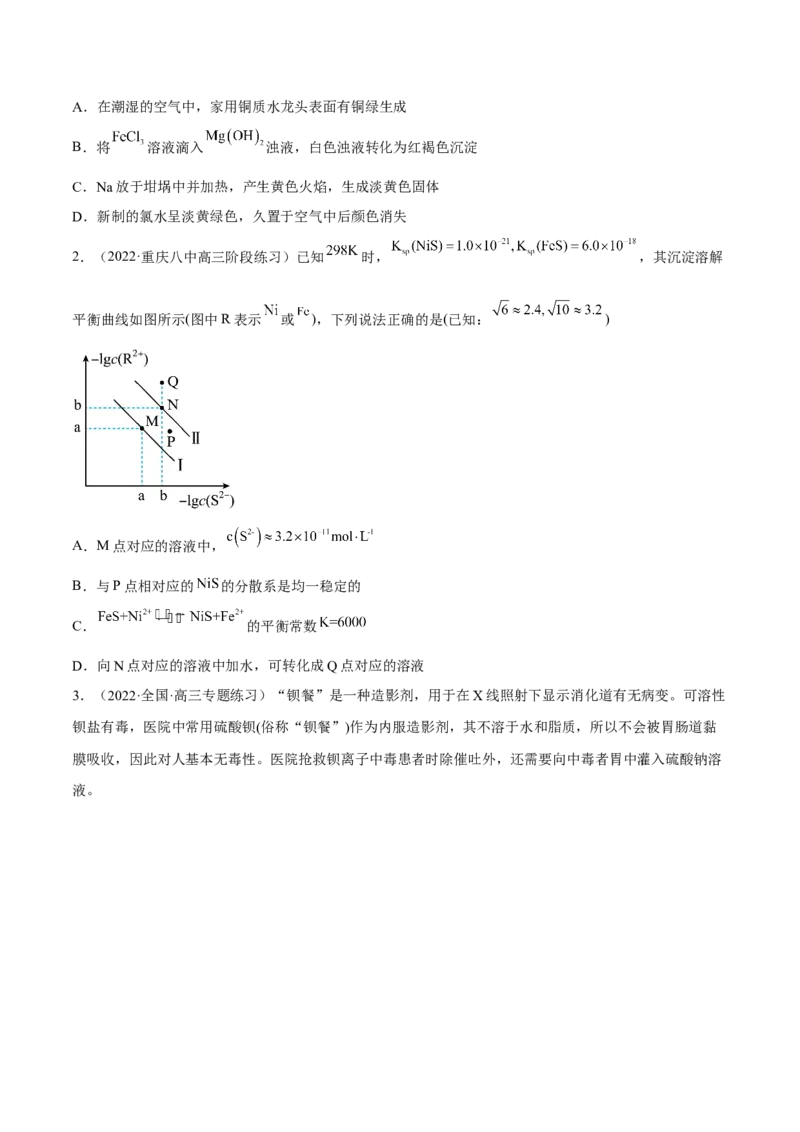
(2022海南,双选)某元素M的氢氧化物 在水中的溶解反应为:
、 ,25℃,-lgc与pH的关系如
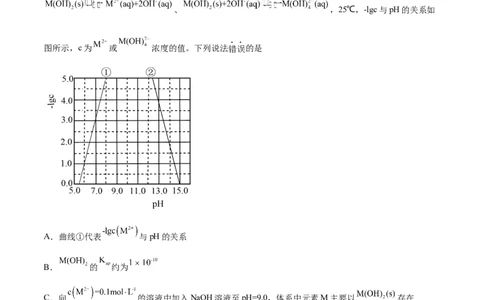
图所示,c为 或 浓度的值。下列说法错误的是
A.曲线①代表 与pH的关系
B. 的 约为
C.向 的溶液中加入NaOH溶液至pH=9.0,体系中元素M主要以 存在
D.向 的溶液中加入等体积0.4mol/L的HCl后,体系中元素M主要以 存在
【答案】BD【分析】由题干信息,M(OH)2(s)
M2+(aq)+2OH-(aq),M(OH)2(s)+2OH-(aq)
M(OH)
2
4
-
(aq),随着
2- 2-
pH增大,c(OH-)增大,则c(M2+)减小,c[M(OH)4 ]增大,即-lg c(M2+)增大,-lg c[M(OH)4 ]减小,因此曲
2-
线①代表-lg c(M2+)与pH的关系,曲线②代表-lg c[M(OH)4 ]与pH的关系,据此分析解答。
【详解】A.由分析可知,曲线①代表-lg c(M2+)与pH的关系,A正确;
B.由图象,pH=7.0时,-lg c(M2+)=3.0,则M(OH)2的Ksp=c(M2+)·c2(OH-)=1×10-17,B错误;
2-
C.向c(M2+)=0.1mol/L的溶液中加入NaOH溶液至pH=9.0,根据图像,pH=9.0时,c(M2+)、c[M(OH)4 ]
均极小,则体系中元素M主要以M(OH)2(s)存在,C正确;
2-
D.c[M(OH)4 ]=0.1mol/L的溶液中,由于溶解平衡是少量的,因此加入等体积的0.4mol/L的HCl后,体系
2-
中元素M仍主要以M(OH)4 存在,D错误;
答案选BD。知识点一 沉淀溶解平衡及应用
1.沉淀溶解平衡的含义
在一定温度下的水溶液中,当沉淀溶解与生成的速率相等时,即建立了沉淀溶解平衡状态。
2.沉淀溶解平衡的建立
固体溶质溶液中的溶质
3.沉淀溶解平衡的特点
4.沉淀溶解平衡的影响因素
(1)内因
难溶电解质本身的性质是决定因素。
(2)外因
[名师点拨] (1)难溶电解质不一定是弱电解质,如BaSO、AgCl等都是强电解质。
4
(2)难溶电解质存在沉淀溶解平衡,如BaSO(s)Ba2+(aq)+SO(aq),遵循化学平衡移动原理。
4
5.沉淀溶解平衡的应用
(1)沉淀的生成
①原理:当Q>K 时,难溶电解质的溶解平衡向左移动,生成沉淀。
c sp
②应用:可利用生成沉淀来达到除去溶液中杂质离子的目的。
③方法
a.调节pH法:如除去NH Cl溶液中的FeCl 杂质,可加入氨水调节pH至4左右,离子方程式为 Fe 3 +
4 3
+ 3NH ·H O == = 。
3 2
b.沉淀剂法:如用HS沉淀Cu2+,离子方程式为 Cu 2 + + H S == =CuS↓ + 2H + 。
2 2[名师点拨] 若一种沉淀剂可使溶液中多种离子产生沉淀时,则可控制条件,使这些离子先后分别沉
淀。
(1)对同一类型的沉淀,K 越小越先沉淀,且K 相差越大分步沉淀效果越好。如在Cl-、Br-、I-的混
sp sp
合溶液中,由于AgCl、AgBr、AgI的K 相差较大,逐滴加入Ag+可按I-、Br-、Cl-的顺序先后沉淀,即
sp
K 最小的首先沉淀出来。
sp
(2)对不同类型的沉淀,其沉淀先后顺序要利用K 计算溶液中离子的浓度,根据离子浓度的大小来判
sp
断沉淀的先后顺序,如AgCl和Ag CrO 的分步沉淀,可通过控制Ag+浓度来完成。
2 4
(2)沉淀的溶解
当沉淀溶解平衡体系中的离子发生反应时,其浓度会降低,沉淀溶解平衡就会向溶解的方向移动,从
而使沉淀溶解。
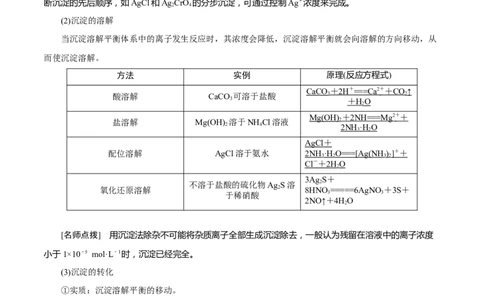
方法 实例 原理(反应方程式)
CaCO + 2H + == =C a 2 + + CO ↑
酸溶解 CaCO 可溶于盐酸 3 2
3 + H O
2
Mg(OH) + 2NH == =M g 2 + +
盐溶解 Mg(OH) 溶于NH Cl溶液 2
2 4 2NH ·H O
3 2
AgCl +
配位溶解 AgCl溶于氨水 2NH ·H O == =[Ag(NH ) ] + +
3 2 3 2
Cl - + 2H O
2
3Ag S+
不溶于盐酸的硫化物Ag S溶 2
氧化还原溶解 2 8HNO=====6AgNO+3S+
于稀硝酸 3 3
2NO↑+4HO
2
[名师点拨] 用沉淀法除杂不可能将杂质离子全部生成沉淀除去,一般认为残留在溶液中的离子浓度
小于1×10-5 mol·L-1时,沉淀已经完全。
(3)沉淀的转化
①实质:沉淀溶解平衡的移动。
②举例:MgCl 溶液――→Mg(OH) ――→Fe(OH) ,则K [Mg(OH) ]>K [Fe(OH) ]。
2 2 3 sp 2 sp 3
③规律:一般说来,溶解度小的沉淀转化成溶解度更小的沉淀容易实现。
④应用
a.锅炉除水垢:将CaSO 转化为CaCO ,离子方程式为CaSO (s) + CO(aq)CaCO (s) + SO(aq) 。
4 3 4 3
b.矿物转化:CuSO 溶液遇ZnS转化为CuS,离子方程式为 ZnS(s) + Cu 2 + (aq)CuS(s) + Zn 2 +
4
(aq)。[名师点拨] 溶解度小的沉淀转化成溶解度更小的沉淀容易实现,但溶解度小的沉淀转化成溶解度稍
大的沉淀,通过控制反应条件也能实现,但前提是溶液的Q>K ,如BaSO[K =1.1×10-10]用饱和NaCO
c sp 4 sp 2 3
溶液浸泡可部分转化为BaCO [K =2.58×10-9]。
3 sp
知识点二 沉淀溶解平衡常数及应用
1.溶度积和离子积
以A B (s) mAn+(aq)+nBm-(aq)为例:
m n
溶度积 离子积
溶液中有关离子浓度幂的乘
概念 沉淀溶解的平衡常数
积
符号 K Q
sp c
K (A B )=cm(An+)·cn(Bm-),
sp m n Q(A B )=cm(An+)·cn(Bm-),
表达式 表达式中的浓度都是平衡浓 c m n
表达式中的浓度是任意浓度
度
判断在一定条件下沉淀能否生成或溶解
①QK :溶液过饱和,有沉淀析出
c sp
应用
②QK :溶液饱和,处于平衡状态
c sp
③QK :溶液未饱和,无沉淀析出
c sp
[名师点拨] (1)K 只与温度有关,与浓度无关;升高温度,大多数固体难溶电解质的K 增大,但
sp sp
Ca(OH) 却相反。
2
(2)对于K 表达式类型相同的物质,如Mg(OH) 和Zn(OH) ,K 的大小反映了难溶电解质在溶液中的
sp 2 2 sp
溶解能力的大小,一般K 越小,则溶解度越小。
sp
(3)对于阴、阳离子的个数比不同的难溶电解质,它们的溶解度不能直接用K 的大小来比较,如
sp
AgCl(K =1.8×10-10)、Ag CrO(K =1.0×10-12),Ag CrO 溶液中的c(Ag+)大于AgCl溶液中的c(Ag+)。
sp 2 4 sp 2 4
2.沉淀溶解平衡曲线中Q 和K 的关系
c sp
难溶电解质(以BaSO 沉淀曲线为例说明)Q 和K 间的关系有以下三种可能:在曲线上任何一点,Q=
4 c sp c
K ,沉淀与溶解达到动态平衡,溶液是饱和溶液。
sp
在曲线右上方Q>K ,溶液处于过饱和,有沉淀析出,直至Q=K 。
c sp c sp
在曲线左下方Q<K ,为不饱和溶液,无沉淀析出,直至Q=K 。
c sp c sp
知识点三 K 的相关计算
sp溶度积计算的几种类型
考查角度 计算技巧
①把离子浓度数据代入K 表达式得Q,
sp c
判断沉淀的生成或沉淀是否 若Q>K ,则有沉淀生成
c sp
完全
②利用K 的数值计算某一离子浓度,若该离子浓度小于10-
sp
5 mol·L-1,则该离子沉淀完全
①根据氢氧化物的K ,先计算初始浓度溶液中c(OH-),再
sp
求得溶液的pH
常温下,计算氢氧化物沉淀
开始和沉淀完全时的pH
②金属阳离子沉淀完全时的离子浓度为10-5 mol·L-1,依据
K 可计算金属阳离子沉淀完全时溶液中的c(OH-),进而求
sp
得pH
计算沉淀转化反应的平衡常 依据沉淀的转化反应和K ,计算该反应的平衡常数,K值越
sp
数,并判断沉淀转化的程度 大,转化反应越易进行,转化程度越大
①若沉淀类型相同,则K 小的化合物先沉淀;
sp
沉淀先后的计算与判断
②若沉淀类型不同,则需要根据K 计算出沉淀时所需离子
sp
浓度,所需离子浓度小的先沉淀
1.向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成。经查资料得知:Ag
++2NH ·H O[Ag(NH)]++2HO,平衡常数记为K,下列分析不正确的是( )
3 2 3 2 2
A.浊液中存在溶解平衡:AgCl(s)Ag+(aq)+Cl-(aq)
B.实验表明实验室可用氨水洗涤附着有银的试管
C.由实验可以判断:NH 结合Ag+的能力比Cl-强
3
D.由资料信息可推知:加浓硝酸后生成的沉淀为AgCl
2.牙齿表面覆盖的牙釉质是人体中最坚硬的部分,起着保护牙齿的作用,其主要成分为羟基磷酸钙
[Ca (PO )OH]。在牙齿表面存在着如下平衡:Ca (PO )OH(s)5Ca2+(aq)+3PO(aq)+OH-(aq), K
5 4 3 5 4 3 sp
=6.8×10-37。已知Ca (PO )F(s)的K =2.8×10-61。下列说法错误的是( )
5 4 3 sp
A.残留在牙齿上的糖发酵会产生H+,经常吃糖易造成龋齿
B.由题述平衡可知,小孩长牙时要少吃糖多补钙
C.若减少OH-的浓度,题述平衡将向右移动,K 的值相应增大
spD.使用含氟牙膏能防止龋齿,是因为Ca (PO )OH(s)转化为更难溶的Ca (PO )F(s)
5 4 3 5 4 3
3.化工生产中常用MnS作沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+MnS(s)CuS(s)+Mn2+
(aq)。下列有关叙述中错误的是( )
A.MnS的K 大于CuS的K
sp sp
B.该反应达到平衡时c(Mn2+)=c(Cu2+)
C.往平衡体系中加入少量CuSO 固体后,c(Mn2+)变大
4
D.该反应的平衡常数K=
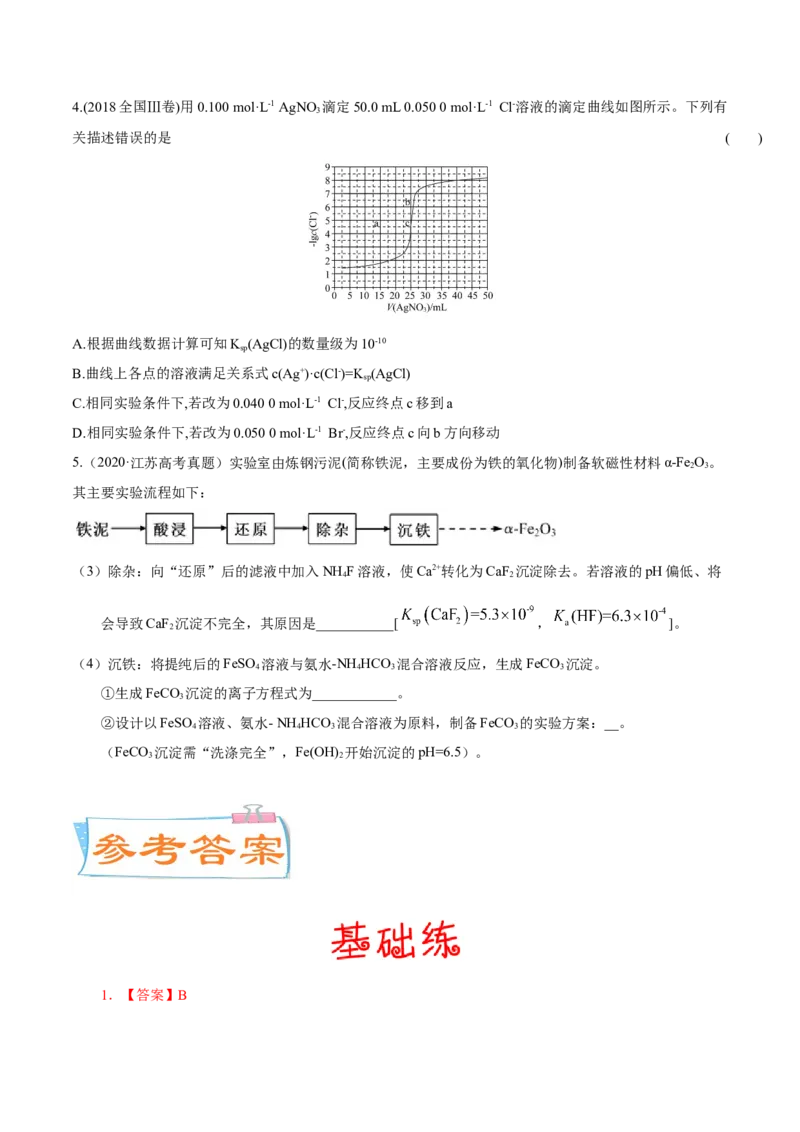
4.根据下列实验操作和现象所得到的结论正确的是( )
选项 实验操作和现象 实验结论
向2.0 mL浓度均为0.1 mol·L-1 NaCl和NaI的混
A 合溶液中滴加2滴0.1 mol·L-1AgNO 溶液,振 K (AgCl)> K (AgI)
3 sp sp
荡,沉淀呈黄色
室温下,将BaSO 投入饱和NaCO 溶液中充分反
4 2 3 K (BaSO)>K (BaC
B 应,向过滤后所得固体中加入足量盐酸,固体部 sp 4 sp
O)
分溶解有无色无味气体产生 3
向10 mL 0.2 mol·L-1NaOH溶液中滴入2滴0.1
K [Mg(OH) ]
C mol·L-1MgCl 溶液,产生白色沉淀后,再滴加2 sp 2
2 >K [Fe(OH) ]
滴0.1 mol·L-1FeCl 溶液,有红褐色沉淀生成 sp 3
3
在2 mL 0.01 mol·L-1NaS溶液中先滴入几滴0.01
2
D mol·L-1ZnSO 溶液,有白色沉淀生成,再滴入 K (CuS) K (BaSO)
sp 3 sp 4
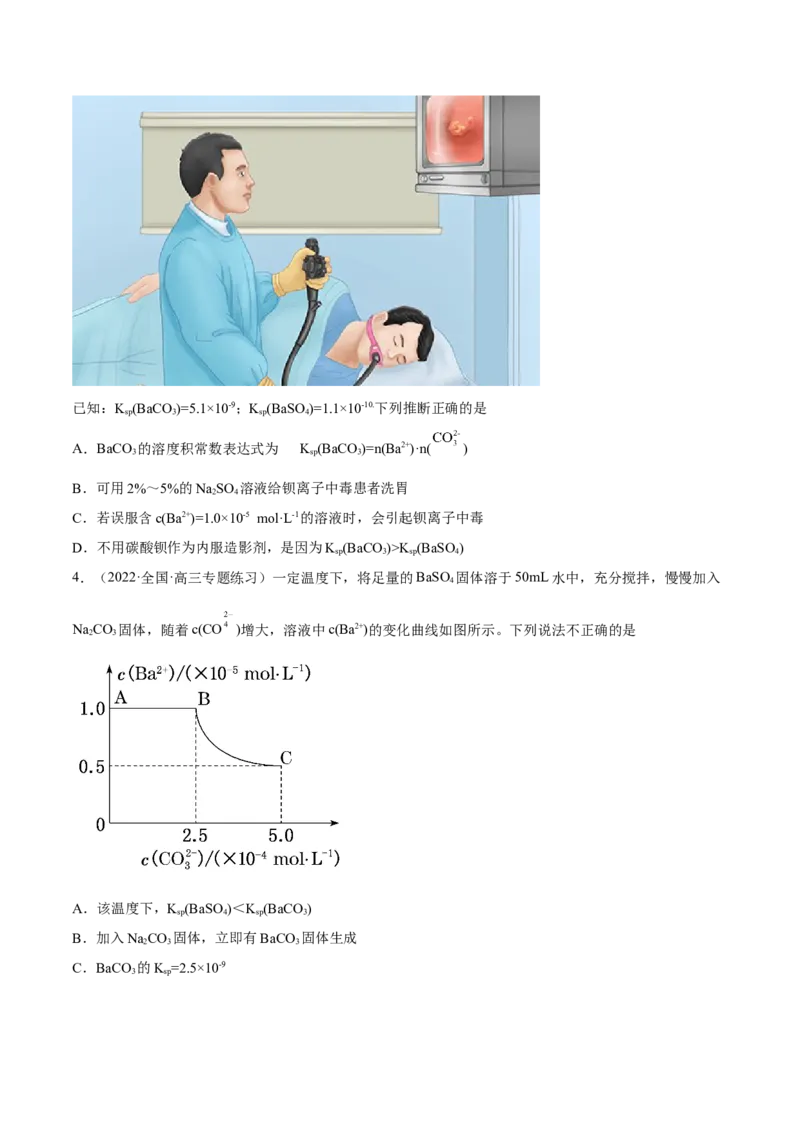
4.(2022·全国·高三专题练习)一定温度下,将足量的BaSO 固体溶于50mL水中,充分搅拌,慢慢加入
4
NaCO 固体,随着c(CO )增大,溶液中c(Ba2+)的变化曲线如图所示。下列说法不正确的是
2 3
A.该温度下,K (BaSO)<K (BaCO)
sp 4 sp 3
B.加入NaCO 固体,立即有BaCO 固体生成
2 3 3
C.BaCO 的K =2.5×10-9
3 spD.曲线BC段内, =25
5.(2022·全国·高三专题练习)已知25℃时,RSO (s)+CO (aq) RCO(s)+SO (aq)的平衡常数
4 3
K=1.75×104,K (RCO)=2.80×10-9,下列叙述中正确的是
sp 3
A.向c(CO )=c(SO )的混合液中滴加RCl 溶液,首先析出RSO 沉淀
2 4
B.将浓度均为6×10-6mol•L-1的RCl 、NaCO 溶液等体积混合后可得到RCO 沉淀
2 2 3 3
C.25℃时,RSO 的K 约为4.9×10-5
4 sp
D.相同温度下,RCO 在水中的K 大于在NaCO 溶液中的K
3 sp 2 3 sp
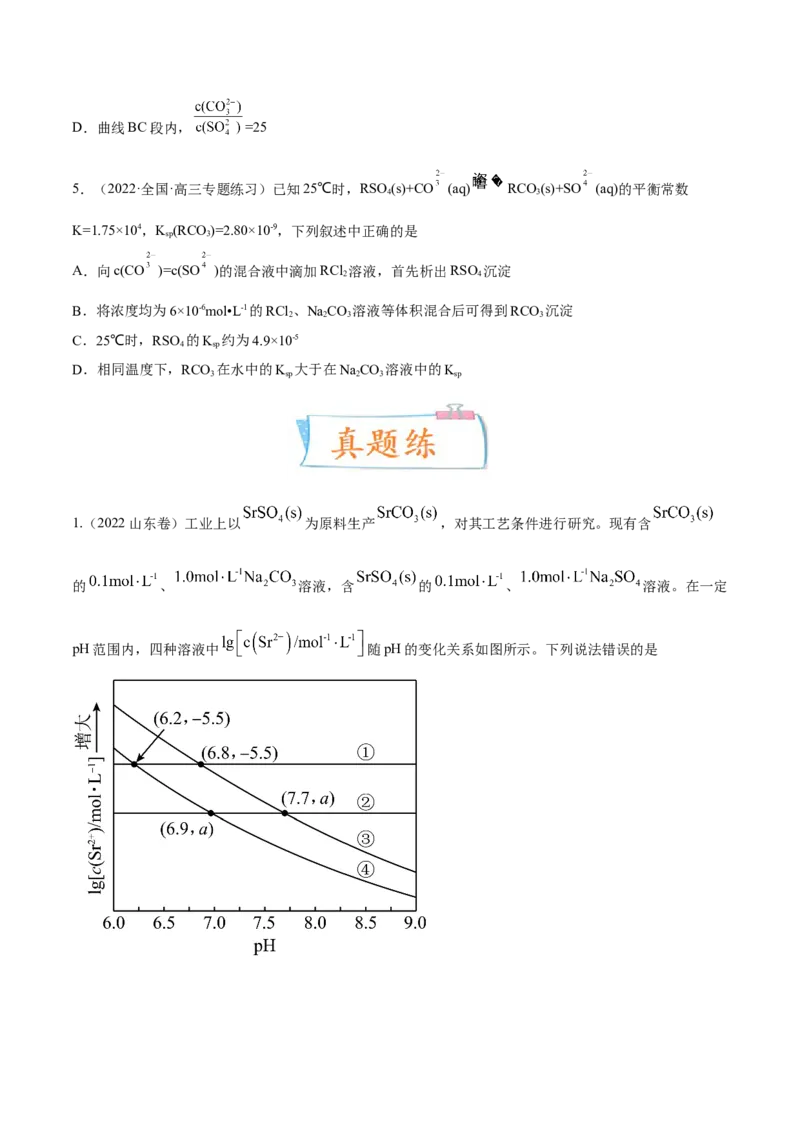
1.(2022山东卷)工业上以 为原料生产 ,对其工艺条件进行研究。现有含
的 、 溶液,含 的 、 溶液。在一定
pH范围内,四种溶液中 随pH的变化关系如图所示。下列说法错误的是A. 反应 的平衡常数
B.
C. 曲线④代表含 的 溶液的变化曲线
D. 对含 且 和 初始浓度均为 的混合溶液, 时才发生沉淀
转化
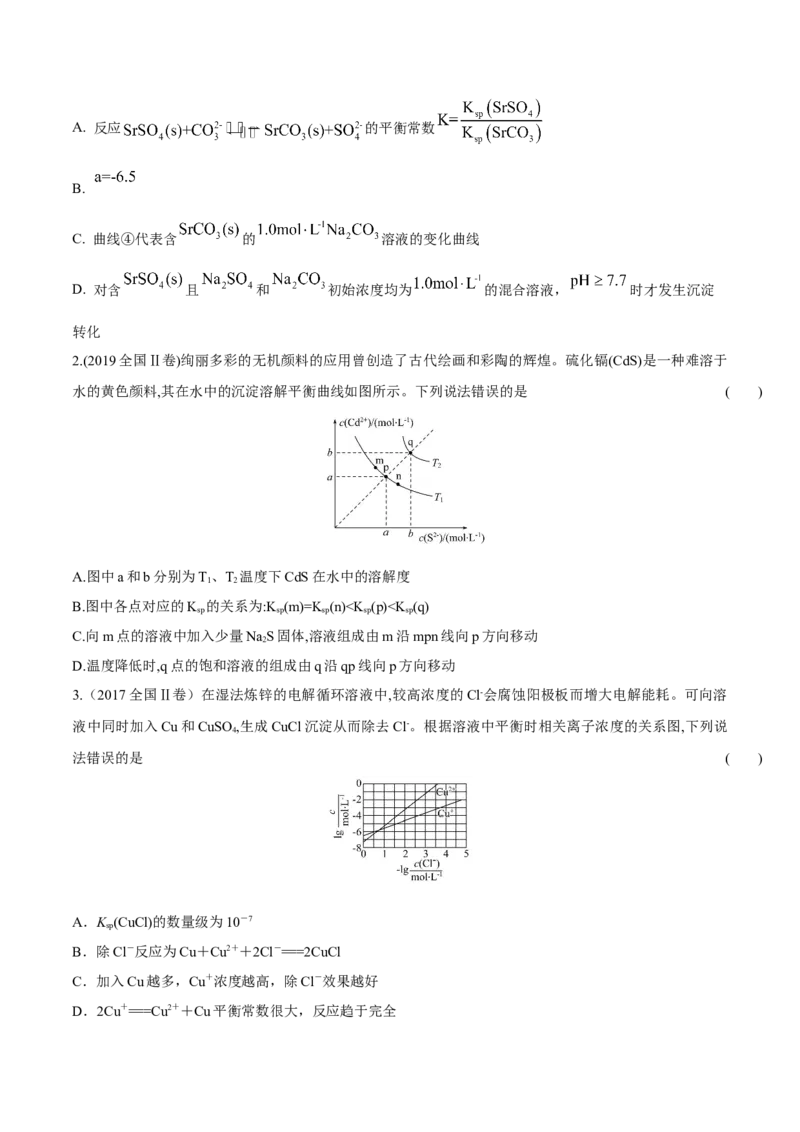
2.(2019全国Ⅱ卷)绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一种难溶于
水的黄色颜料,其在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是 ( )
A.图中a和b分别为T、T 温度下CdS在水中的溶解度
1 2
B.图中各点对应的K 的关系为:K (m)=K (n)K (CuS),A正确;该反应达到平衡时
sp sp
c(Mn2+)和c(Cu2+)保持不变,但不一定相等,B错误;往平衡体系中加入少量CuSO 固体后,平衡向正反
4
应方向移动,c(Mn2+)变大,C正确;该反应的平衡常数K===,D正确。
4. 【答案】A
【解析】沉淀呈黄色,说明加入AgNO 溶液时先生成AgI沉淀,A正确;CO浓度大,BaSO 部分转
3 4
化为BaCO ,不能比较K (BaSO)、K (BaCO)的大小,B错误;NaOH溶液过量,与FeCl 反应生成沉淀,
3 sp 4 sp 3 3
不能判断两者K 的大小,C错误;NaS溶液过量,与CuSO 溶液反应生成CuS,不能说明
sp 2 4
K (CuS)K (RCO),故向c( )=c( )的混合液中滴加RCl
4 3 sp 4 sp 3 2
溶液,首先析出RCO 沉淀,A项错误;
3
B.将浓度均为6×10-6mol•L-1的RCl 、NaCO 溶液等体积混合后,c(R2+)=3×10-6mol•L-1、c( )=3×10-
2 2 3
6mol•L-1,此时的离子积Q=c(R2+)•c( )=3×10-6×3×10-6=9×10-12-
3
lgc(Cl-),即在c点的上方,故D说法正确。
5.【答案】(3) 或
(4)在搅拌下向FeSO 溶液中缓慢加入氨水-NH HCO 混
4 4 3
合溶液,控制溶液pH不大于6.5;静置后过滤,所得沉淀用蒸馏水洗涤2~3次;取最后一次洗涤后的
滤液,滴加盐酸酸化的BaCl 溶液,不出现白色沉淀
2
【解析】铁泥的主要成份为铁的氧化物,铁泥用HSO 溶液“酸浸”得到相应硫酸盐溶液,向“酸浸”后
2 4
的滤液中加入过量铁粉将Fe3+还原为Fe2+;向“还原”后的滤液中加入NH F使Ca2+转化为CaF 沉淀
4 2
而除去;然后进行“沉铁”生成FeCO,将FeCO 沉淀经过系列操作制得α—Fe O;据此分析作答。
3 3 2 3(3)向“还原”后的滤液中加入NH F溶液,使Ca2+转化为CaF 沉淀,K (CaF )=c(Ca2+)·c2(F-),当Ca2+完
4 2 sp 2
全沉淀(某离子浓度小于1×10-5mol/L表明该离子沉淀完全)时,溶液中c(F-)至少为 mol/
L= ×10-2mol/L;若溶液的pH偏低,即溶液中H+浓度较大,H+与F-形成弱酸HF,导致溶液中
c(F-)减小,CaF 沉淀不完全,故答案为:pH偏低形成HF,导致溶液中F-浓度减小,CaF 沉淀不完全。
2 2
(4)①将提纯后的FeSO 溶液与氨水—NH HCO 混合溶液反应生成FeCO 沉淀,生成FeCO 的化学方程
4 4 3 3 3
式为FeSO +NH·H O+NH HCO =FeCO ↓+(NH)SO +H O[或FeSO +NH+NHHCO =FeCO ↓+
4 3 2 4 3 3 4 2 4 2 4 3 4 3 3
(NH )SO ],离子方程式为Fe2++ +NH·H O=FeCO↓+ +H O(或Fe2++
4 2 4 3 2 3 2
+NH=FeCO ↓+ ),答案为:Fe2++ +NH·H O=FeCO↓+ +H O(或Fe2++
3 3 3 2 3 2
+NH=FeCO ↓+ )。
3 3
②根据题意Fe(OH) 开始沉淀的pH=6.5,为防止产生Fe(OH) 沉淀,所以将FeSO 溶液与氨水—NH HCO
2 2 4 4 3
混合溶液反应制备FeCO 沉淀的过程中要控制溶液的pH不大于6.5;FeCO 沉淀需“洗涤完全”,所
3 3
以设计的实验方案中要用盐酸酸化的BaCl 溶液检验最后的洗涤液中不含 ;则设计的实验方案
2
为:在搅拌下向FeSO 溶液中缓慢加入氨水—NH HCO 混合溶液,控制溶液pH不大于6.5;静置后过
4 4 3
滤,所得沉淀用蒸馏水洗涤2~3次;取最后一次洗涤后的滤液,滴加盐酸酸化的BaCl 溶液,不出现
2
白色沉淀,故答案为:在搅拌下向FeSO 溶液中缓慢加入氨水—NH HCO 混合溶液,控制溶液pH不
4 4 3
大于6.5;静置后过滤,所得沉淀用蒸馏水洗涤2~3次;取最后一次洗涤后的滤液,滴加盐酸酸化的
BaCl 溶液,不出现白色沉淀。
2