文档内容
2021 年高一上学期第二次月考检测·化学试卷
(满分100分,考试时间90分钟)
第I卷(选择题 共40分)
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符
合题意。
1. 下列物质和水或二氧化碳反应均能生成氧气的是
A. Na B. NaO C. NaO D.
2 2 2
NaHCO
3
【答案】C
【解析】
【分析】
【详解】A.Na和水剧烈反应产生氢氧化钠和氢气,不生成氧气,A项不选;
B.NaO和水反应生成氢氧化钠,不生成氧气,B项不选;
2
C.NaO 和水反应生成氢氧化钠和氧气,和二氧化碳反应生成碳酸钠和氧气,C项选;
2 2
D.NaHCO 不能和水或二氧化碳反应,D项不选;
3
答案选C。
2. 将足量新制氯水滴入下列物质中,对应现象错误的是
A. FeCl 溶液,溶液由浅绿色变为棕黄色 B. 淀粉-KI溶液,溶液变蓝
2
C. AgNO 溶液,有白色沉淀生成 D. 石蕊试液,溶液变红不褪色
3
【答案】D
【解析】
【分析】
【详解】A.向FeCl 溶液中加入氯水,发生反应:2FeCl +Cl=2FeCl ,因此看到溶液会由
2 2 2 3
浅绿色变为棕黄色,A正确;
B.向淀粉-KI溶液中加入氯水,KI被Cl 氧化产生I,I 遇淀粉溶液变蓝色,B正确;
2 2 2
C.氯水中含有HCl,与AgNO 溶液会发生复分解反应产生AgCl白色沉淀,C正确;
3
D.氯水中含有HCl、HClO,使溶液显酸性,酸能够使紫色石蕊试液变为红色;但由于
HClO同时具有氧化性,又会将红色物质氧化变为无色,因此会看到石蕊试液先变红后褪
色,D错误;
故合理选项是D。
3. 用高铁酸钠(Na FeO)对河水和湖水消毒是城市饮用水处理的新技术。已知反应:
2 4
Fe O+3Na O=2Na FeO+Na O,下列说法正确的是
2 3 2 2 2 4 2
A. NaO 既是氧化剂又是还原剂
2 2
B. 在NaFeO 中Fe为+4价,具有强氧化性
2 4
C. 3molNa O 发生反应,有12mol电子转移
2 2
D. NaFeO 既是氧化产物又是还原产物
2 4【答案】D
【解析】
【详解】A.反应中过氧化钠中氧元素化合价由-1价降低到-2价,做氧化剂,A错误;
B.在NaFeO 中Fe为+6价,B错误;
2 4
C.NaO 发生反应,每个O转移1个电子,故3mol Na O 有6mol电子转移,C错误;
2 2 2 2
D.NaFeO 中的铁元素是从+3价变为+6价,氧元素化合价从-1价变为-2价,所以NaFeO
2 4 2 4
既是氧化产物又是还原产物, D正确;
故选D。
4. 水镁矾(MgSO ·H O)主要产于盐湖中,为盐湖沉积物,是提取镁的一种矿石矿物。下列
4 2
有关1 mol MgSO ·H O的说法正确的是
4 2
A. 摩尔质量为138 B. 质量为138 g
C. 物质的量为138 D. 氧原子总数为4N
A
【答案】B
【解析】
【详解】A.MgSO ·H O式量是138,所以其摩尔质量是138 g/mol,A错误;
4 2
B.MgSO ·H O式量是138,则1 mol MgSO ·H O的质量是138 g,B正确;
4 2 4 2
C.1 mol MgSO ·H O,表明其物质的量是1 mol,C错误;
4 2
D.1个MgSO ·H O中含有4+1=5个O原子,则1 mol MgSO ·H O中含有的氧原子总数为
4 2 4 2
5N ,D错误;
A
选B。
5. 偏二甲肼(C HN)是一种高能燃料,燃烧产生的巨大能量可作为航天运载火箭的推动力。
2 8 2
下列叙述正确的是
A. 偏二甲肼的摩尔质量为60g
B. 6.02×1023个偏二甲肼分子的质量约为60g
C. 1mol偏二甲肼的质量为60g·mol-1
D. 6g偏二甲肼含有N 个偏二甲肼分子
A
【答案】B
【解析】
【分析】
【详解】A.偏二甲肼(C HN )的摩尔质量为(12×2+1×8+14×2)g/mol=60g/mol,故
2 8 2
A错误;
B.6.02×1023个偏二甲肼的物质的量为 ,所以1 mol 偏
二甲肼的质量为60 g,故B正确;
C.1mol偏二甲肼的质量为60 g,故C错误;D.偏二甲肼的物质的量为 ,含有的分子数为0.1×N ,故D
A
错误。
故选:B。
6. 下列关于0.1mol/LH SO 溶液的叙述错误的是
2 4
A. 1L该溶液中含有HSO 的质量为9.8g
2 4
B. 0.5L该溶液中氢离子的物质的量浓度为0.2mol/L
C. 从1L该溶液中取出100mL,则取出的溶液中HSO 的物质的量浓度为0.01mol/L
2 4
D. 取该溶液10mL加水稀释至100mL后,HSO 的物质的量浓度为0.01mol/L
2 4
【答案】C
【解析】
【详解】A.1L该硫酸溶液中含有溶质的物质的量n=cV=0.1mol/L×1L=0.1mol,则其中含有
溶质的质量m=0.1mol×98g/mol=9.8g,A正确;
B.硫酸是二元强酸,根据电解质及其电离产生的离子浓度关系可知
c(H+)=2c(H SO )=0.1 2=0.2mol/L,B正确;
2 4
C.溶液具有均一性,溶液的浓度与其取出的体积大小无关,所以从1L该溶液中取出
×
100mL,则取出的溶液中HSO 的物质的量浓度仍为0.1mol/L,C错误;
2 4
D.溶液在稀释过程中溶质的物质的量不变,所以稀释后溶液的浓度c=
=0.01mol/L,D正确;
故合理选项是C。
7. 用N 表示阿伏伽德罗常数的值,下列说法正确的是( )
A
A. 标准状况下,22.4LCCl 中含原子总数为5N
4 A
B. 物质的量浓度为0.5 MgCl 溶液中,含有Cl—数目为N
2 A
C. 常温常压下,N 个CO 分子占的体积大于22.4L
A 2
D. 3.2g由氧气和臭氧组成的混合物中含有氧气分子的数目为0.1N
A
【答案】C
【解析】
【详解】A. 标况下,CCl 为液态,无法根据体积计算其物质的量,故A错误;
4
B. 只知道浓度,体积未知,无法计算溶液中溶质的多少,故B错误;
C. 常温常压下,气体摩尔体积大于22.4L/mol,N 个CO 分子占的体积大于22.4L,故C正
A 2
确;
D. 氧气和臭氧均是由氧原子构成,故3.2g混合气体中含有的氧原子的物质的量0.2mol,但
氧气分子的物质的量无法确定,分子数目也无法确定,故D错误;
故选C。
8. 下列表中对应关系均正确的是选
俗名 名称 化学式
项
A 苏打 亚硫酸钠 NaSO
2 3
B 小苏打 碳酸氢钠 NaHCO
3
C 苛性钠 钠 Na
D 纯碱 氢氧化钠 NaOH
A. A B. B C. C D. D
【答案】B
【解析】
【分析】
【详解】A.苏打,碳酸钠,NaCO,A错误;
2 3
B.小苏打,碳酸氢钠,NaHCO ,B正确;
3
C.苛性钠,氢氧化钠,NaOH,C错误;
D.纯碱,碳酸钠,NaCO,D错误;
2 3
故答案选B。
9. 下列离子方程式正确的是
A. NaO 投入水中:2HO+2 =4OH-+O ↑
2 2 2 2
B. 金属钠投入MgSO 溶液中:2Na+2HO+Mg2+=Mg(OH) ↓+H ↑
4 2 2 2
C. 小苏打溶液中加入过量澄清石灰水:Ca2++OH-+ =CaCO ↓+H O
3 2
D. 次氯酸钠溶液中通入过量CO:2ClO-+CO +H O= +2HClO
2 2 2
【答案】C
【解析】
【详解】A.NaO 是固体,不能拆,离子方程式应该为:2NaO+2H O=4Na++4OH-+O ↑,
2 2 2 2 2 2
A错误;
B.元素不守恒,离子方程式应该为:2Na+2HO+Mg2+=Mg(OH) ↓+H ↑+2Na+,B错误;
2 2 2
C.反应符合反应事实,遵循物质的拆分原则,C正确;
D.CO 过量,反应产生 ,离子方程式应该为:ClO-+CO +H O= +HClO,D
2 2 2
错误;
故合理选项是C。
10. 将绿豆大的钠块投入如图所示的烧杯中,可能出现的现象是A. 钠块只在煤油层中游动,并放出气体
B. 钠块只在水层中游动,钠块熔化,水层变红
C. 钠块在 层和水层界面处游动并上下跳动,钠块熔化,水层变红
D. 钠块在水层和煤油层界面处游动并上下跳动,钠块熔化,水层变红
【答案】D
【解析】
【详解】A.钠的密度比煤油的大,比水的小,则钠在水层与煤油层界面发生反应,产生
的氢气使钠块四处游动并上下跳动,故A不符合题意;
B.根据A分析得到钠块在水层和煤油层之间上下跳动,生成的NaOH使溶液变红,故B
不符合题意;
C.根据A分析钠块在煤油层和水层界面处并上下跳动,钠块熔化,生成的NaOH使溶液
变红,故C不符合题意;
D.根据前面分析得到钠块在水层和煤油层界面处游动并上下跳动,钠块熔化,水层变红,
故D符合题意。
综上所述,答案 为D。
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项
符合题意,全部选对得4分,选对但不全的得2分,有选错的得0分。
11. 已知氟、氯、溴、碘、砹为同一族元素,其中溴化砹(AtBr)可发生下列反应:
①2AtBr+2Mg=MgBr +MgAt ;②AtBr+2NH(l)=NHBr+AtNH。
2 2 3 4 2
对上述两个反应 的有关说法正确的是
A. 这两个反应都不是氧化还原反应
B. 反应①中MgAt 既是氧化产物,又是还原产物
2
C. 反应②中AtBr既是氧化剂,又是还原剂
D. 反应①中氧化剂与还原剂 的物质的量之比为1∶2
【答案】B
【解析】
【详解】A.反应①中有元素化合价的变化,属于氧化还原反应,反应②中没有元素化合
价变化,不属于氧化还原反应,A错误;
B.反应①中Mg的化合价升高,生成的MgAt 是氧化产物;At的化合价由+1降低到
2
MgAt 中的-1,MgAt 又是还原产物,B正确;
2 2
C.反应②中没有元素化合价变化,不是氧化还原反应,所以反应中无氧化剂、还原剂,C错误;
D.反应①中AtBr作氧化剂,Mg作还原剂,氧化剂与还原剂的物质的量之比为1∶1,D
错误;
故合理选项是B。
12. 下列实验操作、现象、结论均正确的是
选项 实验操作 实验现象 实验结论
将过氧化钠投入滴有酚酞试液的水 过氧化钠与水反应
A 溶液最终为红色
中 生成碱性物质
溶解度:NaCO 小
2 3
B 向饱和NaCO 溶液中通入CO 气体 有晶体析出
2 3 2
于NaHCO
3
集气瓶中产生浓
将镁条点燃后迅速伸入集满CO 的集 镁与CO 发生了置
2 2
C 烟并有黑色颗粒
气瓶 换反应
产生
向某无色溶液中滴加NaOH溶液,
D 试纸不变蓝 原溶液中无
将湿润的红色石蕊试纸置于试管口
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.过氧化钠与水反应产生碱,使酚酞试液变为红色,过氧化钠具有强氧化性,
又将红色物质氧化变为无色,故最终溶液无色,A错误;
B.NaCO 的溶解度大于NaHCO ,B错误;
2 3 3
C.Mg与CO 在点燃时反应产生MgO和C单质,MgO是白色固体,C是黑色物质,因此
2
反应过程中有浓烟并有黑色颗粒产生,该反应基本类型是置换反应,C正确;
D. 的检验操作为:向某无色溶液中滴加NaOH溶液并加热,再将湿润的红色石蕊试
纸置于试管口进行检验,D错误;
选C。
13. 由KSO 、Al (SO )、KAl(SO )·12H O及HSO 组成的混合溶液中测得c(H+)=0.1
2 4 2 4 3 4 2 2 2 4
mol·L-1,c(Al3+)=0.3 mol·L-1,c( )=0.6 mol·L-1,则c(K+)为
A. 0.2 mol·L-1 B. 0.3 mol·L-1 C. 0.4 mol·L-1 D. 0.5
mol·L-1
【答案】A
【解析】
【详解】根据溶液呈电中性,由电荷守恒可得关系式 0.1×1+0.3×3+c(K+)×1=0.6×2 ,解得c(K+)=0.2 mol·L-1,故合理选项是A;
选A。
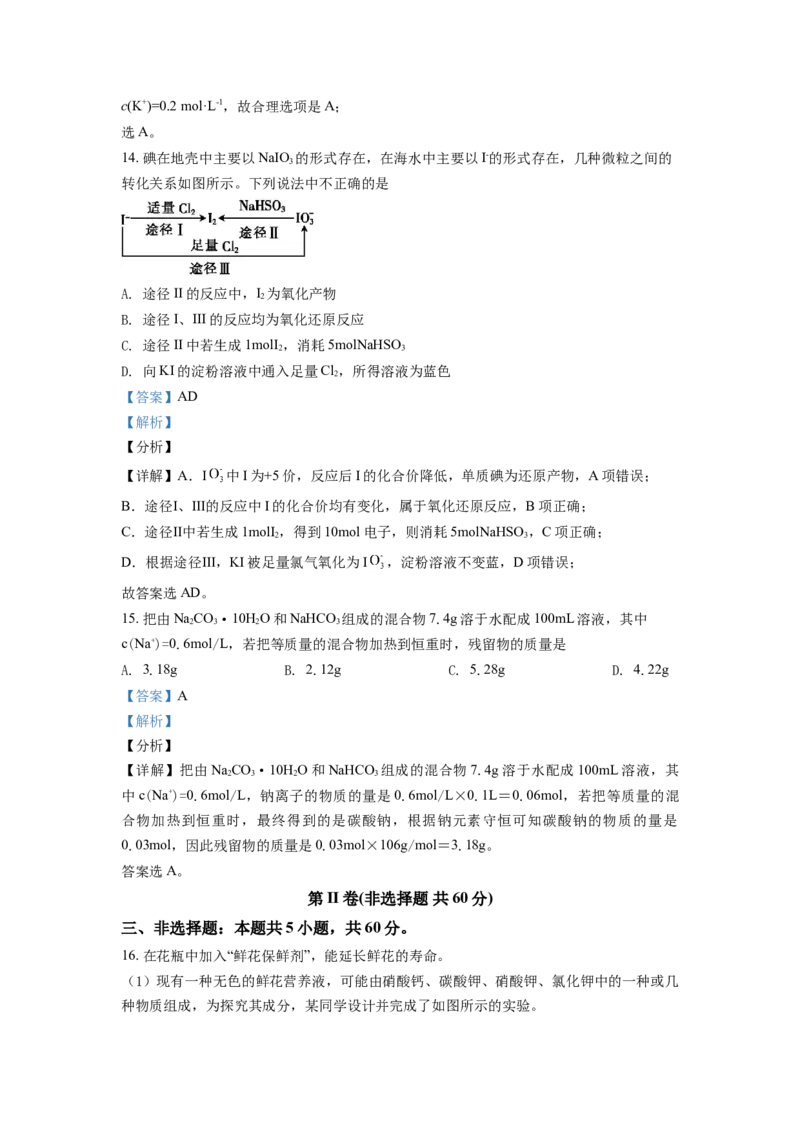
14. 碘在地壳中主要以NaIO 的形式存在,在海水中主要以I-的形式存在,几种微粒之间的
3
转化关系如图所示。下列说法中不正确的是
A. 途径II的反应中,I 为氧化产物
2
B. 途径I、III的反应均为氧化还原反应
C. 途径II中若生成1molI ,消耗5molNaHSO
2 3
D. 向KI的淀粉溶液中通入足量Cl,所得溶液为蓝色
2
【答案】AD
【解析】
【分析】
【详解】A.I 中I为+5价,反应后I的化合价降低,单质碘为还原产物,A项错误;
B.途径Ⅰ、Ⅲ的反应中I的化合价均有变化,属于氧化还原反应,B项正确;
C.途径Ⅱ中若生成1molI ,得到10mol电子,则消耗5molNaHSO ,C项正确;
2 3
D.根据途径Ⅲ,KI被足量氯气氧化为I ,淀粉溶液不变蓝,D项错误;
故答案选AD。
15. 把由NaCO·10HO和NaHCO 组成的混合物7.4g溶于水配成100mL溶液,其中
2 3 2 3
c(Na+)=0.6mol/L,若把等质量的混合物加热到恒重时,残留物的质量是
A. 3.18g B. 2.12g C. 5.28g D. 4.22g
【答案】A
【解析】
【分析】
【详解】把由NaCO·10HO和NaHCO 组成的混合物7.4g溶于水配成100mL溶液,其
2 3 2 3
中c(Na+)=0.6mol/L,钠离子的物质的量是0.6mol/L×0.1L=0.06mol,若把等质量的混
合物加热到恒重时,最终得到的是碳酸钠,根据钠元素守恒可知碳酸钠的物质的量是
0.03mol,因此残留物的质量是0.03mol×106g/mol=3.18g。
答案选A。
第II卷(非选择题 共60分)
三、非选择题:本题共5小题,共60分。
16. 在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。
(1)现有一种无色的鲜花营养液,可能由硝酸钙、碳酸钾、硝酸钾、氯化钾中的一种或几
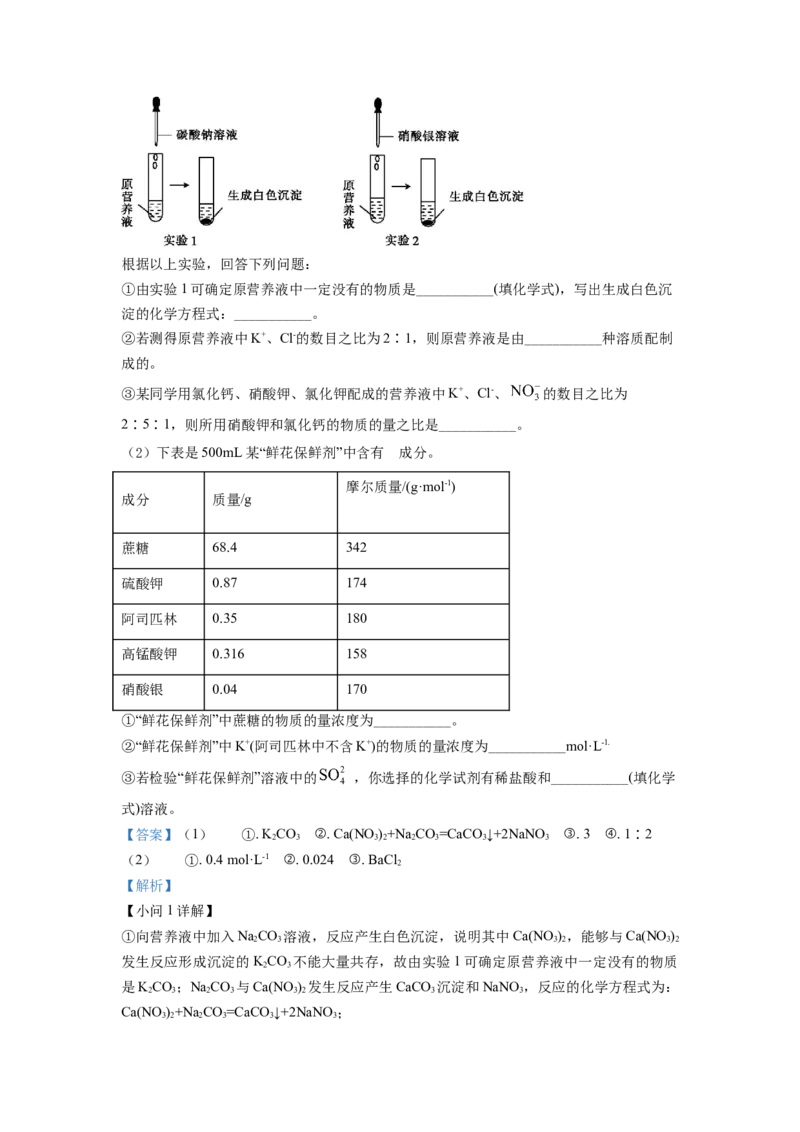
种物质组成,为探究其成分,某同学设计并完成了如图所示的实验。根据以上实验,回答下列问题:
①由实验1可确定原营养液中一定没有的物质是___________(填化学式),写出生成白色沉
淀的化学方程式:___________。
②若测得原营养液中K+、Cl-的数目之比为2∶1,则原营养液是由___________种溶质配制
成的。
③某同学用氯化钙、硝酸钾、氯化钾配成的营养液中K+、Cl-、 的数目之比为
2∶5∶1,则所用硝酸钾和氯化钙的物质的量之比是___________。
(2)下表是500mL某“鲜花保鲜剂”中含有 的成分。
摩尔质量/(g·mol-1)
成分 质量/g
蔗糖 68.4 342
硫酸钾 0.87 174
阿司匹林 0.35 180
高锰酸钾 0.316 158
硝酸银 0.04 170
①“鲜花保鲜剂”中蔗糖的物质的量浓度为___________。
②“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为___________mol·L-1.
③若检验“鲜花保鲜剂”溶液中的 ,你选择的化学试剂有稀盐酸和___________(填化学
式)溶液。
【答案】(1) ①. KCO ②. Ca(NO )+Na CO=CaCO ↓+2NaNO ③. 3 ④. 1∶2
2 3 3 2 2 3 3 3
(2) ①. 0.4 mol·L-1 ②. 0.024 ③. BaCl
2
【解析】
【小问1详解】
①向营养液中加入NaCO 溶液,反应产生白色沉淀,说明其中Ca(NO ) ,能够与Ca(NO )
2 3 3 2 3 2
发生反应形成沉淀的KCO 不能大量共存,故由实验1可确定原营养液中一定没有的物质
2 3
是KCO ;NaCO 与Ca(NO ) 发生反应产生CaCO 沉淀和NaNO ,反应的化学方程式为:
2 3 2 3 3 2 3 3
Ca(NO )+Na CO=CaCO ↓+2NaNO ;
3 2 2 3 3 3②若测得原营养液中K+、Cl-的数目之比为2∶1,根据①分析可知其中不含KCO,含有
2 3
K+的物质还有KCl、KNO,KCl中K+、Cl-的数目之比为1∶1,因此其中一定含KCl、
3
KNO,结合①确定其中含有Ca(NO ),故原营养液是由KCl、KNO、Ca(NO ) 三种物质
3 3 2 3 3 2
组成;
③假如 的物质的量是1 mol,则n(K+)=2 mol,n(Cl-)=5 mol,由 守恒可知
n(KNO)=1 mol,根据K+守恒,可知n(KCl)=2mol-1 mol=1 mol,再根据Cl-守恒,可知
3
n(CaCl )= ,故n(KNO):n(CaCl )=1 mol:2 mol=1:2;
2 3 2
【小问2详解】
①m(蔗糖)=68.4 g,其物质的量n(蔗糖)= ,溶液的体积是500 mL,则
蔗糖溶液的浓度c(蔗糖)= =0.4 mol/L;
②在保鲜剂中KSO 、KMnO 能够电离产生K+,n(K SO )= =0.005 mol;
2 4 4 2 4
n(KMnO)= =0.002 mol,n(K+)=2n(K SO )+n(KMnO)=2×0.005 mol+0.002
4 2 4 4
mol=0.012 mol,溶液的体积是500 mL,则c(K+)= =0.024 mol/L;
③利用BaSO 是白色既不溶于水也不溶于盐酸的性质进行检验。故若检验“鲜花保鲜剂”溶
4
液中的 ,可选择的化学试剂有稀盐酸和BaCl 溶液。
2
17. 目前,能较稳定存在的氯的氧化物有ClO、ClO 、ClO 等。有关数据见下表:
2 2 2 7
化学式 ClO ClO ClO
2 2 2 7
沸点/℃ 3.8 11.0 82.0
回答下列问题:
(1)常温常压下,三种氧化物中属于气体的是___________。
(2)ClO 是一种常用的消毒剂,在消毒水时,ClO 还可将水中的Fe2+、Mn2+等转化成
2 2
Fe(OH) 和MnO 等难溶物除去,说明ClO 具有___________性。
3 2 2
(3)工业上可以用反应2NaClO+H SO +SO=2ClO +2NaHSO 制备ClO ,请用单线桥法表
3 2 4 2 2 4 2
示该反应电子转移的方向和数目:___________。
(4)实验室制备ClO 的反应原理为2NaClO+4HCl(浓)=2ClO ↑+Cl↑+2H O+2NaCl。
2 3 2 2 2
①浓盐酸在反应中体现的性质是___________(填字母)。
A.还原性 B.氧化性 C.酸性
②若上述反应中产生0.1molClO ,则转移的电子数为___________。
2【答案】(1)ClO、ClO
2 2
(2)氧化 (3)
(4) ①. AC ②. 0.1N
A
【解析】
【小问1详解】
室温温度是25℃,当物质沸点高于25℃时物质在室温下呈气态。根据三种氧化物的沸点可
知:常温常压下,三种氧化物中属于气体的是ClO、ClO ;
2 2
【小问2详解】
在消毒水时,ClO 还可将水中的 Fe2+、Mn2+等转化成Fe(OH) 和MnO 等难溶物除去,
2 3 2
Fe2+、Mn2+化合价升高,失去电子被氧化,说明ClO 具有氧化性;
2
【小问3详解】
在反应2NaClO+H SO +SO=2ClO +2NaHSO 中,Cl元素化合价由反应前NaClO 中的+5价
3 2 4 2 2 4 3
变为反应后ClO 中的+4价,化合价降低1×2=2价,得到电子2e-,S元素化合价由反应前
2
SO 中的+4价变为反应后NaHSO 中的+6价,化合价升高2价,失去电子2e-,用单线桥法
2 4
表示该反应电子转移的方向和数目为: ;
【小问4详解】
①在该反应中浓盐酸中的Cl一部分由HCl中-1价变为Cl 中的0价,化合价升高,失去电
2
子表现还原性;一部分仍然是-1价的Cl,与金属阳离子结合形成盐NaCl,其中酸电离产生
H+与O结合形成HO,表现酸性,故浓盐酸表现酸性、还原性,故合理选项是AC;
2
②在该反应中,每反应产生1 mol ClO,反应转移1 mol电子,反应若上述反应中产生0.1
2
mol ClO ,则转移的电子数为0.1N 。
2 A
18. Ba(OH) 是一种强碱,可用于测定天然气中CO 的含量。
2 2
(1)请写出足量氢氧化钡溶液吸收CO 气体的化学方程式:___________。
2
(2)某课外小组通过以下实验操作测定Ba(OH) ·nH O中n的值。
2 2
①称取5.25 g试样(含有杂质)配成100 mL溶液。配制溶液中用到的仪器有天平、
___________、___________、___________和胶头滴管等。若配制过程中定容后经振荡、摇
匀、静置,发现液面下降,再加适量蒸馏水,则所得溶液的浓度将___________(填“偏大”
“不变”或“偏小”)。
②用30.00 mL1 mol·L-1盐酸与上述Ba(OH) 溶液反应,消耗该Ba(OH) 溶液100.00 mL(杂质
2 2
不与酸反应),则该Ba(OH) 溶液的物质的量浓度为___________。
2
③另取5.25g试样加热至失去全部结晶水(杂质不分解),称得剩余固体质量为3.09 g,则
Ba(OH) ·nH O中n=___________。
2 2
【答案】(1)CO+Ba(OH) =BaCO ↓+H O
2 2 3 2
(2) ①. 100 mL容量瓶 ②. 玻璃棒 ③. 烧杯 ④. 偏小 ⑤. 0.15 mol·L-1⑥. 8
【解析】
【小问1详解】
足量氢氧化钡溶液吸收 CO 气体,反应产生 BaCO 沉淀和水,反应的化学方程式为:
2 3
CO+Ba(OH) =BaCO ↓+H O;
2 2 3 2
【小问2详解】
①称取5.25 g试样(含有杂质)配成100 mL溶液。配制溶液中用到的仪器有天平(带砝码)、
药匙、100 mL容量瓶、玻璃棒、烧杯、胶头滴管等;
若配制过程中定容后经振荡、摇匀、静置,发现液面下降,这是由于部分溶液粘在容量瓶
的瓶颈上,若再加适量蒸馏水,溶剂体积偏大,则所得溶液的浓度将偏小;
②HCl与Ba(OH) 反应方程式为:2HCl+ Ba(OH) =BaCl +2H O,n(HCl)=1 mol/L×0.030
2 2 2 2
L=0.03 mol,则n[Ba(OH) ]= n(HCl)=0.015 mol,溶液体积是100 .00 mL,则其浓度
2
c[Ba(OH) ]= ;
2
③5.25 g晶体中含有的结晶水的物质的量n(H O)= ,其中含有氢氧
2
化钡的物质的量n[Ba(OH) ]=0.015 mol,n(H O):n[Ba(OH) ]=0.12 mol:0.015 mol=8。故该
2 2 2
晶体中结晶水的数目是8。
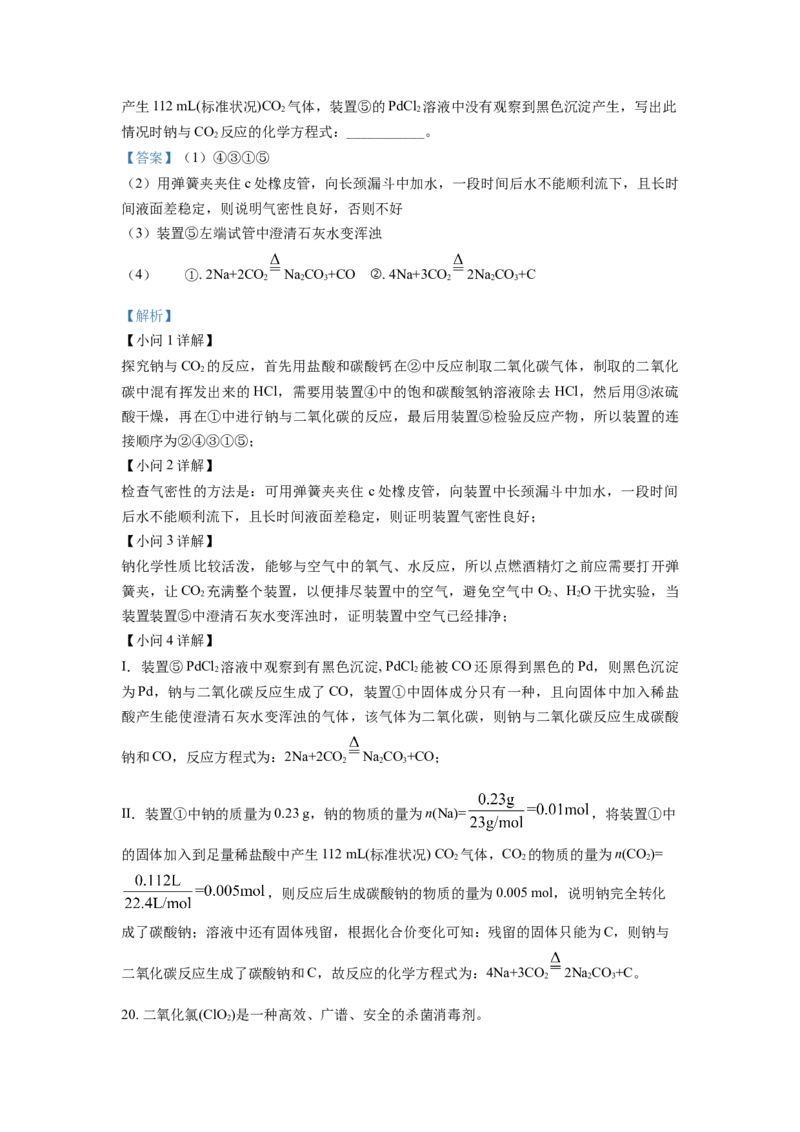
19. 某学生为了探究钠与CO 的反应,利用如图装置进行实验。[已知PdCl (氯化钯)能被CO
2 2
还原得到黑色的Pd]
(1)请将上图各装置按顺序连接完整②→___________(填装置序号)。
(2)检查装置②的气密性的方法是___________。
(3)装好药品后,点燃酒精灯之前应进行的操作是打开弹簧夹,让CO 充满整个装置,当
2
观察到___________时再点燃酒精灯。
(4)通入CO 的量不同可能会导致生成的产物不同。假如反应过程中有下列两种情况,按
2
要求分别写出两种情况时的化学方程式。
I.当装置⑤的PdCl 溶液中观察到有黑色沉淀产生时,装置①中剩余固体成分只有一种,
2
且向剩余固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体,写出此情况时钠与CO 反
2
应的化学方程式:_______。
II.当装置①中钠的质量为0.23 g时,充分反应后,将装置①中的固体加入足量稀盐酸中,产生112 mL(标准状况)CO 气体,装置⑤的PdCl 溶液中没有观察到黑色沉淀产生,写出此
2 2
情况时钠与CO 反应的化学方程式:___________。
2
【答案】(1)④③①⑤
(2)用弹簧夹夹住c处橡皮管,向长颈漏斗中加水,一段时间后水不能顺利流下,且长时
间液面差稳定,则说明气密性良好,否则不好
(3)装置⑤左端试管中澄清石灰水变浑浊
(4) ①. 2Na+2CO NaCO+CO ②. 4Na+3CO 2NaCO+C
2 2 3 2 2 3
【解析】
【小问1详解】
探究钠与CO 的反应,首先用盐酸和碳酸钙在②中反应制取二氧化碳气体,制取的二氧化
2
碳中混有挥发出来的HCl,需要用装置④中的饱和碳酸氢钠溶液除去 HCl,然后用③浓硫
酸干燥,再在①中进行钠与二氧化碳的反应,最后用装置⑤检验反应产物,所以装置的连
接顺序为②④③①⑤;
【小问2详解】
检查气密性的方法是:可用弹簧夹夹住 c处橡皮管,向装置中长颈漏斗中加水,一段时间
后水不能顺利流下,且长时间液面差稳定,则证明装置气密性良好;
【小问3详解】
钠化学性质比较活泼,能够与空气中的氧气、水反应,所以点燃酒精灯之前应需要打开弹
簧夹,让CO 充满整个装置,以便排尽装置中的空气,避免空气中O 、HO干扰实验,当
2 2 2
装置装置⑤中澄清石灰水变浑浊时,证明装置中空气已经排净;
【小问4详解】
I.装置⑤PdCl 溶液中观察到有黑色沉淀, PdCl 能被CO还原得到黑色的Pd,则黑色沉淀
2 2
为Pd,钠与二氧化碳反应生成了CO,装置①中固体成分只有一种,且向固体中加入稀盐
酸产生能使澄清石灰水变浑浊的气体,该气体为二氧化碳,则钠与二氧化碳反应生成碳酸
钠和CO,反应方程式为:2Na+2CO NaCO+CO;
2 2 3
II.装置①中钠的质量为0.23 g,钠的物质的量为n(Na)= ,将装置①中
的固体加入到足量稀盐酸中产生112 mL(标准状况) CO 气体,CO 的物质的量为n(CO)=
2 2 2
,则反应后生成碳酸钠的物质的量为0.005 mol,说明钠完全转化
成了碳酸钠;溶液中还有固体残留,根据化合价变化可知:残留的固体只能为C,则钠与
二氧化碳反应生成了碳酸钠和C,故反应的化学方程式为:4Na+3CO 2NaCO+C。
2 2 3
20. 二氧化氯(ClO )是一种高效、广谱、安全的杀菌消毒剂。
2(1)氯化钠电解法是一种可靠的工业生产ClO 的方法。
2
①用于电解的食盐水需先除去其中的Ca2+、Mg2+、 等杂质。操作为往粗盐水中先加入
过量的___________(填化学式),至沉淀不再产生后,再加入过量的NaCO 和NaOH,充分
2 3
反应。
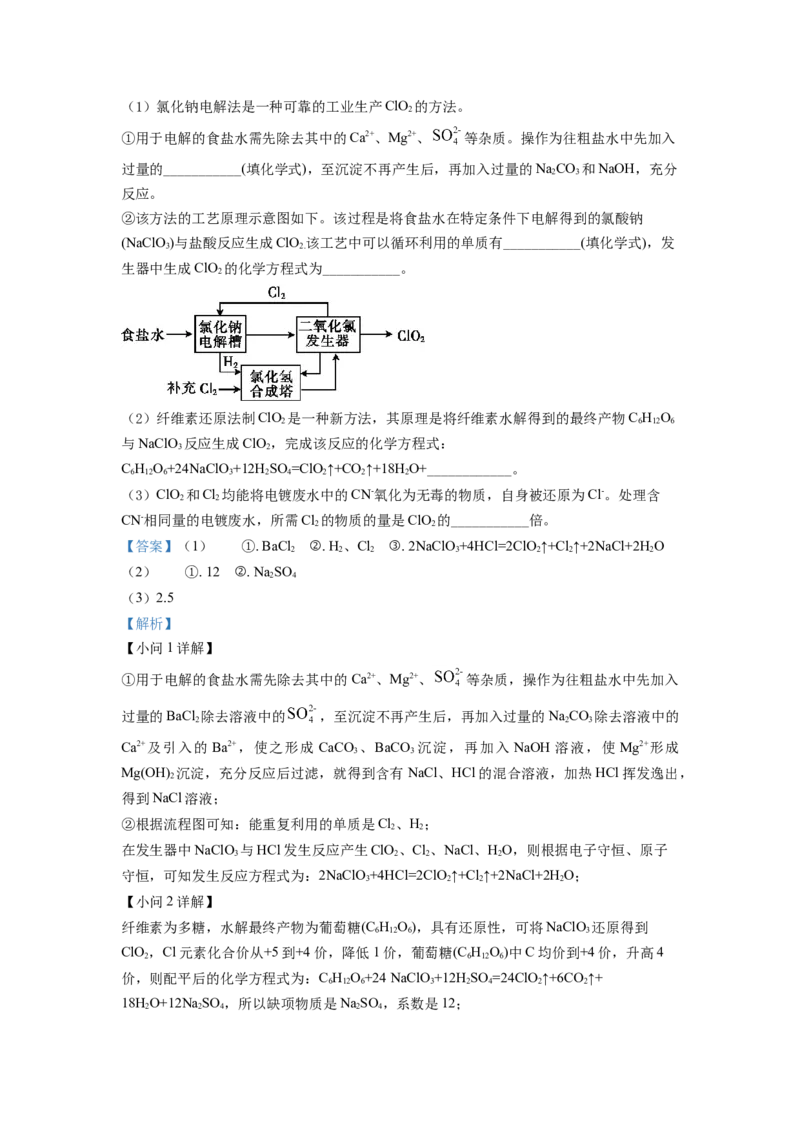
②该方法的工艺原理示意图如下。该过程是将食盐水在特定条件下电解得到的氯酸钠
(NaClO)与盐酸反应生成ClO 该工艺中可以循环利用的单质有___________(填化学式),发
3 2.
生器中生成ClO 的化学方程式为___________。
2
(2)纤维素还原法制ClO 是一种新方法,其原理是将纤维素水解得到的最终产物C H O
2 6 12 6
与NaClO 反应生成ClO ,完成该反应的化学方程式:
3 2
C H O+24NaClO +12H SO =ClO ↑+CO ↑+18H O+____________。
6 12 6 3 2 4 2 2 2
(3)ClO 和Cl 均能将电镀废水中的CN-氧化为无毒的物质,自身被还原为Cl-。处理含
2 2
CN-相同量的电镀废水,所需Cl 的物质的量是ClO 的___________倍。
2 2
【答案】(1) ①. BaCl ②. H、Cl ③. 2NaClO+4HCl=2ClO ↑+Cl↑+2NaCl+2HO
2 2 2 3 2 2 2
(2) ①. 12 ②. NaSO
2 4
(3)2.5
【解析】
【小问1详解】
①用于电解的食盐水需先除去其中的Ca2+、Mg2+、 等杂质,操作为往粗盐水中先加入
过量的BaCl 除去溶液中的 ,至沉淀不再产生后,再加入过量的NaCO 除去溶液中的
2 2 3
Ca2+及引入的 Ba2+,使之形成 CaCO 、BaCO 沉淀,再加入 NaOH 溶液,使 Mg2+形成
3 3
Mg(OH) 沉淀,充分反应后过滤,就得到含有NaCl、HCl的混合溶液,加热HCl挥发逸出,
2
得到NaCl溶液;
②根据流程图可知:能重复利用的单质是Cl、H;
2 2
在发生器中NaClO 与HCl发生反应产生ClO 、Cl、NaCl、HO,则根据电子守恒、原子
3 2 2 2
守恒,可知发生反应方程式为:2NaClO+4HCl=2ClO ↑+Cl↑+2NaCl+2HO;
3 2 2 2
【小问2详解】
纤维素为多糖,水解最终产物为葡萄糖(C H O),具有还原性,可将NaClO 还原得到
6 12 6 3
ClO ,Cl元素化合价从+5到+4价,降低1价,葡萄糖(C H O)中C均价到+4价,升高4
2 6 12 6
价,则配平后的化学方程式为:C H O+24 NaClO+12H SO =24ClO ↑+6CO ↑+
6 12 6 3 2 4 2 2
18HO+12Na SO ,所以缺项物质是NaSO ,系数是12;
2 2 4 2 4【小问3详解】
每摩尔Cl 得到2 mol电子,而每摩尔ClO 得到5 mol电子,则所需Cl 的物质的量是ClO
2 2 2 2
的2.5倍。