文档内容
考点 1 化学反应速率
1.3年真题考点分布
考点分布
年份 卷区
反应速率的计算 反应速率的影响因素 反应速率的图像 综合应用
辽宁 √ √ √
2023
海南 √ √ √
北京 √ √ √
广东 √ √ √
河北 √ √ √
2022
湖南 √ √
辽宁 √ √
浙江 √ √ √
辽宁 √ √ √ √
广东 √ √
2021
浙江 √ √
河北 √ √ √
2.命题规律及备考策略
【命题规律】近3年新高考卷对于该专题主要考查:
(1)化学反应速率的计算
(2)外界条件对化学反应速率的影响
(3)化学反应速率图像
【备考策略】(1)掌握温度、浓度、压强和催化剂对化学反应速率的影响;
(2)反应历程(或机理)图像分析
(3)利用化学反应速率图像,考查分析问题解决问题的能力。
【命题预测】预测2024年主要考查化学反应速率计算,外界条件对速率的影响。命题会以实际生产生活为载
体,将化学反应速率与化工生产、生活实际相结合,应予以重视。
考法 1 化学反应速率
1.化学反应速率
资料整理【淘宝店铺:向阳百分百】2.化学反应速率计算的万能方法——三段式法
对于反应mA(g)+nB(g) pC(g)+qD(g),起始时A的浓度为a mol·L-1,B的浓度为b mol·L-1,反应进行
至ts时,A消耗了x mol·L-1,则化学反应速率可计算如下:
1
mA(g)+nB(g) pC(g)+qD(g)
起始/(mol·L-1) a b 0 0
转化/(mol·L-1) x
t/(mol·L-1) a-x b-
1
则:v(A)= mol·L-1·s-1,v(B)= mol·L-1·s-1,
v(C)= mol·L-1·s-1,v(D)= mol·L-1·s-1。
3.化学反应速率与化学计量数的关系
对于已知反应mA(g)+nB(g)===pC(g)+qD(g),其化学反应速率可用不同的反应物或生成物来表示,当单位相同
时,化学反应速率的数值之比等于化学计量数之比,即v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q。
如一定温度下,在密闭容器中发生反应:3A(g)+B(g) 2C(g)。已知v(A)=0.6 mol·L-1·s-1,则v(B)=0.2
mol·L-1·s-1,v(C)=0.4 mol·L-1·s-1。
4.化学反应速率大小的比较方法
由于同一化学反应的反应速率用不同物质表示时数值可能不同,所以比较反应的快慢不能只看数值的大小,而
要进行一定的转化。
(1)看单位是否统一,若不统一,换算成相同的单位。
(2)单位统一后,换算成同一物质表示的速率,再比较数值的大小。
(3)也可以直接比较化学反应速率与化学计量数的比值,即对于一般反应aA+bB===cC+dD,比较与,若>,
则A表示的反应速率比B的大。
【典例1】(湖南省岳阳市华容县普通高中2023届高三新高考适应性考试)取50 mL过氧化氢水溶液,在少量
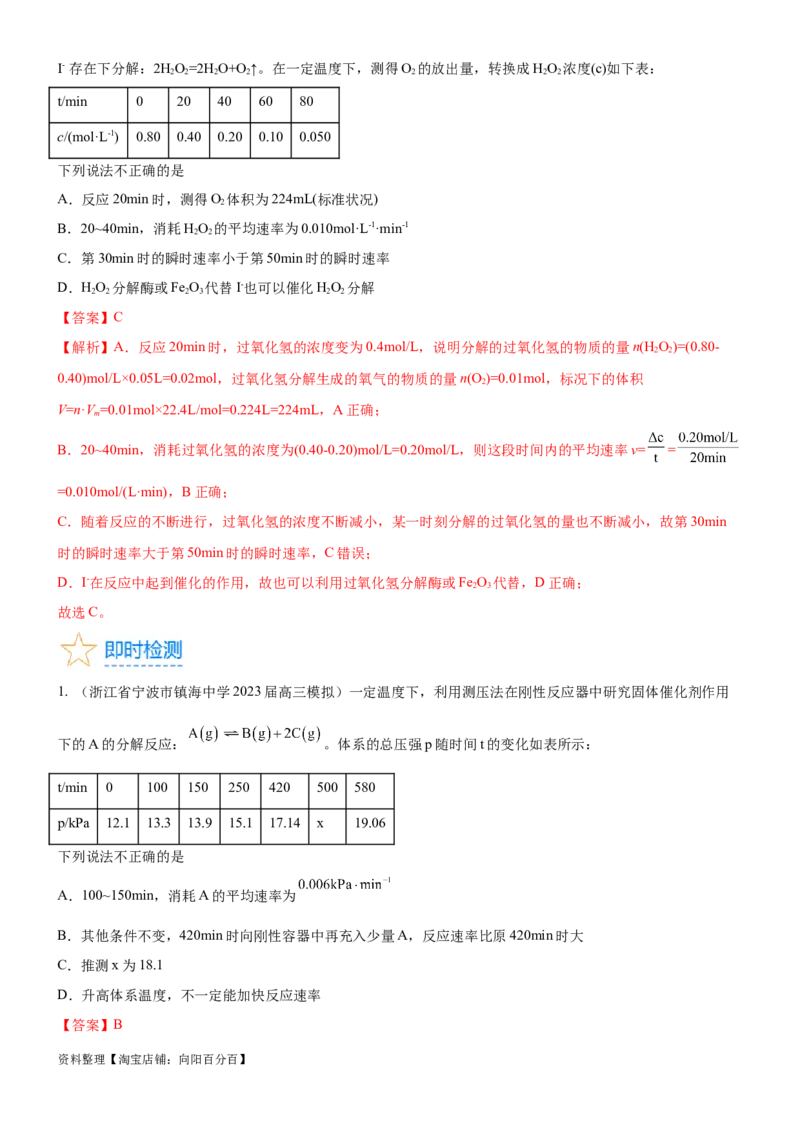
资料整理【淘宝店铺:向阳百分百】I- 存在下分解:2HO=2H O+O↑。在一定温度下,测得O 的放出量,转换成HO 浓度(c)如下表:
2 2 2 2 2 2 2
t/min 0 20 40 60 80
c/(mol·L-1) 0.80 0.40 0.20 0.10 0.050
下列说法不正确的是
A.反应20min时,测得O 体积为224mL(标准状况)
2
B.20~40min,消耗HO 的平均速率为0.010mol·L-1·min-1
2 2
C.第30min时的瞬时速率小于第50min时的瞬时速率
D.HO 分解酶或Fe O 代替I-也可以催化HO 分解
2 2 2 3 2 2
【答案】C
【解析】A.反应20min时,过氧化氢的浓度变为0.4mol/L,说明分解的过氧化氢的物质的量n(H O)=(0.80-
2 2
0.40)mol/L×0.05L=0.02mol,过氧化氢分解生成的氧气的物质的量n(O )=0.01mol,标况下的体积
2
V=n·V =0.01mol×22.4L/mol=0.224L=224mL,A正确;
m
B.20~40min,消耗过氧化氢的浓度为(0.40-0.20)mol/L=0.20mol/L,则这段时间内的平均速率v= =
=0.010mol/(L·min),B正确;
C.随着反应的不断进行,过氧化氢的浓度不断减小,某一时刻分解的过氧化氢的量也不断减小,故第30min
时的瞬时速率大于第50min时的瞬时速率,C错误;
D.I-在反应中起到催化的作用,故也可以利用过氧化氢分解酶或Fe O 代替,D正确;
2 3
故选C。
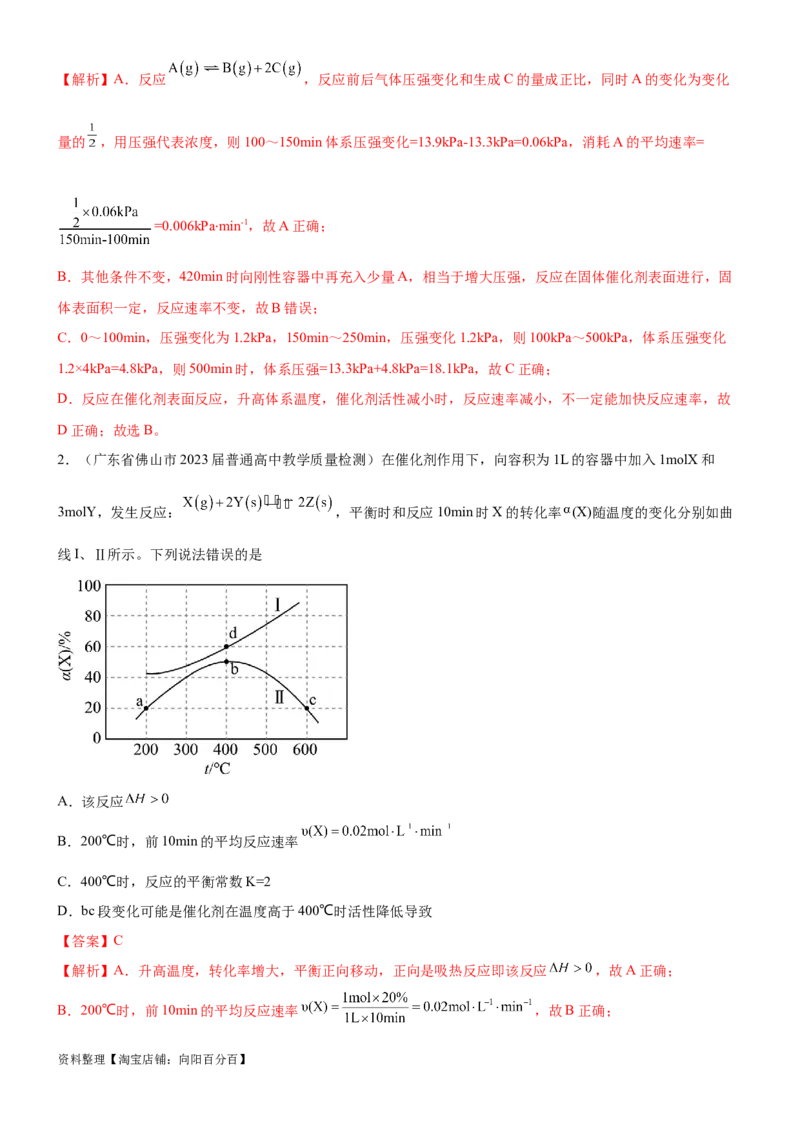
1. (浙江省宁波市镇海中学2023届高三模拟)一定温度下,利用测压法在刚性反应器中研究固体催化剂作用
下的A的分解反应: 。体系的总压强p随时间t的变化如表所示:
t/min 0 100 150 250 420 500 580
p/kPa 12.1 13.3 13.9 15.1 17.14 x 19.06
下列说法不正确的是
A.100~150min,消耗A的平均速率为
B.其他条件不变,420min时向刚性容器中再充入少量A,反应速率比原420min时大
C.推测x为18.1
D.升高体系温度,不一定能加快反应速率
【答案】B
资料整理【淘宝店铺:向阳百分百】【解析】A.反应 ,反应前后气体压强变化和生成C的量成正比,同时A的变化为变化
量的 ,用压强代表浓度,则100~150min体系压强变化=13.9kPa-13.3kPa=0.06kPa,消耗A的平均速率=
=0.006kPamin-1,故A正确;
⋅
B.其他条件不变,420min时向刚性容器中再充入少量A,相当于增大压强,反应在固体催化剂表面进行,固
体表面积一定,反应速率不变,故B错误;
C.0~100min,压强变化为1.2kPa,150min~250min,压强变化1.2kPa,则100kPa~500kPa,体系压强变化
1.2×4kPa=4.8kPa,则500min时,体系压强=13.3kPa+4.8kPa=18.1kPa,故C正确;
D.反应在催化剂表面反应,升高体系温度,催化剂活性减小时,反应速率减小,不一定能加快反应速率,故
D正确;故选B。
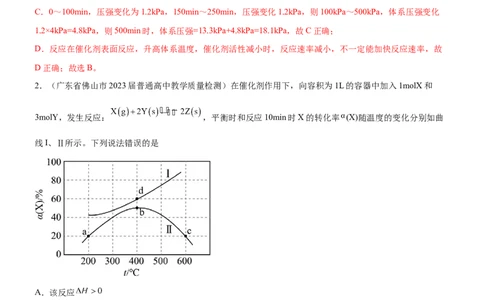
2.(广东省佛山市2023届普通高中教学质量检测)在催化剂作用下,向容积为1L的容器中加入1molX和
3molY,发生反应: ,平衡时和反应10min时X的转化率 (X)随温度的变化分别如曲
线I、Ⅱ所示。下列说法错误的是
A.该反应
B.200℃时,前10min的平均反应速率
C.400℃时,反应的平衡常数K=2
D.bc段变化可能是催化剂在温度高于400℃时活性降低导致
【答案】C
【解析】A.升高温度,转化率增大,平衡正向移动,正向是吸热反应即该反应 ,故A正确;
B.200℃时,前10min的平均反应速率 ,故B正确;
资料整理【淘宝店铺:向阳百分百】C.400℃时,X转化率为60%,反应的平衡常数 ,故C错误;
D.ab阶段随温度升高,转化率增大,bc阶段随温度升高,转化率减小,该变化可能是催化剂在温度高于
400℃时活性降低导致,故D正确。
综上所述,答案为:C。
考法 2 基元反应和有效碰撞理论
1.基元反应:大多数化学反应往往经过多个反应步骤才能实现,每一步反应都被称为基元反应;先后进行的基
元反应反映了反应历程,反应历程又称为反应机理。
2.有效碰撞
①基元反应发生的先决条件是反应物的分子必须发生碰撞。
②反应物分子的每一次碰撞并不是都能发生反应,能够发生化学反应的碰撞叫作有效碰撞。发生有效碰撞的两
个条件是反应物分子能量足够和取向合适。
3.活化分子 活化能
①活化分子:能够发生有效碰撞的分子。
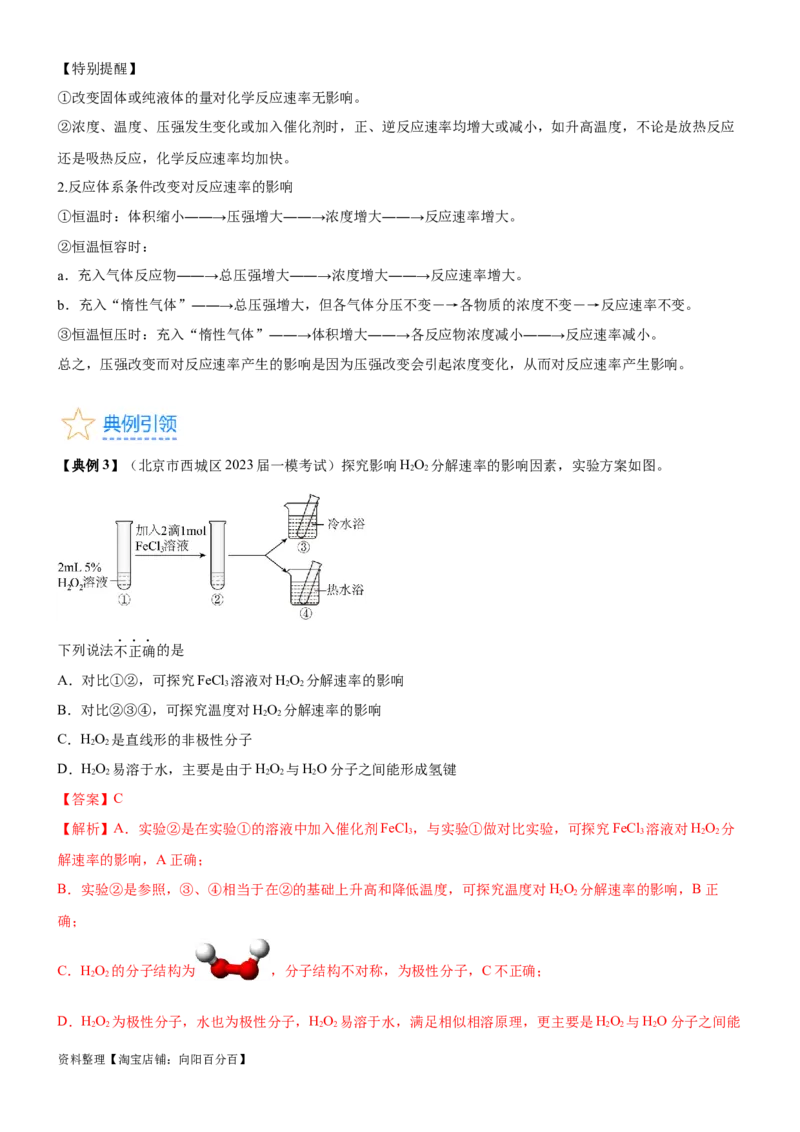
②活化能:如图
图中:E 为正反应的活化能,使用催化剂时的活化能为,反应热为E-E。
1 1 2
4.活化分子、有效碰撞与反应速率的关系
【典例2】(广东省6校2023-2024学年高三上学期第一次联考)叔丁基溴在乙醇中反应的能量变化如图所示。
反应1:
资料整理【淘宝店铺:向阳百分百】反应2:
下列说法错误的是
A.3种过渡态相比,①最不稳定 B.反应1和反应2的 都小于0
C.第一个基元反应是决速步骤 D. 是反应1和反应2共同的催化剂
【答案】D
【解析】A.过渡态能量:①>②>③,过渡态①能量最大,最不稳定,故A正确;
B.根据能量变化可知,反应1和反应2都是放热反应, ,故B正确;
C. 转化为 是第一个基元反应,活化能最大,故C正确;
D. 是反应2的反应物,不是催化剂,故D错误;
故选D。
1.(辽宁省沈阳市第一二〇中学2024届高三质量监测)2SO (g)+O(g) 2SO (g) ∆H=-198kJ•mol-1。在
2 2 3
VO 存在时该反应机理为:①VO+SO→2VO +SO(快);②4VO +O →2VO(慢)。下列说法不正确的是
2 5 2 5 2 2 3 2 2 2 5
A.该反应速率主要由第②步基元反应决定
B.由反应机理可知,VO 和VO 都是该反应的催化剂
2 5 2
C.VO 的存在提高了该反应活化分子百分数,使单位时间内有效碰撞次数增加,反应速率加快
2 5
D.逆反应的活化能比正反应的活化能大198kJ•mol-1
【答案】B
【解析】A.反应①为快反应,反应②为慢反应,总反应速率由最慢的一步决定,该反应速率主要取决于慢反
应,即第②步反应,故A正确;
B.根据反应机理可知,VO 是反应的催化剂,而VO 是中间产物,故B错误;
2 5 2
C.根据反应机理可知,VO 是反应的催化剂,所以提高了该反应活化分子百分数,使有效碰撞次数增加,反
2 5
资料整理【淘宝店铺:向阳百分百】应速率加快,故C正确;
D.∆H=正反应的活化能﹣逆反应的活化能=-198kJ/mol,所以逆反应的活化能大于198kJ/mol,故D正确;
故选B。
2.(四川省成都市第七中学2024届高三月考) 。在 存在
时该反应机理为:① (快);② (慢)。下列说法不正确的是
A.该反应速率主要由第②步基元反应决定
B.基元反应发生的先决条件是反应物分子必须有足够的能量
C. 的存在提高了该反应活化分子百分数,使有效碰撞次数增加,反应速率加快
D.逆反应的活化能比正反应的活化能大
【答案】B
【解析】A.总反应速率是由慢反应决定,根据题中信息可知,该反应速率是由第②基元反应决定,故A正
确;
B.基元反应发生的先决条件是由足够的能量和碰撞方向,故B错误;
C.VO 为该反应的催化剂,降低该反应的活化能,提高反应的活化分子百分数,使有效碰撞次数增加,反应
2 5
速率加快,故C正确;
D.198kJ/mol为该反应的焓变,该反应为放热反应,逆反应的活化能比正反应的活化能大 ,故D正
确;答案为B。
考法 3 影响化学反应速率的因素
1.影响化学反应速率的因素
(1)内因
反应物本身的性质是主要因素。如相同条件下Mg、Al与稀盐酸反应的速率大小关系为Mg>Al。
(2)外因(只改变一个条件,其他条件不变)
资料整理【淘宝店铺:向阳百分百】【特别提醒】
①改变固体或纯液体的量对化学反应速率无影响。
②浓度、温度、压强发生变化或加入催化剂时,正、逆反应速率均增大或减小,如升高温度,不论是放热反应
还是吸热反应,化学反应速率均加快。
2.反应体系条件改变对反应速率的影响
①恒温时:体积缩小――→压强增大――→浓度增大――→反应速率增大。
②恒温恒容时:
a.充入气体反应物――→总压强增大――→浓度增大――→反应速率增大。
b.充入“惰性气体”――→总压强增大,但各气体分压不变―→各物质的浓度不变―→反应速率不变。
③恒温恒压时:充入“惰性气体”――→体积增大――→各反应物浓度减小――→反应速率减小。
总之,压强改变而对反应速率产生的影响是因为压强改变会引起浓度变化,从而对反应速率产生影响。
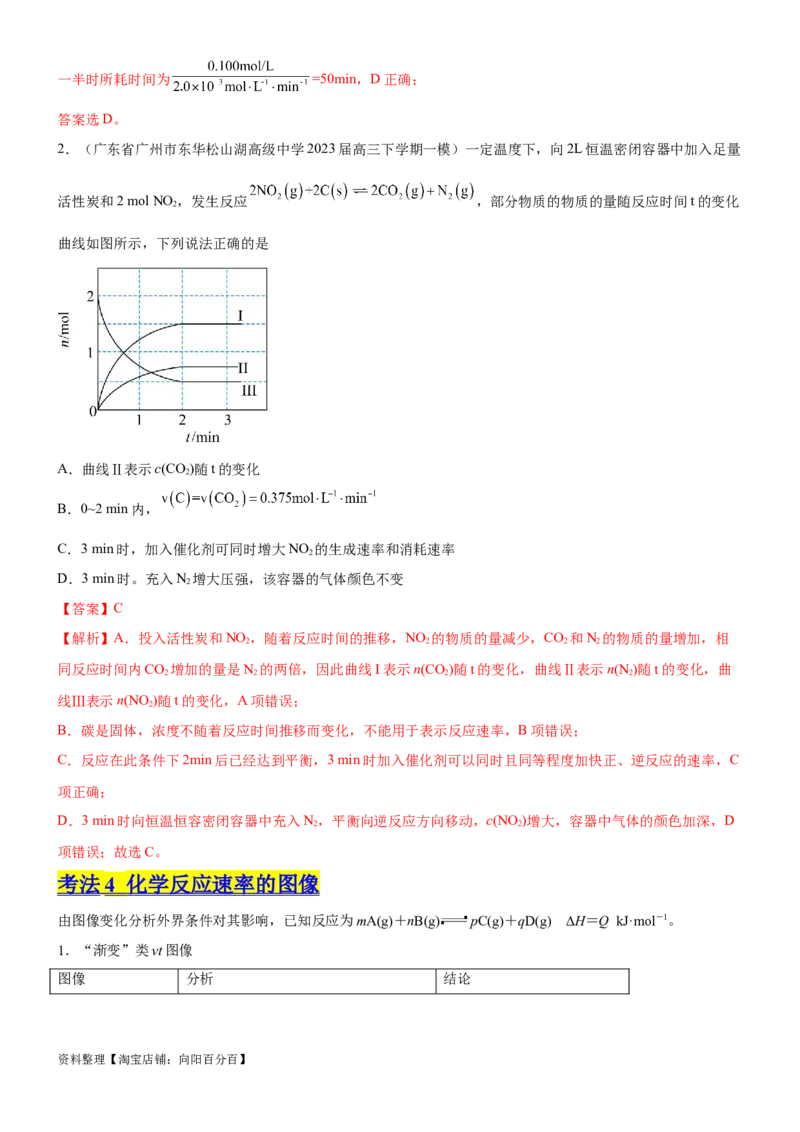
【典例3】(北京市西城区2023届一模考试)探究影响HO 分解速率的影响因素,实验方案如图。
2 2
下列说法不正确的是
A.对比①②,可探究FeCl 溶液对HO 分解速率的影响
3 2 2
B.对比②③④,可探究温度对HO 分解速率的影响
2 2
C.HO 是直线形的非极性分子
2 2
D.HO 易溶于水,主要是由于HO 与HO分子之间能形成氢键
2 2 2 2 2
【答案】C
【解析】A.实验②是在实验①的溶液中加入催化剂FeCl ,与实验①做对比实验,可探究FeCl 溶液对HO 分
3 3 2 2
解速率的影响,A正确;
B.实验②是参照,③、④相当于在②的基础上升高和降低温度,可探究温度对HO 分解速率的影响,B正
2 2
确;
C.HO 的分子结构为 ,分子结构不对称,为极性分子,C不正确;
2 2
D.HO 为极性分子,水也为极性分子,HO 易溶于水,满足相似相溶原理,更主要是HO 与HO分子之间能
2 2 2 2 2 2 2
资料整理【淘宝店铺:向阳百分百】形成氢键,D正确;故选C。
1.(山东省泰安市2023届高三下学期三模)已知 的速率方程为 (k
为速率常数,只与温度、催化剂有关)。实验测得, 在催化剂X表面反应的变化数据如下:
t/min 0 10 20 30 40 50 60 70
0.100 0.080 0.040 0.020 0
下列说法正确的是
A. ,
B. min时,
C.相同条件下,增大 的浓度或催化剂X的表面积,都能加快反应速率
D.保持其他条件不变,若 起始浓度为0.200 mol·L ,当浓度减至一半时共耗时50 min
【答案】D
【分析】根据表中数据分析,该反应的速率始终不变, 的消耗是匀速的,说明反应速率与 无关,
故速率方程中n=0;
【解析】A.由分析可知,n=0,与 浓度无关,为匀速反应,每10min一氧化二氮浓度减小0.02 ,
则 ,A错误;
B.由分析可知,n=0,与 浓度无关,为匀速反应,t=10min时瞬时速率等于平均速率 =
= ≠ ,B错误;
C.速率方程中n=0,反应速率与 的浓度无关,C错误;
D.保持其他条件不变,该反应的反应速率不变,即为 ,若起始浓度 ,减至
资料整理【淘宝店铺:向阳百分百】一半时所耗时间为 =50min,D正确;
答案选D。
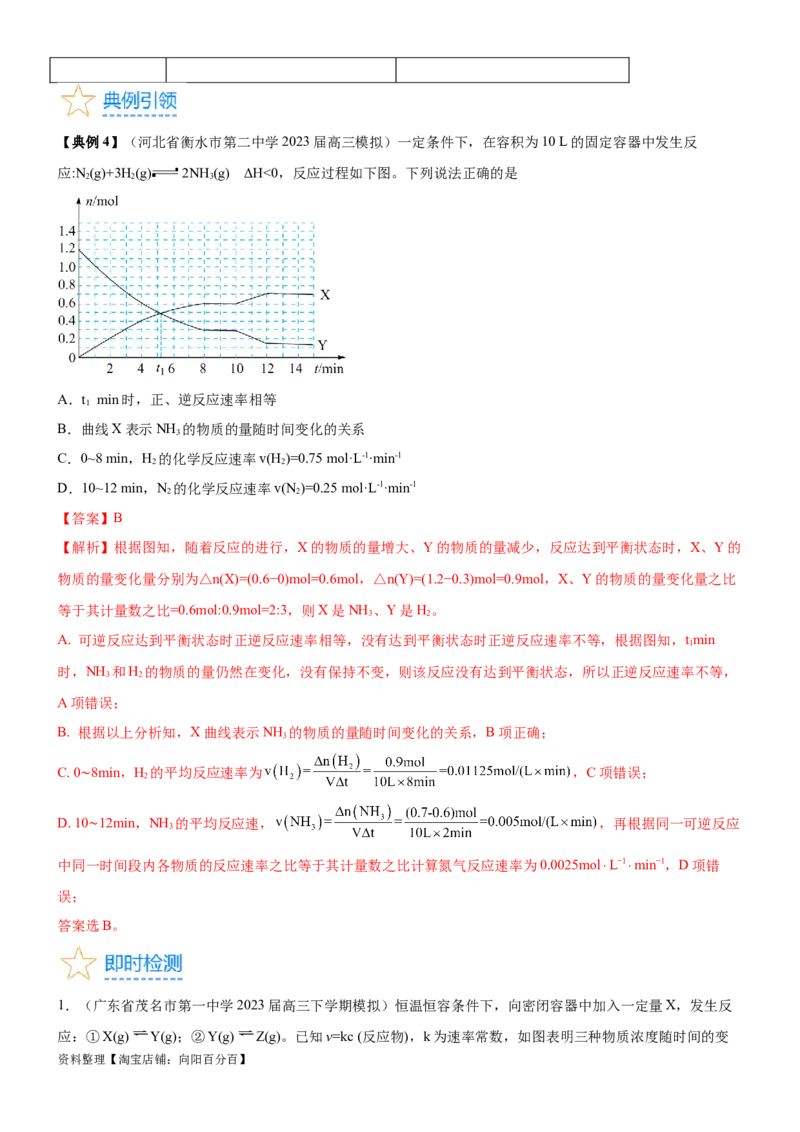
2.(广东省广州市东华松山湖高级中学2023届高三下学期一模)一定温度下,向2L恒温密闭容器中加入足量
活性炭和2 mol NO ,发生反应 ,部分物质的物质的量随反应时间t的变化
2
曲线如图所示,下列说法正确的是
A.曲线Ⅱ表示c(CO)随t的变化
2
B.0~2 min内,
C.3 min时,加入催化剂可同时增大NO 的生成速率和消耗速率
2
D.3 min时。充入N 增大压强,该容器的气体颜色不变
2
【答案】C
【解析】A.投入活性炭和NO ,随着反应时间的推移,NO 的物质的量减少,CO 和N 的物质的量增加,相
2 2 2 2
同反应时间内CO 增加的量是N 的两倍,因此曲线I表示n(CO)随t的变化,曲线Ⅱ表示n(N )随t的变化,曲
2 2 2 2
线Ⅲ表示n(NO )随t的变化,A项错误;
2
B.碳是固体,浓度不随着反应时间推移而变化,不能用于表示反应速率,B项错误;
C.反应在此条件下2min后已经达到平衡,3 min时加入催化剂可以同时且同等程度加快正、逆反应的速率,C
项正确;
D.3 min时向恒温恒容密闭容器中充入N,平衡向逆反应方向移动,c(NO )增大,容器中气体的颜色加深,D
2 2
项错误;故选C。
考法 4 化学反应速率的图像
由图像变化分析外界条件对其影响,已知反应为mA(g)+nB(g ) pC(g)+qD(g) ΔH=Q kJ·mol-1。
1.“渐变”类vt图像
图像 分析 结论
资料整理【淘宝店铺:向阳百分百】t 时v′ 突然增大,v′ 逐渐增大;v′ >v′ t 时其他条件不变,增大反
1 正 逆 正 1
,平衡向正反应方向移动 应物的浓度
逆
t 时v′ 突然减小,v′ 逐渐减小;v′ >v′ t 时其他条件不变,减小反
1 正 逆 逆 1
,平衡向逆反应方向移动 应物的浓度
正
t 时v′ 突然增大,v′ 逐渐增大;v′ >v′ t 时其他条件不变,增大生
1 逆 正 逆 1
,平衡向逆反应方向移动 成物的浓度
正
t 时v′ 突然减小,v′ 逐渐减小;v′ >v′ t 时其他条件不变,减小生
1 逆 正 正 1
,平衡向正反应方向移动 成物的浓度
逆
2.“断点”类vt图像
图像 分析 结论
t 时其他条件不变,增大反应体系的
1
压强且m+n>p+q(正反应为体积减
t 1 时v′ 正 、v′ 逆 均突然增大,且v′ 正 小的反应)
>v′ ;平衡向正反应方向进行
逆
t 时其他条件不变,升高温度且Q>
1
0(吸热反应)
t 时其他条件不变,增大反应体系的
1
压强且m+n<p+q(正反应为体积增
t 1 时v′ 正 、v′ 逆 均突然增大,且v′ 逆 大的反应)
>v′ ;平衡向逆反应方向进行
正
t 时其他条件不变,升高温度且Q<
1
0(放热反应)
t 时其他条件不变,减小反应体系的
1
压强且m+n<p+q(正反应为体积增
t 1 时v′ 正 、v′ 逆 均突然减小,且v′ 正 大的反应)
>v′ ;平衡向正反应方向进行
逆
t 时其他条件不变,降低温度且Q<
1
0(放热反应)
t 时其他条件不变,减小反应体系的
1
压强且m+n>p+q(正反应为体积减
t 1 时v′ 逆 、v′ 正 均突然减小,且v′ 逆 小的反应)
>v′ ;平衡向逆反应方向进行
正
t 时其他条件不变,降低温度且Q>
1
0(吸热反应)
3.“平台”类vt图像
图像 分析 结论
t 时其他条件不变使用催化剂
1
t 1 时v′ 正 、v′ 逆 均突然增大且v′ 正 =v′ t 1 时其他条件不变增大反应体系的
逆 ,平衡不移动 压强且m+n=p+q(反应前后气体
体积无变化)
t 时其他条件不变,减小反应体系
t 时v′ 、v′ 均突然减小且v′ =v′ 1
1 正 逆 正 的压强且m+n=p+q(反应前后气
,平衡不移动
逆 体体积无变化)
资料整理【淘宝店铺:向阳百分百】【典例4】(河北省衡水市第二中学2023届高三模拟)一定条件下,在容积为10 L的固定容器中发生反
应:N (g)+3H(g ) 2NH (g) ΔH<0,反应过程如下图。下列说法正确的是
2 2 3
A.t min时,正、逆反应速率相等
1
B.曲线X表示NH 的物质的量随时间变化的关系
3
C.0~8 min,H 的化学反应速率v(H )=0.75 mol·L-1·min-1
2 2
D.10~12 min,N 的化学反应速率v(N )=0.25 mol·L-1·min-1
2 2
【答案】B
【解析】根据图知,随着反应的进行,X的物质的量增大、Y的物质的量减少,反应达到平衡状态时,X、Y的
物质的量变化量分别为△n(X)=(0.6−0)mol=0.6mol,△n(Y)=(1.2−0.3)mol=0.9mol,X、Y的物质的量变化量之比
等于其计量数之比=0.6mol:0.9mol=2:3,则X是NH 、Y是H。
3 2
A. 可逆反应达到平衡状态时正逆反应速率相等,没有达到平衡状态时正逆反应速率不等,根据图知,tmin
1
时,NH 和H 的物质的量仍然在变化,没有保持不变,则该反应没有达到平衡状态,所以正逆反应速率不等,
3 2
A项错误;
B. 根据以上分析知,X曲线表示NH 的物质的量随时间变化的关系,B项正确;
3
C. 0 8min,H 的平均反应速率为 ,C项错误;
2
∼
D. 10 12min,NH 的平均反应速, ,再根据同一可逆反应
3
∼
中同一时间段内各物质的反应速率之比等于其计量数之比计算氮气反应速率为0.0025mol⋅L−1⋅min−1,D项错
误;
答案选B。
1.(广东省茂名市第一中学2023届高三下学期模拟)恒温恒容条件下,向密闭容器中加入一定量X,发生反
应:①X(g) Y(g);②Y(g) Z(g)。已知v=kc (反应物),k为速率常数,如图表明三种物质浓度随时间的变
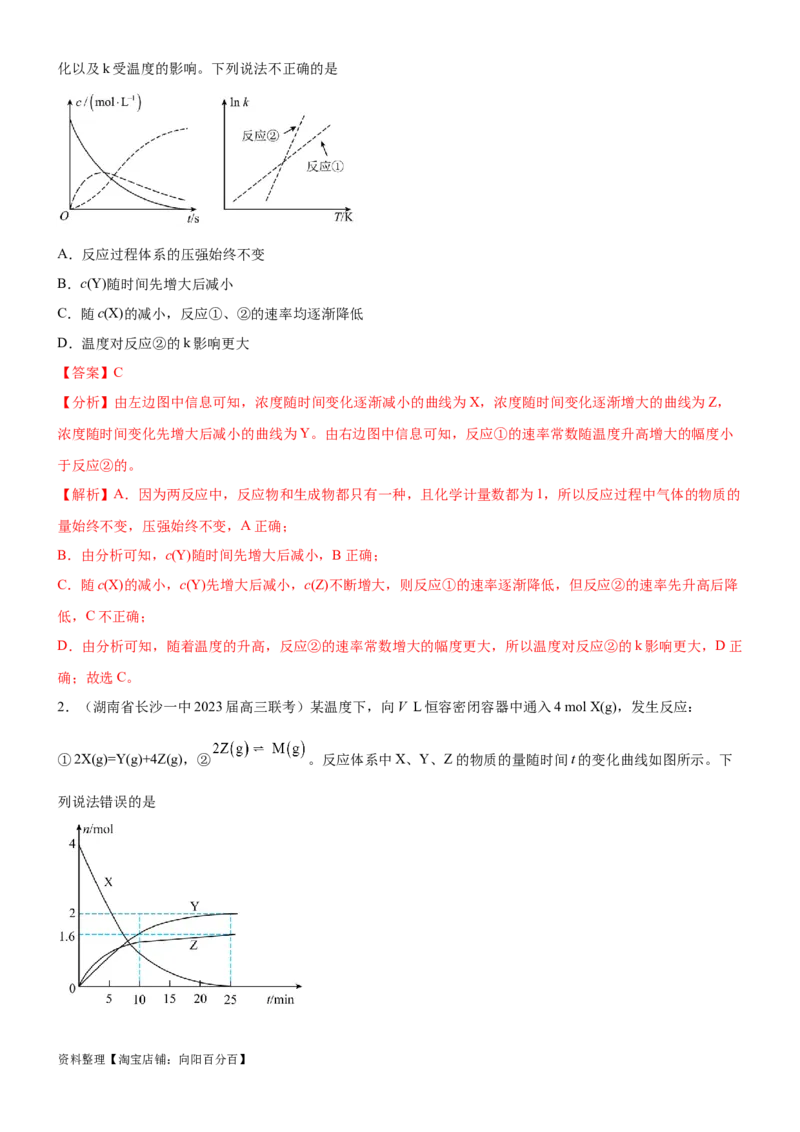
资料整理【淘宝店铺:向阳百分百】化以及k受温度的影响。下列说法不正确的是
A.反应过程体系的压强始终不变
B.c(Y)随时间先增大后减小
C.随c(X)的减小,反应①、②的速率均逐渐降低
D.温度对反应②的k影响更大
【答案】C
【分析】由左边图中信息可知,浓度随时间变化逐渐减小的曲线为X,浓度随时间变化逐渐增大的曲线为Z,
浓度随时间变化先增大后减小的曲线为Y。由右边图中信息可知,反应①的速率常数随温度升高增大的幅度小
于反应②的。
【解析】A.因为两反应中,反应物和生成物都只有一种,且化学计量数都为1,所以反应过程中气体的物质的
量始终不变,压强始终不变,A正确;
B.由分析可知,c(Y)随时间先增大后减小,B正确;
C.随c(X)的减小,c(Y)先增大后减小,c(Z)不断增大,则反应①的速率逐渐降低,但反应②的速率先升高后降
低,C不正确;
D.由分析可知,随着温度的升高,反应②的速率常数增大的幅度更大,所以温度对反应②的k影响更大,D正
确;故选C。
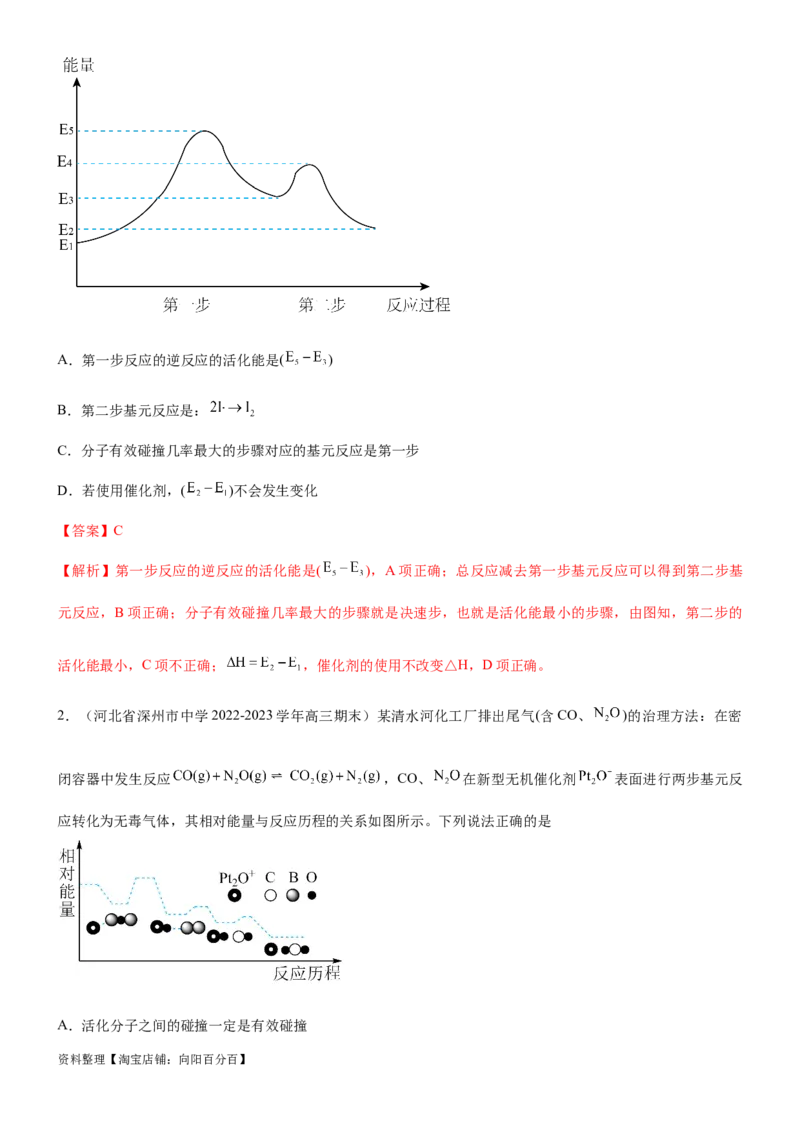
2.(湖南省长沙一中2023届高三联考)某温度下,向V L恒容密闭容器中通入4 mol X(g),发生反应:
①2X(g)=Y(g)+4Z(g),② 。反应体系中X、Y、Z的物质的量随时间t的变化曲线如图所示。下
列说法错误的是
资料整理【淘宝店铺:向阳百分百】A.25 min时,气体X反应完全
B.0~10 min内,气体X的平均反应速率为
C.25 min时,向该体系中仅通入1 mol 后,反应②的平衡不发生移动(保持其他条件不变)
D.该温度下,反应②的平衡常数 Lmol
【答案】D ⋅
【解析】A.由题干图像可知,25 min时,生成了2molY,根据反应方程①可知,消耗4molX,则气体X反应
完全,A正确;
B.由题干图像可知,0~10 min内生成了1.6molY,则消耗3.2molX,故气体X的平均反应速率为
= ,B正确;
C.由A项分析可知,反应①不可逆反应,故25 min时反应①进行完全,恒温恒容下向该体系中仅通入1 mol
Y(g)后,反应②的平衡不发生移动(保持其他条件不变),C正确;
D.由题干图像信息可知,25min时生成了2molY,同时反应①生成了8molZ,而Z的物质的量实际上最终为
1.6mol,说明反应②消耗了6.4mol,生成了3.2molM,该温度下,反应②的平衡常数
Lmol ,D错误;故答案为D。
⋅
【基础过关】
1.(湖北省鄂东南省级示范高中教育教学改革联盟学校2022-2023学年联考)化学反应:
H实际上是经过两步基元反应完成的:第一步: ;第二步:……。该
△
反应过程的能量变化如图所示,下列说法不正确的是
资料整理【淘宝店铺:向阳百分百】A.第一步反应的逆反应的活化能是( )
B.第二步基元反应是:
C.分子有效碰撞几率最大的步骤对应的基元反应是第一步
D.若使用催化剂,( )不会发生变化
【答案】C
【解析】第一步反应的逆反应的活化能是( ),A项正确;总反应减去第一步基元反应可以得到第二步基
元反应,B项正确;分子有效碰撞几率最大的步骤就是决速步,也就是活化能最小的步骤,由图知,第二步的
活化能最小,C项不正确; ,催化剂的使用不改变△H,D项正确。
2.(河北省深州市中学2022-2023学年高三期末)某清水河化工厂排出尾气(含CO、 )的治理方法:在密
闭容器中发生反应 ,CO、 在新型无机催化剂 表面进行两步基元反
应转化为无毒气体,其相对能量与反应历程的关系如图所示。下列说法正确的是
A.活化分子之间的碰撞一定是有效碰撞
资料整理【淘宝店铺:向阳百分百】B.两步反应均为放热反应,第一步反应活化能最大
C.新型无机催化剂 可有效提高CO、 的平衡转化率
D.基元反应的平衡常数越小,反应速率越慢
【答案】B
【解析】A.活化分子之间的碰撞只有一部分是有效碰撞,A项错误;
B.由图可知,两步反应都是放热反应,第一步反应的活化能比第二步反应的活化能大,总反应的化学反应速
率由活化能大的第一步反应决定,B项正确;
C.催化剂Pt O+不能使化学平衡发生移动,不能提高 、NO的平衡转化率,C项错误;
2 2
D.平衡常数的大小与反应速率快慢无关,与温度有关,D项错误;
答案选B。
3.(广东省河源市第一中学2022-2023学年高三模拟) ,在
VO 存在时,该反应机理为:① (快);② (慢)。下列说法正确的
2 5
是
A.该反应速率主要由第①步基元反应决定
B.增大SO 的浓度可显著提高反应速率
2
C. VO 的存在提高该反应活化分子百分数,使有效碰撞次数增加,反应速率加快
2 5
D.该反应的逆反应的活化能为198kJ/mol
【答案】C
【解析】A.一个反应的速率主要由慢反应决定,则该反应速率主要由第②步基元反应决定,A不正确;
B.增大SO 的浓度可提高反应速率,但比起催化剂,速率改变的程度要小得多,所以不能说是显著提高反应速
2
率,B不正确;
C.VO 是反应的催化剂,能降低反应的活化能,使更多的分子成为活化分子,从而提高该反应活化分子百分
2 5
数,使有效碰撞次数增加,反应速率加快,C正确;
D.该反应为放热反应,其逆反应的活化能为“正反应的活化能+198kJ/mol”,D不正确;
故选C。
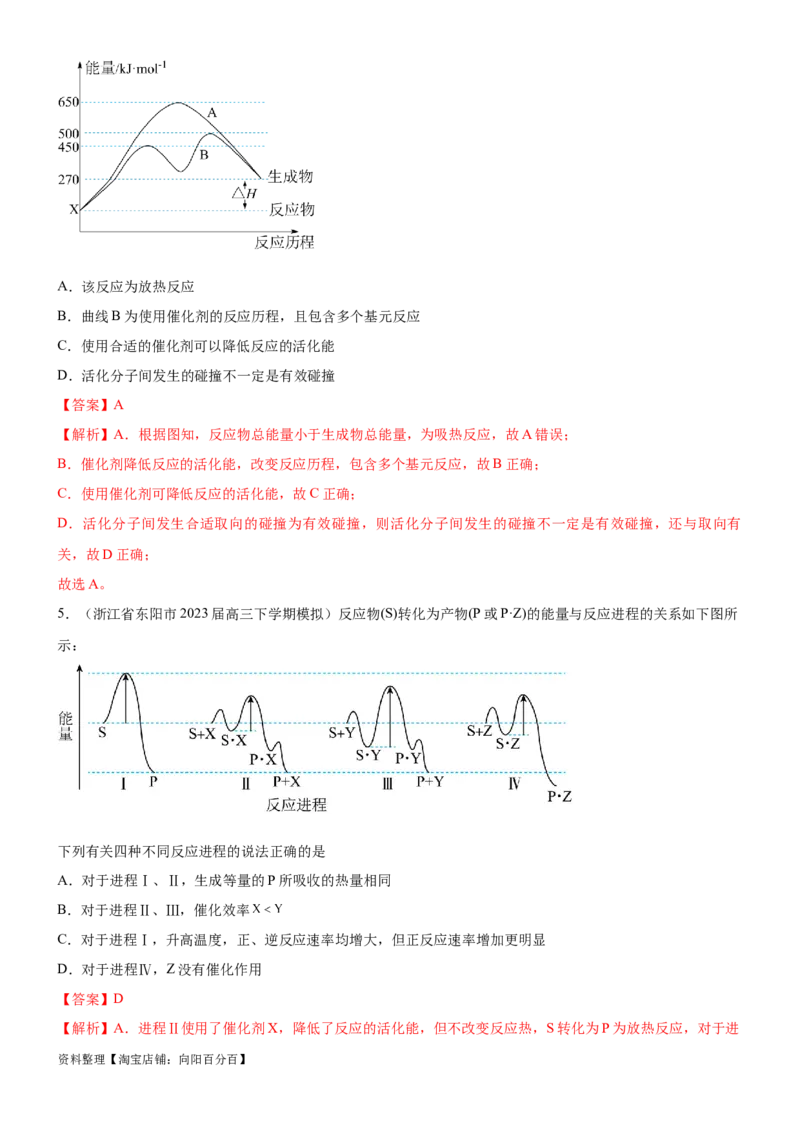
4.(天津市红桥区2022-2023学年度高三模拟)某反应过程的能量变化如图所示,下列说法不正确的是
资料整理【淘宝店铺:向阳百分百】A.该反应为放热反应
B.曲线B为使用催化剂的反应历程,且包含多个基元反应
C.使用合适的催化剂可以降低反应的活化能
D.活化分子间发生的碰撞不一定是有效碰撞
【答案】A
【解析】A.根据图知,反应物总能量小于生成物总能量,为吸热反应,故A错误;
B.催化剂降低反应的活化能,改变反应历程,包含多个基元反应,故B正确;
C.使用催化剂可降低反应的活化能,故C正确;
D.活化分子间发生合适取向的碰撞为有效碰撞,则活化分子间发生的碰撞不一定是有效碰撞,还与取向有
关,故D正确;
故选A。
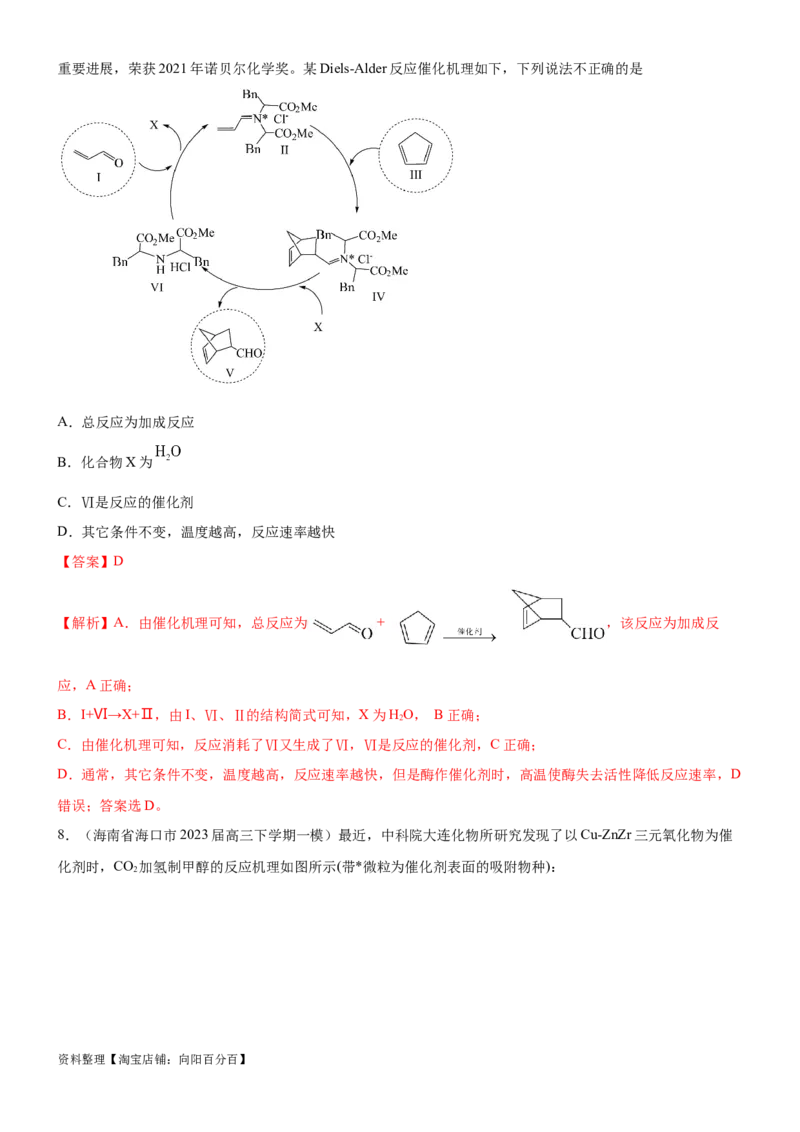
5.(浙江省东阳市2023届高三下学期模拟)反应物(S)转化为产物(P或P·Z)的能量与反应进程的关系如下图所
示:
下列有关四种不同反应进程的说法正确的是
A.对于进程Ⅰ、Ⅱ,生成等量的P所吸收的热量相同
B.对于进程Ⅱ、Ⅲ,催化效率
C.对于进程Ⅰ,升高温度,正、逆反应速率均增大,但正反应速率增加更明显
D.对于进程Ⅳ,Z没有催化作用
【答案】D
【解析】A.进程Ⅱ使用了催化剂X,降低了反应的活化能,但不改变反应热,S转化为P为放热反应,对于进
资料整理【淘宝店铺:向阳百分百】程Ⅰ、Ⅱ,生成等量的P所放出的热量相同,故A错误;
B.由图可知,反应Ⅲ中由S•Y转化为P•Y的活化能高于反应Ⅱ中由S•X转化为P•X的活化能,则反应速率:
反应Ⅱ>反应Ⅲ,催化效率X>Y,故B错误;
C.由图可知,反应I中S的总能量大于产物P的总能量,则进程I是放热反应,升高温度,正、逆反应速率均
增大,但平衡逆移,说明逆反应速率增大程度大于正反应速率的增大幅度,即逆反应速率增加更明显,故C错
误;
D.反应前反应物为S+Z,反应后生成物为P•Z,而不是P+Z,则Z不是该反应的催化剂,没起到催化作用,故
D正确;
故选D。
6.(河北省邯郸市2023届高考第三次模拟)在某催化剂作用下,乙炔选择性加成反应C H(g)+H(g) C H(g)
2 2 2 2 4
ΔH<0。速率方程为v =k c(C H)c(H),v =k c(C H)(k 、k 为速率常数,只与温度、催化剂有关⇌)。一定温
正 正 2 2 2 逆 逆 2 4 正 逆
度下,在2L恒容密闭容器中充入1molC H(g)和1molH (g),只发生上述反应。测得C H 的物质的量如下表所
2 2 2 2 4
示:
t/min 0 5 10 15 20
n/mol 0 0.3 0.5 0.6 0.6
下列说法错误的是
A.0~10min内,v(H )=0.025mol・L-1・min-1
2
B.升高温度,k 增大的倍数小于k 增大的倍数
正 逆
C.净反应速率(v -v )由大到小最终等于0
正 逆
D.在上述条件下,15min时2k =15k
逆 正
【答案】D
【解析】A.由表可知,0~10 min内 ,A正确;
B.根据平衡状态的特点,平衡时正、逆反应速率相等,则K= 。上述反应的正反应是放热反应,升高温
度,平衡常数减小,而升高温度,速率常数增大,由此推知,k 增大的倍数小于k 增大的倍数,B正确;
正 逆
C.根据表格数据可知,开始正反应速率最大,逆反应速率为0,随着反应进行,净反应速率由大到小,最终等
于0(平衡),C正确;
D.15 min时达到平衡,c(C H)=0.2 mol/L ,c(H)=0.2 mol/L ,c(C H)=0.3 mol/ L,故K= =7.5,15k =2k
2 2 2 2 4 逆
,D错误;答案选D。
正
7.(北京市朝阳区2023届高三下学期三模)利用有机分子模拟生物体内“醛缩酶”催化Diels-Alder反应取得
资料整理【淘宝店铺:向阳百分百】重要进展,荣获2021年诺贝尔化学奖。某Diels-Alder反应催化机理如下,下列说法不正确的是
A.总反应为加成反应
B.化合物X为
C.Ⅵ是反应的催化剂
D.其它条件不变,温度越高,反应速率越快
【答案】D
【解析】A.由催化机理可知,总反应为 + ,该反应为加成反
应,A正确;
B.I+Ⅵ→X+Ⅱ,由I、Ⅵ、Ⅱ的结构简式可知,X为HO, B正确;
2
C.由催化机理可知,反应消耗了Ⅵ又生成了Ⅵ,Ⅵ是反应的催化剂,C正确;
D.通常,其它条件不变,温度越高,反应速率越快,但是酶作催化剂时,高温使酶失去活性降低反应速率,D
错误;答案选D。
8.(海南省海口市2023届高三下学期一模)最近,中科院大连化物所研究发现了以Cu-ZnZr三元氧化物为催
化剂时,CO 加氢制甲醇的反应机理如图所示(带*微粒为催化剂表面的吸附物种):
2
资料整理【淘宝店铺:向阳百分百】下列判断错误的是
A.CO 是该反应的氧化剂
2
B.生成的CHOH可用作车用燃料
3
C.催化剂能加快反应速率,但不改变反应的反应热
D.该反应过程中既有非极性键的断裂,又有非极性键的形成
【答案】D
【解析】A.由题干图示信息可知,该反应方程式为:CO+3H CHOH+H O,反应中CO 中C的化合价
2 2 3 2 2
降低,被还原,故是该反应的氧化剂,A正确;
B.甲醇汽车配备了专业的发动机和装置,故生成的CHOH可用作车用燃料,B正确;
3
C.催化剂能降低反应所需要的活化能,从而加快反应速率,但不改变反应的反应热,C正确;
D.由题干图示信息可知,该反应过程中有H-H非极性键和C=O极性键的断裂,但没有非极性键的形成,有C-
H、C-O和H-O极性键的形成,D错误;故答案为D。
【能力提升】
1.(湖南省永州市第一中学2022-2023学年高三模拟)中国科学家研究在Pd/SVG催化剂上H 还原NO生成N
2 2
和NH 的路径,各基元反应及活化能E(kJ·mol-1)如图所示,下列说法错误的是
3 a
A.生成NH 的各基元反应中,N元素均被还原
3
资料整理【淘宝店铺:向阳百分百】B.在Pd/SVG催化剂上,NO更容易被H 还原为NH
2 3
C.决定NO生成NH 速率的基元反应为NH NO→NHNOH
3 2
D.生成NH 的总反应方程式为2NO+5H 2NH +2HO
3 2 3 2
【答案】C
【解析】A.图示可知,生成氨气的过程为:NO→HNO→NH O→NHOH→NH →NH ,每步反应中N元素化合
2 2 2 3
价均是降低,被还原,A正确;
B.NO被还原为N 的最大活化能明显大于还原生成NH ,故在该催化剂作用下,NO更容易被还原为NH ,B
2 3 3
正确;
C.生成NH 的基元反应中,NH O+H→NH OH这一步活化能最大,相同条件下反应速率最慢,是决定NO生
3 2 2
成NH 速率的基元反应,C错误;
3
D.由图可知,总反应为NO与H 反应生成NH 和HO,对应反应的化学方程式:2NO+5H 2NH +
2 3 2 2 3
2HO,D正确;
2
故选C。
2.(浙江省名校协作体2022-2023学年高三二模)在恒温恒容条件下,发生反应 , 随时间
的变化如图中曲线所示,其中 表示 的初始浓度。下列说法不正确的是
A.a点的瞬时速率大于b点的瞬时速率
B. 对应的时间为
C.从a、b两点坐标可求得从 到 时间间隔内该化学反应的平均速率
D.在不同时刻都存在关系:
【答案】B
资料整理【淘宝店铺:向阳百分百】【解析】A.a点的斜率大于b点,则a点的瞬时速率大于b点的瞬时速率,A正确;
B.随着反应进行,物质浓度减小,反应速率减慢,则 对应的时间大于 ,B错误;
C.根据 可知,从a、b两点坐标可求得从 到 时间间隔内该化学反应的平均速率,C正确;
D.反应速率比等于方程式中系数比,故在不同时刻都存在关系: ,D正确;
故选B。
3.(浙江省杭州市鄞州高级中学等22023届高三下学期二模)恒温恒容条件下,向密闭容器中加入一定量X,
发生反应的方程式为①X Y;②Y Z。反应①的速率v=kc(X),反应②的速率v=k(Y),式中k、k 为速
1 1 2 2 1 2
率常数。图甲为该体系中X、Y、Z浓度随时间变化的曲线,图乙为反应①和②的lnk~ 曲线。下列说法不正确
的是
A.随c(X)的减小,反应①②的速率均降低
B.体系中当Y的浓度达到最大值后,v(X) + v(Y) = v(Z)
C.欲提高Y的产率,需提高反应温度且控制反应时间
D.温度低于T 时,总反应速率由反应②决定
1
【答案】A
【解析】A.由图甲中的信息可知,随c(X)的减小,c(Y) 先增大后减小,c(Z)增大,因此,反应①的速率随
c(X)的减小而减小,而反应②的速率先增大后减小,A说法错误;
B.根据体系中发生的反应可知,在Y的浓度达到最大值之前,单位时间内X的减少量等于Y和Z的增加量,
因此,v (X)= v (Y) +v(Z),但是,在Y的浓度达到最大值之后,单位时间内Z的增加量等于Y和X的减少量,
故v (X) + v (Y) = v(Z),B说法正确;
C.升高温度可以可以加快反应①的速率,但是反应①的速率常数随温度升高增大的幅度小于反应②的,且反
应②的的速率随着Y的浓度的增大而增大,因此,欲提高Y的产率,需提高反应温度且控制反应时间,C说法
正确;
D.由图乙信息可知,温度低于T1时,k1>k2,反应②为慢反应,因此,总反应速率由反应②决定,D说法正
资料整理【淘宝店铺:向阳百分百】确;
综上所述,本题选A。
4.(浙江省金丽衢十二校2022-2023学年高三第一次联考)用CH 还原SO 不仅可以消除污染,而且可以得到
4 2
单质S,反应如下: t℃时,在容积为2L的恒容密闭容器
中测的反应在不同时刻各物质的物质的量如下表:
物质的量(mol)时间(min)
0 2 4 6 8 10
物质
SO 4.8 2.64 1.8 1.8 2.1 2.1
2
CO 0 1.08 1.5 1.5 1.75 1.75
2
下列说法不正确的是
A.前2min的平均反应速率v(CH)=0.27mol·L-1·min-1
4
B.6min时SO 的转化率等于10min时SO 的转化率
2 2
C.其它条件不变,在第10min后降低温度,可使容器中的CO 的浓度升高到1.4mol·L-1
2
D.向容器内通入适量的HS,会使平衡逆向移动
2
【答案】C
【解析】A.根据 可知,前2min甲烷物质的量变化1.08mol,则
,故A正确;
B.根据表中数据可知6min时SO 的转化量为4.8mol-1.8mol=3mol,SO 转化率为 =62.5%;6min后
2 2
向反应体系中加入二氧化硫,导致平衡发生移动,10min时处于新的平衡,根据硫原子守恒,加入的SO 的物
2
质的量为0.3mol+(1.75mol-1.5mol) 2=0.8mol,则SO 的转化率为 =62.5%;所以转化率相等,故B
2
正确;
C.10min时,二氧化硫浓度1.05mol/L,二氧化碳浓度0.875mol/L,若不改变容器体积,结合方程式,当二氧
化硫全部转化为二氧化碳的浓度1.2mol/L,但该反应为可逆反应,低温平衡正向移动,二氧化碳浓度不能达到
1.4mol/L,故C错误;
D.HS会与二氧化硫发生氧化还原反应,导致平衡逆向移动,故D正确;
2
答案选C。
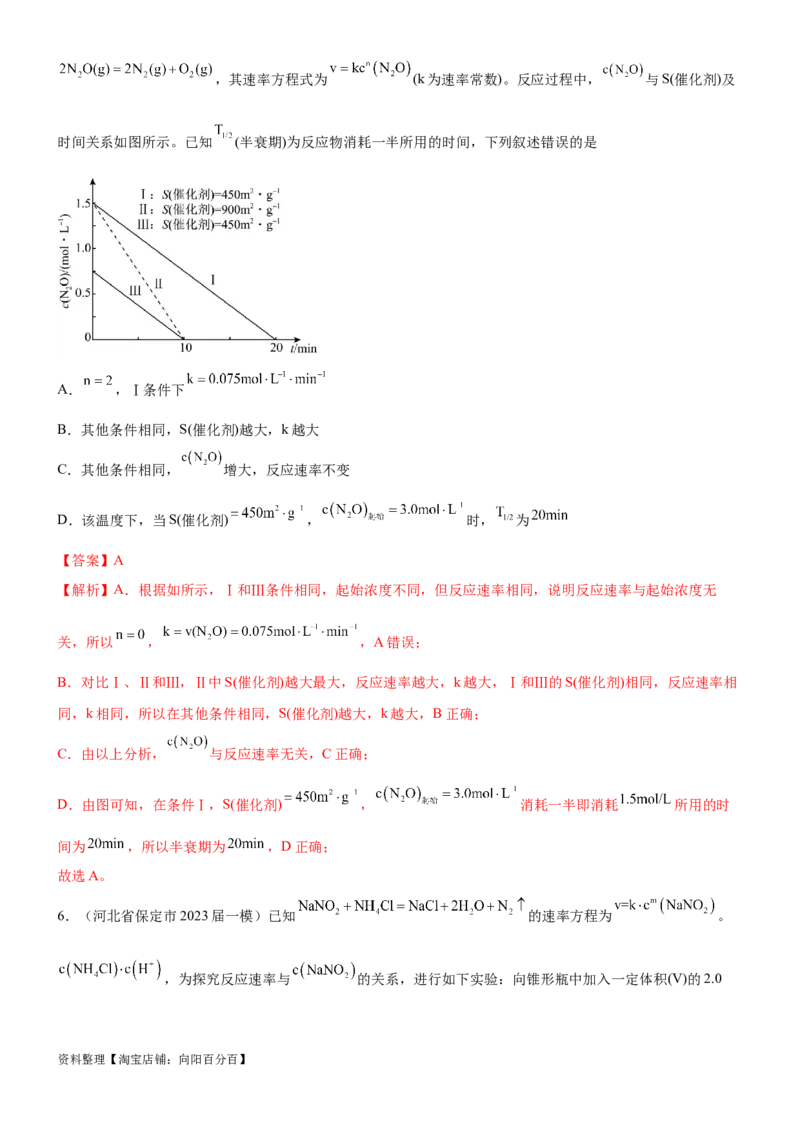
5.(山东省淄博市部分学校2023届高三下学期二模)某温度下,在金表面发生反应:
资料整理【淘宝店铺:向阳百分百】,其速率方程式为 (k为速率常数)。反应过程中, 与S(催化剂)及
时间关系如图所示。已知 (半衰期)为反应物消耗一半所用的时间,下列叙述错误的是
A. ,Ⅰ条件下
B.其他条件相同,S(催化剂)越大,k越大
C.其他条件相同, 增大,反应速率不变
D.该温度下,当S(催化剂) , 时, 为
【答案】A
【解析】A.根据如所示,Ⅰ和Ⅲ条件相同,起始浓度不同,但反应速率相同,说明反应速率与起始浓度无
关,所以 , ,A错误;
B.对比Ⅰ、Ⅱ和Ⅲ,Ⅱ中S(催化剂)越大最大,反应速率越大,k越大,Ⅰ和Ⅲ的S(催化剂)相同,反应速率相
同,k相同,所以在其他条件相同,S(催化剂)越大,k越大,B正确;
C.由以上分析, 与反应速率无关,C正确;
D.由图可知,在条件Ⅰ,S(催化剂) , 消耗一半即消耗 所用的时
间为 ,所以半衰期为 ,D正确;
故选A。
6.(河北省保定市2023届一模)已知 的速率方程为 。
,为探究反应速率与 的关系,进行如下实验:向锥形瓶中加入一定体积(V)的2.0
资料整理【淘宝店铺:向阳百分百】molL 溶液、2.0 molL 溶液、1.0 molL 醋酸和水,充分搅拌,保持体系温度为36℃,用
⋅ ⋅ ⋅
秒表测量收集1.0 mL 所需要的时间(t),实验数据如下表。下列说法正确的是
V/mL
实验 t/s
溶 醋
溶液 水
液 酸
1 4.0 4.0 8.0 332
2 6.0 4.0 4.0 6.0 148
3 4.0 4.0 4.0 83
4 12.0 4.0 4.0 37
A. ;
B.实验3用 表示的反应平均速率 mol·s
C.醋酸不参与反应,其浓度的大小对该反应速率无影响
D.速率方程中
【答案】D
【解析】A.为探究反应速率与 的关系, 浓度不变,根据数据2可知溶液总体积为20mL,根
据变量单一可知 为4.0mL, 为8.0mL, 为0mL,A错误;
B.实验3,没有在标准状况下,不能用22.4来计算物质的量,B错误;
C.反应前后醋酸不变,所以醋酸是催化剂,醋酸的浓度也会影响反应速率,C错误;
D.浓度增大速率加快,根据1和3组数据分析,3的 是1的2倍,1和3所用的时间比 ,根据
分析可知速率和浓度的平方成正比,故m=2,D正确;
故选D。
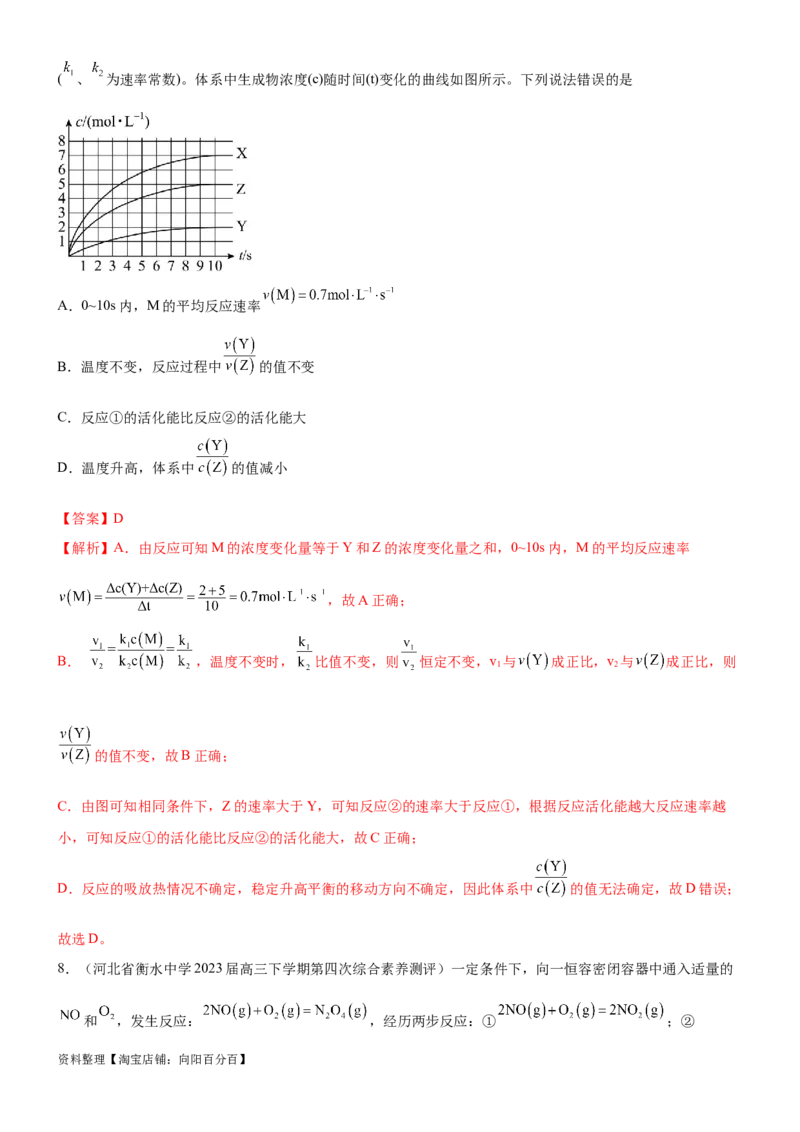
7.(河北省邢台市2022-2023学年高三下学期第一次模拟)室温下,某溶液初始时仅溶有M,同时发生以下两
个反应:① ;② 。反应①的速率可表示为 ,反应②的速率可表示为
资料整理【淘宝店铺:向阳百分百】( 、 为速率常数)。体系中生成物浓度(c)随时间(t)变化的曲线如图所示。下列说法错误的是
A.0~10s内,M的平均反应速率
B.温度不变,反应过程中 的值不变
C.反应①的活化能比反应②的活化能大
D.温度升高,体系中 的值减小
【答案】D
【解析】A.由反应可知M的浓度变化量等于Y和Z的浓度变化量之和,0~10s内,M的平均反应速率
,故A正确;
B. ,温度不变时, 比值不变,则 恒定不变,v 与 成正比,v 与 成正比,则
1 2
的值不变,故B正确;
C.由图可知相同条件下,Z的速率大于Y,可知反应②的速率大于反应①,根据反应活化能越大反应速率越
小,可知反应①的活化能比反应②的活化能大,故C正确;
D.反应的吸放热情况不确定,稳定升高平衡的移动方向不确定,因此体系中 的值无法确定,故D错误;
故选D。
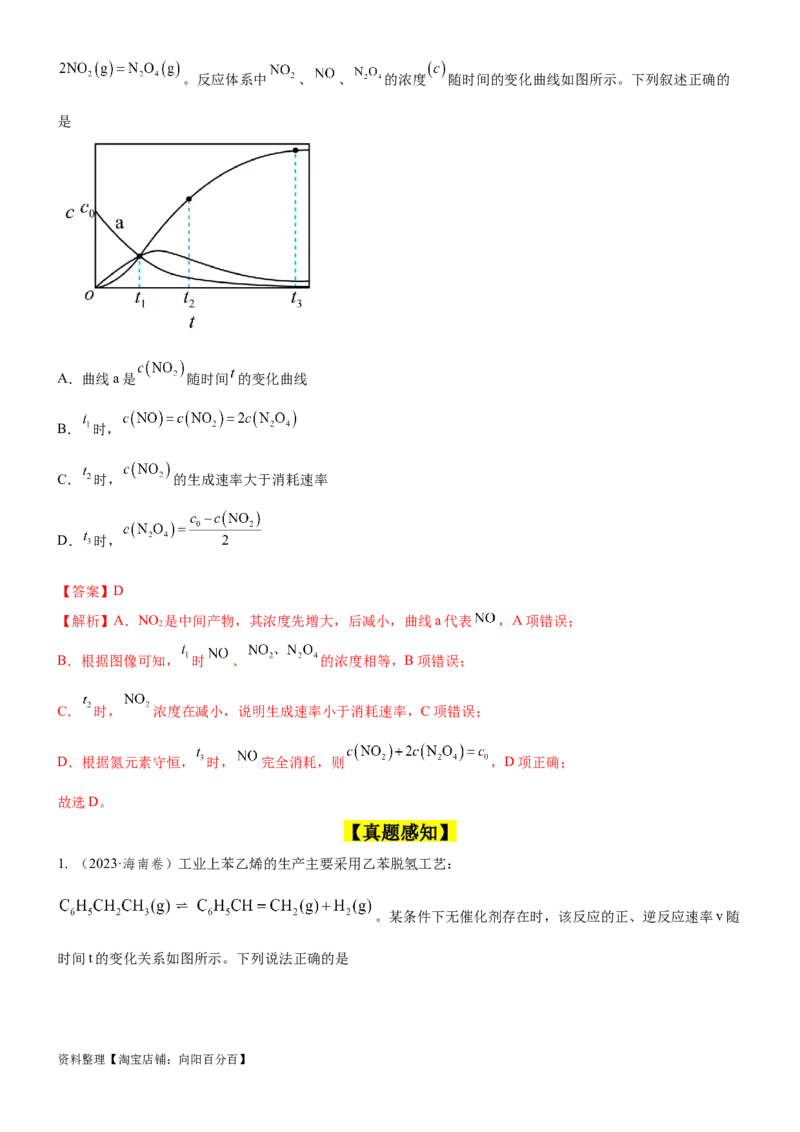
8.(河北省衡水中学2023届高三下学期第四次综合素养测评)一定条件下,向一恒容密闭容器中通入适量的
和 ,发生反应: ,经历两步反应:① ;②
资料整理【淘宝店铺:向阳百分百】。反应体系中 、 、 的浓度 随时间的变化曲线如图所示。下列叙述正确的
是
A.曲线a是 随时间 的变化曲线
B. 时,
C. 时, 的生成速率大于消耗速率
D. 时,
【答案】D
【解析】A.NO 是中间产物,其浓度先增大,后减小,曲线a代表 ,A项错误;
2
B.根据图像可知, 时 、 的浓度相等,B项错误;
C. 时, 浓度在减小,说明生成速率小于消耗速率,C项错误;
D.根据氮元素守恒, 时, 完全消耗,则 ,D项正确;
故选D。
【真题感知】
1. (2023·海南卷)工业上苯乙烯的生产主要采用乙苯脱氢工艺:
。某条件下无催化剂存在时,该反应的正、逆反应速率v随
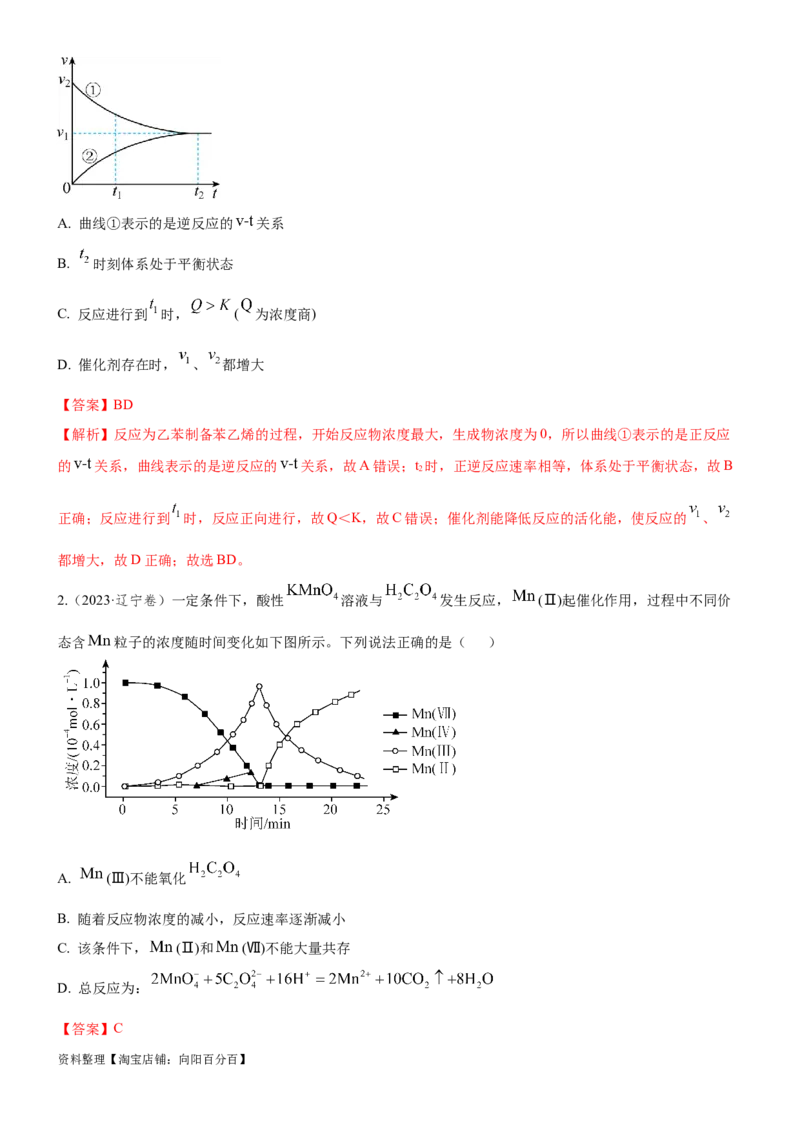
时间t的变化关系如图所示。下列说法正确的是
资料整理【淘宝店铺:向阳百分百】A. 曲线①表示的是逆反应的 关系
B. 时刻体系处于平衡状态
C. 反应进行到 时, ( 为浓度商)
D. 催化剂存在时, 、 都增大
【答案】BD
【解析】反应为乙苯制备苯乙烯的过程,开始反应物浓度最大,生成物浓度为0,所以曲线①表示的是正反应
的 关系,曲线表示的是逆反应的 关系,故A错误;t 时,正逆反应速率相等,体系处于平衡状态,故B
2
正确;反应进行到 时,反应正向进行,故Q<K,故C错误;催化剂能降低反应的活化能,使反应的 、
都增大,故D正确;故选BD。
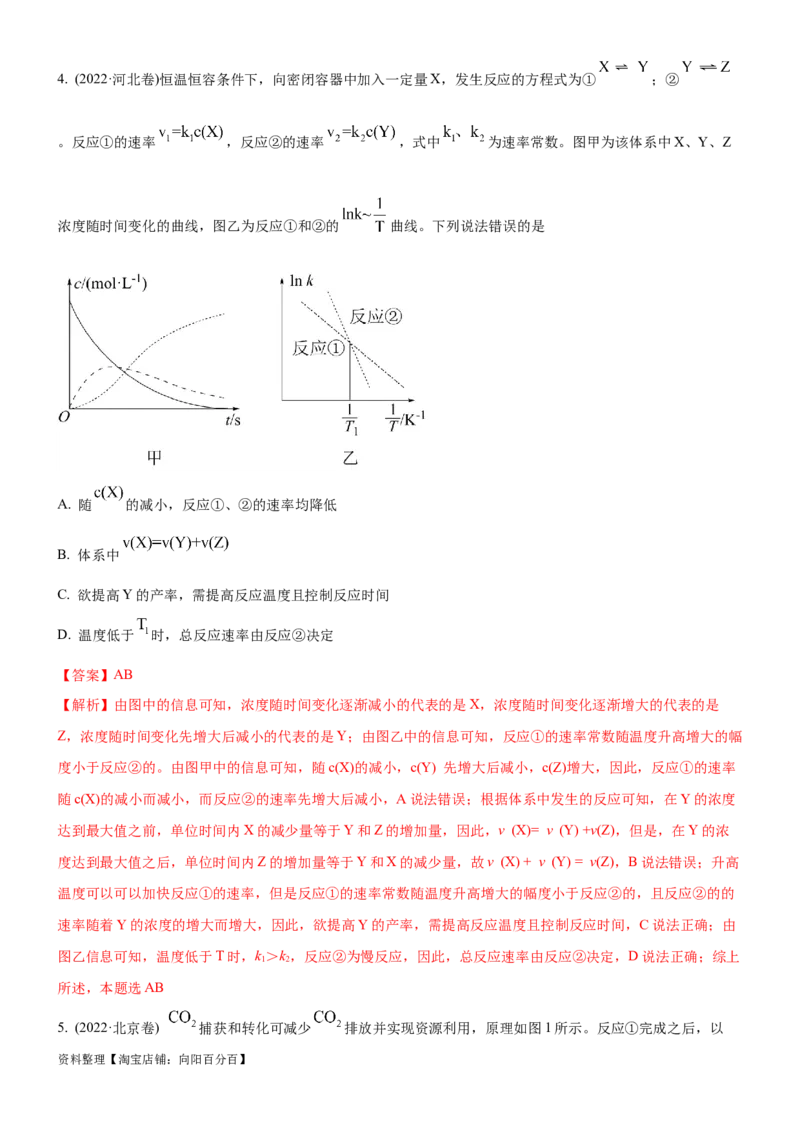
2.(2023·辽宁卷)一定条件下,酸性 溶液与 发生反应, (Ⅱ)起催化作用,过程中不同价
态含 粒子的浓度随时间变化如下图所示。下列说法正确的是( )
A. (Ⅲ)不能氧化
B. 随着反应物浓度的减小,反应速率逐渐减小
C. 该条件下, (Ⅱ)和 (Ⅶ)不能大量共存
D. 总反应为:
【答案】C
资料整理【淘宝店铺:向阳百分百】【解析】开始一段时间(大约13min前)随着时间的推移Mn(VII)浓度减小直至为0,Mn(III)浓度增大直至达到
最大值,结合图像,此时间段主要生成Mn(III),同时先生成少量Mn(IV)后Mn(IV)被消耗;后来(大约13min
后)随着时间的推移Mn(III)浓度减少,Mn(II)的浓度增大;据此作答。由图像可知,随着时间的推移Mn(III)的
浓度先增大后减小,说明开始反应生成Mn(III),后Mn(III)被消耗生成Mn(II),Mn(III)能氧化HC O,A项错
2 2 4
误;随着反应物浓度的减小,到大约13min时开始生成Mn(II),Mn(II)对反应起催化作用,13min后反应速率会
增大,B项错误;由图像可知,Mn(VII)的浓度为0后才开始生成Mn(II),该条件下Mn(II)和Mn(VII)不能大量
共存,C项正确;HC O 为弱酸,在离子方程式中应以化学式保留,总反应为2MnO-+5H C O+6H+=2Mn2+
2 2 4 4 2 2 4
+10CO ↑+8H O,D项错误;故选C。
2 2
3. (2022·广东卷)在相同条件下研究催化剂I、Ⅱ对反应 的影响,各物质浓度c随反应时间t的部分
变化曲线如图,则
A. 无催化剂时,反应不能进行
B. 与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C. a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D. 使用催化剂Ⅰ时, 内,
【答案】D
【解析】由图可知,无催化剂时,随反应进行,生成物浓度也在增加,说明反应也在进行,故A错误;由图可
知,催化剂I比催化剂II催化效果好,说明催化剂I使反应活化能更低,反应更快,故B错误;由图可知,使用
催化剂II时,在0~2min 内Y的浓度变化了2.0mol/L,而a曲线表示的X的浓度变化了2.0mol/L,二者变化量
之比不等于化学计量数之比,所以a曲线不表示使用催化剂II时X浓度随时间t的变化,故C错误;使用催化
剂I时,在0~2min 内,Y的浓度变化了4.0mol/L,则 v(Y)=== =2.0 , v(X) =
(Y) = 2.0 =1.0 ,故D正确;答案选D。
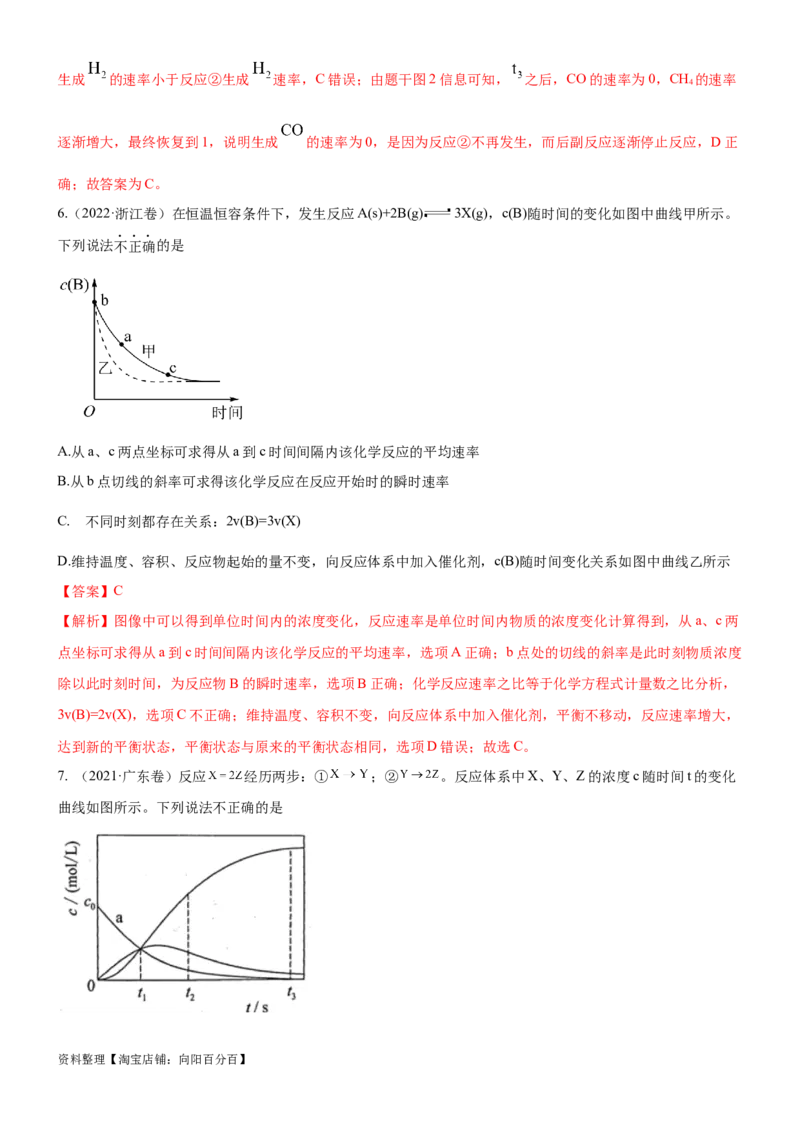
资料整理【淘宝店铺:向阳百分百】4. (2022·河北卷)恒温恒容条件下,向密闭容器中加入一定量X,发生反应的方程式为① ;②
。反应①的速率 ,反应②的速率 ,式中 为速率常数。图甲为该体系中X、Y、Z
浓度随时间变化的曲线,图乙为反应①和②的 曲线。下列说法错误的是
A. 随 的减小,反应①、②的速率均降低
B. 体系中
C. 欲提高Y的产率,需提高反应温度且控制反应时间
D. 温度低于 时,总反应速率由反应②决定
【答案】AB
【解析】由图中的信息可知,浓度随时间变化逐渐减小的代表的是X,浓度随时间变化逐渐增大的代表的是
Z,浓度随时间变化先增大后减小的代表的是Y;由图乙中的信息可知,反应①的速率常数随温度升高增大的幅
度小于反应②的。由图甲中的信息可知,随c(X)的减小,c(Y) 先增大后减小,c(Z)增大,因此,反应①的速率
随c(X)的减小而减小,而反应②的速率先增大后减小,A说法错误;根据体系中发生的反应可知,在Y的浓度
达到最大值之前,单位时间内X的减少量等于Y和Z的增加量,因此,v (X)= v (Y) +v(Z),但是,在Y的浓
度达到最大值之后,单位时间内Z的增加量等于Y和X的减少量,故v (X) + v (Y) = v(Z),B说法错误;升高
温度可以可以加快反应①的速率,但是反应①的速率常数随温度升高增大的幅度小于反应②的,且反应②的的
速率随着Y的浓度的增大而增大,因此,欲提高Y的产率,需提高反应温度且控制反应时间,C说法正确;由
图乙信息可知,温度低于T时,k>k,反应②为慢反应,因此,总反应速率由反应②决定,D说法正确;综上
1 2
所述,本题选AB 。
5. (2022·北京卷) 捕获和转化可减少 排放并实现资源利用,原理如图1所示。反应①完成之后,以
资料整理【淘宝店铺:向阳百分百】为载气,以恒定组成的 混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随
反应时间变化如图2所示。反应过程中始终未检测到 ,在催化剂上有积碳。
下列说法不正确的是
A. 反应①为 ;反应②为
B. , 比 多,且生成 速率不变,可能有副反应
C. 时刻,副反应生成 的速率大于反应②生成 速率
D. 之后,生成 的速率为0,是因为反应②不再发生
【答案】C
【解析】由题干图1所示信息可知,反应①为 ,结合氧化还原反应配平可得反应②为
,A正确;由题干图2信息可知, , 比 多,且生成
速率不变,且反应过程中始终未检测到 ,在催化剂上有积碳,故可能有副反应 ,反应
②和副反应中CH 和H 的系数比均为1:2,B正确;由题干反应②方程式可知,H 和CO的反应速率相等,而
4 2 2
时刻信息可知,H 的反应速率未变,仍然为2mmol/min,而CO变为1~2mmol/min之间,故能够说明副反应
2
资料整理【淘宝店铺:向阳百分百】生成 的速率小于反应②生成 速率,C错误;由题干图2信息可知, 之后,CO的速率为0,CH 的速率
4
逐渐增大,最终恢复到1,说明生成 的速率为0,是因为反应②不再发生,而后副反应逐渐停止反应,D正
确;故答案为C。
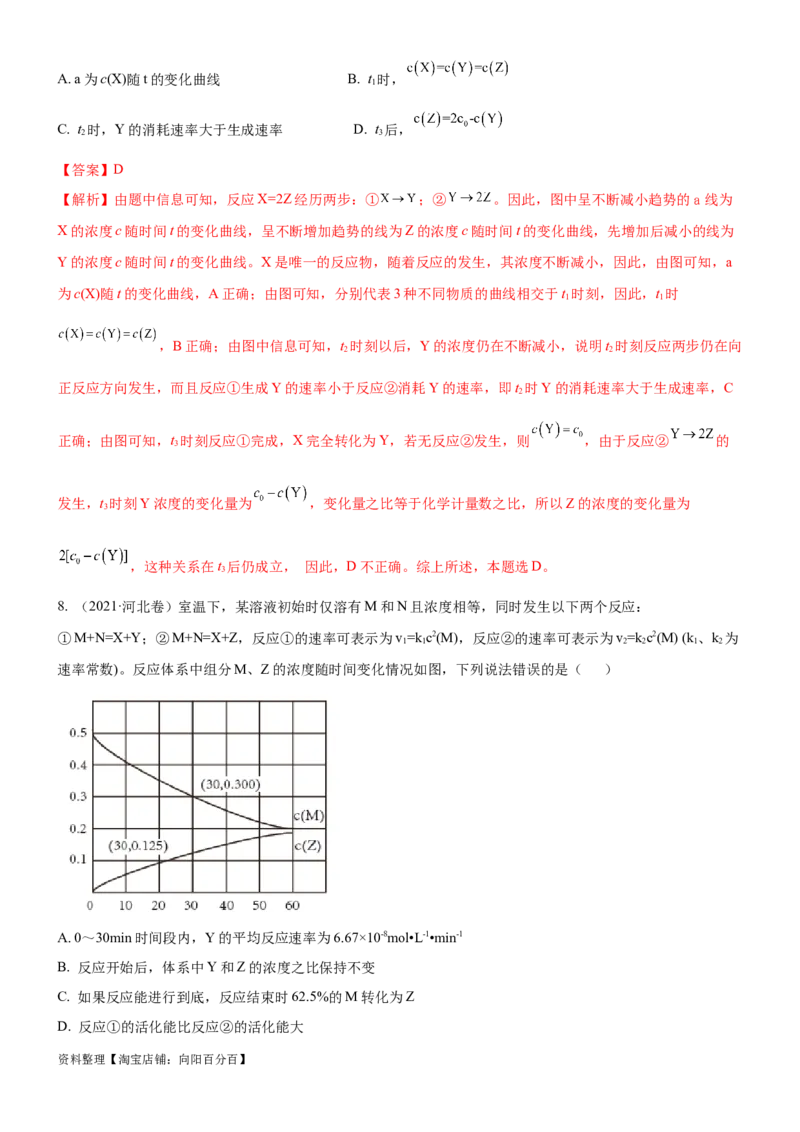
6.(2022·浙江卷)在恒温恒容条件下,发生反应A(s)+2B(g ) 3X(g),c(B)随时间的变化如图中曲线甲所示。
下列说法不正确的是
A.从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率
B.从b点切线的斜率可求得该化学反应在反应开始时的瞬时速率
在
C. 不同时刻都存在关系:2v(B)=3v(X)
D.维持温度、容积、反应物起始的量不变,向反应体系中加入催化剂,c(B)随时间变化关系如图中曲线乙所示
【答案】C
【解析】图像中可以得到单位时间内的浓度变化,反应速率是单位时间内物质的浓度变化计算得到,从a、c两
点坐标可求得从a到c时间间隔内该化学反应的平均速率,选项A正确;b点处的切线的斜率是此时刻物质浓度
除以此时刻时间,为反应物B的瞬时速率,选项B正确;化学反应速率之比等于化学方程式计量数之比分析,
3v(B)=2v(X),选项C不正确;维持温度、容积不变,向反应体系中加入催化剂,平衡不移动,反应速率增大,
达到新的平衡状态,平衡状态与原来的平衡状态相同,选项D错误;故选C。
7. (2021·广东卷)反应 经历两步:① ;② 。反应体系中X、Y、Z的浓度c随时间t的变化
曲线如图所示。下列说法不正确的是
资料整理【淘宝店铺:向阳百分百】A. a为c(X)随t的变化曲线 B. t 时,
1
C. t 时,Y的消耗速率大于生成速率 D. t 后,
2 3
【答案】D
【解析】由题中信息可知,反应X=2Z经历两步:① ;② 。因此,图中呈不断减小趋势的a线为
X的浓度c随时间t的变化曲线,呈不断增加趋势的线为Z的浓度c随时间t的变化曲线,先增加后减小的线为
Y的浓度c随时间t的变化曲线。X是唯一的反应物,随着反应的发生,其浓度不断减小,因此,由图可知,a
为c(X)随t的变化曲线,A正确;由图可知,分别代表3种不同物质的曲线相交于t 时刻,因此,t 时
1 1
,B正确;由图中信息可知,t 时刻以后,Y的浓度仍在不断减小,说明t 时刻反应两步仍在向
2 2
正反应方向发生,而且反应①生成Y的速率小于反应②消耗Y的速率,即t 时Y的消耗速率大于生成速率,C
2
正确;由图可知,t 时刻反应①完成,X完全转化为Y,若无反应②发生,则 ,由于反应② 的
3
发生,t 时刻Y浓度的变化量为 ,变化量之比等于化学计量数之比,所以Z的浓度的变化量为
3
,这种关系在t 后仍成立, 因此,D不正确。综上所述,本题选D。
3
8. (2021·河北卷)室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反应:
①M+N=X+Y;②M+N=X+Z,反应①的速率可表示为v=kc2(M),反应②的速率可表示为v=kc2(M) (k 、k 为
1 1 2 2 1 2
速率常数)。反应体系中组分M、Z的浓度随时间变化情况如图,下列说法错误的是( )
A. 0~30min时间段内,Y的平均反应速率为6.67×10-8mol•L-1•min-1
B. 反应开始后,体系中Y和Z的浓度之比保持不变
C. 如果反应能进行到底,反应结束时62.5%的M转化为Z
D. 反应①的活化能比反应②的活化能大
资料整理【淘宝店铺:向阳百分百】【答案】A
【解析】由图中数据可知,30min时,M、Z的浓度分别为0.300mol•L-1和0.125 mol•L-1,则M的变化量为
0.5mol•L-1-0.300 mol•L-1=0.200 mol•L-1,其中转化为Y的变化量为0.200mol•L-1-0.125 mol•L-1=0.075 mol•L-1。因
此,0~30min时间段内,Y的平均反应速率为 mol•L-1•min-1,A错误;由题中信息可知,反
应①和反应②的速率之比为 ,Y和Z分别为反应①和反应②的产物,且两者与M的化学计量数相同(化学
计量数均为1),因此反应开始后,体系中Y和Z的浓度之比等于 ,由于k、k 为速率常数,故该比值保
1 2
持不变,B正确; 结合A、B的分析可知因此反应开始后,在相同的时间内体系中Y和Z的浓度之比等于
=0.6,因此,如果反应能进行到底,反应结束时有 的M转化为Z,即62.5%的M转化为Z,C正确;由以上
分析可知,在相同的时间内生成Z较多、生成Y较少,因此,反应①的化学反应速率较小,在同一体系中,活
化能较小的化学反应速率较快,故反应①的活化能比反应②的活化能大,D正确。故选A。
9. (2021·浙江卷)取50 mL过氧化氢水溶液,在少量I- 存在下分解:2HO=2H O+O↑。在一定温度下,测得
2 2 2 2
O 的放出量,转换成HO 浓度(c)如下表:
2 2 2
t/min 0 20 40 60 80
c/(mol·L-1) 0.80 0.40 0.20 0.10 0.050
下列说法不正确的是
A. 反应20min时,测得O 体积为224mL(标准状况)
2
B. 20~40min,消耗HO 的平均速率为0.010mol·L-1·min-1
2 2
C. 第30min时的瞬时速率小于第50min时的瞬时速率
D. H O 分解酶或Fe O 代替I-也可以催化HO 分解
2 2 2 3 2 2
【答案】C
【解析】反应20min时,过氧化氢的浓度变为0.4mol/L,说明分解的过氧化氢的物质的量n(H O)=
2 2
(0.80-0.40)mol/L×0.05L=0.02mol,过氧化氢分解生成的氧气的物质的量n(O )=0.01mol,标况下的体积
2
V=n·V =0.01mol×22.4L/mol=0.224L=224mL,A正确;20~40min,消耗过氧化氢的浓度为(0.40-0.20)mol/
m
资料整理【淘宝店铺:向阳百分百】L=0.20mol/L,则这段时间内的平均速率v= = =0.010mol/(L·min),B正确;随着反应的不断进
行,过氧化氢的浓度不断减小,某一时刻分解的过氧化氢的量也不断减小,故第30min时的瞬时速率大于第
50min时的瞬时速率,C错误;I-在反应中起到催化的作用,故也可以利用过氧化氢分解酶或Fe O 代替,D正
2 3
确;故答案选C。
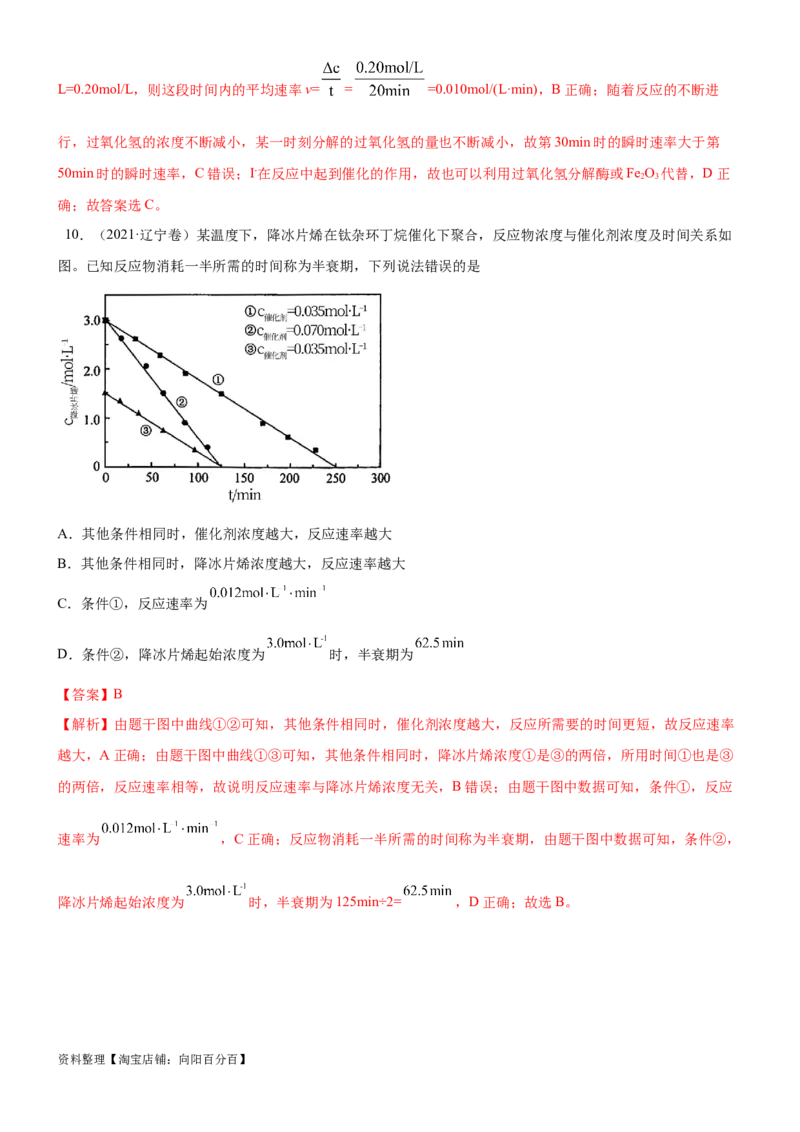
10.(2021·辽宁卷)某温度下,降冰片烯在钛杂环丁烷催化下聚合,反应物浓度与催化剂浓度及时间关系如
图。已知反应物消耗一半所需的时间称为半衰期,下列说法错误的是
A.其他条件相同时,催化剂浓度越大,反应速率越大
B.其他条件相同时,降冰片烯浓度越大,反应速率越大
C.条件①,反应速率为
D.条件②,降冰片烯起始浓度为 时,半衰期为
【答案】B
【解析】由题干图中曲线①②可知,其他条件相同时,催化剂浓度越大,反应所需要的时间更短,故反应速率
越大,A正确;由题干图中曲线①③可知,其他条件相同时,降冰片烯浓度①是③的两倍,所用时间①也是③
的两倍,反应速率相等,故说明反应速率与降冰片烯浓度无关,B错误;由题干图中数据可知,条件①,反应
速率为 ,C正确;反应物消耗一半所需的时间称为半衰期,由题干图中数据可知,条件②,
降冰片烯起始浓度为 时,半衰期为125min÷2= ,D正确;故选B。
资料整理【淘宝店铺:向阳百分百】