文档内容
考点 1 化学反应速率
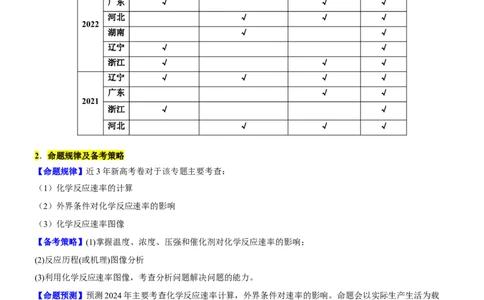
1.3年真题考点分布
考点分布
年份 卷区
反应速率的计算 反应速率的影响因素 反应速率的图像 综合应用
辽宁 √ √ √
2023
海南 √ √ √
北京 √ √ √
广东 √ √ √
河北 √ √ √
2022
湖南 √ √
辽宁 √ √
浙江 √ √ √
辽宁 √ √ √ √
广东 √ √
2021
浙江 √ √
河北 √ √ √
2.命题规律及备考策略
【命题规律】近3年新高考卷对于该专题主要考查:
(1)化学反应速率的计算
(2)外界条件对化学反应速率的影响
(3)化学反应速率图像
【备考策略】(1)掌握温度、浓度、压强和催化剂对化学反应速率的影响;
(2)反应历程(或机理)图像分析
(3)利用化学反应速率图像,考查分析问题解决问题的能力。
【命题预测】预测2024年主要考查化学反应速率计算,外界条件对速率的影响。命题会以实际生产生活为载
体,将化学反应速率与化工生产、生活实际相结合,应予以重视。
考法 1 化学反应速率
1.化学反应速率2.化学反应速率计算的万能方法——三段式法
对于反应mA(g)+nB(g) pC(g)+qD(g),起始时A的浓度为a mol·L-1,B的浓度为b mol·L-1,反应进行
至ts时,A消耗了x mol·L-1,则化学反应速率可计算如下:
1
mA(g)+nB(g) pC(g)+qD(g)
起始/(mol·L-1) a b 0 0
转化/(mol·L-1) x
t/(mol·L-1) a-x b-
1
则:v(A)= mol·L-1·s-1,v(B)= mol·L-1·s-1,
v(C)= mol·L-1·s-1,v(D)= mol·L-1·s-1。
3.化学反应速率与化学计量数的关系
对于已知反应mA(g)+nB(g)===pC(g)+qD(g),其化学反应速率可用不同的反应物或生成物来表示,当单位相同
时,化学反应速率的数值之比等于化学计量数之比,即v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q。
如一定温度下,在密闭容器中发生反应:3A(g)+B(g) 2C(g)。已知v(A)=0.6 mol·L-1·s-1,则v(B)=0.2
mol·L-1·s-1,v(C)=0.4 mol·L-1·s-1。
4.化学反应速率大小的比较方法
由于同一化学反应的反应速率用不同物质表示时数值可能不同,所以比较反应的快慢不能只看数值的大小,而
要进行一定的转化。
(1)看单位是否统一,若不统一,换算成相同的单位。
(2)单位统一后,换算成同一物质表示的速率,再比较数值的大小。
(3)也可以直接比较化学反应速率与化学计量数的比值,即对于一般反应aA+bB===cC+dD,比较与,若>,
则A表示的反应速率比B的大。
【典例1】(湖南省岳阳市华容县普通高中2023届高三新高考适应性考试)取50 mL过氧化氢水溶液,在少量
I- 存在下分解:2HO=2H O+O↑。在一定温度下,测得O 的放出量,转换成HO 浓度(c)如下表:
2 2 2 2 2 2 2t/min 0 20 40 60 80
c/(mol·L-1) 0.80 0.40 0.20 0.10 0.050
下列说法不正确的是
A.反应20min时,测得O 体积为224mL(标准状况)
2
B.20~40min,消耗HO 的平均速率为0.010mol·L-1·min-1
2 2
C.第30min时的瞬时速率小于第50min时的瞬时速率
D.HO 分解酶或Fe O 代替I-也可以催化HO 分解
2 2 2 3 2 2
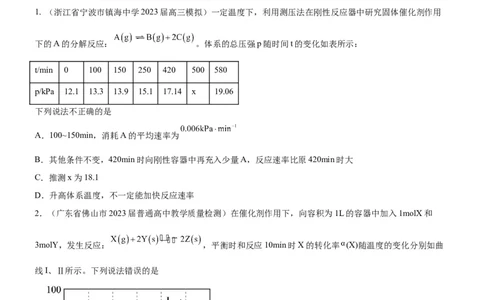
1. (浙江省宁波市镇海中学2023届高三模拟)一定温度下,利用测压法在刚性反应器中研究固体催化剂作用
下的A的分解反应: 。体系的总压强p随时间t的变化如表所示:
t/min 0 100 150 250 420 500 580
p/kPa 12.1 13.3 13.9 15.1 17.14 x 19.06
下列说法不正确的是
A.100~150min,消耗A的平均速率为
B.其他条件不变,420min时向刚性容器中再充入少量A,反应速率比原420min时大
C.推测x为18.1
D.升高体系温度,不一定能加快反应速率
2.(广东省佛山市2023届普通高中教学质量检测)在催化剂作用下,向容积为1L的容器中加入1molX和
3molY,发生反应: ,平衡时和反应10min时X的转化率 (X)随温度的变化分别如曲
线I、Ⅱ所示。下列说法错误的是
A.该反应
B.200℃时,前10min的平均反应速率C.400℃时,反应的平衡常数K=2
D.bc段变化可能是催化剂在温度高于400℃时活性降低导致
考法 2 基元反应和有效碰撞理论
1.基元反应:大多数化学反应往往经过多个反应步骤才能实现,每一步反应都被称为基元反应;先后进行的基
元反应反映了反应历程,反应历程又称为反应机理。
2.有效碰撞
①基元反应发生的先决条件是反应物的分子必须发生碰撞。
②反应物分子的每一次碰撞并不是都能发生反应,能够发生化学反应的碰撞叫作有效碰撞。发生有效碰撞的两
个条件是反应物分子能量足够和取向合适。
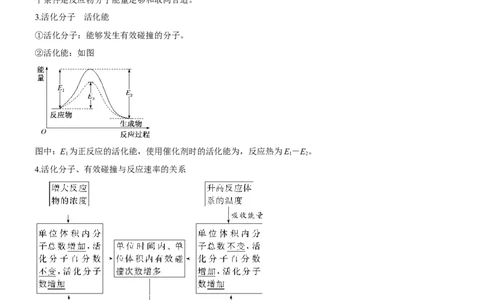
3.活化分子 活化能
①活化分子:能够发生有效碰撞的分子。
②活化能:如图
图中:E 为正反应的活化能,使用催化剂时的活化能为,反应热为E-E。
1 1 2
4.活化分子、有效碰撞与反应速率的关系
【典例2】(广东省6校2023-2024学年高三上学期第一次联考)叔丁基溴在乙醇中反应的能量变化如图所示。
反应1:
反应2:下列说法错误的是
A.3种过渡态相比,①最不稳定 B.反应1和反应2的 都小于0
C.第一个基元反应是决速步骤 D. 是反应1和反应2共同的催化剂
1.(辽宁省沈阳市第一二〇中学2024届高三质量监测)2SO (g)+O(g) 2SO (g) ∆H=-198kJ•mol-1。在
2 2 3
VO 存在时该反应机理为:①VO+SO→2VO +SO(快);②4VO +O →2VO(慢)。下列说法不正确的是
2 5 2 5 2 2 3 2 2 2 5
A.该反应速率主要由第②步基元反应决定
B.由反应机理可知,VO 和VO 都是该反应的催化剂
2 5 2
C.VO 的存在提高了该反应活化分子百分数,使单位时间内有效碰撞次数增加,反应速率加快
2 5
D.逆反应的活化能比正反应的活化能大198kJ•mol-1
2.(四川省成都市第七中学2024届高三月考) 。在 存在
时该反应机理为:① (快);② (慢)。下列说法不正确的是
A.该反应速率主要由第②步基元反应决定
B.基元反应发生的先决条件是反应物分子必须有足够的能量
C. 的存在提高了该反应活化分子百分数,使有效碰撞次数增加,反应速率加快
D.逆反应的活化能比正反应的活化能大
考法 3 影响化学反应速率的因素
1.影响化学反应速率的因素
(1)内因
反应物本身的性质是主要因素。如相同条件下Mg、Al与稀盐酸反应的速率大小关系为Mg>Al。
(2)外因(只改变一个条件,其他条件不变)【特别提醒】
①改变固体或纯液体的量对化学反应速率无影响。
②浓度、温度、压强发生变化或加入催化剂时,正、逆反应速率均增大或减小,如升高温度,不论是放热反应
还是吸热反应,化学反应速率均加快。
2.反应体系条件改变对反应速率的影响
①恒温时:体积缩小――→压强增大――→浓度增大――→反应速率增大。
②恒温恒容时:
a.充入气体反应物――→总压强增大――→浓度增大――→反应速率增大。
b.充入“惰性气体”――→总压强增大,但各气体分压不变―→各物质的浓度不变―→反应速率不变。
③恒温恒压时:充入“惰性气体”――→体积增大――→各反应物浓度减小――→反应速率减小。
总之,压强改变而对反应速率产生的影响是因为压强改变会引起浓度变化,从而对反应速率产生影响。
【典例3】(北京市西城区2023届一模考试)探究影响HO 分解速率的影响因素,实验方案如图。
2 2
下列说法不正确的是
A.对比①②,可探究FeCl 溶液对HO 分解速率的影响
3 2 2
B.对比②③④,可探究温度对HO 分解速率的影响
2 2
C.HO 是直线形的非极性分子
2 2
D.HO 易溶于水,主要是由于HO 与HO分子之间能形成氢键
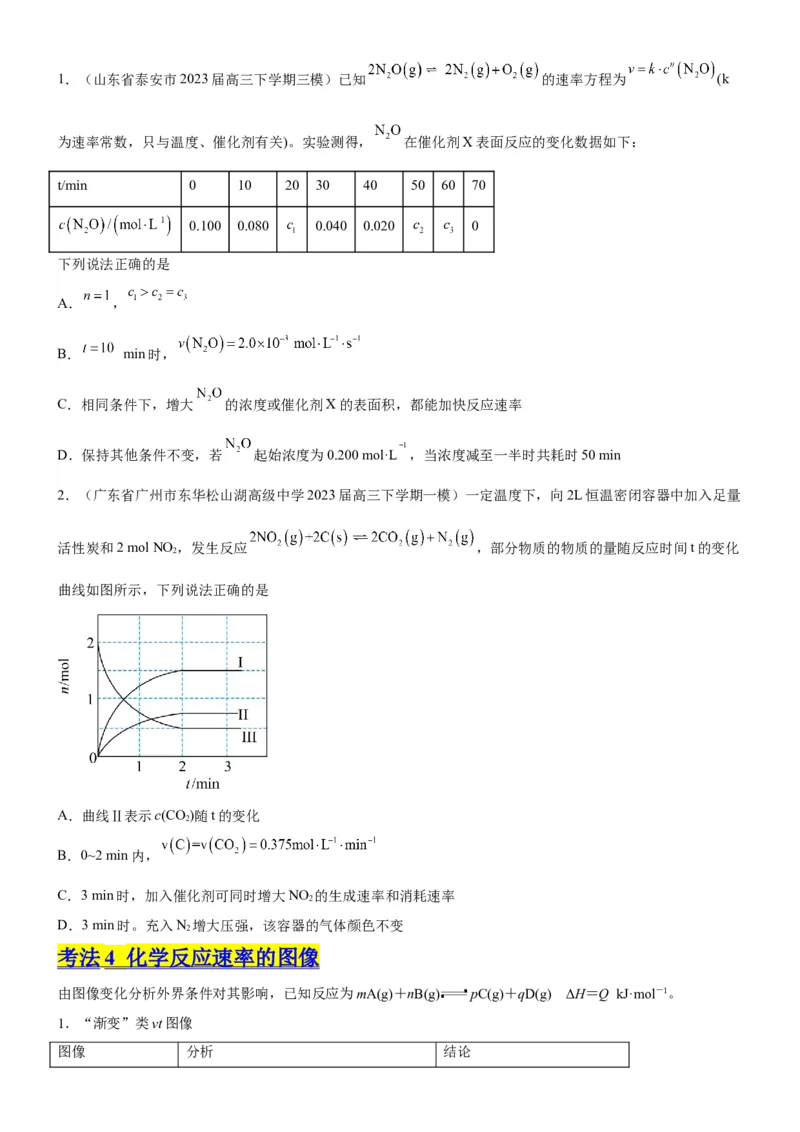
2 2 2 2 21.(山东省泰安市2023届高三下学期三模)已知 的速率方程为 (k
为速率常数,只与温度、催化剂有关)。实验测得, 在催化剂X表面反应的变化数据如下:
t/min 0 10 20 30 40 50 60 70
0.100 0.080 0.040 0.020 0
下列说法正确的是
A. ,
B. min时,
C.相同条件下,增大 的浓度或催化剂X的表面积,都能加快反应速率
D.保持其他条件不变,若 起始浓度为0.200 mol·L ,当浓度减至一半时共耗时50 min
2.(广东省广州市东华松山湖高级中学2023届高三下学期一模)一定温度下,向2L恒温密闭容器中加入足量
活性炭和2 mol NO ,发生反应 ,部分物质的物质的量随反应时间t的变化
2
曲线如图所示,下列说法正确的是
A.曲线Ⅱ表示c(CO)随t的变化
2
B.0~2 min内,
C.3 min时,加入催化剂可同时增大NO 的生成速率和消耗速率
2
D.3 min时。充入N 增大压强,该容器的气体颜色不变
2
考法 4 化学反应速率的图像
由图像变化分析外界条件对其影响,已知反应为mA(g)+nB(g ) pC(g)+qD(g) ΔH=Q kJ·mol-1。
1.“渐变”类vt图像
图像 分析 结论t 时v′ 突然增大,v′ 逐渐增大;v′ >v′ t 时其他条件不变,增大反
1 正 逆 正 1
,平衡向正反应方向移动 应物的浓度
逆
t 时v′ 突然减小,v′ 逐渐减小;v′ >v′ t 时其他条件不变,减小反
1 正 逆 逆 1
,平衡向逆反应方向移动 应物的浓度
正
t 时v′ 突然增大,v′ 逐渐增大;v′ >v′ t 时其他条件不变,增大生
1 逆 正 逆 1
,平衡向逆反应方向移动 成物的浓度
正
t 时v′ 突然减小,v′ 逐渐减小;v′ >v′ t 时其他条件不变,减小生
1 逆 正 正 1
,平衡向正反应方向移动 成物的浓度
逆
2.“断点”类vt图像
图像 分析 结论
t 时其他条件不变,增大反应体系的
1
压强且m+n>p+q(正反应为体积减
t 1 时v′ 正 、v′ 逆 均突然增大,且v′ 正 小的反应)
>v′ ;平衡向正反应方向进行
逆
t 时其他条件不变,升高温度且Q>
1
0(吸热反应)
t 时其他条件不变,增大反应体系的
1
压强且m+n<p+q(正反应为体积增
t 1 时v′ 正 、v′ 逆 均突然增大,且v′ 逆 大的反应)
>v′ ;平衡向逆反应方向进行
正
t 时其他条件不变,升高温度且Q<
1
0(放热反应)
t 时其他条件不变,减小反应体系的
1
压强且m+n<p+q(正反应为体积增
t 1 时v′ 正 、v′ 逆 均突然减小,且v′ 正 大的反应)
>v′ ;平衡向正反应方向进行
逆
t 时其他条件不变,降低温度且Q<
1
0(放热反应)
t 时其他条件不变,减小反应体系的
1
压强且m+n>p+q(正反应为体积减
t 1 时v′ 逆 、v′ 正 均突然减小,且v′ 逆 小的反应)
>v′ ;平衡向逆反应方向进行
正
t 时其他条件不变,降低温度且Q>
1
0(吸热反应)
3.“平台”类vt图像
图像 分析 结论
t 时其他条件不变使用催化剂
1
t 1 时v′ 正 、v′ 逆 均突然增大且v′ 正 =v′ t 1 时其他条件不变增大反应体系的
逆 ,平衡不移动 压强且m+n=p+q(反应前后气体
体积无变化)
t 时其他条件不变,减小反应体系
t 时v′ 、v′ 均突然减小且v′ =v′ 1
1 正 逆 正 的压强且m+n=p+q(反应前后气
,平衡不移动
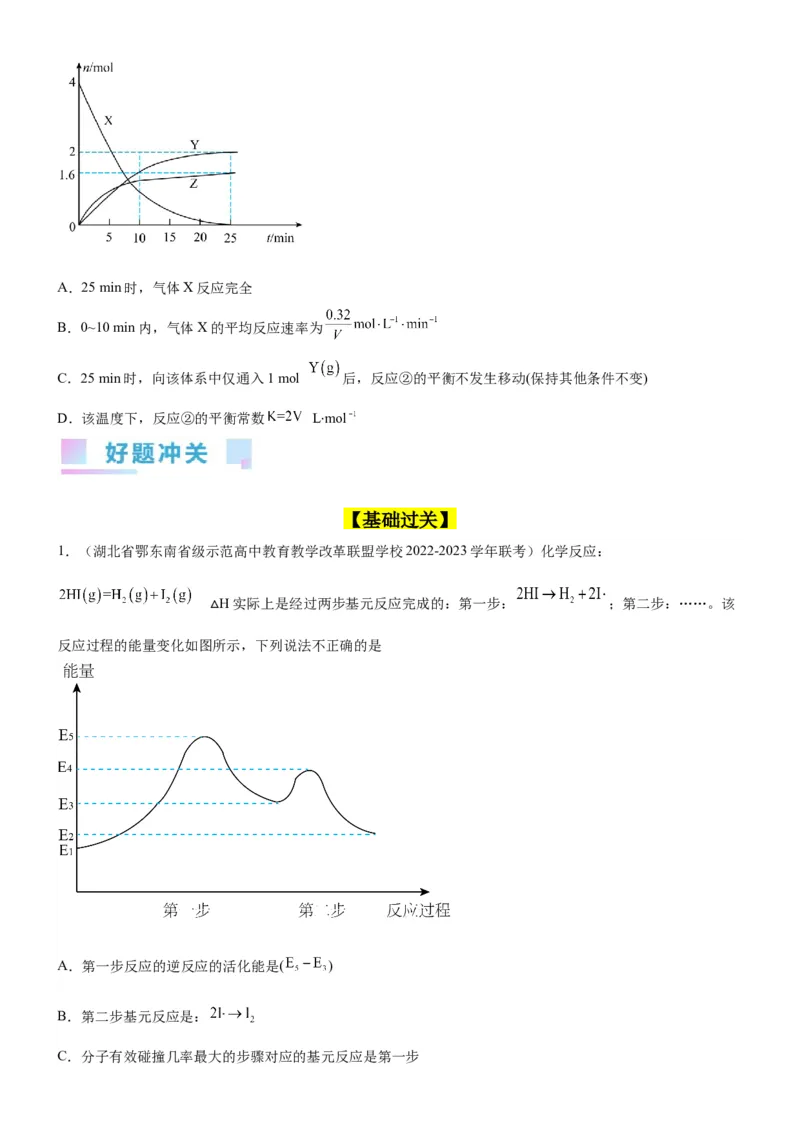
逆 体体积无变化)【典例4】(河北省衡水市第二中学2023届高三模拟)一定条件下,在容积为10 L的固定容器中发生反
应:N (g)+3H(g ) 2NH (g) ΔH<0,反应过程如下图。下列说法正确的是
2 2 3
A.t min时,正、逆反应速率相等
1
B.曲线X表示NH 的物质的量随时间变化的关系
3
C.0~8 min,H 的化学反应速率v(H )=0.75 mol·L-1·min-1
2 2
D.10~12 min,N 的化学反应速率v(N )=0.25 mol·L-1·min-1
2 2
1.(广东省茂名市第一中学2023届高三下学期模拟)恒温恒容条件下,向密闭容器中加入一定量X,发生反
应:①X(g) Y(g);②Y(g) Z(g)。已知v=kc (反应物),k为速率常数,如图表明三种物质浓度随时间的变
化以及k受温度的影响。下列说法不正确的是
A.反应过程体系的压强始终不变
B.c(Y)随时间先增大后减小
C.随c(X)的减小,反应①、②的速率均逐渐降低
D.温度对反应②的k影响更大
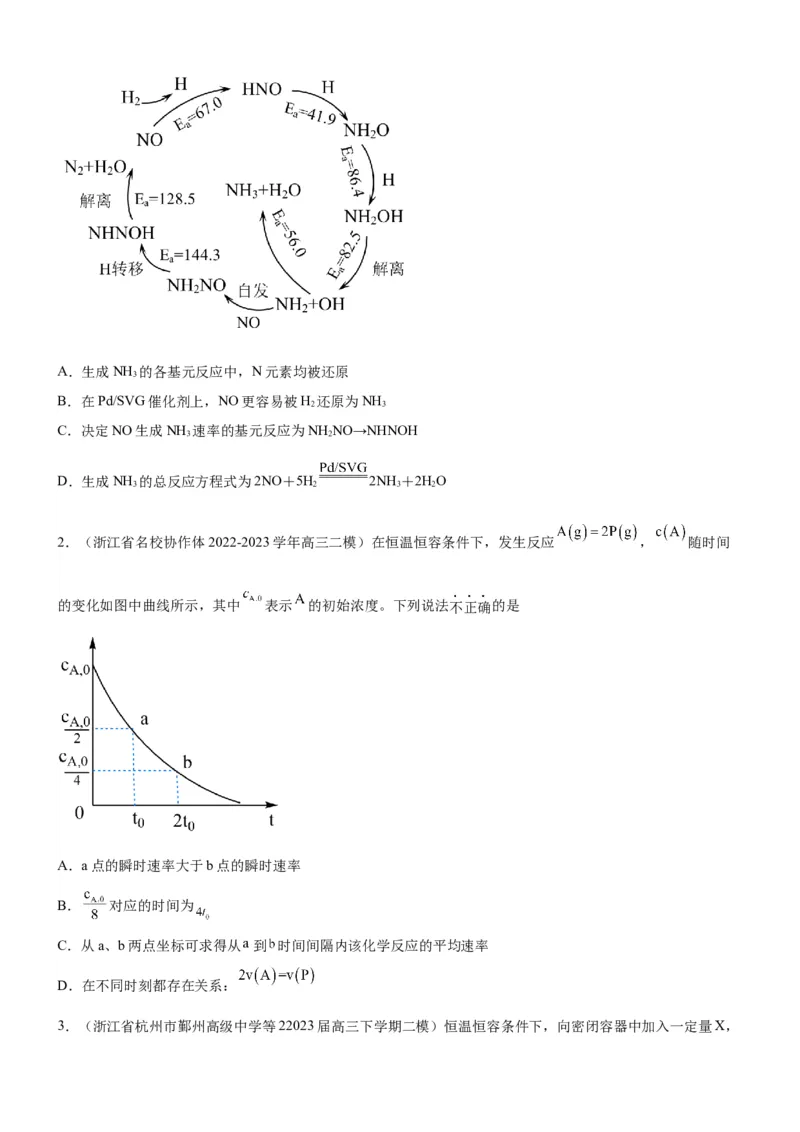
2.(湖南省长沙一中2023届高三联考)某温度下,向V L恒容密闭容器中通入4 mol X(g),发生反应:
①2X(g)=Y(g)+4Z(g),② 。反应体系中X、Y、Z的物质的量随时间t的变化曲线如图所示。下
列说法错误的是A.25 min时,气体X反应完全
B.0~10 min内,气体X的平均反应速率为
C.25 min时,向该体系中仅通入1 mol 后,反应②的平衡不发生移动(保持其他条件不变)
D.该温度下,反应②的平衡常数 Lmol
⋅
【基础过关】
1.(湖北省鄂东南省级示范高中教育教学改革联盟学校2022-2023学年联考)化学反应:
H实际上是经过两步基元反应完成的:第一步: ;第二步:……。该
△
反应过程的能量变化如图所示,下列说法不正确的是
A.第一步反应的逆反应的活化能是( )
B.第二步基元反应是:
C.分子有效碰撞几率最大的步骤对应的基元反应是第一步D.若使用催化剂,( )不会发生变化
2.(河北省深州市中学2022-2023学年高三期末)某清水河化工厂排出尾气(含CO、 )的治理方法:在密
闭容器中发生反应 ,CO、 在新型无机催化剂 表面进行两步基元反
应转化为无毒气体,其相对能量与反应历程的关系如图所示。下列说法正确的是
A.活化分子之间的碰撞一定是有效碰撞
B.两步反应均为放热反应,第一步反应活化能最大
C.新型无机催化剂 可有效提高CO、 的平衡转化率
D.基元反应的平衡常数越小,反应速率越慢
3.(广东省河源市第一中学2022-2023学年高三模拟) ,在
VO 存在时,该反应机理为:① (快);② (慢)。下列说法正确的
2 5
是
A.该反应速率主要由第①步基元反应决定
B.增大SO 的浓度可显著提高反应速率
2
C. VO 的存在提高该反应活化分子百分数,使有效碰撞次数增加,反应速率加快
2 5
D.该反应的逆反应的活化能为198kJ/mol
4.(天津市红桥区2022-2023学年度高三模拟)某反应过程的能量变化如图所示,下列说法不正确的是A.该反应为放热反应
B.曲线B为使用催化剂的反应历程,且包含多个基元反应
C.使用合适的催化剂可以降低反应的活化能
D.活化分子间发生的碰撞不一定是有效碰撞
5.(浙江省东阳市2023届高三下学期模拟)反应物(S)转化为产物(P或P·Z)的能量与反应进程的关系如下图所
示:
下列有关四种不同反应进程的说法正确的是
A.对于进程Ⅰ、Ⅱ,生成等量的P所吸收的热量相同
B.对于进程Ⅱ、Ⅲ,催化效率
C.对于进程Ⅰ,升高温度,正、逆反应速率均增大,但正反应速率增加更明显
D.对于进程Ⅳ,Z没有催化作用
6.(河北省邯郸市2023届高考第三次模拟)在某催化剂作用下,乙炔选择性加成反应C H(g)+H(g) C H(g)
2 2 2 2 4
ΔH<0。速率方程为v =k c(C H)c(H),v =k c(C H)(k 、k 为速率常数,只与温度、催化剂有关⇌)。一定温
正 正 2 2 2 逆 逆 2 4 正 逆
度下,在2L恒容密闭容器中充入1molC H(g)和1molH (g),只发生上述反应。测得C H 的物质的量如下表所
2 2 2 2 4
示:
t/min 0 5 10 15 20
n/mol 0 0.3 0.5 0.6 0.6
下列说法错误的是
A.0~10min内,v(H )=0.025mol・L-1・min-1
2
B.升高温度,k 增大的倍数小于k 增大的倍数
正 逆
C.净反应速率(v -v )由大到小最终等于0
正 逆
D.在上述条件下,15min时2k =15k
逆 正
7.(北京市朝阳区2023届高三下学期三模)利用有机分子模拟生物体内“醛缩酶”催化Diels-Alder反应取得
重要进展,荣获2021年诺贝尔化学奖。某Diels-Alder反应催化机理如下,下列说法不正确的是A.总反应为加成反应
B.化合物X为
C.Ⅵ是反应的催化剂
D.其它条件不变,温度越高,反应速率越快
8.(海南省海口市2023届高三下学期一模)最近,中科院大连化物所研究发现了以Cu-ZnZr三元氧化物为催
化剂时,CO 加氢制甲醇的反应机理如图所示(带*微粒为催化剂表面的吸附物种):
2
下列判断错误的是
A.CO 是该反应的氧化剂
2
B.生成的CHOH可用作车用燃料
3
C.催化剂能加快反应速率,但不改变反应的反应热
D.该反应过程中既有非极性键的断裂,又有非极性键的形成
【能力提升】
1.(湖南省永州市第一中学2022-2023学年高三模拟)中国科学家研究在Pd/SVG催化剂上H 还原NO生成N
2 2
和NH 的路径,各基元反应及活化能E(kJ·mol-1)如图所示,下列说法错误的是
3 aA.生成NH 的各基元反应中,N元素均被还原
3
B.在Pd/SVG催化剂上,NO更容易被H 还原为NH
2 3
C.决定NO生成NH 速率的基元反应为NH NO→NHNOH
3 2
D.生成NH 的总反应方程式为2NO+5H 2NH +2HO
3 2 3 2
2.(浙江省名校协作体2022-2023学年高三二模)在恒温恒容条件下,发生反应 , 随时间
的变化如图中曲线所示,其中 表示 的初始浓度。下列说法不正确的是
A.a点的瞬时速率大于b点的瞬时速率
B. 对应的时间为
C.从a、b两点坐标可求得从 到 时间间隔内该化学反应的平均速率
D.在不同时刻都存在关系:
3.(浙江省杭州市鄞州高级中学等22023届高三下学期二模)恒温恒容条件下,向密闭容器中加入一定量X,发生反应的方程式为①X Y;②Y Z。反应①的速率v=kc(X),反应②的速率v=k(Y),式中k、k 为速
1 1 2 2 1 2
率常数。图甲为该体系中X、Y、Z浓度随时间变化的曲线,图乙为反应①和②的lnk~ 曲线。下列说法不正确
的是
A.随c(X)的减小,反应①②的速率均降低
B.体系中当Y的浓度达到最大值后,v(X) + v(Y) = v(Z)
C.欲提高Y的产率,需提高反应温度且控制反应时间
D.温度低于T 时,总反应速率由反应②决定
1
4.(浙江省金丽衢十二校2022-2023学年高三第一次联考)用CH 还原SO 不仅可以消除污染,而且可以得到
4 2
单质S,反应如下: t℃时,在容积为2L的恒容密闭容器
中测的反应在不同时刻各物质的物质的量如下表:
物质的量(mol)时间(min)
0 2 4 6 8 10
物质
SO 4.8 2.64 1.8 1.8 2.1 2.1
2
CO 0 1.08 1.5 1.5 1.75 1.75
2
下列说法不正确的是
A.前2min的平均反应速率v(CH)=0.27mol·L-1·min-1
4
B.6min时SO 的转化率等于10min时SO 的转化率
2 2
C.其它条件不变,在第10min后降低温度,可使容器中的CO 的浓度升高到1.4mol·L-1
2
D.向容器内通入适量的HS,会使平衡逆向移动
2
5.(山东省淄博市部分学校2023届高三下学期二模)某温度下,在金表面发生反应:
,其速率方程式为 (k为速率常数)。反应过程中, 与S(催化剂)及
时间关系如图所示。已知 (半衰期)为反应物消耗一半所用的时间,下列叙述错误的是A. ,Ⅰ条件下
B.其他条件相同,S(催化剂)越大,k越大
C.其他条件相同, 增大,反应速率不变
D.该温度下,当S(催化剂) , 时, 为
6.(河北省保定市2023届一模)已知 的速率方程为 。
,为探究反应速率与 的关系,进行如下实验:向锥形瓶中加入一定体积(V)的2.0
molL 溶液、2.0 molL 溶液、1.0 molL 醋酸和水,充分搅拌,保持体系温度为36℃,用
⋅ ⋅ ⋅
秒表测量收集1.0 mL 所需要的时间(t),实验数据如下表。下列说法正确的是
V/mL
实验 t/s
溶 醋
溶液 水
液 酸
1 4.0 4.0 8.0 332
2 6.0 4.0 4.0 6.0 148
3 4.0 4.0 4.0 83
4 12.0 4.0 4.0 37
A. ;
B.实验3用 表示的反应平均速率 mol·sC.醋酸不参与反应,其浓度的大小对该反应速率无影响
D.速率方程中
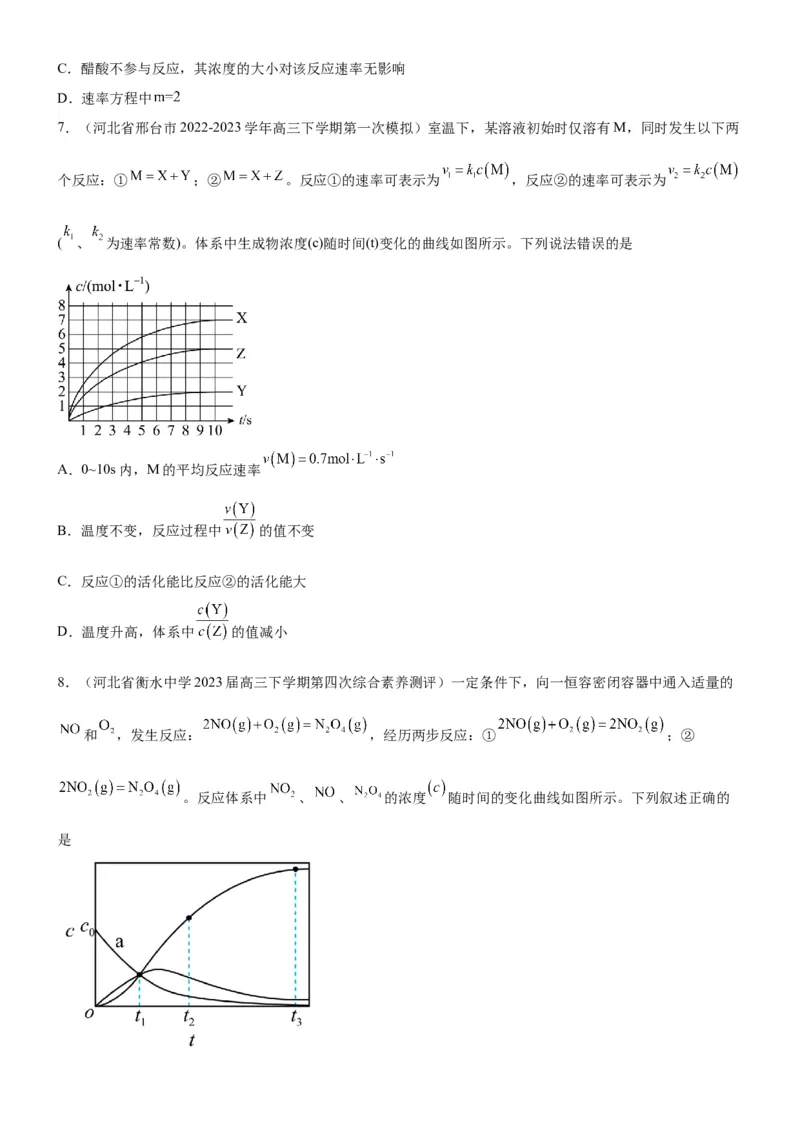
7.(河北省邢台市2022-2023学年高三下学期第一次模拟)室温下,某溶液初始时仅溶有M,同时发生以下两
个反应:① ;② 。反应①的速率可表示为 ,反应②的速率可表示为
( 、 为速率常数)。体系中生成物浓度(c)随时间(t)变化的曲线如图所示。下列说法错误的是
A.0~10s内,M的平均反应速率
B.温度不变,反应过程中 的值不变
C.反应①的活化能比反应②的活化能大
D.温度升高,体系中 的值减小
8.(河北省衡水中学2023届高三下学期第四次综合素养测评)一定条件下,向一恒容密闭容器中通入适量的
和 ,发生反应: ,经历两步反应:① ;②
。反应体系中 、 、 的浓度 随时间的变化曲线如图所示。下列叙述正确的
是A.曲线a是 随时间 的变化曲线
B. 时,
C. 时, 的生成速率大于消耗速率
D. 时,
【真题感知】
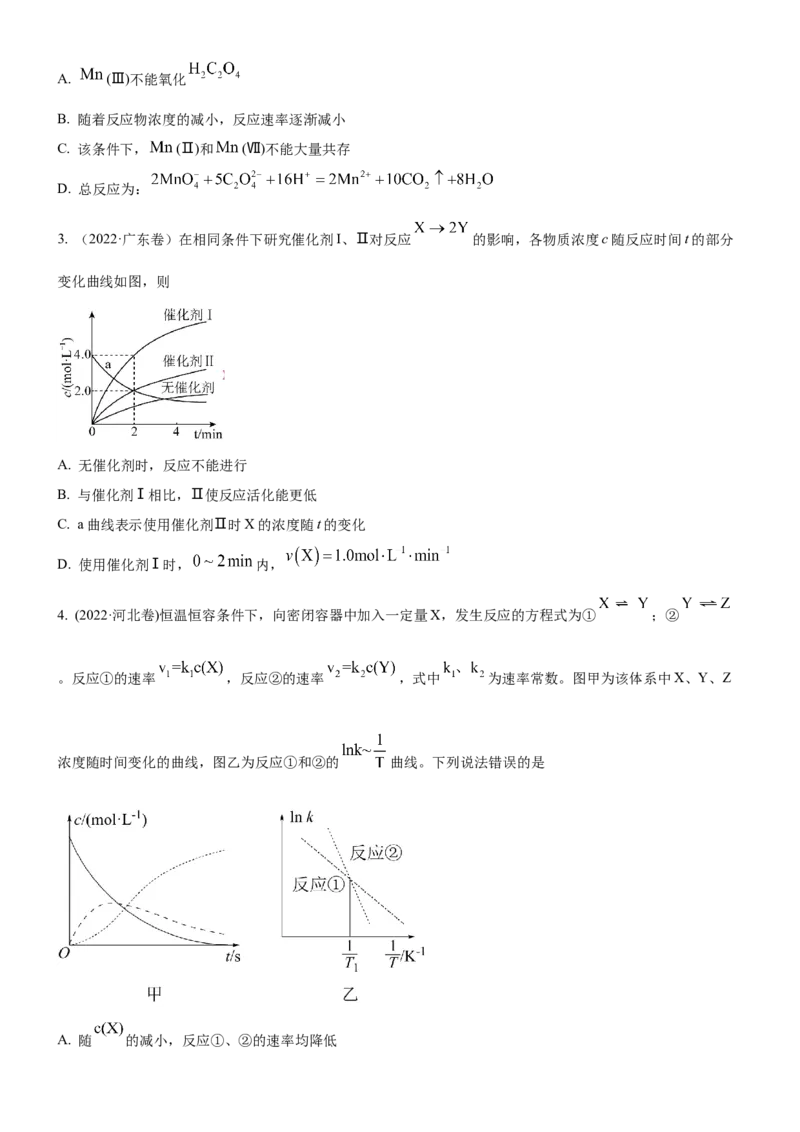
1. (2023·海南卷)工业上苯乙烯的生产主要采用乙苯脱氢工艺:
。某条件下无催化剂存在时,该反应的正、逆反应速率v随
时间t的变化关系如图所示。下列说法正确的是
A. 曲线①表示的是逆反应的 关系
B. 时刻体系处于平衡状态
C. 反应进行到 时, ( 为浓度商)
D. 催化剂存在时, 、 都增大
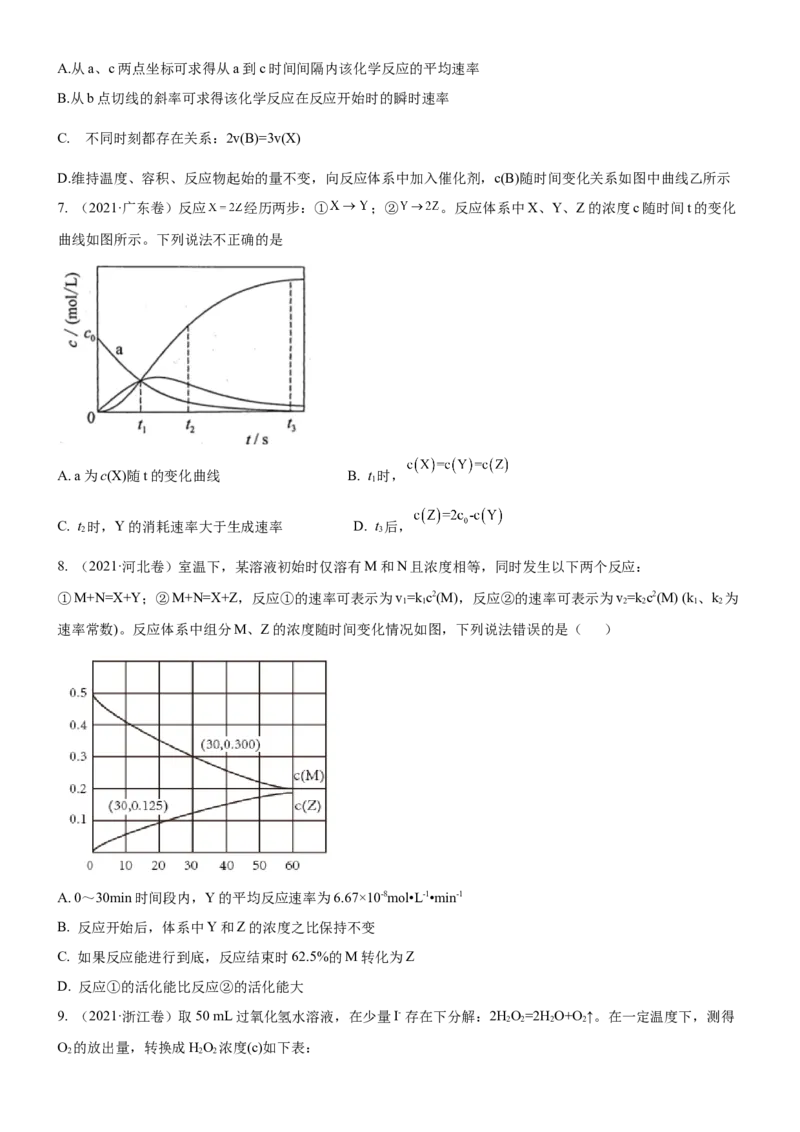
2.(2023·辽宁卷)一定条件下,酸性 溶液与 发生反应, (Ⅱ)起催化作用,过程中不同价
态含 粒子的浓度随时间变化如下图所示。下列说法正确的是( )A. (Ⅲ)不能氧化
B. 随着反应物浓度的减小,反应速率逐渐减小
C. 该条件下, (Ⅱ)和 (Ⅶ)不能大量共存
D. 总反应为:
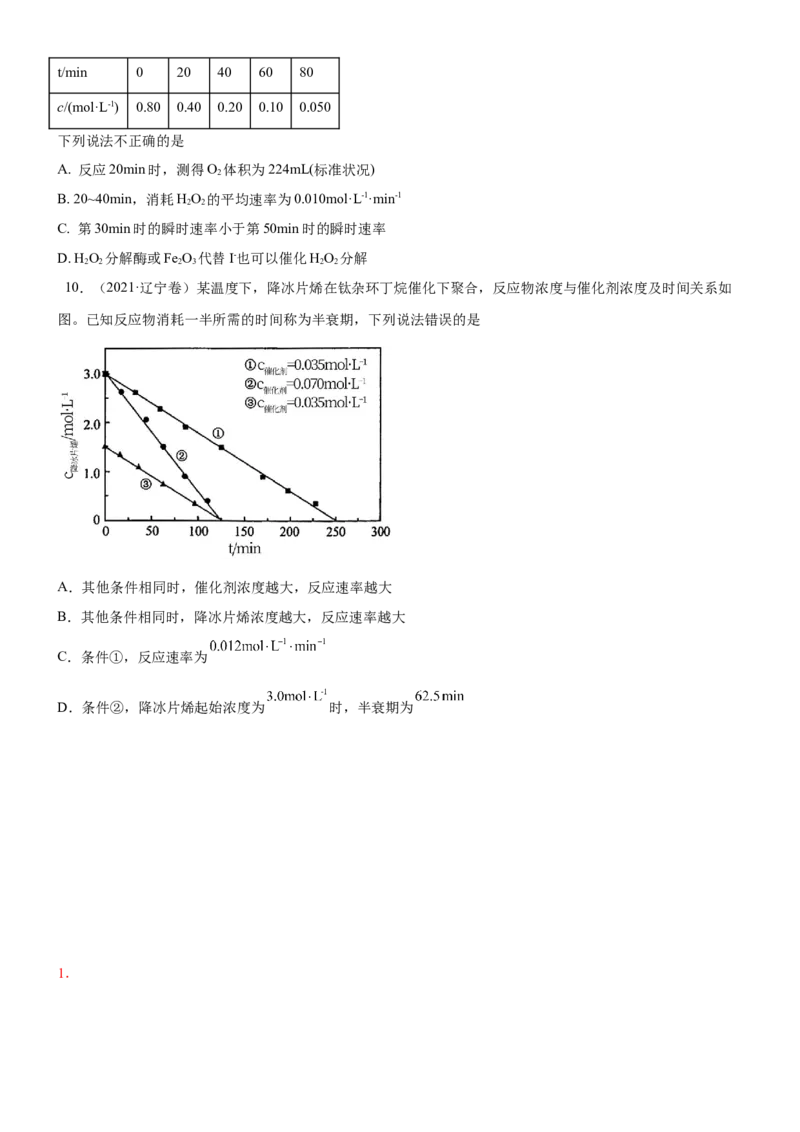
3. (2022·广东卷)在相同条件下研究催化剂I、Ⅱ对反应 的影响,各物质浓度c随反应时间t的部分
变化曲线如图,则
A. 无催化剂时,反应不能进行
B. 与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C. a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D. 使用催化剂Ⅰ时, 内,
4. (2022·河北卷)恒温恒容条件下,向密闭容器中加入一定量X,发生反应的方程式为① ;②
。反应①的速率 ,反应②的速率 ,式中 为速率常数。图甲为该体系中X、Y、Z
浓度随时间变化的曲线,图乙为反应①和②的 曲线。下列说法错误的是
A. 随 的减小,反应①、②的速率均降低B. 体系中
C. 欲提高Y的产率,需提高反应温度且控制反应时间
D. 温度低于 时,总反应速率由反应②决定
5. (2022·北京卷) 捕获和转化可减少 排放并实现资源利用,原理如图1所示。反应①完成之后,以
为载气,以恒定组成的 混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随
反应时间变化如图2所示。反应过程中始终未检测到 ,在催化剂上有积碳。
下列说法不正确的是
A. 反应①为 ;反应②为
B. , 比 多,且生成 速率不变,可能有副反应
C. 时刻,副反应生成 的速率大于反应②生成 速率
D. 之后,生成 的速率为0,是因为反应②不再发生
6.(2022·浙江卷)在恒温恒容条件下,发生反应A(s)+2B(g)3X(g),c(B)随时间的变化如图中曲线甲所示。下列
说法不正确的是A.从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率
B.从b点切线的斜率可求得该化学反应在反应开始时的瞬时速率
在
C. 不同时刻都存在关系:2v(B)=3v(X)
D.维持温度、容积、反应物起始的量不变,向反应体系中加入催化剂,c(B)随时间变化关系如图中曲线乙所示
7. (2021·广东卷)反应 经历两步:① ;② 。反应体系中X、Y、Z的浓度c随时间t的变化
曲线如图所示。下列说法不正确的是
A. a为c(X)随t的变化曲线 B. t 时,
1
C. t 时,Y的消耗速率大于生成速率 D. t 后,
2 3
8. (2021·河北卷)室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反应:
①M+N=X+Y;②M+N=X+Z,反应①的速率可表示为v=kc2(M),反应②的速率可表示为v=kc2(M) (k 、k 为
1 1 2 2 1 2
速率常数)。反应体系中组分M、Z的浓度随时间变化情况如图,下列说法错误的是( )
A. 0~30min时间段内,Y的平均反应速率为6.67×10-8mol•L-1•min-1
B. 反应开始后,体系中Y和Z的浓度之比保持不变
C. 如果反应能进行到底,反应结束时62.5%的M转化为Z
D. 反应①的活化能比反应②的活化能大
9. (2021·浙江卷)取50 mL过氧化氢水溶液,在少量I- 存在下分解:2HO=2H O+O↑。在一定温度下,测得
2 2 2 2
O 的放出量,转换成HO 浓度(c)如下表:
2 2 2t/min 0 20 40 60 80
c/(mol·L-1) 0.80 0.40 0.20 0.10 0.050
下列说法不正确的是
A. 反应20min时,测得O 体积为224mL(标准状况)
2
B. 20~40min,消耗HO 的平均速率为0.010mol·L-1·min-1
2 2
C. 第30min时的瞬时速率小于第50min时的瞬时速率
D. H O 分解酶或Fe O 代替I-也可以催化HO 分解
2 2 2 3 2 2
10.(2021·辽宁卷)某温度下,降冰片烯在钛杂环丁烷催化下聚合,反应物浓度与催化剂浓度及时间关系如
图。已知反应物消耗一半所需的时间称为半衰期,下列说法错误的是
A.其他条件相同时,催化剂浓度越大,反应速率越大
B.其他条件相同时,降冰片烯浓度越大,反应速率越大
C.条件①,反应速率为
D.条件②,降冰片烯起始浓度为 时,半衰期为
1.