文档内容
考点 21 化学反应速率
【基础过关】
1.下列有关化学反应速率的认识中错误的是( )
①可以测定某一反应的瞬时速率
②只能用单位时间内物质的量浓度变化值表示
③反应速率越快的反应其现象越明显
④溶液中发生的反应,速率的快慢主要由温度、浓度决定
A.只有① B.只有①② C.只有③④ D.均错误
【答案】D
【解析】①测定某一反应一段时间内的的平均速率,故①错误;②不仅可以用单位时间内物质的量浓
度变化值表示,还可以用单位时间内其他改变量来表示,故②错误;③反应速率越快的反应其现象可能不
明显,比如酸碱中和反应,故③错误;④溶液中发生的反应,速率的快慢主要物质本身性质决定,温度、
浓度仅仅是一个影响因素,故④错误;因此①②③④错误。故选D。
2.在容积为2L的密闭容器中进行如下反应:A(s)+2B(g) 3C(g)+nD(g),开始时A为4mol,B为
6mol;5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.1 mol/(L·min)。下列说法
错误的是( )
A.前5min内用A表示的化学反应速率v(A)为0.1mol/(L·min)
B.化学方程式中n值为1
C.反应达到平衡时3v (B)=2v (C)
正 逆
D.此反应在两种不同情况下的速率分别表示为:①v(B)=6 mol/(L·min),②v(D)=4.5 mol/(L·min),其
中反应速率快的是②
【答案】A
【解析】A项,A 为固体,不能用浓度变化表示化学反应速率,A错误;B项,
n(C) : n(D)=3: 1,为方程式化学计量系数比,B正确;C项,平衡时正反应速率等于逆反应速率,不同
物质表示速率等于计量数之比 ,C正确;D项,当v(D)=4.5 mol/(L·min),若用B的浓度变化表
示应为v(B)=4.5× 2=9 mol/(L ·min),D正确;故选A。
3.取 过氧化氢水溶液,在少量I-存在下分解:2HO=2H O+O↑。在一定温度下,测得O 的放出
2 2 2 2 2
资料整理【淘宝店铺:向阳百分百】量,转换成c(H O)如下表:
2 2
0 20 40 60 80
c(mol·L-1) 0.80 0.40 0.20 0.10 0.050
下列说法正确的是( )
A.反应 时,测得O 为
2
B. ,消耗HO 的平均速率为
2 2
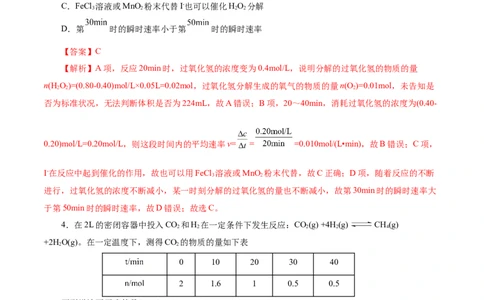
C.FeCl 溶液或MnO 粉末代替I-也可以催化HO 分解
3 2 2 2
D.第 时的瞬时速率小于第 时的瞬时速率
【答案】C
【解析】A项,反应20min时,过氧化氢的浓度变为0.4mol/L,说明分解的过氧化氢的物质的量
n(H O)=(0.80-0.40)mol/L×0.05L=0.02mol,过氧化氢分解生成的氧气的物质的量n(O )=0.01mol,未告知是
2 2 2
否为标准状况,无法判断体积是否为224mL,故A错误;B项,20~40min,消耗过氧化氢的浓度为(0.40-
0.20)mol/L=0.20mol/L,则这段时间内的平均速率v= = =0.010mol/(L•min),故B错误;C项,
I-在反应中起到催化的作用,故也可以用FeCl 溶液或MnO 粉末代替,故C正确;D项,随着反应的不断
3 2
进行,过氧化氢的浓度不断减小,某一时刻分解的过氧化氢的量也不断减小,故第30min时的瞬时速率大
于第50min时的瞬时速率,故D错误;故选C。
4.在2L的密闭容器中投入CO 和H 在一定条件下发生反应:CO(g) +4H (g) CH(g)
2 2 2 2 4
+2H O(g)。在一定温度下,测得CO 的物质的量如下表
2 2
0 10 20 30 40
2 1.6 1 0.5 0.5
下列说法不正确的是( )
A.反应20min时,测得CH 体积为22.4L(标准状况)
4
B. ,生成HO(g)的平均速率为
2
C.第15min时的瞬时速率大于第25min时的瞬时速率
D.第30min时反应到达平衡
【答案】D
【解析】A项,反应20min时,测得CO 为1mol,则消耗CO、生成CH 均为1mol,CH 体积为
2 2 4 4
资料整理【淘宝店铺:向阳百分百】22.4L(标准状况),A正确;B项,20~40min,测得CO 从1mol变为0.5mol,则消耗CO0.5mol、生成
2 2
HO(g)为1mol,生成HO(g)的平均速率为 ,B正确;C项,其它条
2 2
件相同、反应物的浓度越大则反应速率越快, 第15min时反应物的浓度大于第25min时的浓度,则第
15min时瞬时速率大于第25min时的瞬时速率,C正确;D项,由图知第30min时的二氧化碳含量已不再
变化、则反应已经处于平衡状态,D不正确;故选D。
5.乙醛在少量 存在下分解反应为 。某温度下,测得CHCHO的浓
3
度变化情况如下表:
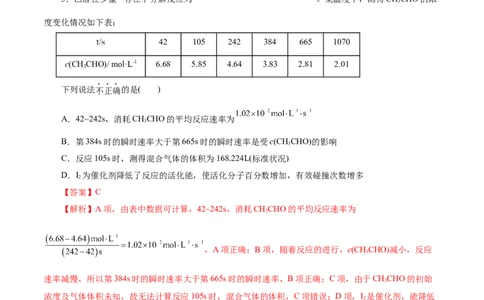
42 105 242 384 665 1070
c(CHCHO)/ mol·L-1 6.68 5.85 4.64 3.83 2.81 2.01
3
下列说法不正确的是( )
A.42~242s,消耗CHCHO的平均反应速率为
3
B.第384s时的瞬时速率大于第665s时的瞬时速率是受c(CHCHO)的影响
3
C.反应105s时,测得混合气体的体积为168.224L(标准状况)
D.I 为催化剂降低了反应的活化能,使活化分子百分数增加,有效碰撞次数增多
2
【答案】C
【解析】A项,由表中数据可计算,42~242s,消耗CHCHO的平均反应速率为
3
,A项正确;B项,随着反应的进行,c(CHCHO)减小,反应
3
速率减慢,所以第384s时的瞬时速率大于第665s时的瞬时速率,B项正确;C项,由于CHCHO的初始
3
浓度及气体体积未知,故无法计算反应105s时,混合气体的体积,C项错误;D项,I 是催化剂,能降低
2
反应的活化能,使活化分子百分数增加,有效碰撞次数增多,提高反应速率,D项正确;故选C。
6.(2023·福建省莆田市场高三毕业班第四次教学质量检测)工业上在VO 催化作用下生产SO 的反应
2 5 3
为2SO (g)+ O (g) 2SO (g) ΔH=-198 kJ·mol-1,该反应可看作两步:①VO+SO→2VO +SO
2 2 3 2 5 2 2 3
(快);②4VO +O →2VO (慢)。下列说法正确的是
2 2 2 5
A.该反应活化能为
B.减小O 的浓度能降低SO 的生成速率
2 3
C.VO 的存在使有效碰撞次数增加,降低了该反应的焓变
2 5
资料整理【淘宝店铺:向阳百分百】D.①的活化能一定大于②的活化能
【答案】B
【解析】A项,ΔH=正反应的活化能-逆反应的活化能=-198kJ/mol,所以逆反应的活化能大于198kJ/
mol,故A错误;B项,慢反应是决速步,O 是慢反应的反应物,减小O 的浓度会降低正反应速率,降低
2 2
SO 的生成速率,故B正确;C项,VO 是催化剂,催化剂不能改变反应的焓变,故C错误;D项,反应
3 2 5
①是快反应,反应②是慢反应,活化能越小反应越快,①的活化能小于②的活化能,故D错误;故选B。
7.(2023·山东省泰安市三模)已知2NO (g) 2N (g)+ O (g)的速率方程为 (k为速率
2 2 2
常数,只与温度、催化剂有关)。实验测得,NO在催化剂X表面反应的变化数据如下:
2
2 5
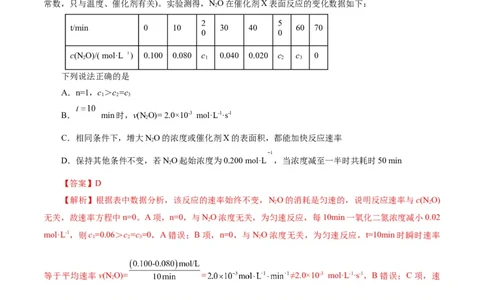
t/min 0 10 30 40 60 70
0 0
c(N O)/( mol·L ) 0.100 0.080 c 0.040 0.020 c c 0
2 1 2 3
下列说法正确的是
A.n=1,c>c=c
1 2 3
B. min时,v(N O)= 2.0×10-3 mol·L-1·s-1
2
C.相同条件下,增大NO的浓度或催化剂X的表面积,都能加快反应速率
2
D.保持其他条件不变,若NO起始浓度为0.200 mol·L ,当浓度减至一半时共耗时50 min
2
【答案】D
【解析】根据表中数据分析,该反应的速率始终不变,NO的消耗是匀速的,说明反应速率与c(N O)
2 2
无关,故速率方程中n=0。A项,n=0,与NO浓度无关,为匀速反应,每10min一氧化二氮浓度减小0.02
2
mol·L-1,则c=0.06>c=c =0,A错误;B项,n=0,与NO浓度无关,为匀速反应,t=10min时瞬时速率
1 2 3 2
等于平均速率v(N O)= = ≠2.0×10-3 mol·L-1·s-1,B错误;C项,速
2
率方程中n=0,反应速率与NO的浓度无关,C错误;D项,保持其他条件不变,该反应的反应速率不变,
2
即为 ,若起始浓度 0.200 mol·L ,减至一半时所耗时间为
=50min,D正确;故选D。
8.NaNO 溶液和NHCl溶液可发生反应:NaNO +NHCl=NaCl+N ↑+2H O,为探究反应速率与
2 4 2 4 2 2
c(NaNO )的关系,进行如下实验:常温常压下,向锥形瓶中加入一定体积(V)的2.0mol·L-1 NaNO 溶液、
2 2
资料整理【淘宝店铺:向阳百分百】2.0mol·L-1NHCl溶液和水,充分搅拌。控制体系温度,再通过分液漏斗向锥形瓶中加入1.0 醋酸。
4
当导管口气泡均匀稳定冒出时,开始用排水法收集气体。用秒表测量收集1.0mLN 所需要的时间(t)。实验
2
数据如下表。下列说法正确的是( )
V/mL
NaNO 溶液 NHCl溶液 醋酸 水
2 4
1 4.0 V 4.0 8.0 334
1
2 V 4.0 4.0 V 150
2 3
3 8.0 4.0 4.0 4.0 83
4 12.0 4.0 4.0 0.0 38
A.实验3用 表示的反应平均速率
B.若实验4从反应开始到反应结束历时bs,则用NHCl表示的反应平均速率
4
C.V=4.0;若V=6.0,则V=6.0
1 2 3
D.醋酸的作用是加快反应速率,改变其浓度对该反应速率无影响
【答案】C
【解析】A项,实验在常温常压下进行,不是标准状况,故气体摩尔体积不为22.4L/mol,故速率不是
,故A错误;B项,实验4开始时NH Cl的浓度为 =0.4mol/L,从反应开
4
始到反应结束历时bs,则用NH Cl表示的反应平均速率 ,故B错误;C项,根据实验3、
4
4可知,溶液的总体积为20.0mL,则V=20.0—4.0-4.0-8.0=4.0;若V=6.0,V=20.0-4.0-4.0-6.0=6.0,故C
1 2 3
正确;D项,醋酸的作用是加快反应速率,增大浓度该反应速率加快,故D错误;故选C。
9.以反应 5HC O+2MnO -+6H+ = 10CO↑+ 2Mn2+ + 8H O 为例探究“外界条件对化学反应速率的
2 2 4 4 2 2
影响”。实验时,分别量取 H2C2O 溶液和酸性 KMnO 溶液,迅速混合并开始计时,通过测定溶液褪色
4 4
所需时间来判断反应的快慢。
资料整理【淘宝店铺:向阳百分百】下列说法不正确的是( )
A.实验①、 ②、 ③所加的HC O 溶液均要过量
2 2 4
B.若实验①测得 KMnO 溶液的褪色时间为 40 s,则这段时间内平均反应速率 v(KMnO)= 2. 5×10-
4 4
4 mol/L/s
C.实验①和实验②是探究浓度对化学反应速率的影响,实验②和③是探究温度对化学反应速率的影
响
D.实验①和②起初反应均很慢,过了一会儿速率突然增大,可能是生成的 Mn2+对反应起催化作用
【答案】B
【解析】A项,根据反应方程式可得5HC O~2MnO-,由实验数据分析可知,在这三个实验中,所加
2 2 4 4
HC O 溶液均过量,A 正确;B 项,根据已知数据可得 v(KMnO)=0.010mol/L×0.004L/40s =1.0×10-6
2 2 4 4
mol/L/s,B错误;C项,分析表中数据可知,实验①和实验②只是浓度不同,实验②和③只是温度不同,
C是正确的;D项,在其它条件都相同时,开始速率很小,过一会儿速率突然增大,说明反应生成了具有
催化作用的物质,其中水没有这种作用,CO 释放出去了,所以可能起催化作用的是Mn2+,故D正确。故
2
选B。
10.取 过氧化氢水溶液,在少量 存在下分解,2HO=2H O+O↑。在一定温度下,测得 的放
2 2 2 2
出量,转换成 浓度(c)如下表:
0 20 40 60 80
0.80 0.40 0.20 0.010 0.050
下列说法错误的是( )
A.第 时的瞬时速率小于第 时的瞬时速率
B. 和 都可代替 作HO 分解的催化剂
2 2
C.反应 时,测得O 体积为 (标准状况)
2
资料整理【淘宝店铺:向阳百分百】D. ,消耗HO 的平均速率为
2 2
【答案】A
【解析】A项,随着反应的不断进行,过氧化氢的浓度不断减小,某一时刻分解的过氧化氢的量也不
断减小,故第 时的瞬时速率大于第 时的瞬时速率,A错误;B项,I-在反应中起到的是催化作
用, 和 在该反应中也起到催化作用,故也可以利用 和 代替,B正确;C项,反应
时,过氧化氢的浓度变为 ,说明分解的过氧化氢的物质的量
,过氧化氢分解生成的氧气的物质的量 为 ,
标况下的体积 ,C正确;D项, ,消耗过氧化
氢的浓度为 ,则这段时间内的平均速率
,D正确;故选A。
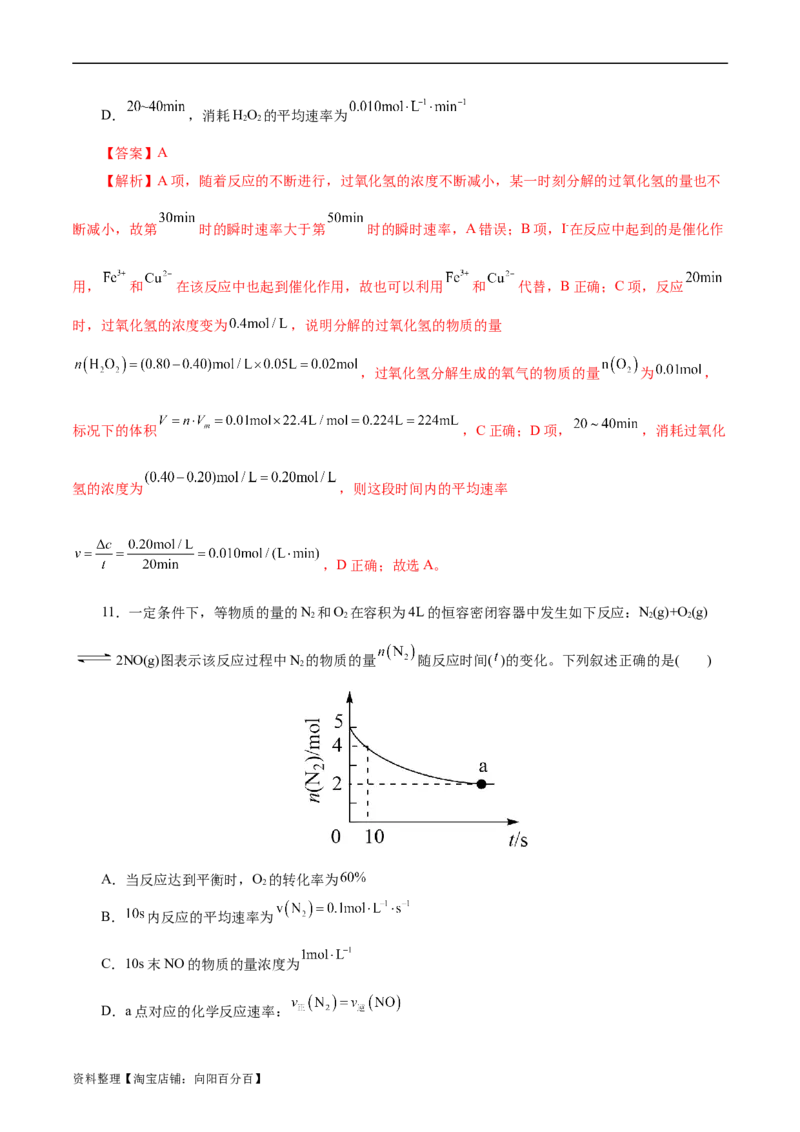
11.一定条件下,等物质的量的N 和O 在容积为4L的恒容密闭容器中发生如下反应:N(g)+O(g)
2 2 2 2
2NO(g)图表示该反应过程中N 的物质的量 随反应时间( )的变化。下列叙述正确的是( )
2
A.当反应达到平衡时,O 的转化率为
2
B. 内反应的平均速率为
C.10s末NO的物质的量浓度为
D.a点对应的化学反应速率:
资料整理【淘宝店铺:向阳百分百】【答案】A
【解析】A项,根据图示,当反应达到平衡时,氮气的物质的量由5mol变为2mol,N 和O 的投料相
2 2
等,则O 的转化率为 ,故A正确;B项,10s内氮气的物质的量由5mol变为4mol,反
2
应的平均速率为 ,故B错误; C项,10s内消耗1mol氮气,10s末NO
的物质的量是2mol,NO的浓度为 ,故C错误;D项,a点反应达到平衡状态,正逆反
应速率比等于系数比,对应的化学反应速率: ,故D错误;故选A。
12.(2023·安徽省卓越县中联盟高三第一次联考)一定温度下,在 恒容密闭容器中投入1 mol CO (g)
2
与4 mol H (g)制备CHOH(g),不考虑副反应,其物质的量随时间变化的关系如图所示:
2 3
下列说法中正确的是( )
A.该反应的化学方程式为CO(g)+3H(g) CHOH(g) +HO(g)
2 2 3 2
B.0~30min内,用H 表示的平均反应速率为0.05 mol·L-1·min-1
2
C.逆反应速率:a点大于b点
D.故选的平衡转化率是50%
【答案】D
【解析】从图可看出,物质的量随时间逐渐减少的两条曲线从上到下分别表示氢气和二氧化碳的变化
曲线,物质的量随时间逐渐增加的曲线表示甲醇的变化曲线,30min时达到平衡。A项,由图像可知该反
应有一定的限度,是可逆反应,故用“ ”表示,A错误;B项,0~30min内,用H 表示的平均反应
2
资料整理【淘宝店铺:向阳百分百】速率为 ,B错误;C项,反应未达到平衡之前,逆反应速率一直增大,C错
误;D项,CO 达到平衡时转化0.5mol,故平衡转化率是50%,D正确; 故选D。
2
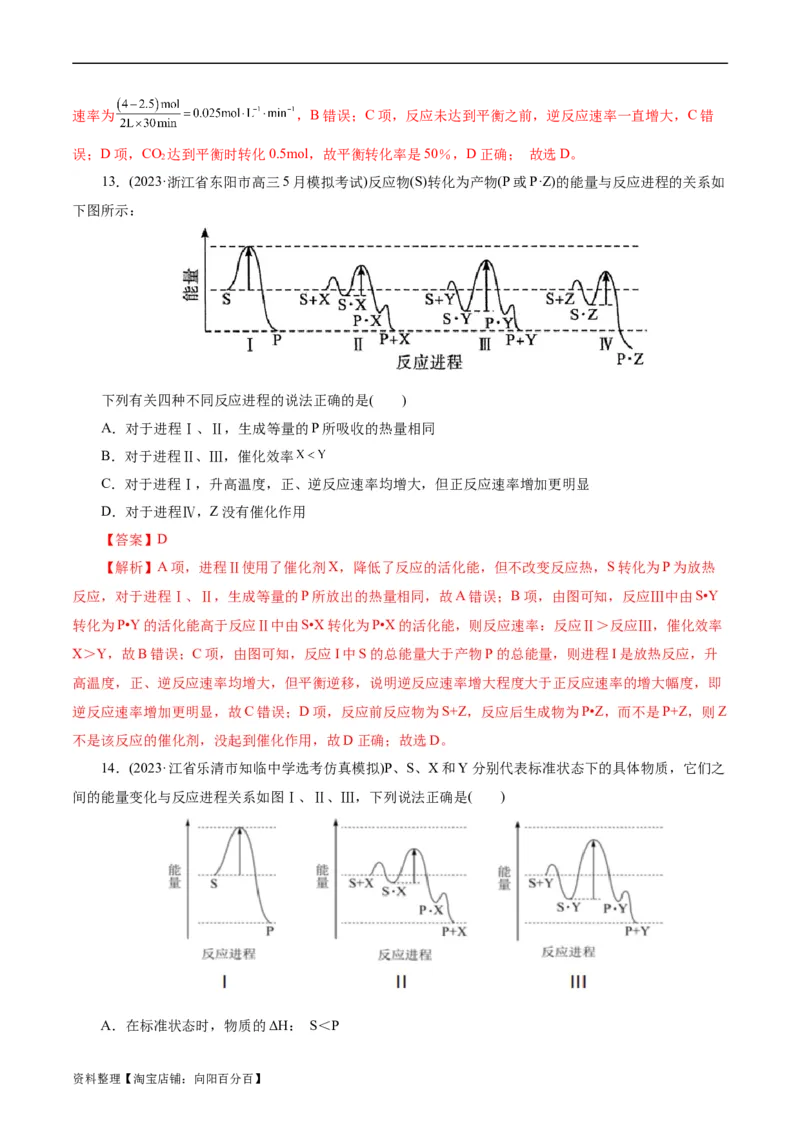
13.(2023·浙江省东阳市高三5月模拟考试)反应物(S)转化为产物(P或P·Z)的能量与反应进程的关系如
下图所示:
下列有关四种不同反应进程的说法正确的是( )
A.对于进程Ⅰ、Ⅱ,生成等量的P所吸收的热量相同
B.对于进程Ⅱ、Ⅲ,催化效率
C.对于进程Ⅰ,升高温度,正、逆反应速率均增大,但正反应速率增加更明显
D.对于进程Ⅳ,Z没有催化作用
【答案】D
【解析】A项,进程Ⅱ使用了催化剂X,降低了反应的活化能,但不改变反应热,S转化为P为放热
反应,对于进程Ⅰ、Ⅱ,生成等量的P所放出的热量相同,故A错误;B项,由图可知,反应Ⅲ中由S•Y
转化为P•Y的活化能高于反应Ⅱ中由S•X转化为P•X的活化能,则反应速率:反应Ⅱ>反应Ⅲ,催化效率
X>Y,故B错误;C项,由图可知,反应I中S的总能量大于产物P的总能量,则进程I是放热反应,升
高温度,正、逆反应速率均增大,但平衡逆移,说明逆反应速率增大程度大于正反应速率的增大幅度,即
逆反应速率增加更明显,故C错误;D项,反应前反应物为S+Z,反应后生成物为P•Z,而不是P+Z,则Z
不是该反应的催化剂,没起到催化作用,故D正确;故选D。
14.(2023·江省乐清市知临中学选考仿真模拟)P、S、X和Y分别代表标准状态下的具体物质,它们之
间的能量变化与反应进程关系如图Ⅰ、Ⅱ、Ⅲ,下列说法正确是( )
A.在标准状态时,物质的ΔH: S<P
资料整理【淘宝店铺:向阳百分百】B. 和 为催化剂,进程Ⅰ、Ⅱ、Ⅲ中:ΔH<ΔH<ΔH<0
1 2 3
C.反应S P达平衡所需时间:进程Ⅰ<Ⅱ<Ⅲ
D.反应S P平衡时 的产率:进程Ⅰ=Ⅱ=Ⅲ
【答案】D
【解析】A项,由图可知,进程Ⅰ为放热反应,在标准状态时,物质的ΔH:S>P,故A错误;B项,
催化剂不影响反应热的大小,X和Y为催化剂,故进程Ⅰ、Ⅱ、Ⅲ中:ΔH=ΔH =ΔH <0,故B错误;C
1 2 3
项,反应活化能越低,反应则越快,反应Ⅲ的活化能高于反应Ⅱ的活化能,则反应S P达平衡所需
时间:Ⅰ<Ⅲ<Ⅱ,故C错误;D项,催化剂不能使平衡发生移动,故反应S P平衡时生成P的量
一样多,则平衡时P的产率:进程Ⅰ=Ⅱ=Ⅲ,故D正确;故选D。
15.在恒温恒容的密闭容器中发生反应C(s)+2NO(g) CO(g)+N(g) ΔH (其中碳足量),反应体
2 2
系中CO(g)的浓度随时间的变化如表所示,下列说法中正确的是( )
2
反应时间 0 80 90 100 110
浓度
0.00 0.30 0.32 0.33 0.33
A.增加C的量可以加快反应速率
B.反应在100 s时刚好平衡
C.80~90 s之间的平均速率 , 之间的平均反应速率
D.反应平衡后升高温度,则NO的平衡转化率一定增大
【答案】C
【解析】A项,C是固体物质,其浓度不变,所以向反应容器中加入C的量,化学速率不会加快,A
错误;B项,反应在100 s后时CO(g)浓度不再发生变化,则在100℃时反应可能刚好平衡,也可能在90~
2
100℃时反应就已经达到了平衡状态,B错误;C项,反应在80~90 s之间△c(CO)=0.02 mol/L,则用CO
2 2
的浓度变化表示的平均速率v(CO)= ;反应在100 s反应已经达到了平衡状态,
2
物质的浓度不再发生变化,所以用CO 的浓度变化表示的平均速率v(CO)=0,C正确;D项,题目已知信
2 2
息不能确定该反应的热效应,所以不能确定温度对化学平衡移动的影响,反应平衡后升高温度,NO的平
衡转化率可能是增大也可能是减小,D错误;故选C。
资料整理【淘宝店铺:向阳百分百】