文档内容
考点 21 化学反应速率
【基础过关】
1.下列有关化学反应速率的认识中错误的是( )
①可以测定某一反应的瞬时速率
②只能用单位时间内物质的量浓度变化值表示
③反应速率越快的反应其现象越明显
④溶液中发生的反应,速率的快慢主要由温度、浓度决定
A.只有① B.只有①② C.只有③④ D.均错误
2.在容积为2L的密闭容器中进行如下反应:A(s)+2B(g) 3C(g)+nD(g),开始时A为4mol,B为
6mol;5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.1 mol/(L·min)。下列说法
错误的是( )
A.前5min内用A表示的化学反应速率v(A)为0.1mol/(L·min)
B.化学方程式中n值为1
C.反应达到平衡时3v (B)=2v (C)
正 逆
D.此反应在两种不同情况下的速率分别表示为:①v(B)=6 mol/(L·min),②v(D)=4.5 mol/(L·min),其
中反应速率快的是②
3.取 过氧化氢水溶液,在少量I-存在下分解:2HO=2H O+O↑。在一定温度下,测得O 的放出
2 2 2 2 2
量,转换成c(H O)如下表:
2 2
0 20 40 60 80
c(mol·L-1) 0.80 0.40 0.20 0.10 0.050
下列说法正确的是( )
A.反应 时,测得O 为
2
B. ,消耗HO 的平均速率为
2 2
C.FeCl 溶液或MnO 粉末代替I-也可以催化HO 分解
3 2 2 2
D.第 时的瞬时速率小于第 时的瞬时速率
4.在2L的密闭容器中投入CO 和H 在一定条件下发生反应:CO(g) +4H (g) CH(g)
2 2 2 2 4
+2H O(g)。在一定温度下,测得CO 的物质的量如下表
2 2
0 10 20 30 40
2 1.6 1 0.5 0.5
1下列说法不正确的是( )
A.反应20min时,测得CH 体积为22.4L(标准状况)
4
B. ,生成HO(g)的平均速率为
2
C.第15min时的瞬时速率大于第25min时的瞬时速率
D.第30min时反应到达平衡
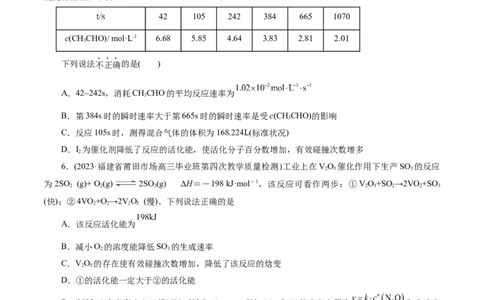
5.乙醛在少量 存在下分解反应为 。某温度下,测得CHCHO的浓
3
度变化情况如下表:
42 105 242 384 665 1070
c(CHCHO)/ mol·L-1 6.68 5.85 4.64 3.83 2.81 2.01
3
下列说法不正确的是( )
A.42~242s,消耗CHCHO的平均反应速率为
3
B.第384s时的瞬时速率大于第665s时的瞬时速率是受c(CHCHO)的影响
3
C.反应105s时,测得混合气体的体积为168.224L(标准状况)
D.I 为催化剂降低了反应的活化能,使活化分子百分数增加,有效碰撞次数增多
2
6.(2023·福建省莆田市场高三毕业班第四次教学质量检测)工业上在VO 催化作用下生产SO 的反应
2 5 3
为2SO (g)+ O (g) 2SO (g) ΔH=-198 kJ·mol-1,该反应可看作两步:①VO+SO→2VO +SO
2 2 3 2 5 2 2 3
(快);②4VO +O →2VO (慢)。下列说法正确的是
2 2 2 5
A.该反应活化能为
B.减小O 的浓度能降低SO 的生成速率
2 3
C.VO 的存在使有效碰撞次数增加,降低了该反应的焓变
2 5
D.①的活化能一定大于②的活化能
7.(2023·山东省泰安市三模)已知2NO (g) 2N (g)+ O (g)的速率方程为 (k为速率
2 2 2
常数,只与温度、催化剂有关)。实验测得,NO在催化剂X表面反应的变化数据如下:
2
2 5
t/min 0 10 30 40 60 70
0 0
c(N O)/( mol·L ) 0.100 0.080 c 0.040 0.020 c c 0
2 1 2 3
下列说法正确的是
A.n=1,c>c=c
1 2 3
2B. min时,v(N O)= 2.0×10-3 mol·L-1·s-1
2
C.相同条件下,增大NO的浓度或催化剂X的表面积,都能加快反应速率
2
D.保持其他条件不变,若NO起始浓度为0.200 mol·L ,当浓度减至一半时共耗时50 min
2
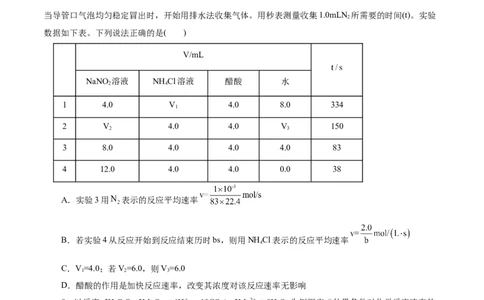
8.NaNO 溶液和NHCl溶液可发生反应:NaNO +NHCl=NaCl+N ↑+2H O,为探究反应速率与
2 4 2 4 2 2
c(NaNO )的关系,进行如下实验:常温常压下,向锥形瓶中加入一定体积(V)的2.0mol·L-1 NaNO 溶液、
2 2
2.0mol·L-1NHCl溶液和水,充分搅拌。控制体系温度,再通过分液漏斗向锥形瓶中加入1.0 醋酸。
4
当导管口气泡均匀稳定冒出时,开始用排水法收集气体。用秒表测量收集1.0mLN 所需要的时间(t)。实验
2
数据如下表。下列说法正确的是( )
V/mL
NaNO 溶液 NHCl溶液 醋酸 水
2 4
1 4.0 V 4.0 8.0 334
1
2 V 4.0 4.0 V 150
2 3
3 8.0 4.0 4.0 4.0 83
4 12.0 4.0 4.0 0.0 38
A.实验3用 表示的反应平均速率
B.若实验4从反应开始到反应结束历时bs,则用NHCl表示的反应平均速率
4
C.V=4.0;若V=6.0,则V=6.0
1 2 3
D.醋酸的作用是加快反应速率,改变其浓度对该反应速率无影响
9.以反应 5HC O+2MnO -+6H+ = 10CO↑+ 2Mn2+ + 8H O 为例探究“外界条件对化学反应速率的
2 2 4 4 2 2
影响”。实验时,分别量取 H2C2O 溶液和酸性 KMnO 溶液,迅速混合并开始计时,通过测定溶液褪色
4 4
所需时间来判断反应的快慢。
3下列说法不正确的是( )
A.实验①、 ②、 ③所加的HC O 溶液均要过量
2 2 4
B.若实验①测得 KMnO 溶液的褪色时间为 40 s,则这段时间内平均反应速率 v(KMnO)= 2. 5×10-
4 4
4 mol/L/s
C.实验①和实验②是探究浓度对化学反应速率的影响,实验②和③是探究温度对化学反应速率的影
响
D.实验①和②起初反应均很慢,过了一会儿速率突然增大,可能是生成的 Mn2+对反应起催化作用
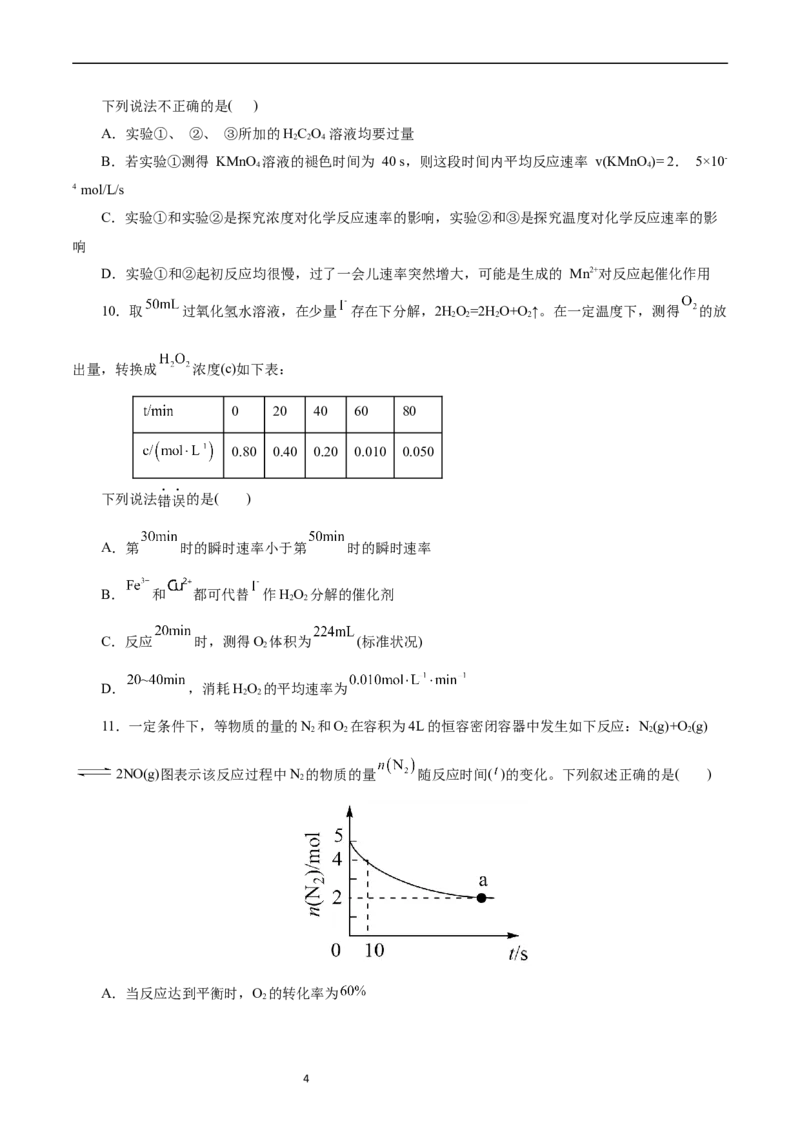
10.取 过氧化氢水溶液,在少量 存在下分解,2HO=2H O+O↑。在一定温度下,测得 的放
2 2 2 2
出量,转换成 浓度(c)如下表:
0 20 40 60 80
0.80 0.40 0.20 0.010 0.050
下列说法错误的是( )
A.第 时的瞬时速率小于第 时的瞬时速率
B. 和 都可代替 作HO 分解的催化剂
2 2
C.反应 时,测得O 体积为 (标准状况)
2
D. ,消耗HO 的平均速率为
2 2
11.一定条件下,等物质的量的N 和O 在容积为4L的恒容密闭容器中发生如下反应:N(g)+O(g)
2 2 2 2
2NO(g)图表示该反应过程中N 的物质的量 随反应时间( )的变化。下列叙述正确的是( )
2
A.当反应达到平衡时,O 的转化率为
2
4B. 内反应的平均速率为
C.10s末NO的物质的量浓度为
D.a点对应的化学反应速率:
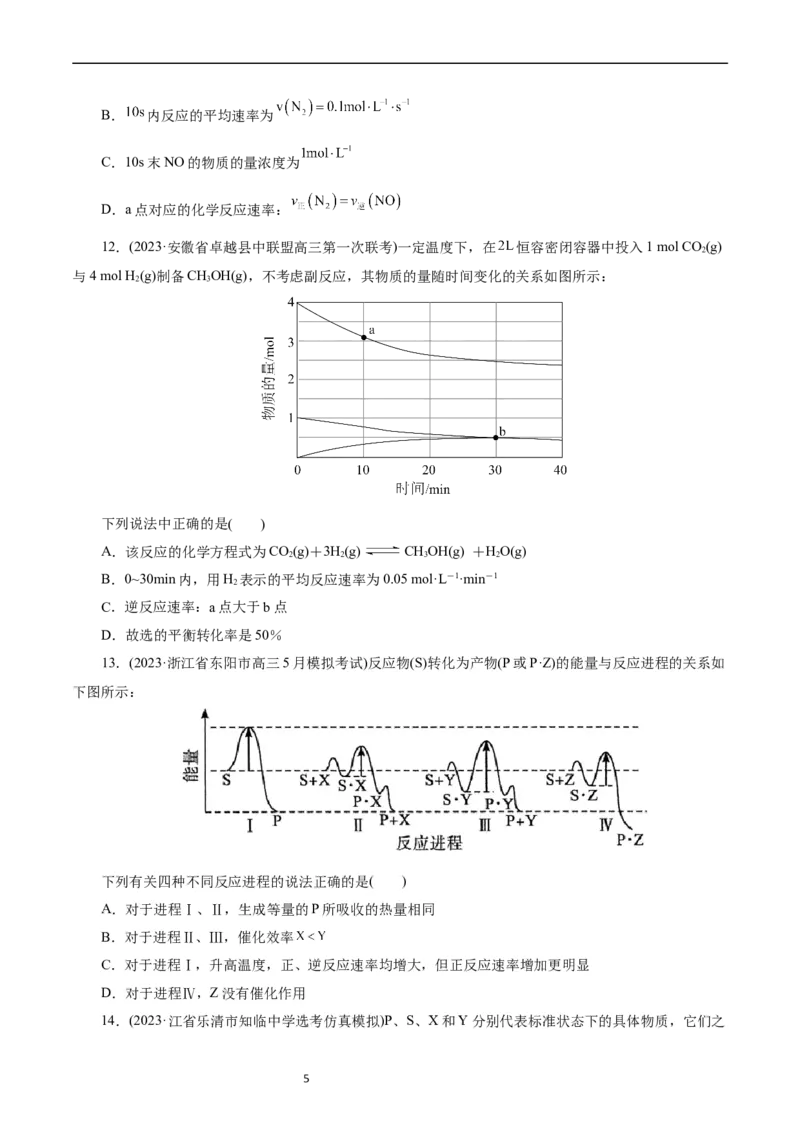
12.(2023·安徽省卓越县中联盟高三第一次联考)一定温度下,在 恒容密闭容器中投入1 mol CO (g)
2
与4 mol H (g)制备CHOH(g),不考虑副反应,其物质的量随时间变化的关系如图所示:
2 3
下列说法中正确的是( )
A.该反应的化学方程式为CO(g)+3H(g) CHOH(g) +HO(g)
2 2 3 2
B.0~30min内,用H 表示的平均反应速率为0.05 mol·L-1·min-1
2
C.逆反应速率:a点大于b点
D.故选的平衡转化率是50%
13.(2023·浙江省东阳市高三5月模拟考试)反应物(S)转化为产物(P或P·Z)的能量与反应进程的关系如
下图所示:
下列有关四种不同反应进程的说法正确的是( )
A.对于进程Ⅰ、Ⅱ,生成等量的P所吸收的热量相同
B.对于进程Ⅱ、Ⅲ,催化效率
C.对于进程Ⅰ,升高温度,正、逆反应速率均增大,但正反应速率增加更明显
D.对于进程Ⅳ,Z没有催化作用
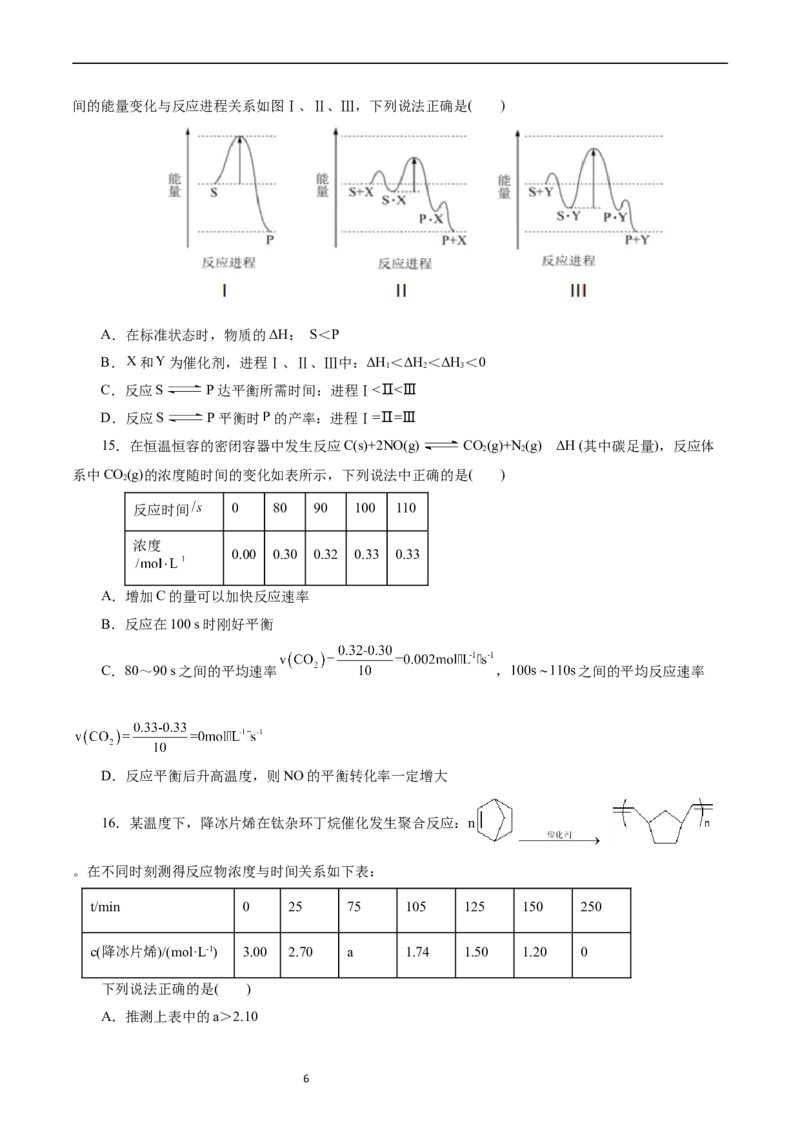
14.(2023·江省乐清市知临中学选考仿真模拟)P、S、X和Y分别代表标准状态下的具体物质,它们之
5间的能量变化与反应进程关系如图Ⅰ、Ⅱ、Ⅲ,下列说法正确是( )
A.在标准状态时,物质的ΔH: S<P
B. 和 为催化剂,进程Ⅰ、Ⅱ、Ⅲ中:ΔH<ΔH<ΔH<0
1 2 3
C.反应S P达平衡所需时间:进程Ⅰ<Ⅱ<Ⅲ
D.反应S P平衡时 的产率:进程Ⅰ=Ⅱ=Ⅲ
15.在恒温恒容的密闭容器中发生反应C(s)+2NO(g) CO(g)+N(g) ΔH (其中碳足量),反应体
2 2
系中CO(g)的浓度随时间的变化如表所示,下列说法中正确的是( )
2
反应时间 0 80 90 100 110
浓度
0.00 0.30 0.32 0.33 0.33
A.增加C的量可以加快反应速率
B.反应在100 s时刚好平衡
C.80~90 s之间的平均速率 , 之间的平均反应速率
D.反应平衡后升高温度,则NO的平衡转化率一定增大
16.某温度下,降冰片烯在钛杂环丁烷催化发生聚合反应:n
。在不同时刻测得反应物浓度与时间关系如下表:
t/min 0 25 75 105 125 150 250
c(降冰片烯)/(mol·L-1) 3.00 2.70 a 1.74 1.50 1.20 0
下列说法正确的是( )
A.推测上表中的a>2.10
6B.若将钛杂环丁烷催化剂制成蜂窝形状可提高该反应的平衡转化率
C.105-155min,生成聚降冰片烯的平均速率为0.012mol·L-1·min-1
D.其他条件相同时,若将降冰片烯起始浓度减少为1.5mol/L,则该反应速率不变
【能力提升】
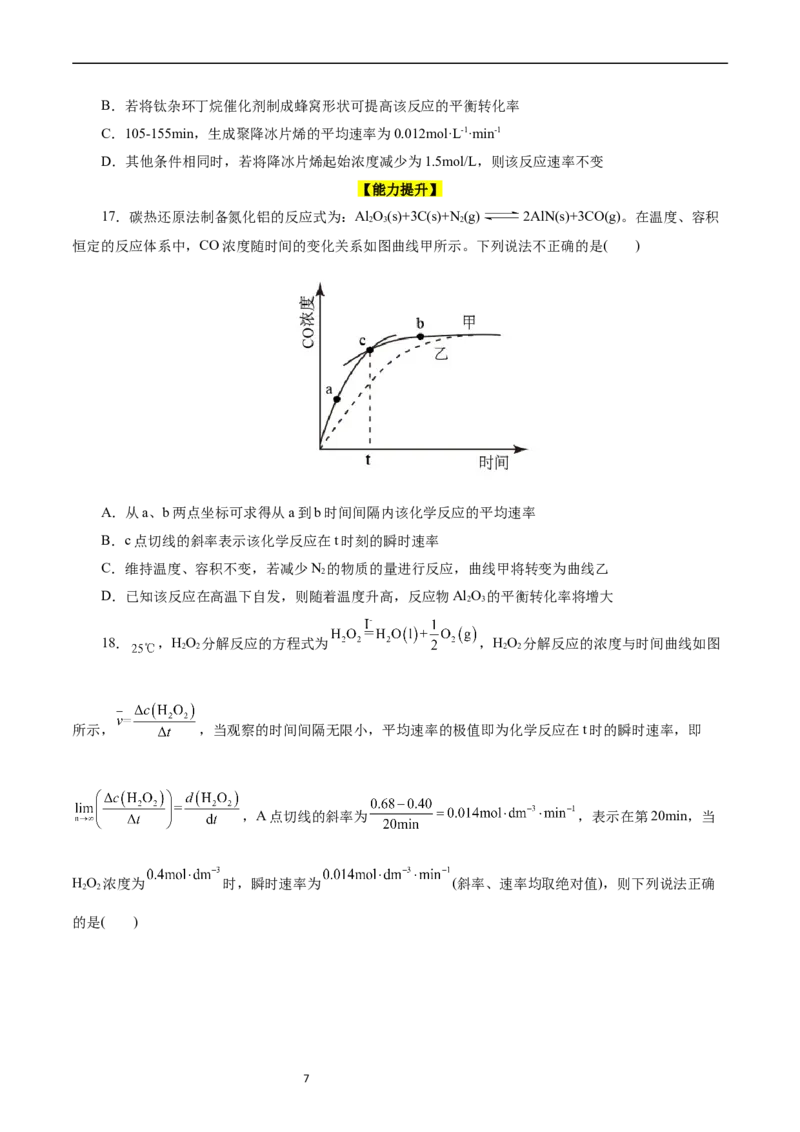
17.碳热还原法制备氮化铝的反应式为:Al O(s)+3C(s)+N (g) 2AlN(s)+3CO(g)。在温度、容积
2 3 2
恒定的反应体系中,CO浓度随时间的变化关系如图曲线甲所示。下列说法不正确的是( )
A.从a、b两点坐标可求得从a到b时间间隔内该化学反应的平均速率
B.c点切线的斜率表示该化学反应在t时刻的瞬时速率
C.维持温度、容积不变,若减少N 的物质的量进行反应,曲线甲将转变为曲线乙
2
D.已知该反应在高温下自发,则随着温度升高,反应物Al O 的平衡转化率将增大
2 3
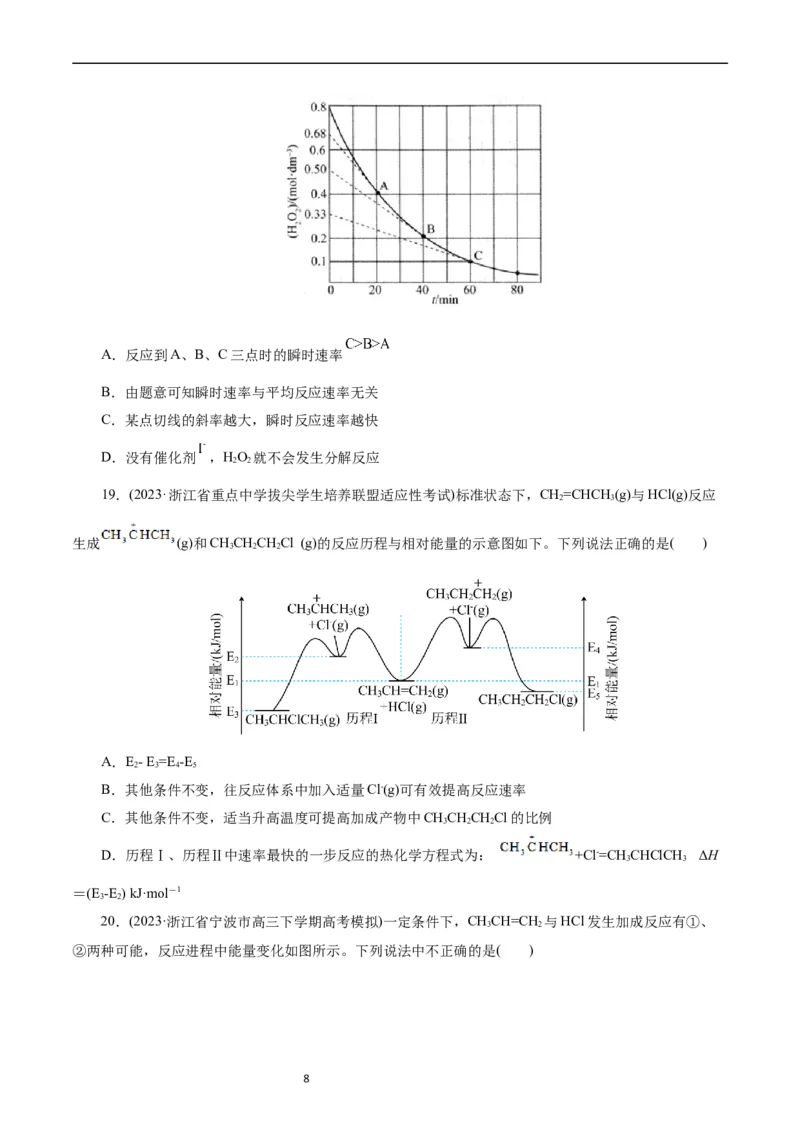
18. ,HO 分解反应的方程式为 ,HO 分解反应的浓度与时间曲线如图
2 2 2 2
所示, ,当观察的时间间隔无限小,平均速率的极值即为化学反应在t时的瞬时速率,即
,A点切线的斜率为 ,表示在第20min,当
HO 浓度为 时,瞬时速率为 (斜率、速率均取绝对值),则下列说法正确
2 2
的是( )
7A.反应到A、B、C三点时的瞬时速率
B.由题意可知瞬时速率与平均反应速率无关
C.某点切线的斜率越大,瞬时反应速率越快
D.没有催化剂 ,HO 就不会发生分解反应
2 2
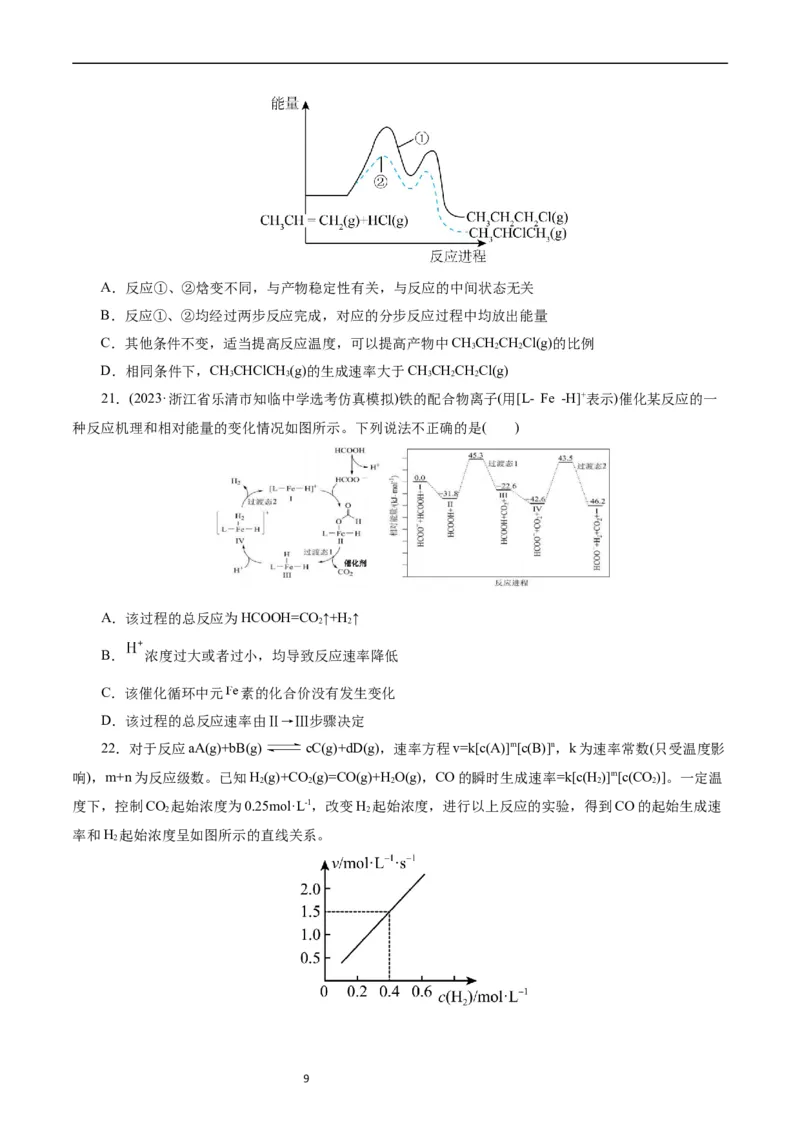
19.(2023·浙江省重点中学拔尖学生培养联盟适应性考试)标准状态下,CH=CHCH(g)与HCl(g)反应
2 3
生成 (g)和CHCHCHCl (g)的反应历程与相对能量的示意图如下。下列说法正确的是( )
3 2 2
A.E- E =E-E
2 3 4 5
B.其他条件不变,往反应体系中加入适量Cl-(g)可有效提高反应速率
C.其他条件不变,适当升高温度可提高加成产物中CHCHCHCl的比例
3 2 2
D.历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为: +Cl-=CH CHClCH ΔH
3 3
=(E -E ) kJ·mol-1
3 2
20.(2023·浙江省宁波市高三下学期高考模拟)一定条件下,CHCH=CH 与HCl发生加成反应有①、
3 2
②两种可能,反应进程中能量变化如图所示。下列说法中不正确的是( )
8A.反应①、②焓变不同,与产物稳定性有关,与反应的中间状态无关
B.反应①、②均经过两步反应完成,对应的分步反应过程中均放出能量
C.其他条件不变,适当提高反应温度,可以提高产物中CHCHCHCl(g)的比例
3 2 2
D.相同条件下,CHCHClCH (g)的生成速率大于CHCHCHCl(g)
3 3 3 2 2
21.(2023·浙江省乐清市知临中学选考仿真模拟)铁的配合物离子(用[L- Fe -H]+表示)催化某反应的一
种反应机理和相对能量的变化情况如图所示。下列说法不正确的是( )
A.该过程的总反应为HCOOH=CO ↑+H ↑
2 2
B. 浓度过大或者过小,均导致反应速率降低
C.该催化循环中元 素的化合价没有发生变化
D.该过程的总反应速率由Ⅱ→Ⅲ步骤决定
22.对于反应aA(g)+bB(g) cC(g)+dD(g),速率方程v=k[c(A)]m[c(B)]n,k为速率常数(只受温度影
响),m+n为反应级数。已知H(g)+CO (g)=CO(g)+HO(g),CO的瞬时生成速率=k[c(H )]m[c(CO)]。一定温
2 2 2 2 2
度下,控制CO 起始浓度为0.25mol·L-1,改变H 起始浓度,进行以上反应的实验,得到CO的起始生成速
2 2
率和H 起始浓度呈如图所示的直线关系。
2
9(1)该反应的反应级数为__________。
(2)速率常数k=__________。
(3)当H 的起始浓度为0.2mol·L-1,反应进行到某一时刻时,测得CO 的浓度为0.2mol·L-1,此时CO的
2 2
生成瞬时速率v=__________mol·L-1·s-1。
23.某兴趣小组同学探究KMnO 酸性溶液与草酸(H C O )溶液反应速率的影响因素。将
4 2 2 4
的KMnO 酸性溶液与 草酸溶液按如下比例混合。
4
【设计实验】
序号 V(KMnO 酸性溶液)/mL V(草酸溶液)/mL V(H O)/mL 反应温度/
4 2
① 2.0 2.0 0 20
② 2.0 1.0 1.0 20
(1)补全KMnO 酸性溶液与草酸溶液反应的离子方程式:_______。
4
2MnO -+5H C O+__________=2 Mn2++10CO ↑+8H O
4 2 2 4 2 2
(2)实验①和②的目的是_______。
【进行实验】
小组同学进行实验①和②,发现紫色并未直接褪去,而是分成两个阶段:
Ⅰ.紫色溶液变为青色溶液;Ⅱ.青色溶液逐渐褪至无色溶液。
【查阅资料】
a.KMnO 酸性溶液与草酸溶液的反应主要包含如下几个过程:
4
反应ⅰ.MnO -+2H C O+4H+=Mn3+(无色)+4CO ↑+4H O
4 2 2 4 2 2
反应ⅱ.Mn3++2H C O=[Mn(C O)]- (青绿色)+ 4H+
2 2 4 2 4 2
反应ⅲ。2Mn3++H C O=2 Mn2+(无色)+2CO ↑+ 2H+
2 2 4 2
b.[Mn(C O)]-的氧化性较弱,在本实验条件下不能氧化HC O。
2 4 2 2 2 4
c.MnO 2-呈绿色,在酸性条件下不稳定,迅速分解为MnO -和MnO 。
4 4 2
【继续探究】
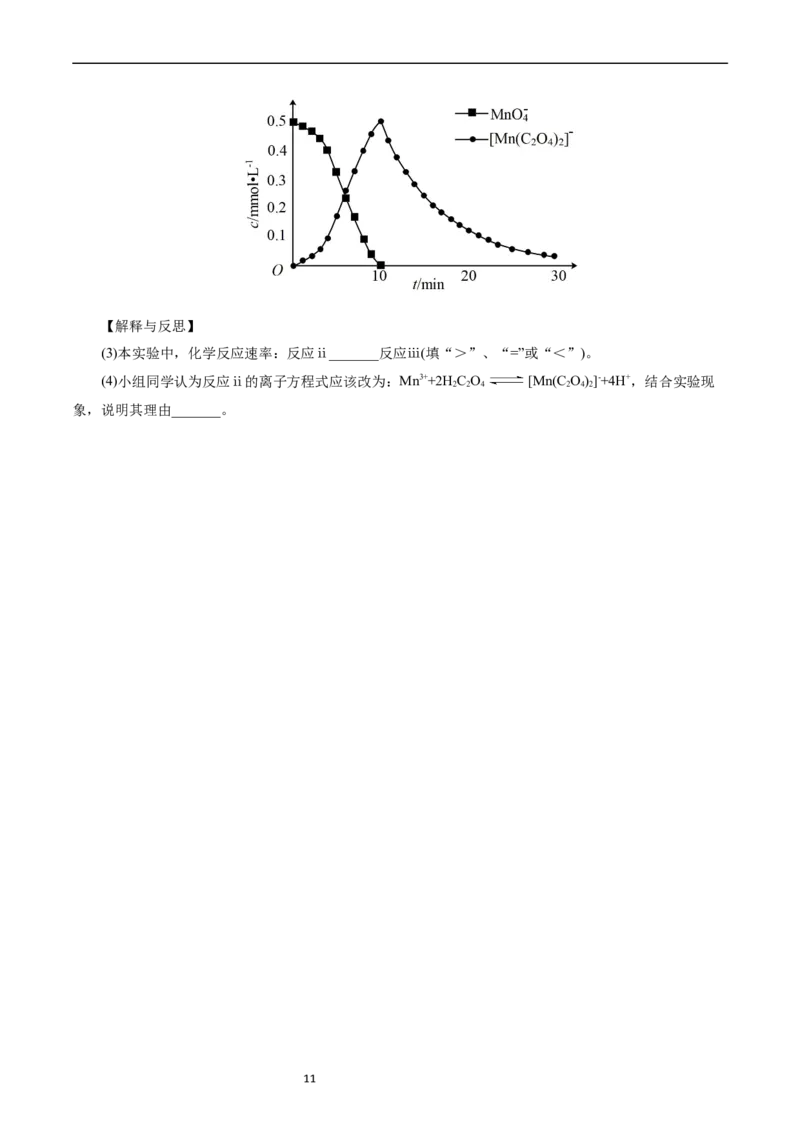
进一步实验证明溶液中含有[Mn(C O)]-,实验①反应过程中MnO -和[Mn(C O)]-的浓度随时间的变化
2 4 2 4 2 4 2
如下图。
10【解释与反思】
(3)本实验中,化学反应速率:反应ⅱ_______反应ⅲ(填“>”、“=”或“<”)。
(4)小组同学认为反应ⅱ的离子方程式应该改为:Mn3++2H C O [Mn(C O)]-+4H+,结合实验现
2 2 4 2 4 2
象,说明其理由_______。
11