文档内容
考点 23 化学平衡常数
【基础过关】
1.一定温度下,反应MgCl (l) Mg(l)+Cl (g)达到平衡时,下列说法错误的是( )
2 2
A.该反应的平衡常数K=c(Cl )
2
B.将容器体积压缩为原来一半,当体系再次达到平衡时,Cl 的浓度增大
2
C.减小氯气浓度,平衡正向移动,平衡常数不变
D.温度升高该反应的化学平衡常数K增大
2.(2023·安徽省皖江名校高三第四次联考)在PdCl -CuCl 做催化剂和适宜的温度条件下,用O 将HCl
2 2 2
氧化为Cl:4HCl(g)+O (g)=2HO(g)+2Cl (g) ΔH<0,下列有关说法不正确的是( )
2 2 2 2
A.降低温度,可提高Cl 产率
2
B.提高 ,该反应的平衡常数增大
C.若断开1molH-Cl键的阿时有1molH-O键断开,则表明该反应达到平衡状态
D.该反应的平衡常数表达式
3.加热NO ,依次发生的分解反应为①NO NO +O ,②NO NO+O ;在2 L密闭
2 5 2 5 2 3 2 2 3 2 2
容器中充入8 mol N O ,加热到t ℃,达到平衡状态后O 为9 mol,NO 为3.4 mol。则t ℃时反应①的平
2 5 2 2 3
衡常数为( )
A.10.7 B.8.5 C.9.6 D.10.2
4.利用IO 可消除CO污染,其反应为:反应为IO(s)+5CO(g) 5CO(g)+I(s);不同温度下,
2 5 2 5 2 2
向装有足量IO 固体的2 L恒容密闭容器中通入2 mol CO,测得CO 气体体积分数φ(CO)随时间t变化曲
2 5 2 2
线如图所示。下列说法正确的是( )
A.b点时,CO的转化率为20%
B.容器内的压强保持恒定,表明反应达到平衡状态
1C.b点和d点的化学平衡常数:K>K
b d
D.0到0.5 min反应速率v(CO)=0.3 mol·L-1·min-1
5.在PdCl -CuCl 做催化剂和适宜的温度条件下,用O 将HCl氧化为Cl:4HCl(g)+O (g)=2HO(g)
2 2 2 2 2 2
+2Cl(g) ΔH<0,下列有关说法不正确的是( )
2
A.降低温度,可提高Cl 产率
2
B.提高 ,该反应的平衡常数增大
C.若断开1molH-Cl键的阿时有1molH-O键断开,则表明该反应达到平衡状态
D.该反应的平衡常数表达式
6.(2023·河北省部分学校高三联考)高炉炼铁中的一个反应为FeO(s)+CO(g) Fe(s)+CO (g) ΔH>
2
0,在1100℃下,若CO起始浓度为1.2mol/L,10min后达到平衡时 的体积分数为 ,下列说法错误的
是( )
A.1100℃下,此反应的平衡常数
B.达到平衡过程中,反应的平均速率为v(CO)=0.02 mol·L-1·min-1
C.达到平衡后,若增大c(CO),则达到新平衡时, 增大
2
D.测得某时刻c(CO)=0.8mol/L,则此时
7.(2023·江西省九江市十校高三联考)向体积均为1L的两恒容容器中分别充入2molX和1molY发生反
应:2X(g)+Y(g) Z(g) ΔH,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化
曲线如图所示。下列说法不正确的是( )
A.a点平衡常数: B.气体的总物质的量:n<n
a c
C.ΔH<0 D.平衡转化率:甲<乙
8.合成氨是人类科学技术发展史上的一项重大突破,目前工业上用氢气和氮气直接合成氨:N(g)
2
2+3H (g) 2NH (g)。T℃时,在2L恒容密闭容器中加入1.2molN 和2molH 模拟一定条件下工业固氮,
2 3 2 2
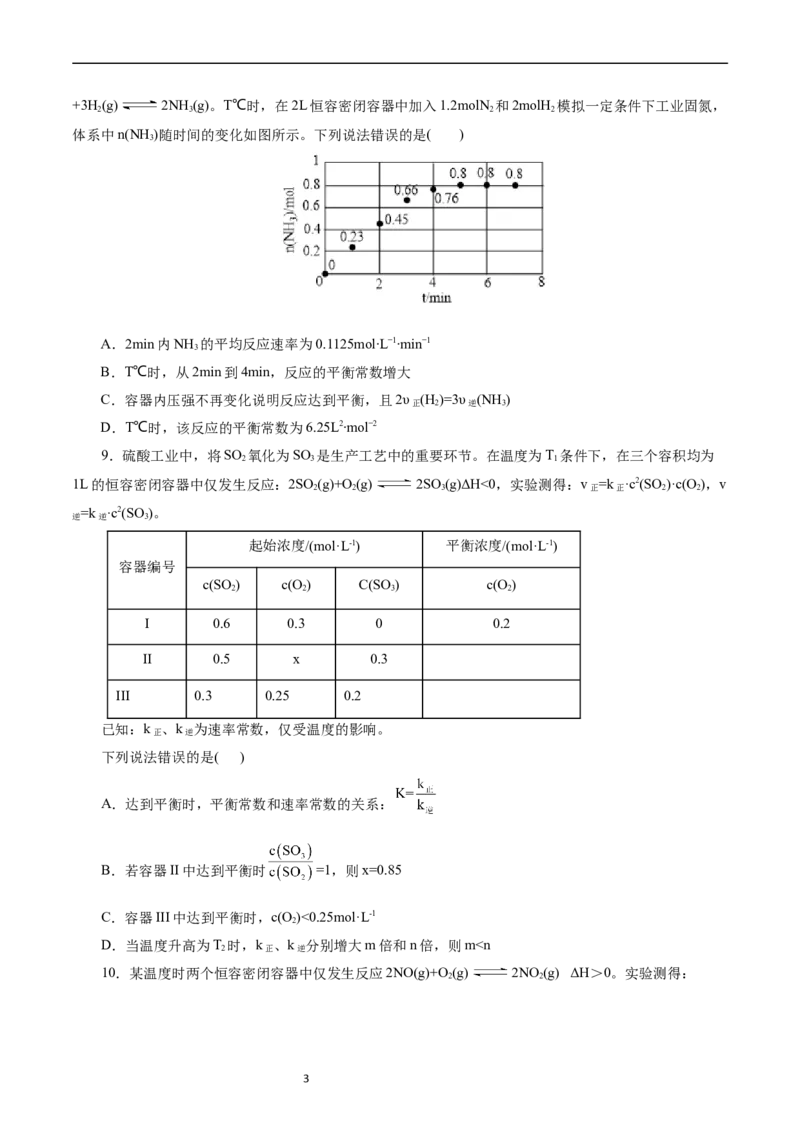
体系中n(NH )随时间的变化如图所示。下列说法错误的是( )
3
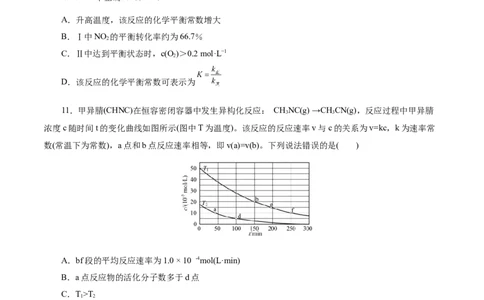
A.2min内NH 的平均反应速率为0.1125mol∙L−1∙min−1
3
B.T℃时,从2min到4min,反应的平衡常数增大
C.容器内压强不再变化说明反应达到平衡,且2υ (H )=3υ (NH )
正 2 逆 3
D.T℃时,该反应的平衡常数为6.25L2∙mol−2
9.硫酸工业中,将SO 氧化为SO 是生产工艺中的重要环节。在温度为T 条件下,在三个容积均为
2 3 1
1L的恒容密闭容器中仅发生反应:2SO (g)+O(g) 2SO (g)ΔH<0,实验测得:v =k ·c2(SO )·c(O),v
2 2 3 正 正 2 2
=k ·c2(SO )。
逆 逆 3
起始浓度/(mol·L-1) 平衡浓度/(mol·L-1)
容器编号
c(SO ) c(O) C(SO ) c(O)
2 2 3 2
I 0.6 0.3 0 0.2
II 0.5 x 0.3
III 0.3 0.25 0.2
已知:k 、k 为速率常数,仅受温度的影响。
正 逆
下列说法错误的是( )
A.达到平衡时,平衡常数和速率常数的关系:
B.若容器II中达到平衡时 =1,则x=0.85
C.容器III中达到平衡时,c(O)<0.25mol·L-1
2
D.当温度升高为T 时,k 、k 分别增大m倍和n倍,则mT
1 2
D.3v(d)=2v(e)
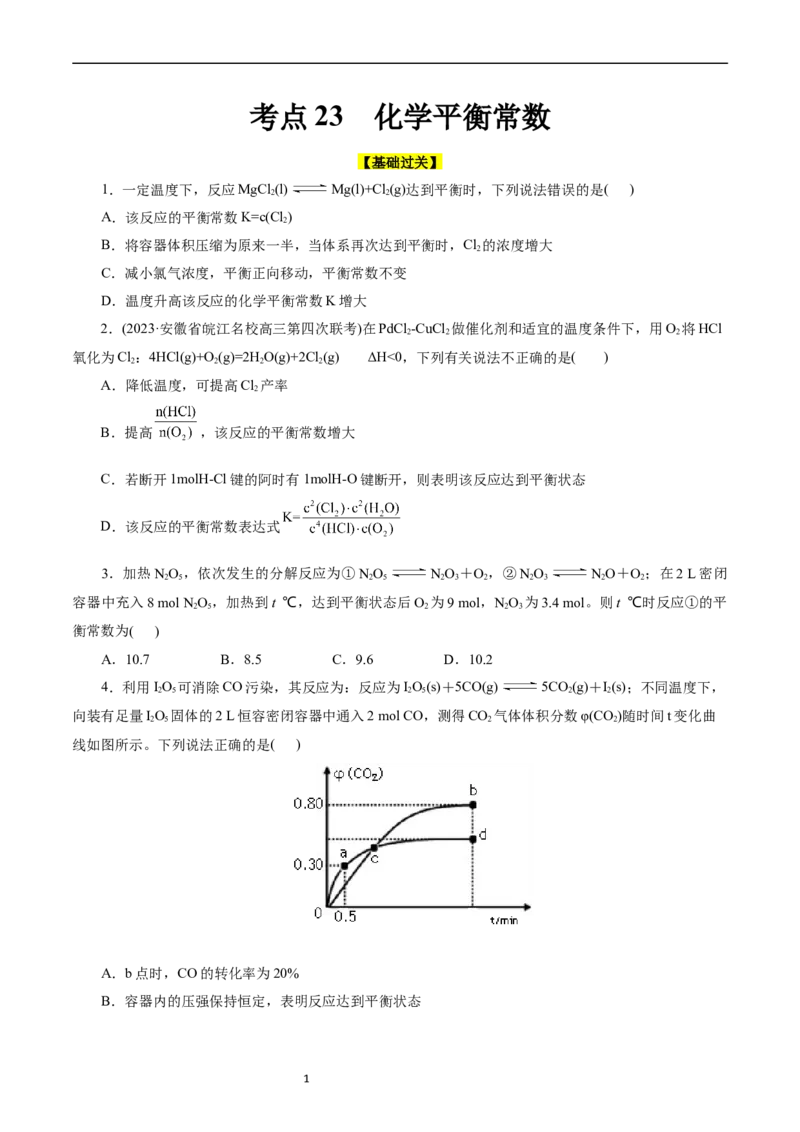
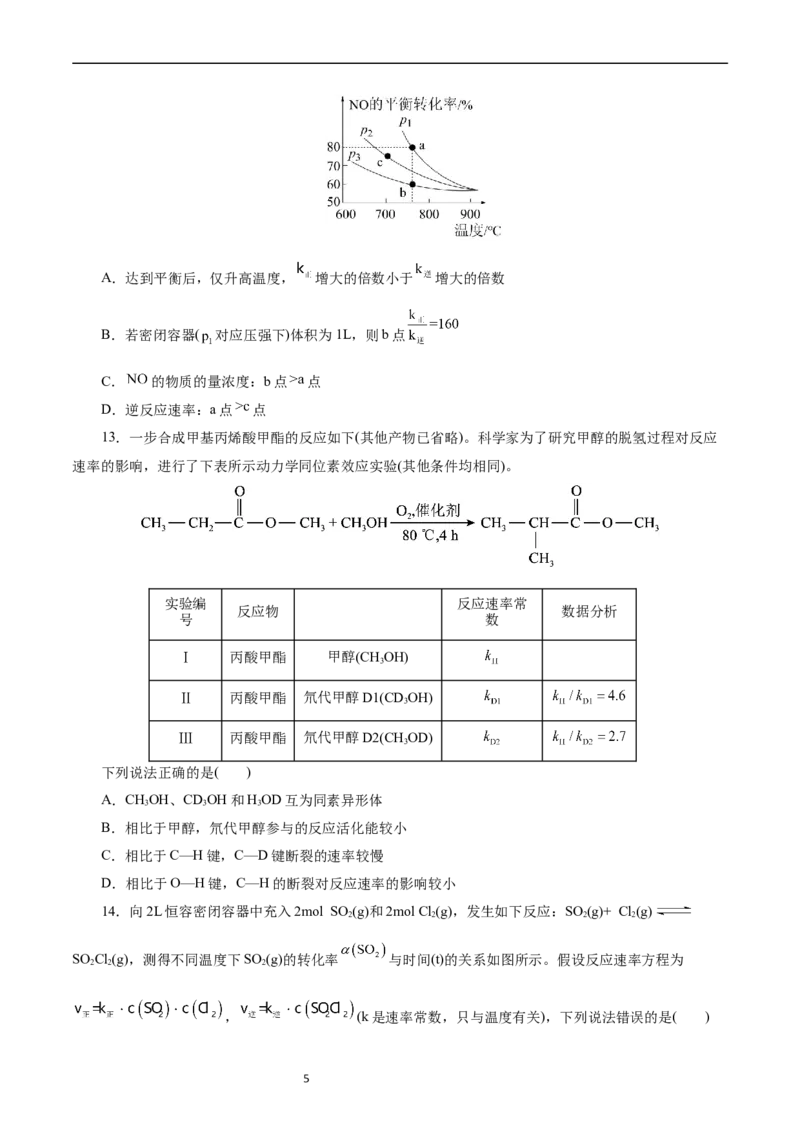
12.在密闭容器中充入1 和1 ,在一定条件下发生反2NO(g)+2CO(g) N(g)
2
+2CO (g),测得 的平衡转化率与温度及压强的关系如图所示。实验测得, ,
2
( 、 为速率常数,只与温度有关),下列说法错误的是( )
4A.达到平衡后,仅升高温度, 增大的倍数小于 增大的倍数
B.若密闭容器( 对应压强下)体积为1L,则b点
C. 的物质的量浓度:b点 点
D.逆反应速率:a点 点
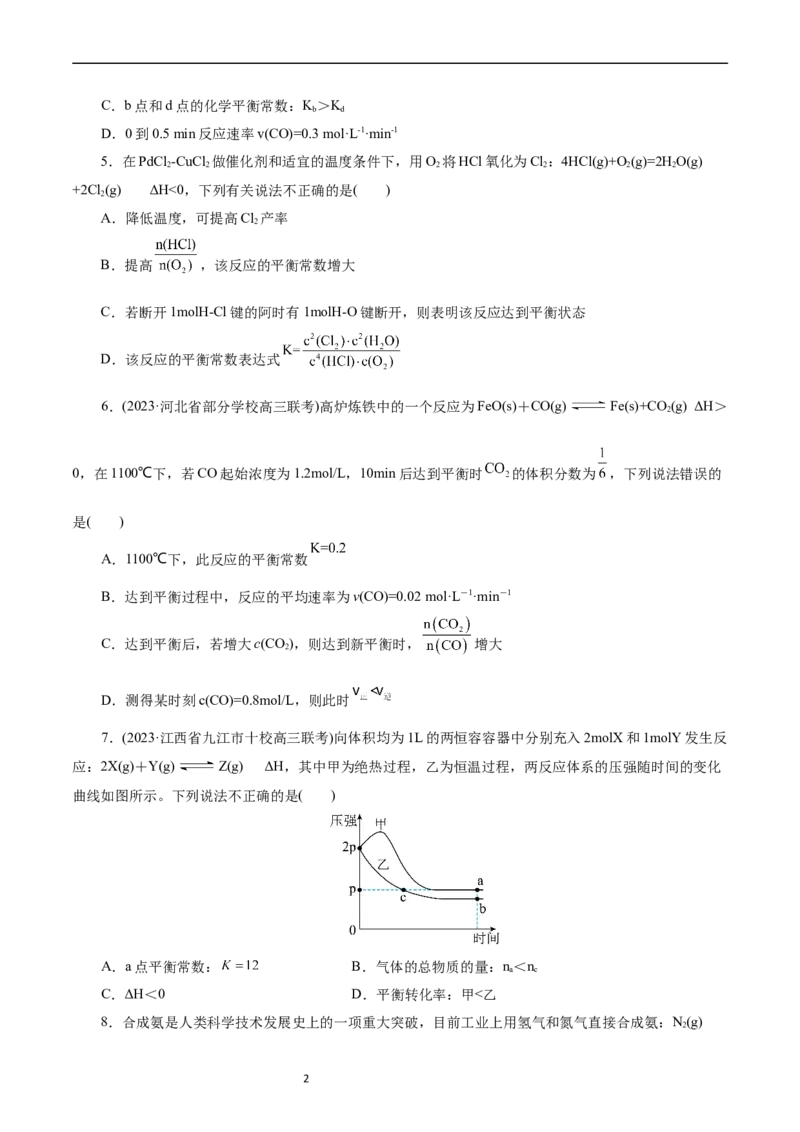
13.一步合成甲基丙烯酸甲酯的反应如下(其他产物已省略)。科学家为了研究甲醇的脱氢过程对反应
速率的影响,进行了下表所示动力学同位素效应实验(其他条件均相同)。
实验编 反应速率常
反应物 数据分析
号 数
Ⅰ 丙酸甲酯 甲醇(CHOH)
3
Ⅱ 丙酸甲酯 氘代甲醇D1(CD OH)
3
Ⅲ 丙酸甲酯 氘代甲醇D2(CH OD)
3
下列说法正确的是( )
A.CHOH、CDOH和HOD互为同素异形体
3 3 3
B.相比于甲醇,氘代甲醇参与的反应活化能较小
C.相比于C—H键,C—D键断裂的速率较慢
D.相比于O—H键,C—H的断裂对反应速率的影响较小
14.向2L恒容密闭容器中充入2mol SO (g)和2mol Cl (g),发生如下反应:SO (g)+ Cl (g)
2 2 2 2
SO Cl(g),测得不同温度下SO (g)的转化率 与时间(t)的关系如图所示。假设反应速率方程为
2 2 2
, (k是速率常数,只与温度有关),下列说法错误的是( )
5A.该反应的ΔH<0
B. 时,
C.M点:
D.升高温度, 增大的倍数大于 增大的倍数
15.NO 在一定条件下可发生分解:2NO(g) 4NO (g)+O(g) H>0。向恒容密闭容器加入
2 5 2 5 2 2
N 2 O 5 。某温度下测得恒容密闭容器中N 2 O 5 浓度随时间的变化如下表: △
t/min 0.00 1.00 2.00 3.00 4.00 5.00
c(NO)/(mo·L-1) 1.00 0.71 0.50 0.35 0.35 0.35
2 5
反应开始时体系压强为P,第3.00min时体系压强为p,则p:p=________。该温度下反应的平衡常
0 1 1 0
数K=____________(用平衡分压代替平衡浓度计算,分压=总压×物质的量的分数,请列出用P 表示平衡常
p 0
数表达式,不用计算)。
16.在恒容密闭容器中,加入足量的 MoS 和O ,仅发生反应:2MoS (s)+7O(g) 2MoO (s)+
2 2 2 2 3
4SO (g) ΔH。
2
测得氧气的平衡转化率与起始压强、温度的关系如图所示:
(1)p、p、p 的大小:________。
1 2 3
6(2)若初始时通入7.0 mol O,p 为7.0 kPa,则A点平衡常数K =________(用气体平衡分压代替气体平
2 2 p
衡浓度计算,分压=总压×气体的物质的量分数,写出计算式即可)。
17.如图是当反应器中按n(N )∶n(H )=1∶3投料后,在200 ℃、400 ℃、600 ℃反应达到平衡时,混
2 2
合物中NH 的物质的量分数随总压强的变化曲线。
3
(1)曲线a、b对应温度较高的是 (填“a”或“b”)。
(2)列出b点平衡常数的计算式K= (用平衡分压代替平衡浓度计算,分压=总压×
p
物质的量分数;不要求计算结果)。
18.NO 在一定条件下可发生分解:2NO(g) 4NO (g)+O(g) H>0。向恒容密闭容器加入
2 5 2 5 2 2
N 2 O 5 。某温度下测得恒容密闭容器中N 2 O 5 浓度随时间的变化如下表: △
t/min 0.00 1.00 2.00 3.00 4.00 5.00
c(NO)/(mo·L-1) 1.00 0.71 0.50 0.35 0.35 0.35
2 5
反应开始时体系压强为P,第3.00min时体系压强为p,则p:p=________。该温度下反应的平衡常
0 1 1 0
数K=____________(用平衡分压代替平衡浓度计算,分压=总压×物质的量的分数,请列出用P 表示平衡常
p 0
数表达式,不用计算)。
19.(1)工业合成NH 的反应,解决了世界约三分之一的人粮食问题。已知:N +3H 2NH ,且
3 2 2 3
该反应的v =k ·c(N)·c3(H ),v =k ·c2(NH ),则反应N +H NH 的平衡常数K=________(用k
正 正 2 2 逆 逆 3 2 2 3
和k 表示)。
正 逆
(2)500 ℃时,向容积为2 L的密闭容器中通入1 mol N 和3 mol H ,模拟合成氨的反应,容器内的压强
2 2
随时间的变化如下表所示:
时间/min 0 10 20 30 40 +∞
压强/MPa 20 17 15 13.2 11 11
①达到平衡时N 的转化率为________。
2
②用压强表示该反应的平衡常数K =________(K 等于平衡时生成物分压幂的乘积与反应物分压幂的
p p
乘积的比值,某物质的分压等于总压×该物质的物质的量分数)。
③随着反应的进行合成氨的正反应速率与NH 的体积分数的关系如下图所示,若升高温度再次达到平
3
衡时,可能的点为________(从点“A、B、C、D”中选择)
720.环戊二烯( )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
某温度,等物质的量的碘和环戊烯( )在刚性容器内发生反应 (g)+I(g) (g)+2HI(g)
2
ΔH>0,起始总压为105 Pa,平衡时总压增加了20%,环戊烯的转化率为________,该反应的平衡常数K
p
=__________Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有________(填标号)。
A.通入惰性气体 B.提高温度 C.增加环戊烯浓度 D.增加碘浓度
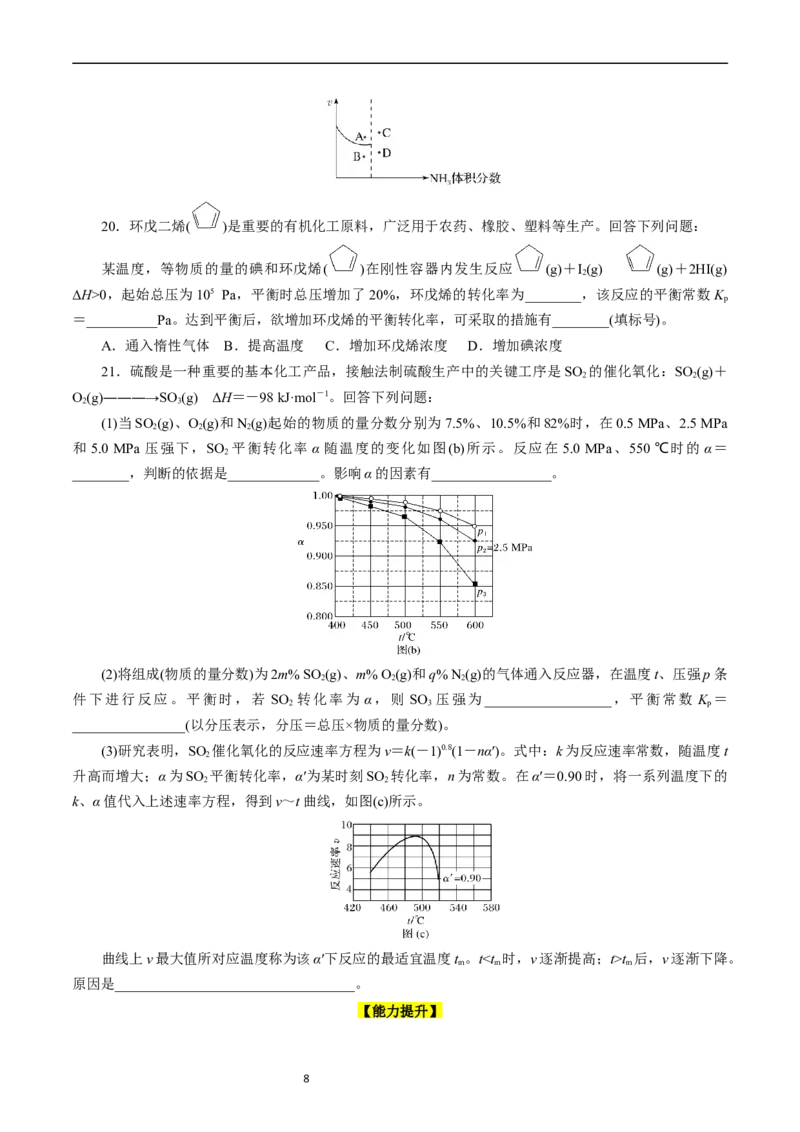
21.硫酸是一种重要的基本化工产品,接触法制硫酸生产中的关键工序是SO 的催化氧化:SO (g)+
2 2
O(g)―――→SO (g) ΔH=-98 kJ·mol-1。回答下列问题:
2 3
(1)当SO (g)、O(g)和N(g)起始的物质的量分数分别为7.5%、10.5%和82%时,在0.5 MPa、2.5 MPa
2 2 2
和 5.0 MPa 压强下,SO 平衡转化率 α 随温度的变化如图(b)所示。反应在 5.0 MPa、550 ℃时的 α=
2
________,判断的依据是_____________。影响α的因素有_________________。
(2)将组成(物质的量分数)为2m% SO(g)、m% O (g)和q% N (g)的气体通入反应器,在温度t、压强p条
2 2 2
件下进行反应。平衡时,若 SO 转化率为 α,则 SO 压强为__________________,平衡常数 K =
2 3 p
________________(以分压表示,分压=总压×物质的量分数)。
(3)研究表明,SO 催化氧化的反应速率方程为v=k(-1)0.8(1-nα′)。式中:k为反应速率常数,随温度t
2
升高而增大;α为SO 平衡转化率,α′为某时刻SO 转化率,n为常数。在α′=0.90时,将一系列温度下的
2 2
k、α值代入上述速率方程,得到v~t曲线,如图(c)所示。
曲线上v最大值所对应温度称为该α′下反应的最适宜温度t 。tt 后,v逐渐下降。
m m m
原因是__________________________________。
【能力提升】
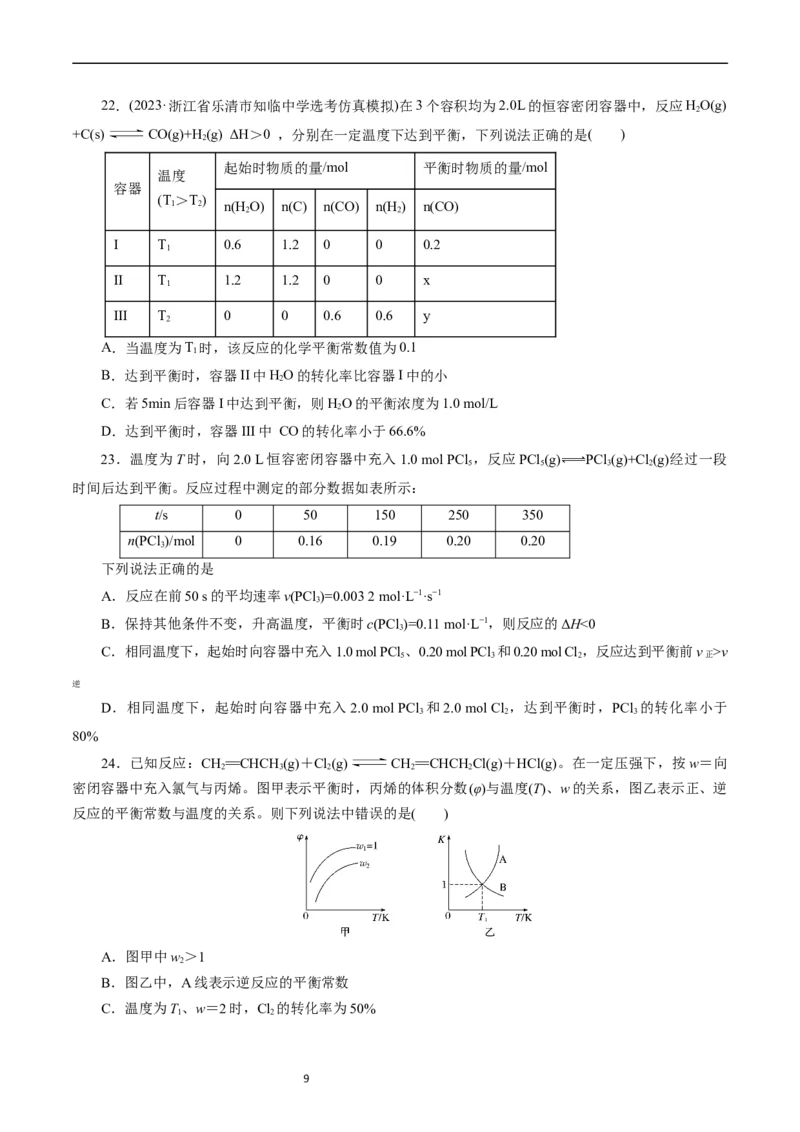
822.(2023·浙江省乐清市知临中学选考仿真模拟)在3个容积均为2.0L的恒容密闭容器中,反应HO(g)
2
+C(s) CO(g)+H(g) ΔH>0 ,分别在一定温度下达到平衡,下列说法正确的是( )
2
起始时物质的量/mol 平衡时物质的量/mol
温度
容器
(T >T)
1 2 n(H O) n(C) n(CO) n(H ) n(CO)
2 2
I T 0.6 1.2 0 0 0.2
1
II T 1.2 1.2 0 0 x
1
III T 0 0 0.6 0.6 y
2
A.当温度为T 时,该反应的化学平衡常数值为0.1
1
B.达到平衡时,容器II中HO的转化率比容器I中的小
2
C.若5min后容器I中达到平衡,则HO的平衡浓度为1.0 mol/L
2
D.达到平衡时,容器III中 CO的转化率小于66.6%
23.温度为T时,向2.0 L恒容密闭容器中充入1.0 mol PCl ,反应PCl (g) PCl (g)+Cl (g)经过一段
5 5 3 2
时间后达到平衡。反应过程中测定的部分数据如表所示:
t/s 0 50 150 250 350
n(PCl )/mol 0 0.16 0.19 0.20 0.20
3
下列说法正确的是
A.反应在前50 s的平均速率v(PCl )=0.003 2 mol·L−1·s−1
3
B.保持其他条件不变,升高温度,平衡时c(PCl )=0.11 mol·L−1,则反应的ΔH<0
3
C.相同温度下,起始时向容器中充入1.0 mol PCl 、0.20 mol PCl 和0.20 mol Cl ,反应达到平衡前v >v
5 3 2 正
逆
D.相同温度下,起始时向容器中充入 2.0 mol PCl 和2.0 mol Cl ,达到平衡时,PCl 的转化率小于
3 2 3
80%
24.已知反应:CH==CHCH (g)+Cl(g) CH==CHCH Cl(g)+HCl(g)。在一定压强下,按w=向
2 3 2 2 2
密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数(φ)与温度(T)、w的关系,图乙表示正、逆
反应的平衡常数与温度的关系。则下列说法中错误的是( )
A.图甲中w >1
2
B.图乙中,A线表示逆反应的平衡常数
C.温度为T、w=2时,Cl 的转化率为50%
1 2
9D.若在恒容绝热装置中进行上述反应,达到平衡时,装置内的气体压强增大
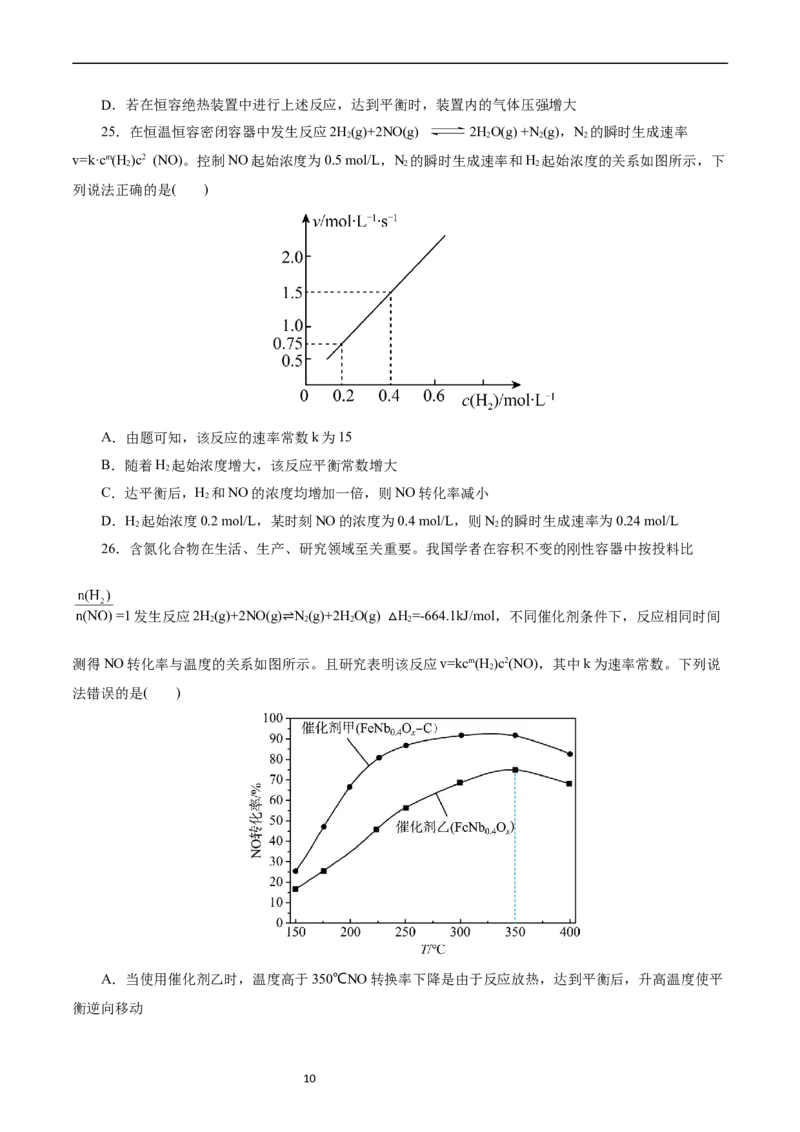
25.在恒温恒容密闭容器中发生反应2H(g)+2NO(g) 2HO(g) +N (g),N 的瞬时生成速率
2 2 2 2
v=k·cm(H )c2 (NO)。控制NO起始浓度为0.5 mol/L,N 的瞬时生成速率和H 起始浓度的关系如图所示,下
2 2 2
列说法正确的是( )
A.由题可知,该反应的速率常数k为15
B.随着H 起始浓度增大,该反应平衡常数增大
2
C.达平衡后,H 和NO的浓度均增加一倍,则NO转化率减小
2
D.H 起始浓度0.2 mol/L,某时刻NO的浓度为0.4 mol/L,则N 的瞬时生成速率为0.24 mol/L
2 2
26.含氮化合物在生活、生产、研究领域至关重要。我国学者在容积不变的刚性容器中按投料比
=1发生反应2H(g)+2NO(g) N(g)+2HO(g) H=-664.1kJ/mol,不同催化剂条件下,反应相同时间
2 2 2 2
⇌ △
测得NO转化率与温度的关系如图所示。且研究表明该反应v=kcm(H )c2(NO),其中k为速率常数。下列说
2
法错误的是( )
A.当使用催化剂乙时,温度高于350℃NO转换率下降是由于反应放热,达到平衡后,升高温度使平
衡逆向移动
10B.使用催化剂甲比使用催化剂乙正反应的活化能更低
C.对于反应2H(g)+2NO(g) N(g)+2HO(g),其他条件不变,加压使平衡正向移动
2 2 2
D.T℃的初始速率为V,当H 转化率为60%时,反应速率为0.064V ,由此可知m=1
1 0 2 0
27.(2023·黑龙江省哈尔滨三中高三期中)工业合成氨是人类科学技术的一项重大突破,目前已有三位
科学家因其获得诺贝尔奖,反应为:N(g)+3H(g) 2NH
2 2 3
。请回答下列问题:
(1)常温下,合成氨反应_______(填“能”或“不能”)自发进行,其平衡常数表达式K=_______。
(2)_______温(填“高”或“低”)有利于提高反应速率,_______温(填“高”或“低”)有利于提高平
衡转化率,综合考虑催化剂(铁触媒)活性等因素,工业常采用400~500℃。
(3)针对反应速率与平衡产率的矛盾,我国科学家提出了解决方案:双温—双控—双催化剂。使用
双催化剂,通过光辐射产生温差(如体系温度为495℃时,Fe的温度为547℃,而 的温
度为415℃)。
该方案的优势:①_______;②_______。
(4)一定温度和催化剂的条件下,将0.1mol NH 通入3L的密闭容器中进行mol·L-1·min-1分解为N 和
3 2
H 的反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
2
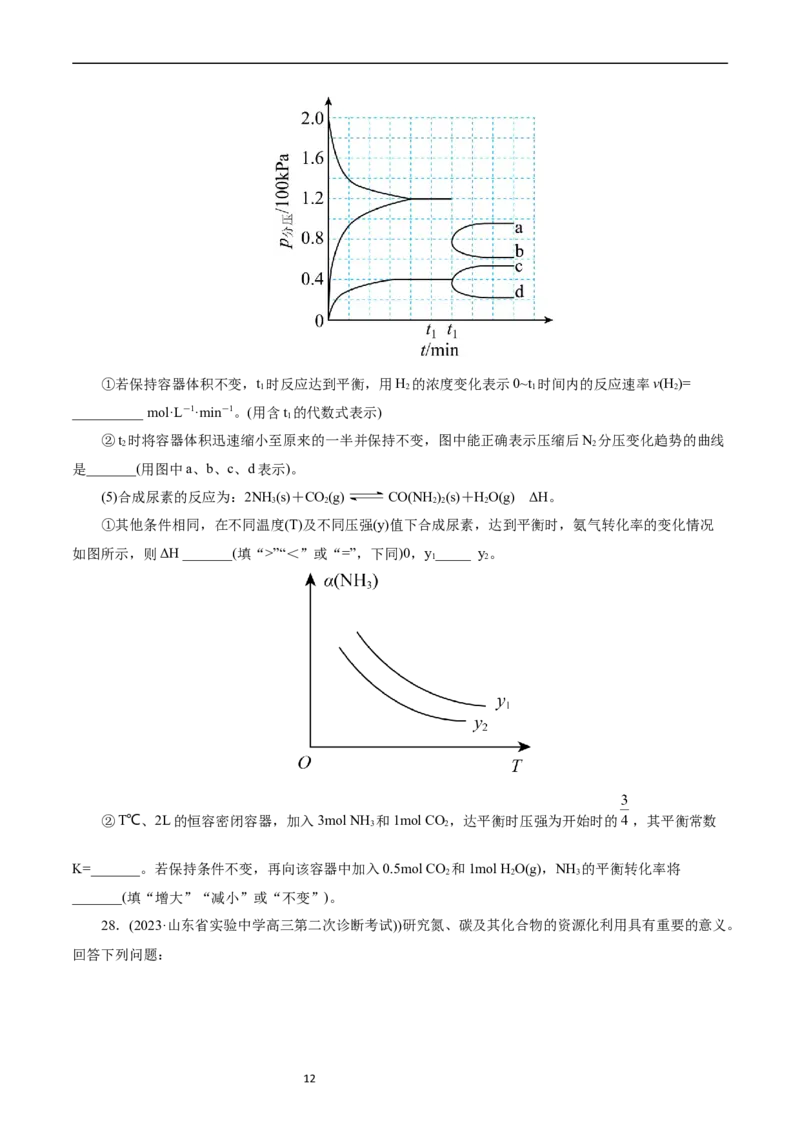
11①若保持容器体积不变,t 时反应达到平衡,用H 的浓度变化表示0~t 时间内的反应速率v(H )=
1 2 1 2
__________mol·L-1·min-1。(用含t 的代数式表示)
1
②t 时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后N 分压变化趋势的曲线
2 2
是_______(用图中a、b、c、d表示)。
(5)合成尿素的反应为:2NH (s)+CO(g) CO(NH)(s)+HO(g) ΔH。
3 2 2 2 2
①其他条件相同,在不同温度(T)及不同压强(y)值下合成尿素,达到平衡时,氨气转化率的变化情况
如图所示,则ΔH _______(填“>”“<”或“=”,下同)0,y_____ y 。
1 2
②T℃、2L的恒容密闭容器,加入3mol NH 和1mol CO,达平衡时压强为开始时的 ,其平衡常数
3 2
K=_______。若保持条件不变,再向该容器中加入0.5mol CO 和1mol HO(g),NH 的平衡转化率将
2 2 3
_______(填“增大”“减小”或“不变”)。
28.(2023·山东省实验中学高三第二次诊断考试))研究氮、碳及其化合物的资源化利用具有重要的意义。
回答下列问题:
12(1)已知氢气还原氮气合成氨低温下自发发生。若将2.0 mol N 和6.0molH 通入体积为1L的密闭容器中,
2 2
分别在T 和T 温度下进行反应。曲线A表示T 温度下n(H )的变化,曲线B表示T 温度下n(NH )的变化,
1 2 2 2 1 3
T 温度下反应到a点恰好达到平衡。
2
①温度T______(填“>”“<”或“=”下同) T 。T 温度下恰好平衡时,曲线B上的点为b(m,n),则
1 2 1
m______12,n_____2;
②T 温度下,若某时刻容器内气体的压强为起始时的80%,则此时v(正)________(填“>”“<”或
2
“=”)v(逆)。
(2)以焦炭为原料,在高温下与水蒸气反应可制得水煤气,涉及反应如下:
I.C(s)+HO(g) CO(g)+ H (g) ΔH =+131.3kJ·mol−1 K
2 2 1 1
II.C(s)+2HO(g) CO(g)+ 2H (g) ΔH =+90.3kJ·mol−1 K
2 2 2 1 2
III.CO(g)+ H O(g) CO(g)+H(g) ΔH =-41.0kJ·mol−1 K
2 2 2 3 3
三个反应的平衡常数随温度变化的关系如图所示,则表示K、K 的曲线依次是_______、_______。
1 3
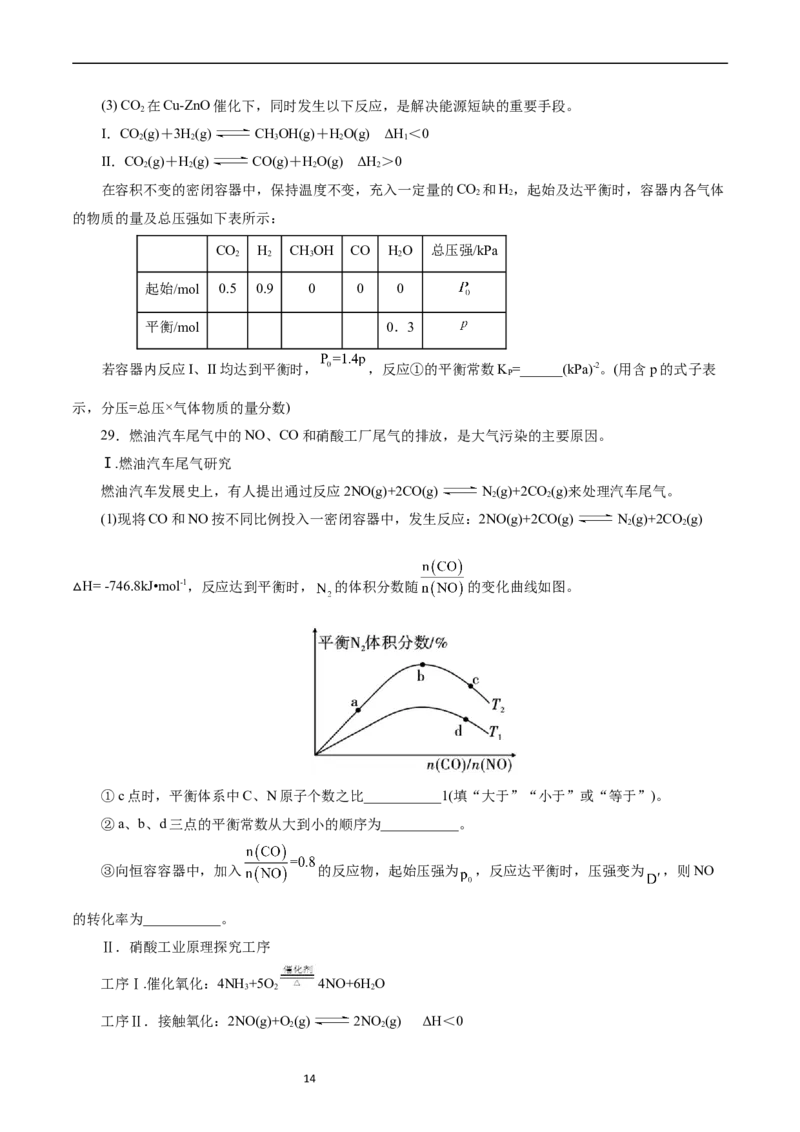
13(3) CO 在Cu-ZnO催化下,同时发生以下反应,是解决能源短缺的重要手段。
2
I.CO(g)+3H(g) CHOH(g)+HO(g) ΔH <0
2 2 3 2 1
II.CO(g)+H(g) CO(g)+HO(g) ΔH >0
2 2 2 2
在容积不变的密闭容器中,保持温度不变,充入一定量的CO 和H,起始及达平衡时,容器内各气体
2 2
的物质的量及总压强如下表所示:
CO H CHOH CO HO 总压强/kPa
2 2 3 2
起始/mol 0.5 0.9 0 0 0
平衡/mol 0.3
若容器内反应I、II均达到平衡时, ,反应①的平衡常数K =______(kPa)-2。(用含p的式子表
P
示,分压=总压×气体物质的量分数)
29.燃油汽车尾气中的NO、CO和硝酸工厂尾气的排放,是大气污染的主要原因。
Ⅰ.燃油汽车尾气研究
燃油汽车发展史上,有人提出通过反应2NO(g)+2CO(g) N(g)+2CO (g)来处理汽车尾气。
2 2
(1)现将CO和NO按不同比例投入一密闭容器中,发生反应:2NO(g)+2CO(g) N(g)+2CO (g)
2 2
H= -746.8kJ•mol-1,反应达到平衡时, 的体积分数随 的变化曲线如图。
△
①c点时,平衡体系中C、N原子个数之比___________1(填“大于”“小于”或“等于”)。
②a、b、d三点的平衡常数从大到小的顺序为___________。
③向恒容容器中,加入 的反应物,起始压强为 ,反应达平衡时,压强变为 ,则NO
的转化率为___________。
Ⅱ.硝酸工业原理探究工序
工序Ⅰ.催化氧化:4NH +5O 4NO+6H O
3 2 2
工序Ⅱ.接触氧化:2NO(g)+O (g) 2NO (g) ΔH<0
2 2
14工序Ⅲ.水吸收: 4NO +2H O O=4HNO
2 2 + 2 3
(2)将工序Ⅰ中产生的气体(温度高于800℃)快速冷却到100℃以下,然后再送入接触氧化设备中发生工
序Ⅱ,目的是___________(任答一条即可)。
(3)工序Ⅱ中,以2:1的比例通入NO和O,达到一定转化率所需时间(t)和温度(T)、压强(p)的关系如
2
下表所示
达到NO转化率所需时间(t)/s
压强(p)/ ( 温度
) (T)/℃
50% 90% 98%
30 12.4 248 2830
1
90 25.3 508 5760
30 0.19 3.88 36.4
8
90 0.59 7.86 74
由表中数据可知,工序Ⅱ是在___________(填“加”“减”或“常”)压、___________(填“高”
“低”或“常”)温下进行的。
(4)只需一步完成的反应称为基元反应,基元反应如 的速率方程,v =k ·ca(A)·cd(D),
正 正
v =k ·cg(G)·ch(H)。非基元反应由多个基元反应组成,非基元反应的速率方程可由反应机理推定。
逆 逆
工序Ⅱ:2NO(g)+O (g) 2NO (g) ΔH<0 (非基元反应)
2 2
一种可能的机理为
(i) 2NO(g) NO(g) 快速平衡ΔH<0平衡常数(K )
2 2 1
(ii) NO(g)+O(g) 2NO (g)慢反应(即控速步)
2 2 2 2
①求出k与k、k 、k 的关系为_________(用含有k、k、k 、k 的表达式表示)
1 -1 2 1 -1 2
②反应2NO(g)+O (g) 2NO (g)几乎是自然界唯一的“升高温度,速率反而减慢”的例子,目前
2 2
的研究认为和上述机理有关,下表为平衡常数(K )和第二步的速率常数( )在不同温度下的数值:
1
T/K 300 350 400 500
平衡常数(K )
1
速率常数( ) 2.5 25.8
根据表中数据推测:升高温度,工序Ⅱ的反应速率反而减慢的原因可能是___________。
1516