文档内容
高 2025 级高一上期第二次月考试卷
化学试卷
考试时间:75分钟 满分:100分
注意事项:
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。请将答案写在
答题卡上,写在本试卷上无效。
可能用到的相对原子质量:O-16 Na-23 K-39 Fe-56 Cu-64 Zn-65 Cl-35.5
第Ⅰ卷 选择题
一、本卷共15小题,每题只有1个选项符合题意(每题3分,共45分)
1.下列物质属于钠盐的是
A.Na O B.NaOH C.NaHCO D.Na O
2 3 2 2
2.下列化合物中Mn的化合价为+4价的是
A.MnO B.KMnO C.MnCl D.
2 4 2
K MnO
2 4
3.下列说法正确的是
A.CO 、NO均属于酸性氧化物 B.金刚石与石墨互为同素异形体
2
C.凡能电离出H+的化合物均属于酸 D.盐类物质一定含有金属阳离子
4.下列有关胶体的说法不正确的是
A.制备:将饱和氯化铁溶液滴入稀氢氧化钠溶液中加热,可制得氢氧化铁胶
体
B.鉴别:淀粉胶体能够发生丁达尔现象,而NaCl溶液则不能
C.分离提纯:用半透膜能分离淀粉胶体和NaCl溶液
D.应用:用Fe(OH) 胶体吸附水中的杂质颗粒净水
3
5.下列反应不属于离子反应的是
A.氢气在氧气中燃烧 B.锌和稀硫酸的反应
C.氯化钡溶液和硫酸钠溶液反应 D.氢氧化钾溶液和硫酸铜溶液反
应
6.生活中处处存在化学,下列关于生活中常见的物质的分类错误的是A. 人们常使用酒精消毒,酒精属于有机物
B. 含氯泡腾片可以有效杀灭新冠病毒,其主要成分为ClO ,ClO 属于氧化物
2 2
C. 加碘食盐中含碘的物质是KIO ,KIO 属于盐
3 3
D. 纯碱可以用于除去油污,纯碱属于碱
7.生活处处皆化学,它已渗透到社会生活各方面。下列叙述不合理的是
A. 实验室中若金属钠失火,不能采用泡沫灭火器灭火
B. 维生素C具有还原性,可用作水果罐头的抗氧化剂
C. 牙膏中的摩擦剂(如CaCO 、SiO 等)一般都易溶于水
3 2
D. 家庭中84消毒液杀菌、消毒过程中发生了氧化还原反应
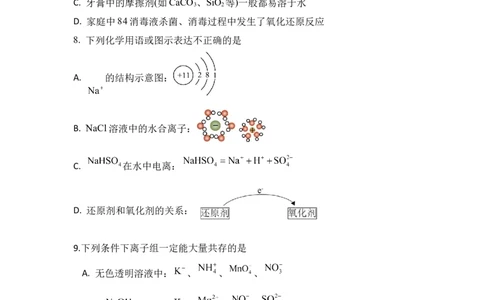
8. 下列化学用语或图示表达不正确的是
A. 的结构示意图:
B. NaCl溶液中的水合离子:
C. 在水中电离:
D. 还原剂和氧化剂的关系:
9.下列条件下离子组一定能大量共存的是
A. 无色透明溶液中: 、 、 、
B. 在 溶液中: 、 、 、
C. 含有 的溶液中: 、 、 、
D. 澄清透明溶液中: 、 、 、
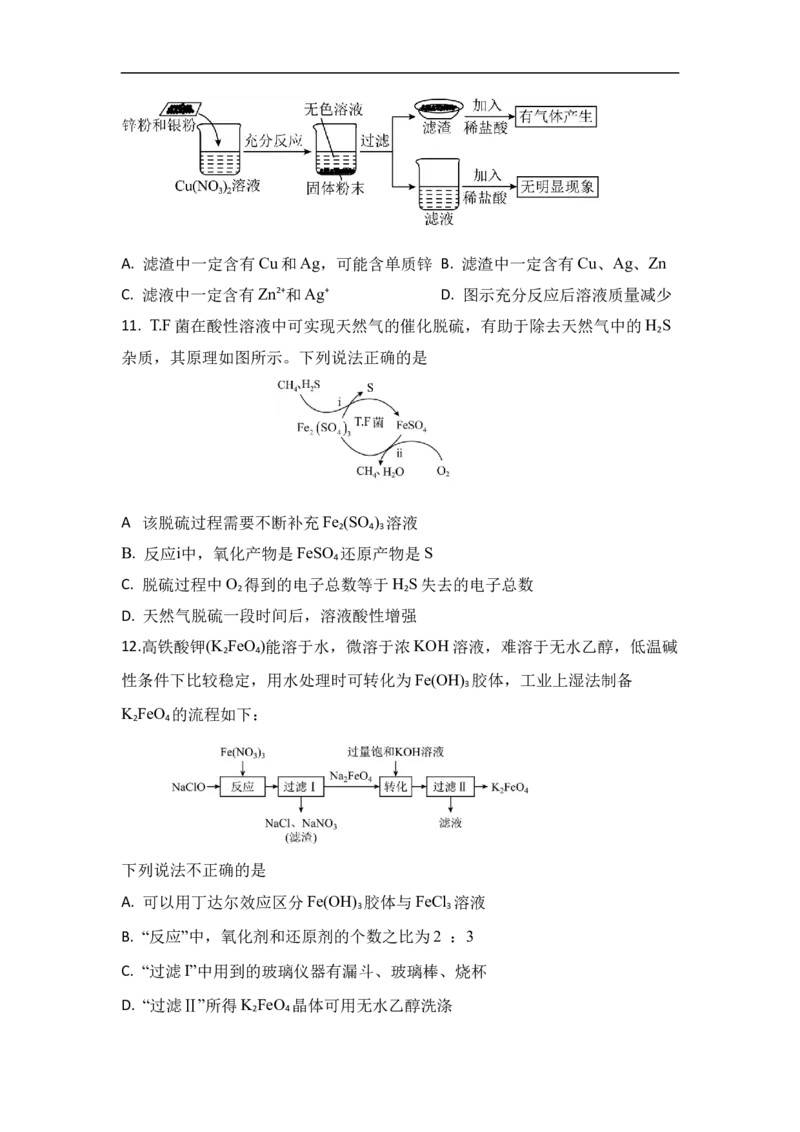
10.为了探究金属和盐溶液的反应规律,将一定质量的锌粉和银粉加入硝酸铜溶
液中,充分反应,实验过程及实验现象如下图所示,则下列说法中正确的是A. 滤渣中一定含有Cu和Ag,可能含单质锌 B. 滤渣中一定含有Cu、Ag、Zn
C. 滤液中一定含有Zn2+和Ag+ D. 图示充分反应后溶液质量减少
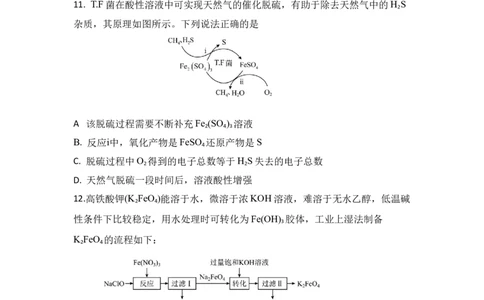
11. T.F菌在酸性溶液中可实现天然气的催化脱硫,有助于除去天然气中的H S
2
杂质,其原理如图所示。下列说法正确的是
.
A 该脱硫过程需要不断补充Fe (SO ) 溶液
2 4 3
B. 反应ⅰ中,氧化产物是FeSO 还原产物是S
4
C. 脱硫过程中O 得到的电子总数等于H S失去的电子总数
2 2
D. 天然气脱硫一段时间后,溶液酸性增强
12.高铁酸钾(K FeO )能溶于水,微溶于浓KOH溶液,难溶于无水乙醇,低温碱
2 4
性条件下比较稳定,用水处理时可转化为Fe(OH) 胶体,工业上湿法制备
3
K FeO 的流程如下:
2 4
下列说法不正确的是
A. 可以用丁达尔效应区分Fe(OH) 胶体与FeCl 溶液
3 3
B. “反应”中,氧化剂和还原剂的个数之比为2 :3
C. “过滤I”中用到的玻璃仪器有漏斗、玻璃棒、烧杯
D. “过滤Ⅱ”所得K FeO 晶体可用无水乙醇洗涤
2 413.下列离子方程式正确的是
A. 过氧化钠与二氧化碳反应:
B. H S通入氯水中:
2
C. CaCO 溶于CH COOH:
3 3
D. 将稀硫酸滴在铁片上:
14.常温下,在水溶液中发生如下反应:① ;
② ;③ 。下列说法错误的是
A. C 在反应①中是氧化产物
2
B. 氧化性由强到弱的顺序是
C. 还原性由强到弱的顺序是
D. 反应 可以进行
15.有一瓶无色透明溶液,只含 、 中的某
几种,且各离子的个数相等,进行实验:
①取少量原溶液加入足量的 溶液产生白色沉淀
②取少量原溶液加 溶液不产生沉淀
③取少量原溶液加 溶液产生白色沉淀,再加稀硝酸,白色沉淀不溶解
下列说法正确的是
A. 原溶液中一定含有的离子是:
B. 一定不含有的离子是: 、
C. 可能含有的离子是:
D. 涉及的离子方程式有:
第Ⅱ卷 非选择题
二、填空题(本卷共4小题,共55分)
16.(每空2分,共12分)铜器久置于空气(①)中会和空气中的 (②)、
(③)、 (④)作用产生“绿锈”,该“绿锈”俗称“铜绿”,又称“孔雀石”[化学式为 ,(⑤)],“铜绿”能跟盐酸(⑥)反应生成氯化铜(⑦)、
和 ,在其溶液中滴入NaOH(⑧)溶液,生成 (⑨),过滤干燥灼
烧可以得到CuO(⑩),电解氯化铜溶液可以制备Cu( )和 ( )。
⑪ ⑫
(1)上述短文标有序号 物的质中,属于混合物的是_______(填序号,下同);属
于酸性氧化物的是_______;属于碱的是_______。
(2)从物质的类别来看, 、Cu和 都属于_______。
(3)以上属于电解质的是_______。
(4)请用离子方程式表示 的生成过程:_______。
17.(每空2分,共22分)物质类别和核心元素的价态是学习元素及其化合物性
质的两个重要认识视角。下图为钠及其化合物的“价—类”二维图,回答下列
问题:
(1)物质①与水反应的离子方程式为_______,所以通常将其保存在_______中。
(2)写出淡黄色固体②与二氧化碳反应的化学方程式,并用双线桥表示其电子
转移的方向和数目:_______;将44 g CO 通过装有足量淡黄色固体②的试管完
2
全反应后,固体增重质量为______g。
(3)从核心元素价态的视角看,NaH中H元素的化合价为_____价;从H的价
态分析,常用作____(填“氧化剂”或“还原剂”),与水反应生成一种强碱和
可燃性气体,反应的化学方程式为_____。室温下NaH能结合CO 制氢:
2,该反应中氧化产物和还原产物的个数之比为
_____。
(4)将一小块①投入 溶液中,观察到的现象是___________(填序号)。
发生反应的总反应化学方程式为___________。
①浮于液面上;②熔化成小球;③发出嘶嘶的响声,放出气体;④有蓝色沉淀
产生;⑤析出大量红色的铜。
(5)汽车安全气囊的气体发生剂 可由金属钠生产。某汽车安全气囊内含
、 和 等物质。当汽车发生较严重的碰撞时,引发 分解
,从而为气囊充气,产生的Na立即与 发生置换反应
生成白色固体②,写出该反应的化学方程式___________。
18.(除注明外每空2分,共9分) 高铁酸钾( )是一种新型绿色消毒剂,
主要用于饮用水处理。它在温度低于 或强碱性条件下相当稳定,其稳定性
随酸性增强而降低,其氧化性随酸性增强而逐渐显现。
(1)NaClO碱溶液中倒入硝酸铁溶液,可以生成高铁酸钠,请配平其离子方程
式:
_____ ____ ___ ____=___ _____ ____。(3
分)
得到高铁酸钠晶体后,用饱和 溶液转化:
,则反应后体系的导电能力_____(选填
“增强”,“减弱”,“不变”,“不一定”)
(2)实验室也可以用氯气与 在氢氧化钾溶液中反应制备少量 ,
该反应中每制得 ,消耗的氯气质量为_______g;在高铁酸钾溶液中
滴加盐酸,有黄绿色氯气产生,原因是_______(用文字描述)。19. (共12分,每空2分)空气与我们的生存息息相关。SO 是主要的大气污
2
染物之一,CO 是主要的温室气体。
2
(1)SO 属于酸性氧化物,下列物质中可以与其发生反应的是___________。
2
A.Na O B.NaCl C.CO D.H O
2 2 2
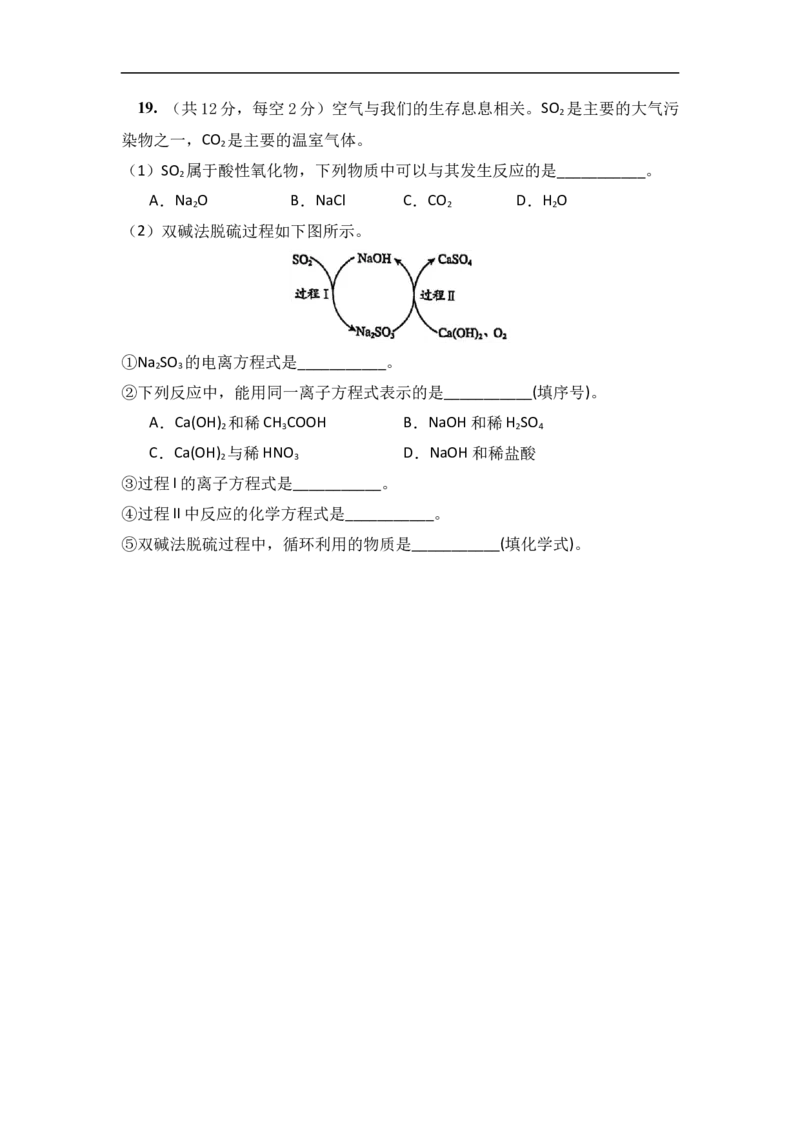
(2)双碱法脱硫过程如下图所示。
①Na SO 的电离方程式是___________。
2 3
②下列反应中,能用同一离子方程式表示的是___________(填序号)。
A.Ca(OH) 和稀CH COOH B.NaOH和稀H SO
2 3 2 4
C.Ca(OH) 与稀HNO D.NaOH和稀盐酸
2 3
③过程I的离子方程式是___________。
④过程II中反应的化学方程式是___________。
⑤双碱法脱硫过程中,循环利用的物质是___________(填化学式)。高 2025 级高一上期第二次月考试卷
化学参考答案
一、选择题(每题3分,共45分)
1.C 2.A 3.B 4.A 5.A 6.D 7.C 8.A 9.D 10.B
11.C 12.B 13.C 14.C 15.D
二、填空题
16. (每空2分,共12分)
(1) ①. ①⑥ ②. ③ ③. ⑧⑨
(2)单质 (3)②⑤⑦⑧⑨⑩
(4)
17. (每空2分,共22分)
(1) ①. ②. 煤油或石蜡油
(2) 28 (3) ①. -1 ②. 还原剂 ③.
2:1
(4) ①②③④
(5)
18. (除注明外每空2分,共9分)
(1) ①. 3 2 4 10 OH-=2 3 5HO (3分)
2
②. 减弱
(2) ①. 213 ②. 酸性条件下, 表现强氧化性,将HCl氧化生成氯气
19.(每空2分,共12分)
(1)AD
(2) BCD注:合理答案酌情给分