文档内容
考点 23 化学平衡常数
【基础过关】
1.一定温度下,反应MgCl (l) Mg(l)+Cl (g)达到平衡时,下列说法错误的是( )
2 2
A.该反应的平衡常数K=c(Cl )
2
B.将容器体积压缩为原来一半,当体系再次达到平衡时,Cl 的浓度增大
2
C.减小氯气浓度,平衡正向移动,平衡常数不变
D.温度升高该反应的化学平衡常数K增大
【答案】B
【解析】A项,化学平衡常数(固体或液体纯物质一般不列入平衡常数)是指反应达到平衡时,各生成
物浓度的化学计量数次幂的乘积与各反应物浓度的化学计量数次幂的乘积的比值,则该反应的平衡常数
K=c(Cl ),故A正确;B项,K=c(Cl ),温度不变,平衡常数不变,因此将容器体积压缩为原来一半,当体
2 2
系再次达到平衡时,Cl 的浓度不变,故B错误;C项,平衡常数只与温度有关,温度不变,平衡常数不变,
2
故C正确;D项,镁在氯气中燃烧是放热反应,则MgCl (l) Mg(l)+Cl (g)为吸热反应,升高温度,平
2 2
衡正向移动,平衡常数K增大,故D正确;故选B。
2.(2023·安徽省皖江名校高三第四次联考)在PdCl -CuCl 做催化剂和适宜的温度条件下,用O 将HCl
2 2 2
氧化为Cl:4HCl(g)+O (g)=2HO(g)+2Cl (g) ΔH<0,下列有关说法不正确的是( )
2 2 2 2
A.降低温度,可提高Cl 产率
2
B.提高 ,该反应的平衡常数增大
C.若断开1molH-Cl键的阿时有1molH-O键断开,则表明该反应达到平衡状态
D.该反应的平衡常数表达式
【答案】B
【解析】A项,此反应正向为放热反应,降低温度,平衡正向移动,可提高氯气产率,A正确;B项,
温度不变,平衡常数不变,B不正确;C项,若断开1mol H-Cl键的同时有1molH-O键断开,说明正逆反
应速率相等,则表明该反应达到平衡状态,C正确;D项,各组分均为气体,平衡常数表达式正确,D正
确。故选B。
3.加热NO ,依次发生的分解反应为①NO NO +O ,②NO NO+O ;在2 L密闭
2 5 2 5 2 3 2 2 3 2 2
容器中充入8 mol N O ,加热到t ℃,达到平衡状态后O 为9 mol,NO 为3.4 mol。则t ℃时反应①的平
2 5 2 2 3
衡常数为( )
A.10.7 B.8.5 C.9.6 D.10.2
资料整理【淘宝店铺:向阳百分百】【答案】B
【解析】题设中有两个反应,可理解为先发生反应①,其中生成的NO 有一部分再发生分解反应②,
2 3
且在两个反应中都有O 生成,再由已知条件列方程组求解。设反应①中生成NO 物质的量浓度为x,反应
2 2 3
②中生成NO物质的量浓度为y。则:
2
NO(g) NO(g)+O(g)
2 5 2 3 2
起始浓度/(mol·L−1) 4 0 0
转化浓度/(mol·L−1) x x x
平衡浓度/(mol·L−1) 4−x x x
NO(g) NO(g)+O(g)
2 3 2 2
起始浓度/(mol·L−1) x 0 0
转化浓度/(mol·L−1) y y y
平衡浓度/(mol·L−1) x−y y y
依题意O 的平衡浓度为x+y=4.5 mol·L−1,NO 的平衡浓度为x−y=1.7 mol·L−1,解得x=3.1 mol·L−1
2 2 3
,y=1.4 mol·L−1,NO 的平衡浓度为4 mol·L−1−3.1 mol·L−1=0.9 mol·L−1,NO的平衡浓度为1.4 mol·L−1,
2 5 2
则反应①的平衡常数K=(1.7×4.5)/0.9=8.5。
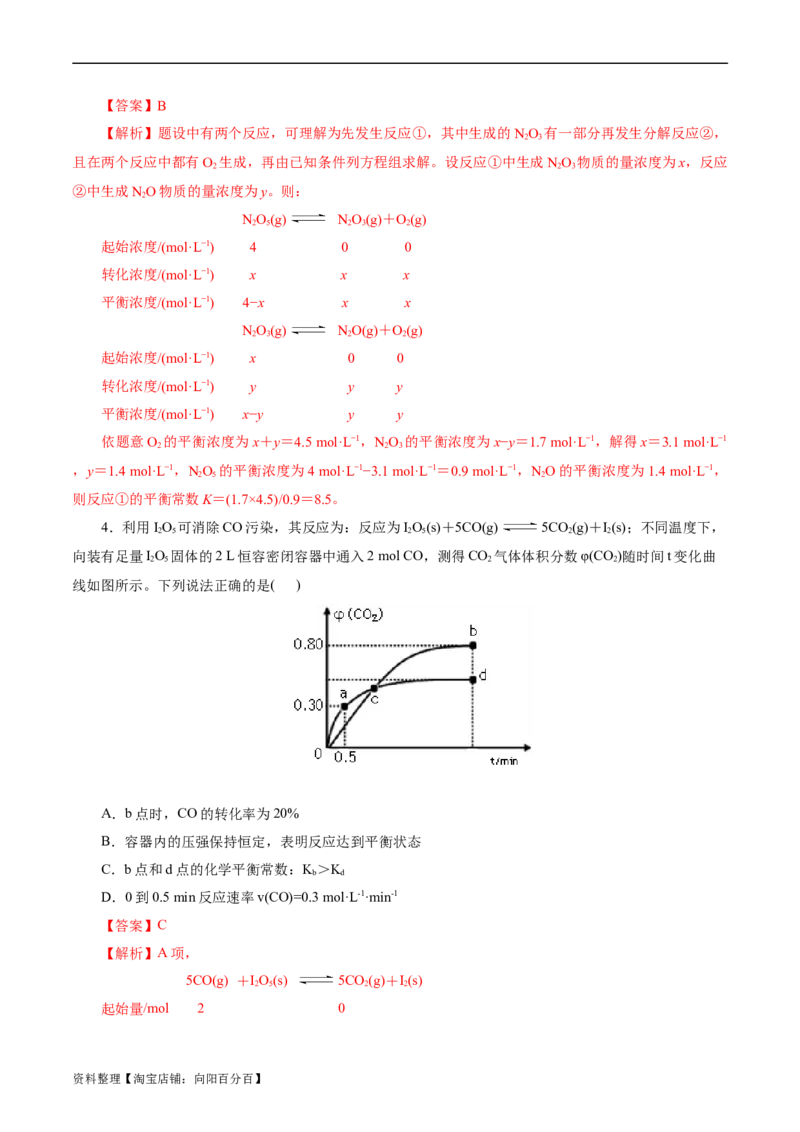
4.利用IO 可消除CO污染,其反应为:反应为IO(s)+5CO(g) 5CO(g)+I(s);不同温度下,
2 5 2 5 2 2
向装有足量IO 固体的2 L恒容密闭容器中通入2 mol CO,测得CO 气体体积分数φ(CO)随时间t变化曲
2 5 2 2
线如图所示。下列说法正确的是( )
A.b点时,CO的转化率为20%
B.容器内的压强保持恒定,表明反应达到平衡状态
C.b点和d点的化学平衡常数:K>K
b d
D.0到0.5 min反应速率v(CO)=0.3 mol·L-1·min-1
【答案】C
【解析】A项,
5CO(g) +IO(s) 5CO(g)+I(s)
2 5 2 2
起始量/mol 2 0
资料整理【淘宝店铺:向阳百分百】转化量/mol y y
b点量/mol 2-y y
根据b点时CO 的体积分数φ(CO)=y÷2=0.80,得y=1.6mol,转化率等于=(变化量÷起始
2 2
量)×100%=(1.6÷2)×100%=80%,A错误;B项,两边计量数相等,所以压强始终不变,不能做平衡状态的
标志,B错误;C项,b点比d点时生成物CO 体积分数大,说明进行的程度大,则化学平衡常数:K>
2 b
K,C正确;D项,0到0.5min时:
d
5CO(g) +IO(s) 5CO(g)+I(s)
2 5 2 2
起始量/mol 2 0
转化量/mol x x
a点量/mol 2-x x
根据a点时CO 的体积分数φ(CO)=x÷2=0.30,得x=0.6mol;则从反应开始至a点时的反应速率为
2 2
v(CO)=(0.6mol÷2L)÷0.5min=0.6 mol·L-1·min-1,D错误。故选C。
5.在PdCl -CuCl 做催化剂和适宜的温度条件下,用O 将HCl氧化为Cl:4HCl(g)+O (g)=2HO(g)
2 2 2 2 2 2
+2Cl(g) ΔH<0,下列有关说法不正确的是( )
2
A.降低温度,可提高Cl 产率
2
B.提高 ,该反应的平衡常数增大
C.若断开1molH-Cl键的阿时有1molH-O键断开,则表明该反应达到平衡状态
D.该反应的平衡常数表达式
【答案】B
【解析】A项,此反应正向为放热反应,降低温度,平衡正向移动,可提高氯气产率,A正确;B项,
温度不变,平衡常数不变,B不正确;C项,若断开1mol H-Cl键的同时有1molH-O键断开,说明正逆反
应速率相等,则表明该反应达到平衡状态,C正确;D项,各组分均为气体,平衡常数表达式正确,D正
确。故选B。
6.(2023·河北省部分学校高三联考)高炉炼铁中的一个反应为FeO(s)+CO(g) Fe(s)+CO (g) ΔH>
2
0,在1100℃下,若CO起始浓度为1.2mol/L,10min后达到平衡时 的体积分数为 ,下列说法错误的
是( )
A.1100℃下,此反应的平衡常数
B.达到平衡过程中,反应的平均速率为v(CO)=0.02 mol·L-1·min-1
资料整理【淘宝店铺:向阳百分百】C.达到平衡后,若增大c(CO),则达到新平衡时, 增大
2
D.测得某时刻c(CO)=0.8mol/L,则此时
【答案】C
【解析】列三段式:
平衡时CO 的体积分数 ,解得 ,c(CO)=1mol/L,c(CO)=0.2mol/L。A项,
2 2
1100℃下此反应的平衡常数 ,A 正确; B 项,反应的平均速率为
,B正确;C项,该反应属于反应前后气体分子数不变的反应,加压平
衡不移动。该反应生成物中只有CO 是气体,达到平衡后,若增大c(CO),等效于加压,平衡不移动,则
2 2
达到新平衡时, 不变,C错误;D项,达到平衡时,c(CO)=1mol/L,测得某时刻c(CO)=0.8mol·L-
1,说明反应还未达到平衡,平衡逆向进行,则此时 ,D正确; 故选C。
7.(2023·江西省九江市十校高三联考)向体积均为1L的两恒容容器中分别充入2molX和1molY发生反
应:2X(g)+Y(g) Z(g) ΔH,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化
曲线如图所示。下列说法不正确的是( )
资料整理【淘宝店铺:向阳百分百】A.a点平衡常数: B.气体的总物质的量:n<n
a c
C.ΔH<0 D.平衡转化率:甲<乙
【答案】A
【解析】A项,a设Z平衡物质的量为x,列出三段式:
恒温恒容条件下,气体的压强之比等于物质的量之比,则 x=0.75mol,
,c点平衡常数为12,甲容器时绝热容器,实际上达到平衡时温度升高,
平衡逆向进行,故a点的平衡常数K<12,A错误;B项,a、c两点压强相等,容积体积相等,依据阿伏
伽德罗定律,此时气体的物质的量与温度成反比,需注意a点温度比c点对应温度高,则气体总物质的量
n<n,B正确;C项,由图像可知,在容器甲中是绝热条件下,开始压强增大,说明反应温度升高,故反
a c
应为放热ΔH<0,C正确;D项,甲在绝热条件下的反应,该反应是放热反应,相当于升高温度,平衡逆
向进行,所以平衡转化率,甲<乙,D正确;故选A。
8.合成氨是人类科学技术发展史上的一项重大突破,目前工业上用氢气和氮气直接合成氨:N(g)
2
+3H (g) 2NH (g)。T℃时,在2L恒容密闭容器中加入1.2molN 和2molH 模拟一定条件下工业固氮,
2 3 2 2
体系中n(NH )随时间的变化如图所示。下列说法错误的是( )
3
A.2min内NH 的平均反应速率为0.1125mol∙L−1∙min−1
3
B.T℃时,从2min到4min,反应的平衡常数增大
C.容器内压强不再变化说明反应达到平衡,且2υ (H )=3υ (NH )
正 2 逆 3
D.T℃时,该反应的平衡常数为6.25L2∙mol−2
【答案】B
资料整理【淘宝店铺:向阳百分百】【解析】A项,2min内NH 的平均反应速率为 ,故A正确;
3
B项,T℃时,从2min到4min,反应的平衡常数不变,平衡常数只与温度有关,温度不变,平衡常数不变,
故B错误;C项,该反应是体积减小的反应,当容器内压强不再变化说明反应达到平衡,根据速率之比等
于计量数之比得到2υ (H )=3υ (NH ),故C正确;D项,T℃时,平衡是氨气物质的量为0.8mol,则氮气
正 2 逆 3
消耗0.4mol,剩余氮气0.8mol,氢气消耗1.2mol,剩余氢气0.8mol,因此该反应的平衡常数为
,故D正确。故选B。
9.硫酸工业中,将SO 氧化为SO 是生产工艺中的重要环节。在温度为T 条件下,在三个容积均为
2 3 1
1L的恒容密闭容器中仅发生反应:2SO (g)+O(g) 2SO (g)ΔH<0,实验测得:v =k ·c2(SO )·c(O),v
2 2 3 正 正 2 2
=k ·c2(SO )。
逆 逆 3
起始浓度/(mol·L-1) 平衡浓度/(mol·L-1)
容器编号
c(SO ) c(O) C(SO ) c(O)
2 2 3 2
I 0.6 0.3 0 0.2
II 0.5 x 0.3
III 0.3 0.25 0.2
已知:k 、k 为速率常数,仅受温度的影响。
正 逆
下列说法错误的是( )
A.达到平衡时,平衡常数和速率常数的关系:
B.若容器II中达到平衡时 =1,则x=0.85
C.容器III中达到平衡时,c(O)<0.25mol·L-1
2
D.当温度升高为T 时,k 、k 分别增大m倍和n倍,则mK,
此时平衡向逆反应方向移动,则平衡时O 的浓度c(O)>0.25mol·L-1,C项错误;D项,ΔH<0,温度升高,
2 2
平衡向逆反应方向移动,k 增大的幅度更大,n>m,D项正确。故选C。
逆
10.某温度时两个恒容密闭容器中仅发生反应2NO(g)+O (g) 2NO (g) ΔH>0。实验测得:
2 2
, , 、 为速率常数,只受温度影响。
起始浓度 (mol/L) 平衡浓度(mol/L)
容器编号
c(NO ) c(NO) c(O) c(O)
2 2 2
Ⅰ 0.6 0 0 0.2
Ⅱ 0.6 0.1 0
下列说法不正确的是( )
A.升高温度,该反应的化学平衡常数增大
B.Ⅰ中NO 的平衡转化率约为66.7%
2
C.Ⅱ中达到平衡状态时,c(O)>0.2 mol·L−1
2
D.该反应的化学平衡常数可表示为
【答案】C
【解析】先用三段式法计算出实验Ⅰ中各组分的改变浓度和平衡浓度:
资料整理【淘宝店铺:向阳百分百】