文档内容
考点 24 化学反应的方向
【基础过关】
1.下列过程是非自发的是( )
A.水由高处向低处流 B.氯气和溴化钾溶液的反应
C.铁在潮湿空气中生锈 D.室温下水结成冰
【答案】D
【解析】A项,水由高处向低处流,是自发进行的过程,故A不选;B项,氯气的氧化性比溴强,氯
气能够与KBr溶液发生置换反应,属于自发进行的过程,故B不选;C项,铁生锈为自发进行的氧化还原
反应,反应放热,常温下可自发进行,故C不选;D项,室温下冰会自发的融化,室温下水结成冰不是自
发进行的过程,故D选;故选D。
2.下列过程是非自发过程的是( )
A.气体的扩散 B.室温下水结成冰
C.水由高处向低处流 D.有序排列的火柴散落成无序排列
【答案】B
【解析】A项,气体扩散,分子自由移动,自发进行,A不符合题意;B.水结成冰这个变化,虽然
是放热的,但是同时也是熵减的,因此必须在某一温度(0°C)以下才能自发进行,要在室温下结成冰需借助
外力,B符合题意;C.水由高处向低处流势能减小,自发进行,C不符合题意;D.有序排列的火柴散落
成无序排列,体系混乱度增大,为自发过程,D不符合题意;故选B。
3.下列说法正确的是( )
A.凡是放热反应都是自发的 B.铁在潮湿空气中生锈是自发过程
C.熵增大的反应都是自发反应 D.电解池的反应是属于自发反应
【答案】B
【解析】A项,所有放热反应△H>0,但焓变和温度未知,所以不一定都是自发反应,选项A错误;
B项,铁生锈是发生了电化学的吸氧腐蚀,是自发进行反应,选项B正确;C项,依据△H-T S<0判断反
应是自发进行的反应,熵增的反应只能是△S>0,熵变和温度未知,所以不一定都是自发反应△,选项C错
误;D项,电解反应可以是自发反应,也可以是非自发的氧化还原反应,选项D错误;故选B。
4.知道了某过程有自发性之后,则( )
A.可判断出过程的方向 B.可确定过程是否一定会发生
C.可预测过程发生完成的快慢 D.可判断过程的热效应
【答案】A
【解析】判断某反应是否自发,只是判断反应的方向,与是否会发生、反应的快慢、反应的热效应无
关。
5.下列反应在任何温度下均能自发进行的是( )
资料整理【淘宝店铺:向阳百分百】A.2N(g)+O(g)===2N O(g) ΔH=163 kJ·mol-1
2 2 2
B.Ag(s)+Cl(g)===AgCl(s) ΔH=-127 kJ·mol-1
2
C.HgO(s)===Hg(l)+O(g) ΔH=91 kJ·mol-1
2
D.HO(l)===O(g)+HO(l) ΔH=-98 kJ·mol-1
2 2 2 2
【答案】D
【解析】对于A项,ΔH>0,ΔS<0,在任何温度下,ΔH-TΔS>0,即任何温度下反应都不能自发进行;
对于B项,ΔH<0,ΔS<0,在较低温度下,ΔH-TΔS<0,即低温下反应能自发进行;对于C项,ΔH>0,
ΔS>0,若使反应自发进行,即ΔH-TΔS<0,必须升高温度,即反应只有在较高温度时能自发进行;对于
D项,ΔH<0,ΔS>0,在任何温度下,ΔH-TΔS<0,即在任何温度下反应均能自发进行。
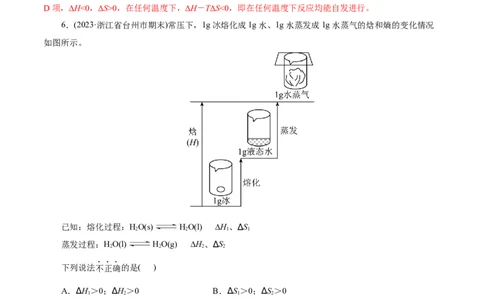
6.(2023·浙江省台州市期末)常压下,1g冰熔化成1g水、1g水蒸发成1g水蒸气的焓和熵的变化情况
如图所示。
已知:熔化过程:HO(s) HO(l) ∆H、∆S
2 2 1 1
蒸发过程:HO(l) HO(g) ∆H、∆S
2 2 2 2
下列说法不正确的是( )
A.∆H>0;∆H>0 B.∆S>0;∆S>0
1 2 1 2
C. ∆S>∆S D.蒸发过程属于高温自发过程
1 2
【答案】C
【解析】A项,水由固态转化为液态吸收能量,熔化过程为吸热过程,则∆H>0,蒸发过程为吸热过
1
程,则∆H>0,A正确;B项,同种物质不同状态的混乱度:g>l>s,混乱度越大熵变值越大,则∆S>0;
2 1
∆S>0,B正确;C项,蒸发过程熵变值更大,即∆S>∆S,C错误;D项,蒸发过程∆H>0,∆S>0,
2 2 1 2 2
根据自发进行的判据:ΔG=ΔH-TΔS <0,该反应需要高温条件自发进行,D正确;故选C。
2
7.已知凡气体分子总数增多的反应一定是熵增大的反应。一定条件下,下列反应不能自发进行的是(
)
资料整理【淘宝店铺:向阳百分百】A.2O(g)=3O(g) ΔH<0 B.2CO(g)=2C(s)+O (g) ΔH>0
3 2 2
C.N(g)+3H(g) 2NH (g) ΔH<0 D.CaCO (s)=CaO(s)+CO (g) ΔH>0
2 2 3 3 2
【答案】B ⇌
【解析】利用ΔG= H-TΔS进行分析,凡ΔG<0的反应,能自发进行。A项,反应2O(g)=3O(g),
3 2
ΔH<0,ΔS>0,该反应一△定能自发进行,A不合题意; B项,反应2CO(g)=2C(s)+O
2
(g),ΔH>0,ΔS<0,
该反应一定不能自发进行,B符合题意;C项,反应N(g)+3H(g) 2NH (g),ΔH<0,ΔS<0,该反
2 2 3
应在低温下能自发进行,C不合题意;D项,反应CaCO (s)=CaO(s)+CO (g),ΔH>0,ΔS>0,该反应在高温
3 2
下能自发进行,D不合题意;故选B。
8.25 ℃、1.01×105Pa时,反应2NO(g)=4NO (g)+O(g) ΔH=+109.8 kJ·mol-1,该反应能自发进行的
2 5 2 2
原因是( )
A.该反应是吸热反应 B.该反应是放热反应
C.该反应是熵减小的反应 D.该反应的熵增大效应大于能量效应
【答案】D
【解析】该反应是吸热反应,能够自发进行是由于该反应为熵增大的反应,并且熵增效应大于能量效
应。
9.下列说法正确的是( )
A.凡是放热反应都是自发的,因为吸热反应都是非自发的
B.自发反应的熵一定增大,非自发反应的熵一定减小
C.常温下,反应C(s)+CO(g) 2CO(g)不能自发进行,则该反应的ΔH>0
2
D.反应2Mg(s)+CO (g)=C(s)+2MgO(s)能自发进行,则该反应的ΔH>0
2
【答案】C
【解析】反应的自发性是由熵变和焓变共同决定的,若 ΔH<0,ΔS>0,则一定自发,若 ΔH>0,
ΔS<0,则一定不能自发,若ΔH<0,ΔS<0或ΔH>0,ΔS>0,反应能否自发,和温度有关,A错误、B错误;
该反应的ΔS>0,若ΔH<0,则一定自发,现常温下不自发,说明ΔH>0,C正确;该反应的ΔS<0,能自发,
说明ΔH<0,D错误。
10.下列说法正确的是( )
A.ΔH<0、ΔS>0的反应在温度低时不能自发进行
B.NH HCO (s)=NH (g)+HO(g)+CO(g) ΔH=+185.57 kJ/mol能自发进行,原因是体系有自发地向
4 3 3 2 2
混乱度增加的方向转变的倾向
C.焓变和熵变都与反应的自发性有关,因此焓变或熵变均可单独作为反应自发性的判据
D.在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向
【答案】B
【解析】A项,根据ΔH+TΔS<0反应能自发进行判断ΔH<0、ΔS>0的反应在任何温度下都能自发进
资料整理【淘宝店铺:向阳百分百】行,错误;B项,根据ΔH+TΔS<0反应能自发进行判断,NH HCO (s)===NH (g)+HO(g)+CO(g) ΔH=
4 3 3 2 2
+185.57 kJ/mol能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向,正确;C项,焓变
和熵变都与反应的自发性有关,但焓变或熵变均不能单独作为反应自发性的判据,错误;D项,在其他外
界条件不变的情况下,使用催化剂,不能改变化学反应进行的方向,错误。
11.已知凡气体分子总数增多的反应一定是熵增大的反应。一定条件下,下列反应不能自发进行的是(
)
A.2O(g)=3O(g) ΔH<0 B.2CO(g)=2C(s)+O (g) ΔH>0
3 2 2
C.N(g)+3H(g) 2NH (g) ΔH<0 D.CaCO (s)=CaO(s)+CO (g) ΔH>0
2 2 3 3 2
【答案】B
【解析】利用ΔG= H-TΔS进行分析,凡ΔG<0的反应,能自发进行。A项,反应2O(g)=3O(g),
3 2
ΔH<0,ΔS>0,该反应一△定能自发进行,A不合题意; B项,反应2CO(g)=2C(s)+O
2
(g),ΔH>0,ΔS<0,
该反应一定不能自发进行,B符合题意;C项,反应N(g)+3H(g) 2NH (g),ΔH<0,ΔS<0,该反
2 2 3
应在低温下能自发进行,C不合题意;D项,反应CaCO (s)=CaO(s)+CO (g),ΔH>0,ΔS>0,该反应在高温
3 2
下能自发进行,D不合题意;故选B。
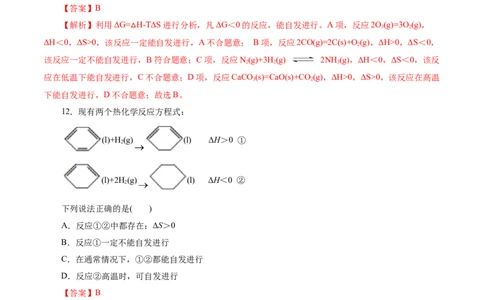
12.现有两个热化学反应方程式:
(l)+H (g) (l) ΔH>0 ①
2
(l)+2H (g) (l) ΔH<0 ②
2
下列说法正确的是( )
A.反应①②中都存在:ΔS>0
B.反应①一定不能自发进行
C.在通常情况下,①②都能自发进行
D.反应②高温时,可自发进行
【答案】B
【解析】A项,由题中热化学反应方程式可知,反应①②均为熵减反应,即ΔS<0,A项错误;B项,
由题可知,反应①ΔH>0,ΔS<0,则ΔH-TΔS>0,所有温度下反应都不能自发进行,B项正确;项,由
B项可知,反应①在所有温度下都不能自发进行;反应②的ΔH<0,ΔS<0,则在低温条件下,ΔH-TΔS<
0,即反应②低温时,可自发进行,C项错误;D项,由题可知,反应②ΔH<0,ΔS<0,则在低温条件下,
ΔH-TΔS<0,即反应②低温时,可自发进行,D项错误;故选B。
13.某化学反应A(s)=D(g)+E(g) ΔH-TΔS=(-4500+11T)kJ·mol-1(其中ΔH为焓变,ΔS为熵变,T为热
力学温度,单位为K),要防止反应发生,温度必须( )
资料整理【淘宝店铺:向阳百分百】A.高于409 K B.低于136 K
C.高于136 K而低于409 K D.低于409 K
【答案】A
【解析】要防止反应发生,ΔH-TΔS>0,则-4500+11T>0,解得T>409,故选A。
14.反应进行的方向是化学反应原理的三个重要组成部分之一、下列说法中正确的是( )
A. , 的反应一定可以自发进行
B.根据反应的自发性可以预测该反应发生的快慢
C.可逆反应正向进行时,正反应具有自发性, 一定小于零
D.常温下,反应C(s)+ CO (g) 2CO(g)不能自发进行,该反应的ΔH>0
2
【答案】D
【解析】A项,ΔG<0,反应自发进行,由ΔG =ΔH -TΔS可知,若ΔH>0,ΔS>0,则在低温下ΔG
可能大于0,反应非自发,A项错误;B项,反应的自发性只能判断反应的方向,不能确定反应的快慢,B
项错误;C项,可逆反应正向进行时,由ΔG =ΔH -TΔS可知,若ΔH>0,ΔS>0且高温条件下正反应具有
自发性,C项错误;D项,ΔH -TΔS>0,反应非自发进行,反应ΔS>0,满足ΔH -TΔS>0,则ΔH>0,D
项正确;故选D。
15.(2023·浙江省部分校高三模拟考试)下列说法正确的是( )
A.相同温度和压强下,熵值:1 mol C(s,金刚石)>1 mol C(s,石墨)
B.Ca(g)→Ca2+(g)+2e- ΔH小于0
C.NH NO 溶于水,ΔH>0,ΔS<0
4 3
D.分子间氢键数量:1 molHO(g) <1 molHO(l) <1 molHO(s)
2 2 2
【答案】D
【解析】A项,由于金刚石中C的排列比石墨中的C的排列更有序,所以1 mol C(s,金刚石)的熵值
<1 mol C(s,石墨),A错误;B项,原子失电子变成离子需要吸收热量,则Ca(g)→Ca2+(g)+2e- ΔH大于
0,故B错误;C项,NH NO 溶于水为吸热过程,混乱度增大,故ΔH>0,ΔS>0,C错误;D项,冰→
4 3
液态水→水蒸气,破坏分子间氢键和范德华力,分子间氢键数量:1 molHO(s)>1 molHO(l)>1
2 2
molH O(g),故D正确;故选D。
2
16.已知体系自由能变化 时反应能自发进行.两个氢化反应的 与温度的关
系如图所示,下列说法正确的是( )
资料整理【淘宝店铺:向阳百分百】A.反应①的∆S<0 B.反应②在 时的反应速率很快
C.温度大于 时,反应①能自发进行 D.反应②的∆H>0
【答案】C
【解析】由图像分析可知:反应①随温度的升高,∆G逐渐减小;反应②随温度的升高∆G逐渐增大,
结合∆G =∆H -T∆S分析解答。A项,反应①随温度的升高,∆G逐渐减小,则∆S>0,故A错误;B项,
该题我们可以推测自发反应时的温度,但无法推测什么温度的反应快慢,故B错误;C项,因∆G<0时,
反应能自发进行,反应①在温度大于1000℃时∆G<0,故此时反应①能自发进行,故C正确;D项,根据
数学知识可知,∆H为该图像的截距,而反应而的截距小于0,故∆H<0,故D错误;故选C。
17.假定X 与Y 都是理想气体(气体本身不占体积,不考虑气体间相互作用,不考虑碰撞能量损失),
2 2
在如图所示的过程中,下列说法正确的是( )
A.若X、Y 均为O,则 ,混合过程自发进行
2 2 2
B.若X、Y 均为O,则 ,混合过程不自发
2 2 2
C.若X、Y 分别为N 与O,则 ,混合过程自发进行
2 2 2 2
D.若X、Y 分别为N 与O,则 ,混合过程不自发
2 2 2 2
【答案】C
【解析】A项,若 X 、Y 均为O,混合前后气体浓度、分压、温度均相同,则 ΔS=0 ,混合过程
2 2 2
自发进行,A错误;B项,若 X 、Y 均为O,混合前后气体浓度、分压、温度均相同,则 ΔS=0 ,混合
2 2 2
过程自发进行,B错误;C项,若 X 、 Y 分别为 N 与 O ,混合前后气体温度均相同,但浓度、分
2 2 2 2
压均减小,则 ΔS>0 ,混合过程自发进行,C正确;D项,若 X 、 Y 分别为 N 与 O ,混合前后气
2 2 2 2
体温度均相同,但浓度、分压均减小,则 ΔS>0 ,混合过程自发进行,D错误;故选C。
资料整理【淘宝店铺:向阳百分百】18.下列对化学反应预测正确的是( )
选项 化学方程式 已知条件 预测
A M(s)==X(g)+Y(s) ΔH>0 它是非自发反应
B W(s)+xG(g)=4Q(g) ΔH>0,自发反应 x可能等于1、2、3
C W(s)+xG(g)=4Q(g)+6G(g) 能自发反应 ΔH一定小于0
D 4M(s)+N(g)+2 W(l)=4Q(s) 常温下,自发进行 ΔH>0
【答案】B
【解析】A项,该反应的反应物是固体,生成了气体,所以ΔS>0,该反应的ΔH>0,所以该反应在高
温下自发,故A错误;B项,该反应ΔH>0,能自发进行,则ΔS>0,所以x可能等于1、2、3,故B正确;
C项,该反应是气体系数之和增大的反应,所以ΔS>0,该反应能自发,则ΔH>0,故C错误;D项,该反
应的反应物有气体,反应后无气体,则ΔS<0,该反应常温下能自发进行,则ΔH应该小于0,故D错误;
故选B。
19.已知在100 kPa、298.15 K时石灰石分解反应:
CaCO (s)=CaO(s)+CO (g) ΔH=178.3 kJ·mol-1 ΔS=160.4 J·(mol·K)-1,则:
3 2
(1)该反应 (填“能”或“不能”)自发进行。
(2)据本题反应数据分析,温度 (填“能”或“不能”)成为反应方向的决定因素。
(3)若温度能决定反应方向,则该反应自发进行的最低温度为 。
【答案】(1)不能 (2)能 (3)1 111.6 K
【解析】(1)ΔG=ΔH-TΔS=178.3 kJ·mol-1-298.15 K×160.4×10-3 kJ·(mol·K)-1≈130.5 kJ·mol-1>0,所以该反
应不能自发进行(2)因为该反应ΔH>0、ΔS>0,所以根据ΔG=ΔH-TΔS可知,在温度较高的时候,ΔG可能
小于0(3)根据ΔG=ΔH-TΔS<0时,反应可自发进行,则有:T>ΔH/ΔS≈1 111.6 K。
20.已知甲烷隔绝空气在不同温度下有可能发生如下两个裂解反应:①CH(g) C(s)+2H(g);
4 2
②2CH(g) C H(g)+3H(g)某同学为了得到用天然气制取炭黑的允许温度范围和最佳温度,在图书馆中
4 2 2 2
查到了如下热力学数据:
反应①的ΔH(298 K)=+74.848 kJ·mol-1,ΔS(298 K)=+80.674 J·mol-1·K-1。
反应②的ΔH(298 K)=+376.426 kJ·mol-1,ΔS(298 K)=+220.211 J·mol-1·K-1。
已知焓变和熵变随温度变化很小。请参考上述信息,回答下列问题:
(1)这两个反应在 (填“高温”或“低温”)下自发进行。
(2)反应①在常温下 (填“能”或“不能”)自发进行。
(3)制取炭黑的允许温度范围为 。
(4)为了提高甲烷的炭化程度,下面四个温度中最合适的是 (填字母)
A.905.2 K B.927 K C.1273 K D.2000 K
资料整理【淘宝店铺:向阳百分百】【答案】(1)高温 (2)不能 (3)927.8~1790.4 K (4)C
【解析】(1)该反应是吸热的熵增反应,在高温下自发进行。(2)ΔH-TΔS=74.848 kJ·mol-1-80.674×10-3
kJ·mol-1·K-1×298 K=50.807 kJ·mol-1>0,所以该反应在常温下不能自发进行。(3)甲烷裂解为炭黑和氢气时,
ΔH-TΔS=74.848 kJ·mol-1-80.674×10-3 kJ·mol-1·K-1×T<0,解得T>927.8 K;裂解为乙炔时,ΔH-TΔS=376.426
kJ·mol-1-220.211×10-3 kJ·mol-1·K-1×T<0,解得T>1709.4 K,即温度高于1709.4 K时自发裂解为乙炔和氢气
所以要制取炭黑,必须控制温度在927.8~1790.4 K。(4)要提高甲烷的炭化程度,应在927.8~1790.4 K的范
围内尽可能提高温度。
21.有A、B、C、D四个反应:
反应 A B C D
ΔH/(kJ·mol-1) 10.5 1.80 -126 -11.7
ΔS/(J·mol-1·K-1) 30.0 -113.0 84.0 -105.0
(1)在任何温度下都能自发进行的反应是______;
(2)任何温度下都不能自发进行的反应是______;
(3)另两个反应中,在温度高于______℃时可自发进行的反应是______;在温度低于______℃时可自发
进行的反应是______。
【答案】(1)C (2)B (3)77 A -161.6 D
【解析】①自发反应需满足△G=ΔH-TΔS<0,若ΔH<0且ΔS>0,则△G一定小于0,反应在任何温
度下都能自发进行,故此处填C;②若ΔH>0且ΔS<0,则△G一定大于0,反应在任何温度下都不能自
发进行,故此处填B;③将反应A对应数据代入ΔH-TΔS<0计算,得反应自发进行的温度要求为:T>
350 K,即350-273=77 ℃,故此处A、77 ℃;将反应D对应数据代入ΔH-TΔS<0计算,得反应自发进行
的温度要求为:T<111.4 K,即111.4-273= -161.6 ℃,故此处D、-161.6 ℃。
【能力提升】
22.相同的温度和压强下,有关下列两个反应的说法不正确的是( )
反应 ΔH/kJ/mol
MgCO(s) MgO(s)+CO(g) 117.6 1 a
3 2
CaCO (s) CaO(s)+CO(g) 177.9 1 b
3 2
注:①其中 表示反应方程式中气体化学计量数差;
②ΔH-TΔS<0的反应方向自发
A.因为 相同,所以a与b大小相近
B.热分解温度:MgCO(s)>CaCO (s)
3 3
C.a-b=S[MgO(s)]+S[CaCO (s)]-S[MgCO(s)]- S[CaO(s)]
3 3
资料整理【淘宝店铺:向阳百分百】