文档内容
考点 24 化学反应的方向
【基础过关】
1.下列过程是非自发的是( )
A.水由高处向低处流 B.氯气和溴化钾溶液的反应
C.铁在潮湿空气中生锈 D.室温下水结成冰
2.下列过程是非自发过程的是( )
A.气体的扩散 B.室温下水结成冰
C.水由高处向低处流 D.有序排列的火柴散落成无序排列
3.下列说法正确的是( )
A.凡是放热反应都是自发的 B.铁在潮湿空气中生锈是自发过程
C.熵增大的反应都是自发反应 D.电解池的反应是属于自发反应
4.知道了某过程有自发性之后,则( )
A.可判断出过程的方向 B.可确定过程是否一定会发生
C.可预测过程发生完成的快慢 D.可判断过程的热效应
5.下列反应在任何温度下均能自发进行的是( )
A.2N(g)+O(g)===2N O(g) ΔH=163 kJ·mol-1
2 2 2
B.Ag(s)+Cl(g)===AgCl(s) ΔH=-127 kJ·mol-1
2
C.HgO(s)===Hg(l)+O(g) ΔH=91 kJ·mol-1
2
D.HO(l)===O(g)+HO(l) ΔH=-98 kJ·mol-1
2 2 2 2
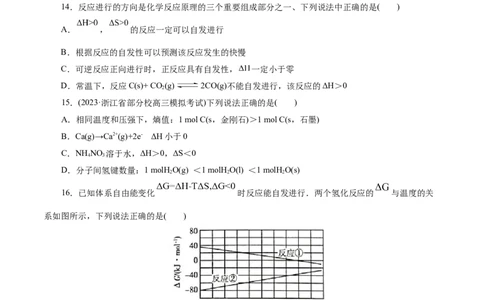
6.(2023·浙江省台州市期末)常压下,1g冰熔化成1g水、1g水蒸发成1g水蒸气的焓和熵的变化情况
如图所示。
已知:熔化过程:HO(s) HO(l) ∆H、∆S
2 2 1 1
蒸发过程:HO(l) HO(g) ∆H、∆S
2 2 2 2
1下列说法不正确的是( )
A.∆H>0;∆H>0 B.∆S>0;∆S>0
1 2 1 2
C. ∆S>∆S D.蒸发过程属于高温自发过程
1 2
7.已知凡气体分子总数增多的反应一定是熵增大的反应。一定条件下,下列反应不能自发进行的是(
)
A.2O(g)=3O(g) ΔH<0 B.2CO(g)=2C(s)+O (g) ΔH>0
3 2 2
C.N(g)+3H(g) 2NH (g) ΔH<0 D.CaCO (s)=CaO(s)+CO (g) ΔH>0
2 2 3 3 2
8.25 ℃、1.01⇌×105Pa时,反应2N
2
O
5
(g)=4NO
2
(g)+O
2
(g) ΔH=+109.8 kJ·mol-1,该反应能自发进行的
原因是( )
A.该反应是吸热反应 B.该反应是放热反应
C.该反应是熵减小的反应 D.该反应的熵增大效应大于能量效应
9.下列说法正确的是( )
A.凡是放热反应都是自发的,因为吸热反应都是非自发的
B.自发反应的熵一定增大,非自发反应的熵一定减小
C.常温下,反应C(s)+CO(g) 2CO(g)不能自发进行,则该反应的ΔH>0
2
D.反应2Mg(s)+CO (g)=C(s)+2MgO(s)能自发进行,则该反应的ΔH>0
2
10.下列说法正确的是( )
A.ΔH<0、ΔS>0的反应在温度低时不能自发进行
B.NH HCO (s)=NH (g)+HO(g)+CO(g) ΔH=+185.57 kJ/mol能自发进行,原因是体系有自发地向
4 3 3 2 2
混乱度增加的方向转变的倾向
C.焓变和熵变都与反应的自发性有关,因此焓变或熵变均可单独作为反应自发性的判据
D.在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向
11.已知凡气体分子总数增多的反应一定是熵增大的反应。一定条件下,下列反应不能自发进行的是(
)
A.2O(g)=3O(g) ΔH<0 B.2CO(g)=2C(s)+O (g) ΔH>0
3 2 2
C.N(g)+3H(g) 2NH (g) ΔH<0 D.CaCO (s)=CaO(s)+CO (g) ΔH>0
2 2 3 3 2
12.现有两个热化学反应方程式:
(l)+H (g) (l) ΔH>0 ①
2
(l)+2H (g) (l) ΔH<0 ②
2
下列说法正确的是( )
2A.反应①②中都存在:ΔS>0
B.反应①一定不能自发进行
C.在通常情况下,①②都能自发进行
D.反应②高温时,可自发进行
13.某化学反应A(s)=D(g)+E(g) ΔH-TΔS=(-4500+11T)kJ·mol-1(其中ΔH为焓变,ΔS为熵变,T为热
力学温度,单位为K),要防止反应发生,温度必须( )
A.高于409 K B.低于136 K
C.高于136 K而低于409 K D.低于409 K
14.反应进行的方向是化学反应原理的三个重要组成部分之一、下列说法中正确的是( )
A. , 的反应一定可以自发进行
B.根据反应的自发性可以预测该反应发生的快慢
C.可逆反应正向进行时,正反应具有自发性, 一定小于零
D.常温下,反应C(s)+ CO (g) 2CO(g)不能自发进行,该反应的ΔH>0
2
15.(2023·浙江省部分校高三模拟考试)下列说法正确的是( )
A.相同温度和压强下,熵值:1 mol C(s,金刚石)>1 mol C(s,石墨)
B.Ca(g)→Ca2+(g)+2e- ΔH小于0
C.NH NO 溶于水,ΔH>0,ΔS<0
4 3
D.分子间氢键数量:1 molHO(g) <1 molHO(l) <1 molHO(s)
2 2 2
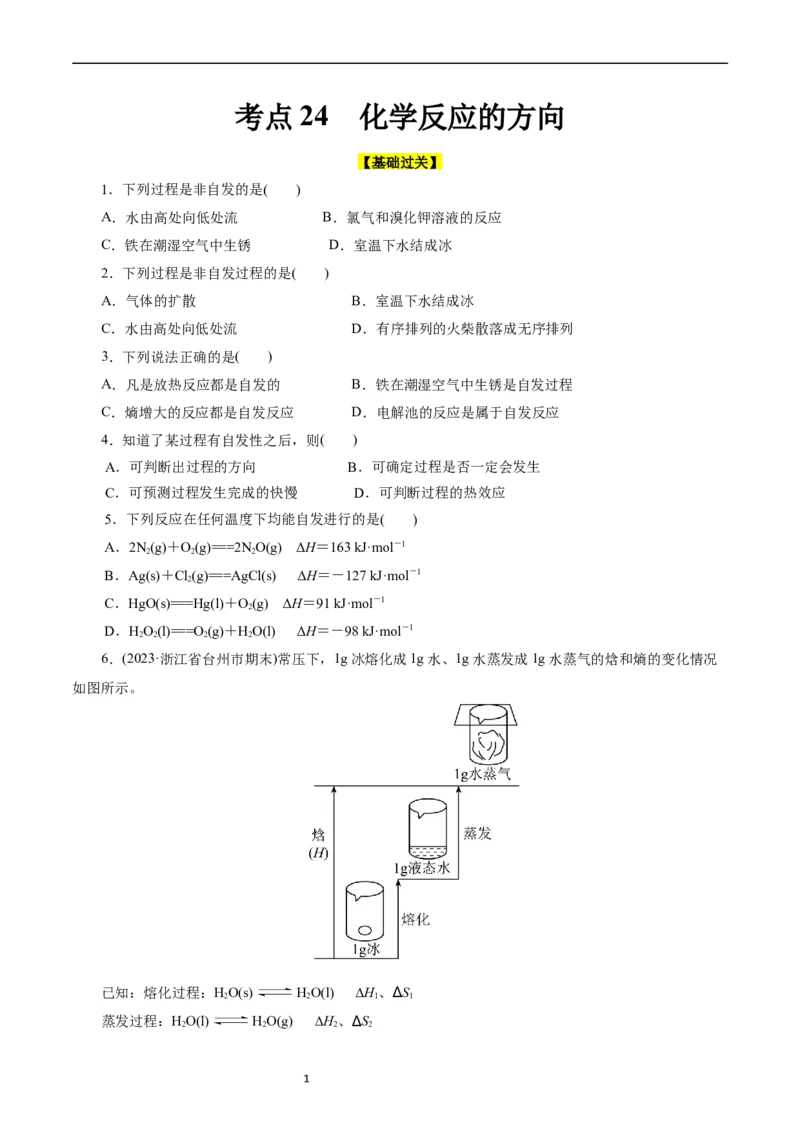
16.已知体系自由能变化 时反应能自发进行.两个氢化反应的 与温度的关
系如图所示,下列说法正确的是( )
A.反应①的∆S<0 B.反应②在 时的反应速率很快
C.温度大于 时,反应①能自发进行 D.反应②的∆H>0
17.假定X 与Y 都是理想气体(气体本身不占体积,不考虑气体间相互作用,不考虑碰撞能量损失),
2 2
在如图所示的过程中,下列说法正确的是( )
3A.若X、Y 均为O,则 ,混合过程自发进行
2 2 2
B.若X、Y 均为O,则 ,混合过程不自发
2 2 2
C.若X、Y 分别为N 与O,则 ,混合过程自发进行
2 2 2 2
D.若X、Y 分别为N 与O,则 ,混合过程不自发
2 2 2 2
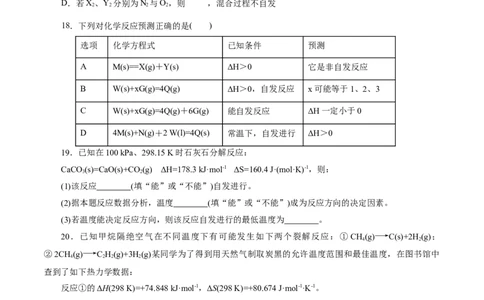
18.下列对化学反应预测正确的是( )
选项 化学方程式 已知条件 预测
A M(s)==X(g)+Y(s) ΔH>0 它是非自发反应
B W(s)+xG(g)=4Q(g) ΔH>0,自发反应 x可能等于1、2、3
C W(s)+xG(g)=4Q(g)+6G(g) 能自发反应 ΔH一定小于0
D 4M(s)+N(g)+2 W(l)=4Q(s) 常温下,自发进行 ΔH>0
19.已知在100 kPa、298.15 K时石灰石分解反应:
CaCO (s)=CaO(s)+CO (g) ΔH=178.3 kJ·mol-1 ΔS=160.4 J·(mol·K)-1,则:
3 2
(1)该反应 (填“能”或“不能”)自发进行。
(2)据本题反应数据分析,温度 (填“能”或“不能”)成为反应方向的决定因素。
(3)若温度能决定反应方向,则该反应自发进行的最低温度为 。
20.已知甲烷隔绝空气在不同温度下有可能发生如下两个裂解反应:①CH(g) C(s)+2H(g);
4 2
②2CH(g) C H(g)+3H(g)某同学为了得到用天然气制取炭黑的允许温度范围和最佳温度,在图书馆中
4 2 2 2
查到了如下热力学数据:
反应①的ΔH(298 K)=+74.848 kJ·mol-1,ΔS(298 K)=+80.674 J·mol-1·K-1。
反应②的ΔH(298 K)=+376.426 kJ·mol-1,ΔS(298 K)=+220.211 J·mol-1·K-1。
已知焓变和熵变随温度变化很小。请参考上述信息,回答下列问题:
(1)这两个反应在 (填“高温”或“低温”)下自发进行。
(2)反应①在常温下 (填“能”或“不能”)自发进行。
(3)制取炭黑的允许温度范围为 。
(4)为了提高甲烷的炭化程度,下面四个温度中最合适的是 (填字母)
A.905.2 K B.927 K C.1273 K D.2000 K
21.有A、B、C、D四个反应:
4反应 A B C D
ΔH/(kJ·mol-1) 10.5 1.80 -126 -11.7
ΔS/(J·mol-1·K-1) 30.0 -113.0 84.0 -105.0
(1)在任何温度下都能自发进行的反应是______;
(2)任何温度下都不能自发进行的反应是______;
(3)另两个反应中,在温度高于______℃时可自发进行的反应是______;在温度低于______℃时可自发
进行的反应是______。
【能力提升】
22.相同的温度和压强下,有关下列两个反应的说法不正确的是( )
反应 ΔH/kJ/mol
MgCO(s) MgO(s)+CO(g) 117.6 1 a
3 2
CaCO (s) CaO(s)+CO(g) 177.9 1 b
3 2
注:①其中 表示反应方程式中气体化学计量数差;
②ΔH-TΔS<0的反应方向自发
A.因为 相同,所以a与b大小相近
B.热分解温度:MgCO(s)>CaCO (s)
3 3
C.a-b=S[MgO(s)]+S[CaCO (s)]-S[MgCO(s)]- S[CaO(s)]
3 3
D.两个反应在不同温度下的ΔH和 都大于零
23.(2023·浙江省模拟)用一种较活泼的金属把另一种金属从化合物中还原出来的方法称为金属热还原
法。钠、镁、铝是常用的还原剂。一些常见的金属热还原反应如下:
序
反应 H/kJ/mol S/J/(mol·K)
号
△ △
① 2Al(l) + 3BaO(s)=3Ba(g) +Al O(s) 487 207.53
2 3
② 2Al(s) + 3BaO(s)=3Ba(s)+Al O(s) 4 -15.70
2 3
③ Mg(l) + 2RbCl(s)=2Rb(g)+MgCl (s) 381.77 223.06
2
④ 4Na(l)+TiCl (g)=Ti(s)+4NaCl(s) -899.8 -291
4
下列说法不正确的是
A.反应①表明金属沸点:Al>Ba
B.对于反应:2Ba(s)+O(g)=2BaO(s) H,4Al(s)+3O (g)=2Al O(s) H,由反应②可以推出
2 1 2 2 3 2
3 H 1 ≈ H 2 △ △
△ △
5C.反应③说明金属活动性顺序:Mg>Rb
D.对于反应④:| H|>>|T S|说明焓变对该反应的自发性起主要影响作用
24.CO 2 催化加氢 △ 制甲醇有 △ 利于减少 CO 2 的排放,实现“碳达峰”,其反应可表示为:CO 2 (g)+3H 2
(g) =CH OH (g)+HO (g) ΔH=−49 kJ•mol−1。CO 催化加氢制甲醇的反应通过如下步骤来实现:
3 2 2
①CO(g)+H(g) =CO(g)+H O(g) ΔH=41 kJ•mol−1
2 2 2 1
②CO(g)+2H(g) =CH OH(g) ΔH
2 3 2
反应过程中各物质的相对能量变化情况如图所示。下列说法不正确的是( )
A.步骤①反应的ΔS>0
B.步骤②反应的ΔH=−90 kJ•mol−1
2
C.CO 催化加氢制甲醇的总反应速率由步骤②决定
2
D.升高温度,各步骤的正、逆反应速率均增大
25.已知固态、气态离子的标准熵是根据热力学第三定律求出的绝对值,水合态离子的标准熵是以
298K时H+(aq)的标准熵为0算得的相对值。298K时一些离子在不同状态下的标准熵值数据如表所示,通
过数据分析得出的下列结论不正确的是( )
标准熵值/J·mol·L-1 Li+ Na+ K+ Be2+ Mg2+ Ca2+ Al3+
固态离子标准熵S (s) 29.1 51.3 64.7 9.5 32.7 41.6 28.3
气态离子标准熵S (g) 138.8 153.7 160.3 136.3 148.6 154.9 164.6
水合态离子标准熵S (aq) 13.4 59 102.5 -129.7 -138.1 -53.1 -321.7
A.金属离子由固态到气态,标准熵值增加
B.同周期金属离子价态越高,水合态离子的标准熵值越小
C.同主族金属离子半径越小,水合态离子的标准熵值越小
6D.同主族金属元素固态或气态离子的标准熵值随原子序数增大而增大
26.回答下列问题:
(1)用钌的配合物作催化剂,一定条件下可直接光催化分解CO,发生反应:2CO(g)=2CO(g)+O(g),
2 2 2
该反应的∆H________(填“>”或“<”,下同)0,∆S_______0,在低温下,该反应________(填“能”或“不
能”)自发进行。
(2)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中
的NO和CO转变成CO 和N,化学方程式为2NO+2CO 2CO+N 。反应在常温下能够自发进行,则
2 2 2 2
反应的∆H______(填“>”或“<”)0。
(3)已知在 、298K时石灰石分解反应CaCO (s)=CaO(s)+CO (g)的∆H>0、∆S>0。
3 2
①常温下,该反应________(填“能”或“不能”)自发进行。
②据本题反应数据分析,温度________(填“能”或“不能”)成为反应进行方向的决定因素。
(4)已知CaSO(s)+ CO(g)=CaO(s)+SO (g)+CO (g) ΔH=+218kJ·mol-1,该反应能够自发进行的反应条件
4 2 2
是__________________________。
(5)某吸热反应能自发进行,则该反应的∆S_____(填“>”或“<”)0。
7