文档内容
考点 28 盐类的水解
【基础过关】
1.下列说法正确的是( )
A.pH=0的溶液不存在 B.使用广范pH试纸测得某溶液的pH=3.5
C.中性溶液的pH不一定等于7 D.K =10-14适用于任何温度、任何溶液
w
2.下列说法不正确的是( )
A.任何水溶液的K =1.0×10-14
W
B.25℃,1 ml pH=5的CHCOOH溶液稀释到 ,所得溶液的 接近7
3
C.25℃时,NH ·H O与CHCOOH的电离平衡常数相等,某浓度的NH Cl溶液的pH=4.3,则相同浓
3 2 3 4
度的CHCOONa溶液的pH=9.7
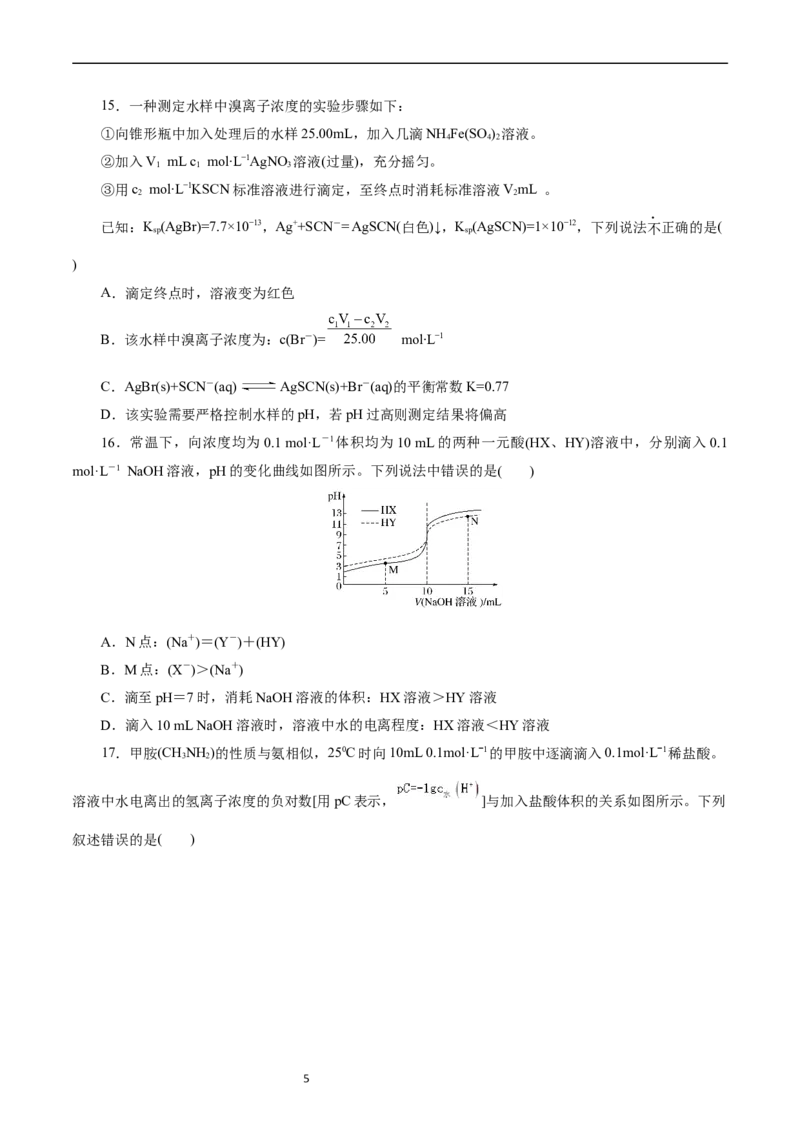
3
D.25℃时,当 和 的物质的量之比为1∶2溶于水得到的溶液 ,则溶液中
3.某研究小组为测定食用白醋中醋酸的含量进行了如下操作,正确的是( )
A.用碱式滴定管量取一定体积的待测白醋放入锥形瓶中
B.称取4.0 g NaOH放到100 mL容量瓶中,加水至刻度线,配成1.00 mol/L NaOH标准溶液
C.用NaOH溶液滴定白醋,使用酚酞作指示剂,溶液颜色恰好由无色变为浅红色,且半分钟内不褪
色时为滴定终点
D.滴定时眼睛要注视着滴定管内NaOH溶液的液面变化,防止滴定过量
4.用标准盐酸滴定未知浓度的氢氧化钠溶液,用甲基橙作指示剂,下列说法不正确的是( )
A.可以用酚酞代替指示剂
B.滴定前不能用待测液润洗锥形瓶
C.若氢氧化钠吸收少量CO,不影响滴定结果
2
D.当锥形瓶内溶液由橙色变为红色,且半分钟内颜色不恢复,即达到滴定终点
5.准确移取20.00 mL某待测 HCl溶液于锥形瓶中,用0.1000 mol·L-1 NaOH溶液滴定。下列说法正
确的是( )
A.滴定管用蒸馏水洗涤后,装入NaOH溶液进行滴定
B.随着NaOH溶液的滴入,锥形瓶中溶液pH由小变大
C.用酚酞作指示剂,当锥形瓶中溶液由红色变为无色时停止滴定
D.滴定达到终点时,发现滴定管尖嘴部分有悬滴,则测定结果偏小
6.(2023·四川省成都市石室中学期中)T℃时,水的离子积常数K =10-13,该温度下,V mLpH=12的
w 1
1Ba(OH) 稀溶液与V mLpH=2的稀硫酸充分反应(混合后的体积变化忽略不计),恢复到T℃,测得混合溶
2 2
液的pH=3,则V:V 的值为( )
1 2
A.9∶101 B.99∶101 C.1∶100 D.1∶10
7.(2023·四川省成都市高二期末)为探究浓度对醋酸电离程度的影响,用 计测定 时不同浓度醋
酸的 结果如下,下列说法正确的是( )
浓度/ 0.0010 0.010 0.020 0.10 0.20
3.88 3.38 3.23 2.88 2.83
A.实验过程中可以改用广泛 试纸
B. 溶液稀释过程中,醋酸电离程度及溶液导电性都增大
C. 时,电离常数K(CH COOH)的数量级为10-5
3
D.CHCOOH溶液稀释过程中不可能出现c(H+)>c(OH―)>c(CHCOO-)
3 3
8.(2023·江苏省徐州市高二期末)水的离子积常数随着温度的变化关系如表:
温度/℃ 25 50 75 100
K /×10-14 1.0 5.5 20.0 56.0
W
下列说法正确的是( )
A.纯水中c(H+)的大小与温度无关
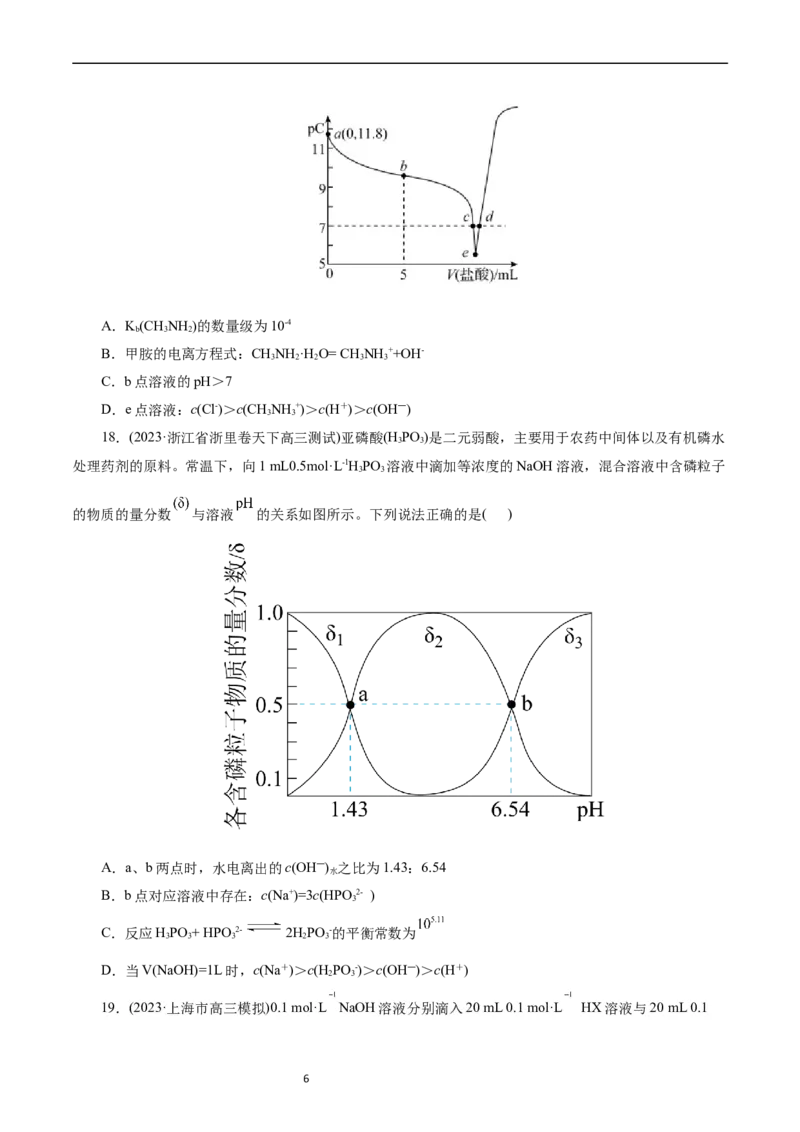
B.水的电离度a(50℃)c>b>a
20.(2023·河南省南阳市三模)常温下,向10 mL0.1 mol·L-1HA溶液中逐滴加入0.1 mol·L-1的MOH溶
液,其导电率、pH与加入MOH溶液体积的关系如图所示(假设反应过程中温度不变)。
下列说法正确的是( )
A.a→d过程中,水的电离程度逐渐增大
B.加入10 mL→13 mL MOH溶液时,导电率降低是因为离子总数减小
C.常温下,K (MOH) =K(HA)≈10 -4.6
b a
D.b点溶液中c (HA) +2c (H+) =c (A-) +2c (MOH) +c (OH- )
21.(2023·山东省高三联考)一定条件下,乙酸酐[(CH CO) O]醇解反应
3 2
7[(CH CO) O+ROH→CH COOR+CH COOH]可进行完全,利用此反应定量测定有机醇(ROH)中的羟基含
3 2 3 3
量,实验过程中酯的水解可忽略。实验步骤如下:
①配制一定浓度的乙酸酐-苯溶液。
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入 样品,充分反应后,加适量水使剩余乙酸
酐完全水解:(CHCO) O+HO→2CH COOH。
3 2 2 3
③加指示剂并用cmol·L-1NaOH-甲醇标准溶液滴定至终点,消耗标准溶液VmL。
1
④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加指示剂并用
cmol·L-1NaOH-甲醇标准溶液滴定至终点,消耗标准溶液VmL。根据上述实验原理,下列说法正确的是(
2
)
A.可以用乙酸代替乙酸酐进行上述实验
B.若因甲醇挥发造成标准溶液浓度发生变化,将导致测定结果偏小
C.步骤③滴定时,不慎将锥形瓶内溶液溅出,将导致测定结果偏小
D.步骤④中,若加水量不足,将导致测定结果偏大
22.使用硫酸亚铁铵晶体[(NH )Fe(SO )·6H O]滴定法可以测定青铜中铬元素的含量。实验步骤如下:
4 2 4 2 2
步骤1:称量硫酸亚铁铵晶[(NH )Fe(SO )·6H O]溶于稀硫酸,加水稀释配成1000 mL0.0200 mol/L
4 2 4 2 2
(NH )Fe(SO ) 标准溶液。
4 2 4 2
步骤2:称取1.00 g青铜样品于250 mL维形瓶中,加入适量稀硝酸使其完全溶解,再加入适量过硫酸
[(NH )SO]溶液,加热煮沸,使样品中的铬元素完全转化为HCrO,冷却后加蒸馏水配制成250 mL溶液,
4 2 2 8 2 4
摇匀。
步骤3:取25 mL上述溶液置于锥形瓶中,加入硫酸酸化,滴入4滴N-苯代邻氨基苯甲酸指示剂,用
(NH )Fe(SO ) 标准溶液满淀至终点。重复上述操作3次。测得消耗(NH )Fe(SO ) 标准溶液的体积分别为
4 2 4 2 4 2 4 2
18.90 mL、17.97 mL、18.03 mL。发生反应的离子方程式为:HCrO+Fe2++H+→Cr3++Fe3++H O (未配平)
2 4 2
下列说法不正确的是( )
A.在“步骤1”中,用到的玻璃仪器有1000 mL容量瓶、烧杯、玻璃棒、胶头滴管
B.在“步骤2”中,铜与硝酸反应的离子方程式为:3Cu+2NO-+8H+=3Cu2++2NO↑+4HO
3 2
C.青铜中铬元素的质量分数为6.344%
D.实验中,如果盛放(NH )Fe(SO ) 标准溶液的滴定管没有润洗,则测量结果将偏大
4 2 4 2
23.下表是常温下几种常见弱酸的电离平衡常数,回答下列问题:
弱酸 电离平衡常数K
CHCOOH K=1.6×10−5
3
HC O K=5.9×10−2 K=6.4×10−5
2 2 4 1 2
8HCO K=4.4×10−7 K=5.6×10−11
2 3 1 2
HS K=9.1×10−8 K=1.1×10−15
2 1 2
(1)某温度下,纯水中的 c(H+)=2.0×10−7mol/L,则此时溶液中 c(OH−)为______________mol/L;此时温
度________25℃(填“大于”,“小于”或“等于”),若温度不变,滴入稀硫酸使 c(H+)=8.0×10−6mol/L,
则由水电离出的 c(H+)为__________mol/L。
(2)下列四种离子结合H+能力最强的是_________。
A.HCO - B.C O2- C.S2− D.CHCOO−
3 2 4 3
(3)该温度下1.0 mol·L−1的CHCOOH溶液中的c(H+)=__________mol·L−1
3
(4)常温下,加水稀释0.1 mol·L−1的HC O 溶液,下列说法正确的是___________。
2 2 4
A.溶液中n(H+)×n(OH−)保持不变
B.溶液中水电离的c(H+)×c(OH−)保持不变
C.溶液中c(HC O-)/c(H C O)保持不变
2 4 2 2 4
D.溶液中c(OH−)增大
24.过氧化氢的水溶液适用于医用消毒、环境消毒和食品消毒。
Ⅰ.过氧化氢性质探究实验
(1)酸性条件下HO 可将Fe2+转化成Fe3+,由此说明HO 具有______性。
2 2 2 2
(2)已知HO 是一种二元弱酸,其中K =2.20×10-12、K =1.05×10-25,则HO 的电离方程式为______,
2 2 a1 a2 2 2
常温下,1mol∙L-1的HO 溶液的pH约为______。
2 2
Ⅱ.过氧化氢含量的测定实验。某兴趣小组同学用0.1000mol∙L-1的酸性高锰酸钾标准溶液滴定试样中的
过氧化氢,反应原理为2 MnO-+5H O+6H+=2Mn2++8H O+5O↑。
4 2 2 2 2
(3)滴定达到终点的现象是______。
(4)用移液管移取25.00mL试样置于锥形瓶中,重复滴定四次,每次消耗酸性高锰酸钾标准溶液的体积
如表所示:
第一 第三
第二次 第四次
次 次
V(KMnO 溶液)/mL 17.10 18.10 18.00 17.90
4
计算试样中过氧化氢的浓度为______mol∙L-1。
(5)若滴定前滴定管尖嘴处有气泡,滴定后消失,则测定结果______(填“偏高”“偏低”或“不变”)。
【能力提升】
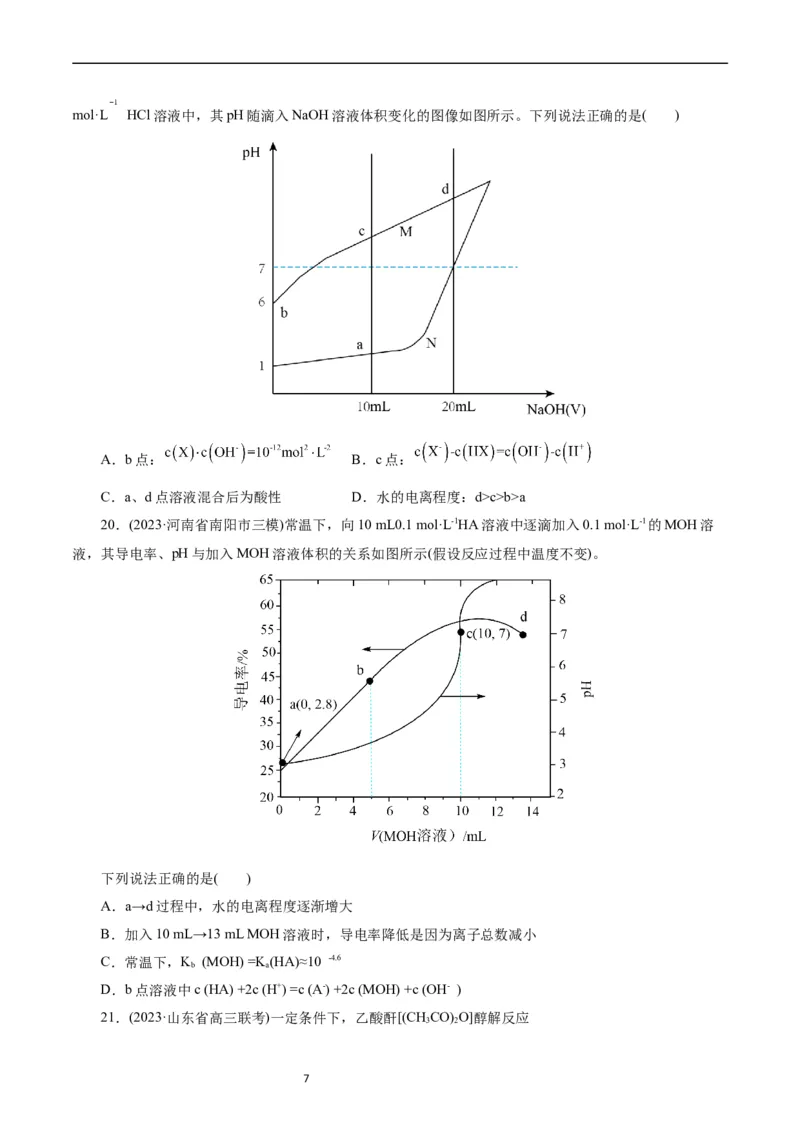
25.(2023·浙江省天域全国名校协作体高三联考)已知:酸碱质子理论认为,凡是能给够出质子(H+)的
物质是酸(比如NH +),能接受质子的物质是碱(比如 ),而酸给出质子转变为相应的碱,碱接受质子转
4
变为相应的酸,这种得失质子可以相互转变的一对酸碱型体称为共轭酸碱对。常温下,调节HA溶液的
9pH,HA所占物质的量分数δ(分布系数)随pH变化、A-所占物质的量分数δ(分布系数)随pH变化的关系如
图所示[比如HA的分布系数 ]。下列表述不正确的是
A.A-是HA的共轭碱 B.
C.增大pH过程中, 的值减小 D.图像上任意一点均满足
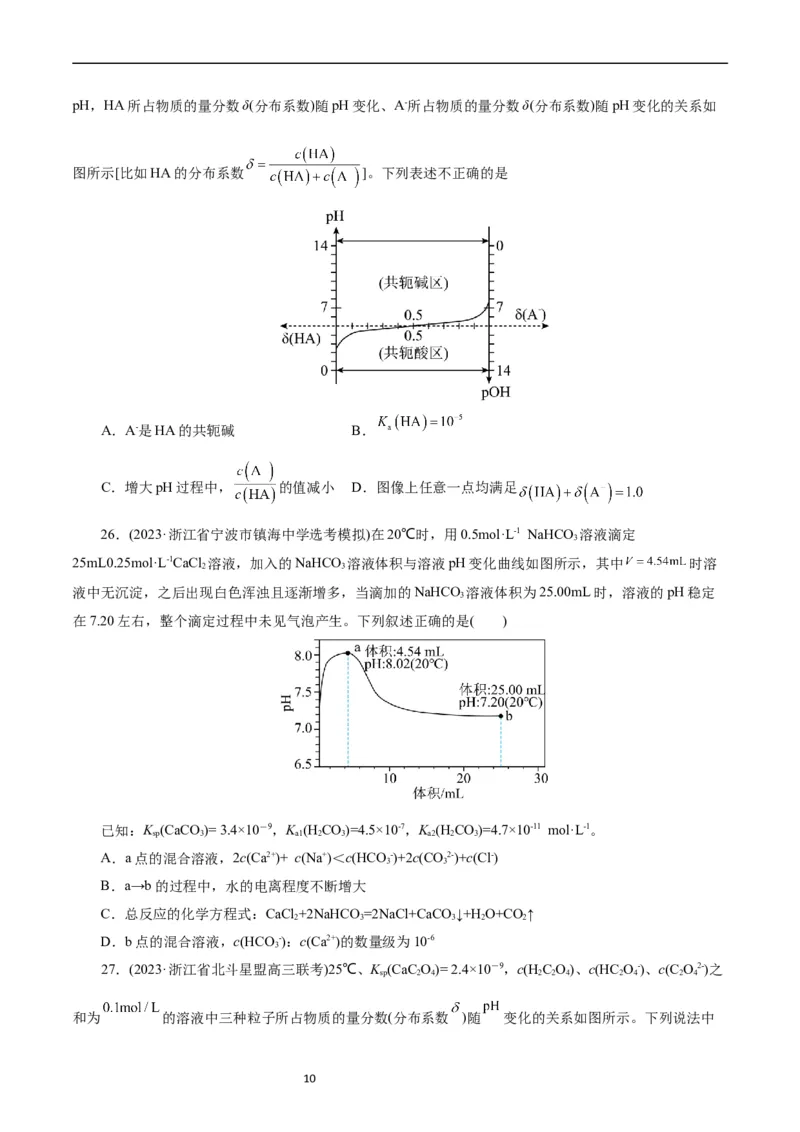
26.(2023·浙江省宁波市镇海中学选考模拟)在20℃时,用0.5mol·L-1 NaHCO 溶液滴定
3
25mL0.25mol·L-1CaCl 溶液,加入的NaHCO 溶液体积与溶液pH变化曲线如图所示,其中 时溶
2 3
液中无沉淀,之后出现白色浑浊且逐渐增多,当滴加的NaHCO 溶液体积为25.00mL时,溶液的pH稳定
3
在7.20左右,整个滴定过程中未见气泡产生。下列叙述正确的是( )
已知:K (CaCO)= 3.4×10-9,K (H CO)=4.5×10-7,K (H CO)=4.7×10-11 mol·L-1。
sp 3 a1 2 3 a2 2 3
A.a点的混合溶液,2c(Ca2+)+ c(Na+)<c(HCO -)+2c(CO2-)+c(Cl-)
3 3
B.a→b的过程中,水的电离程度不断增大
C.总反应的化学方程式:CaCl +2NaHCO=2NaCl+CaCO ↓+H O+CO↑
2 3 3 2 2
D.b点的混合溶液,c(HCO -):c(Ca2+)的数量级为10-6
3
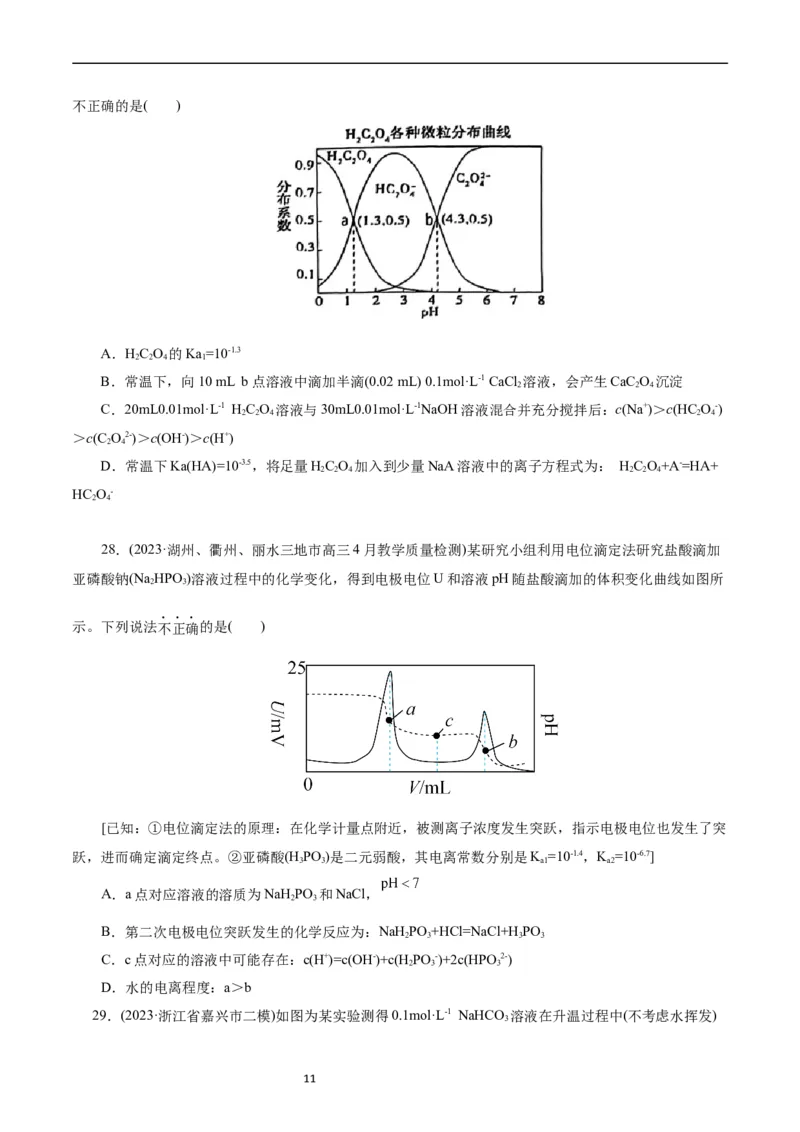
27.(2023·浙江省北斗星盟高三联考)25℃、K (CaC O)= 2.4×10-9,c(H C O)、c(HC O-)、c(C O2-)之
sp 2 4 2 2 4 2 4 2 4
和为 的溶液中三种粒子所占物质的量分数(分布系数 )随 变化的关系如图所示。下列说法中
10不正确的是( )
A.HC O 的Ka=10-1.3
2 2 4 1
B.常温下,向10 mL b点溶液中滴加半滴(0.02 mL) 0.1mol·L-1 CaCl 溶液,会产生CaC O 沉淀
2 2 4
C.20mL0.01mol·L-1 HC O 溶液与30mL0.01mol·L-1NaOH溶液混合并充分搅拌后:c(Na+)>c(HC O-)
2 2 4 2 4
>c(C O2-)>c(OH-)>c(H+)
2 4
D.常温下Ka(HA)=10-3.5,将足量HC O 加入到少量NaA溶液中的离子方程式为: HC O+A-=HA+
2 2 4 2 2 4
HC O-
2 4
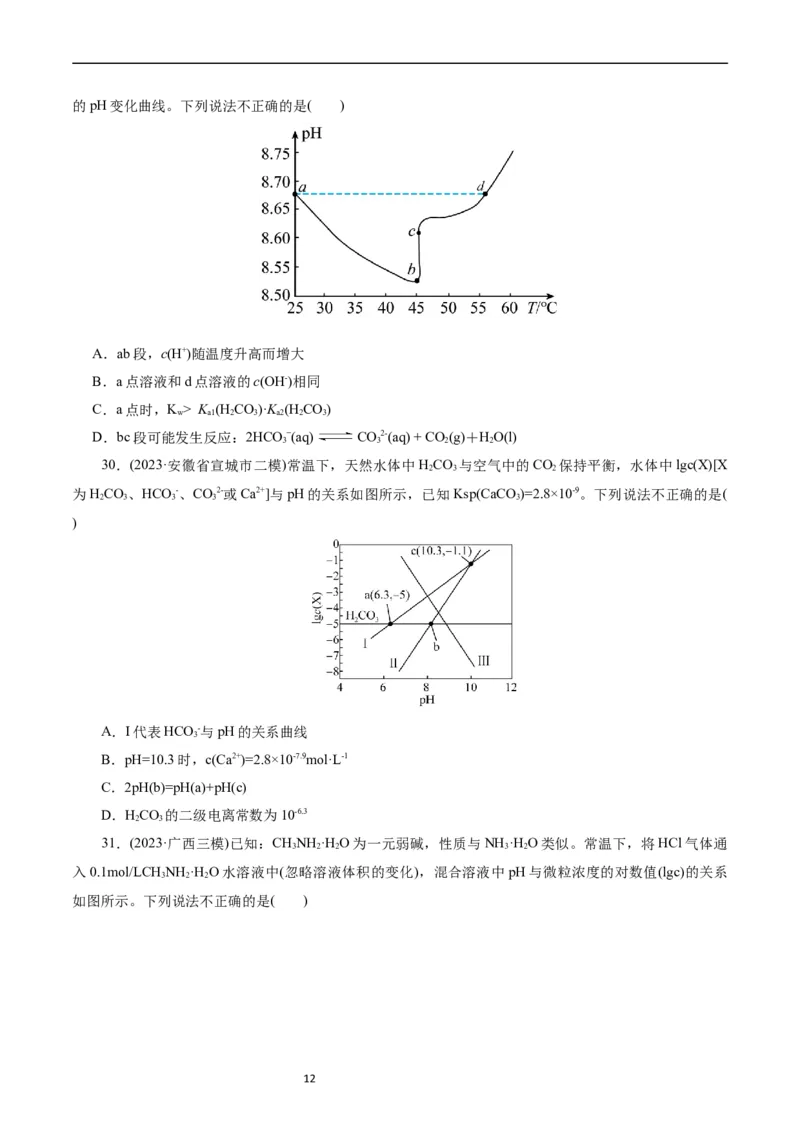
28.(2023·湖州、衢州、丽水三地市高三4月教学质量检测)某研究小组利用电位滴定法研究盐酸滴加
亚磷酸钠(Na HPO )溶液过程中的化学变化,得到电极电位U和溶液pH随盐酸滴加的体积变化曲线如图所
2 3
示。下列说法不正确的是( )
[已知:①电位滴定法的原理:在化学计量点附近,被测离子浓度发生突跃,指示电极电位也发生了突
跃,进而确定滴定终点。②亚磷酸(H PO )是二元弱酸,其电离常数分别是K =10-1.4,K =10-6.7]
3 3 a1 a2
A.a点对应溶液的溶质为NaH PO 和NaCl,
2 3
B.第二次电极电位突跃发生的化学反应为:NaH PO +HCl=NaCl+H PO
2 3 3 3
C.c点对应的溶液中可能存在:c(H+)=c(OH-)+c(H PO -)+2c(HPO 2-)
2 3 3
D.水的电离程度:a>b
29.(2023·浙江省嘉兴市二模)如图为某实验测得0.1mol·L-1 NaHCO 溶液在升温过程中(不考虑水挥发)
3
11的pH变化曲线。下列说法不正确的是( )
A.ab段,c(H+)随温度升高而增大
B.a点溶液和d点溶液的c(OH-)相同
C.a点时,K > K (H CO)·K (H CO)
w a1 2 3 a2 2 3
D.bc段可能发生反应:2HCO −(aq) CO2-(aq) + CO (g)+HO(l)
3 3 2 2
30.(2023·安徽省宣城市二模)常温下,天然水体中HCO 与空气中的CO 保持平衡,水体中lgc(X)[X
2 3 2
为HCO 、HCO -、CO2-或Ca2+]与pH的关系如图所示,已知Ksp(CaCO )=2.8×10-9。下列说法不正确的是(
2 3 3 3 3
)
A.I代表HCO -与pH的关系曲线
3
B.pH=10.3时,c(Ca2+)=2.8×10-7.9mol·L-1
C.2pH(b)=pH(a)+pH(c)
D.HCO 的二级电离常数为10-6.3
2 3
31.(2023·广西三模)已知:CHNH ·H O为一元弱碱,性质与NH ·H O类似。常温下,将HCl气体通
3 2 2 3 2
入0.1mol/LCH NH ·H O水溶液中(忽略溶液体积的变化),混合溶液中pH与微粒浓度的对数值(lgc)的关系
3 2 2
如图所示。下列说法不正确的是( )
12A.CHNH ·H O的水溶液中存在:CHNH ·H O CHNH ++OH-
3 2 2 3 2 2 3 3
B.K(CHNH ·H O)的数量级为10-5
a 3 2 2
C.P点,c(Cl-)+c(CH NH +)+c(CH NH ·H O)=0.2mol/L
3 3 3 2 2
D.P点之后,溶液中存在c(Cl-)+c(OH-)=c(CH NH +)+c(H+)
3 3
32.(2023·重庆市长寿区期末)乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H C O·xHO)
2 2 4 2
进行的探究性学习的过程,请你参与并协助他们完成相关学习任务。
该组同学的研究课题是:探究测定草酸晶体(H C O·xHO)中的x值。通过查阅资料和网络查寻得,草
2 2 4 2
酸易溶于水,水溶液可以用酸性KMnO 溶液进行滴定:2MnO -+5HC O+6H+=2Mn2++5CO ↑+8H O。学习
4 4 2 2 4 2 2
小组的同学设计了如下步骤用滴定的方法测定x值。
①称取1.260 g纯草酸晶体,将其制成 水溶液为待测液。
②取 待测液放入锥形瓶中,再加入适量的稀HSO 。
2 4
③用浓度为 的酸性KMnO 标准溶液进行滴定,达到终点时消耗 。
4
(1)上述步骤②中使用的锥形瓶是否需要用待测液润洗_______,(填“是”或“否”)滴定时,将酸性
KMnO 标准液装入_______(填“酸式”或“碱式”)滴定管中。
4
(2)本实验滴定达到终点的标志是_______。
(3)通过上述数据,求得 _______。
(4)若滴定终点时俯视滴定管刻度,则由此测得的x值会_______(填偏“大”、“偏小”或“不变”)。
(5)根据上述实验计算的数据可信性不强,为了提高实验的准确性,请写出改进措施_______。
13