文档内容
考点 28 盐类的水解
【基础过关】
1.下列说法正确的是( )
A.pH=0的溶液不存在 B.使用广范pH试纸测得某溶液的pH=3.5
C.中性溶液的pH不一定等于7 D.K =10-14适用于任何温度、任何溶液
w
【答案】C
【解析】由pH=-lg c(H+)可知,pH=0时,c(H+)=1 mol·L-1,A项错误;广范pH试纸测得的溶液的pH
只能取整数,B项错误;100 ℃时,中性溶液的pH<7,C项正确;25 ℃时,K 为1.0×10-14,改变温度,
w
K 也会发生变化,D项错误。
w
2.下列说法不正确的是( )
A.任何水溶液的K =1.0×10-14
W
B.25℃,1 ml pH=5的CHCOOH溶液稀释到 ,所得溶液的 接近7
3
C.25℃时,NH ·H O与CHCOOH的电离平衡常数相等,某浓度的NH Cl溶液的pH=4.3,则相同浓
3 2 3 4
度的CHCOONa溶液的pH=9.7
3
D.25℃时,当 和 的物质的量之比为1∶2溶于水得到的溶液 ,则溶液中
【答案】A
【解析】A项,K 只与温度有关,温度不同K 值不同,故应为25℃时,任何水溶液的K =1.0×10-14,
w w W
A项错误;B项,25℃,1 ml pH=5的CHCOOH溶液稀释1000倍,但酸溶液再稀释也不可能稀释成中性
3
溶液或者碱性溶液,故所得溶液的pH接近7,B项正确;C项,25℃时,NH ·H O与CHCOOH的电离平
3 2 3
衡常数相等,说明NH +和CHCOO-水解能力相同,某浓度的NH Cl溶液的pH=4.3,说明NH +水解生成的
4 3 4 4
c(H+)约为10-4.3mol/L,故相同浓度的CHCOONa溶液,CHCOO-水解生成的c(OH-)约为10-4.3mol/L,故
3 3
pH=9.7,C项正确;D项,pH=7,根据电荷守恒可得c(Na+)=c(X-),再根据物料守恒3c(Na+)= c(HX)
+c(X-),故可得c(X-)∶c(HX)=1∶2,D项正确;故选A。
3.某研究小组为测定食用白醋中醋酸的含量进行了如下操作,正确的是( )
A.用碱式滴定管量取一定体积的待测白醋放入锥形瓶中
B.称取4.0 g NaOH放到100 mL容量瓶中,加水至刻度线,配成1.00 mol/L NaOH标准溶液
C.用NaOH溶液滴定白醋,使用酚酞作指示剂,溶液颜色恰好由无色变为浅红色,且半分钟内不褪
色时为滴定终点
D.滴定时眼睛要注视着滴定管内NaOH溶液的液面变化,防止滴定过量
资料整理【淘宝店铺:向阳百分百】【答案】C
【解析】A项不能用碱式滴定管量取白醋,应用酸式滴定管,错误;B项应先在烧杯中溶解固体,不
能直接在容量瓶中溶解,错误;C项强碱滴定弱酸,用酚酞作指示剂,颜色变化符合滴定终点判断,正确;
D项滴定时眼睛应注视锥形瓶内溶液颜色变化,错误。
4.用标准盐酸滴定未知浓度的氢氧化钠溶液,用甲基橙作指示剂,下列说法不正确的是( )
A.可以用酚酞代替指示剂
B.滴定前不能用待测液润洗锥形瓶
C.若氢氧化钠吸收少量CO,不影响滴定结果
2
D.当锥形瓶内溶液由橙色变为红色,且半分钟内颜色不恢复,即达到滴定终点
【答案】D
【解析】 A项,强酸与强碱滴定时,可以选用酚酞作指示剂,正确;B项,滴定前若用待测液润洗锥
形瓶,会导致n(NaOH)增大,盐酸消耗的量偏大,滴定结果偏大,正确;C项,若NaOH吸收少量CO ,
2
发生的反应为CO+2OH-=CO 2-+H O,再滴入盐酸,盐酸先和剩余的OH-反应,H++OH-=H O,再与CO2-反
2 3 2 2 3
应,CO2-+2H+=H O+CO↑,存在关系2OH-~ CO2-~2H+,因此消耗HCl的物质的量始终等于NaOH的物质
3 2 2 3
的量,所以氢氧化钠吸收少量CO ,不影响测定结果,正确;D项,当锥形瓶内溶液颜色由黄色变为橙色,
2
且半分钟内颜色不恢复,即到达滴定终点,如果变为红色说明盐酸已经过量,错误。
5.准确移取20.00 mL某待测 HCl溶液于锥形瓶中,用0.1000 mol·L-1 NaOH溶液滴定。下列说法正
确的是( )
A.滴定管用蒸馏水洗涤后,装入NaOH溶液进行滴定
B.随着NaOH溶液的滴入,锥形瓶中溶液pH由小变大
C.用酚酞作指示剂,当锥形瓶中溶液由红色变为无色时停止滴定
D.滴定达到终点时,发现滴定管尖嘴部分有悬滴,则测定结果偏小
【答案】B
【解析】A项,滴定管用蒸馏水洗涤后,需用NaOH溶液润洗后才能装入NaOH溶液进行滴定。B项,
随着NaOH溶液的滴入,锥形瓶内溶液中c(H+)越来越小,故pH由小变大。C项,用酚酞作指示剂,当锥
形瓶内溶液由无色变为浅红色,且半分钟内不褪去时,说明达到滴定终点,应停止滴定。D项,滴定达到
终点时,滴定管尖嘴部分有悬滴,则所计算加入标准NaOH溶液的量偏多,测定结果偏大。
6.(2023·四川省成都市石室中学期中)T℃时,水的离子积常数K =10-13,该温度下,V mLpH=12的
w 1
Ba(OH) 稀溶液与V mLpH=2的稀硫酸充分反应(混合后的体积变化忽略不计),恢复到T℃,测得混合溶
2 2
液的pH=3,则V:V 的值为( )
1 2
A.9∶101 B.99∶101 C.1∶100 D.1∶10
【答案】A
【解析】T℃时,水的离子积常数K =10-13,该温度下,V mLpH=12的Ba(OH) 稀溶液,c(H+)=10-12
w 1 2
资料整理【淘宝店铺:向阳百分百】mol/L,则c(OH-)=10-1 mol/L mol/L;V mLpH=2的稀硫酸c(H+)=10-2 mol/L,二者反应后恢复到T℃,测得
2
混合溶液的pH=3,c(H+)=10-3 mol/L,说明酸过量,则c(H+)= ,解得V:
1
V=9∶101,故选A。
2
7.(2023·四川省成都市高二期末)为探究浓度对醋酸电离程度的影响,用 计测定 时不同浓度醋
酸的 结果如下,下列说法正确的是( )
浓度/ 0.0010 0.010 0.020 0.10 0.20
3.88 3.38 3.23 2.88 2.83
A.实验过程中可以改用广泛 试纸
B. 溶液稀释过程中,醋酸电离程度及溶液导电性都增大
C. 时,电离常数K(CH COOH)的数量级为10-5
3
D.CHCOOH溶液稀释过程中不可能出现c(H+)>c(OH―)>c(CHCOO-)
3 3
【答案】C
【解析】A项,广泛pH试纸测得溶液的pH为范围值,不是精确值,所以实验过程中不能改用广泛
pH试纸测定不同浓度醋酸的pH,故A错误;B项,0.20mol/L醋酸溶液稀释过程中,溶液中的离子浓度减
小,溶液导电性减弱,故B错误;C项,由表格数据可知,25℃时,0.0010mol/L醋酸溶液pH为3.88,则
电离常数约为 =10—4.76,电离常数的数量积为10—5,故C正确;D项,在极稀的醋酸溶液中,
氢氧根离子浓度大于醋酸根离子浓度,所以醋酸溶液稀释过程中可能出现c(H+)>c(OH―)>c(CHCOO-),
3
故D错误;故选C。
8.(2023·江苏省徐州市高二期末)水的离子积常数随着温度的变化关系如表:
温度/℃ 25 50 75 100
K /×10-14 1.0 5.5 20.0 56.0
W
下列说法正确的是( )
A.纯水中c(H+)的大小与温度无关
B.水的电离度a(50℃)C>A=D=E,B正确;C项,
从A点到D点,温度不变,Kw不变,加酸,c(H+)变大,c(OH-)变小,C正确;D项,若处在B点时,
pH=3的稀硫酸中c(H+) =10-3 mol·L−1, pH=9的KOH中c(OH)= ,溶液显中性,
D正确;故选A。
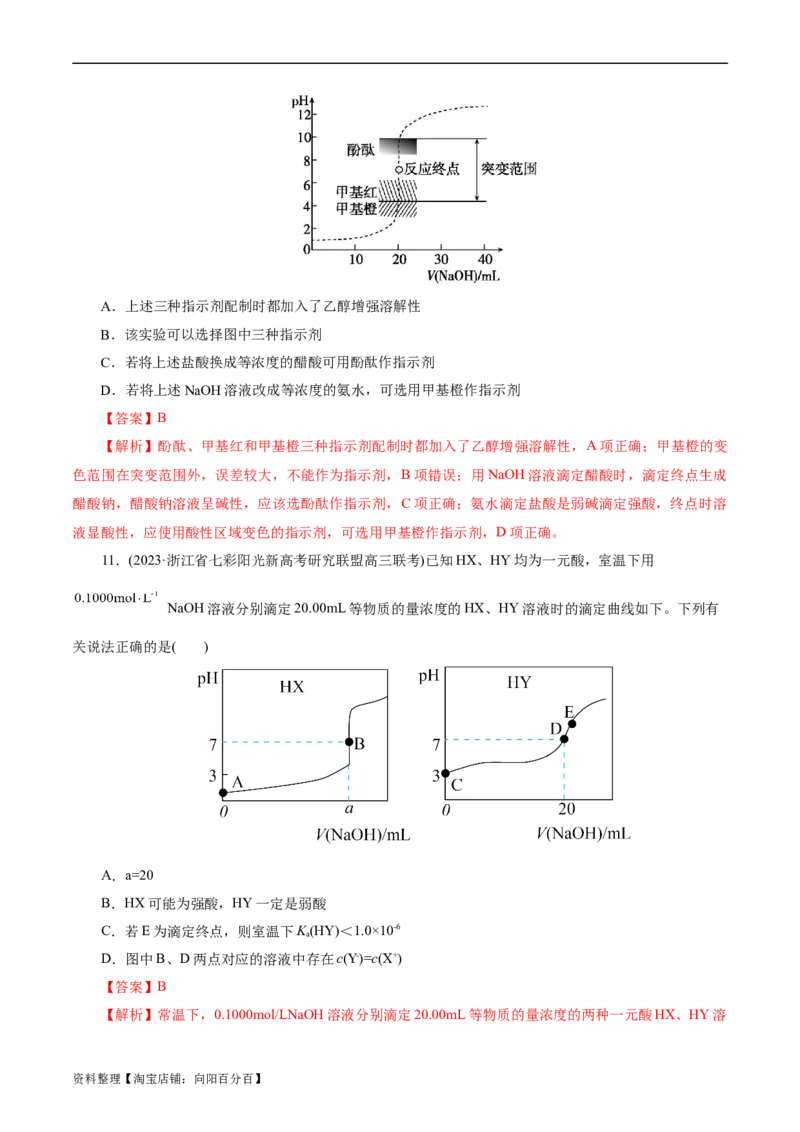
10.室温下,向20.00 mL 0.100 0 mol·L-1盐酸中滴加0.100 0 mol·L-1 NaOH溶液,溶液的pH随NaOH
溶液体积的变化如下图所示,下列说法中不正确的是 ( B )
资料整理【淘宝店铺:向阳百分百】A.上述三种指示剂配制时都加入了乙醇增强溶解性
B.该实验可以选择图中三种指示剂
C.若将上述盐酸换成等浓度的醋酸可用酚酞作指示剂
D.若将上述NaOH溶液改成等浓度的氨水,可选用甲基橙作指示剂
【答案】B
【解析】酚酞、甲基红和甲基橙三种指示剂配制时都加入了乙醇增强溶解性,A项正确;甲基橙的变
色范围在突变范围外,误差较大,不能作为指示剂,B项错误;用NaOH溶液滴定醋酸时,滴定终点生成
醋酸钠,醋酸钠溶液呈碱性,应该选酚酞作指示剂,C项正确;氨水滴定盐酸是弱碱滴定强酸,终点时溶
液显酸性,应使用酸性区域变色的指示剂,可选用甲基橙作指示剂,D项正确。
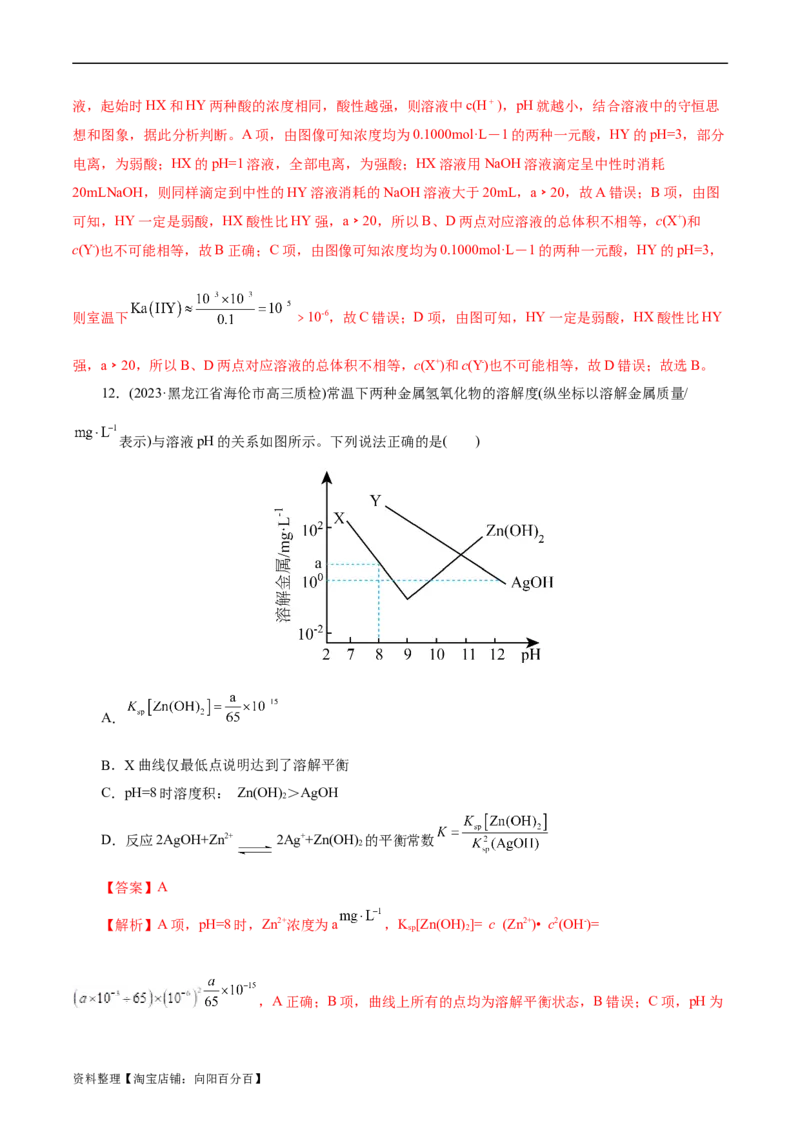
11.(2023·浙江省七彩阳光新高考研究联盟高三联考)已知HX、HY均为一元酸,室温下用
NaOH溶液分别滴定20.00mL等物质的量浓度的HX、HY溶液时的滴定曲线如下。下列有
关说法正确的是( )
A.a=20
B.HX可能为强酸,HY一定是弱酸
C.若E为滴定终点,则室温下K(HY)<1.0×10-6
a
D.图中B、D两点对应的溶液中存在c(Y-)=c(X+)
【答案】B
【解析】常温下,0.1000mol/LNaOH溶液分别滴定20.00mL等物质的量浓度的两种一元酸HX、HY溶
资料整理【淘宝店铺:向阳百分百】液,起始时HX和HY两种酸的浓度相同,酸性越强,则溶液中c(H + ),pH就越小,结合溶液中的守恒思
想和图象,据此分析判断。A项,由图像可知浓度均为0.1000mol·L-1的两种一元酸,HY的pH=3,部分
电离,为弱酸;HX的pH=1溶液,全部电离,为强酸;HX溶液用NaOH溶液滴定呈中性时消耗
20mLNaOH,则同样滴定到中性的HY溶液消耗的NaOH溶液大于20mL,a﹥20,故A错误;B项,由图
可知,HY一定是弱酸,HX酸性比HY强,a﹥20,所以B、D两点对应溶液的总体积不相等,c(X+)和
c(Y-)也不可能相等,故B正确;C项,由图像可知浓度均为0.1000mol·L-1的两种一元酸,HY的pH=3,
则室温下 ﹥10-6,故C错误;D项,由图可知,HY一定是弱酸,HX酸性比HY
强,a﹥20,所以B、D两点对应溶液的总体积不相等,c(X+)和c(Y-)也不可能相等,故D错误;故选B。
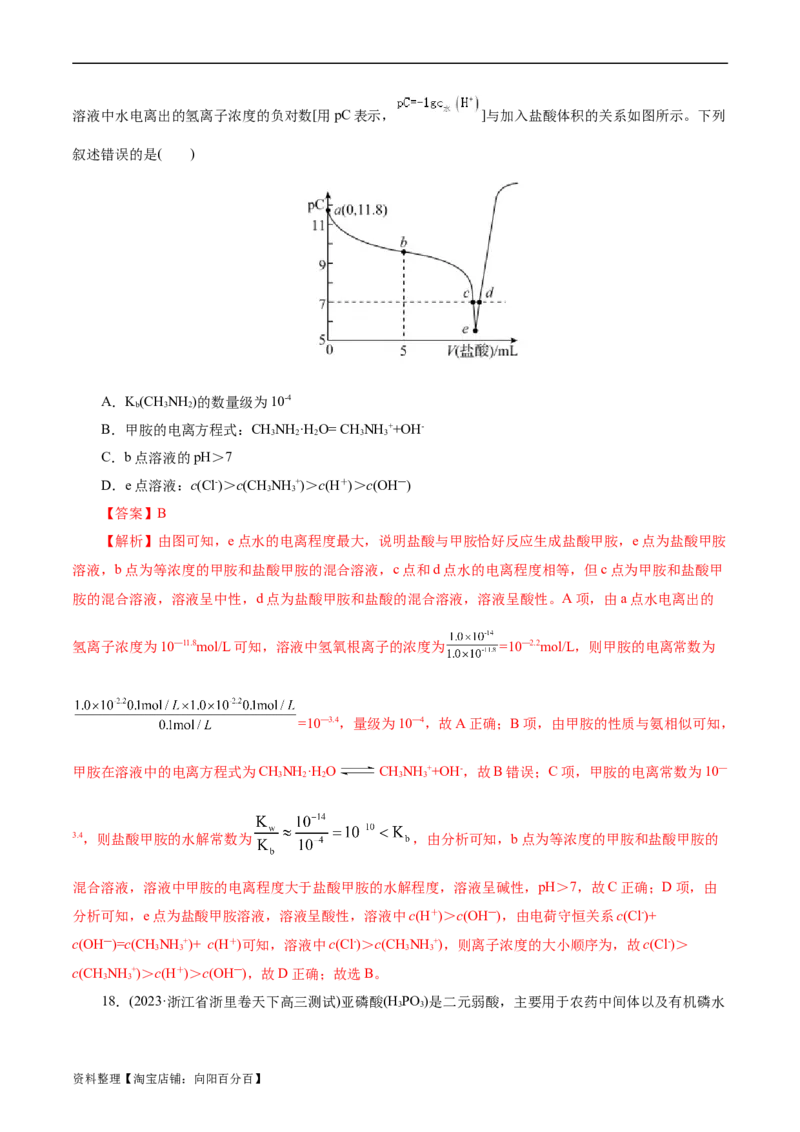
12.(2023·黑龙江省海伦市高三质检)常温下两种金属氢氧化物的溶解度(纵坐标以溶解金属质量/
表示)与溶液pH的关系如图所示。下列说法正确的是( )
A.
B.X曲线仅最低点说明达到了溶解平衡
C.pH=8时溶度积: Zn(OH) >AgOH
2
D.反应2AgOH+Zn2+ 2Ag++Zn(OH) 的平衡常数
2
【答案】A
【解析】A项,pH=8时,Zn2+浓度为a ,K [Zn(OH) ]= c (Zn2+)• c2(OH-)=
sp 2
,A正确;B项,曲线上所有的点均为溶解平衡状态,B错误;C项,pH为
资料整理【淘宝店铺:向阳百分百】8时,Zn2+的浓度比Ag+小得多且c(OH-)小于1,则AgOH的溶度积c (Ag+)• c(OH-)比Zn(OH) 的溶度积c
2
(Zn2+)• c2(OH-)大,C错误;D项,2AgOH+Zn2+ 2Ag++Zn(OH) 平衡常数
2
,D错误;故选A。
13.白云石[CaMg(CO )]中钙含量测定常用KMnO 滴定的方法。具体做法是将其酸溶后转化为草酸钙,
3 2 4
过滤后用酸溶解,再用KMnO 滴定。则下列说法错误的是( )
4
A.KMnO 滴定草酸发生反应的离子方程式为:2MnO -+5H C O+6H+=2Mn2++10CO ↑+8H O
4 4 2 2 4 2 2
B.实验过程中两次用酸溶解,均需使用稀盐酸
C.KMnO 滴定草酸过程中,标准状况下每产生448mLCO 气体理论上转移0.02mole-
4 2
D.滴定过程中若滴加KMnO 过快会发生反应4MnO -+12H+=4Mn2++5O ↑+6H O,将导致测定结果偏
4 4 2 2
高
【答案】B
【解析】A项,草酸是弱酸,具有还原性,会被高锰酸钾氧化,根据质量守恒和化合价升降守恒等可
知KMnO 滴定草酸发生反应的离子方程式为:2MnO -+5H C O+6H+=2Mn2++10CO ↑+8H O,A正确;B项,
4 4 2 2 4 2 2
高锰酸钾具有强氧化性,会氧化盐酸产生氯气造成误差,所以实验过程中不可使用稀盐酸,B错误;C项,
KMnO 滴定草酸过程中,存在 关系,标准状况下448mLCO 气体物质
4 2
的量为 ,根据关系式可知理论上转移0.02mole-,C正确;D项,根据质量守恒
定律和的失电守恒定律可以得出: ,滴定过程中若滴加KMnO 过
4
快会发生反应4MnO -+12H+=4Mn2++5O ↑+6H O,消耗的KMnO 溶液体积会偏大,会导致测定结果偏高,
4 2 2 4
D正确;故选B。
14.常温下,有关物质的溶度积如下
物质 CaCO MgCO Ca(OH) Mg(OH) Fe(OH)
3 3 2 2 3
K 4.96×10-9 6.82×10-6 4.68×10-6 5.61×10-12 2.64×10-39
sp
下列有关说法不正确的是( )
A.常温下,除去NaCl溶液中的MgCl 杂质,选用NaOH溶液比NaCO 溶液效果好
2 2 3
B.常温下,除去NaCl溶液中的CaCl 杂质,选用NaOH溶液比NaCO 溶液效果好
2 2 3
C. 向含有Mg 2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg
资料整理【淘宝店铺:向阳百分百】2+)∶c(Fe3+)=2 .125×1021
D.将适量的Ca(OH) 固体溶于100mL水中,刚好达到饱和[c(Ca2+)=1.054×10-2mol/L],若保持温度不
2
变, 向其中加入100mL 0.012mol/L的NaOH,则该溶液变为不饱和溶液。
【答案】B
【解析】A项, 因为MgCO 是微溶物,其溶度积远远大于Mg(OH) ,所以除去NaCl溶液中的MgCl
3 2 2
杂质,选用NaOH溶液比NaCO 溶液效果好,A项正确;B项, 因为Ca(OH) 是微溶物,其溶度积远大
2 3 2
于CaCO ,所以除去NaCl溶液中的CaCl 杂质,选用NaCO 溶液比NaOH溶液效果好,B项错误;C项,
3 2 2 3
向 含 有 Mg2+ 、 Fe3+ 的 溶 液 中 滴 加 NaOH 溶 液 , 当 两 种 沉 淀 共 存 且 溶 液 的 pH=8 时 ,
, , 所 以
,C项正确;D项,将适量的Ca(OH) 固体溶于100mL水中,
2
刚好达到饱和,c(Ca2+)=1.054×10-2mol/L,c(OH-)=2.108×10-2mol/L,若保持温度不变,向其中加入
100mL 0.012mol/L 的 NaOH , 混 合 后 , c(Ca2+)=0.527×10-2mol/L ,
, 此 时 Ca(OH) 的 离 子 积
2
,则该溶液变为不饱和溶液,D项正确;
故选B。
15.一种测定水样中溴离子浓度的实验步骤如下:
①向锥形瓶中加入处理后的水样25.00mL,加入几滴NH Fe(SO ) 溶液。
4 4 2
②加入V mL c mol∙L−1AgNO 溶液(过量),充分摇匀。
1 1 3
③用c mol∙L−1KSCN标准溶液进行滴定,至终点时消耗标准溶液VmL 。
2 2
已知:K (AgBr)=7.7×10−13,Ag++SCN-= AgSCN(白色)↓,K (AgSCN)=1×10−12,下列说法不正确的是(
sp sp
)
A.滴定终点时,溶液变为红色
B.该水样中溴离子浓度为:c(Br-)= mol∙L−1
C.AgBr(s)+SCN-(aq) AgSCN(s)+Br-(aq)的平衡常数K=0.77
D.该实验需要严格控制水样的pH,若pH过高则测定结果将偏高
资料整理【淘宝店铺:向阳百分百】【答案】D
【解析】A项,加入几滴NH Fe(SO ) 指示剂,滴定终点时,KSCN过量,会与铁离子反应,因此溶液
4 4 2
变为红色,故A正确;B项,25mL溶液中Br-物质的量n(Br-)= V ×10−3 L×c mol∙L−1− V ×10−3 L×c
1 1 2 2
mol∙L−1=(V c − V c ) ×10−3 mol,因此该水样中溴离子浓度为:c(Br-)= mol∙L−1,故B正确;
1 1 2 2
C项,AgBr(s)+SCN-(aq) AgSCN(s)+Br-(aq)的平衡常数
,故C正确;D项,该实验需要严格控制水样的pH,若pH
过高,银离子会与氢氧根反应,则得到的溴离子物质的量减少,则测定结果将偏低,故D错误。故选D。
16.常温下,向浓度均为0.1 mol·L-1体积均为10 mL的两种一元酸(HX、HY)溶液中,分别滴入0.1
mol·L-1 NaOH溶液,pH的变化曲线如图所示。下列说法中错误的是( )
A.N点:(Na+)=(Y-)+(HY)
B.M点:(X-)>(Na+)
C.滴至pH=7时,消耗NaOH溶液的体积:HX溶液>HY溶液
D.滴入10 mL NaOH溶液时,溶液中水的电离程度:HX溶液<HY溶液
【答案】A
【解析】据图可知,浓度均为0.1 mol·L-1的两种一元酸(HX、HY)溶液的pH都大于1,说明HX和
HY均为弱酸,N点加入NaOH溶液的体积为15 mL,NaOH与HY的物质的量之比为3∶2,则根据物料守
恒得2(Na+)=3 c(Y-)+3 c(HY),A项错误;M点加入NaOH溶液的体积为5 mL,根据反应方程式:
NaOH+HX===NaX+HO可知,反应后所得溶液中HX和NaX的物质的量相等,此时溶液的pH<7,说明
2
HX的电离程度大于X-的水解程度,所以(X-)>(Na+),B项正确;据图可知,浓度均为0.1 mol·L-1的两种
一元酸HX、HY溶液的pH大小关系为pH(HX)<pH(HY),说明酸性HX>HY,因酸性越弱其对应的阴离
子水解程度越大,所以滴至pH=7时,消耗NaOH溶液的体积:HX溶液>HY溶液,C项正确;滴入10
mL NaOH溶液时,HX和HY均恰好完全反应分别得到NaX溶液和NaY溶液,因酸性HX>HY,则X-的
水解程度小于Y-的水解程度,溶液中水的电离程度:HX溶液<HY溶液,D项正确。
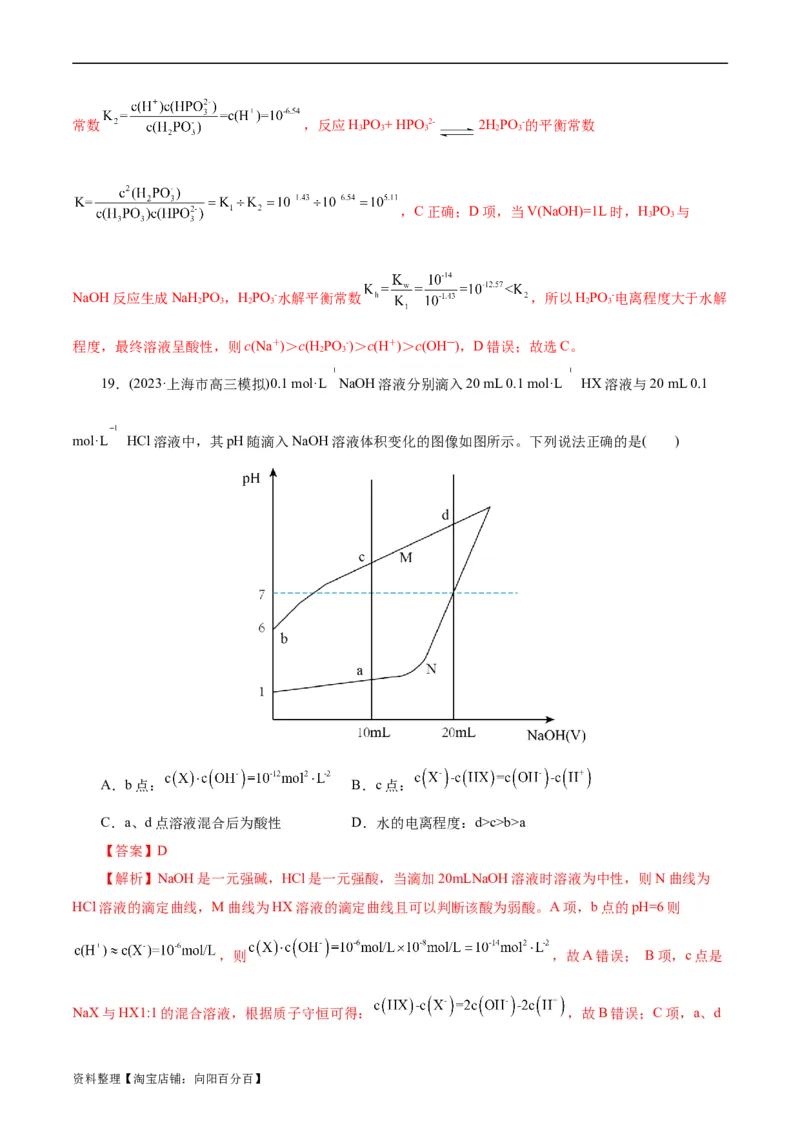
17.甲胺(CHNH )的性质与氨相似,250C时向10mL 0.1mol·Lˉ1的甲胺中逐滴滴入0.1mol·Lˉ1稀盐酸。
3 2
资料整理【淘宝店铺:向阳百分百】溶液中水电离出的氢离子浓度的负对数[用pC表示, ]与加入盐酸体积的关系如图所示。下列
叙述错误的是( )
A.K(CHNH )的数量级为10-4
b 3 2
B.甲胺的电离方程式:CHNH ·H O= CH NH ++OH-
3 2 2 3 3
C.b点溶液的pH>7
D.e点溶液:c(Cl-)>c(CHNH +)>c(H+)>c(OH―)
3 3
【答案】B
【解析】由图可知,e点水的电离程度最大,说明盐酸与甲胺恰好反应生成盐酸甲胺,e点为盐酸甲胺
溶液,b点为等浓度的甲胺和盐酸甲胺的混合溶液,c点和d点水的电离程度相等,但c点为甲胺和盐酸甲
胺的混合溶液,溶液呈中性,d点为盐酸甲胺和盐酸的混合溶液,溶液呈酸性。A项,由a点水电离出的
氢离子浓度为10—11.8mol/L可知,溶液中氢氧根离子的浓度为 =10—2.2mol/L,则甲胺的电离常数为
=10—3.4,量级为10—4,故A正确;B项,由甲胺的性质与氨相似可知,
甲胺在溶液中的电离方程式为CHNH ·H O CHNH ++OH-,故B错误;C项,甲胺的电离常数为10—
3 2 2 3 3
3.4,则盐酸甲胺的水解常数为 ,由分析可知,b点为等浓度的甲胺和盐酸甲胺的
混合溶液,溶液中甲胺的电离程度大于盐酸甲胺的水解程度,溶液呈碱性,pH>7,故C正确;D项,由
分析可知,e点为盐酸甲胺溶液,溶液呈酸性,溶液中c(H+)>c(OH―),由电荷守恒关系c(Cl-)+
c(OH―)=c(CHNH +)+ c(H+)可知,溶液中c(Cl-)>c(CHNH +),则离子浓度的大小顺序为,故c(Cl-)>
3 3 3 3
c(CHNH +)>c(H+)>c(OH―),故D正确;故选B。
3 3
18.(2023·浙江省浙里卷天下高三测试)亚磷酸(H PO )是二元弱酸,主要用于农药中间体以及有机磷水
3 3
资料整理【淘宝店铺:向阳百分百】处理药剂的原料。常温下,向1 mL0.5mol·L-1HPO 溶液中滴加等浓度的NaOH溶液,混合溶液中含磷粒子
3 3
的物质的量分数 与溶液 的关系如图所示。下列说法正确的是( )
A.a、b两点时,水电离出的c(OH―) 之比为1.43:6.54
水
B.b点对应溶液中存在:c(Na+)=3c(HPO 2- )
3
C.反应HPO + HPO 2- 2HPO -的平衡常数为
3 3 3 2 3
D.当V(NaOH)=1L时,c(Na+)>c(H PO -)>c(OH―)>c(H+)
2 3
【答案】C
【解析】亚磷酸(H PO )是二元弱酸,常温下,向1 mL0.5mol·L-1HPO 溶液中滴加等浓度的NaOH溶
3 3 3 3
液,先后发生的反应为① HPO +OH-= H PO -+H O,②HPO -+OH-= HPO 2-+H O,则HPO 逐渐减少,
3 3 2 3 2 2 3 3 2 3 3
HPO -先增多后减少,HPO 2-逐渐增多,故 表示HPO 变化曲线, 表示HPO -变化曲线, 表示
2 3 3 3 3 2 3
HPO 2-变化曲线。A项,a、b两点均为酸性溶液,则水电离出的c(OH―) 分别为10-12.57 mol·L-1、10-7.46
3 水
mol·L-1,其之比为1:105.11,A错误;B项,b点时,c(H PO -)=c(HPO 2-),根据电荷守恒可知,c(Na+)+c(H
2 3 3
+)=c(OH―)+c(H PO -)+2c(HPO 2-)=c(OH―)+3c(HPO 2-),因b点不是中性点,即c(OH―)≠c(H+),则c(Na
2 3 3 3
+)≠3c(HPO 2-),B错误;C项,a点时,c(H PO )=c(H PO -),则反应HPO H++HPO -的平衡常数
3 3 3 2 3 3 3 2 3
,b点时,c(H PO -)=c(HPO 2-),则反应HPO - H++HPO 2-的平衡
2 3 3 2 3 3
资料整理【淘宝店铺:向阳百分百】常数 ,反应HPO + HPO 2- 2HPO -的平衡常数
3 3 3 2 3
,C正确;D项,当V(NaOH)=1L时,HPO 与
3 3
NaOH反应生成NaH PO ,HPO -水解平衡常数 ,所以HPO -电离程度大于水解
2 3 2 3 2 3
程度,最终溶液呈酸性,则c(Na+)>c(H PO -)>c(H+)>c(OH―),D错误;故选C。
2 3
19.(2023·上海市高三模拟)0.1 mol·L NaOH溶液分别滴入20 mL 0.1 mol·L HX溶液与20 mL 0.1
mol·L HCl溶液中,其pH随滴入NaOH溶液体积变化的图像如图所示。下列说法正确的是( )
A.b点: B.c点:
C.a、d点溶液混合后为酸性 D.水的电离程度:d>c>b>a
【答案】D
【解析】NaOH是一元强碱,HCl是一元强酸,当滴加20mLNaOH溶液时溶液为中性,则N曲线为
HCl溶液的滴定曲线,M曲线为HX溶液的滴定曲线且可以判断该酸为弱酸。A项,b点的pH=6则
,则 ,故A错误; B项,c点是
NaX与HX1:1的混合溶液,根据质子守恒可得: ,故B错误;C项,a、d
资料整理【淘宝店铺:向阳百分百】点溶液混合即30mLNaOH溶液与20 mL 0.1 mol·L-1 HX溶液与20 mL 0.1 mol·L-1 HCl溶液混合,溶质为
NaCl 和1:1的NaX与HX,酸碱性等价于c点,由图可知呈碱性,故C错误;D项,d点溶质只有NaX对
水的电离起促进作用,c点NaX与HX1:1的混合溶液,溶液显碱性说明水解程度大于电离程度,HCl是一
元强酸而HX为弱酸,强酸对水的电离的抑制程度更大,所以水的电离程度:d>c>b>a,故D正确;故选
D。
20.(2023·河南省南阳市三模)常温下,向10 mL0.1 mol·L-1HA溶液中逐滴加入0.1 mol·L-1的MOH溶
液,其导电率、pH与加入MOH溶液体积的关系如图所示(假设反应过程中温度不变)。
下列说法正确的是( )
A.a→d过程中,水的电离程度逐渐增大
B.加入10 mL→13 mL MOH溶液时,导电率降低是因为离子总数减小
C.常温下,K (MOH) =K(HA)≈10 -4.6
b a
D.b点溶液中c (HA) +2c (H+) =c (A-) +2c (MOH) +c (OH- )
【答案】C
【解析】起点a点对应的pH值为2.8,说明HA是弱酸,c点加入MOH10ml时二者完全反应呈中性,
也说明MOH是弱碱,MA是呈中性的弱酸弱碱盐,b点是加入5ml时让HA中和一半,此时溶液中存在
MA和HA物质的量为1:1。A项,a→c过程是由酸到正盐的过程,水的电离程度逐渐增大,c→d是碱过
量又抑制水的电离,故A错误;B项,10 mL→13 mL是碱过量,离子数目继续增加,溶液体积继续增大,
但是离子浓度在减小,所以导电率减小,故B错误;C项,因为生成的弱酸弱碱盐呈中性,说明K
b
(MOH) =K(HA),在a点pH=2.8,c(H+)=c(A-)=10-2.8 mol/L,c(HA)=0.1mol/L,
a
,故C正确;D项,b点是加入5ml时让HA中和一半,此时溶液
资料整理【淘宝店铺:向阳百分百】中存在MA和HA物质的量为1:1,根据物料守恒和电荷守恒得出如下式子c(HA)+c(A-)=2c(M+)+2c(MOH)
(1)和c(H+)+c(M+)=c(A-)+c(OH-)(2),(1)+(2)×2得到如下式子:c (HA) +2c (H+) =c (A-) +2c (MOH) +2c
(OH- ),故D错误;故选C。
21.(2023·山东省高三联考)一定条件下,乙酸酐[(CH CO) O]醇解反应
3 2
[(CH CO) O+ROH→CH COOR+CH COOH]可进行完全,利用此反应定量测定有机醇(ROH)中的羟基含
3 2 3 3
量,实验过程中酯的水解可忽略。实验步骤如下:
①配制一定浓度的乙酸酐-苯溶液。
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入 样品,充分反应后,加适量水使剩余乙酸
酐完全水解:(CHCO) O+HO→2CH COOH。
3 2 2 3
③加指示剂并用cmol·L-1NaOH-甲醇标准溶液滴定至终点,消耗标准溶液VmL。
1
④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加指示剂并用
cmol·L-1NaOH-甲醇标准溶液滴定至终点,消耗标准溶液VmL。根据上述实验原理,下列说法正确的是(
2
)
A.可以用乙酸代替乙酸酐进行上述实验
B.若因甲醇挥发造成标准溶液浓度发生变化,将导致测定结果偏小
C.步骤③滴定时,不慎将锥形瓶内溶液溅出,将导致测定结果偏小
D.步骤④中,若加水量不足,将导致测定结果偏大
【答案】B
【解析】用cmol·L-1NaOH-甲醇标准溶液滴定乙酸酐完全水解生成的乙酸,消耗标准溶液VmL,则消
2
耗NaOH的物质的量为(V ×c×10-3) mol,即乙酸酐的总物质的量为 ,ROH与乙酸酐反应
2
后剩余的乙酸酐的物质的量为 ,所以与ROH反应消耗的乙酸酐的物质的量为
。A项,乙酸与醇的酯化反应可逆,不能用乙酸代替乙酸酐进行上述实验,
A项错误;B项,若甲醇挥发,NaOH-甲醇溶液的浓度将偏大,滴定时消耗NaOH-甲醇溶液的体积偏小,
步骤④中所得V 偏小,而ROH的物质的量为 ,故将导致测定结果偏小,B
2
资料整理【淘宝店铺:向阳百分百】项正确;C项,步骤③滴定时,不慎将锥形瓶内溶液溅出,消耗NaOH-甲醇溶液的体积偏小即V 偏小,而
1
ROH的物质的量为 ,故将导致测定结果偏大,C项错误;D项,步骤④中,
若加水量不足,乙酸酐未完全水解,生成乙酸的物质的量偏小,消耗NaOH-甲醇溶液的体积偏小即V 偏
2
小,而ROH的物质的量为 ,故将导致测定结果偏小,D项错误;故选B。
22.使用硫酸亚铁铵晶体[(NH )Fe(SO )·6H O]滴定法可以测定青铜中铬元素的含量。实验步骤如下:
4 2 4 2 2
步骤1:称量硫酸亚铁铵晶[(NH )Fe(SO )·6H O]溶于稀硫酸,加水稀释配成1000 mL0.0200 mol/L
4 2 4 2 2
(NH )Fe(SO ) 标准溶液。
4 2 4 2
步骤2:称取1.00 g青铜样品于250 mL维形瓶中,加入适量稀硝酸使其完全溶解,再加入适量过硫酸
[(NH )SO]溶液,加热煮沸,使样品中的铬元素完全转化为HCrO,冷却后加蒸馏水配制成250 mL溶液,
4 2 2 8 2 4
摇匀。
步骤3:取25 mL上述溶液置于锥形瓶中,加入硫酸酸化,滴入4滴N-苯代邻氨基苯甲酸指示剂,用
(NH )Fe(SO ) 标准溶液满淀至终点。重复上述操作3次。测得消耗(NH )Fe(SO ) 标准溶液的体积分别为
4 2 4 2 4 2 4 2
18.90 mL、17.97 mL、18.03 mL。发生反应的离子方程式为:HCrO+Fe2++H+→Cr3++Fe3++H O (未配平)
2 4 2
下列说法不正确的是( )
A.在“步骤1”中,用到的玻璃仪器有1000 mL容量瓶、烧杯、玻璃棒、胶头滴管
B.在“步骤2”中,铜与硝酸反应的离子方程式为:3Cu+2NO-+8H+=3Cu2++2NO↑+4HO
3 2
C.青铜中铬元素的质量分数为6.344%
D.实验中,如果盛放(NH )Fe(SO ) 标准溶液的滴定管没有润洗,则测量结果将偏大
4 2 4 2
【答案】C
【解析】A项,在“步骤1”中配制溶液需要的玻璃仪器:1000 mL容量瓶、烧杯、玻璃棒、胶头滴管,
故A正确;B项,在“步骤2”中,铜与硝酸反应的离子方程式根据电子、电荷、原子守恒配平得方程式为:
3Cu+2NO-+8H+=3Cu2++2NO↑+4HO ,故B正确;C项,根据滴定过程(NH )Fe(SO ) 标准溶液的体积分别
3 2 4 2 4 2
为18.90 mL、17.97 mL、18.03 mL,因为第一组实验数据与第二、三组误差大而舍去,故平均消耗的溶液
体积为:V= ,反应关系式计算: ,
资料整理【淘宝店铺:向阳百分百】解得x=1.2×10-4mol,则铬元素的质量分数为: = 6.24%,故C不正确;D项,实验
中,如果盛放(NH )Fe(SO ) 标准溶液的滴定管没有润洗,实际标准液被稀释,导致滴加的体积偏大,在计
4 2 4 2
算时导致测量结果偏大,故D正确;故选C。
23.下表是常温下几种常见弱酸的电离平衡常数,回答下列问题:
弱酸 电离平衡常数K
CHCOOH K=1.6×10−5
3
HC O K=5.9×10−2 K=6.4×10−5
2 2 4 1 2
HCO K=4.4×10−7 K=5.6×10−11
2 3 1 2
HS K=9.1×10−8 K=1.1×10−15
2 1 2
(1)某温度下,纯水中的 c(H+)=2.0×10−7mol/L,则此时溶液中 c(OH−)为______________mol/L;此时温
度________25℃(填“大于”,“小于”或“等于”),若温度不变,滴入稀硫酸使 c(H+)=8.0×10−6mol/L,
则由水电离出的 c(H+)为__________mol/L。
(2)下列四种离子结合H+能力最强的是_________。
A.HCO - B.C O2- C.S2− D.CHCOO−
3 2 4 3
(3)该温度下1.0 mol·L−1的CHCOOH溶液中的c(H+)=__________mol·L−1
3
(4)常温下,加水稀释0.1 mol·L−1的HC O 溶液,下列说法正确的是___________。
2 2 4
A.溶液中n(H+)×n(OH−)保持不变
B.溶液中水电离的c(H+)×c(OH−)保持不变
C.溶液中c(HC O-)/c(H C O)保持不变
2 4 2 2 4
D.溶液中c(OH−)增大
【答案】(1)2.0×10−7 大于 5.0×10−9 (2)C (3)4.0×10−3 (14)D
【解析】(1)水电离产生的氢离子浓度和氢氧根离子浓度相等,某温度下,纯水中的
c(H+)=2.0×10−7mol/L,则此时溶液中 c(OH−)=2.0×10−7mol/L;
K =c(OH−)×c(H+)=2.0×10−7mol/L×2.0×10−7mol/L=4.0×10−14;而常温下,K =1.0×10−14,水的电离过程吸热,
w w
升高温度,促进电离,所以此时温度大于25℃;酸抑制水电离,酸溶液中的氢氧根离子浓度与水电离出的
c(H+)相等,即酸溶液中c(H+)=8.0×10−6mol/L,根据K =c(OH−)×c(H+)可知,c(OH−)= =5.0×10−9
w
mol/L,所以水电离出的 c(H+)为5.0×10−9 mol/L;(2)电离平衡常数越大,酸的电离程度越大,溶液的酸性
越强;根据表中数据,酸性:HC O->CH COOH >H CO >HS-,酸的酸性越弱,对应的酸根离子结合氢离
2 4 3 2 3
资料整理【淘宝店铺:向阳百分百】