文档内容
考点 27 水的电离与溶液的 pH
(核心考点精讲精练)
一、3年真题考点分布
考点内容 考题统计
2023湖南卷12题,4分;2021辽宁卷15题,3
中和滴定曲线分析 分;2021湖北卷14题,3分;2021海南卷14
题,4分;
二、命题规律及备考策略
【命题规律】
从近三年高考试题来看,涉及本考点的试题难度一般较大,常结合盐类水解、电离平衡以及离子浓
度大小比较等进行综合命题,常见的命题形式:(1)结合图像考查溶液的酸碱性判断、pH的计算,以及离
子浓度的大小比较等;(2)以酸碱中和滴定为载体,考查“强”滴“弱”过程中微粒浓度的变化以及其他相
关知识;(3)以滴定为基础,考查相关操作和计算等。
【备考策略】
(1)认识溶液的酸碱性及pH,掌握检测溶液pH的方法。
(2)能进行溶液pH的简单计算,能正确测定溶液pH,能调控溶液的酸碱性。
(3)能选择实例说明溶液pH的调控在工农业生产和科学研究中的重要作用。
(4)理解酸碱中和滴定,能根据实验试题要求分析或处理实验数据,得出合理结论;能够分析以图像形
式考查滴定曲线。
【命题预测】
预测2024年本考点依然会结合图像,考查水的电离平衡与溶液酸碱性的关系,以及pH的相关计算
等;还会基于中和滴定,考查氧化还原滴定、沉淀滴定等有关计算,注意滴定现象、操作、滴定终点判断
的规范表达,能进行误差分析。
考法 1 水的电离
1.水的电离
水是极弱的电解质,其电离方程式为2HO HO++OH-或HO H++OH-。
2 3 2
2.水的离子积常数
(1)表达式:K =c(H+)·c(OH-)。室温下,K =1×10-14。
w w(2)影响因素:只与温度有关,水的电离是吸热过程,升高温度,K 增大。
w
(3)适用范围:K 不仅适用于纯水,也适用于稀的电解质水溶液。在任何水溶液中均存在 H+和OH-,
w
只要温度不变,K 不变。
w
3.影响水电离平衡的因素
(1)升高温度,水的电离程度增大,K 增大。
w
(2)加入酸或碱,水的电离程度减小,K 不变。
w
(3)加入可水解的盐(如FeCl 、NaCO),水的电离程度增大,K 不变。
3 2 3 w
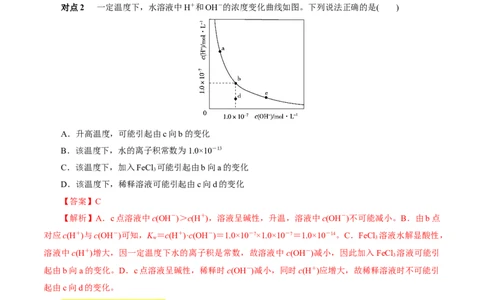
外界条件对水电离平衡的具体影响
条件 体系变化 平衡移动方向 K 水的电离程度 c(OH-) c(H+)
w
HCl 逆 不变 减小 减小 增大
NaOH 逆 不变 减小 增大 减小
NaCO 正 不变 增大 增大 减小
可水解 2 3
的盐
NH Cl 正 不变 增大 减小 增大
4
升温 正 增大 增大 增大 增大
温度
降温 逆 减小 减小 减小 减小
其他:如加入Na 正 不变 增大 增大 减小
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)温度一定时,水的电离常数与水的离子积常数相等( )
(2)100 ℃的纯水中c(H+)=1×10-6 mol·L-1,此时水呈酸性( )
(3)在蒸馏水中滴加浓HSO ,K 不变( )
2 4 w
(4)NaCl溶液和CHCOONH 溶液均显中性,两溶液中水的电离程度相同( )
3 4
(5)室温下,0.1 mol·L-1的HCl溶液与0.1 mol·L-1的NaOH溶液中水的电离程度相等( )
(6)任何水溶液中均存在H+和OH-,且水电离出的c(H+)和c(OH-)相等( )
(7)25 ℃时,0.1 mol·L-1的NaOH溶液中K =1×10-13 mol2·L-2 ( )
W
(8)某温度下,纯水中的c(H+)=2×10-7mol·L-1,则c(OH-)=( )
(9)25 ℃时,0.01 mol·L-1的盐酸中,c(OH-)=1.0×10-12mol·L-1 ( )
答案:(1)× (2)× (3)× (4)× (5)√ (6)√ (7)× (8)× (9)√
例1 25°C时,水的电离达到平衡:HO H++OH-,下列叙述不正确的是( )
2A.将纯水加热到95℃时,K 变大,pH减小,水仍呈中性
w
B.向纯水中加入稀氨水,平衡逆向移动,c(OH-)增大,K 不变
w
C.向水中加入少量固体硫酸氢钠,c(H+)增大,平衡逆向移动,K 不变
W
D.向水中通入HCl气体,平衡逆向移动,溶液导电能力减弱
【答案】D
【解析】A项,水加热到95℃,水的离子积常数变大,氢离子浓度增大,pH减小,但c(H+)=c(OH-),
因此仍呈中性,A不符合题意;B项,向纯水中加入稀氨水,水的电离平衡逆向移动,溶液中c(OH-)增大,
但由于温度不变,所以水的离子积常数K 不变,B不符合题意;C项,水中加入硫酸氢钠,硫酸氢钠电离
w
产生H+,使溶液中c(H+)增大,水的电离平衡逆向移动,但水温度不变,因此水的离子积常数K 不变,C
w
不符合题意;D项,水中通入氯化氢,HCl电离产生H+,使溶液中c(H+)增大,水的电离平衡逆向移动,由
于溶液中自由移动的离子浓度增大,因此溶液的导电性增强,D符合题意;故选D。
例2 常温下,向20.00 mL 0.1 mol·L-1 HA溶液中滴入0.1 mol·L-1 NaOH溶液,溶液中由水电离出
的氢离子浓度的负对数[-lg c(H+) ]与所加NaOH溶液体积的关系如图所示,下列说法中不正确的是( )
水
A.常温下,K(HA)约为10-5 B.M、P两点溶液对应的pH=7
a
C.b=20.00 D.M点后溶液中均存在c(Na+)>c(A-)
【答案】B
【解析】0.1 mol·L-1 HA溶液中,-lg c(H+) =11,c(H+) =c(OH-) =10-11 mol·L-1,根据常温下
水 水 水
水的离子积求出溶液中c(H+)=10-3 mol·L-1,HAH++A-,c(H+)=c(A-)=10-3 mol·L-1,K(HA)=
a
mol·L-1=10-5 mol·L-1,A项正确;N点水电离出的H+浓度最大,说明HA与NaOH恰好完全反应生成
NaA,P点溶质为NaOH和NaA,溶液显碱性,即P点pH不等于7,B项错误;0~b段水的电离程度逐渐
增大,当达到 b点时水的电离程度达到最大,即溶质为 NaA,说明 HA和NaOH恰好完全反应,b=
20.00,C项正确;M点溶液pH=7,根据溶液呈电中性,存在c(Na+)=c(A-),M点后,c(Na+)>c(A-),
D项正确。
对点1 已知NaHSO 在水中的电离方程式为NaHSO===Na++H++SO。某温度下,向c(H+)=1×10
4 4
-6 mol·L-1的蒸馏水中加入NaHSO 晶体,保持温度不变,测得溶液的c(H+)=1×10-2 mol·L-1。下列对该溶
4
液的叙述不正确的是( )A.该温度高于25 ℃
B.由水电离出来的H+的浓度为1×10-10 mol·L-1
C.加入NaHSO 晶体抑制水的电离
4
D.取该溶液加水稀释100倍,溶液中的c(OH-)减小
【答案】D
【解析】A项,K =1×10-6×1×10-6 mol2·L-2=1×10-12 mol2·L-2,温度高于25 ℃;B、C项,NaHSO
w 4
电离出的H+抑制HO电离,c(H+) =c(OH-)=1×10-10 mol·L-1;D项,加HO稀释,c(H+)减小,而
2 水 2
c(OH-)增大。
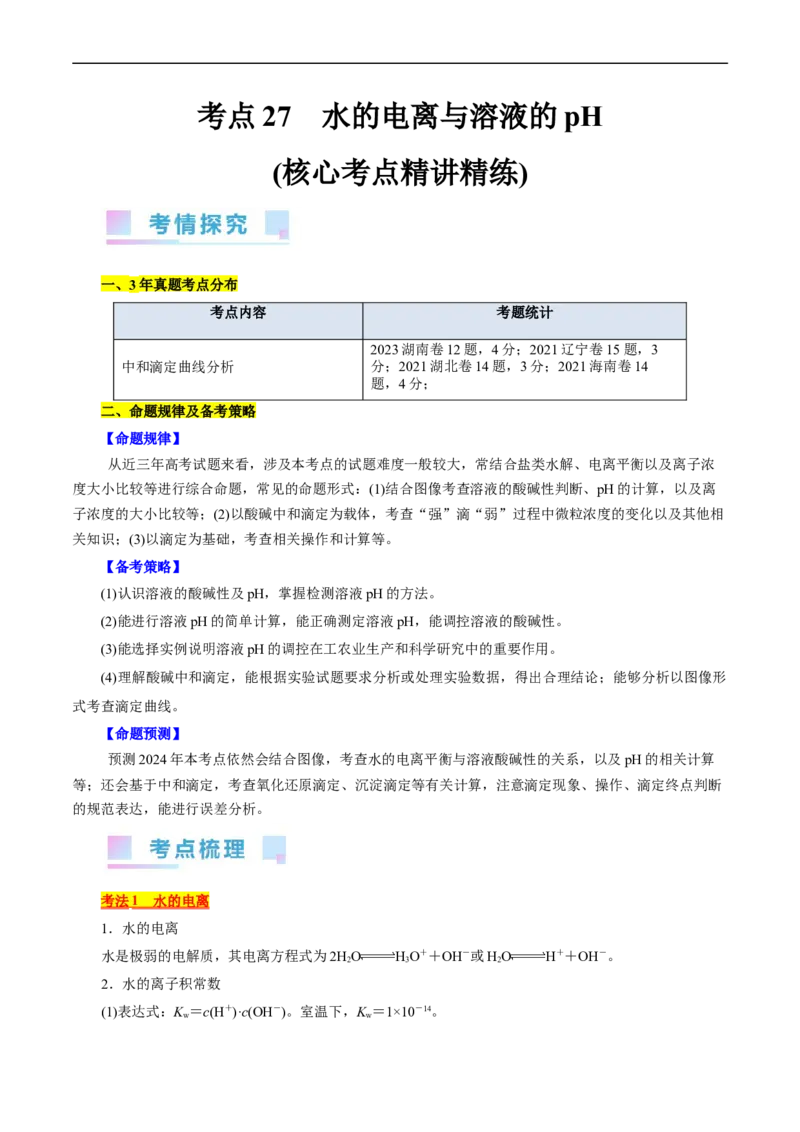
对点2 一定温度下,水溶液中H+和OH-的浓度变化曲线如图。下列说法正确的是( )
A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10-13
C.该温度下,加入FeCl 可能引起由b向a的变化
3
D.该温度下,稀释溶液可能引起由c向d的变化
【答案】C
【解析】A.c点溶液中c(OH-)>c(H+),溶液呈碱性,升温,溶液中c(OH-)不可能减小。B.由b点
对应c(H+)与c(OH-)可知,K =c(H+)·c(OH-)=1.0×10-7×1.0×10-7=1.0×10-14。C.FeCl 溶液水解显酸性,
w 3
溶液中c(H+)增大,因一定温度下水的离子积是常数,故溶液中 c(OH-)减小,因此加入FeCl 溶液可能引
3
起由b向a的变化。D.c点溶液呈碱性,稀释时c(OH-)减小,同时c(H+)应增大,故稀释溶液时不可能引
起由c向d的变化。
考法 2 溶液的酸碱性和 pH
1.溶液的酸碱性是由溶液中c(H+)与c(OH-)的相对大小决定的。请填写下表:
c(H+)与c(OH-) 相对大小 c(H+)的范围(25 ℃)
中性溶液 c(OH-)=c(H+) c(H+)=1.0×10-7 mol·L-1
酸性溶液 c(OH-)1.0×10-7 mol·L-1
碱性溶液 c(OH-)>c(H+) c(H+)<1.0×10-7 mol·L-1
2.溶液的pH
(1)定义:pH是c(H+)的负对数,其表达式是pH=-lgc(H+)。(2)pH大小能反映出溶液中c(H+)的大小,即能表示溶液的酸碱性强弱。
在25 ℃时,pH>7,表示溶液呈碱性,pH越大,溶液的碱性越强,pH每增加1个单位,
c(OH-)增大到原来的10倍;pH=7,溶液呈中性;pH<7,表示溶液呈酸性,pH越小,溶液酸性越强,
pH每减小1个单位,溶液中c(H+)增大到原来的10倍。
(3)pH的取值范围为0~14,即只适用于c(H+)≤1 mol·L-1或c(OH-)≤1 mol·L-1的电解质溶液,当c(H+)
或c(OH-)>1 mol·L-1时,直接用c(H+)或c(OH-)表示溶液的酸碱性。
3.溶液酸碱性的测定方法
(1)酸碱指示剂法(只能测定溶液的pH范围)。常见酸碱指示剂的变色范围:
指示剂 变色范围(颜色与pH的关系)
石蕊 红色←5.0紫色8.0→蓝色
酚酞 无色←8.2粉红色10.0→红色
甲基橙 红色←3.1橙色4.4→黄色
(2)利用pH试纸测定,使用的正确操作为取一小片pH试纸,放在洁净的表面皿上或玻璃片上,用干燥
洁净的玻璃棒蘸取试液点在试纸上,当试纸颜色变化稳定后迅速与标准比色卡对照,读出pH。
(3)利用pH计测定,仪器pH计可精确测定试液的pH(读至小数点后2位)。
1.溶液显酸碱性的实质是溶液中c(H+)与c(OH-)的相对大小。
2.用pH判断溶液酸碱性时,要注意条件,即温度。不能简单地认为pH等于7的溶液一定为中性,如
100℃时,pH=6为中性,pH<6才显酸性,pH>6显碱性,所以使用pH时需注明温度,若未注明温度,一
般认为是常温,就以pH=7为中性。
3.常温下,酸或碱溶液稀释过程的变化规律
溶液 稀释前溶液pH 稀释后溶液pH
强酸 pH=a+n
酸 pH=a 加水稀释到体积
弱酸 a