文档内容
考点 29 沉淀溶解平衡
(核心考点精讲精练)
一、3年真题考点分布
考点内容 考题统计
沉淀溶解平衡的应用 2023浙江1月选考15题,3分;
2023辽宁卷15题,3分;2023全国甲卷13题,6分;2023全国
新课标卷13题,6分;2023山东卷15题,4分;2023北京卷14
离子曲线 题,3分;2022福建卷7题,4分;2022湖南卷10题,3分;
2022山东卷14题,4分;2022海南卷14题,4分;2021全国甲
卷12题,6分;2021全国乙卷13题,6分;
二、命题规律及备考策略
【命题规律】
从近三年高考试题来看,本考点考查的重点是溶度积常数的相关计算及应用,试题通常以图象形式直
观呈现微观浓度的变化,考查数形结合能力、信息整合能力和对溶解平衡的理解应用能力。
【备考策略】
(1)用化学平衡的观点来研究的沉淀溶解平衡,运用平衡模型解释化学现象,揭示现象本质和规律。
(2)关注溶度积的计算和应用,善于数值之间的相互转化和公式的变式;
(3)能够运用平衡移动的观点对沉淀的溶解、生成和转化进行分析,并能解释一些生活问题,提高化学
核心素养。
(4)掌握沉淀溶解平衡曲线的分析技巧,能从图像或者文字的形式沉淀溶解平衡情境问题,获取有效
信息,提高证据推理能力。。
【命题预测】
预测2024年备考仍以K 的相关计算及应用为重点,试题可能会盐类水解、溶液中微粒浓度关系相融
sp
合,以选择题、图象题的形式呈现,在工艺流程题中出现概率很大。
考法 1 沉淀溶解平衡
1.难溶、可溶、易溶界定:
20 ℃时,电解质在水中的溶解度与溶解性存在如下关系:2.沉淀溶解平衡
(1)溶解平衡的建立
溶质溶解的过程是一个可逆过程:
固体溶质 溶液中的溶质
(2)特点(同其他化学平衡):逆、等、定、动、变(适用平衡移动原理)
3.影响沉淀溶解平衡的因素
(1)内因
难溶电解质本身的性质,这是决定因素。
(2)外因
①浓度:加水稀释,平衡向沉淀溶解的方向移动;
②温度:绝大多数难溶盐的溶解是吸热过程,升高温度,平衡向沉淀溶解的方向移动;
③同离子效应:向平衡体系中加入难溶物溶解产生的离子,平衡向生成沉淀的方向移动;
④其他:向平衡体系中加入可与体系中某些离子反应生成更难溶或更难电离或气体的离子时,平衡向
沉淀溶解的方向移动。
外界条件对溶解平衡的影响
(1)温度升高,多数溶解平衡向溶解的方向移动。
(2)加水稀释,浓度减小,溶解平衡向溶解方向移动,但平衡后因仍存在溶解平衡,故离子浓度保持不
变。
(3)加入与难溶电解质构成微粒相同的物质,溶解平衡向生成沉淀的方向移动。
(4)加入与难溶电解质溶解所得的离子反应的物质,溶解平衡向溶解的方向移动。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)电解质在水中存在沉淀溶解平衡,是一种动态平衡( )
(2)AgCl沉淀的生成和溶解不断进行,但速率相等( )
(3)AgCl难溶于水,溶液中没有Ag+和Cl-( )
(4)升高温度,AgCl的溶解度不变( )
(5)向AgCl沉淀的溶解平衡体系中加入NaCl固体,AgCl的溶解度不变( )
(6)只有易溶电解质在溶液中才存在溶解平衡( )
(7)难溶电解质在溶液中只存在溶解平衡,不存在电离平衡( )
(8)溶解平衡只能通过电解质溶解于水时建立( )(9)升高温度,沉淀溶解平衡一定正向移动( )
(10)室温下,AgCl在水中的溶解度小于在食盐水中的溶解度( )
(11)难溶电解质达到沉淀溶解平衡时,增加难溶电解质的量,平衡向溶解方向移动( )
(12)向NaSO 溶液中加入过量的BaCl 溶液,则SO沉淀完全,溶液中只含Ba2+、Na+和Cl-,不含SO(
2 4 2
)
(13)饱和NaCO 溶液与CaSO 固体反应:CO+CaSO CaCO +SO( )
2 3 4 4 3
答案:(1)√ (2)√ (3)× (4)× (5)× (6)× (7)× (8)× (9)× (10)× (11)× (12)×
例1 某种盐MCrO(s)一定温度下在水中的溶解度为0.032g/L。比较该盐在0.05mol/L的MNO 溶液
2 4 3
中的溶解度与相同温度下在水中的溶解度,下列叙述正确的是( )
A.在MNO 溶液中溶解度更高,因为MNO 的摩尔质量比MCrO 的小
3 3 2 4
B.在MNO 溶液中溶解度更低,因为溶液中已经含有M
3
C.溶解度相同,因为M+的物质的量浓度都是CrO2-的二倍
4
D.溶解度相同,因为K 只受温度影响
sp
【答案】B
【解析】A项,在MNO 溶液中含M+、M+浓度增大使沉淀溶解平衡MCrO(s) 2 M+ (aq) +
3 2 4
CrO2- (aq)左移,因此溶解度比纯水中更低,A错误;B项,结合选项A可知在MNO 溶液中溶解度更低,
4 3
B正确;C项,MCrO(s)溶解度随溶液中M+、CrO2-的浓度变化,只有在纯水中M+的物质的量浓度是
2 4 4
CrO2-的二倍,C错误;D项,虽然 K (M CrO)= c2 (M+) c(CrO 2-)只受温度影响,但MCrO(s)溶解度随溶
4 sp 2 4 4 2 4
液中M+、CrO2-的浓度变化, D错误;故选B。
4
例2 把足量熟石灰加入蒸馏水中,一段时间后达到平衡:Ca(OH) (s) Ca2+(aq)+2OH-(aq)。下
2
列叙述正确的是( )。
A.给溶液加热,溶液的pH升高
B.恒温下向溶液中加入CaO,溶液的pH升高
C.向溶液中加入NaCO 溶液,Ca(OH) 固体增多
2 3 2
D.向溶液中加入少量的NaOH固体,Ca(OH) 固体增多
2
【答案】D
【解析】A 项,加热时 Ca(OH) 的溶解度减小,平衡逆向移动,c(OH-)减小,pH 减小;B 项,
2
CaO+H O=Ca(OH) ,由于保持恒温,Ca(OH) 的溶解度不变,c(OH-)不变,因此 pH不变;C项,CO2-
2 2 2 3
+Ca2+=CaCO ↓,平衡正向移动,Ca(OH) 固体减少;D项,加入NaOH固体,c(OH-)增大,平衡逆向移动,
3 2
因此Ca(OH) 固体增多。
2对点1 饱和BaCO 溶液中存在平衡:BaCO (s) Ba2+(aq)+CO2-(aq)。当碳酸钡固体在水中达
3 3 3
到溶解平衡后,为使溶液中Ba2+的物质的量浓度增大,下列操作不可行的是( )
A.加入少量0.1 mol·L-1盐酸 B.加入少量硝酸钡固体
C.加入少量0.1 mol·L-1硫酸 D.加入少量氢氧化钡固体
【答案】C
【解析】A项,加入少量0.1 mol·L-1盐酸,氢离子会与CO2-发生反应,使平衡右移,Ba2+的物质的
3
量浓度增大,故A可行;B项,加入少量硝酸钡固体,硝酸钡溶于水使Ba2+浓度增大,虽然平衡会左移,
但根据化学平衡移动原理可知Ba2+的物质的量浓度依然增大,故B可行;C项,加入少量0.1 mol·L-1硫酸,
硫酸会电离出氢离子和硫酸根,虽然氢离子会与CO2-发生反应,但BaSO 的溶解度比BaCO 更小,所以
3 4 3
溶液中Ba2+的物质的量浓度会减小,故C不可行;D项,加入少量氢氧化钡固体,氢氧化钡溶于水使Ba2+
浓度增大,虽然平衡会左移,但根据化学平衡移动原理可知Ba2+的物质的量浓度依然增大,故D可行;故
选C。
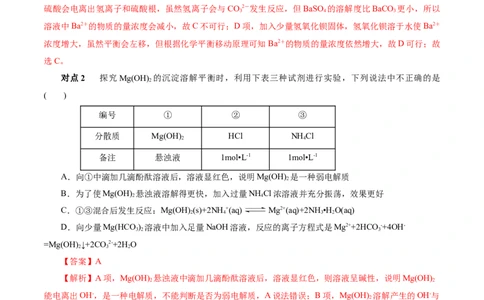
对点2 探究Mg(OH) 的沉淀溶解平衡时,利用下表三种试剂进行实验,下列说法中不正确的是
2
( )
编号 ① ② ③
分散质 Mg(OH) HCl NH Cl
2 4
备注 悬浊液 1mol•L-1 1mol•L-1
A.向①中滴加几滴酚酞溶液后,溶液显红色,说明Mg(OH) 是一种弱电解质
2
B.为了使Mg(OH) 悬浊液溶解得更快,加入过量NH Cl浓溶液并充分振荡,效果更好
2 4
C.①③混合后发生反应:Mg(OH) (s)+2NH +(aq) Mg2+(aq)+2NH•H O(aq)
2 4 3 2
D.向少量Mg(HCO ) 溶液中加入足量NaOH溶液,反应的离子方程式是Mg2++2HCO-+4OH-
3 2 3
=Mg(OH) ↓+2CO 2-+2H O
2 3 2
【答案】A
【解析】A项,Mg(OH) 悬浊液中滴加几滴酚酞溶液后,溶液显红色,则溶液呈碱性,说明Mg(OH)
2 2
能电离出OH-,是一种电解质,不能判断是否为弱电解质,A说法错误;B项,Mg(OH) 溶解产生的OH-与
2
NH Cl溶液中的NH +生成NH •H O,能加快Mg(OH) 悬浊液的溶解,B说法正确;C项,①③混合后,
4 4 3 2 2
OH-与NH +发生反应生成NH •H O,其方程式为Mg(OH) (s)+2NH +(aq) Mg2+(aq)+2NH•H O(aq),C
4 3 2 2 4 3 2
说法正确;D项,因相同温度下,氢氧化镁比碳酸镁更难溶,碱过量时生成Mg(OH) ,D说法正确;故选
2
A。
考法 2 沉淀溶解平衡的应用
1.沉淀的生成
(1)调节pH法
如:除去 NH Cl 溶液中的 FeCl 杂质,可加入氨水调节 pH 至 7~8,离子方程式为 Fe3++
4 33NH ·H O===Fe(OH) ↓+3NH。
3 2 3
(2)沉淀剂法
如:用HS沉淀Cu2+,离子方程式为HS+Cu2+===CuS↓+2H+。
2 2
2.沉淀的溶解
(1)酸溶解法
如:CaCO 溶于盐酸,离子方程式为CaCO +2H+===Ca2++HO+CO↑。
3 3 2 2
(2)盐溶液溶解法
如:Mg(OH) 溶于NH Cl溶液,离子方程式为Mg(OH) +2NH===Mg2++2NH ·H O。
2 4 2 3 2
(3)氧化还原溶解法
如:不溶于盐酸的硫化物Ag S溶于稀HNO。
2 3
(4)配位溶解法
如:AgCl溶于氨水,离子方程式为AgCl+2NH ·H O===[Ag(NH )]++Cl-+2HO。
3 2 3 2 2
3.沉淀的转化
(1)实质:沉淀溶解平衡的移动(沉淀的溶解度差别越大,越容易转化)。
如:AgNO 溶液――→AgCl(白色沉淀)――→AgBr(浅黄色沉淀)――→AgI(黄色沉淀)――→Ag S(黑色
3 2
沉淀)。
(2)应用
a.锅炉除垢:将CaSO 转化为易溶于酸的CaCO ,离子方程式为 CaSO(s)+CO(aq)CaCO (s)+
4 3 4 3
SO(aq)。
b.矿物转化:
CuSO 溶液遇PbS转化为CuS,离子方程式为Cu2+(aq)+PbS(s) CuS(s)+Pb2+(aq)。
4
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)难溶电解质在水溶液中达到沉淀溶解平衡时,沉淀和溶解即停止( )
(2)相同温度下,AgCl在水中的溶解能力与在NaCl溶液中的相同( )
(3)在一定条件下,溶解度较小的沉淀也可以转化成溶解度较大的沉淀( )(4)为减少洗涤过程中固体的损耗,最好选用稀HSO 代替HO来洗涤BaSO 沉淀(√)
2 4 2 4
(5)洗涤沉淀时,洗涤次数越多越好( )
(6)用稀盐酸洗涤AgCl沉淀比用水洗涤损耗的AgCl少( )
(7)AgCl难溶于水,所以将AgCl加入水中所得溶液中不含Ag+、Cl-( )
(8)饱和石灰水中加入一定量生石灰,温度明显升高,所得溶液的pH会增大( )
(9)硬水含有较多Ca2+、Mg2+、HCO -、SO 2-加热煮沸可以完全除去其中的Ca2+、Mg2+( )
3 4
(10)钡中毒患者可尽快使用苏打溶液洗胃,随即导泻使Ba2+转化为BaCO 而排出( )
3
(11)向AgCl沉淀中加入KI溶液,由白色沉淀转变成黄色沉淀,是由于K (AgI)K ,溶液过饱和,有沉淀析出;
c sp
Q=K ,溶液饱和,沉淀与溶解处于平衡状态;
c sp
Q