文档内容
考点 29 沉淀溶解平衡
【基础过关】
1.把Ca(OH) 放入蒸馏水中,一段时间后达到平衡:Ca(OH) (s) Ca2+(aq)+2OH-(aq)。下列说
2 2
法正确的是( )
A.恒温下向溶液中加入CaO,溶液的pH升高
B.给溶液加热,溶液的pH升高
C.向溶液中加入NaCO 溶液,其中固体质量增加
2 3
D.向溶液中加入少量NaOH固体,Ca(OH) 固体质量不变
2
【答案】C
【解析】恒温下K 不变,加入CaO后,溶液仍为Ca(OH) 的饱和溶液,pH不变,A项错误;加热,
sp 2
Ca(OH) 的溶解度减小,溶液的pH降低,B项错误;加入NaCO 溶液,沉淀溶解平衡向右移动,Ca(OH)
2 2 3 2
固体转化为CaCO 固体,固体质量增加,C项正确;加入NaOH固体,溶液温度升高,Ca(OH) 溶解度减
3 2
小,且溶液中c(OH-)增大,平衡向左移动,Ca(OH) 固体质量增加,D项错误。
2
2.向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成。经查资料得知:
Ag++ 2NH ·H O Ag(NH)+ 2H O。下列分析不正确的是( )
3 2 3 2 2
A.浊液中存在沉淀溶解平衡:AgCl (s) Ag+(aq)+Cl-(aq)
B.实验可以证明NH 结合Ag+能力比Cl-强
3
C.实验表明实验室可用氨水洗涤银镜反应后的试管
D.由资料信息可推知:加浓硝酸后生成的沉淀为AgCl
【答案】C
【解析】A项,因为是浊液,所以存在沉淀溶解平衡,A正确;B项,Ag+与氨气分子结合生成二氨合
银离子,导致银离子浓度减小,促使AgCl (s) Ag+(aq)+Cl-(aq)正向移动,说明NH 结合Ag+能力比Cl-
3
强,B正确;C项,银镜反应后的试管壁上是银单质,银离子能够与氨水反应,银单质不能,C错误;D
项,浓硝酸能够中和一水合氨,使反应Ag++2NH•H O Ag(NH)++2H O逆向移动,二氨合银离子生成银
3 2 3 2 2
离子,与溶液中的氯离子结合生成沉淀,所以加浓硝酸后⇌生成的沉淀为AgCl,D正确;故选C。
3.往锅炉注入NaCO 溶液浸泡,将水垢中的CaSO 转化为CaCO ,再用盐酸去除,下列叙述中正确
2 3 4 3
的是( )
A.温度升高,NaCO 溶液的K 和c(H+)均会增大
2 3 w
B.CaSO 能转化为CaCO ,说明K (CaCO)>K (CaSO)
4 3 sp 3 sp 4
C.CaCO 溶解于盐酸而CaSO 不溶,是因为硫酸酸性强于盐酸
3 4
D.沉淀转化的离子方程式为CO(aq)+CaSO(s) CaCO (s)+SO(aq)
4 3
【答案】D
【解析】温度升高,水的电离平衡正向移动,K 增大;温度升高,NaCO 的水解平衡正向移动,[OH
w 2 3
资料整理【淘宝店铺:向阳百分百】-]增大,[H+]减小,A项错误;K (CaCO)<K (CaSO),B项错误;CaCO 与盐酸反应生成可溶性的氯化
sp 3 sp 4 3
钙、水和二氧化碳,CaSO 与盐酸不满足复分解反应发生的条件,与酸性强、弱无关,C项错误;硫酸钙
4
较为致密,可转化为较为疏松且溶解度更小的碳酸钙,反应的离子方程式为 CaSO(s)+CO(aq)
4
CaCO (s)+SO(aq),D项正确。
3
4.工业上用化学法除锅炉的水垢时,先向锅炉中注入饱和NaCO 溶液浸泡,将水垢中的CaSO 转化
2 3 4
为CaCO ,再用盐酸除去[已知:K (CaCO)=1×10-10,K (CaSO)=9×10-6]。下列说法不正确的是( )
3 sp 3 sp 4
A.温度升高,NaCO 溶液的K 和c(OH-)均会增大
2 3 w
B.沉淀转化的离子方程式为CO(aq)+CaSO(s) CaCO (s)+SO(aq)
4 3
C.该条件下,CaCO 的溶解度小于CaSO
3 4
D.CaCO 和CaSO 共存的悬浊液中,c(SO 2-)/c(CO 2-)=1 105
3 4 4 3
【答案】D
【解析】A项,水电离、盐水解都吸热,温度升高,NaCO 溶液的K 和c(OH-)均会增大,故A正确;
2 3 w
B项,加入碳酸钠溶液,把硫酸钙转化为碳酸钙:CO+CaSO CaCO +SO 2-,故B正确;C项,该
4 3 4
条件下,设溶液为1L,由c(CO2-)=c(Ca2+)= =10-5 mol·L-1,则 =
3
=1 10-4g,CaCO 的溶解度约为1×10-4,显然,CaCO 的溶解度小于CaSO,故C正确;D项,CaCO 和
3 3 4 3
CaSO 共存的悬浊液中, =9 104,故D错误;故选D。
4
5.(2023·江苏省高三第二次大联考)室温下,通过下列实验探究有关AgNO 的性质[已知:
3
]。
实验1:向 0.1mol·L-1的AgNO 溶液中滴加 0.1mol·L-1的NaCl溶液,产生白色沉淀,过滤,
3
实验2:向实验1所得滤液中滴加 0.1mol·L-1 溶液,产生淡黄色沉淀,过滤。
实验3:向实验2所得滤液中逐滴滴加氨水,产生沉淀先变多后变少,直至消失。
下列说法正确的是( )
A.实验1过滤后滤液中c(Ag+)=10-4.9mol·L-1
B.通过实验1和实验2可得出
资料整理【淘宝店铺:向阳百分百】C.实验2所得滤液中c(Ag+)+c(H+)=c(Cl-)+c(Br-)+ c(OH-)
D.实验3滴加氨水过程中,c(Ag+)一直减小
【答案】D
【解析】A项, 向10mL0.1mol/L的AgNO 溶液中滴加1mL0.1mol/L的NaCl溶液,发生反应
3
AgNO+NaCl=AgCl↓+NaNO ,反应后AgNO 过量,过滤后所得滤液中c(Ag+)=
3 3 3
=0.082mol/L,A项错误;B项,实验1所得滤液中含过量的AgNO、
3
NaNO 和饱和AgCl,滴加1mL0.1mol/LNaBr溶液,AgNO 直接与NaBr发生沉淀反应生成淡黄色的AgBr
3 3
沉淀,不能说明发生了沉淀的转化,不能比较AgCl、AgBr的K ,B项错误;C项,实验2中发生的反应
sp
为AgNO+NaBr=AgBr↓+NaNO ,反应后AgNO 仍然过量,过滤所得滤液中含过量的AgNO、NaNO 、饱
3 3 3 3 3
和AgCl和AgBr,滤液中NO -物质的量为0.1mol/L×0.01L=0.001mol、Na+物质的量为0.1mol/
3
L×0.001L+0.1mol/L×0.001L=0.0002mol,溶液中的电荷守恒为c(Ag+)+c(H+)+c(Na+)=c(Cl-)+c(Br-)+c(NO -)
3
+c(OH-),C项错误;D项,向实验2所得滤液中逐滴滴加氨水,随着氨水的滴入,依次发生反应:
AgNO+NH∙HO=AgOH↓+NH NO 、AgOH+2NH∙HO=[Ag(NH)]OH+2H O,故产生沉淀先变多后变少,
3 3 2 4 3 3 2 3 2 2
直至消失,c(Ag+)一直减小,D项正确;故选D。
6.(2023·浙江省临海、新昌两地高三适应性考试5月模考)印尼苏拉威西岛特产的椰子蟹具有异常坚
硬的甲壳,这归功于摄入的椰子中的月桂酸(C H COOH),在表面的角质层中形成难溶的月桂酸磷酸钙,
11 23
存在如下平衡:Ca PO (OOCC H )(s) 3Ca2+(aq)+PO (aq)+3C H COO-(aq) K =7.3×10-35,已知
3 4 11 23 3 11 23 sp
CaCO 的K =2.8×10-9。下列说法不正确的是( )
3 sp
A.椰子蟹摄入月桂酸含量较高的椰肉有助于形成更加坚硬的甲壳
B.弱碱性的海水可以保护椰子蟹外壳,使其不易被腐蚀
C.将少量月桂酸磷酸钙投入适量1mol•L-1碳酸钠溶液中,可实现其与碳酸钙的转化
D.海水中CO 浓度升高,会腐蚀椰子蟹的外壳,使K 增大
2 sp
【答案】D
【解析】A项,由题干可知,月桂酸利于促进形成难溶的月桂酸磷酸钙,故椰子蟹摄入月桂酸含量较
高的椰肉有助于形成更加坚硬的甲壳,A正确;B项,弱碱性的海水利于月桂酸形成月桂酸根离子,使得
Ca PO (OOCC H )(s) 3Ca2+(aq)+PO3-(aq)+3C H COO-(aq)平衡逆向移动,利于保护椰子蟹外壳,
3 4 11 23 3 4 11 23
使其不易被腐蚀,B正确;C项,将少量月桂酸磷酸钙投入适量1mol•L-1碳酸钠溶液中,较高浓度的碳酸
根离子使得Ca PO (OOCC H )(s)转化为CaCO (s),实现其与碳酸钙的转化,C正确;D项,海水中CO
3 4 11 23 3 3 2
浓度升高,溶液酸性增强,使得月桂酸根离子转化为月桂酸,促使Ca PO (OOCC H )(s) 3Ca2+(aq)
3 4 11 23 3
资料整理【淘宝店铺:向阳百分百】+PO3-(aq)+3C H COO-(aq)平衡正向移动,导致腐蚀椰子蟹的外壳,但不会使K 增大,D错误;故选
4 11 23 sp
D。
7.(2023·浙江省杭州地区(含周边)重点中学高三联考化)可溶性钡盐有毒,医院中常用硫酸钡这种钡盐
作为内服造影剂。已知:K (BaCO)=5.0×10-9;K (BaSO)=1.0×10-10。下列推断正确的是( )
sp 3 sp 4
A.饱和BaCO 溶液中存在:c(Ba2+)=c(HCO -)+c(CO2-)
3 3 3
B.向BaCO 、BaSO 的饱和混合溶液中加入少量BaCl ,溶液中 减小
3 4 2
C.不用碳酸钡作为内服造影剂,是因为K (BaCO)>K (BaSO)
sp 3 sp 4
D.若每次加入1 L2mol·L-1的NaCO 溶液,至少需要6次可将0.2mol BaSO 转化为BaCO
2 3 4 3
【答案】D
【解析】A项,BaCO 是难溶性盐,饱和BaCO 溶液中存在:BaCO (s) Ba2+ (aq)+ CO 2- (aq),
3 3 3 3
根据物料守恒:c(Ba2+)=c(HCO -)+c(CO2-)+c(H CO),故A错误;B项,BaCO 、BaSO 的饱和混合溶液中
3 3 2 3 3 4
存在平衡:BaCO (s)+SO 2-(aq) BaSO (s)+ CO 2- (aq),溶液中 ,少量
3 4 4 3
BaCl ,度不变,K (BaCO)和K (BaSO)不变, 不变,故B错误;C项,胃液中含有盐酸,不用
2 sp 3 sp 4
碳酸钡作为内服造影剂的原因是:碳酸钡能和盐酸反应而溶解,和溶度积常数无关,故C错误;D项,向
BaSO 中加入NaCO 溶液,发生反应BaSO (s)+CO 2-(aq) BaCO (s)+ SO 2- (aq),该反应的平衡常
4 2 3 4 3 3 4
数K= ,若每次加入1 L2mol·L-1的NaCO 溶液,能处理BaSO 物质的
2 3 4
量xmol,则K= ,x= , ,所以至少6次可以将0.2mol BaSO 转化为
4
BaCO ,故D正确;故选D。
3
8.已知:①AgCl为难溶于水和酸的白色固体,Ag S为难溶于水和酸的黑色固体。
2
②室温下,K (AgCl)=2.0×10-10,K (Ag S)=2.0×10-48。
sp sp 2
向AgCl的悬浊液中加入一定量的NaS溶液并振荡,白色固体向黑色固体转化。下列说法正确的是(
2
)
A.NaS溶液中存在:c(OH-)=c(H+)+c(HS-)+2c(S2-)
2
B.向AgCl悬浊液加入足量氨水,溶液变澄清。反应的离子方程式为:AgCl+4NH•H O=[Ag(NH)]+
3 2 3 4
资料整理【淘宝店铺:向阳百分百】+Cl-+4H O
2
C.反应2AgCl+S2- Ag S+2Cl-正向进行,需满足 <2×1028
2
D.将转化后的体系静置,上层清液中离子存在关系:c(Ag+)= 且c(Ag+)>
【答案】C
【解析】A项,NaS溶液中存在质子守恒:c(OH-)=c(H+)+c(HS-)+2c(H S),A错误;
2 2
B项,向AgCl悬浊液加入足量氨水,溶液变澄清,得到银氨溶液,离子方程式为
AgCl+2NH•H O=[Ag(NH)]++Cl-+2H O,B错误;C项,反应2AgCl+S2- Ag S+2Cl-的平衡常数K=
3 2 3 2 2 2
= = = =2×1028,当浓度商Q= <K时,反应正向移动,C
正确;D项,根据题意沉淀发生转化,即体系中不会生成AgCl沉淀,所以c(Ag+)< ,D错误;
故选C。
9.已知:25℃时,K [Ni(OH) ]=2.0×10-15,K [Fe(OH) ]=4.0×10-38。将含Fe O 、Ag、Ni的某型废催化
sp 2 sp 3 2 3
剂溶于盐酸,过滤,滤渣为Ag,所得溶液中c(Ni2+)=c(Fe3+)=0.4mol/L。向该溶液中滴加一定浓度的NaOH
溶液(假设溶液体积不变)。下列说法中正确的是( )
A.金属活动性:Ag>Ni
B.加入NaOH溶液时,先产生Ni(OH) 沉淀
2
c
Ni2+
C.当滴定到溶液pH=5时,溶液中lg
c
Fe3+ 约为10
D.当滴定到溶液呈中性时,Ni2+已沉淀完全
【答案】C
【解析】A项,Ag不能与盐酸反应,而Ni能与盐酸反应,因此金属活动性:Ni>Ag,故A错误;B
项 , c(Ni2+)=0.4mol/L 时 , Ni2+ 刚 好 开 始 沉 淀 时 溶 液 中
K [Ni(OH) ] 21015
c OH- sp 2 mol/L= 0.510-7mol/L
c(Ni2+) 0.4 ,c(Fe3+)=0.4mol/L时,Fe3+刚好开始沉淀时溶液
资料整理【淘宝店铺:向阳百分百】c OH- 3
K
sp
[Fe(OH)
3
]
3
41038
mol/L=30.110-12mol/L< 0.510-7mol/L
中 c(Fe3) 0.4 ,故先产生 Fe(OH) 沉淀,故 B错
3
K 11014
c OH- W mol/L=110-9mol/L
误 ; C 项 , 溶 液 pH=5 时 c(H+)=10-5mol/L , 溶 液 中 c H 1105 ,
K [Fe(OH) ] 41038
c(Fe3+) sp 3 mol/L=41011mol/L
c3(OH) 11093 ,
K [Ni(OH) ] 21015
c(Ni2+) sp 2 mol/L=2103mol/L>0.4mol/L
c2(OH) 11092 ,则 Ni2+未沉淀,c(Ni2+)=0.4mol/L,则
c
Ni2+
0.4
lg lg 10
c Fe3+ 41011 ,故C正确;D项,当溶液呈中性时,c(OH-)=1×10-7mol/L,此时溶液中
K [Ni(OH) ] 21015
c(Ni2+) sp 2 mol/L=0.2mol/L
c2(OH) 11072 ,故Ni2+未沉淀完全,故D错误;故选C。
10.牙齿表面存在如下平衡:Ca (PO )OH(s) 5Ca 2+(aq)+3 PO 3-(aq) +OH-(aq) K =6.8×10-37,
5 4 3 4 sp
Ca (PO )F的K =2.8×10-61。下列说法错误的是( )
5 4 3 sp
A.在牙膏中添加适量的磷酸盐,能起到保护牙齿的作用
B.口腔中的食物残渣能产生有机酸,容易导致龋齿,使K 增大
sp
C.正常口腔的pH接近中性,有利于牙齿健康
D.使用含氟牙膏,当Ca (PO )OH(s)与Ca (PO )F(s)共存时,
5 4 3 5 4 3
【答案】B
【解析】A项,在牙膏中添加适量的磷酸盐,使平衡逆向移动,Ca (PO )OH(s) 5Ca 2+(aq)+3
5 4 3
PO 3-(aq) +OH-(aq),生成Ca (PO )OH(s)覆盖在牙齿表面,能起到保护牙齿的作用,A正确;B项,K 只与
4 5 4 3 sp
温度有关,与溶液的酸碱性无关,B错误;C项,正常口腔的pH接近中性,防止Ca (PO )OH(s)与
5 4 3
Ca (PO )F(s)溶解,有利于牙齿健康,C正确;D项,
5 4 3
资料整理【淘宝店铺:向阳百分百】,D正确; 故选B。
11.(2023·浙江省金、丽、衢十二校高三二模)草酸钙是常见的难溶物。将过量草酸钙粉末置于水中
达到溶解平衡:CaC O (s) Ca2+ (aq)+ C O2- (aq)[已知K (CaC O)=2.3×10-9,K(CHCOOH)=1.75×10-
2 4 2 4 sp 2 4 a 3
5,HC O 的电离常数K =5.6×10-2,K =1.5×10-4,下列有关说法不正确的是( )
2 2 4 a1 a2
A.上层清液中含碳微粒最主要以C O2-形式存在
2 4
B.上层清液中存在:c(Ca2+)=c(C O2-)+c(HC O-)+c(H C O)
2 4 2 4 2 2 4
C.HC O 加入CaCl 溶液时,加入适量醋酸钠粉末,有利于生成CaC O 沉淀
2 2 4 2 2 4
D.向上层清液中通入 至pH=1,则:2c(Ca2+)-2c(C O2-)-c(HC O-)- c(OH―)= 0.1mol·L-1
2 4 2 4
【答案】D
【解析】A项,溶解在水中的草酸钙电离出草酸根离子,草酸根离子能水解,但程度很小,故含碳的
微粒最主要的是草酸根离子,A正确;B项,根据物料守恒钙原子和碳原子物质的量浓度相等,故有
c(Ca2+)=c(C O2-)+c(HC O-)+c(H C O),B正确;C项,草酸加入氯化钙中反应生成草酸钙,加入醋酸钠粉
2 4 2 4 2 2 4
末,根据电离平衡常数分析,醋酸根离子水解程度大于草酸根离子,故醋酸钠的碱性抑制草酸根离子水解,
有利于生成草酸钙,C正确;D项,向上层清液中通入HCl至pH=1,则有电荷守恒:2c(Ca2+)+c(H
+)=2c(C O2-)+c(HC O-)+c(OH―)+c(Cl-),根据氢离子浓度为0.1mol/L分析,2c(Ca2+)-2c(C O2-)-c(HC O-)-
2 4 2 4 2 4 2 4
c(OH―)=c(Cl-)-c(H+),不能确定氯离子浓度,故D错误;故选D。
12.(2023·浙江省温州市高三第三次模拟适应性考试)H S是常见的二元弱酸(电离常数
2
K (H S)=1.1×10-7,K (H S)=1.3×10-13)。氢氧化铁[K = 2.8×10-39]、氢氧化锌[K = 3.0×10-17]均为难溶多元弱
a1 2 a2 2 sp sp
碱,硫化锌[K = 1.6×10-24]为难溶盐。所有数据均为25℃的值。下列有关说法不正确的是( )
sp
A.因为HS的K >>K ,所以c(S2-)≈K =1.3×10-13mol/L
2 a1 a2 a2
B.Fe(OH) 饱和溶液中的c(Fe3+)≈1×10-10mol/L
3
C.分别向等体积等浓度的(CHCOO) Zn、ZnSO 溶液中通入等物质的量的HS沉淀ZnS后,前者
3 2 4 2
c(Zn2+)更小
D.pH=13的NaS溶液与相同物质的量的ZnSO 反应,只沉淀ZnS
2 4
【答案】D
【解析】A项,HS在水溶液中的电离方程式为:HS H++HS-、HS H++S2-,K =
2 2 a1
,K = ,因为HS的K >>K ,可以任务c(H+)≈c(HS-),所以c(S2-)≈K =1.3×10-
a2 2 a1 a2 a2
13mol/L,故A正确;B项,Fe(OH) 溶于水所得饱和溶液中存在平衡:Fe(OH) Fe3++3OH-,设
3 3
c(Fe3+)=amol/L,则c(OH-)=3amol/L,K [Fe(OH) ]=c(Fe3+)c3(OH-)=a×(3a)3=2.8×10-39,解得a 1×10-10mol/L,
sp 3
资料整理【淘宝店铺:向阳百分百】故B正确;C项,(CHCOO) Zn是强碱弱酸盐,其水溶液呈碱性,抑制HS的电离,c(S2-)更大,沉淀
3 2 2
Zn2+更加彻底,c(Zn2+)更小,故C正确;D项,氢氧化锌的K = 3.0×10-17,则当0.1mol/L的ZnSO 溶液中
sp 4
Zn2+开始沉淀时,c(OH-)= ,pH=
,则pH=13的NaS溶液与相同物质的量的ZnSO 反应,除了
2 4
沉淀ZnS还会生成Zn(OH) ,故D错误;故选D。
2
13.(2023·浙江省义乌市高三高考适应性考试)在25℃时,下列几种难溶电解质的溶度积常数(K )如表
sp
所示,下列说法不正确的是( )
BaSO(白) BaCO (白) AgCl(白) Ag S(黑) Ag CrO(砖红)
4 3 2 2 4
1.1×10-10 2.6×10-9 1.8×10-10 6.3×10-50 2.0×10-7
A.重晶石的主要成分是BaSO 工业上常用饱和碳酸钠溶液反复浸泡重晶石,将难处理的BaSO 转化
4 4
为更易处理的BaCO
3
B.在食盐除杂实验中,利用BaCl 除去溶液中的SO 2-后,应先过滤,再加入NaCO 除去溶液中的
2 4 2 3
Ba2+和Ca2+,过滤的目的是防止BaSO 转化为BaCO
4 3
C.在含银工业废水的处理中,相同浓度的NaS溶液比NaCl溶液沉淀效果好,而且NaS溶液可以沉
2 2
淀多种重金属离子
D.将浓度均为0.2mol•L-1的NaCl溶液和NaCrO 溶液等体积混合后,滴加AgNO 溶液,先析出
2 4 3
Ag CrO 沉淀
2 4
【答案】D
【解析】A项,虽然BaSO 比BaCO 更难溶于水,但在CO2-浓度较大的溶液中,BaSO 溶解在水中的
4 3 3 4
Ba2+能与CO2-结合生成BaCO 沉淀。只要一直保持溶液中较大的CO2-浓度,Ba2+就会与CO2-结合不断生
3 3 3 3
成BaCO ,故A正确;B项,在食盐除杂实验中,利用BaCl 除去溶液中的SO 2-后,应先过滤,再加入
3 2 4
NaCO 除去溶液中的Ba2+和Ca2+。由A分析可知,在CO2-浓度较大的溶液中,BaSO 溶解在水中的Ba2+能
2 3 3 4
与CO2-结合生成BaCO 沉淀;过滤的目的是防止BaSO 转化为BaCO ,故B正确;C项,由表可知,Ag S
3 3 4 3 2
的溶解度小于AgCl;因此在含银工业废水的处理中,相同浓度的NaS溶液比NaCl溶液沉淀效果好,故C
2
正确;D项,将浓度均为0.2mol•L-1的NaCl溶液和NaCrO 溶液等体积混合后,刚开始生成Ag CrO 沉淀
2 4 2 4
需要的Ag+浓度为 ;刚开始生成AgCl沉淀需要的Ag+浓度为
资料整理【淘宝店铺:向阳百分百】;所以滴加AgNO 溶液,先析出AgCl沉淀,故D错误;故选D。
3
14.(2023·浙江省浙南名校联盟高三第二次联考)常温下,向20mL0.1mol/LNaHCO 溶液中再加入少量
3
的NaHCO 固体,一段时间后,少量气体X从溶液底部固体中缓慢逸出,最终固体全部溶解,得到溶液
3
Y,pH值为8.7。
已知:K (CaCO)=4.96×10-9 K (MgCO )=6.82×10-6,K [Mg(OH) ]=1.8×10-11
sp 3 sp 3 sp 2
HCO:pK =6.3、pK =10.3;Mg(OH) 沉淀范围:pH9.4~12.4。
2 3 a1 a2 2
下列说法正确的是( )
A.X气体是CO,饱和NaHCO 溶液的
2 3
B.因为K (MgCO )>K [Mg(OH) ],Mg(OH) 更难溶
sp 3 sp 2 2
C.向溶液Y中滴加MgCl 溶液,有Mg(OH) 生成
2 2
D.向0.1mol/L NaHCO 溶液中加入MgCl 溶液,无明显现象,但改为同浓度的CaCl 溶液,可生成沉
3 2 2
淀。
【答案】D
【解析】A项,在NaHCO 溶液中既存在水解平衡HCO -+H O HCO+OH-、又存在电离平衡HCO -
3 3 2 2 3 3
⇌ ⇌
H++ CO2-,HCO -的水解平衡常数K = = =10-7.7>10-10.3,NaHCO 溶液呈碱性,向其中加入少量
3 3 h 3
NaHCO 固体,上述平衡正向移动,生成的HCO 分解产生少量气体CO,即X气体是CO,同时有CO2-
3 2 3 2 2 3
生成,即溶液Y中含CO2-,由HCO 的K 、K 可知CO2-的水解能力大于HCO -,溶液Y的pH为8.7,
3 2 3 a1 a2 3 3
则饱和NaHCO 溶液的pH<8.7,A项错误;B项,MgCO 、Mg(OH) 不属于同类型的难溶电解质,不能直
3 3 2
接由K 的大小判断溶解度的大小,K (MgCO )=6.82×10-6,饱和MgCO 溶液的浓度c(MgCO )=
sp sp 3 3 3
= mol/L= ×10-3mol/L,K [Mg(OH) ]=1.8×10-11,饱和Mg(OH) 溶液的浓度
sp 2 2
c[Mg(OH) ]= = mol/L= ×10-4mol/L< ×10-3mol/L,Mg(OH) 更难溶,B
2 2
项错误;C项,Mg(OH) 沉淀的范围:pH9.4~12.4,即pH=9.4时Mg2+开始形成Mg(OH) 沉淀,Y溶液的
2 2
pH为8.7,故向溶液Y中滴加MgCl 溶液,没有Mg(OH) 生成,C项错误;D项,NaHCO 溶液中存在平
2 2 3
衡HCO - H++ CO2-,由于K (CaCO) <K (MgCO ),说明Ca2+结合CO2-的能力比Mg2+强,故
3 3 sp 3 sp 3 3
向0.1mol⇌/LNaHCO
3
溶液中加入MgCl
2
溶液,无明显现象,但改为同浓度的CaCl
2
溶液,可生成沉淀,D项
正确;故选D。
资料整理【淘宝店铺:向阳百分百】15.(2023·浙江省诸暨市高三适应性考试)氢氧化镁是常见难溶物,将过量氢氧化镁粉末置于水中达到
溶解平衡:Mg(OH) (s) Mg2+ (aq)+ 2OH-(aq)。已知K [Mg(OH) ]=1.8×10-11,K (MgCO )=3.5×10-8;
2 sp 2 sp 3
通常,溶液中某离子的浓度小于1.0×10-5mol·L-1时,可以认为该离子已沉淀完全。下列有关说法不正确的
是( )
A.滴入几滴稀硫酸,溶液的pH先下降后上升,最后保持一个稳定值
B.MgCO 的饱和溶液中c(Mg2+)>c(CO2-)
3 3
C.NaOH溶液可使MgCO 较彻底地转化为Mg(OH)
3 2
D.氢氧化镁可处理印染厂的酸性废水,处理后c(Mg2+)=1.8×10-3mol·L-1,此时溶液呈碱性
【答案】B
【解析】A项,滴入几滴稀硫酸后,氢离子和氢氧根离子反应生成水,氢氧根离子浓度降低,pH降低,
随后沉淀溶解平衡正向移动,氢氧根离子浓度增大,pH增大,A正确;B项,碳酸镁电离产生镁离子和碳
酸根离子,但是碳酸根离子会水解,故镁离子浓度大于碳酸根离子,B错误;C项,通过信息可知,氢氧
化镁的溶度积常数要小的多,故碳酸镁更加容易转化为氢氧化镁,则NaOH溶液可使MgCO 较彻底地转化
3
为Mg(OH) ,C正确;D项,处理后 ,则此时
2
,氢氧根离子浓度较大,溶液显碱性,D
正确;故选B。
16.(2023·浙江省宁波市高三下学期高考模拟)向工业废水中加入硫化物可以获得CuS、FeS纳米粒子
[已知K (FeS)= 6.3×10-18,K (CuS)= 1.3×10-36],下列说法正确的是( )
sp sp
A.FeS固体不能用于去除工业废水中的Cu2+
B.向FeSO 和CuSO 混合溶液中加入NaS溶液,当两种沉淀共存时,
4 4 2
C.向CuS饱和溶液中加入CuCl 固体,CuS的溶解平衡逆向移动,滤液中一定存在
2
D.已知HS溶液中 ,可判断CuS易溶于稀盐酸
2
【答案】C
【解析】A项,根据K (FeS)>K (CuS)可知,FeS固体能用于去除工业废水中的Cu2+,故A错误;B
sp sp
项,向FeSO 和CuSO 混合溶液中加入NaS溶液,当两种沉淀共存时,
4 4 2
资料整理【淘宝店铺:向阳百分百】,故B错误;C项,CuS存在溶解平衡CuS(s) Cu2+(aq)
+S2−(aq),向CuS饱和溶液中加入CuCl 固体,铜离子浓度增大,因此CuS的溶解平衡逆向移动,根据溶度
2
积常数得到滤液中一定存在 ,故C正确;D项,若要溶解CuS+2H+= Cu2++H S,则
2
,平衡常数很小,反应几乎不能发生,可判断CuS难
溶于稀盐酸,故D错误。故选C。
17.(2023·安徽省高三调研)常温下,K (NiS)=1.0×10-21,K (FeS)=6.0×10-18。RS的沉淀溶解平衡曲线
sp sp
如图所示(R表示Ni或Fe)。下列说法正确的是( )
A.图中II表示FeS溶解平衡曲线
B.常温下,NiS+Fe2+ FeS+Ni2+的平衡常数K=6000
C.常温下,与Q点相对应的NiS的分散系固-液共存
D.常温下,向P点对应的溶液中加适量NaS固体,可转化成M点对应的溶液
2
【答案】D
【解析】A项,图I表示FeS溶解平衡曲线,A项错误;B项,常温下,NiS+Fe2+ FeS+Ni2+的平
衡常数K=6000,B项错误;C项,Q点处, ,分散系中无固体,C项错误;D项,P点对应的
溶液中加适量NaS固体,S2-浓度增大,R2+浓度减小,可使溶液由P点转化成M点对应的溶液,D项正确;
2
故选D。
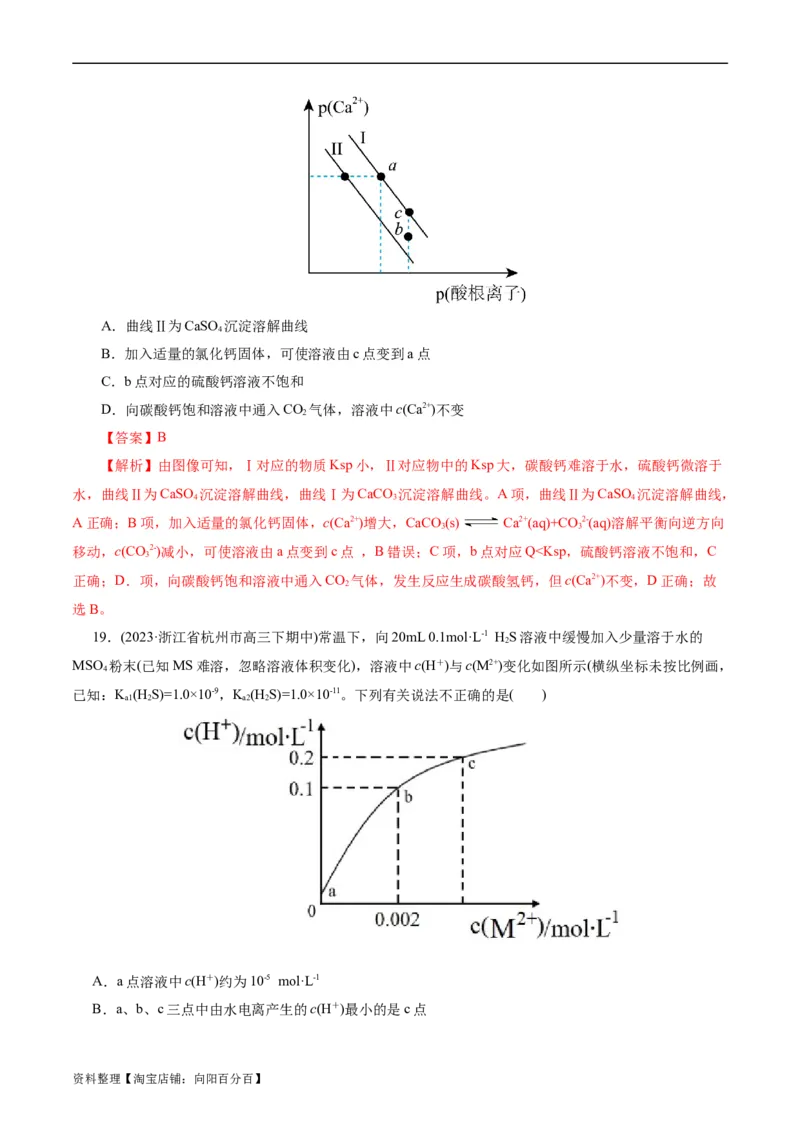
18.(2023·湖州、衢州、丽水三地市高三4月教学质量检测)常温时,碳酸钙和硫酸钙的沉淀溶解平衡
关系如图所示,已知 , (酸根离子) (酸根离子)。下列说法不正确的是( )
资料整理【淘宝店铺:向阳百分百】A.曲线Ⅱ为CaSO 沉淀溶解曲线
4
B.加入适量的氯化钙固体,可使溶液由c点变到a点
C.b点对应的硫酸钙溶液不饱和
D.向碳酸钙饱和溶液中通入CO 气体,溶液中c(Ca2+)不变
2
【答案】B
【解析】由图像可知,Ⅰ对应的物质Ksp小,Ⅱ对应物中的Ksp大,碳酸钙难溶于水,硫酸钙微溶于
水,曲线Ⅱ为CaSO 沉淀溶解曲线,曲线Ⅰ为CaCO 沉淀溶解曲线。A项,曲线Ⅱ为CaSO 沉淀溶解曲线,
4 3 4
A正确;B项,加入适量的氯化钙固体,c(Ca2+)增大,CaCO (s) Ca2+(aq)+CO 2-(aq)溶解平衡向逆方向
3 3
移动,c(CO2-)减小,可使溶液由a点变到c点 ,B错误;C项,b点对应Q