文档内容
考点 38 有机合成
目录
...................................................................................................................................1
1.高考真题考点分布...................................................................................................................................1
2.命题规律及备考策略...............................................................................................................................1
...................................................................................................................................2
考法01 碳骨架的构建...............................................................................................................................2
考法02 官能团的引入和转化...................................................................................................................4
考法03 有机合成路线的设计...................................................................................................................9
.................................................................................................................................13
1.高考真题考点分布
考点内容 考点分布
2024·安徽卷,15分;2024·湖北卷,15分;2024·江苏卷,15分;2024·甘肃卷,15
分;
2024·广东卷,15分;2024·湖南卷,15分;2023江苏卷,15分;2023海南卷,15分;
有机合成路线
2023广东卷,15分;2023浙江卷,12分;2023湖南卷,15分;2022海南卷,14分;
2022河北卷,15分;2022山东卷,12分;2022湖南卷,15分;2022浙江卷,12分;
2022江苏卷,15分;2022广东卷,14分;
2.命题规律及备考策略
【命题规律】
高频考点从近几年全国高考试题来看,官能团、反应类型、同分异构体的书写和判断、有机合成路线设计
仍是高考命题的热点。
【备考策略】解答有机合成路线设计题的方法
此类试题情境新颖,体现化学的应用性,拓宽学生视野,但不用纠结于情境,灵活运用正推法和逆推法:【命题预测】
预计2025年高考会以新的情境载体考查有机合成路线设计知识,结合陌生复杂信息或陌生反应信息对有机
化合物的组成、结构、性质和反应进行系统推理,对有机化合物的有机合成路线进行综合推断、设计或评
价,题目难度一般较大。
考法01 碳骨架的构建
1.碳链的增长
(1)卤代烃的取代反应
①溴乙烷与氰化钠的反应:CHCHBr+NaCN―→CHCHCN+NaBr,CHCHCN――――→CHCHCOOH。
3 2 3 2 3 2 3 2
②溴乙烷与丙炔钠的反应:CHCHBr+NaC≡CCH―→CHCHC≡CCH+NaBr。
3 2 3 3 2 3
(2)醛、酮的加成反应
①丙酮与HCN的反应: +HCN――→ 。
②乙醛与HCN的反应:CHCHO+HCN――→ 。
3
③羟醛缩合(以乙醛为例):CHCHO+CHCHO――→ 。
3 3
2.碳链的缩短
(1)与酸性KMnO 溶液的氧化反应
4
①烯烃、炔烃的反应
如 ――――→CH COOH + 。
3
②苯的同系物的反应
如 ――――→ 。
(2)脱羧反应
无水醋酸钠与氢氧化钠的反应:CHCOONa+NaOH――→CH↑+NaCO。
3 4 2 3
3.成环反应(1)二元醇成环,如HOCH CHOH――→ +HO。
2 2 2
(2)羟基酸酯化成环,如: +HO。
2
(3)氨基酸成环,如:HNCH CHCOOH―→ +HO。
2 2 2 2
(4)二元羧酸成环,如:HOOCCH CHCOOH――→ +HO。
2 2 2
(5)利用题目所给信息成环,如常给信息二烯烃与单烯烃的聚合成环: + ―――→ 。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
1.乙酸与乙醇的酯化反应,可以使碳链减短( )
2.裂化石油制取汽油,可以使碳链减短( )
3.乙烯的聚合反应,可以使碳链减短( )
4.烯烃与酸性KMnO 溶液的反应,可以使碳链减短( )
4
5.卤代烃与NaCN的取代反应,可以使碳链减短( )
6.环氧乙烷开环聚合,可以使碳链减短( )
【答案】1.× 2.√ 3.× 4.√ 5.× 6.×
考向01 考查碳骨架的构建
【例1】(2024·广东湛江·模拟)构建碳骨架反应是有机合成中的重要知识,其中第尔斯-阿尔德反应在合
成碳环这一领域有着举足轻重的地位,其模型为 ,则下列判断正确的是( )
A.合成 的原料为 和
B.合成 的原料为 和
C.合成 的原料为 和D.合成 的原料只能为 和
【答案】B
【解析】合成 的原料为 和 ,A错误; 中含有2个碳碳双键,合成 的原料可以
是 和 CH≡CH,也可以是 和 ,C 错误; 和 发生第尔斯-阿尔德反应也生成
,D错误。
【对点1】(2024·安徽六安·模拟)以丙烯为基础原料,可制备离子导体材料中有机溶剂的单体丙烯酸丁酯,
其合成路线如下:
下列判断错误的是( )
A.反应①是一个碳链增长的反应
B.反应②是还原反应,可以通过加成的方式实现
C.反应③需要的条件是浓硫酸和加热
D.该合成工艺的原子利用率为100%
【答案】D
【解析】对比反应①的反应物和生成物,可知反应①是一个碳链增长的反应,A项正确;反应②是醛基被
还原为羟基,在一定条件下,醛基与H 加成可得到羟基,B项正确;反应③是酯化反应,反应条件是浓硫
2
酸和加热,C项正确;反应③有水生成,故该合成工艺的原子利用率小于100%,D项错误。
考法02 官能团的引入和转化
1.各类官能团的引入方法
官能团 引入方法
①烃、酚的取代; ②醇与氢卤酸(HX)的取代
碳卤键
③不饱和烃与HX、X(X代表卤素原子,下同)的加成;
2
①烯烃与水的加成; ②醛、酮与氢气的加成;
羟基
③卤代烃在碱性条件下的水解; ④酯的水解; ⑤葡萄糖发酵产生乙醇
碳碳双键 ①某些醇或卤代烃的消去; ②炔烃不完全加成; ③烷烃的裂化①醇的催化氧化; ②连在同一个碳上的两个羟基脱水;
碳氧双键
③寡糖或多糖水解可引入醛基; ④含碳碳三键的物质与水的加成
羧基 ①醛基的氧化; ②酯、酰胺、肽、蛋白质、羧酸盐的水解
苯环上引入 ①卤代:X 和Fe; ②硝化:浓硝酸和浓硫酸共热;
2
不同的官能团 ③烃基氧化; ④先卤代后水解
2.官能团的消除
(1)通过加成反应消除不饱和键(双键、三键)。
(2)通过消去、氧化、酯化反应消除羟基。
(3)通过加成或氧化反应消除醛基。
(4)通过水解反应消除酯基、肽键、碳卤键。
3.官能团的保护与恢复
(1)碳碳双键:在氧化其他基团前可以利用其与HCl等的加成反应将其保护起来,待氧化后再利用消去反应
转变为碳碳双键。
HOCH CH==CHCH OH――→HOCH CHCHClCH OH――――→ ――――→
2 2 2 2 2
HOOC—CH==CH—COOH。
(2)酚羟基:在氧化其他基团前可以用NaOH溶液或CHI保护。
3
――→ ――→ 。
(3)醛基(或酮羰基):在氧化其他基团前可以用乙醇(或乙二醇)加成保护。
① ―――→ ―――→ 。
② ―――――――――→ ―――→ 。
(4)氨基:在氧化其他基团前可以用醋酸酐将氨基转化为酰胺,然后再水解转化为氨基。
――――→ ――――→ 。
(5)醇羟基、羧基可以成酯保护。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
1. 可发生消去反应引入碳碳双键( )2. 可发生催化氧化反应引入羧基( )
3.CHCHBr可发生取代反应引入羟基( )
3 2
4. 与CH==CH 可发生加成反应引入环( )
2 2
5.烷烃取代反应,不能引入—OH( )
6.如果以乙烯为原料,经过加成反应、取代反应可制得乙二醇( )
【答案】1.√ 2.× 3.√ 4.√ 5.√ 6.√
考向01 考查官能团的引入与转化
【例1】(2024·山东淄博·模拟)下列反应中,不可能在有机物中引入羧基的是( )
A.卤代烃的水解
B.有机物RCN在酸性条件下水解
C.醛的氧化
D.烯烃的氧化
【答案】A
【解析】卤代烃水解引入了羟基,RCN 水解生成 RCOOH,RCHO 被氧化生成 RCOOH,烯烃如
RCH==CHR被氧化后可以生成RCOOH。
考向02 考查官能团的保护
【例2】(2024·安徽池州·模拟)沙丁胺醇有明显的支气管舒张作用,临床上主要用于治疗喘息型支气管炎、
支气管哮喘等,其中一条通用的合成路线如下:已知:①R—OH ―――――――――→ROOCCH +CHCOOH
3 3
②
设计D→E的目的是________________。
【答案】保护酚羟基
【解析】根据已知①结合E的分子式可知E的结构简式: ;再根据I、J的结构知,设计
D→E的目的是保护酚羟基。
【对点1】(2024·广东茂名·模拟)有机物甲的分子式为C HNO ,可以通过如图路线合成(分离方法和其
7 7 2
他产物已省略)。下列说法不正确的是( )
――――――――→ \o(――――→ \o(―――――――→戊(C HON)\o(―――→甲
9 9 3
A.甲的结构简式为 ,可发生取代反应、加成反应B.步骤Ⅰ反应的化学方程式为 + ―――→ +HCl
C.步骤Ⅱ在苯环上引入醛基,步骤Ⅳ的反应类型是取代反应
D.步骤Ⅰ和Ⅳ在合成甲过程中的目的是保护氨基不被氧化
【答案】A
【解析】戊是 ,步骤Ⅳ中酰胺基发生水解得到甲,则甲为 ,含有氨基、羧基和苯环,可以
发生取代反应、加成反应,A错误;步骤Ⅱ中生成物含—CHO,则该步引入醛基,戊的结构简式为
,步骤Ⅳ是戊中的酰胺基发生水解反应,则反应类型是取代反应,C正确;氨基易被氧化,因
此步骤Ⅰ和Ⅳ在合成甲过程中的目的是保护氨基不被氧化,D正确。
【对点2】(2024·吉林辽源·模拟)重要的有机合成中间体W是一种多环化合物,以下为W的一种合成路
线(部分反应条件已简化):
已知:(ⅰ) + ―――――→ +R OH
1
(ⅱ)2CHCHO――→
3
结合D→E的反应过程,说明由B→C这步转化的作用是________。
【答案】保护酮羰基
【解析】由结构简式可知,A、E中都含有酮羰基,则B→C转化的作用是保护酮羰基。考法03 有机合成路线的设计
1.基本流程
2.合成路线的核心
合成路线的核心在于构建目标化合物分子的碳骨架和引入必需的官能团。
3.合成路线的推断方法
(1)正推法
①路线:某种原料分子―――――→目标分子。
②过程:首先比较原料分子和目标化合物分子在结构上的异同,包括官能团和碳骨架两个方面的异同;然
后,设计由原料分子转向目标化合物分子的合成路线。
(2)逆推法
①路线:目标分子――→原料分子。
②过程:在逆推过程中,需要逆向寻找能顺利合成目标化合物的中间有机化合物,直至选出合适的起始原
料。
(3)优选合成路线依据
①合成路线是否符合化学原理。
②合成操作是否安全可靠。
③绿色合成。绿色合成主要出发点是:有机合成中的原子经济性;原料的绿色化;试剂与催化剂的无公害
性。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)有机合成的关键是目标化合物分子碳骨架的构建和官能团的引入( )
(2)设计有机合成路线的方法有正推法和逆推法( )
(3)逆推法设计合成路线时往往先推出一些中间产物,然后逐步推出原料分子( )
(4)由丙烯合成1,2-丙二醇:第一步加成反应,第二步取代反应( )
(5)由1-溴丁烷合成1,3-丁二烯:第一步消去反应,第二步加聚反应( )
(6)由乙醇合成乙炔:第一步消去反应,第二步加成反应,第三步消去反应(
(7)由乙烯合成乙二醛:第一步加成反应,第二步取代反应,第三步氧化反应( )
(8)绿色合成思想只要求所有原料都转化为目标化合物( )【答案】(1) √ (2)√ (3) √ (4) √ (5) × (6)√ (7) √ (8)×
考向01 结合已知信息和目标产物的官能团寻找合成路径
【例1】(2024·黑龙江伊春·模拟)请设计合理方案,以苯甲醇( )为主要原料合成
(无机试剂及有机溶剂任用)。
已知:① ――→ ;
②R—CN――→R—COOH。
【答案】 ――――→ ―――→ ――→ ―――→
【解析】将目标分子拆解成两个 ,结合已知信息,苯甲醛先与HCN加成,再在酸性条件下水解,
即可得到 。
考向02 从有机物的合成路线图中分析、提取信息设计路线
【例2】(2024·河南周口·模拟)沙罗特美是一种长效平喘药,其合成的部分路线如图:请写出以 、 、CHNO 为原料制备 的合成路线流程图(无机试剂任用,
3 2
合成路线流程图示例见本题题干)。
【答案】
【解析】根据已知的流程图A→E的转化过程可推知,若要制备 ,则需将 与
(CH)C(OCH ) 发生取代反应得到 ,再与CHNO 反应得到 ,再利用羟基的消去反应引
3 2 3 2 3 2
入碳碳双键,将碳碳双键与硝基通过加氢最终还原生成氨基,合成路线见答案。
【对点1】(2024·浙江宁波·模拟)已知:
①
② ―――→
根据上述信息,写出以苯酚的一种同系物及HOCH CHCl为原料合成 的路线(不需注明反应条件)。
2 2
【答案】 ―――――→ ―――――→ ―――→
【解析】根据题给已知条件,对甲基苯酚与 HOCH CHCl反应能得到 ,之后发生水解反应得
2 2,得到目标产物需要利用已知反应①,合成路线见答案。
【对点2】(2024·山西吕梁·模拟)物质J是一种具有生物活性的化合物。该化合物的合成路线如下:
参照上述合成路线,以 和 为原料,设计合成 的路线(无机试剂任选)。
【答案】
【解析】结合G→I的转化过程可知,可先将 转化为 ,再使 和 反应生成
,并最终转化为 。1.(2024·黑龙江齐齐哈尔·模拟预测)有机物G是一种重要的化工原料,其合成路线如图:
(1) 的官能团名称是 。
(2)反应2为取代反应,反应物(Me) SO 中的“Me”的名称是 ,该反应的化学方程式是 。
2 4
(3)反应④所需的另一反应物名称是 ,该反应的条件是 ,反应类型是 。
(4)满足下列条件的 的同分异构体有 种(不考虑立体异构)。
①苯环上连有两个取代基
②能发生银镜反应
③能发生水解反应
(5)以 为原料,合成 。
合成路线图示例如下:A B C……→H
【答案】(1)溴原子
(2)甲基 2 (Me) SO 2 +H SO ;
2 4 2 4
(3)乙醇 浓硫酸,加热 酯化反应(取代反应)
(4)6
(5)
【分析】反应①为取代反应,碳链骨架不变,则 中Br原子被-CN取代,生成;反应②为取代反应,碳链骨架不变,则 中1个-H原子被-CH 取代,
3
生成 ;反应③ 在氢离子的作用下,生成 ;反
应④为酯化反应, 与乙醇发生酯化反应,生成 。
【解析】(1)
的官能团为溴原子,故答案为溴原子;
(2)
反应②为取代反应,碳链骨架不变,则-CHCN中1个-H原子被-CH 取代,则反应物(Me) SO 中的“Me”
2 3 2 4
表示甲基;反应的化学方程式为2 (Me) SO 2 +H SO ,故答案为:
2 4 2 4
甲基;2 (Me) SO 2 +H SO ;
2 4 2 4
(3)
反应④为酯化反应, 与乙醇发生酯化反应,生成 ,酯化反应
的条件为浓硫酸,加热,故答案为:乙醇;浓硫酸,加热;酯化反应(取代反应);
(4)
满足①苯环上连有两个取代基,②能发生银镜反应,③能发生水解反应,说明有一个
必须为甲酯基,则两个取代基可能是-OOCH、-C H 或-CHOOCH、-CH,每种组合均存在邻、间、对三种
2 5 2 3
位置异构,总共有6种,故答案为6;
(5)
以 为原料,根据题干信息,通过①③,可以合成 ,
用氢氧化钠取代,可以制备 , 与 在浓硫酸加热下,发生酯化反应,得到 ,具体合成路线为:
。
2.(2024·天津·模拟预测)化合物G是用于治疗面部疱疹药品泛昔洛韦的合成中间体,其合成路线如下:
已知: —代表
(1)A中碳原子的杂化类型 ,一氯代物有 种。
(2) 的名称为 , 的反应类型为 。
(3)写出 的化学方程式 。
(4)G中含氧官能团的名称是 。
(5)C中最多有 个碳原子共面,E分子核磁共振氢谱中有 组峰。
(6)F的分子式为 ,则 的反应的化学方程式为 。
(7)C有多种同分异构体,同时满足下列条件的同分异构体有 种。
①分子中含有苯环;②分子中含有2个 。
(8)请结合题目所给信息,设计以苯甲醇和丙二酸二乙酯为原料合成 的路线:
。
【答案】(1) sp2、sp3 4
(2) 乙二醇 取代反应
(3) +Br +HBr
2
(4)酯基、醚键(5) 9 9
(6) +2 +2
(7)10
(8)
【分析】A中甲基上的氢原子被溴原子取代生成B,B中溴原子被取代生成C,C中羟基被取代生成D,D
中溴原子被取代生成E,F发生取代反应生成G,F的分子式为C H O,根据E、G的结构简式知,F为
12 18 3
;
【解析】(1)A中苯环上C采用sp2杂化,甲基上C采用sp3杂化;A中有4种等效氢,一氯代物有4种;
(2) 的名称为乙二醇;由分析可知 的反应类型为取代反应;
(3)A中甲基上的氢原子被溴原子取代, 的化学方程式为 +Br +HBr;
2
(4)根据G的结构简式可知,其含氧官能团为酯基、醚键;
(5)根据单键可以绕轴旋转,C中碳原子都可能共面,共9个;根据E的结构简式,共有9种等效氢,即
核磁共振氢谱中有9组峰;
(6)F为 ,则F→G的反应方程式为 +2 →
+2 ,
(7)C的同分异构体符合下列条件:①分子中含有苯环;②分子中含有2个-CHOH,取代基可能是-
2
CHCHOH、-CHOH,两个取代基有邻位、间位、对位3种;取代基可能是2个-CHOH和-CH,两个取
2 2 2 2 3
代基2个-CHOH相邻时,甲基有2种排列方式,2个-CHOH相间时,甲基有3种排列方式,如果2个-
2 2
CHOH相对时,甲基有1种排列方式;取代基可能是-CH(CH OH),有1种结构,所以符合条件的同分异
2 2
构体有3+(2+3+1)+1=10种;(8)
模仿生成F的过程, 与氢溴酸在加热条件反应生成 , 与
在NaH/THF条件下反应生成 ,然后用LiAlH /THF还原
4
生成 ,合成路线为
。
3.(2024·福建泉州·模拟预测)唑草酮是一种药性强、易降解、污染少的除草剂,其中一种合成路线为:
已知:①DPPA是一种叠氮化试剂;
② 。
回答下列问题:
(1) 中含有官能团的名称为 。
(2) 与 反应得到 和 (填结构简式),该反应的目的是 。
(3) 的化学方程式为 。
(4)已知 中 键极性越大,则碱性越弱,则下列物质的碱性由弱到强的顺序为 (填
标号)a. b. c.
(5) 的结构简式为 。
(6) 存在多种同分异构体,写出符合下列条件的结构简式 (不考虑立体异构)。
①分子骨架为 ,且能发生银镜反应;
②核磁共振氢谱图中有4组峰,且峰面积比为3:2:2:1。
(7)化合物 的合成路线如下图(部分反应条件已略去),则 的结构简式为 。
【答案】(1)碳氟键、氨基
(2) 保护氨基
(3)
(4)b、c、a
(5)
(6)
(7)
【分析】由有机物的转化关系可知,A 与B(乙酸酐)发生取代反应生成C,C与SOCl 发生取代反应生成D ,D在氢氧化钠溶液中发生
2
水解反应生成E ,E一定条件下转化为F ,F与CHCOCOOH发生取
3
代反应生成G ,G在DPPA作用下发生取代反应生成H ,一
定条件下 与CFHCl发生取代反应生成 ,
2
经多步转化生成唑草酮 。
【解析】(1)由结构简式可知, 的官能团为碳氟键、氨基,故答案为:碳氟键、氨基。
(2)由分析可知, 与乙酸酐发生取代反应生成 和乙酸,
和 分子中都含有氨基,说明该步反应的作用是保护氨基,故答案为:CHCOOH;保护
3
氨基。
(3) 在氢氧化钠溶液中发生水解反应生成 ,反应为:
。
(4)元素的电负性越大,非金属性越强,有机物分子中C−X键的极性越大,元素的电负性大小顺序为:F
>Cl>H,则C−X键的极性大小顺序为C—F>C—Cl>C—H,所以由题给信息可知,三种物质碱性由弱到强的顺序为 > > ,故答案为:b、c、a。
(5)根据分析可知, G的结构简式为 ,故答案为:
。
(6)C为 ,满足条件为①分子骨架为 ,且能发生银镜反应,说明含有一个醛
基,②核磁共振氢谱图中有4组峰,且峰面积比为3:2:2:1,说明含有甲基,可能得结构简式为:
,故答案为: 。
(7)由题给合成路线可知,以苯胺为原料合成的合成步骤为: 一定条件下转化为
, 与 发生取代反应生成 ,DPPA
作用下 转化为 ,可知M为 。
4.(2024·江苏南京·模拟预测)某降血脂药物吉非罗齐(G)的一种合成路线如下:
(1)下列关于化合物E和G的说法正确的是___________。
A.官能团种类相同 B.都含有手性碳原子C.都能使酸性KMnO 溶液褪色 D.可以使用质谱仪区分
4
(2)标出B中酸性最强的氢原子 。
(3)已知C的分子式为C H BrO,C的结构简式为 。
11 15
(4)E→F的反应需经历E→X→F的过程,中间产物X和G互为同分异构体,写出该中间产物X的结构简式
。
(5)写出满足下列条件的D的一种同分异构体的结构简式 。
能和FeCl 溶液显色;碱性条件下水解酸化后得到的产物中均有2种不同的氢原子。
3
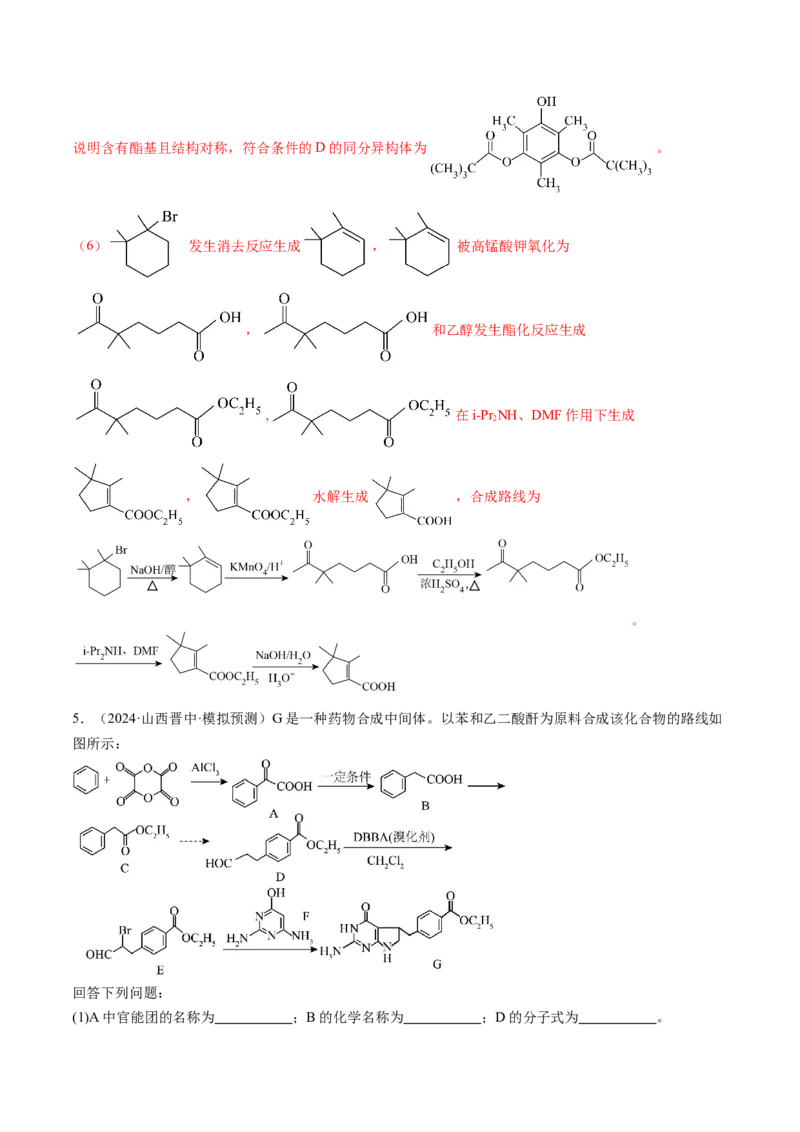
(6)已知: 。写出以 、乙醇为原料制备
的合成路线图 (须使用i-Pr NH、DMF,无机试剂和有机溶剂任用,合成路线流程
2
图示例见本题题干)。
【答案】(1)ACD
(2)
(3)
(4)
(5)(6)
【分析】C的分子式为C H BrO,B和C发生取代反应生成D和HBr,由D逆推,可知C为
11 15
。
【解析】(1)A.化合物E和G都含羧基、醚键,官能团种类相同,故A正确;
B.化合物E中连羧基的碳为手性碳原子,G不含有手性碳原子,故B错误;
C.苯环上都连有甲基,都能使酸性KMnO 溶液褪色,故C正确;
4
D.化合物E和G相对分子质量不同,可以使用质谱仪区分,故D正确;
选ACD。
(2)O原子电负性大,吸电子能力强, 2个羰基中间的碳原子上的H原子酸性更强,B中酸性最强的氢
原子是 。
(3)C的分子式为C H BrO,B和C发生取代反应生成D和HBr,由D逆推,C的结构简式为
11 15
;
(4)E→F的反应需经历E→X→F的过程,中间产物X和G互为同分异构体,则X可能是E与CHI发生
3
取代反应生成酯,中间产物X的结构简式为 。
(5)能和FeCl 溶液显色,说明含有酚羟基;碱性条件下水解酸化后得到的产物中均有2种不同的氢原子,
3说明含有酯基且结构对称,符合条件的D的同分异构体为 。
(6) 发生消去反应生成 , 被高锰酸钾氧化为
, 和乙醇发生酯化反应生成
, 在i-Pr NH、DMF作用下生成
2
, 水解生成 ,合成路线为
。
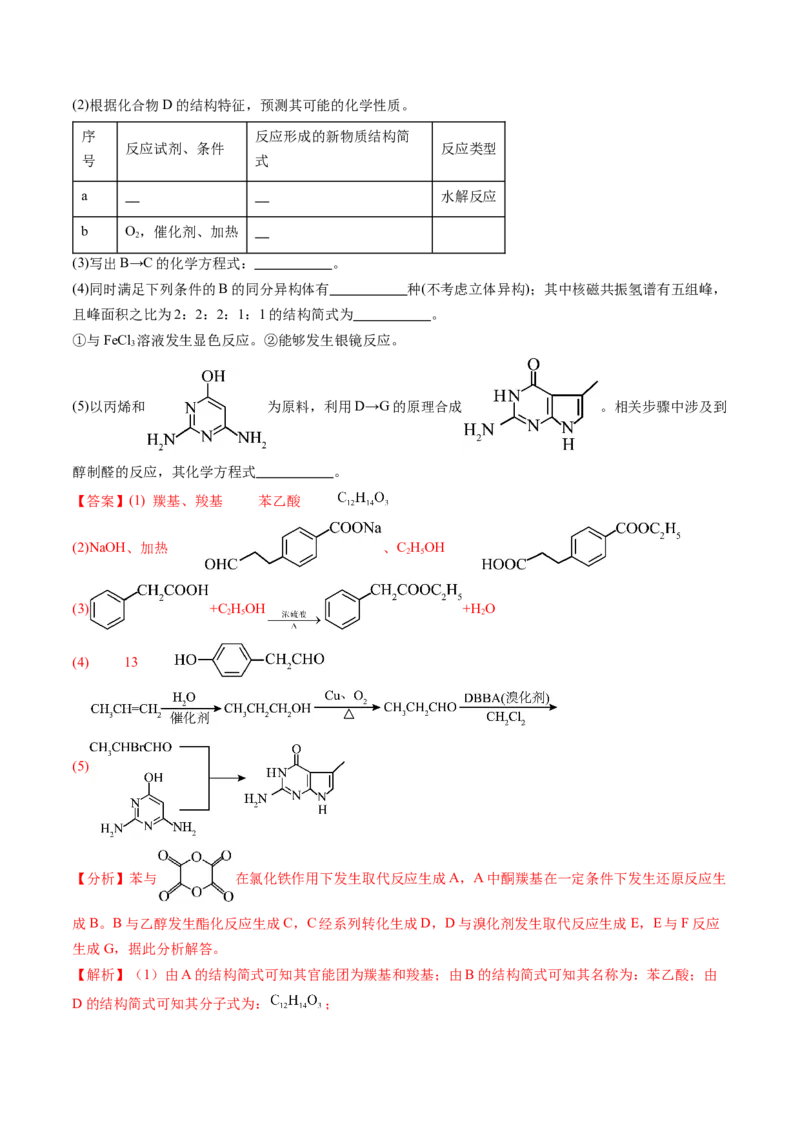
5.(2024·山西晋中·模拟预测)G是一种药物合成中间体。以苯和乙二酸酐为原料合成该化合物的路线如
图所示:
回答下列问题:
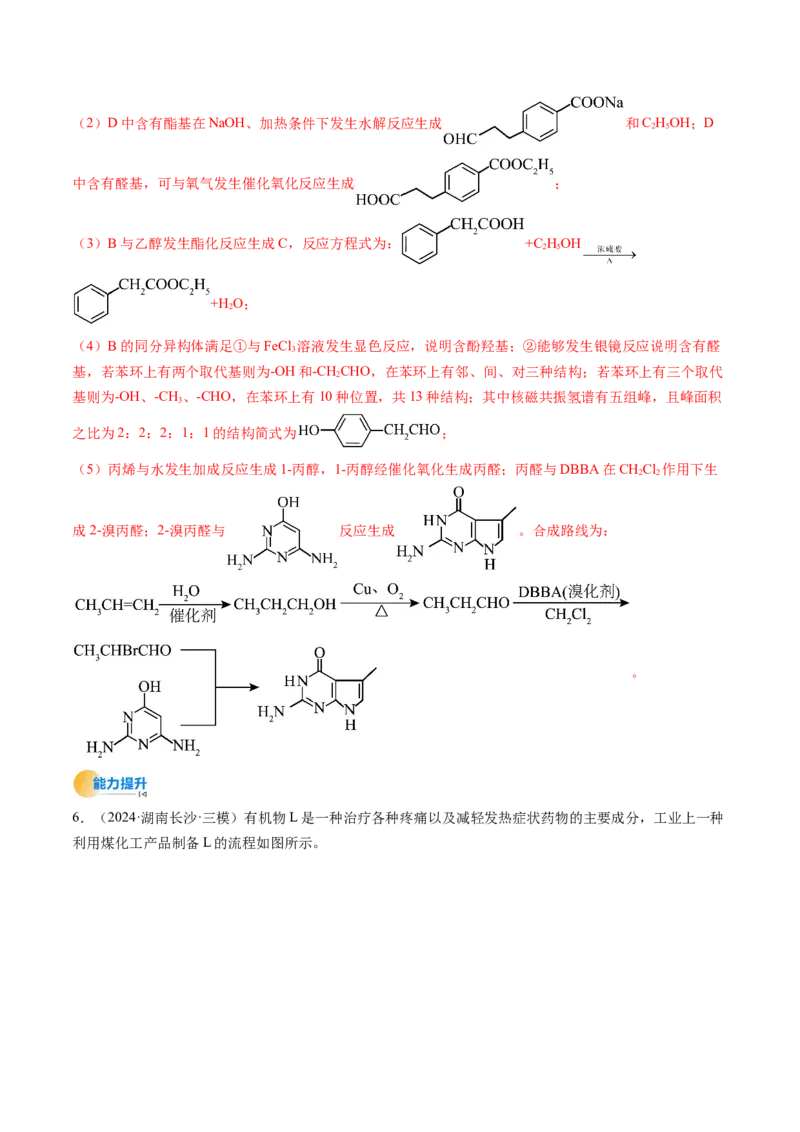
(1)A中官能团的名称为 ;B的化学名称为 ;D的分子式为 。(2)根据化合物D的结构特征,预测其可能的化学性质。
序 反应形成的新物质结构简
反应试剂、条件 反应类型
号 式
a 水解反应
b O,催化剂、加热
2
(3)写出B→C的化学方程式: 。
(4)同时满足下列条件的B的同分异构体有 种(不考虑立体异构);其中核磁共振氢谱有五组峰,
且峰面积之比为2:2:2:1:1的结构简式为 。
①与FeCl 溶液发生显色反应。②能够发生银镜反应。
3
(5)以丙烯和 为原料,利用D→G的原理合成 。相关步骤中涉及到
醇制醛的反应,其化学方程式 。
【答案】(1) 羰基、羧基 苯乙酸
(2)NaOH、加热 、C HOH
2 5
(3) +C HOH +H O
2 5 2
(4) 13
(5)
【分析】苯与 在氯化铁作用下发生取代反应生成A,A中酮羰基在一定条件下发生还原反应生
成B。B与乙醇发生酯化反应生成C,C经系列转化生成D,D与溴化剂发生取代反应生成E,E与F反应
生成G,据此分析解答。
【解析】(1)由A的结构简式可知其官能团为羰基和羧基;由B的结构简式可知其名称为:苯乙酸;由
D的结构简式可知其分子式为: ;(2)D中含有酯基在NaOH、加热条件下发生水解反应生成 和C HOH;D
2 5
中含有醛基,可与氧气发生催化氧化反应生成 ;
(3)B与乙醇发生酯化反应生成C,反应方程式为: +C HOH
2 5
+H O;
2
(4)B的同分异构体满足①与FeCl 溶液发生显色反应,说明含酚羟基;②能够发生银镜反应说明含有醛
3
基,若苯环上有两个取代基则为-OH和-CHCHO,在苯环上有邻、间、对三种结构;若苯环上有三个取代
2
基则为-OH、-CH、-CHO,在苯环上有10种位置,共13种结构;其中核磁共振氢谱有五组峰,且峰面积
3
之比为2:2:2:1:1的结构简式为 ;
(5)丙烯与水发生加成反应生成1-丙醇,1-丙醇经催化氧化生成丙醛;丙醛与DBBA在CHCl 作用下生
2 2
成2-溴丙醛;2-溴丙醛与 反应生成 。合成路线为:
。
6.(2024·湖南长沙·三模)有机物L是一种治疗各种疼痛以及减轻发热症状药物的主要成分,工业上一种
利用煤化工产品制备L的流程如图所示。回答下列问题:
(1)C的分子式为 ;D的化学名称为 。
(2)K的结构简式为 。
(3) 的化学方程式为 ;反应类型为 。
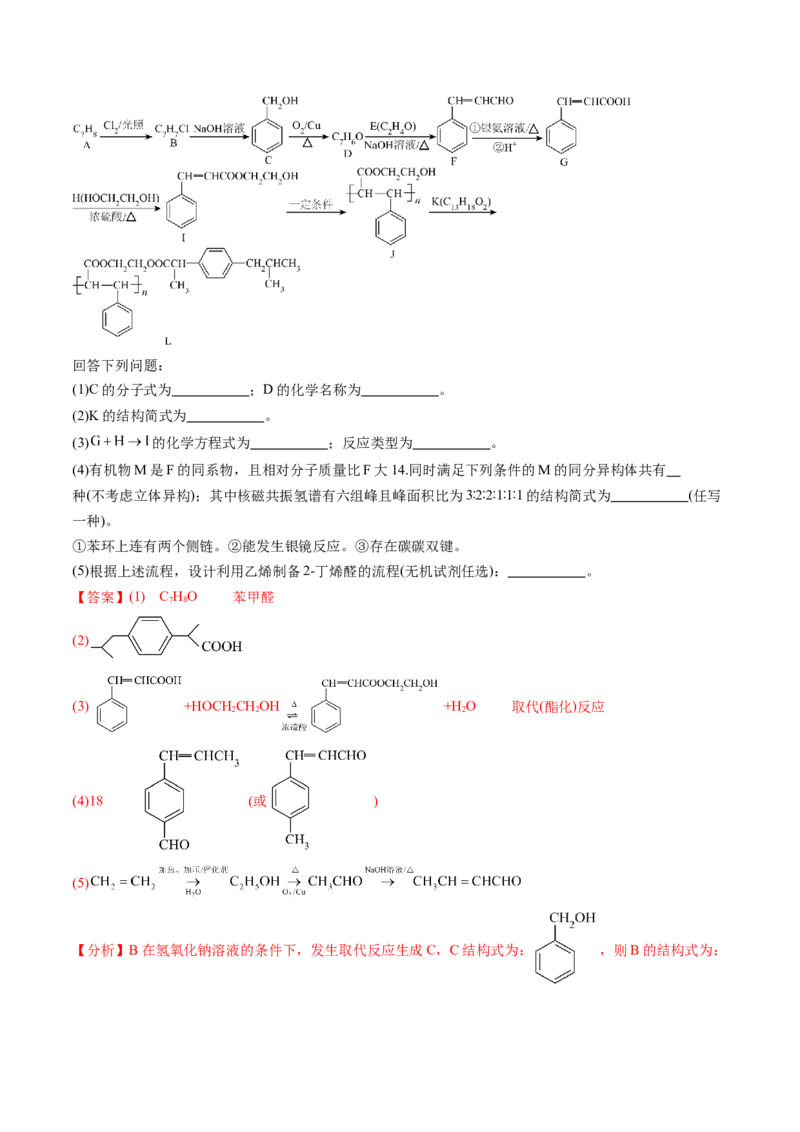
(4)有机物M是F的同系物,且相对分子质量比F大14.同时满足下列条件的M的同分异构体共有
种(不考虑立体异构);其中核磁共振氢谱有六组峰且峰面积比为3∶2∶2∶1∶1∶1的结构简式为 (任写
一种)。
①苯环上连有两个侧链。②能发生银镜反应。③存在碳碳双键。
(5)根据上述流程,设计利用乙烯制备2-丁烯醛的流程(无机试剂任选): 。
【答案】(1) C HO 苯甲醛
7 8
(2)
(3) +HOCH CHOH +H O 取代(酯化)反应
2 2 2
(4)18 (或 )
(5)
【分析】B在氢氧化钠溶液的条件下,发生取代反应生成C,C结构式为: ,则B的结构式为:,A与氯气在光照条件下,生成B,则A为 ,C在催化剂氧气条件下,生成D,D的结构
式为: ,D先发生加成反应,再发生消去,生成F , 中醛基被氧
化生成羧基,生成G ,G与乙二醇发生取代反应,生成I ,
I发生聚合反应,生成J , 又发生取代反应生成L
。
【解析】(1)①C的分子式为C HO,;②结合流程图分析可知,D为苯甲醛;
7 8
(2)根据J和L的结构简式,结合K的分子式,可知k的结构简式为 ;
(3) 的化学方程式为
+H O;
2
②该反应类型为取代(酯化)反应;
(4)同系物是指结构相似、分子组成相差若干个“CH”原子团的有机化合物。化合物F的同系物M比F
2
的相对分子质量大14,则M比F多一个碳,且存在碳碳双键、醛基。M的同分异构体能发生银镜反应,
则含有醛基;苯环上有两个取代基,则2个取代基可以分别为-CH=CHCHO、-CH;-CHCHO、-
3 2
CH=CH;-CHO、-CH=CHCH ;-CHO、-C(CH)=CH ;-C(CHO)=CH ,-CH;-CHO,-CHCH=CH,每
2 3 3 2 2 3 2 2
种情况均存在邻间对3种位置关系,共18种,故答案为:18;
②其中核磁共振氢谱有六组峰且峰面积比为3∶2∶2∶1∶1∶1的结构简式为 或 ;
(5)乙烯和水发生加成反应生成乙醇,然后催化氧化得到乙醛,最后发生类似D→F的反应得到目标产物,合成路线为 。
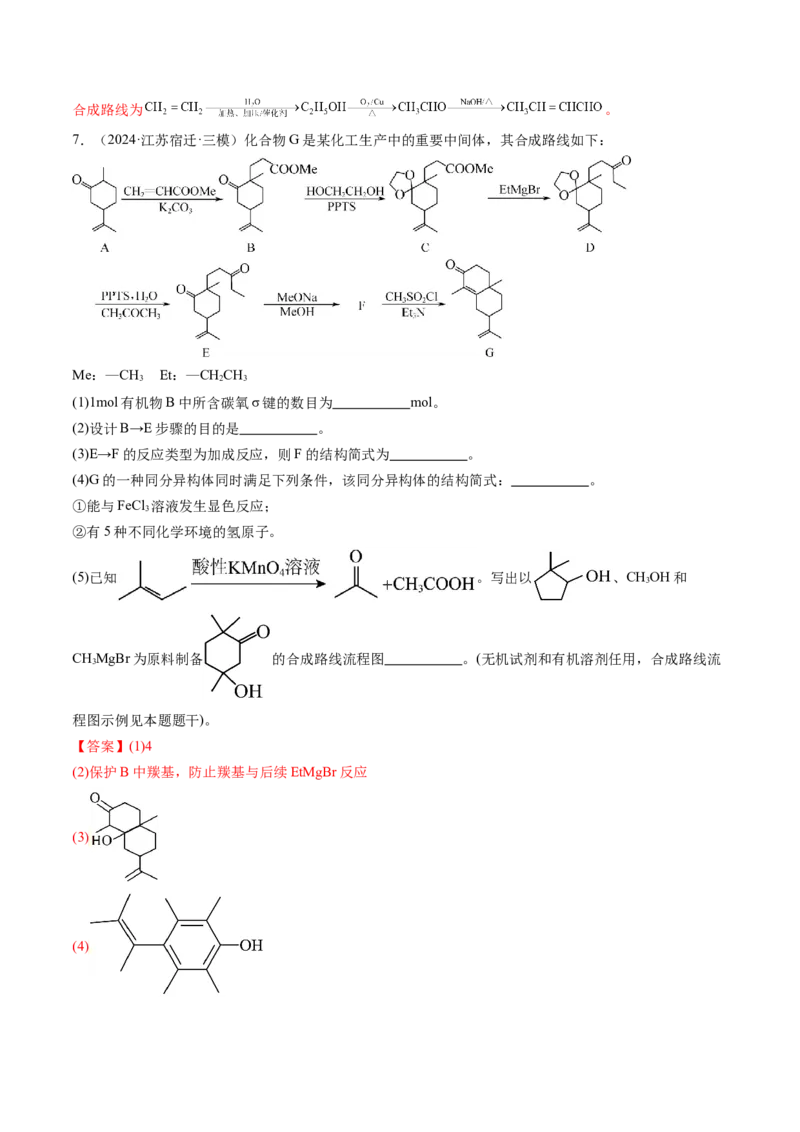
7.(2024·江苏宿迁·三模)化合物G是某化工生产中的重要中间体,其合成路线如下:
Me:—CH Et:—CHCH
3 2 3
(1)1mol有机物B中所含碳氧σ键的数目为 mol。
(2)设计B→E步骤的目的是 。
(3)E→F的反应类型为加成反应,则F的结构简式为 。
(4)G的一种同分异构体同时满足下列条件,该同分异构体的结构简式: 。
①能与FeCl 溶液发生显色反应;
3
②有5种不同化学环境的氢原子。
(5)已知 。写出以 、CHOH和
3
CHMgBr为原料制备 的合成路线流程图 。(无机试剂和有机溶剂任用,合成路线流
3
程图示例见本题题干)。
【答案】(1)4
(2)保护B中羰基,防止羰基与后续EtMgBr反应
(3)
(4)(5)
【分析】由有机物的转化关系可知,碳酸钾作用下A 与CH=CHCOOMe发生加成反应生成B
2
,在PPTS作用下与乙二醇发生加成反应生成C ,C
与EtMgBr发生取代反应生成D ,D在PPTS、水、丙酮作用下转化为E
,E在MeONa和MeOH作用下发生分子内加成反应生成F ,则F为
;F在CHSO Cl和EtN作用下发生消去反应生成G 。
3 2 3
【解析】(1)B为 ,结构中有1个羰基、1个酯基,因此则1molB所含碳氧σ键
的数目为4mol。
(2)设计B→E步骤的目的是:保护B中羰基,防止羰基与后续EtMgBr反应,故答案为:保护B中羰基,
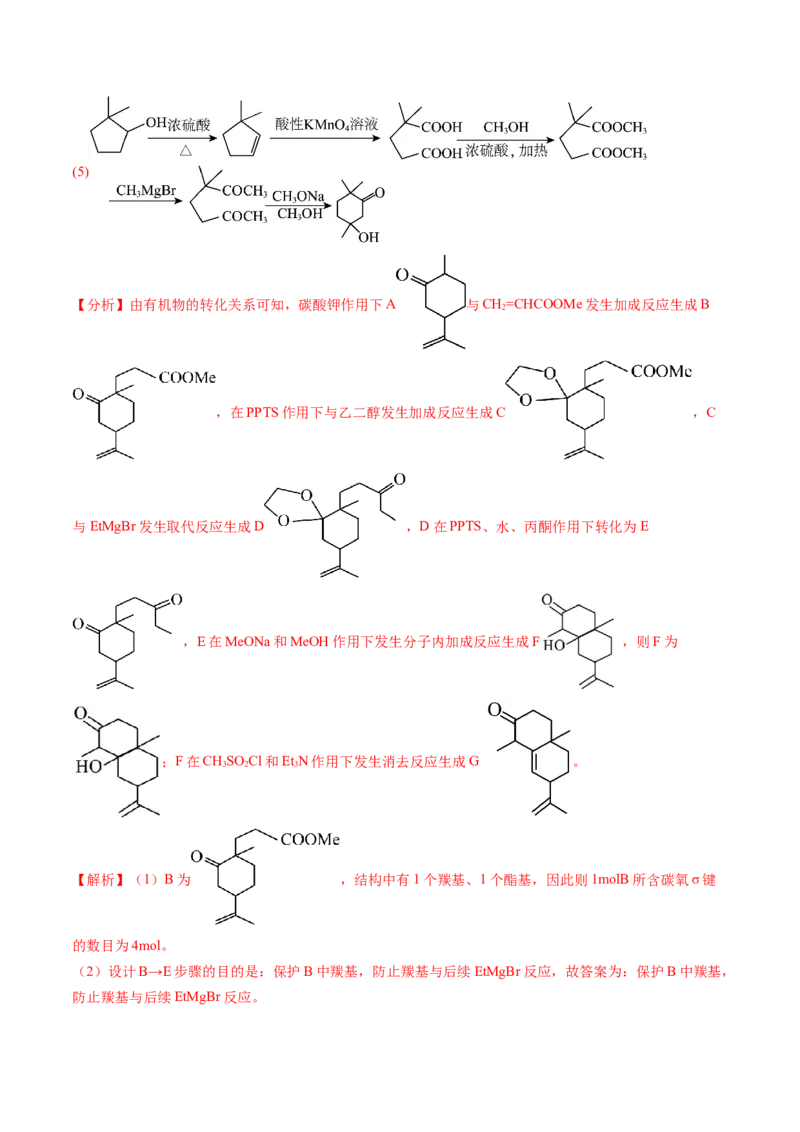
防止羰基与后续EtMgBr反应。(3)由分析可知,F的结构简式为 。
(4)G为 ,分子式为C H O,G的同分异构体能与氯化铁溶液发生显色反应,分子中含
15 22
有1个酚羟基,有五种不同化学环境的氢原子,符合条件的结构简式为: 。
(5)以 、CHOH和CHMgBr为原料制备 的合成路线为:
3 3
。
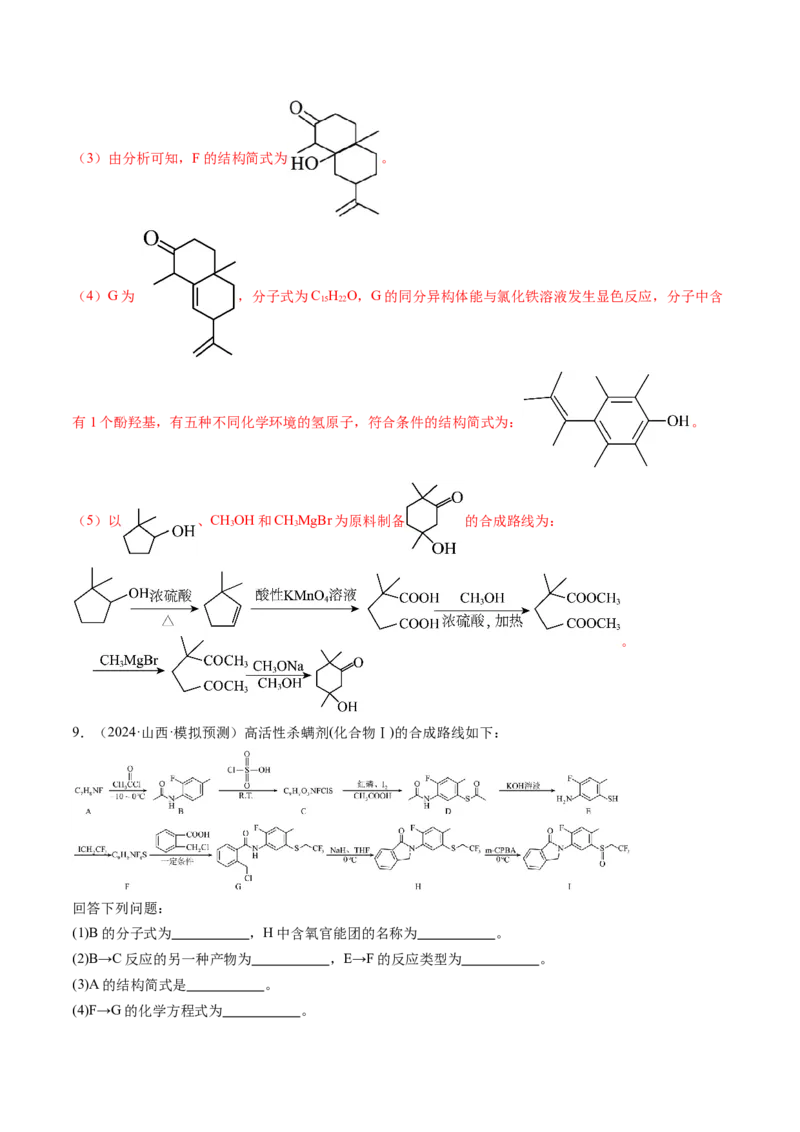
9.(2024·山西·模拟预测)高活性杀螨剂(化合物Ⅰ)的合成路线如下:
回答下列问题:
(1)B的分子式为 ,H中含氧官能团的名称为 。
(2)B→C反应的另一种产物为 ,E→F的反应类型为 。
(3)A的结构简式是 。
(4)F→G的化学方程式为 。(5)化合物B的同分异构体中满足下列条件的有 种(不考虑立体异构);其中核磁共振氢谱有5组
峰且峰面积之比为3:2:2:2:1的结构简式为 。
①苯环上含有两个取代基且能发生银镜反应;
②分子中含有-NH 且-NH 与苯环直接相连。
2 2
【答案】(1) C H OFN 酰胺基
9 10
(2)H O 取代反应
2
(3)
(4) + +H O
2
(5) 12
【分析】A发生取代反应生成B,由B的结构简式,结合A的分子式可推出则A为 ,B
与 发生取代反应生成C和水,结合分子式可推C的结构简式为 ,
C在红磷、I、CHCOOH的条件下生成D,D在KOH溶液中生成E,E与ICHCF 发生取代反应生成HI
2 3 2 3
和F,结合分子式可推知F为 ,F与 在一定条件下发生取代反
应生成G和水,G与NaH、THF、0℃下生成H,H在m-CPBA、0℃下反应生成I,据此回答。
【解析】(1)B为 ,故分子式为C H OFN;H为 ,
9 10
含氧官能团的名称为酰胺键;(2)由分析知,B 与 发生取代反应生成C
和水;由分析知,E与ICHCF 发生取代反应生成HI和F;
2 3
(3)由分析知,A的结构简式是 ;
(4)由分析知,F与 在一定条件下发生取代反应生成G和水,方程式为
+ +H O;
2
(5)化合物B的同分异构体中满足①苯环上含有两个取代基且能发生银镜反应;
②分子中含有-NH 且-NH 与苯环直接相连的有 、 、
2 2
、 ,共12种,其中,核磁共振氢谱显示为5组峰,且峰面积之
比为3:2:2:2:1的同分异构体的结构简式为 。
10.(2024·辽宁沈阳·模拟预测)薄荷酮是重要的医药合成原料,由薄荷酮合成并环化合物路线如下:已知:①迈克尔加成反应:
②羟醛缩合反应:(酮类也有类似性质)
(1)下列说法正确的是___________。
A.B中sp3杂化的原子有12个 B.C→D的反应类型是消去反应
C.F中有三种含氧官能团 D.H存在芳香族化合物的同分异构体
(2)D→E发生迈克尔加成反应,则E的结构简式为 。
(3)G→H还产生一种无色气体,写出该反应的化学方程式 。
(4)化合物A的同分异构体中满足下列条件的有 种。(不考虑立体异构)
①含六元环且环上只有一个取代基;
②能发生银镜反应。
(5)根据流程中的信息,以 与 为原料合成 的路线如图,(部分反应条
件已略)
其中M和N的结构简式分别为 和 。
(6)碳可以形成多种杂环化合物,如呋喃( )、吡咯( )。
①沸点:呋喃 吡咯(填“>”或“<”)。
②吡咯分子中所有原子共平面。已知大π键可以用 表示,其中m表示参与形成大π键的原子数,n代表大π键中的电子数,则吡咯中大π键可以表示为 。
【答案】(1)BD
(2)
(3)
(4)5
(5)
(6) <
【分析】C发生消去反应生成D,D→E发生迈克尔加成反应,E的结构简式为 ,E发
生信息反应②生成F,F先在碱性条件下发生水解反应,再酸化得到G为 ,据此分析
解答。
【解析】(1)A.B中sp3杂化的原子有12个饱和碳原子和1个N原子,共有13个,错误;
B.C→D脱去小分子 ,D中生成碳碳双键,故反应类型是消去反应,正确;
C.F中有酯基、羰基两种含氧官能团,错误;
D. H的不饱和度为4,且碳原子数超过6个,故存在芳香族化合物的同分异构体,正确
故选BD。,
(2)D→E发生迈克尔加成反应,根据已知信息反应①,可知E的结构简式为 。(3)G为 ,G→H还产生一种无色气体,对比G、H的结构简式,该无色气体为
CO,该反应的化学方程式为 。
2
(4)A为 ,化合物A的同分异构体中满足下列条件:①含六元环且环上只有一个取代基;②
能发生银镜反应,含有醛基;六元环为饱和六元碳环,故该同分异构体可以看成醛基取代 、
侧链上的氢原子, 侧链上有2种氢原子, 侧链上有3
种氢原子,故共有5种。
(5) 与 发生迈克尔加成反应生成M为 ,
发生信息反应②生成N,因为羟基在发生消去反应时可能有三种消去方式,故N
可能有3种结构 ,
(6)①吡咯可以形成分子间氢键,故沸点:呋喃<吡咯。
②吡咯分子中所有原子共平面,则C、N原子均采取sp2杂化,每个C原子各有一个未参与杂化的p轨道,
该p轨道上有一个电子参与形成π键,N原子未参与杂化的p轨道上有一对电子,则在形成的大π键中,
每个C原子各提供一个电子,N原子也提供一对电子,则吡咯中大π键可以表示为 。
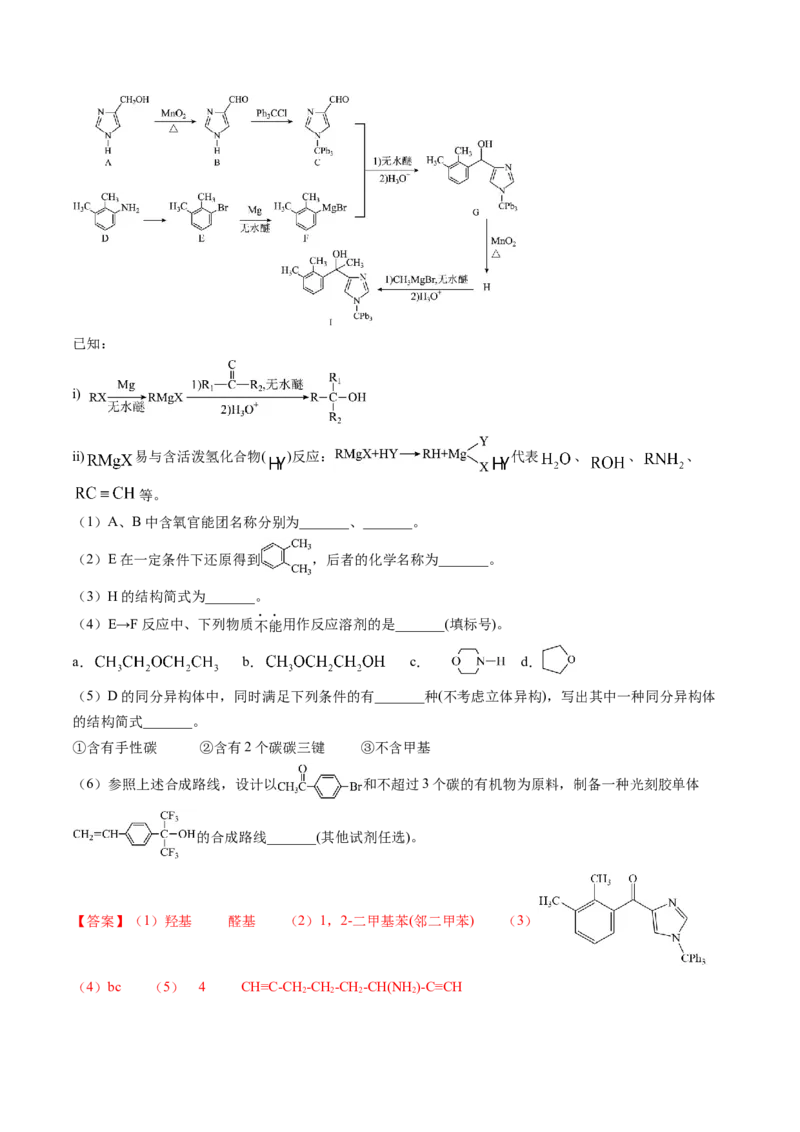
1.(2024·安徽卷)化合物1是一种药物中间体,可由下列路线合成( 代表苯基,部分反应条件略去):已知:
i)
ii) 易与含活泼氢化合物( )反应: 代表 、 、 、
等。
(1)A、B中含氧官能团名称分别为_______、_______。
(2)E在一定条件下还原得到 ,后者的化学名称为_______。
(3)H的结构简式为_______。
(4)E→F反应中、下列物质不能用作反应溶剂的是_______(填标号)。
a. b. c. d.
(5)D的同分异构体中,同时满足下列条件的有_______种(不考虑立体异构),写出其中一种同分异构体
的结构简式_______。
①含有手性碳 ②含有2个碳碳三键 ③不含甲基
(6)参照上述合成路线,设计以 和不超过3个碳的有机物为原料,制备一种光刻胶单体
的合成路线_______(其他试剂任选)。
【答案】(1)羟基 醛基 (2)1,2-二甲基苯(邻二甲苯) (3)
(4)bc (5) 4 CH≡C-CH -CH-CH-CH(NH)-C≡CH
2 2 2 2(6):
【解析】有机物A中的羟基在MnO 的催化下与氧气反应生成醛基,有机物B与Ph CCl发生取代反应生成
2 3
有机物C;有机物D中的氨基发生取代反应生成有机物E,D中的氨基变为E中的Cl,E发生已知条件i的
两步反应与有机物C作用最终生成有机物G;有机物G在MnO 的催化先与氧气反应生成有机物H,有机
2
物H的结构为 ,有机物H最终发生已知条件i的反应生成目标化合物I。
(1)根据流程中A和B的结构,A中的含氧官能团为羟基,B中的含氧官能团为醛基。
(2)根据题目中的结构,该结构的化学名称为1,2-二甲基苯(邻二甲苯)。
(3)根据分析,H的结构简式为 。
(4)根据已知条件ii,RMgX可以与含有活泼氢的化合物(HO、ROH、RNH 、RC≡CH等)发生反应,
2 2
b中含有羟基,c中含有N-H,其H原子为活泼H原子,因此不能用b、c作溶剂。
(5)根据题目所给条件,同分异构体中含有2个碳碳三键,说明结构中不含苯环,结构中不含甲基,说明
三键在物质的两端,同分异构体中又含有手性碳原子,因此,可能的结构有:CH≡C-CH -CH-CH-
2 2 2
CH(NH)-C≡CH、CH≡C-CH -CH-CH(NH)-CH -C≡CH、H≡C-CH-CH(CH NH )-CH -CH-C≡CH、H≡C-CH-
2 2 2 2 2 2 2 2 2 2 2
CH(CH CHNH )-CH -C≡CH,共4种。
2 2 2 2
(6)根据题目给出的流程,先将原料中的羰基还原为羟基,后利用浓硫酸脱水生成双键,随后将物质与
Mg在无水醚中反应生成中间产物,后再与CFCOCF 在无水醚中反应再水解生成目标化合物,具体的流程
3 3
如下:
。
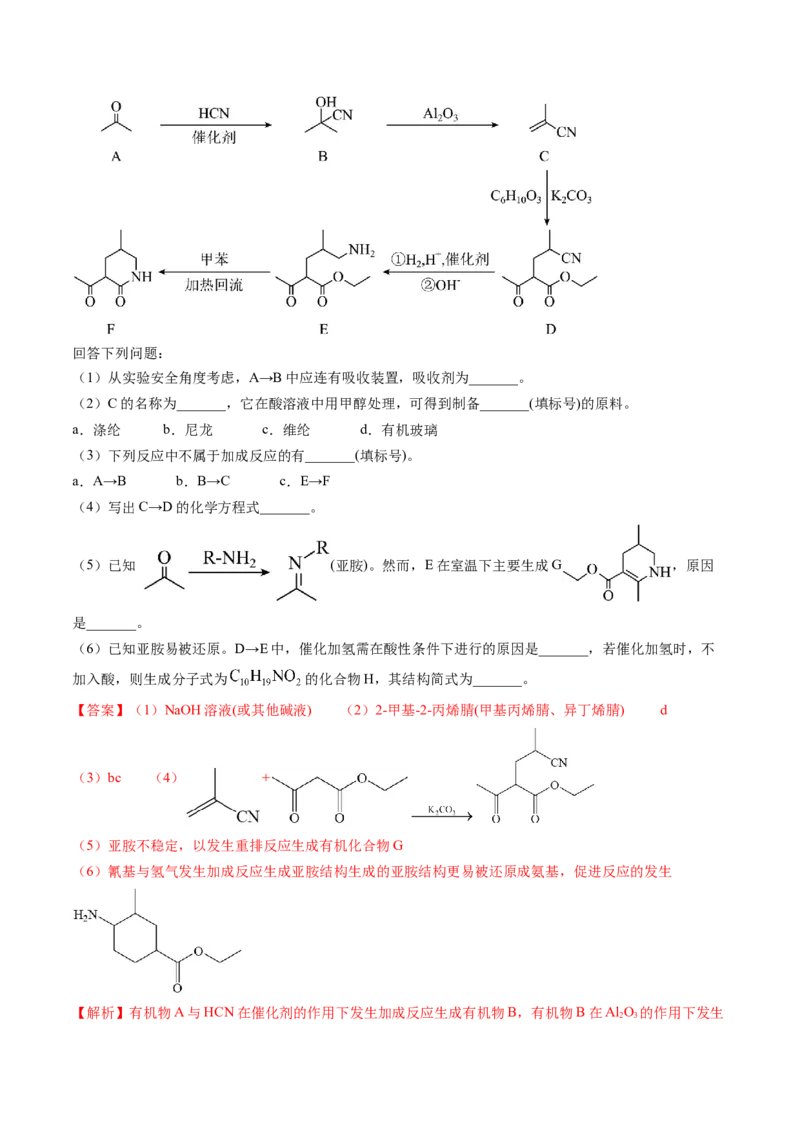
2.(2024·湖北卷)某研究小组按以下路线对内酰胺F的合成进行了探索:回答下列问题:
(1)从实验安全角度考虑,A→B中应连有吸收装置,吸收剂为_______。
(2)C的名称为_______,它在酸溶液中用甲醇处理,可得到制备_______(填标号)的原料。
a.涤纶 b.尼龙 c.维纶 d.有机玻璃
(3)下列反应中不属于加成反应的有_______(填标号)。
a.A→B b.B→C c.E→F
(4)写出C→D的化学方程式_______。
(5)已知 (亚胺)。然而,E在室温下主要生成G ,原因
是_______。
(6)已知亚胺易被还原。D→E中,催化加氢需在酸性条件下进行的原因是_______,若催化加氢时,不
加入酸,则生成分子式为 的化合物H,其结构简式为_______。
【答案】(1)NaOH溶液(或其他碱液) (2)2-甲基-2-丙烯腈(甲基丙烯腈、异丁烯腈) d
(3)bc (4) +
(5)亚胺不稳定,以发生重排反应生成有机化合物G
(6)氰基与氢气发生加成反应生成亚胺结构生成的亚胺结构更易被还原成氨基,促进反应的发生
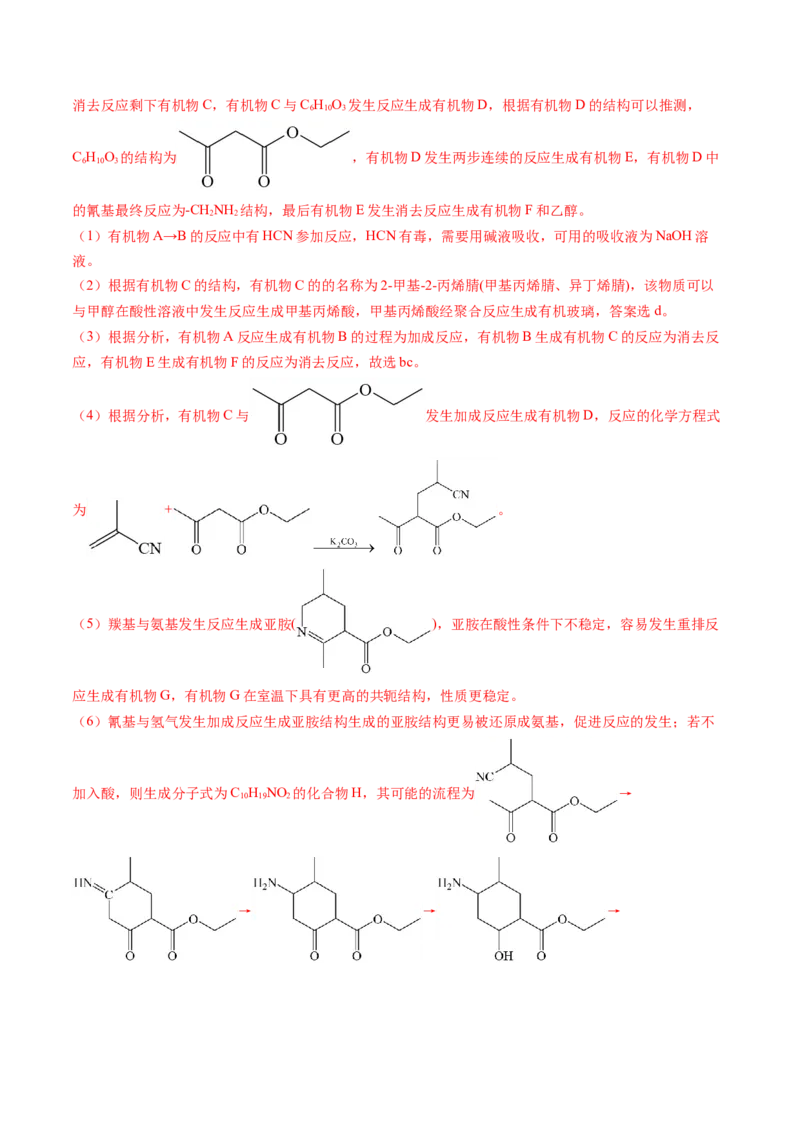
【解析】有机物A与HCN在催化剂的作用下发生加成反应生成有机物B,有机物B在Al O 的作用下发生
2 3消去反应剩下有机物C,有机物C与C H O 发生反应生成有机物D,根据有机物D的结构可以推测,
6 10 3
C H O 的结构为 ,有机物D发生两步连续的反应生成有机物E,有机物D中
6 10 3
的氰基最终反应为-CHNH 结构,最后有机物E发生消去反应生成有机物F和乙醇。
2 2
(1)有机物A→B的反应中有HCN参加反应,HCN有毒,需要用碱液吸收,可用的吸收液为NaOH溶
液。
(2)根据有机物C的结构,有机物C的的名称为2-甲基-2-丙烯腈(甲基丙烯腈、异丁烯腈),该物质可以
与甲醇在酸性溶液中发生反应生成甲基丙烯酸,甲基丙烯酸经聚合反应生成有机玻璃,答案选d。
(3)根据分析,有机物A反应生成有机物B的过程为加成反应,有机物B生成有机物C的反应为消去反
应,有机物E生成有机物F的反应为消去反应,故选bc。
(4)根据分析,有机物C与 发生加成反应生成有机物D,反应的化学方程式
为 + 。
(5)羰基与氨基发生反应生成亚胺( ),亚胺在酸性条件下不稳定,容易发生重排反
应生成有机物G,有机物G在室温下具有更高的共轭结构,性质更稳定。
(6)氰基与氢气发生加成反应生成亚胺结构生成的亚胺结构更易被还原成氨基,促进反应的发生;若不
加入酸,则生成分子式为C H NO 的化合物H,其可能的流程为 →
10 19 2
→ → →→ ,因此,有机物H的结构为
。
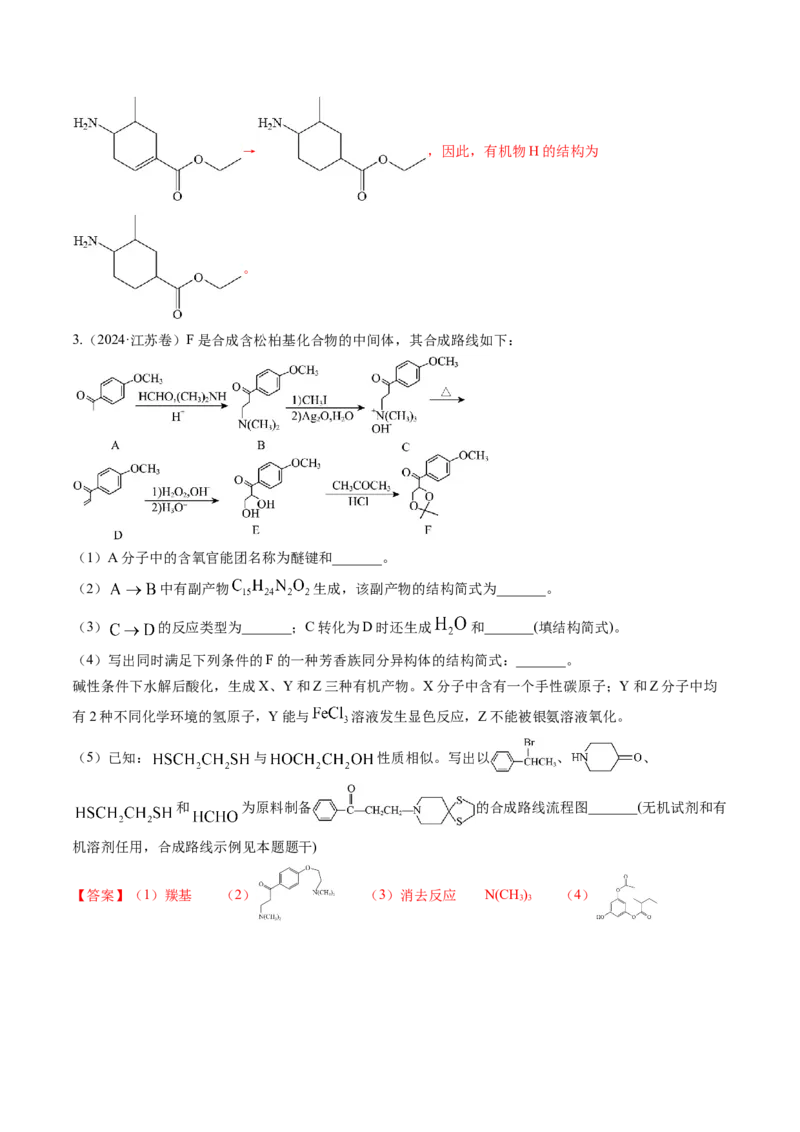
3.(2024·江苏卷)F是合成含松柏基化合物的中间体,其合成路线如下:
(1)A分子中的含氧官能团名称为醚键和_______。
(2) 中有副产物 生成,该副产物的结构简式为_______。
(3) 的反应类型为_______;C转化为D时还生成 和_______(填结构简式)。
(4)写出同时满足下列条件的F的一种芳香族同分异构体的结构简式:_______。
碱性条件下水解后酸化,生成X、Y和Z三种有机产物。X分子中含有一个手性碳原子;Y和Z分子中均
有2种不同化学环境的氢原子,Y能与 溶液发生显色反应,Z不能被银氨溶液氧化。
(5)已知: 与 性质相似。写出以 、 、
和 为原料制备 的合成路线流程图_______(无机试剂和有
机溶剂任用,合成路线示例见本题题干)
【答案】(1)羰基 (2) (3)消去反应 N(CH ) (4)
3 3(5)
【解析】A中羰基相连的甲基发生加成反应,得到的羟基与(CH)NH发生取代反应,得到物质B,B中N
3 2
原子在CHI和Ag O、HO的先后作用下,引入一个CH,得到物质C;C受热发生消去反应,+N(CH ) 同
3 2 2 3 3 3
OH-与相邻C上的H发生消去反应生成HO和N(CH ),生成碳碳双键得到物质D,D的碳碳双键在HO
2 3 3 2 2
的碱溶液作用下发生反应,后再酸化引入两个羟基则得到物质E,两个羟基与CHCOCH 在HCl环境中脱
3 3
去HO得到物质F。
2
(1)根据题中A分子的结构可知,其含氧官能团有醚键和羰基。
(2)A生成B的过程是甲醛与A中羰基相连的甲基发生加成反应,得到的羟基与(CH)NH发生取代反
3 2
应,结合副产物的分子式 ,可推断该副产物是一分子A结合了两分子的HCHO和(CH)NH,
3 2
结构简式为 。
(3)据分析, 的反应类型为消去反应;C转化为D时还生成 和N(CH )
3 3。
(4)由题中F的结构简式可知其分子式是C H O,其不饱和度为6,其芳香族同分异构体在碱性条件下
13 16 5
水解后酸化,生成X、Y和Z三种有机产物,推断该同分异构体中含有两个酯基。X分子中含有一个手性
碳原子,则有一个碳原子连接着四种互不相同的原子或原子团;Y和Z分子中均有2种不同化学环境的氢
原子,Y能与 溶液发生显色反应,则Y含有酚羟基,推断Y的结构简式是 ,Z不能被银
氨溶液氧化,则Z不含醛基,推断Z的结构简式是CHCOOH;则X分子中共含有5个C原子,其中有-
3
COOH,则推断其结构简式是 ;综上分析,该芳香族同分异构体的一种结构简式是
。
(5)结合物质E生成F的结构变化可推断 与 反应可生成目标产物的 部
分;产物的 部分可由 生成 后与HCHO反应增长碳链得到,故设计合成路线:
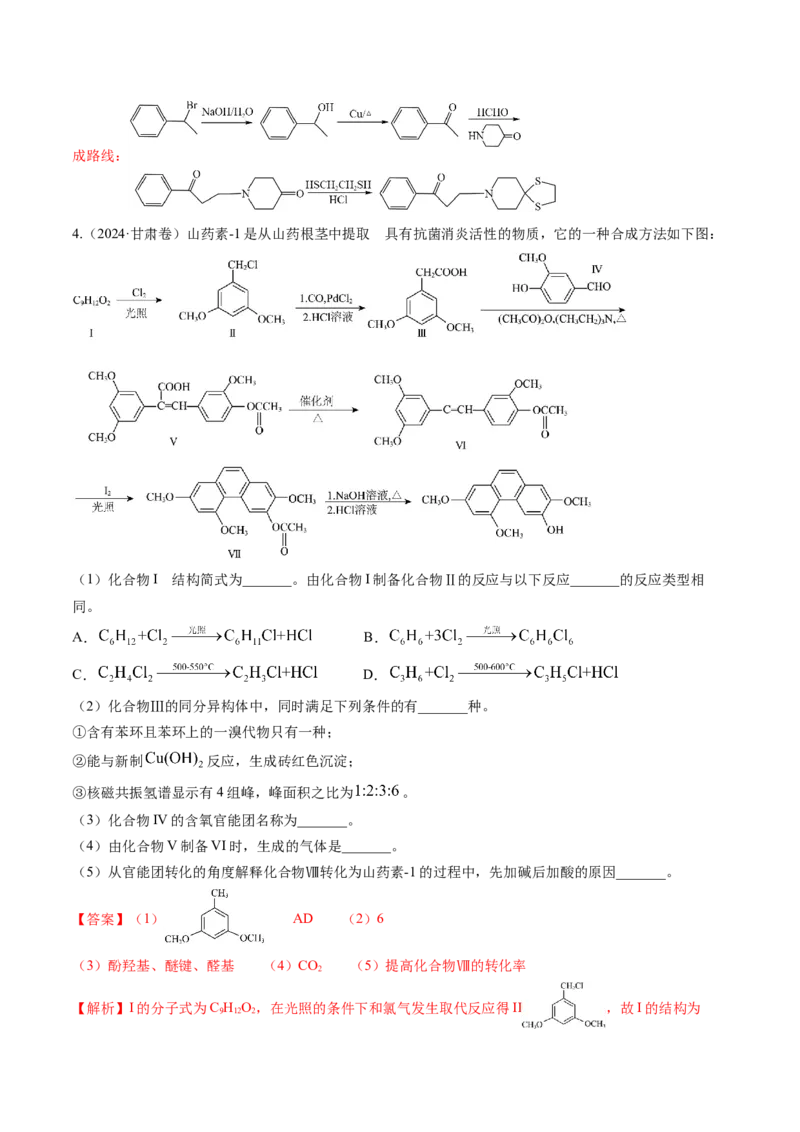
4.(2024·甘肃卷)山药素-1是从山药根茎中提取 的具有抗菌消炎活性的物质,它的一种合成方法如下图:
(1)化合物I 的结构简式为_______。由化合物I制备化合物Ⅱ的反应与以下反应_______的反应类型相
同。
A. B.
C. D.
(2)化合物Ⅲ的同分异构体中,同时满足下列条件的有_______种。
①含有苯环且苯环上的一溴代物只有一种;
②能与新制 反应,生成砖红色沉淀;
③核磁共振氢谱显示有4组峰,峰面积之比为 。
(3)化合物IV的含氧官能团名称为_______。
(4)由化合物V制备VI时,生成的气体是_______。
(5)从官能团转化的角度解释化合物Ⅷ转化为山药素-1的过程中,先加碱后加酸的原因_______。
【答案】(1) AD (2)6
(3)酚羟基、醚键、醛基 (4)CO (5)提高化合物Ⅷ的转化率
2
【解析】I的分子式为C H O,在光照的条件下和氯气发生取代反应得II ,故I的结构为
9 12 2;化合物V转化为化合物VI发生脱羧反应,有CO 生成;
2
(1)由分析,I的结构简式为 ,由化合物I制备化合物Ⅱ的反应类型为取代反应,A、D
都是烃与氯气发生取代反应,B是苯在光照条件下和氯气发生加成反应,C是C HCl 发生消去反应,故选
2 4 2
AD;
(2)化合物Ⅲ为 ,分子式C H O,同时满足下列条件:①含有苯环且苯环上的一溴代
10 12 4
物只有一种,说明苯环上只有一种化学环境的氢原子;②能与新制Cu(OH) 反应,生成砖红色沉淀,说明
2
有醛基,根据分子式,不饱和度为5,除去苯环的不饱和度,只有一个醛基;③核磁共振氢谱显示有4组
峰,峰面积之比为1:2:3:6,说明分子中有4种不同化学环境的氢原子,数目分别为1、2、3、6,故满足条
件的同分异构体有: 、 、 、 、
、 ,共6种;
(3)化合物IV的结构为 ,其中含氧官能团的名称为酚羟基、醚键、醛基;
(4)对比化合物V和化合物VI的结构,化合物VI比化合物V少一个碳原子两个氧原子,由化合物V制
备VI时,生成的气体是CO;
2
(5)化合物Ⅷ转化为山药素-1的过程发生的是酯基水解,酯在碱性条件下水解更彻底,再加入酸将酚羟
基的盐转化为酚羟基得目标产物山药素-1,若直接加酸,由于酯在酸性条件下的水解可逆,产率较低,故
先加碱后加酸是为了提高化合物Ⅷ的转化率。
5.(2024·广东卷)将3D打印制备的固载铜离子陶瓷催化材料,用于化学催化和生物催化一体化技术,以
实现化合物Ⅲ的绿色合成,示意图如下(反应条件路)。
(1)化合物I的分子式为_______,名称为_______。
(2)化合物Ⅱ中含氧官能团的名称是_______。化合物Ⅱ的某同分异构体含有苯环,在核磁共振氢谱图上
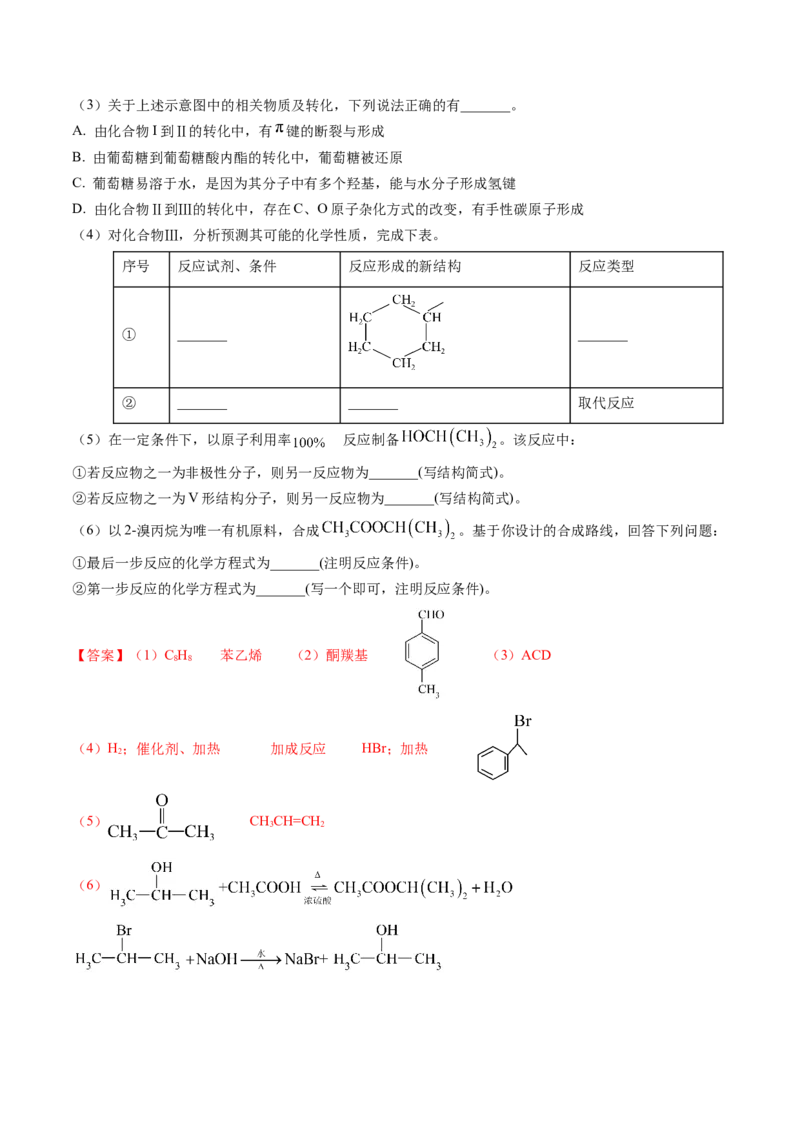
只有4组峰,且能够发生银镜反应,其结构简式为_______。(3)关于上述示意图中的相关物质及转化,下列说法正确的有_______。
A. 由化合物I到Ⅱ的转化中,有 键的断裂与形成
B. 由葡萄糖到葡萄糖酸内酯的转化中,葡萄糖被还原
C. 葡萄糖易溶于水,是因为其分子中有多个羟基,能与水分子形成氢键
D. 由化合物Ⅱ到Ⅲ的转化中,存在C、O原子杂化方式的改变,有手性碳原子形成
(4)对化合物Ⅲ,分析预测其可能的化学性质,完成下表。
序号 反应试剂、条件 反应形成的新结构 反应类型
① _______ _______
② _______ _______ 取代反应
(5)在一定条件下,以原子利用率 的反应制备 。该反应中:
①若反应物之一为非极性分子,则另一反应物为_______(写结构简式)。
②若反应物之一为V形结构分子,则另一反应物为_______(写结构简式)。
(6)以2-溴丙烷为唯一有机原料,合成 。基于你设计的合成路线,回答下列问题:
①最后一步反应的化学方程式为_______(注明反应条件)。
②第一步反应的化学方程式为_______(写一个即可,注明反应条件)。
【答案】(1)C H 苯乙烯 (2)酮羰基 (3)ACD
8 8
(4)H;催化剂、加热 加成反应 HBr;加热
2
(5) CHCH=CH
3 2
(6)(或 )
【分析】苯乙烯的碳碳双键先与水加成得到 , 上的羟基发生催化氧化得到
Ⅱ,Ⅰ转化为Ⅱ的本质是苯乙烯被O 氧化为 ,Ⅱ转化为Ⅲ的本质是 被葡萄糖
2
还原为 。
【解析】(1)由I的结构可知,其分子式为C H;名称为:苯乙烯;
8 8
(2)由Ⅱ的结构可知,其含氧官能团为:酮羰基;化合物Ⅱ的某同分异构体含有苯环,在核磁共振氢谱
图上只有4组峰,且能够发生银镜反应,即具有4种等效氢,含有醛基,符合条件的结构简式为:
;
(3)由化合物I到Ⅱ的转化中,I的碳碳双键先与水加成得到 , 上的羟基催化氧化得到
Ⅱ,有π键的断裂与形成,故A正确;葡萄糖为HOCH -(CHOH)CHO,被氧化为葡萄糖酸:HOCH -
2 4 2
(CHOH)COOH,葡萄糖酸中的羧基和羟基发生酯化反应生成葡萄糖酸内脂,由该过程可知,葡萄糖被
4
氧化,故B错误;葡萄糖为HOCH -(CHOH)CHO,有多个羟基,能与水分子形成氢键,使得葡萄糖易
2 4
溶于水,故C正确;化合物Ⅱ 图中所示C为sp2杂化,转化为Ⅲ 图中所示C
为sp3杂化,C原子杂化方式改变,且该C为手性碳原子,O的杂化方式由sp2转化为sp3,故D正确;故选
ACD;
(4)①由Ⅲ的结构可知,Ⅲ中的苯环与H 加成可得新结构 ,反应试剂、条件为:H,催
2 2
化剂、加热,反应类型为加成反应;②Ⅲ可发生多种取代反应,如:Ⅲ与HBr在加热的条件下羟基被Br取代,反应试剂、条件为:HBr,加热,反应形成新结构 ,(其他合理答案也可);
(5)原子利用率 的反应制备 ,反应类型应为加成反应,
①若反应物之一为非极性分子,该物质应为H,即该反应为 与H 加成;
2 2
若反应物之一为V形结构分子,该物质应为HO,即该反应为CHCH=CH 与HO加成;
2 3 2 2
(6) 与NaOH水溶液在加热条件下反应得到 , 与
NaOH醇溶液在加热条件下反应得到CHCH=CH,CHCH=CH 被酸性高锰酸钾溶液氧化为CHCOOH,
3 2 3 2 3
和CHCOOH在浓硫酸作催化剂,加热的条件下发生酯化反应生成
3
,具体合成路线为:
。
①最后一步为 和CHCOOH在浓硫酸作催化剂,加热的条件下发生酯化反应生成
3
,反应化学方程式为:
;
②第一步的化学方程式为: 或
。
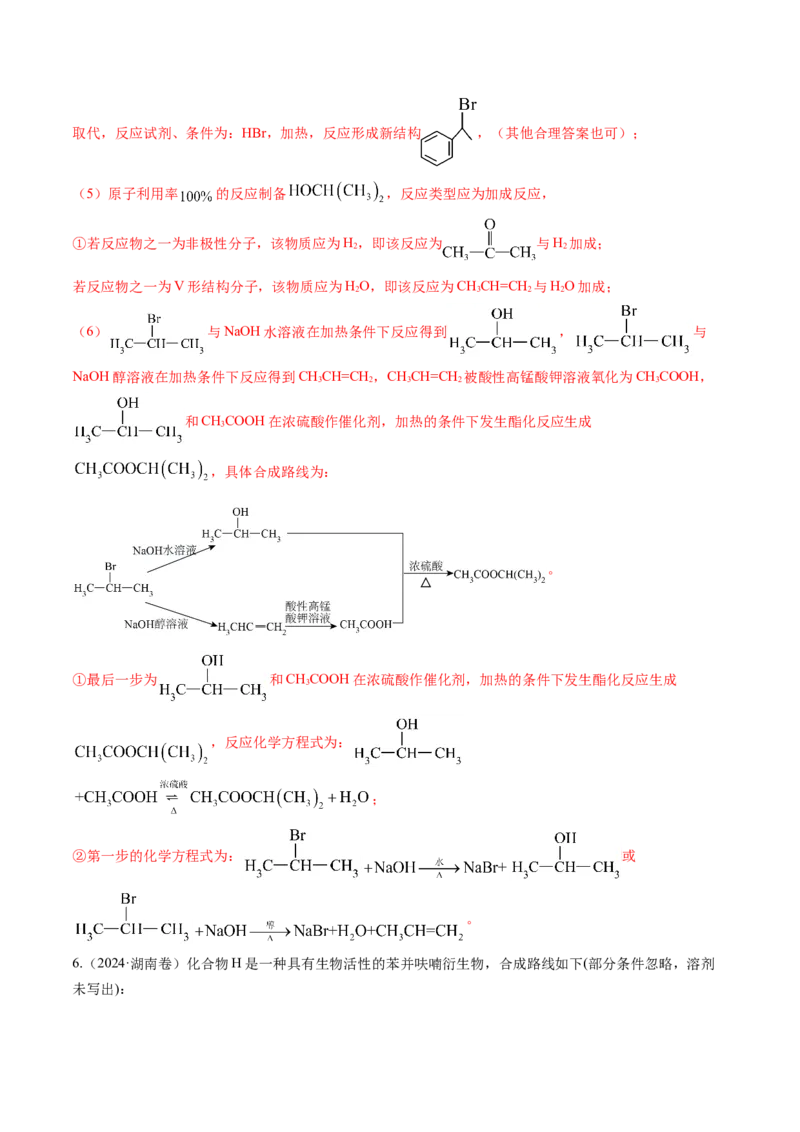
6.(2024·湖南卷)化合物H是一种具有生物活性的苯并呋喃衍生物,合成路线如下(部分条件忽略,溶剂
未写出):回答下列问题:
(1)化合物A在核磁共振氢谱上有_______组吸收峰;
(2)化合物D中含氧官能团的名称为_______、_______;
(3)反应③和④的顺序不能对换的原因是_______;
(4)在同一条件下,下列化合物水解反应速率由大到小的顺序为_______(填标号);
① ② ③
(5)化合物 的合成过程中,经历了取代、加成和消去三步反应,其中加成反应的化学方程式为
_______;
(6)依据以上流程信息,结合所学知识,设计以 和 为原料合成
的路线_______(HCN等无机试剂任选)。
【答案】(1)6 (2)醛基 醚键 (3)先进行反应③再进行反应④可以防止酚羟基被氧化
(4)①③② (5) ;
(6)
【解析】A与氯化剂在加热条件下反应得到B,B在BBr ,0℃的条件下,甲基被H取代得到C,C与
3
CHBrCHBr在KCO 的作用下发生取代反应得到D,D被氧化剂氧化为E,E中存在酯基,先水解,再酸
2 2 2 3
化得到F,F与ClCHOCH 在TiCl 的作用下苯环上一个H被醛基取代得到G,G与ClCH COCH 经历了取
2 3 4 2 3代、加成和消去三步反应得到H。
(1)由A的结构可知,A有6种等效氢,即核磁共振氢谱上有6组吸收峰;
(2)由D的结构可知,化合物D中含氧官能团的名称为:醛基、醚键;
(3)反应③和④的顺序不能对换,先进行反应③再进行反应④可以防止酚羟基被氧化;
(4) 中F的电负性很强,-CF 为吸电子基团,使得-OOCH中C-O键更易断裂,水解反应更
3
易进行, 中-CH 是斥电子集团,使得-OOCH中C-O键更难断裂,水解反应更难进行,因此
3
在同一条件下,化合物水解反应速率由大到小的顺序为:①③②;
(5)化合物G→H的合成过程中,G发生取代反应羟基上的H被-CHCOCH 取代,得到 ,
2 3
中的醛基加成得到 , 中的羟基发生消去反应得到 ,其
中加成反应的化学方程式为: ;
(6) 和ClCHOCH 在TiCl 的作用下发生类似反应⑥的反应得到 , 与HCN加成得到
2 3 4
, 酸性水解得到 , 发生缩聚反应得到 ,
具体合成路线为: 。
7.(2023·广东卷)室温下可见光催化合成技术,对于人工模仿自然界、发展有机合成新方法意义重大。一
种基于CO、碘代烃类等,合成化合物ⅶ的路线如下(加料顺序、反应条件略):
(1)化合物i的分子式为___________。化合物x为i的同分异构体,且在核磁共振氢谱上只有2组峰。x
的结构简式为___________(写一种),其名称为___________。
(2)反应②中,化合物ⅲ与无色无味气体y反应,生成化合物ⅳ,原子利用率为100%。y为___________。
(3)根据化合物V的结构特征,分析预测其可能的化学性质,完成下表。
反应试剂、条
序号 反应形成的新结构 反应类型
件
a ___________ ___________ 消去反应
b ___________ ___________ 氧化反应(生成有机产物)
(4)关于反应⑤的说法中,不正确的有___________。
A. 反应过程中,有 键和 键断裂
B. 反应过程中,有 双键和 单键形成
C. 反应物i中,氧原子采取 杂化,并且存在手性碳原子
D. 属于极性分子,分子中存在由p轨道“头碰头”形成的 键
(5)以苯、乙烯和 为含碳原料,利用反应③和⑤的原理,合成化合物ⅷ。
基于你设计的合成路线,回答下列问题:
(a)最后一步反应中,有机反应物为___________(写结构简式)。
(b)相关步骤涉及到烯烃制醇反应,其化学方程式为___________。
(c)从苯出发,第一步的化学方程式为___________(注明反应条件)。
【答案】(1) C H O (或 或 ) 3-戊酮(或2,2-二甲基丙醛或
5 10
3,3-二甲基氧杂环丁烷) (2)O 或氧气
2
(3) 浓硫酸,加热 O、Cu,加热(或酸性KMnO 溶液)
2 4
(或 ) (4)CD
(5) 和CHCHOH
3 2【解析】 与HBr加热发生取代反应生成 ,②乙烯在催化剂作用下氧化生成
,③ 与 发生开环加成生成 ,④ 发生取代反应生成
,⑤ 与 及CO反应生成 。
(1)化合物i 的分子式为C H O。 不饱和度为1,x可形成碳碳双键或碳氧双键或
5 10
一个圆环,化合物x为i的同分异构体,且在核磁共振氢谱上只有2组峰,说明分子中有对称结构,不对称
的部分放在对称轴上,x的结构简式含酮羰基时为 (或含醛基时为 或含圆环是为
),其名称为3-戊酮(或2,2-二甲基丙醛或3,3-二甲基氧杂环丁烷)。
(2)反应②中,化合物ⅲ与无色无味气体y反应,生成化合物ⅳ,原子利用率为100%,②乙烯在催化剂
作用下氧化生成 ,y为O 或氧气。
2
(3)根据化合物V 的结构特征,分析预测其可能的化学性质:含有羟基,且与羟基相连
的碳的邻碳上有氢,可在浓硫酸、加热条件下发生消去反应生成 ,与羟基相连的碳上有氢,可
在铜或银催化作用下氧化生成 ,或酸性KMnO 溶液中氧化生成 ,见下
4
表:
序号 反应试剂、条件 反应形成的新结构 反应类型
a 浓硫酸,加热 消去反应
O、Cu,,加热
2
氧化反应(生成有机产
b (或酸性KMnO 溶 (或 )
4
物)
液)
(4)从产物中不存在C-I键和H-O键可以看出,反应过程中,有C-I键和H-O键断裂,故A正确;反应物
中不存在CCOO双键,酰碘基中碘原子离去与羟基中氢离去,余下的部分结合形成酯基中C-O单键,所以反应过程中,有C=O双键和C-O单键形成,故B正确;反应物i 中,氧原子采取sp3杂化,但
与羟基相连的碳有对称轴,其它碳上均有2个氢,分子中不存在手性碳原子,故C错误;CO属于极性分
子,分子中存在由p轨道“肩并肩”形成的π键,故D错误;故答案为CD;
(5)以苯、乙烯和CO为含碳原料,利用反应③和⑤的原理,合成化合物ⅷ。乙烯与水在催化剂加热加压
条件下合成乙醇;乙烯在银催化作用下氧化生成环氧乙醚;苯在铁催化作用下与溴生成溴苯,溴苯与环氧
乙醚生成 ,与HI反应合成 ,最后根据反应⑤的原理, 与乙
醇、CO合成化合物ⅷ。(a)最后一步反应中,有机反应物为 和CHCHOH。 (b)相关步骤
3 2
涉及到烯烃制醇反应,其化学方程式为 。 (c)从苯出发,第一
步的化学方程式为 。
8.(2023·湖北卷)碳骨架的构建是有机合成的重要任务之一。某同学从基础化工原料乙烯出发,针对二酮
H设计了如下合成路线:
回答下列问题:
(1)由A→B的反应中,乙烯的碳碳_______键断裂(填“π”或“σ”)。
(2)D的同分异构体中,与其具有相同官能团的有_______种(不考虑对映异构),其中核磁共振氢谱有三
组峰,峰面积之比为 的结构简式为_______。
(3)E与足量酸性 溶液反应生成的有机物的名称为_______、_______。
(4)G的结构简式为_______。
(5)已知: ,H在碱性溶液中易发生分子内缩合从而构建双环结构,主要产物为I( )和另一种α,β-不饱和酮J,J的结构简式为_______。若经此路线由H
合成I,存在的问题有_______(填标号)。
a.原子利用率低 b.产物难以分离 c.反应条件苛刻 d.严重污染环境
【答案】(1)π (2)7 (3)乙酸 丙酮
(4) (5) ab
【解析】A为CH=CH ,与HBr发生加成反应生成B(CHCHBr),B与Mg在无水乙醚中发生生成C
2 2 3 2
(CHCHMgBr),C与CHCOCH 反应生成D( ),D在氧化铝催化下发生消去反应生成E
3 2 3 3
( ),E和碱性高锰酸钾反应生成F( ),参考D~E反应,F在氧化铝催化
下发生消去反应生成G( ),G与 反应加成反应生成二酮H,据此分析解答。
(1)A为CH=CH ,与HBr发生加成反应生成B(CHCHBr),乙烯的π键断裂;
2 2 3 2
(2)D为 ,分子式为C H O,含有羟基的同分异构体分别为:
5 12
共8种,除去D自身,还有7种同分
异构体,其中核磁共振氢谱有三组峰,峰面积之比为9:2:1的结构简式为 ;
(3)E为 ,酸性高锰酸钾可以将双键氧化断开,生成 和 ,名称分别为乙
酸和丙酮;(4)由分析可知,G为 ;
(5)根据已知 的反应特征可知,H在碱性溶液中易发生分子内缩
合从而构建双环结构,主要产物为I( ))和J( )。若经此路线由H合成I,会同时
产生两种同分异构体,导致原子利用率低,产物难以分离等问题。
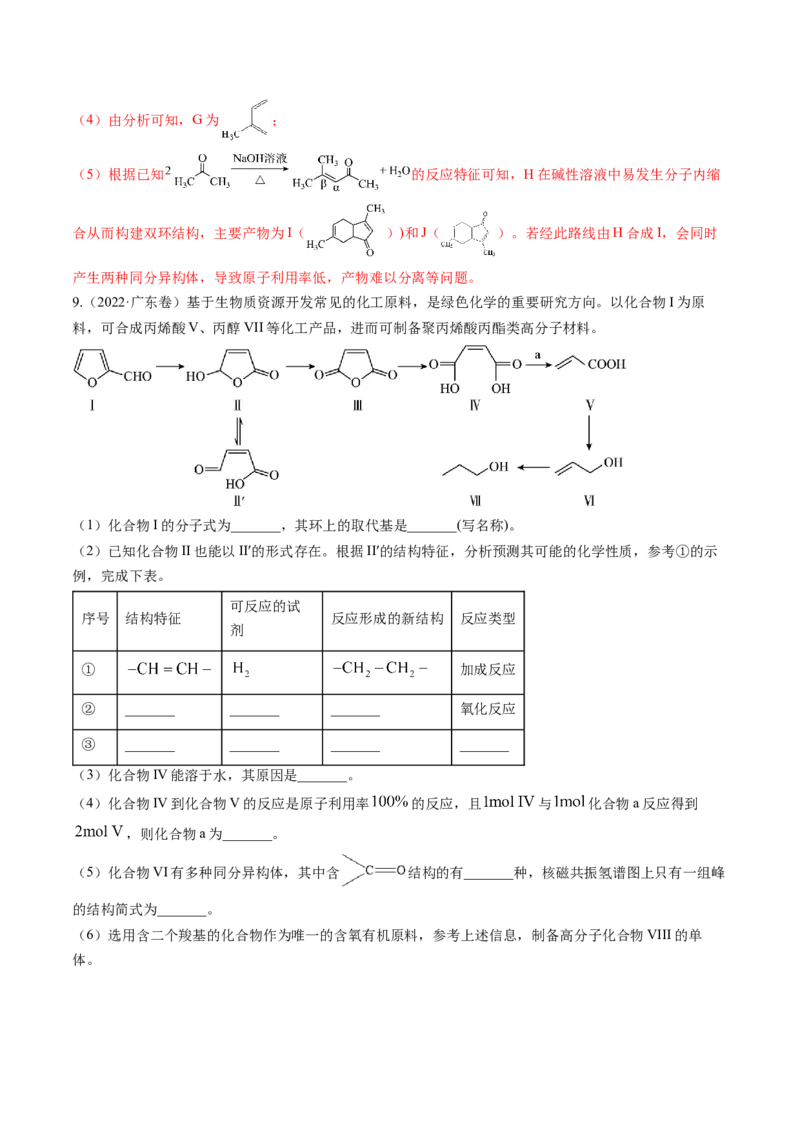
9.(2022·广东卷)基于生物质资源开发常见的化工原料,是绿色化学的重要研究方向。以化合物I为原
料,可合成丙烯酸V、丙醇VII等化工产品,进而可制备聚丙烯酸丙酯类高分子材料。
(1)化合物I的分子式为_______,其环上的取代基是_______(写名称)。
(2)已知化合物II也能以II′的形式存在。根据II′的结构特征,分析预测其可能的化学性质,参考①的示
例,完成下表。
可反应的试
序号 结构特征 反应形成的新结构 反应类型
剂
① 加成反应
② _______ _______ _______ 氧化反应
③ _______ _______ _______ _______
(3)化合物IV能溶于水,其原因是_______。
(4)化合物IV到化合物V的反应是原子利用率 的反应,且 与 化合物a反应得到
,则化合物a为_______。
(5)化合物VI有多种同分异构体,其中含 结构的有_______种,核磁共振氢谱图上只有一组峰
的结构简式为_______。
(6)选用含二个羧基的化合物作为唯一的含氧有机原料,参考上述信息,制备高分子化合物VIII的单
体。写出VIII的单体的合成路线_______(不用注明反应条件)。
【答案】(1)C HO 醛基
5 4 2
(2) ② -CHO O -COOH ③ -COOH CH OH - COOCH 酯化反应(取代反应)
2 3 3
(3)Ⅳ中羟基能与水分子形成分子间氢键
(4)乙烯 (5)2
(6)
【解析】(1)根据化合物Ⅰ的结构简式可知,其分子式为C HO;其环上的取代基为醛基,故答案为:
5 4 2
C HO;醛基;
5 4 2
(2)②化合物Ⅱ'中含有的-CHO可以被氧化为-COOH,故答案为:-CHO;O;-COOH;
2
③化合物Ⅱ'中含有-COOH,可与含有羟基的物质(如甲醇)发生酯化反应生成酯,故答案为:-COOH;
CHOH;- COOCH ;酯化反应(取代反应);
3 3
(3)化合物Ⅳ中含有羟基,能与水分子形成分子间氢键,使其能溶于水,故答案为:Ⅳ中羟基能与水分
子形成分子间氢键;
(4)化合物Ⅳ到化合物Ⅴ的反应是原子利用率100%的反应,且1 molⅣ与1 mola反应得到2molV,则a
的分子式为C H,为乙烯,故答案为:乙烯;
2 4
(5)化合物Ⅵ的分子式为C HO,其同分异构体中含有 ,则符合条件的同分异构体有
3 6
和 ,共2种,其中核磁共振氢谱中只有一组峰的结构简式为 ;
(6)根据化合物Ⅷ的结构简式可知,其单体为 ,其原料中的含氧有机物只有一种含二个羧
基的化合物,原料可以是 , 发生题干Ⅳ→V的反应得到 , 还原
为 ,再加成得到 , 和 发生酯化反应得到目标产物,则合成路线为。