文档内容
考点 3 电解池 金属的腐蚀与防护
1.3年真题考点分布
考点分布
年份 卷区
电解池原理 电解池的应用 金属的腐蚀与防护 综合应用
广东 √ √
湖北 √ √
湖南 √
2023
辽宁 √ √
浙江 √ √
北京 √
广东 √ √
海南 √
2022
湖南 √
山东 √
浙江 √ √
广东 √
海南 √ √
2021
湖北 √ √
辽宁 √
2.命题规律及备考策略
【命题规律】近3年新高考卷对于该专题主要考查:
①电解池的工作原理及其应用;
②金属腐蚀与防护;
③电化学计算及综合应用。
【备考策略】电化学类试题主要考查电解池的工作原理及其应用,意在考查考生的变化观念与平衡思想、证据
推理与模型认知的学科素养,及信息获取、理解掌握和知识整合的学科关键能力。
【命题预测】能分析、解释电解池的工作原理,利用电化学原理解释金属腐蚀现象,选择并设计防腐措施。
考法 1 电解池原理及其应用
一、电解的原理
1.电解和电解池
(1)电解:在电流作用下,电解质在两个电极上分别发生氧化反应和还原反应的过程。(2)电解池:电能转化为化学能的装置。
(3)电解池的构成
①有与电源相连的两个电极。
②电解质溶液(或熔融电解质)。
③形成闭合回路。
2.电解池的工作原理
(1)电极名称及电极反应式(电解CuCl 溶液为例)
2
总反应式:CuCl =====Cu+Cl↑
2 2
(2)电子和离子的移动方向
①电子:从电源负极流出后,流向电解池阴极;从电解池的阳极流出后流向电源的正极。
②离子:阳离子移向电解池的阴极,阴离子移向电解池的阳极。
3.阴阳两极上放电顺序
(1)阴极:(与电极材料无关)。氧化性强的先放电,放电顺序:
(2)阳极:若是活性电极作阳极,则活性电极首先失电子,发生氧化反应。
若是惰性电极作阳极,放电顺序为
【特别提醒】①阴极不管是什么材料,电极本身都不反应,一定是溶液(或熔融电解质)中的阳离子放电。②最
常用、最重要的放电顺序为阳极:Cl->OH-;阴极:Ag+>Cu2+>H+。③电解水溶液时,K+~Al3+不可能在阴极
放电,即不可能用电解水溶液的方法得到K、Ca、Na、Mg、Al等金属。
4.电解规律
(1)阳极放电规律
①活性电极(除Au、Pt以外的金属材料作电极),电极材料失电子,生成金属阳离子。
②惰性电极(Pt、Au、石墨),要依据阴离子的放电顺序加以判断。
阴离子的放电顺序:S2->I->Br->Cl->OH->含氧酸根离子。
S2-、I-、Br-、Cl-放电,产物分别是S、I、Br 、Cl;若OH-放电,则得到HO和O。
2 2 2 2 2
(2)阴极产物的判断
直接根据阳离子放电顺序进行判断。阳离子放电顺序:Ag+>Fe3+>Cu2+>H+(酸)>Fe2+>Zn2+>H+(水)>Al3+>Mg2+。
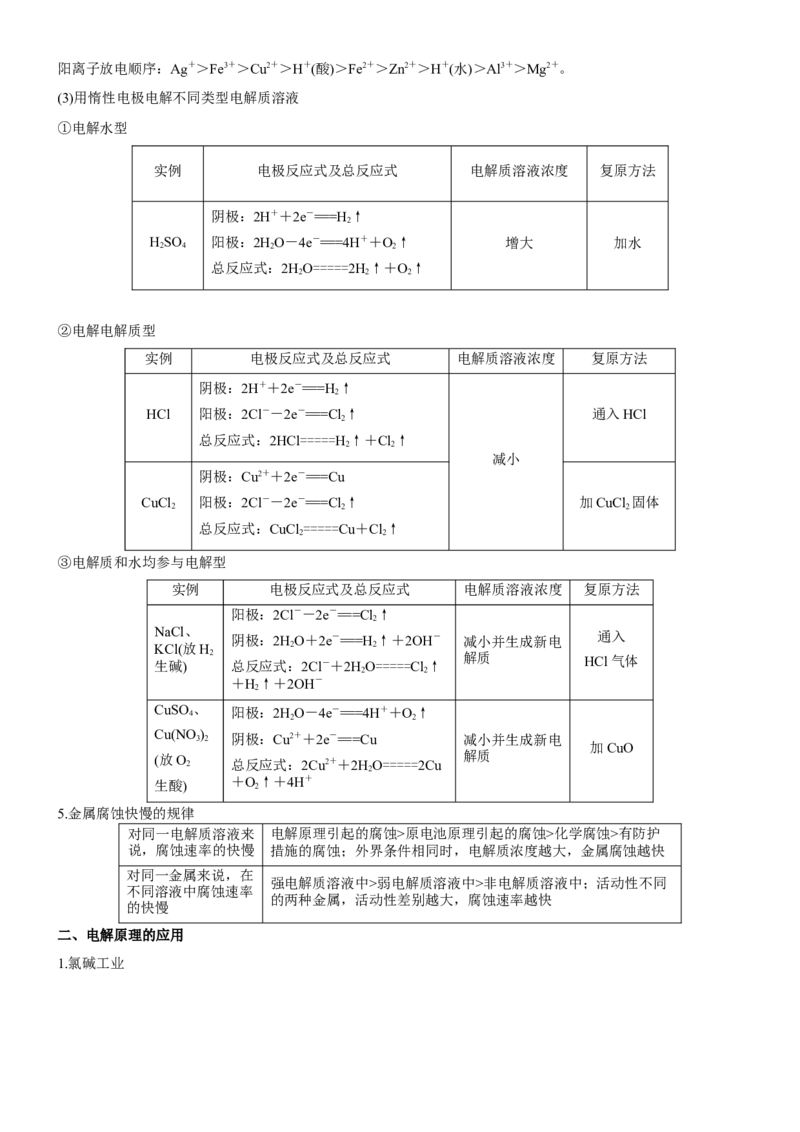
(3)用惰性电极电解不同类型电解质溶液
①电解水型
实例 电极反应式及总反应式 电解质溶液浓度 复原方法
阴极:2H++2e-===H↑
2
HSO 阳极:2HO-4e-===4H++O↑ 增大 加水
2 4 2 2
总反应式:2HO=====2H↑+O↑
2 2 2
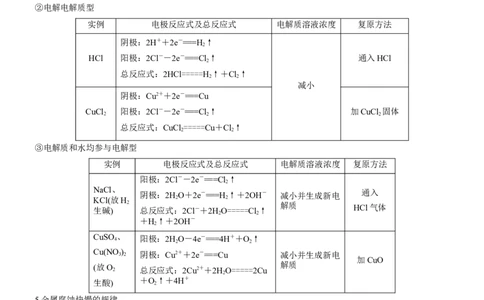
②电解电解质型
实例 电极反应式及总反应式 电解质溶液浓度 复原方法
阴极:2H++2e-===H↑
2
HCl 阳极:2Cl--2e-===Cl↑ 通入HCl
2
总反应式:2HCl=====H↑+Cl↑
2 2
减小
阴极:Cu2++2e-===Cu
CuCl 阳极:2Cl--2e-===Cl↑ 加CuCl 固体
2 2 2
总反应式:CuCl =====Cu+Cl↑
2 2
③电解质和水均参与电解型
实例 电极反应式及总反应式 电解质溶液浓度 复原方法
阳极:2Cl--2e-===Cl↑
2
NaCl、
阴极:2HO+2e-===H↑+2OH- 减小并生成新电 通入
KCl(放H 2 2
生碱)
2
总反应式:2Cl-+2HO=====Cl↑
解质 HCl气体
2 2
+H↑+2OH-
2
CuSO 4 、 阳极:2H 2 O-4e-===4H++O 2 ↑
Cu(NO 3 ) 2 阴极:Cu2++2e-===Cu 减小并生成新电
加CuO
(放O
2 总反应式:2Cu2++2HO=====2Cu
解质
2
生酸) +O 2 ↑+4H+
5.金属腐蚀快慢的规律
对同一电解质溶液来 电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护
说,腐蚀速率的快慢 措施的腐蚀;外界条件相同时,电解质浓度越大,金属腐蚀越快
对同一金属来说,在
强电解质溶液中>弱电解质溶液中>非电解质溶液中;活动性不同
不同溶液中腐蚀速率
的两种金属,活动性差别越大,腐蚀速率越快
的快慢
二、电解原理的应用
1.氯碱工业阳极反应式:2Cl--2e-===Cl ↑(氧化反应)
2
阴极反应式:2H++2e-===H↑(还原反应)
2
总反应方程式:
2NaCl+2HO=====2NaOH+H↑+Cl↑
2 2 2
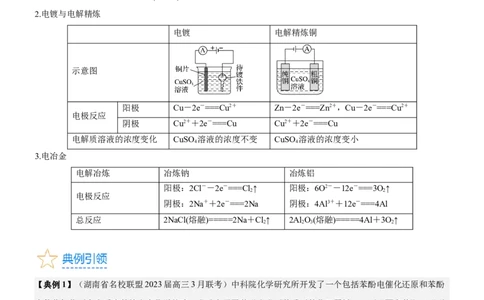
2.电镀与电解精炼
电镀 电解精炼铜
示意图
阳极 Cu-2e-===Cu2+ Zn-2e-===Zn2+,Cu-2e-===Cu2+
电极反应
阴极 Cu2++2e-===Cu Cu2++2e-===Cu
电解质溶液的浓度变化 CuSO 溶液的浓度不变 CuSO 溶液的浓度变小
4 4
3.电冶金
电解冶炼 冶炼钠 冶炼铝
阳极:2Cl--2e-===Cl ↑ 阳极:6O2--12e-===3O↑
2 2
电极反应
阴极:2Na++2e-===2Na 阴极:4Al3++12e-===4Al
总反应 2NaCl(熔融)=====2Na+Cl↑ 2Al O(熔融)=====4Al+3O↑
2 2 3 2
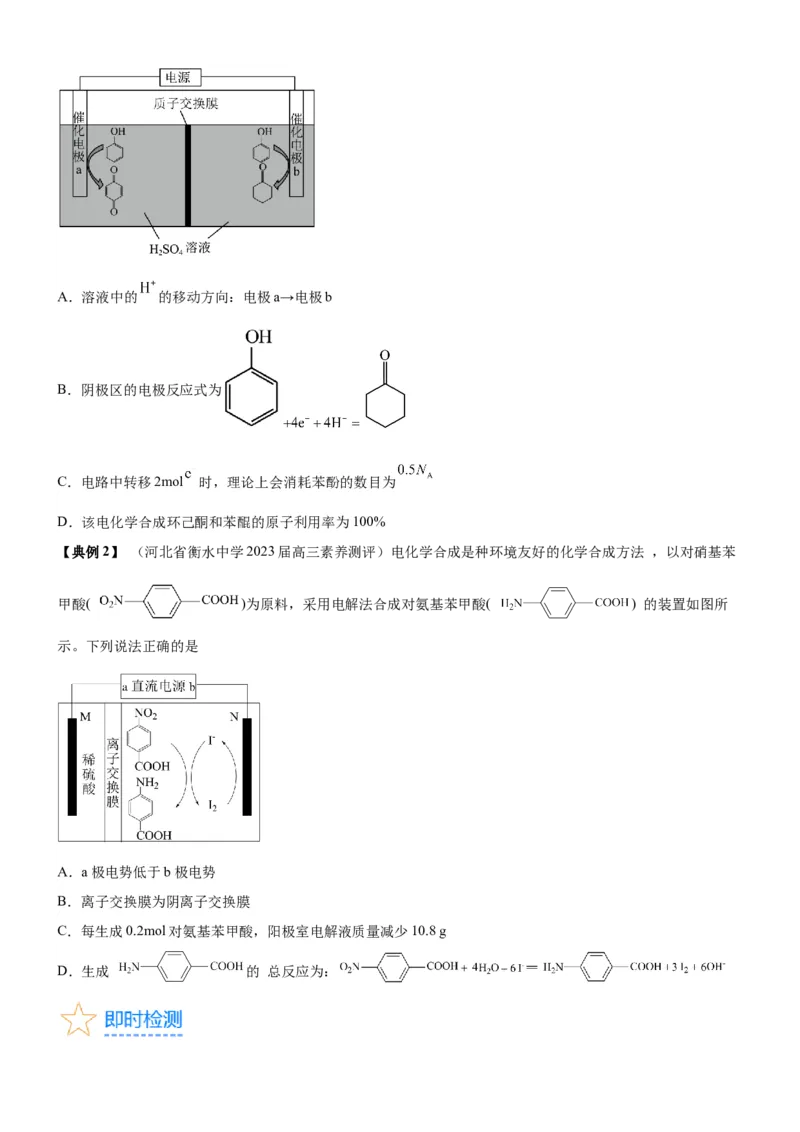
【典例1】(湖南省名校联盟2023届高三3月联考)中科院化学研究所开发了一个包括苯酚电催化还原和苯酚
电催化氧化两个半反应的综合电化学策略,成功实现了苯酚合成两种重要的化工原料——环己酮和苯醌。下列
说法错误的是A.溶液中的 的移动方向:电极a→电极b
B.阴极区的电极反应式为
C.电路中转移2mol 时,理论上会消耗苯酚的数目为
D.该电化学合成环己酮和苯醌的原子利用率为100%
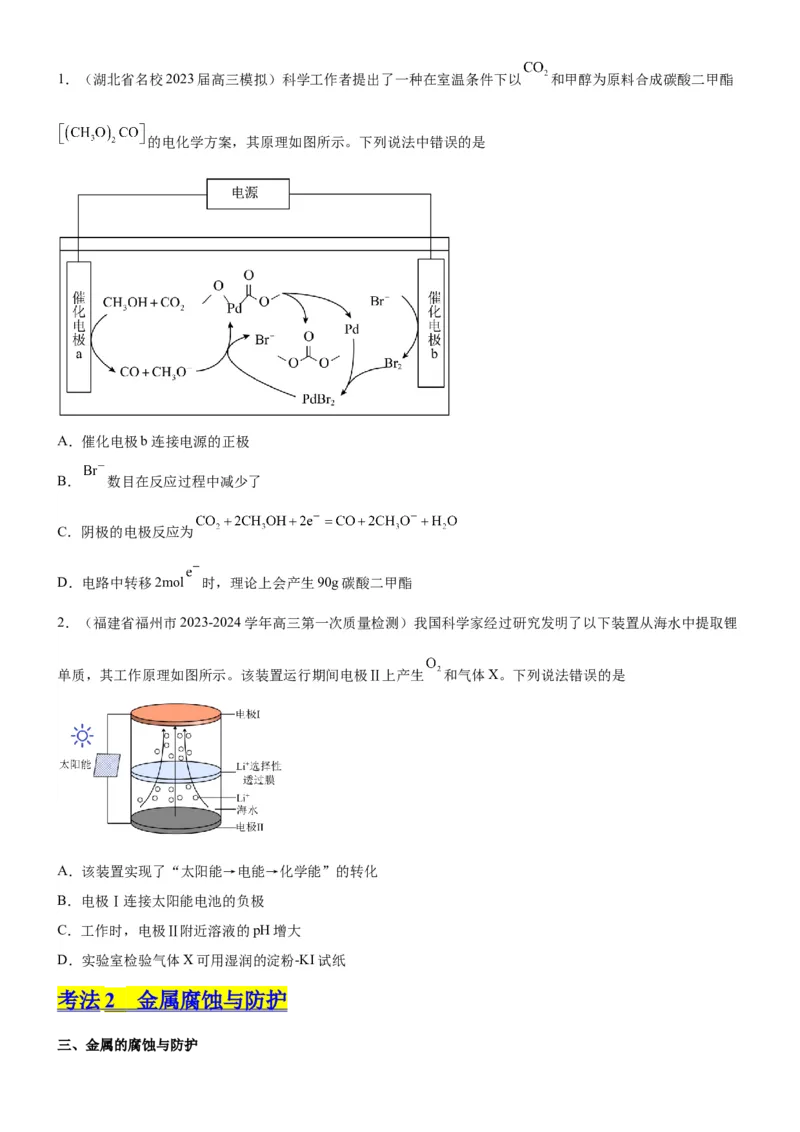
【典例2】 (河北省衡水中学2023届高三素养测评)电化学合成是种环境友好的化学合成方法 ,以对硝基苯
甲酸( )为原料,采用电解法合成对氨基苯甲酸( ) 的装置如图所
示。下列说法正确的是
A.a极电势低于b极电势
B.离子交换膜为阴离子交换膜
C.每生成0.2mol对氨基苯甲酸,阳极室电解液质量减少10.8 g
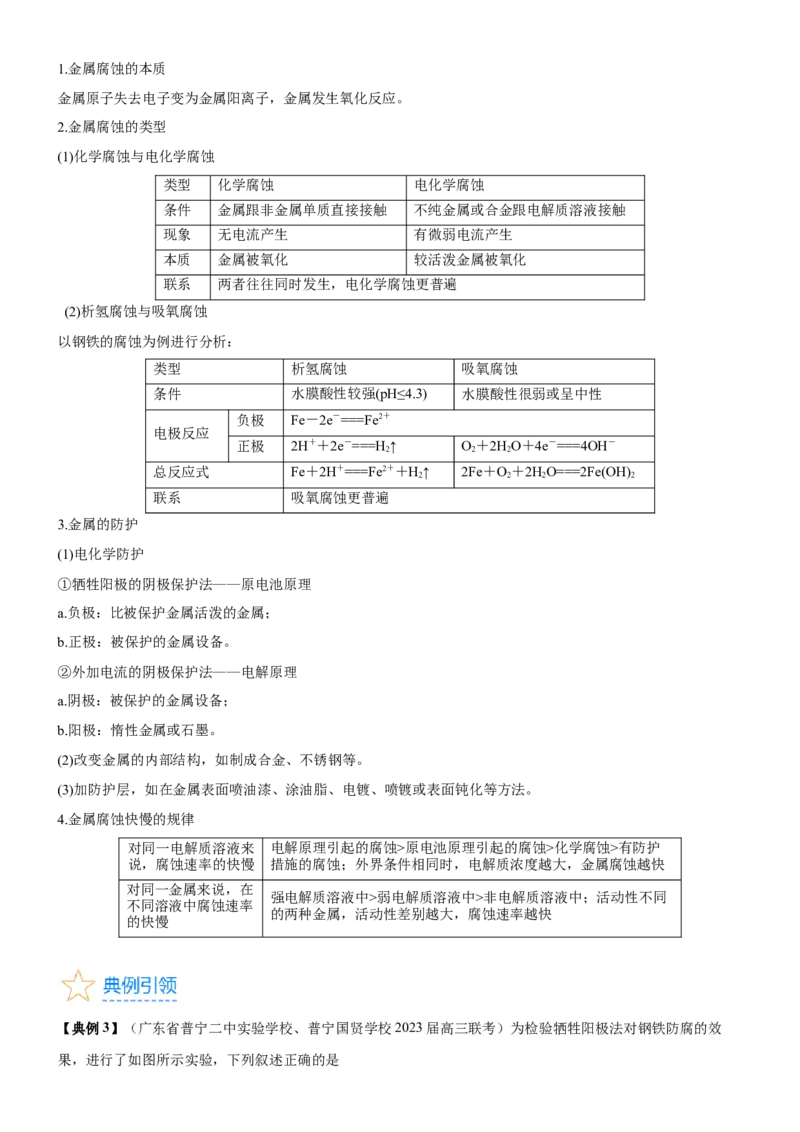
D.生成 的 总反应为:1.(湖北省名校2023届高三模拟)科学工作者提出了一种在室温条件下以 和甲醇为原料合成碳酸二甲酯
的电化学方案,其原理如图所示。下列说法中错误的是
A.催化电极b连接电源的正极
B. 数目在反应过程中减少了
C.阴极的电极反应为
D.电路中转移2mol 时,理论上会产生90g碳酸二甲酯
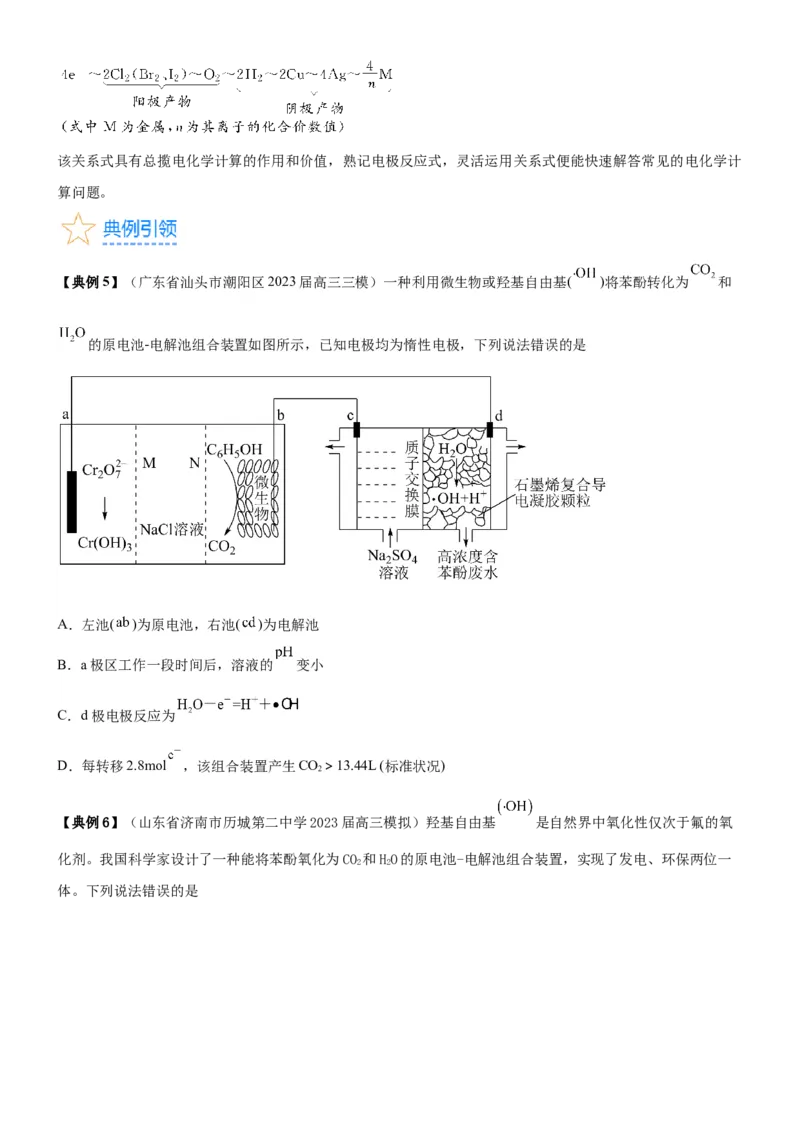
2.(福建省福州市2023-2024学年高三第一次质量检测)我国科学家经过研究发明了以下装置从海水中提取锂
单质,其工作原理如图所示。该装置运行期间电极Ⅱ上产生 和气体X。下列说法错误的是
A.该装置实现了“太阳能→电能→化学能”的转化
B.电极Ⅰ连接太阳能电池的负极
C.工作时,电极Ⅱ附近溶液的pH增大
D.实验室检验气体X可用湿润的淀粉-KI试纸
考法 2 金属腐蚀与防护
三、金属的腐蚀与防护1.金属腐蚀的本质
金属原子失去电子变为金属阳离子,金属发生氧化反应。
2.金属腐蚀的类型
(1)化学腐蚀与电化学腐蚀
类型 化学腐蚀 电化学腐蚀
条件 金属跟非金属单质直接接触 不纯金属或合金跟电解质溶液接触
现象 无电流产生 有微弱电流产生
本质 金属被氧化 较活泼金属被氧化
联系 两者往往同时发生,电化学腐蚀更普遍
(2)析氢腐蚀与吸氧腐蚀
以钢铁的腐蚀为例进行分析:
类型 析氢腐蚀 吸氧腐蚀
条件 水膜酸性较强(pH≤4.3) 水膜酸性很弱或呈中性
负极 Fe-2e-===Fe2+
电极反应
正极 2H++2e-===H↑ O+2HO+4e-===4OH-
2 2 2
总反应式 Fe+2H+===Fe2++H↑ 2Fe+O+2HO===2Fe(OH)
2 2 2 2
联系 吸氧腐蚀更普遍
3.金属的防护
(1)电化学防护
①牺牲阳极的阴极保护法——原电池原理
a.负极:比被保护金属活泼的金属;
b.正极:被保护的金属设备。
②外加电流的阴极保护法——电解原理
a.阴极:被保护的金属设备;
b.阳极:惰性金属或石墨。
(2)改变金属的内部结构,如制成合金、不锈钢等。
(3)加防护层,如在金属表面喷油漆、涂油脂、电镀、喷镀或表面钝化等方法。
4.金属腐蚀快慢的规律
对同一电解质溶液来 电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护
说,腐蚀速率的快慢 措施的腐蚀;外界条件相同时,电解质浓度越大,金属腐蚀越快
对同一金属来说,在
强电解质溶液中>弱电解质溶液中>非电解质溶液中;活动性不同
不同溶液中腐蚀速率
的两种金属,活动性差别越大,腐蚀速率越快
的快慢
【典例3】(广东省普宁二中实验学校、普宁国贤学校2023届高三联考)为检验牺牲阳极法对钢铁防腐的效
果,进行了如图所示实验,下列叙述正确的是A.一段时间后,铁钉底部a、c处滤纸上均能看到出现蓝色沉淀
B.一段时间后,薄锌片底部b处能看到滤纸变红色
C.薄锌片两端铁钉均为该原电池的正极
D.薄锌片发生的电极反应式为
【典例4】(湖南省九校联盟2023届高三第二次联考)某同学利用如图所示装置探究金属的腐蚀与防护,下列
说法不正确的是
A.③区电极电势Cu高于Fe
B.①区Fe电极和③区Fe电极电极反应均为Fe—2e—=Fe2+
C.②区Zn电极和④区Cu电极电极反应均为2HO+2e—=H ↑+2OH—
2 2
D.②区Fe电极和④区Fe电极附近滴加K[Fe(CN) ]溶液,均会出现蓝色沉淀
3 6
1.(辽宁省名校联盟2023届高考模拟)“北溪”天然气管道至少泄漏8万吨天然气,近20年间甲烷的温室效
应率是 的84倍。已知管道接口处有钢铁材料等,海水的pH约为8.0。设 为阿伏伽德罗常数的值。下列
有关叙述不正确的是
A.损坏的钢铁材料在海水中主要发生吸氧腐蚀
B.制造管道时表面涂层能起到抗腐蚀作用
C. 铁在海水中完全发生电化学腐蚀时转移电子数一定为
D.修复管道时在钢管表面镶嵌锌块,这种方法叫牺牲阳极法2.(重庆市南开中学校2023届高三模拟)某同学利用下图所示装置探究金属的腐蚀与防护条件。
下列说法不合理的是
A.①区Cu电极上产生气泡,Fe电极附近滴加KFe(CN) 溶液后出现蓝色,Fe被腐蚀
3 6
B.②区Cu电极附近滴加酚酞后变成红色,Fe电极附近滴加K[Fe(CN) ]溶液出现蓝色,Fe被腐蚀
3 6
C.③区Zn电极的电极反应式为Zn-2e-=Zn2+,Fe电极附近滴加K[Fe(CN) ]溶液未出现蓝色,Fe被保护
3 6
D.④区Zn电极的电极反应式为2HO+2e-=H ↑+2OH-,Fe电极附近滴加K[Fe(CN) ]溶液出现蓝色,Fe被腐蚀
2 2 3 6
考法 3 电化学综合应用
四、电化学综合应用
1.电解池与原电池的比较
电解池 原电池
使“不能”变为“能”或使“能”
能否自发 能自发进行
变为“易”
能量转化 电能转化为化学能 化学能转化为电能
装置 有外加电源 无外加电源
由外加电源决定:
由电极或反应物性质决定,称为正
电极 阳极:连电源的正极;
极或负极
阴极:连电源的负极
反应 阳极:氧化反应; 负极:氧化反应;
类型 阴极:还原反应 正极:还原反应
阳离子移向阴极; 阳离子移向正极;
离子移动
阴离子移向阳极 阴离子移向负极
相同点 都是电极上的氧化还原反应,都必须有离子导体
2.电解计算中常用的方法
(1)根据总反应式计算
先写出电极反应式,再写出总反应式,最后根据总反应式列出比例式计算。
(2)根据得失电子守恒计算
①用于串联电路中阴阳两极产物、正负两极产物、相同电量等类型的计算,其依据是电路中转移的电子数相
等。
②用于混合溶液中电解的分阶段计算。
③根据得失电子守恒定律建立起已知量与未知量之间的桥梁,构建计算所需的关系式。
如以通过4 mol e-为桥梁可构建如下关系式:该关系式具有总揽电化学计算的作用和价值,熟记电极反应式,灵活运用关系式便能快速解答常见的电化学计
算问题。
【典例5】(广东省汕头市潮阳区2023届高三三模)一种利用微生物或羟基自由基( )将苯酚转化为 和
的原电池-电解池组合装置如图所示,已知电极均为惰性电极,下列说法错误的是
A.左池( )为原电池,右池( )为电解池
B.a极区工作一段时间后,溶液的 变小
C.d极电极反应为
D.每转移2.8mol ,该组合装置产生CO>13.44L (标准状况)
2
【典例6】(山东省济南市历城第二中学2023届高三模拟)羟基自由基 是自然界中氧化性仅次于氟的氧
化剂。我国科学家设计了一种能将苯酚氧化为CO 和HO的原电池-电解池组合装置,实现了发电、环保两位一
2 2
体。下列说法错误的是A.a极1 mol Cr O 参与反应,理论上NaCl溶液中减少的离子为12N
2 A
B.电池工作时,b极附近pH减小
C.右侧装置中,c、d两极产生气体的体积比(相同条件下)为7:3
D.d极区苯酚被氧化的化学方程式为
1.(重庆市育才中学校2023届高三冲刺)利用光伏电池与膜电解法制备Ce(SO) 溶液的装置如图所示。下列
4 2
说法正确的是
A.该光伏电池可将化学能转化为电能
B.该离子交换膜为阴离子交换膜,SO 由左池向右池迁移
C.电解池中阳极发生还原反应,电极反应式为Ce3+-e-=Ce4+
D.电路中有0.2mol电子通过时,阴极室溶液质量变化为16g
2.(江苏省南京市2023届高三模拟)磷及其化合物有着广泛的运用。白磷的结构为 ,溶于CS,
2
易自燃。其氧化物有PO、PO 。两种氧化物中均只有一种化学环境的P原子。P 与KOH溶液共热可制备
4 6 4 10 4
PH 。白磷与Cl 反应可生成PCl 和PCl 。固态PCl 中含有PCl 、PCl 两种离子。Ca(HPO ) 是磷肥的有效成
3 2 3 5 5 2 4 2
分。利用CH 燃料电池电解制备Ca(HPO ),并得到副产物H、Cl 等,装置如图所示。下列说法不正确的是
4 2 4 2 2 2A.a极反应:CH-8e-+4O2-=CO +2H O
4 2 2
B.L膜为阳离子交换膜,电解时阴极室中NaOH溶液的浓度变大
C.可用铁电极替换阴极的石墨电极
D.a极上通入标况下2.24LCH ,阳极室Ca2+减少0.4mol
4
【基础过关】
1.(广东省广州市天河区2023届高三三模)文物的腐蚀是指出土前由于自然的侵蚀、损坏而破坏文物的原
貌,电化学腐蚀也是重要因素之一。三星堆是中华文明的重要组成部分,下列出土文物可能涉及电化学腐蚀的
是
A B C D
青铜神树 玉璋 陶瓷马头 黄金面罩
2.(河北省重点中学2023届高三二模)考古中出土的锡青铜(铜锡合金)文物常有Cu (OH) Cl覆盖在其表面。
2 3
下列说法正确的是
A.锡青铜的熔点比纯铜高
B.锡青铜文物在潮湿环境中的腐蚀比干燥环境中快
C.锡青铜中的锡加速了铜的腐蚀速度
D.生成Cu (OH) Cl覆盖物是电化学腐蚀过程,但不是化学反应过程
2 3
3.(广东省重点中学2023届高三联考)深中通道是集“桥、岛、隧、地下互通”于一体的超级跨海集群工
程,使用了多种新材料。下列关于深中通道的说法错误的是
A.悬索主缆采用的高强耐久2060MPa钢丝属于合金
B.桥面铺装了耐盐耐高温的环氧沥青,石油分馏可获得沥青
C.隧道沉管之间采用的GINA橡胶止水带属于有机高分子材料D.在沉管外部加装了铜管用于保护钢壳沉管,利用了牺牲阳极保护法
4.(河北省沧州市第一中学2023届高三三模)出土于陕西的两千多年前的越王剑(主要成分为铁),现藏于广州
博物馆,该剑剑格左右侧皆以鸟虫书体铸刻“王戊”二字,剑色为水银古,时至如今,依然锋利。剑脊含铜量
较多,韧性好,不易折断;刃部含锡高,硬度强,可见其性能优异,锻造技术优良。下列叙述错误的是
已知:剑在地下因构成原电池发生了腐蚀,导致生锈(Fe O)。
2 3
A.铁与铜、锡构成原电池时,铁为负极
B.铁发生的电极反应为Fe-3e-=Fe3+
C.酸性环境下剑腐蚀的过程中会产生氢气
D.生成80gFe O 时理论上转移3mol电子
2 3
5.(山东省潍坊市2023届高三二模)地下管道表面附着的硫酸盐会促进钢铁发生厌氧腐蚀,为减少腐蚀的发
生,可使钢管与外接电源相连,使其表面形成致密的 。下列说法错误的是
A.钢管应与电源的负极相连 B.电压过高有可能会加剧腐蚀
C.发生厌氧腐蚀会使土壤碱性增强 D.厌氧腐蚀过程中有 生成
6.(浙江省乐清市知临中学2023届高三模拟)电化学原理(如图所示)治理硝酸盐污水中 ,下列说法不正
确是A.直流电源电极: 为正极、 为负极
B.电解过程,溶液中质子从 电极向 电极移动
C.在阳极发生的电极反应:
D.当转移 电子时,阴极室质量减少
7.(浙江省十校联盟2023届高三联考)含磷有机物应用广泛。电解法可实现由白磷直接制备 ,过
程如图所示 为甲基 。下列说法不正确的是
A.石墨电极与电源正极相连,发生氧化反应
B.铂电极上的电极反应为:
C.在电解过程中 向石墨电极移动
D.生成 ,理论上外电路需要转移 电子
8.(江苏南京师范大学附属中学2022-2023学年高三一模)电催化氮气制备铵盐和硝酸盐的原理如图所示。下
列说法正确的是A.a极反应式为N+12OH--10e-=2NO +6H O
2 2
B.电解一段时间,a、b两电极区的pH均减小
C.电解过程中H+从a极通过质子交换膜转移至b极
D.相同时间内,a、b两极消耗N 的物质的量之比为5∶3
2
【能力提升】
9.(山东省济宁市2023届高三二模)可用电化学原理进行氮的氧化物脱除,下图装置可同时吸收 和
NO(已知连二亚硫酸稀 )。
下列说法错误的是
A.N为直流电源的负极
B.装置中P为阳离子交换膜
C.左室的电极反应式为:
D.吸收池中的反应为:
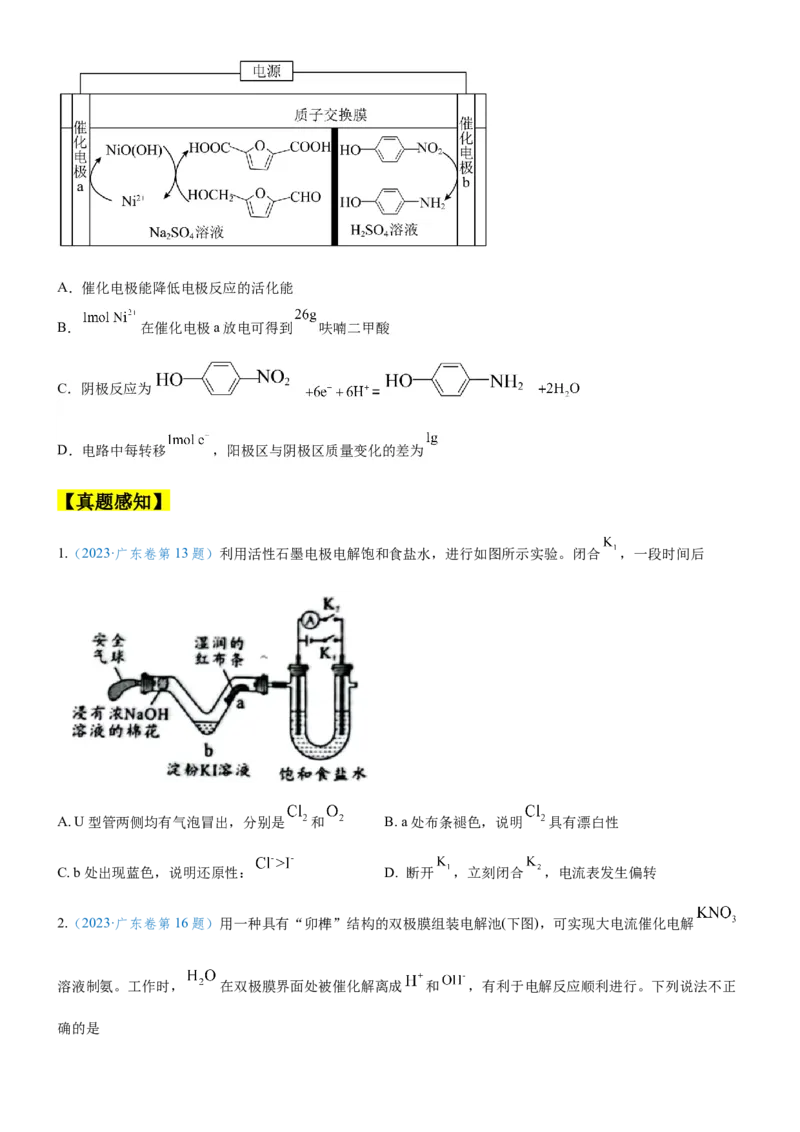
10.(湖南省娄底市2023届高三模拟)近日,湘潭大学丁锐教授课题组设计了一种新型的A位K/Na掺杂Ni-
Co-Zn-Mn钙钛矿氟化物(K/Na-NCZMF)电极材料,并构建了先进的水系锌基电池,如图所示(注明:0.1M代表
)。下列叙述错误的是A.充电时,N极附近溶液pH升高
B.放电时,M极上能生成 、 、
C.放电时,N极反应式为
D.充电时,电解质溶液中KOH、LiOH浓度一定不变
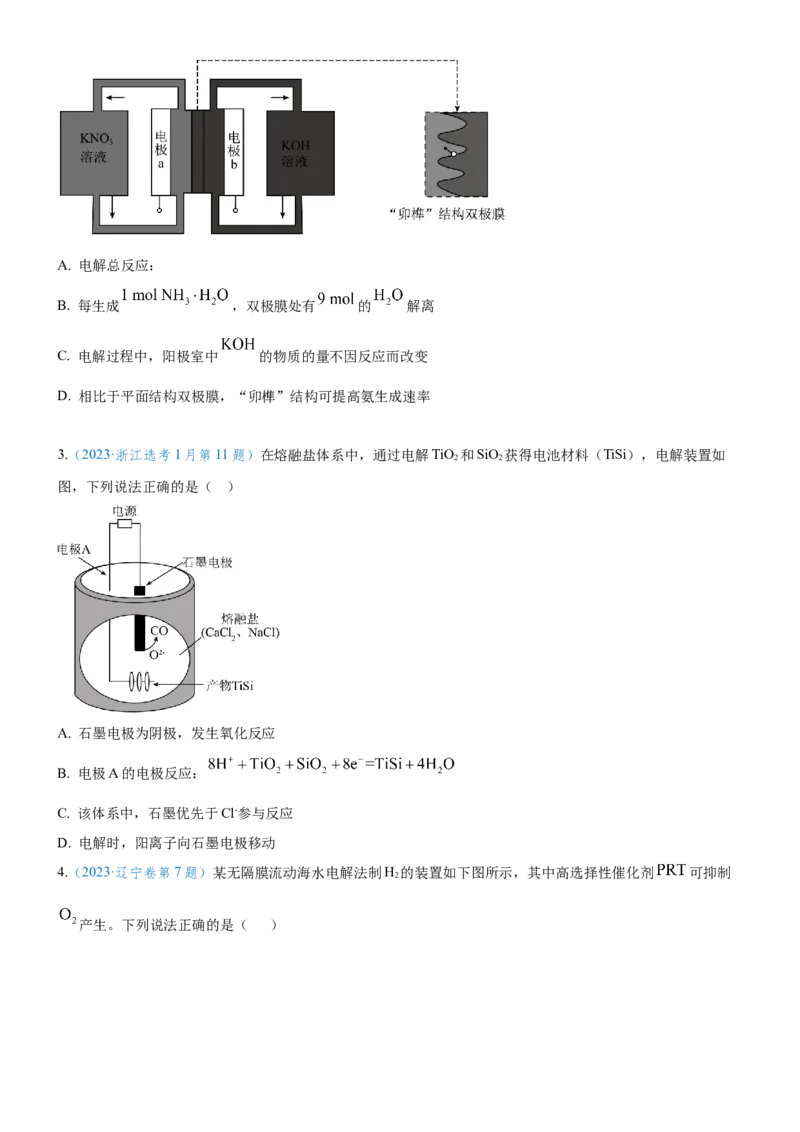
11.(辽宁省名校联盟2023届高三模拟)镍离子( )和钴离子( )性质相似,可用如图所示装置实现二者
分离。图中的双极膜中间层中的 解离为 和 ,并在直流电场作用下分别向两极迁移; 与乙酰丙
酮不反应。下列说法正确的是
A.石墨M电极上的电势低于石墨N电极上的电势
B.石墨M电极的电极反应式为 。
C.水解离出的 可以抑制Ⅱ室中的转化反应
D.导线中流过 ,Ⅰ室与Ⅲ室溶液质量变化之差约为130g
12.(江苏省徐州市2023届高三模拟)利用电化学原理控制反应条件能将 电催化还原为HCOOH,电解过
程中还伴随着析氢反应,反应过程原理的示意图如图。下列有关说法正确的是A.玻碳电极发生还原反应
B.铂电极发生的电极反应为
C.电池工作时,电流由玻碳电极经电解质溶液到铂电极
D.当电路中转移1mol 时,阳极室溶液的质量减少8g
13.(河北省保定市定州中学2023届高三模拟)双极膜是由阳离子交换膜和阴离子交换膜复合而成的,其内层
为水层,装置工作时水层中的HO解离成H+和OH-,分别向两侧发生迁移。CO 电化学还原法制备甲醇的电解
2 2
原理如图所示。该装置工作时,下列说法正确的是
A.催化电极上发生氧化反应
B.石墨电极区溶液pH不变
C.H+穿过b膜进入右室溶液
D.电解一段时间后,右室HCO的物质的量减少
14.(广东省深圳市高级中学2023届高三模拟)我国科学家以CO 与辛胺[CH(CH)NH ]为原料能够高选择性
2 3 2 7 2
的合成甲酸和辛腈[CH(CH)CN],实现了CO 的再利用,有益于解决全球变暖问题。其工作原理如图,已知右
3 2 6 2
池反应过程中无气体生成。下列说法不正确的是A.Ni P电极的电势高于In/In O 电极
2 2 3-x
B.In/In O 电极上可能有副产物H 生成
2 3-x 2
C.阴极上的电极反应:CO + H O +2e-= +OH-
2 2
D.标准状况下,33.6L CO 参与反应时,Ni P电极有1.5 mol辛腈生成
2 2
15.(湖南四大名校2024届高三第一次联考)含有硝酸盐和亚硝酸盐的酸性废水可导致水体富营养化,引发环
境污染。如图是利用电化学原理处理 的原理,下列有关叙述错误的是
A.直流电源为铅蓄电池时, 极连接X电极
B.Y电极上发生还原反应
C.阳极电极反应方程式为
D.当产生28g 时,一定有6 mol 穿过质子交换膜
16.(重庆市巴蜀中学校2023学年高三模拟)电有机合成相对于传统有机合成具有显著优势,利用如图所示装
置实现电催化合成呋喃二甲酸。下列说法错误的是A.催化电极能降低电极反应的活化能
B. 在催化电极a放电可得到 呋喃二甲酸
C.阴极反应为
D.电路中每转移 ,阳极区与阴极区质量变化的差为
【真题感知】
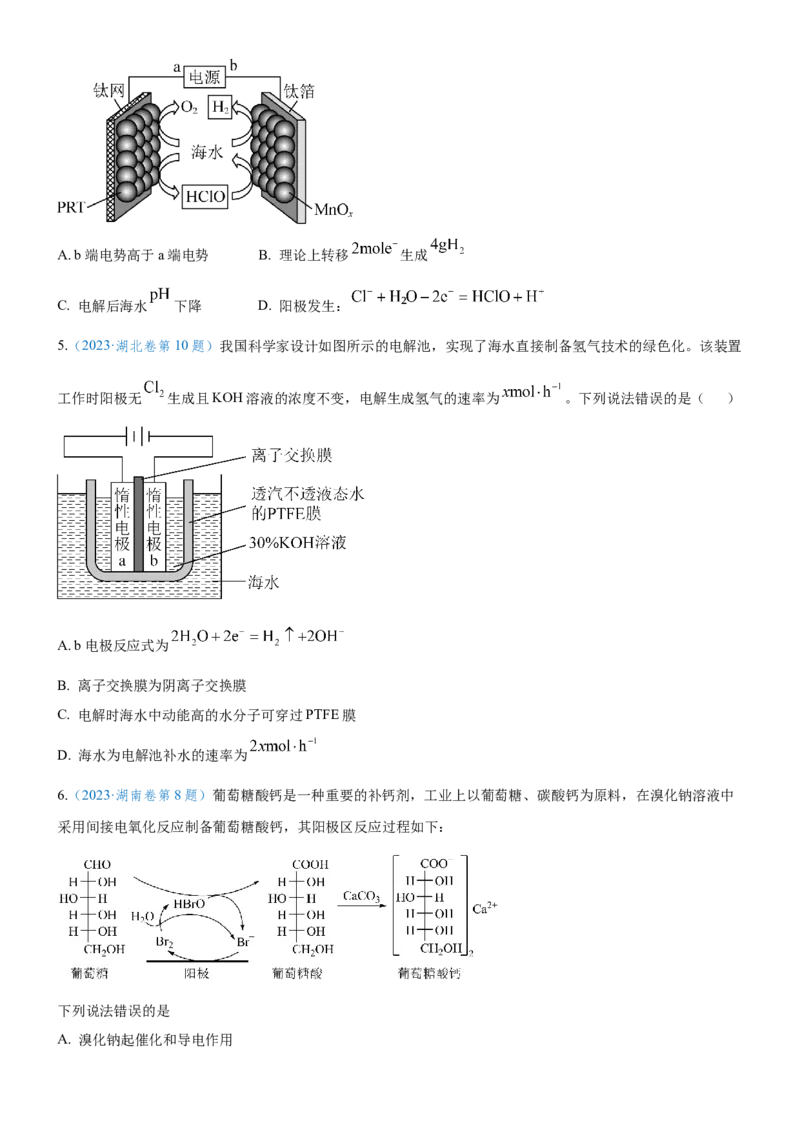
1.(2023·广东卷第13题)利用活性石墨电极电解饱和食盐水,进行如图所示实验。闭合 ,一段时间后
A. U型管两侧均有气泡冒出,分别是 和 B. a处布条褪色,说明 具有漂白性
C. b处出现蓝色,说明还原性: D. 断开 ,立刻闭合 ,电流表发生偏转
2.(2023·广东卷第16题)用一种具有“卯榫”结构的双极膜组装电解池(下图),可实现大电流催化电解
溶液制氨。工作时, 在双极膜界面处被催化解离成 和 ,有利于电解反应顺利进行。下列说法不正
确的是A. 电解总反应:
B. 每生成 ,双极膜处有 的 解离
C. 电解过程中,阳极室中 的物质的量不因反应而改变
D. 相比于平面结构双极膜,“卯榫”结构可提高氨生成速率
3.(2023·浙江选考1月第11题)在熔融盐体系中,通过电解TiO 和SiO 获得电池材料(TiSi),电解装置如
2 2
图,下列说法正确的是( )
A. 石墨电极为阴极,发生氧化反应
B. 电极A的电极反应:
C. 该体系中,石墨优先于Cl-参与反应
D. 电解时,阳离子向石墨电极移动
4.(2023·辽宁卷第7题)某无隔膜流动海水电解法制H 的装置如下图所示,其中高选择性催化剂 可抑制
2
产生。下列说法正确的是( )A. b端电势高于a端电势 B. 理论上转移 生成
C. 电解后海水 下降 D. 阳极发生:
5.(2023·湖北卷第10题)我国科学家设计如图所示的电解池,实现了海水直接制备氢气技术的绿色化。该装置
工作时阳极无 生成且KOH溶液的浓度不变,电解生成氢气的速率为 。下列说法错误的是( )
A. b电极反应式为
B. 离子交换膜为阴离子交换膜
C. 电解时海水中动能高的水分子可穿过PTFE膜
D. 海水为电解池补水的速率为
6.(2023·湖南卷第8题)葡萄糖酸钙是一种重要的补钙剂,工业上以葡萄糖、碳酸钙为原料,在溴化钠溶液中
采用间接电氧化反应制备葡萄糖酸钙,其阳极区反应过程如下:
下列说法错误的是
A. 溴化钠起催化和导电作用B. 每生成 葡萄糖酸钙,理论上电路中转移了 电子
C. 葡萄糖酸能通过分子内反应生成含有六元环状结构的产物
D. 葡萄糖能发生氧化、还原、取代、加成和消去反应
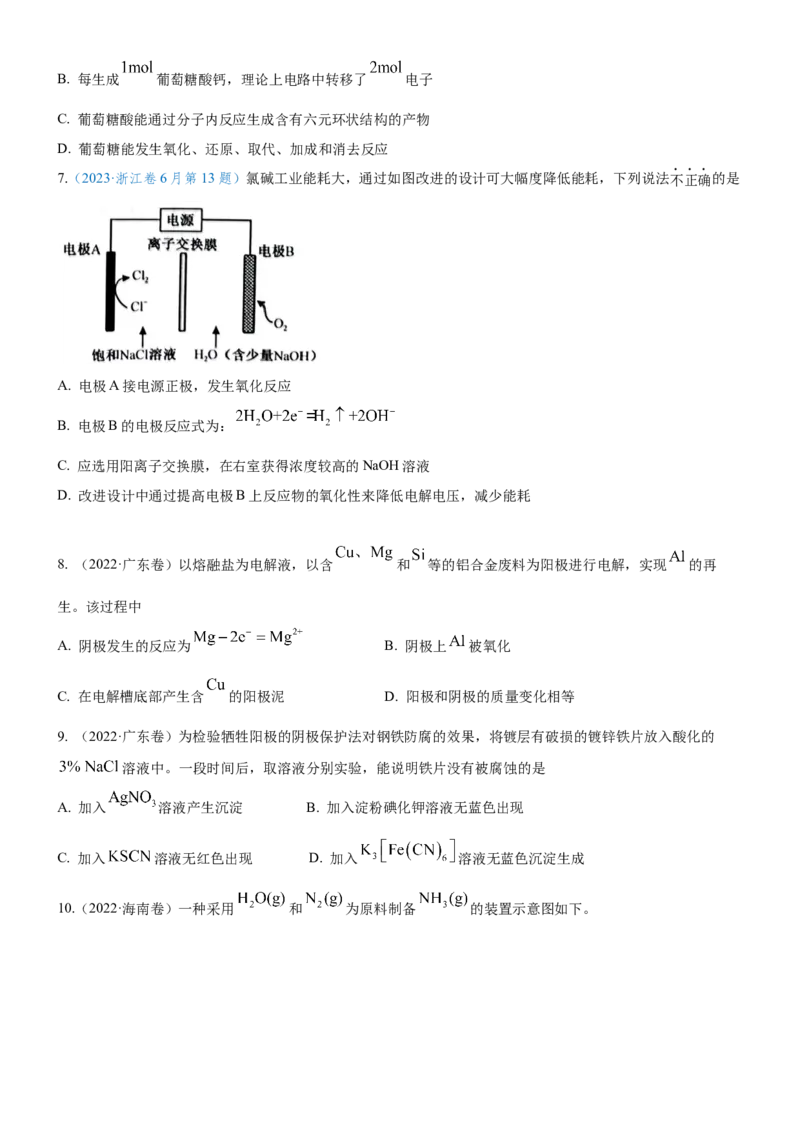
7.(2023·浙江卷6月第13题)氯碱工业能耗大,通过如图改进的设计可大幅度降低能耗,下列说法不正确的是
A. 电极A接电源正极,发生氧化反应
B. 电极B的电极反应式为:
C. 应选用阳离子交换膜,在右室获得浓度较高的NaOH溶液
D. 改进设计中通过提高电极B上反应物的氧化性来降低电解电压,减少能耗
8. (2022·广东卷)以熔融盐为电解液,以含 和 等的铝合金废料为阳极进行电解,实现 的再
生。该过程中
A. 阴极发生的反应为 B. 阴极上 被氧化
C. 在电解槽底部产生含 的阳极泥 D. 阳极和阴极的质量变化相等
9. (2022·广东卷)为检验牺牲阳极的阴极保护法对钢铁防腐的效果,将镀层有破损的镀锌铁片放入酸化的
溶液中。一段时间后,取溶液分别实验,能说明铁片没有被腐蚀的是
A. 加入 溶液产生沉淀 B. 加入淀粉碘化钾溶液无蓝色出现
C. 加入 溶液无红色出现 D. 加入 溶液无蓝色沉淀生成
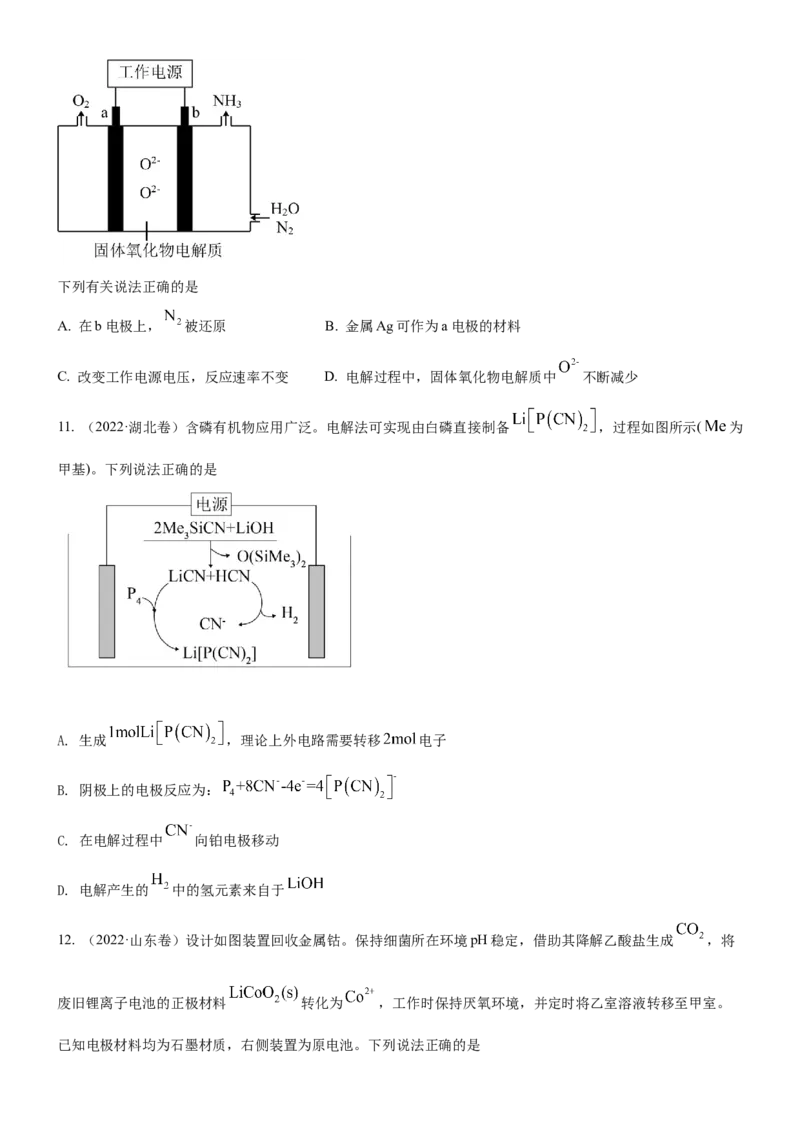
10.(2022·海南卷)一种采用 和 为原料制备 的装置示意图如下。下列有关说法正确的是
A. 在b电极上, 被还原 B. 金属Ag可作为a电极的材料
C. 改变工作电源电压,反应速率不变 D. 电解过程中,固体氧化物电解质中 不断减少
11. (2022·湖北卷)含磷有机物应用广泛。电解法可实现由白磷直接制备 ,过程如图所示( 为
甲基)。下列说法正确的是
A. 生成 ,理论上外电路需要转移 电子
B. 阴极上的电极反应为:
C. 在电解过程中 向铂电极移动
D. 电解产生的 中的氢元素来自于
12. (2022·山东卷)设计如图装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸盐生成 ,将
废旧锂离子电池的正极材料 转化为 ,工作时保持厌氧环境,并定时将乙室溶液转移至甲室。
已知电极材料均为石墨材质,右侧装置为原电池。下列说法正确的是A. 装置工作时,甲室溶液pH逐渐增大
B. 装置工作一段时间后,乙室应补充盐酸
C. 乙室电极反应式为
D. 若甲室 减少 ,乙室 增加 ,则此时已进行过溶液转移
13. (2022·北京卷)利用下图装置进行铁上电镀铜的实验探究。
序
装置示意图 电解质溶液 实验现象
号
阴极表面有无色气体,一段时间后阴
① 极表面有红色固体,气体减少。经检
验电解液中有
阴极表面未观察到气体,一段时间后
② 阴极表面有致密红色固体。经检验电
解液中无 元素
下列说法不正确的是
A. ①中气体减少,推测是由于溶液中 减少,且 覆盖铁电极,阻碍 与铁接触
B. ①中检测到 ,推测可能发生反应:
C. 随阴极析出 ,推测②中溶液 减少, 平衡逆移
D. ②中 生成 ,使得 比①中溶液的小, 缓慢析出,镀层更致密
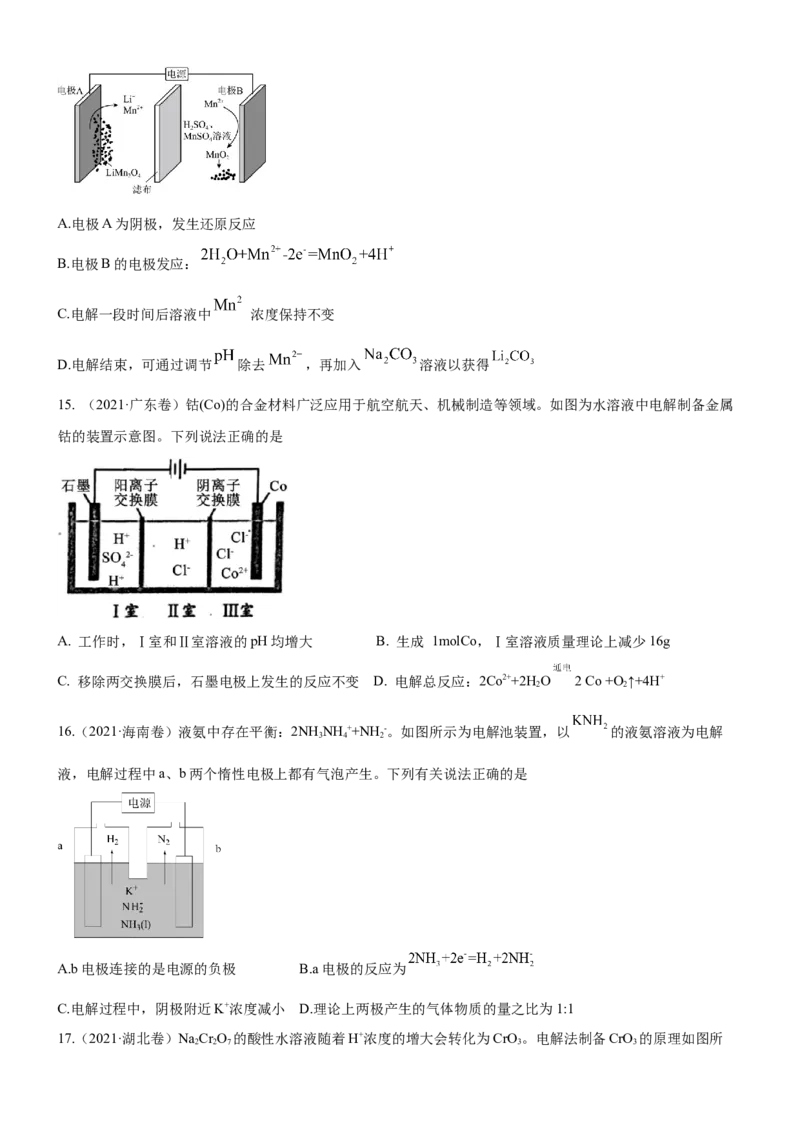
14.(2022·浙江卷)通过电解废旧锂电池中的 可获得难溶性的 和 ,电解示意图如下(其
中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略不计)。下列说法不正确的
是A.电极A为阴极,发生还原反应
B.电极B的电极发应:
C.电解一段时间后溶液中 浓度保持不变
D.电解结束,可通过调节 除去 ,再加入 溶液以获得
15. (2021·广东卷)钴(Co)的合金材料广泛应用于航空航天、机械制造等领域。如图为水溶液中电解制备金属
钴的装置示意图。下列说法正确的是
A. 工作时,Ⅰ室和Ⅱ室溶液的pH均增大 B. 生成 1molCo,Ⅰ室溶液质量理论上减少16g
C. 移除两交换膜后,石墨电极上发生的反应不变 D. 电解总反应:2Co2++2H O 2 Co +O ↑+4H+
2 2
16.(2021·海南卷)液氨中存在平衡:2NH NH ++NH-。如图所示为电解池装置,以 的液氨溶液为电解
3 4 2
液,电解过程中a、b两个惰性电极上都有气泡产生。下列有关说法正确的是
A.b电极连接的是电源的负极 B.a电极的反应为
C.电解过程中,阴极附近K+浓度减小 D.理论上两极产生的气体物质的量之比为1:1
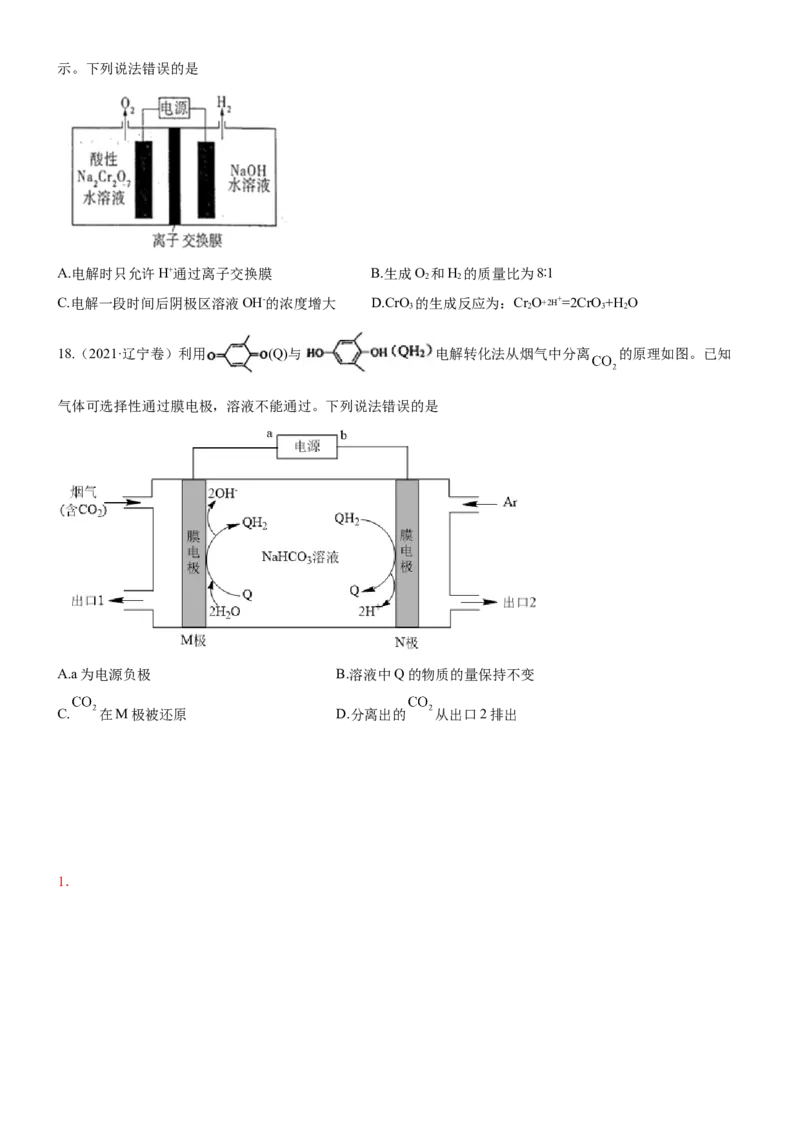
17.(2021·湖北卷)NaCr O 的酸性水溶液随着H+浓度的增大会转化为CrO。电解法制备CrO 的原理如图所
2 2 7 3 3示。下列说法错误的是
A.电解时只允许H+通过离子交换膜 B.生成O 和H 的质量比为8∶1
2 2
C.电解一段时间后阴极区溶液OH-的浓度增大 D.CrO
3
的生成反应为:Cr
2
O+2H+=2CrO
3
+H
2
O
18.(2021·辽宁卷)利用 (Q)与 电解转化法从烟气中分离 的原理如图。已知
气体可选择性通过膜电极,溶液不能通过。下列说法错误的是
A.a为电源负极 B.溶液中Q的物质的量保持不变
C. 在M极被还原 D.分离出的 从出口2排出
1.