文档内容
考点 40 有机合成
(核心考点精讲精练)
一、3年真题考点分布
考点内容 考题统计
2023浙江1月选考21题,12分;2023湖南卷18题,15分;2022海南
卷18题,14分;2022河北卷18题,15分;2022山东卷19题,12
分;2022湖南卷19题,15分;2022浙江1月选考31题,12分;2022
浙江6月选考31题,12分;2022江苏卷16题,15分;2022广东卷21
有机推断与合成
题,14分;2021全国甲卷36题,15分;2021浙江1月选考31题,12
分;2021浙江6月选考31题,12分;2021湖南卷19题,15分;2021
河北卷18题,15分;2021广东卷20题,14分;2021山东卷19题,12
分;2021天津卷18题,14分;2021海南卷18题,14分;
二、命题规律及备考策略
【命题规律】
从近三年高考试题来看,有机合成路线设计往往是有机大题中的重要设问之一,一般以新药物或中间
体、新材料等制备为背景,根据目标产物结构简式的特点,利用信息,通过对有机合成路线、绿色化学的分析,
设计或选择最佳合成路线。在进行有机合成路线设计时,要充分利用有机物之间的转化关系和题目中给定的
转化信息,并结合题目流程,用正推、逆推或正逆推结合的方式,通过信息迁移,联系官能团的引入、转换、保
护方法或将片段拼接衍变,得到合成路线。
【备考策略】
1.掌握官能团的引入、消除与转化方法,掌握使碳链增长、减短、成环的主要反应,学会综合分析
推断,熟练合成技法。
(1)正合成分析法。从基础原料入手,找出合成所需的直接或间接的中间体,逐步推向合成的目标有机物,
其合成示意图为基础原料→中间体1→中间体2……→目标有机物。
(2)逆合成分析法。设计复杂有机物的合成路线时常用的方法。它是由目标有机物倒推寻找上一步反应
的中间体n,而中间体n又可以由中间体(n-1)得到,依次倒推,最后确定最适宜的基础原料和最终的合成路线。
2.设计流程
(1)比较原料与目标产物中基团变化与碳、氢、氧、氮、卤原子的变化,找到原料之间的用量比。
2)引进基团时要考虑定位效应(信息会提示)和基团保护,据此设计引进基团的顺序。
(3)基团的保护与复原,还有一些原有基团被酸(碱)化或氧化(还原)后,要复原成原基团。
【命题预测】预计2024年仍以非选择题为主,尤其设计合成路线的程序和选择,复习时要加以关注。
考法 1 碳骨架的构建
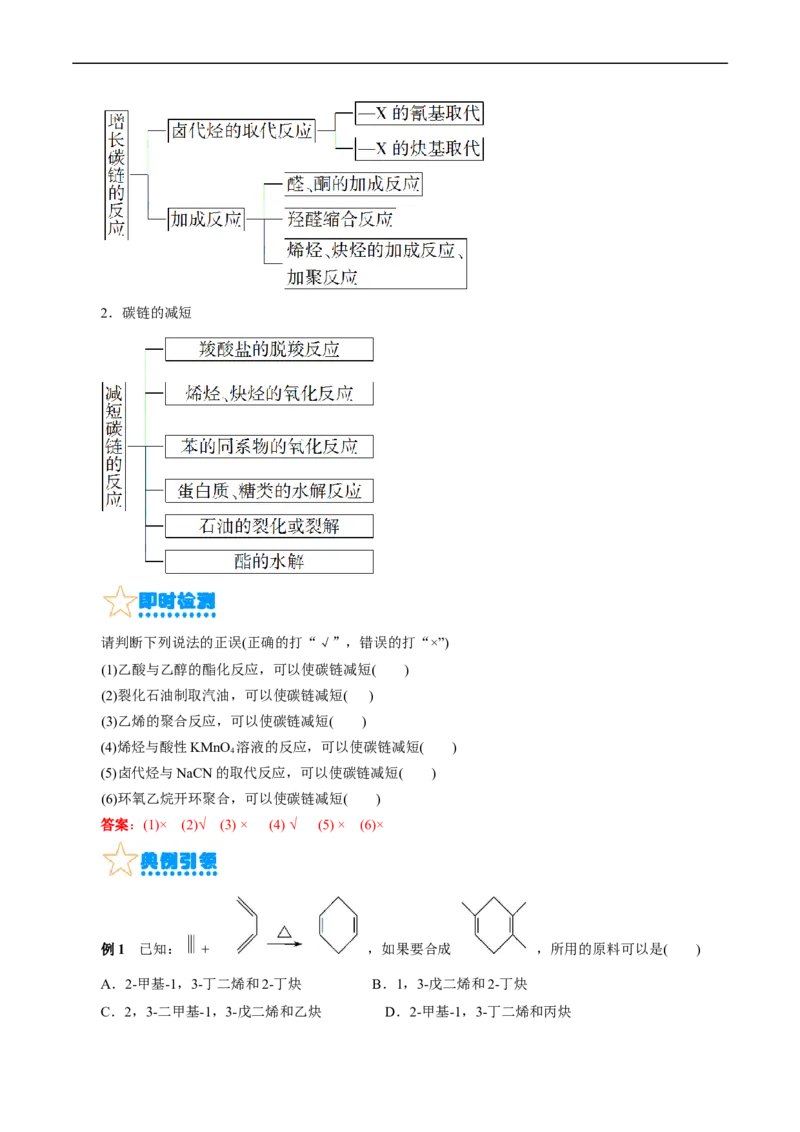
1.碳链的增长
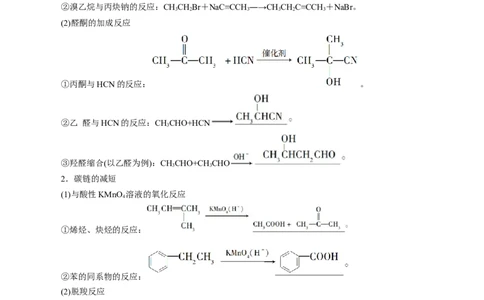
(1)卤代烃的取代反应
① 溴 乙 烷 与 氰 化 钠 的 反 应 : CHCHBr + NaCN―→CHCHCN + NaBr ,
3 2 3 2
CHCHCN――→CHCHCOOH。
3 2 3 2
②溴乙烷与丙炔钠的反应:CHCHBr+NaC≡CCH ―→CHCHC≡CCH +NaBr。
3 2 3 3 2 3
(2)醛酮的加成反应
①丙酮与HCN的反应: 。
②乙 醛与HCN的反应:CHCHO+HCN
3
③羟醛缩合(以乙醛为例):CHCHO+CH CHO
3 3
2.碳链的减短
(1)与酸性KMnO 溶液的氧化反应
4
①烯烃、炔烃的反应:
②苯的同系物的反应:
(2)脱羧反应
无水醋酸钠与碱石灰的反应:CHCOONa+NaOH――→CH↑+NaCO。
3 4 2 3
1.碳链的增长2.碳链的减短
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)乙酸与乙醇的酯化反应,可以使碳链减短( )
(2)裂化石油制取汽油,可以使碳链减短( )
(3)乙烯的聚合反应,可以使碳链减短( )
(4)烯烃与酸性KMnO 溶液的反应,可以使碳链减短( )
4
(5)卤代烃与NaCN的取代反应,可以使碳链减短( )
(6)环氧乙烷开环聚合,可以使碳链减短( )
答案:(1)× (2)√ (3) × (4) √ (5) × (6)×
例1 已知: + ,如果要合成 ,所用的原料可以是( )
A.2-甲基-1,3-丁二烯和2-丁炔 B.1,3-戊二烯和2-丁炔
C.2,3-二甲基-1,3-戊二烯和乙炔 D.2-甲基-1,3-丁二烯和丙炔【答案】A
【解析】类比1,3-丁二烯与乙炔的加成反应,采用逆合成分析法可知,若按 断键可得到 (2-
甲基-1,3-丁二烯)和 (2-丁炔),若按 断键可得到 (2,3-二甲基-1,3-丁二烯)和 (丙炔),故选
A。
例2 以丙烯为基础原料,可制备离子导体材料中有机溶剂的单体丙烯酸丁酯,其合成路线如下:
下列判断错误的是( )
A.反应①是一个碳链增长的反应
B.反应②是还原反应,可以通过加成的方式实现
C.反应③需要的条件是浓硫酸和加热
D.该合成工艺的原子利用率为100%
【答案】D
【解析】A项,对比反应①的反应物和生成物,可知反应①是一个碳链增长的反应,A项正确;B项,
反应②是醛基被还原为羟基,在一定条件下,醛基与H 加成可得到羟基,B项正确;C项,反应③是酯化
2
反应,反应条件是浓硫酸和加热,C项正确;D项,反应③有水生成,故该合成工艺的原子利用率小于
100%,D项错误。故选D。
对点1 卤代烃能够发生下列反应:2CHCHBr+2Na→CH CHCHCH +2NaBr。下列有机物可合成
3 2 3 2 2 3
环丙烷的是( )
A.CHCHCHCl B.CHCHBrCH Br
3 2 2 3 2
C.CHBrCHCHBr D.CHCHBrCH CHBr
2 2 2 3 2 2
【答案】C
【解析】由信息2CHCHBr+2Na―→CHCHCHCH +2NaBr可知,反应机理为:分子内碳溴键断裂
3 2 3 2 2 3
后,两个断键重新结合为碳碳键,溴与钠结合为 NaBr。A 中两分子 CHCHCHCl 可合成
3 2 2
CHCHCHCHCHCH ; B 中 一 分 子 CHCHBrCH Br 不 能 成 环 , 两 分 子 生 成
3 2 2 2 2 3 3 2
;C中一分子CHBrCHCHBr可合成 ;D
2 2 2中一分子CHCHBrCH CHBr可合成 。
3 2 2
对点2 是一种有机醚,可由链状烃A(分子式为C H)通过如图路线制得。下列说法正确的是(
4 6
)
A B C
A.A的结构简式是CH=CHCHCH
2 2 3
B.B中含有的官能团有碳溴键、碳碳双键
C.C在Cu或Ag作催化剂、加热条件下不能被O 氧化为醛
2
D.①、②、③的反应类型分别为加成反应、取代反应、消去反应
【答案】B
【解析】由有机醚的结构及反应③的条件可知C为 ,结合反应①和②的条
件可推知 B 为 ,A 为 ,A 项错误;B 的结构简式为
, B 中 含 有 的 官 能 团 是 碳 碳 双 键 和 碳 溴 键 , B 项 正 确 ; C 为
,连接醇羟基的碳原子上含有2个H原子,所以C能被催化氧化生成醛,C项
错误;烯烃能和溴单质发生加成反应,卤代烃能发生水解反应,水解反应属于取代反应,醇生成醚的反应
为取代反应,所以①、②、③分别是加成反应、取代反应、取代反应,D项错误。
考法 2 官能团的引入和转化
1.官能团的引入
类别 反应物 化学方程式
CHCHOH CHCHOH――→CH===CH ↑+HO
3 2 3 2 2 2 2
碳碳双键
CHCHBr CHCHBr+NaOH――→CH===CH ↑+NaBr+HO
3 2 3 2 2 2 2
CH===CH 与HCl CH===CH +HCl―→CHCHCl
2 2 2 2 3 2
卤素原子
CHCHOH与HBr CHCHOH+HBr―→CHCHBr+HO
3 2 3 2 3 2 2
CH===CH 与HO CH===CH +HO――→CHCHOH
2 2 2 2 2 2 3 2
羟基 CHCHCl CHCHCl+NaOH――→CHCHOH+NaCl
3 2 3 2 3 2
CHCHO与H CHCHO+H――→CHCHOH
3 2 3 2 3 2
RCHCH===CH RCHCH===CH ――→RCHCOOH+CO↑
2 2 2 2 2 2
羧基
CHCHCN CHCHCN――→CHCHCOOH
3 2 3 2 3 2
羰基
2.官能团的转化
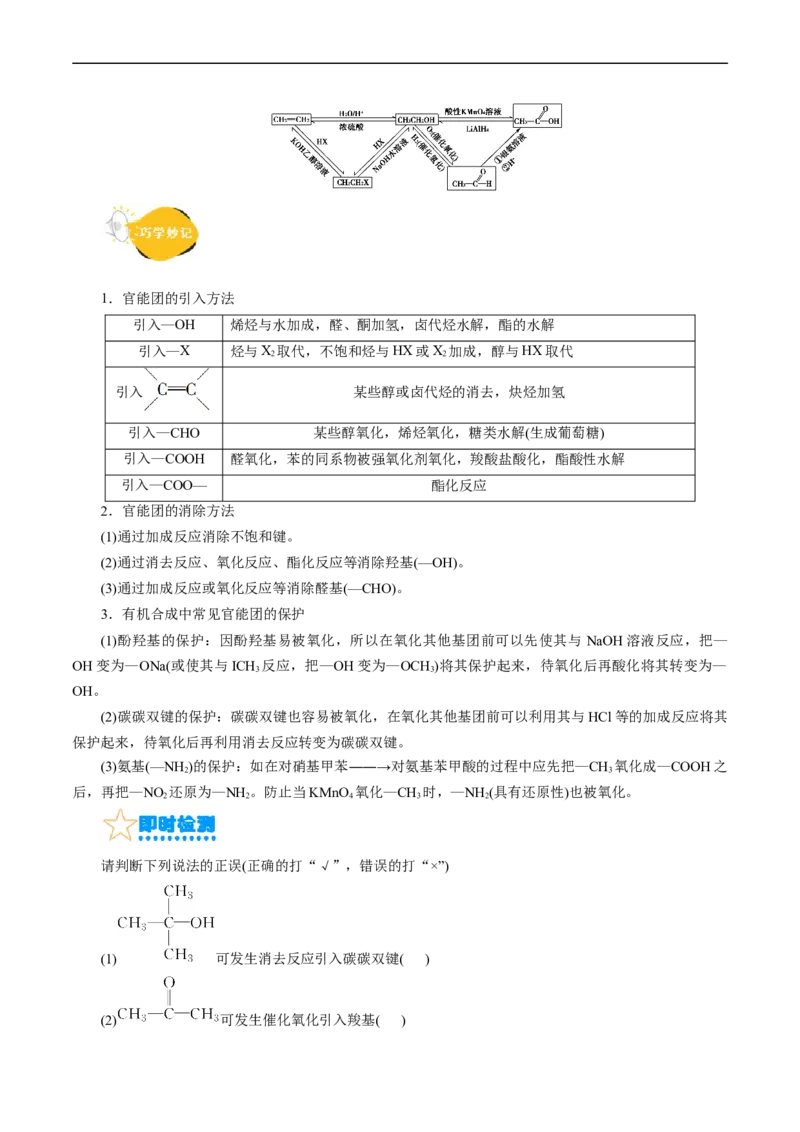
官能团的转化可以通过取代、消去、加成、氧化、还原等反应实现。下面是以乙烯为起始物,通过一
系列化学反应实现的官能团间的转化。1.官能团的引入方法
引入—OH 烯烃与水加成,醛、酮加氢,卤代烃水解,酯的水解
引入—X 烃与X 取代,不饱和烃与HX或X 加成,醇与HX取代
2 2
引入 某些醇或卤代烃的消去,炔烃加氢
引入—CHO 某些醇氧化,烯烃氧化,糖类水解(生成葡萄糖)
引入—COOH 醛氧化,苯的同系物被强氧化剂氧化,羧酸盐酸化,酯酸性水解
引入—COO— 酯化反应
2.官能团的消除方法
(1)通过加成反应消除不饱和键。
(2)通过消去反应、氧化反应、酯化反应等消除羟基(—OH)。
(3)通过加成反应或氧化反应等消除醛基(—CHO)。
3.有机合成中常见官能团的保护
(1)酚羟基的保护:因酚羟基易被氧化,所以在氧化其他基团前可以先使其与 NaOH溶液反应,把—
OH变为—ONa(或使其与ICH 反应,把—OH变为—OCH )将其保护起来,待氧化后再酸化将其转变为—
3 3
OH。
(2)碳碳双键的保护:碳碳双键也容易被氧化,在氧化其他基团前可以利用其与HCl等的加成反应将其
保护起来,待氧化后再利用消去反应转变为碳碳双键。
(3)氨基(—NH )的保护:如在对硝基甲苯――→对氨基苯甲酸的过程中应先把—CH 氧化成—COOH之
2 3
后,再把—NO 还原为—NH 。防止当KMnO 氧化—CH 时,—NH (具有还原性)也被氧化。
2 2 4 3 2
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1) 可发生消去反应引入碳碳双键( )
(2) 可发生催化氧化引入羧基( )(3)CH CHBr可发生取代反应引入羟基( )
3 2
(4) 与CH===CH 可发生加成反应引入环( )
2 2
(5)烷烃取代反应,不能引入-OH( )
(6)如果以乙烯为原料,经过加成反应、取代反应反应可制得乙二醇( )
答案:(1) √ (2) × (3) √ (4) √ (5)√ (6)√
例1 下列反应中,不可能在有机物中引入羧基的是( )
A.卤代烃的水解 B.有机物RCN在酸性条件下水解
C.醛的氧化 D.烯烃的氧化
【答案】A
【解析】卤代烃水解引入了羟基,RCN水解生成RCOOH,RCHO被氧化生成RCOOH,烯烃如RCH
=CHR被氧化后可以生成RCOOH。
例2 由CHCHCHBr制备CHCH(OH)CH OH,依次从左至右发生的反应类型和反应条件都正确的
3 2 2 3 2
是 ( )
选项 反应类型 反应条件
A 加成反应;取代反应;消去反应 KOH醇溶液、加热;KOH水溶液、加热;常温
B 消去反应;加成反应;取代反应 NaOH水溶液、加热;常温;NaOH醇溶液、加热
C 氧化反应;取代反应;消去反应 加热;KOH醇溶液、加热;KOH水溶液、加热
D 消去反应;加成反应;取代反应 NaOH醇溶液、加热;常温;NaOH水溶液、加热
【答案】D
【解析】CHCH(OH)CH OH可以由CHCHBrCH Br水解得到,而CHCHBrCH Br可以由CHCH=CH
3 2 3 2 3 2 3 2
与溴单质加成得到,CHCH=CH 可由 CHCHCHBr 发生消去反应得到,故合成路线为 CHCHCHBr
3 2 3 2 2 3 2 2
CHCH CH CHCHBrCH Br CHCH(OH)CH OH,发生的反应类型依次是
3 2 3 2 3 2
消去反应、加成反应、取代反应。
对点1 由石油裂解产物乙烯制取HOCH COOH,需要经历的反应类型有( )
2
A.氧化——氧化——取代——水解 B.加成——水解——氧化——氧化
C.氧化——取代——氧化——水解 D.水解——氧化——氧化——取代
【答案】A
【解析】由乙烯 CH==CH 合成 HOCH COOH 的步骤:2CH==CH +O―――→2CHCHO,
2 2 2 2 2 2 3
2CHCHO+O―――→2CHCOOH,CHCOOH+Cl――→Cl—CH COOH+HCl,Cl—CH COOH+
3 2 3 3 2 2 2
HO―――→HOCH COOH+HCl,故反应类型:氧化——氧化——取代——水解。
2 2对点2 在给定条件下,下列选项中所示物质间的转化均能实现的是( )
A.CHCHCHBr――→CHCH===CH ――→CHCHBrCH Br
3 2 2 3 2 3 2
B.NaOH(aq)――→C HONa(aq)――→NaHCO (aq)
6 5 3
C.NaOH(aq)――→Cu(OH) 悬浊液――→Cu O(s)
2 2
D.石油――→CHCH===CH ――→
3 2
【答案】B
【解析】 CHCHCHBr和氢氧化钠醇溶液共热条件下发生消去反应得 CHCH===CH ,A错误;苯
3 2 2 3 2
酚有弱酸性,苯酚能与氢氧化钠反应生成苯酚钠和水,苯酚的电离能力介于碳酸的一级电离和二级电离之
间,苯酚钠可以和二氧化碳反应生成碳酸氢钠和苯酚,B正确;蔗糖不是还原性糖,不会与新制的氢氧化
铜悬浊液反应,C错误;聚丙烯的正确的结构简式为 ,D错误。
考法 3 有机合成路线的设计
1.基本流程
2.合成路线的核心
合成路线的核心在于构建目标化合物分子的碳骨架和引入必需的官能团。
3.合成路线的推断方法
(1)正推法
①路线:某种原料分子 ――→目标分子。
②过程:首先比较原料分子和目标化合物分子在结构上的异同,包括官能团和碳骨架两个方面的异同;
然后,设计由原料分子转向目标化合物分子的合成路线。
(2)逆推法
①路线:目标分子――→原料分子。
②过程:在逆推过程中,需要逆向寻找能顺利合成目标化合物的中间有机化合物,直至选出合适的起
始原料。
(3)优选合成路线依据
①合成路线是否符合化学原理。
②合成操作是否安全可靠。
③绿色合成。绿色合成主要出发点是:有机合成中的原子经济性;原料的绿色化;试剂与催化剂的无公害性。
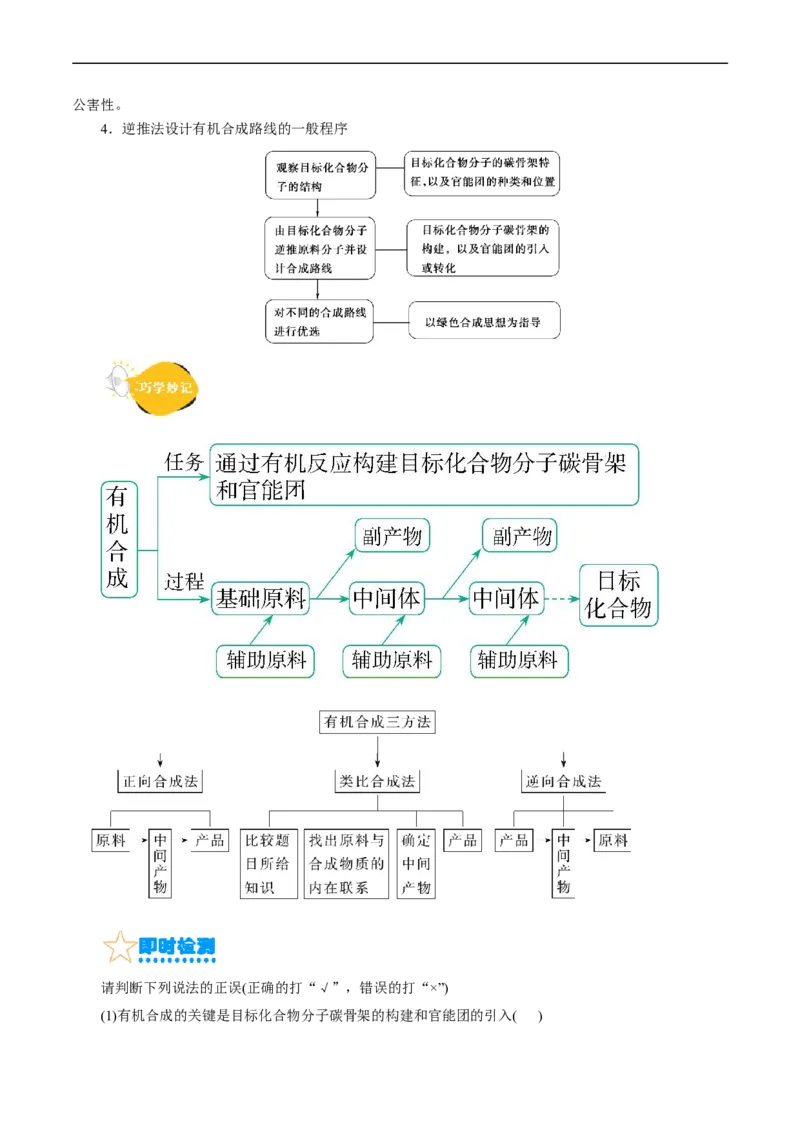
4.逆推法设计有机合成路线的一般程序
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)有机合成的关键是目标化合物分子碳骨架的构建和官能团的引入( )(2)设计有机合成路线的方法有正推法和逆推法( )
(3)逆推法设计合成路线时往往先推出一些中间产物,然后逐步推出原料分子( )
(4)由丙烯合成1,2-丙二醇:第一步加成反应,第二步取代反应( )
(5)由1-溴丁烷合成1,3-丁二烯:第一步消去反应,第二步加聚反应( )
(6)由乙醇合成乙炔:第一步消去反应,第二步加成反应,第三步消去反应(
(7)由乙烯合成乙二醛:第一步加成反应,第二步取代反应,第三步氧化反应( )
(8)绿色合成思想只要求所有原料都转化为目标化合物( )
答案:(1) √ (2)√ (3) √ (4) √ (5) × (6)√ (7) √ (8)×
例1 关于由 的说法正确的是( )
A.为有机分子碳链增加的过程 B.第1步反应需引入碳碳双键
C.该过程须通过两步反应完成 D.该过程不可能发生加成反应
【答案】B
【解析】该合成路线为: 。
例2 下列合成路线不合理的是( )
A.用乙醇合成正丁醇:
B.用二甲基二氯硅烷合成硅橡胶:
硅橡胶
C.用乙烯合成1,4-二氧杂环己烷( ):D.用1,3-丁二烯合成2-氯-1,3-丁二烯:
【答案】D
【解析】A项,乙醇催化氧化产生CHCHO,CHCHO分子之间发生加成反应产生
3 3
CHCH(OH)CH CHO,CHCH(OH)CH CHO在催化剂存在条件下加热发生消去反应产生CHCH=CHCHO,
3 2 3 2 3
CHCH=CHCHO与H 在Ni催化下加热,发生加成反应产生CHCHCHCHOH,A正确;B项,
3 2 3 2 2 2
(CH)SiCl 发生水解反应产生(CH)Si(OH) ,该物质在一定条件下发生聚合反应产生 ,
3 2 2 3 2 2
该物质发生交联产生硅橡胶,B正确;C项,CH=CH 与Br 发生加成反应产生CHBrCHBr,CHBrCHBr
2 2 2 2 2 2 2
与NaOH的水溶液发生水解反应产生HOCH CHOH,HOCH CHOH与浓硫酸混合加热发生脱水反应产生
2 2 2 2
,C正确;D项,CH=CH-CH=CH 与Cl 发生1,4-加成反应产生Cl-CH -CH=CH-CH -Cl,该物质
2 2 2 2 2
与NaOH的水溶液发生水解反应产生HO-CH-CH=CH-CH -OH,HO-CH-CH=CH-CH -OH与HCl发生加成
2 2 2 2
反应产生HO-CH-CH-CHCl-CH -OH,HO-CH-CH-CHCl-CH -OH与浓硫酸混合加热发生消去反应产生
2 2 2 2 2 2
CH=CCl-CH=CH ,D错误;故选D。
2 2
对点1 以溴乙烷为原料制备1,2-二溴乙烷,下列方案中最合理的是( )
⃗NaOH溶液
A.CHCHBr △ CHCHOH CH=CH CHBrCHBr
3 2 3 2 2 2 2 2
B.CHCHBr CHBrCHBr
3 2 2 2
⃗NaOH醇溶液
C.CHCHBr △ CH=CH CHCHBr CHBrCHBr
3 2 2 2 3 2 2 2
⃗NaOH醇溶液
D.CHCHBr △ CH=CH CHBrCHBr
3 2 2 2 2 2【答案】D
【解析】题干中强调的是最合理的方案,A项与D项相比,步骤多一步,且在乙醇发生消去反应时,
容易发生分子间脱水、氧化反应等副反应;B项步骤最少,但取代反应不会停留在“CHBrCHBr”阶段,
2 2
副产物多,分离困难,原料浪费;C项比D项多一步取代反应,显然不合理;D项相对步骤少,操作简单,
副产物少,较合理。
对点2 以环戊烷为原料制备环戊二烯的合成路线如图,则( )
A.A的结构简式是
B.①②的反应类型分别是取代、消去
C.反应②③的条件分别是浓硫酸加热、光照
D.酸性KMnO 溶液褪色可证明 已完全转化为
4
【答案】B
【 解 析 】 以 环 戊 烷 为 原 料 制 备 环 戊 二 烯 的 合 成 路 线 为
。A项,由上述分析可知,A为氯代环戊烷;B项,反应
①为光照条件下的取代反应,反应②为在氢氧化钠醇溶液中加热发生的消去反应;C项,反应②的反应试
剂和反应条件为氢氧化钠醇溶液、加热,反应③的条件为常温;D项,B为环戊烯,含碳碳双键,与环戊
二烯均能使高锰酸钾溶液褪色,则酸性KMnO 溶液褪色,不能证明环戊烷已完全转化成环戊二烯。
4
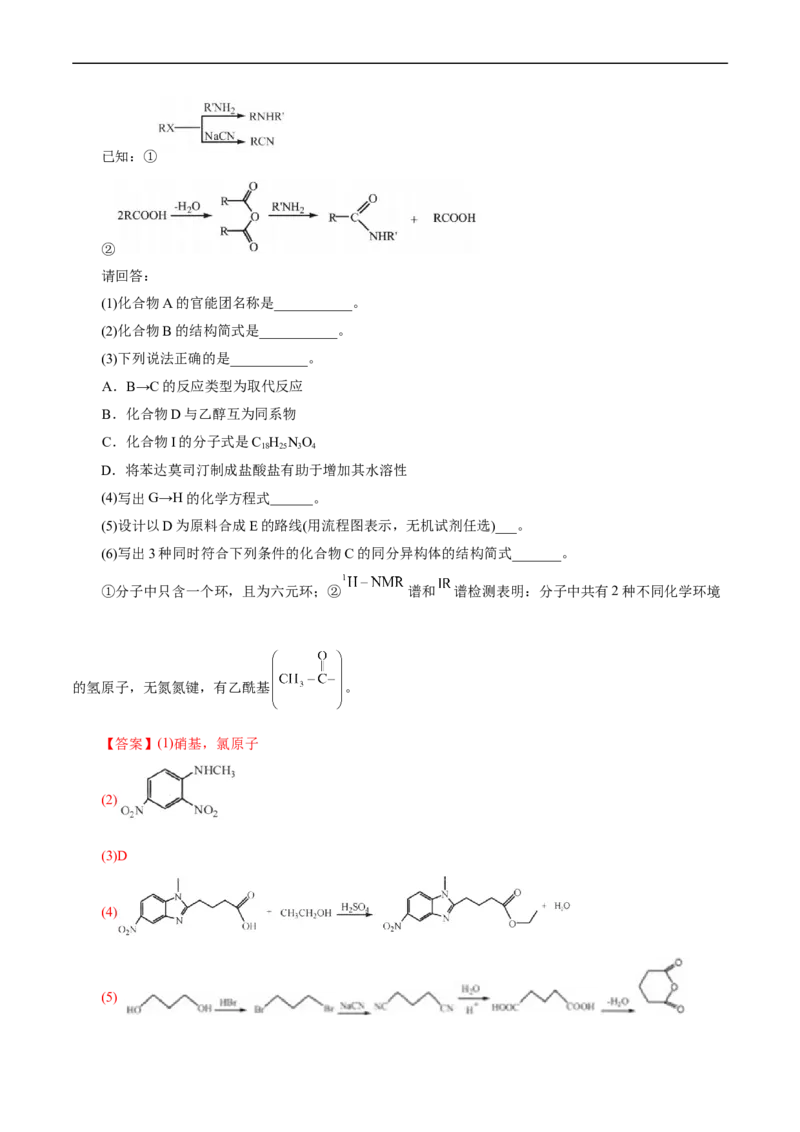
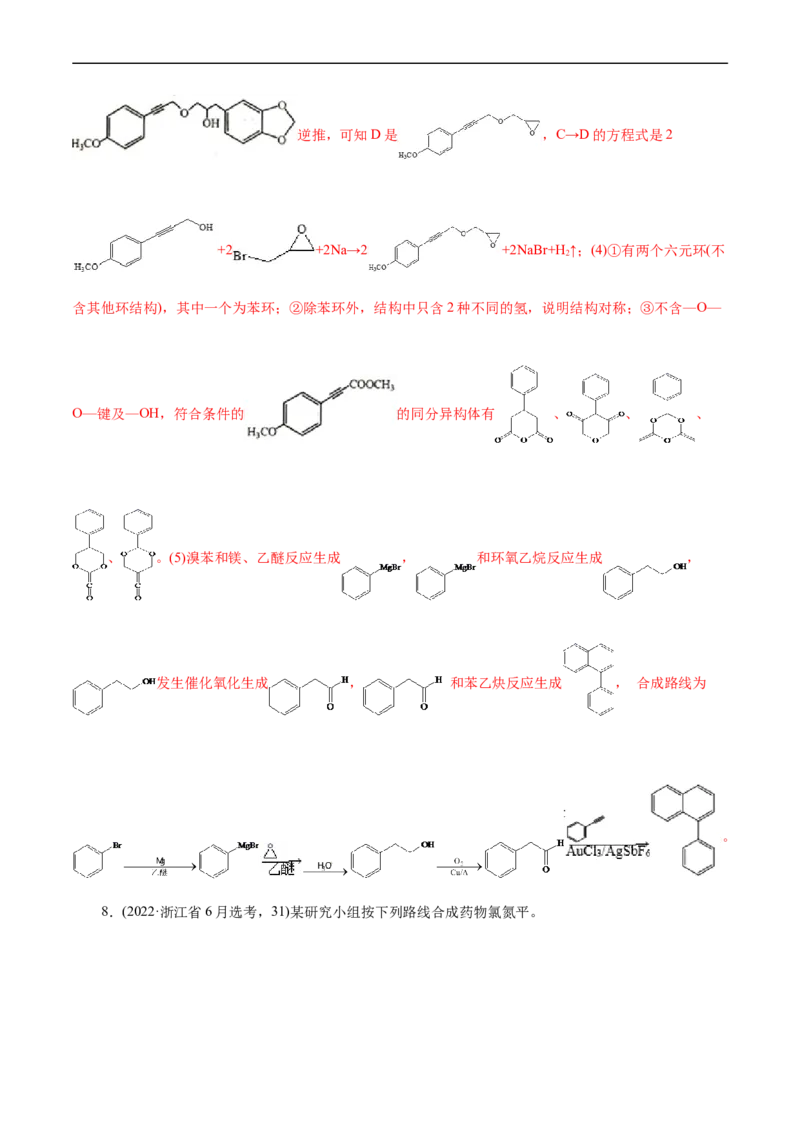
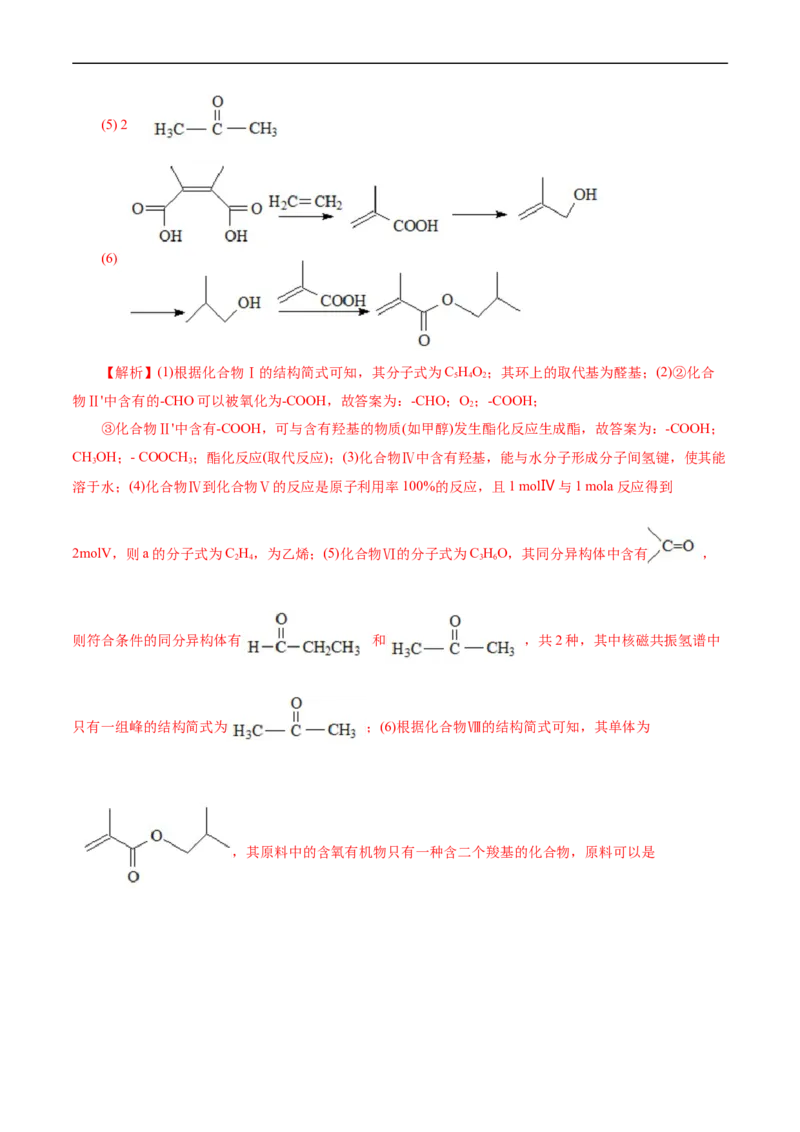
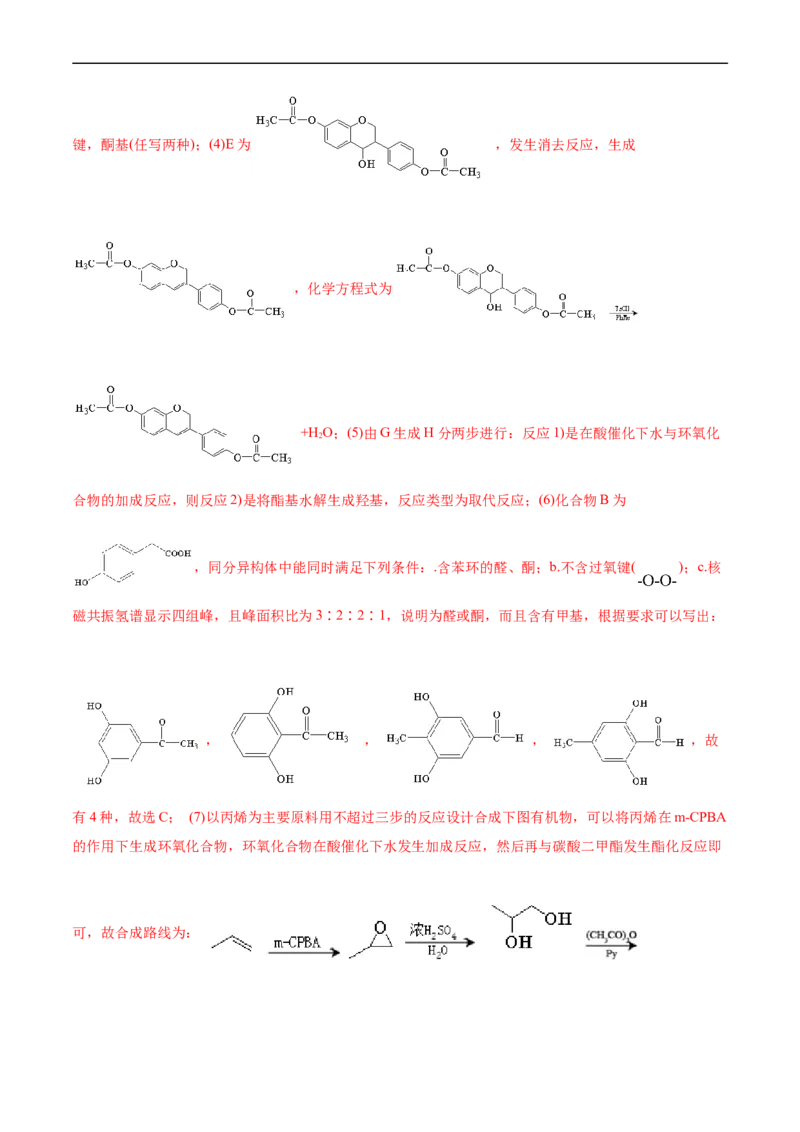
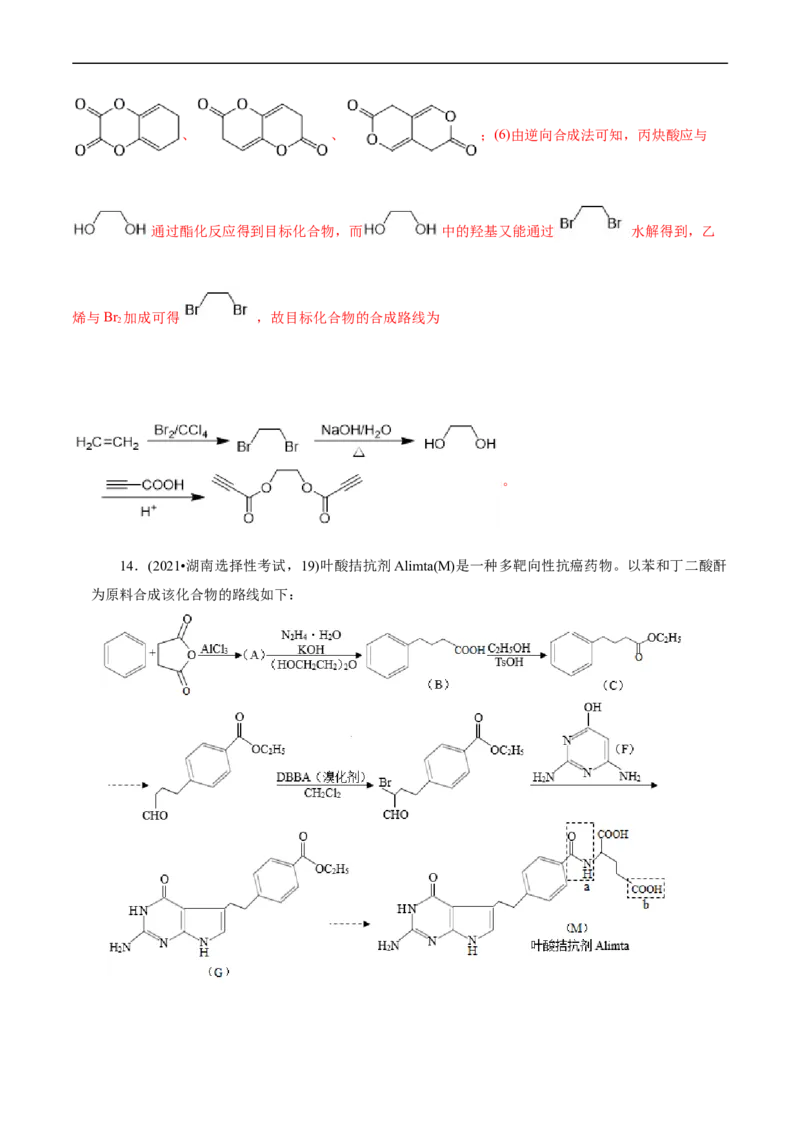
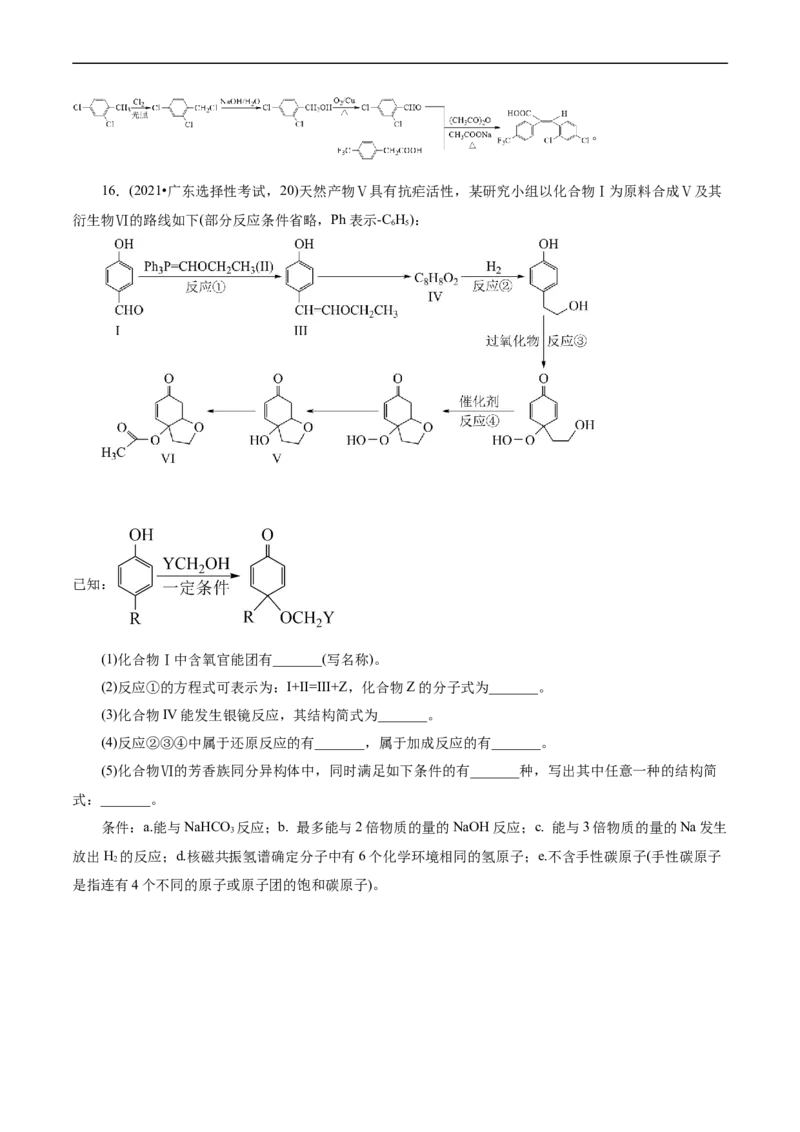
1.(2023•浙江省1月选考,21) (12分)某研究小组按下列路线合成抗癌药物盐酸苯达莫司汀。已知:①
②
请回答:
(1)化合物A的官能团名称是___________。
(2)化合物B的结构简式是___________。
(3)下列说法正确的是___________。
A.B→C的反应类型为取代反应
B.化合物D与乙醇互为同系物
C.化合物I的分子式是C H NO
18 25 3 4
D.将苯达莫司汀制成盐酸盐有助于增加其水溶性
(4)写出G→H的化学方程式______。
(5)设计以D为原料合成E的路线(用流程图表示,无机试剂任选)___。
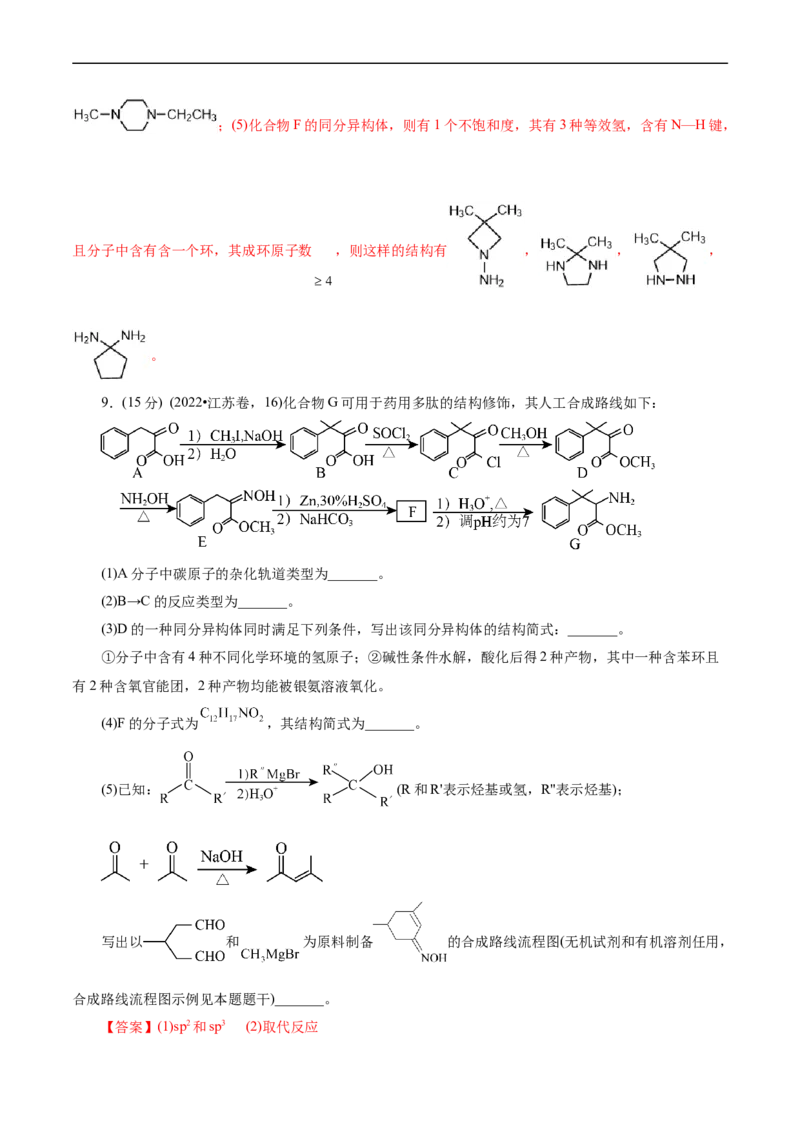
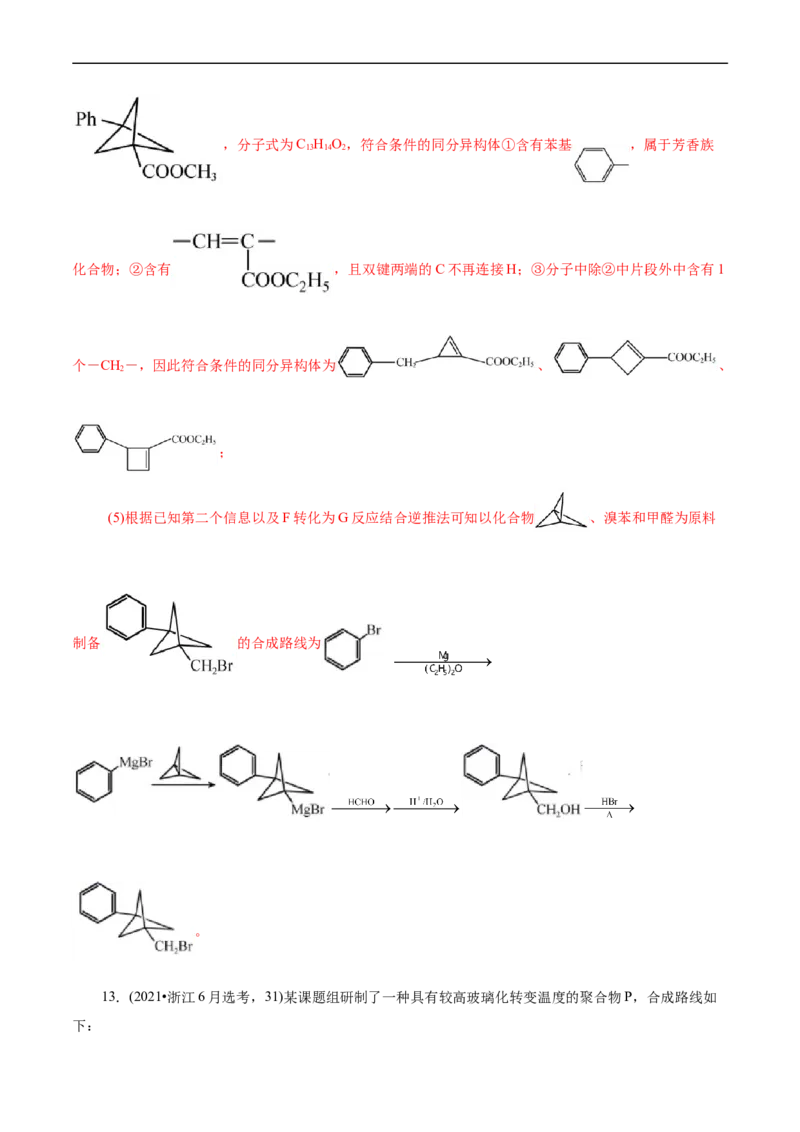
(6)写出3种同时符合下列条件的化合物C的同分异构体的结构简式_______。
①分子中只含一个环,且为六元环;② 谱和 谱检测表明:分子中共有2种不同化学环境
的氢原子,无氮氮键,有乙酰基 。
【答案】(1)硝基,氯原子
(2)
(3)D
(4)
(5)(6)
【解析】 与CHNH 反应生成B,B与硫化钠发生还原反应生成C,结合C的结构可知
3 2
A到B为取代反应,B为 ,C与E发生已知中反应生成F,F为
,F脱水生成G ,G与乙醇发生酯化反应生成H
,H与氢气加成后再与环氧乙烷发生反应生成I,I与SOCl 发生取代反应后
2
再与盐酸反应生成盐酸苯达莫司汀。(1)由A的结构可知其所含官能团为硝基和氯原子;(2)由以上分析可
知化合物B的结构简式 ;(3)A项,B→C的反应中B中一个硝基转化为氨基,反应类
型为还原反应,故错误;B项,化合物D中含有两个羟基,与乙醇不是同系物,故错误;C项,化合物I
的分子式是C H NO,故错误;D项,将苯达莫司汀制成盐酸盐,可以增加其水溶性,利于吸收,故正
18 27 3 4
确;故选D;(4)G与乙醇发生酯化反应生成H ,反应方程式为:
;(5)1,3-丙二醇与HBr发生取代反应生成1,3-二溴丙烷,1,3-二溴丙烷与NaCN发生取代反应生成 , 发生水
解生成戊二酸,戊二酸分子内脱水生成 ,合成路线为:
;(6)化合物C的同分异构体①分子中只含一个环,且
为六元环;② 谱和 谱检测表明:分子中共有2种不同化学环境的氢原子,无氮氮键,有乙酰
基 ,除乙酰基外只有一种氢,则六元环上的原子均不与氢相连,该物质具有很高的对称性,符
合的结构有 、 、 、 。
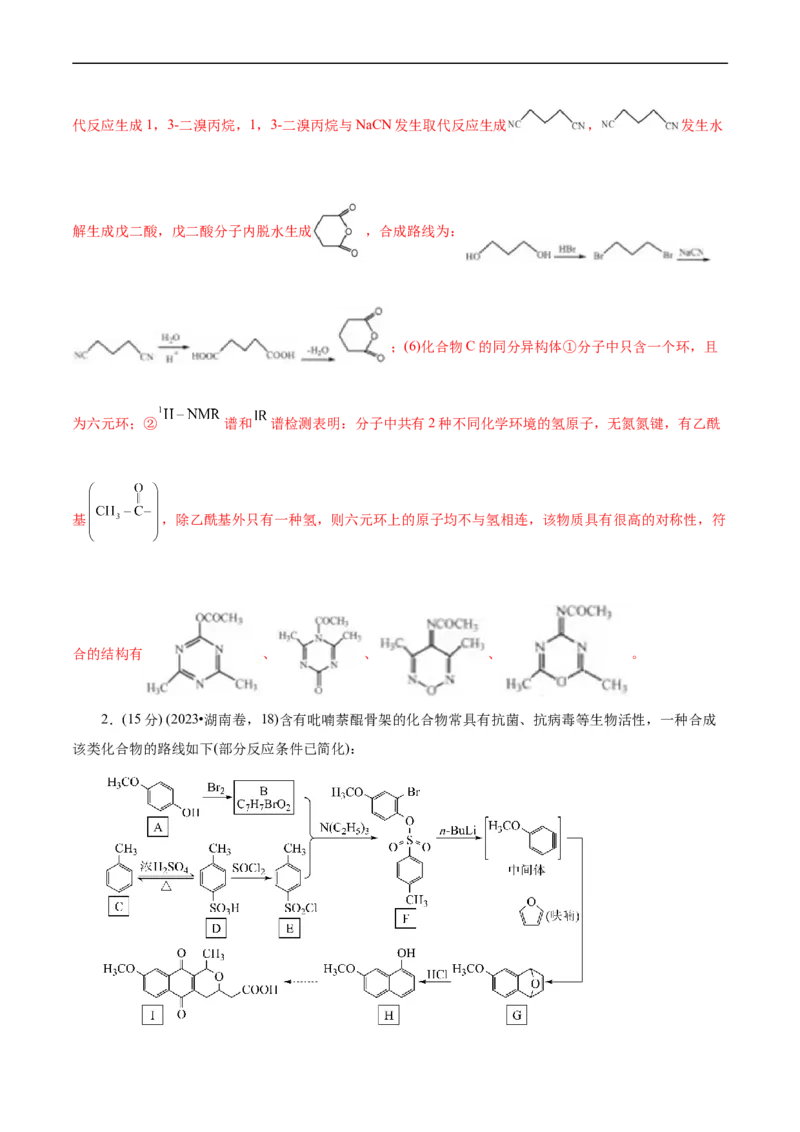
2.(15分) (2023•湖南卷,18)含有吡喃萘醌骨架的化合物常具有抗菌、抗病毒等生物活性,一种合成
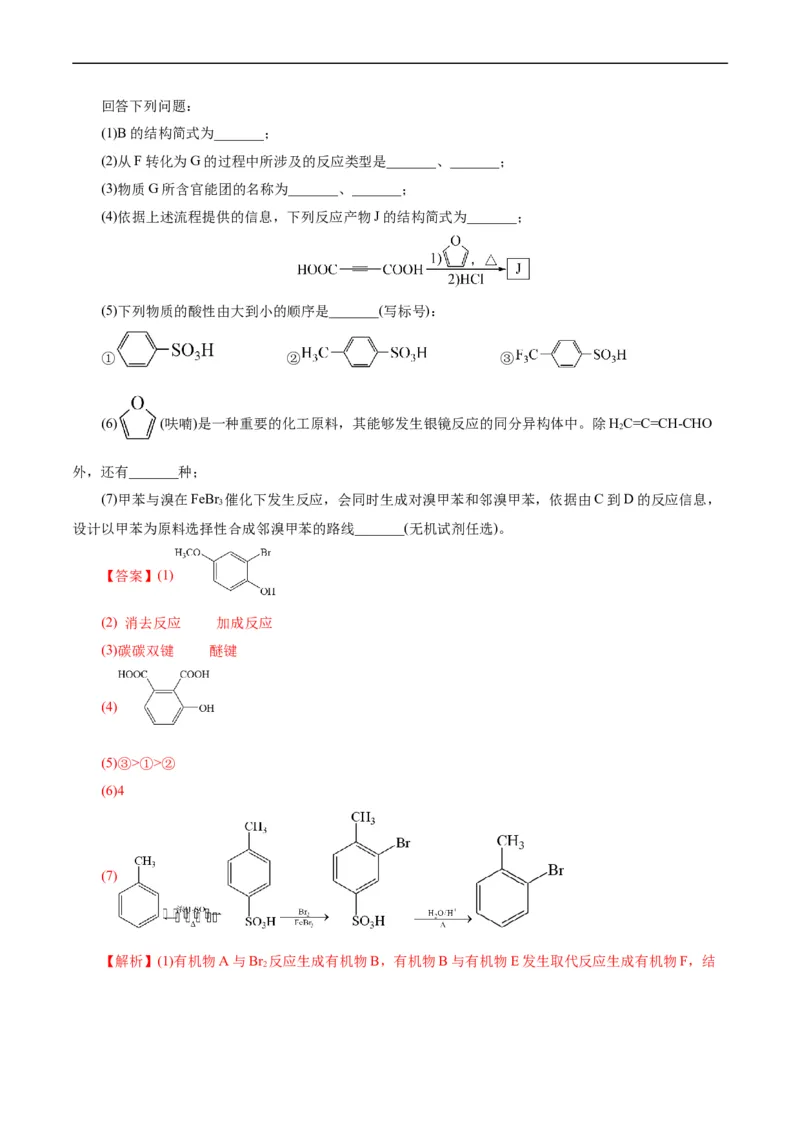
该类化合物的路线如下(部分反应条件已简化):回答下列问题:
(1)B的结构简式为_______;
(2)从F转化为G的过程中所涉及的反应类型是_______、_______;
(3)物质G所含官能团的名称为_______、_______;
(4)依据上述流程提供的信息,下列反应产物J的结构简式为_______;
(5)下列物质的酸性由大到小的顺序是_______(写标号):
① ② ③
(6) (呋喃)是一种重要的化工原料,其能够发生银镜反应的同分异构体中。除HC=C=CH-CHO
2
外,还有_______种;
(7)甲苯与溴在FeBr 催化下发生反应,会同时生成对溴甲苯和邻溴甲苯,依据由C到D的反应信息,
3
设计以甲苯为原料选择性合成邻溴甲苯的路线_______(无机试剂任选)。
【答案】(1)
(2) 消去反应 加成反应
(3)碳碳双键 醚键
(4)
(5)③>①>②
(6)4
(7)
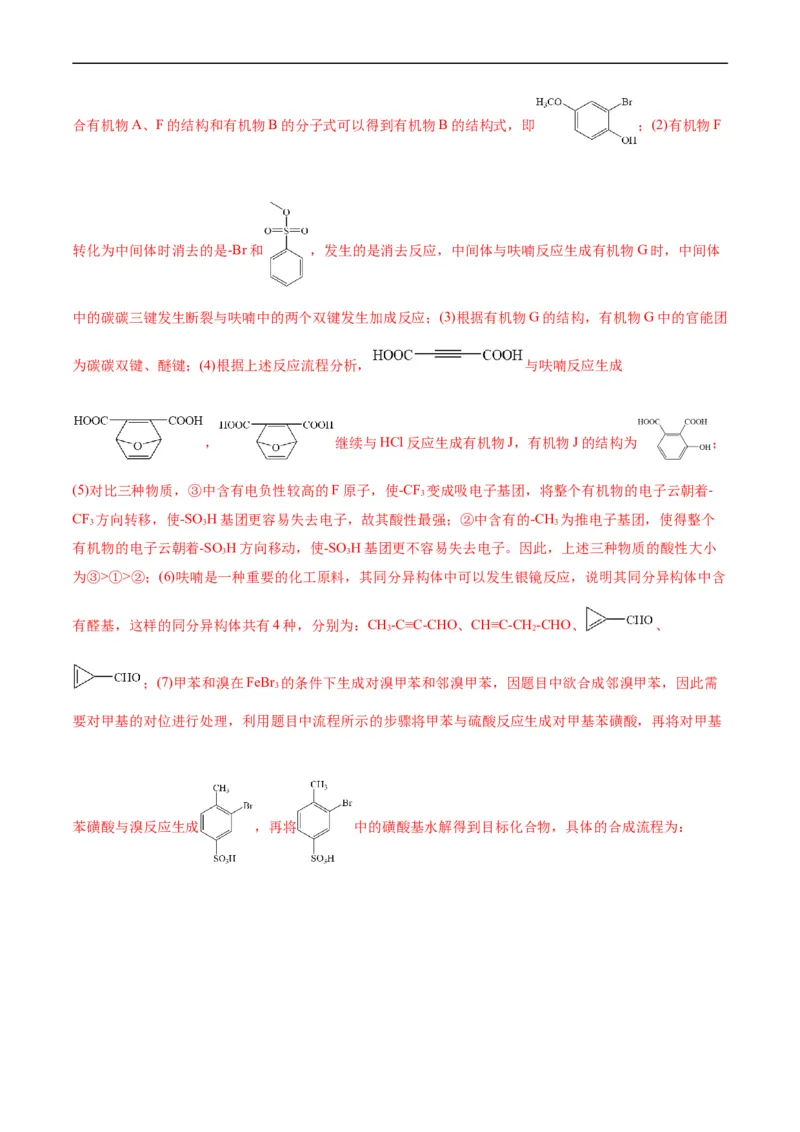
【解析】(1)有机物A与Br 反应生成有机物B,有机物B与有机物E发生取代反应生成有机物F,结
2合有机物A、F的结构和有机物B的分子式可以得到有机物B的结构式,即 ;(2)有机物F
转化为中间体时消去的是-Br和 ,发生的是消去反应,中间体与呋喃反应生成有机物G时,中间体
中的碳碳三键发生断裂与呋喃中的两个双键发生加成反应;(3)根据有机物G的结构,有机物G中的官能团
为碳碳双键、醚键;(4)根据上述反应流程分析, 与呋喃反应生成
, 继续与HCl反应生成有机物J,有机物J的结构为 ;
(5)对比三种物质,③中含有电负性较高的F原子,使-CF 变成吸电子基团,将整个有机物的电子云朝着-
3
CF 方向转移,使-SO H基团更容易失去电子,故其酸性最强;②中含有的-CH 为推电子基团,使得整个
3 3 3
有机物的电子云朝着-SO H方向移动,使-SO H基团更不容易失去电子。因此,上述三种物质的酸性大小
3 3
为③>①>②;(6)呋喃是一种重要的化工原料,其同分异构体中可以发生银镜反应,说明其同分异构体中含
有醛基,这样的同分异构体共有4种,分别为:CH-C≡C-CHO、CH≡C-CH -CHO、 、
3 2
;(7)甲苯和溴在FeBr 的条件下生成对溴甲苯和邻溴甲苯,因题目中欲合成邻溴甲苯,因此需
3
要对甲基的对位进行处理,利用题目中流程所示的步骤将甲苯与硫酸反应生成对甲基苯磺酸,再将对甲基
苯磺酸与溴反应生成 ,再将 中的磺酸基水解得到目标化合物,具体的合成流程为:。
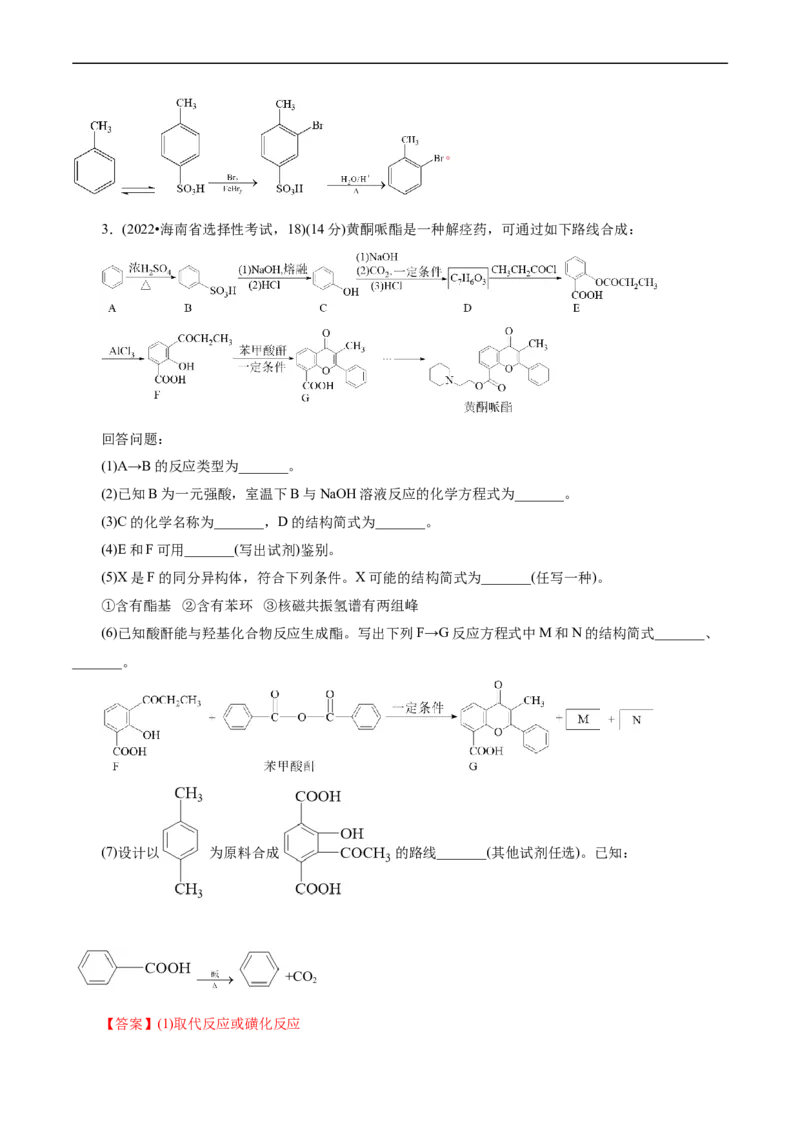
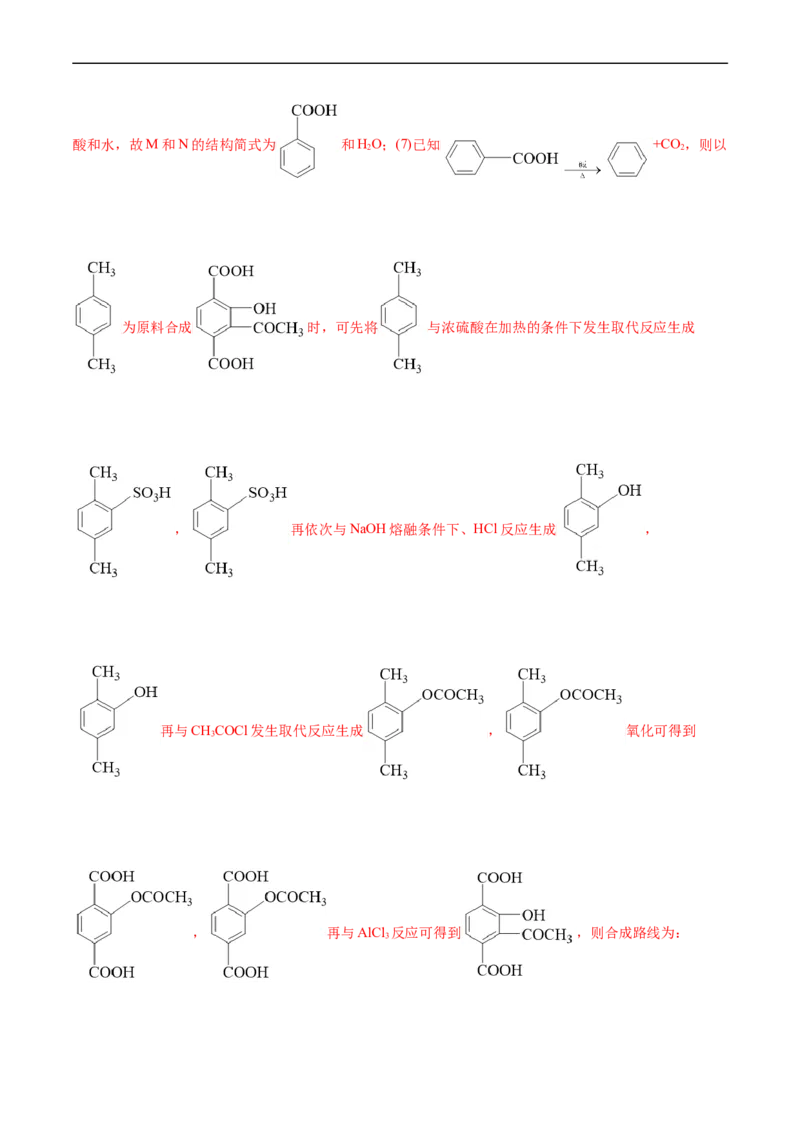
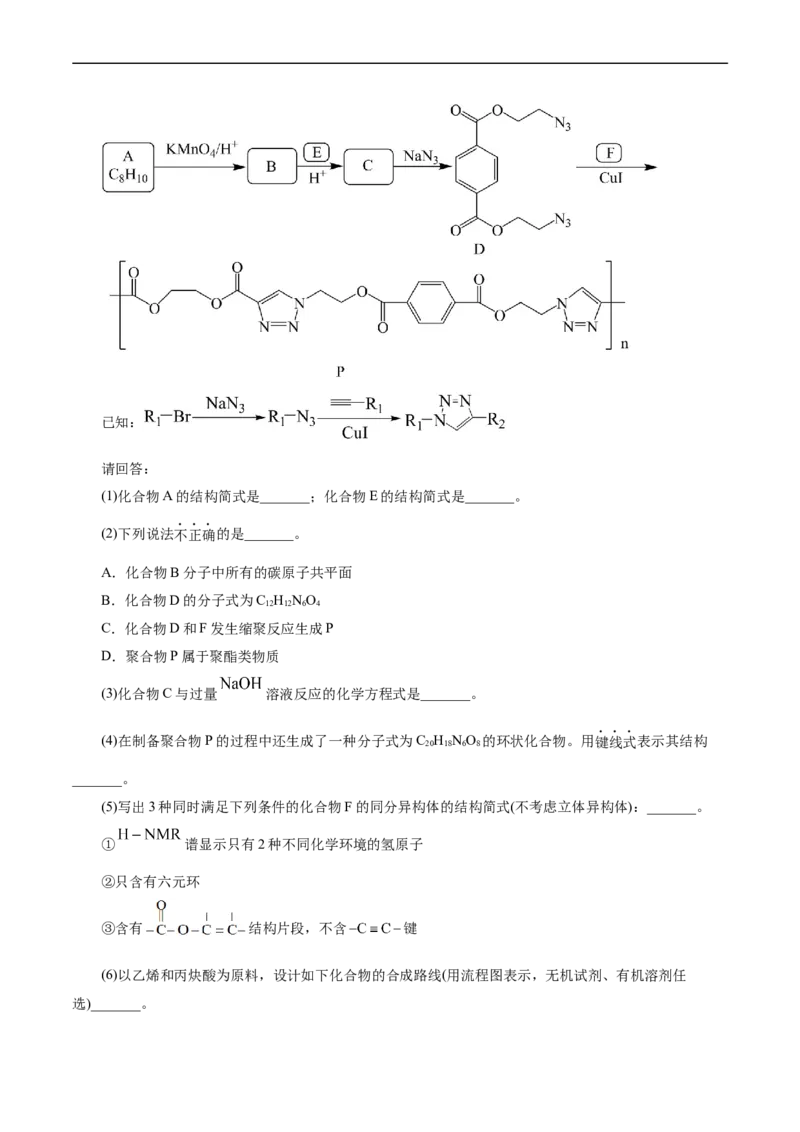
3.(2022•海南省选择性考试,18)(14分)黄酮哌酯是一种解痉药,可通过如下路线合成:
回答问题:
(1)A→B的反应类型为_______。
(2)已知B为一元强酸,室温下B与NaOH溶液反应的化学方程式为_______。
(3)C的化学名称为_______,D的结构简式为_______。
(4)E和F可用_______(写出试剂)鉴别。
(5)X是F的同分异构体,符合下列条件。X可能的结构简式为_______(任写一种)。
①含有酯基 ②含有苯环 ③核磁共振氢谱有两组峰
(6)已知酸酐能与羟基化合物反应生成酯。写出下列F→G反应方程式中M和N的结构简式_______、
_______。
(7)设计以 为原料合成 的路线_______(其他试剂任选)。已知:
+CO
2
【答案】(1)取代反应或磺化反应(2) +NaOH→ +H O
2
(3)苯酚
(4) FeCl (溶液)或其他合理答案
3
(5) 或 (6) h o
2
(7)
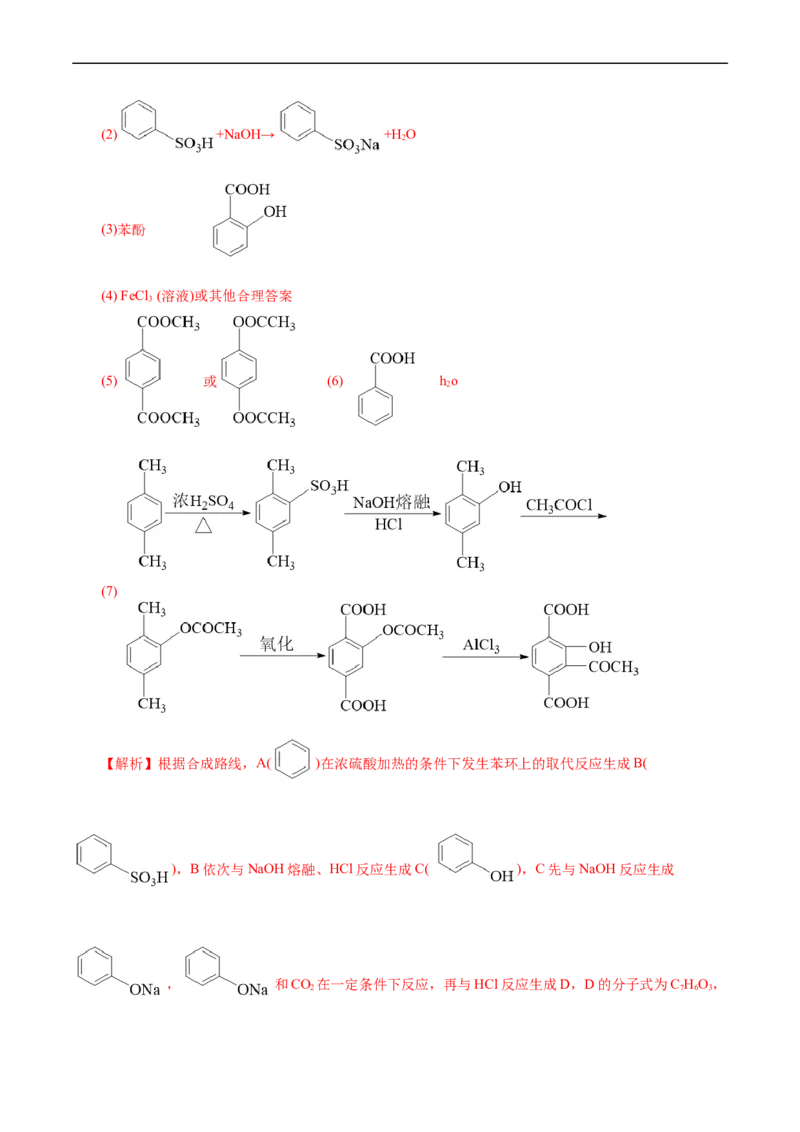
【解析】根据合成路线,A( )在浓硫酸加热的条件下发生苯环上的取代反应生成B(
),B依次与NaOH熔融、HCl反应生成C( ),C先与NaOH反应生成
, 和CO 在一定条件下反应,再与HCl反应生成D,D的分子式为C HO,
2 7 6 3则D为 ,D再与CHCHCOCl发生取代反应生成E,E与AlCl 反应生成F,F与苯甲酸肝在
3 2 3
一定条件下生成G,G经一系列反应生成黄铜哌酯。(1)由分析可知,A( )在浓硫酸加热的条件下发
生苯环上的取代反应生成B( ),即反应类型为取代反应(或磺化反应);(2)B为一元强酸,室
温下B与NaOH溶液反应生成 和HO,反应的化学方程式为 +NaOH→
2
+H O;(3)C的结构简式为 ,则化学名称为苯酚,根据分析可知,D的结构
2
简式为 ;(4)由E、F的结构简式可知,F含有酚羟基,而E没有,因此可用FeCl 溶液鉴别二
3
者,前者溶液变成紫色,后者无明显现象;(5)F的分子式为C H O,X是F的同分异构体,X含有苯环
10 10 4
和酯基,其核磁共振氢谱有两组峰,说明X只有2种不同环境的H原子,则满足条件的X的结构简式为:
或 ;(6)酸酐能与羟基化合物反应生成酯,则F与苯甲酸肝反应可生成G、苯甲酸和水,故M和N的结构简式为 和HO;(7)已知 +CO ,则以
2 2
为原料合成 时,可先将 与浓硫酸在加热的条件下发生取代反应生成
, 再依次与NaOH熔融条件下、HCl反应生成 ,
再与CHCOCl发生取代反应生成 , 氧化可得到
3
, 再与AlCl 反应可得到 ,则合成路线为:
3。
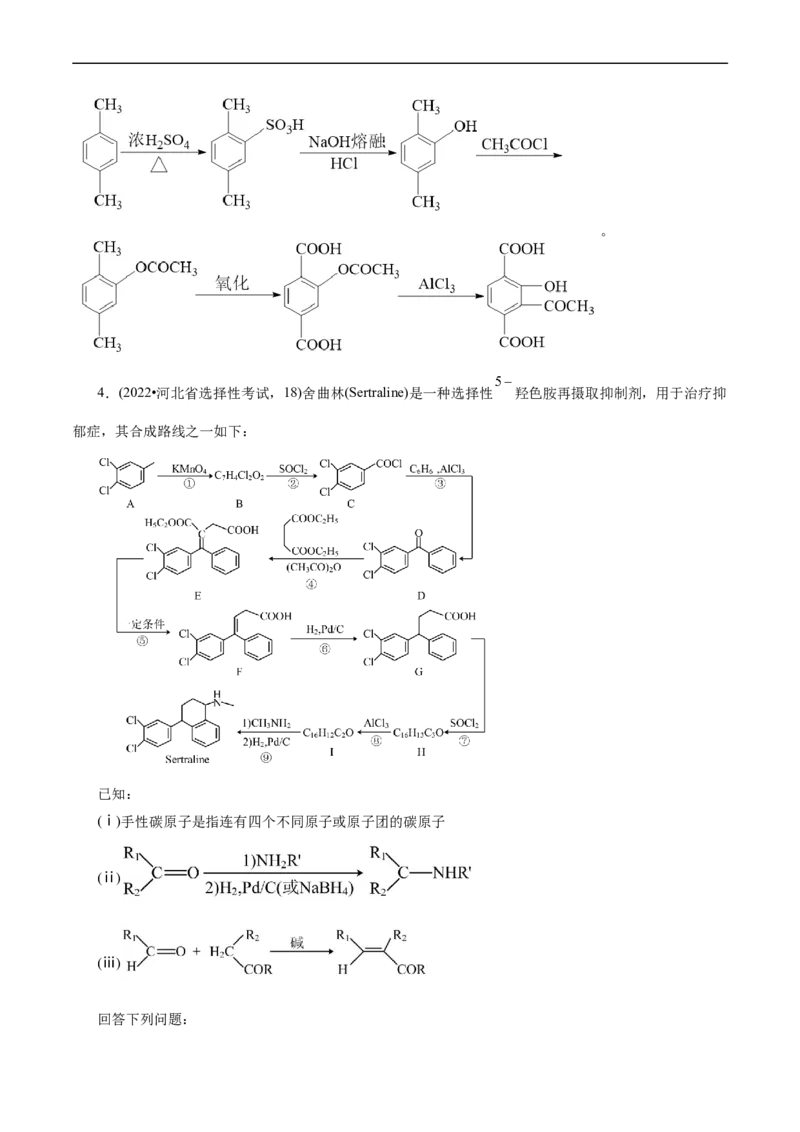
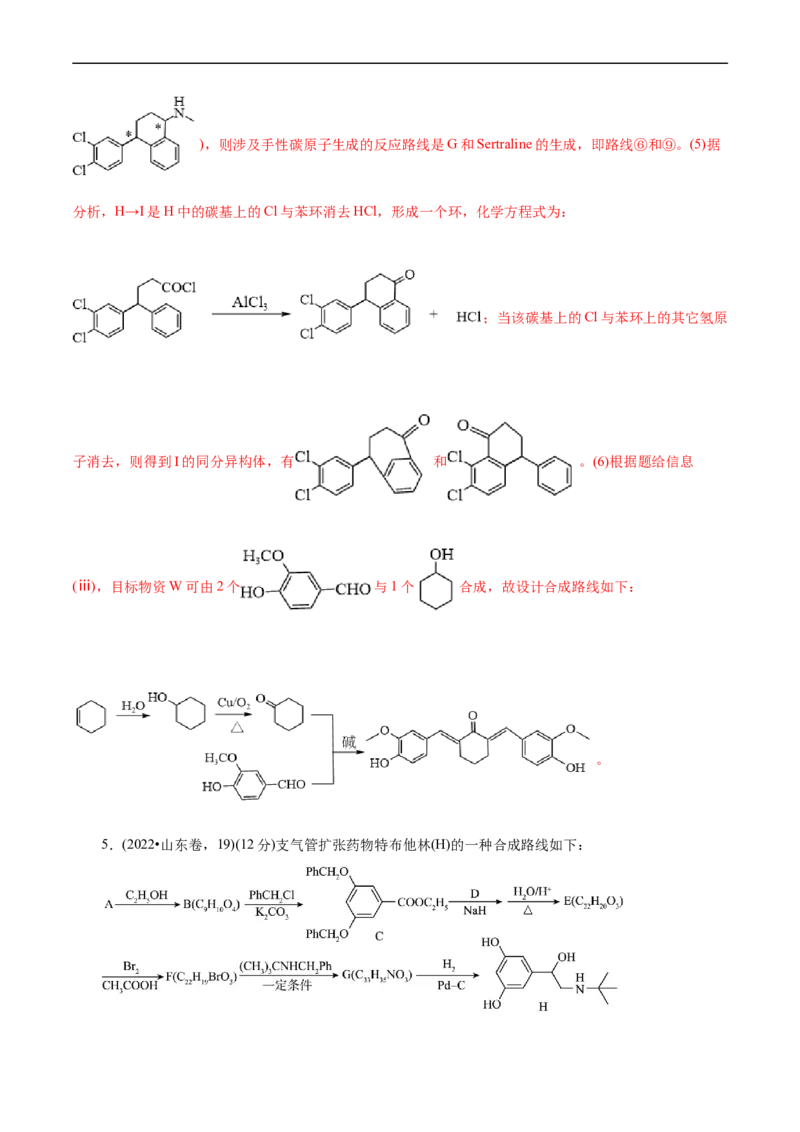
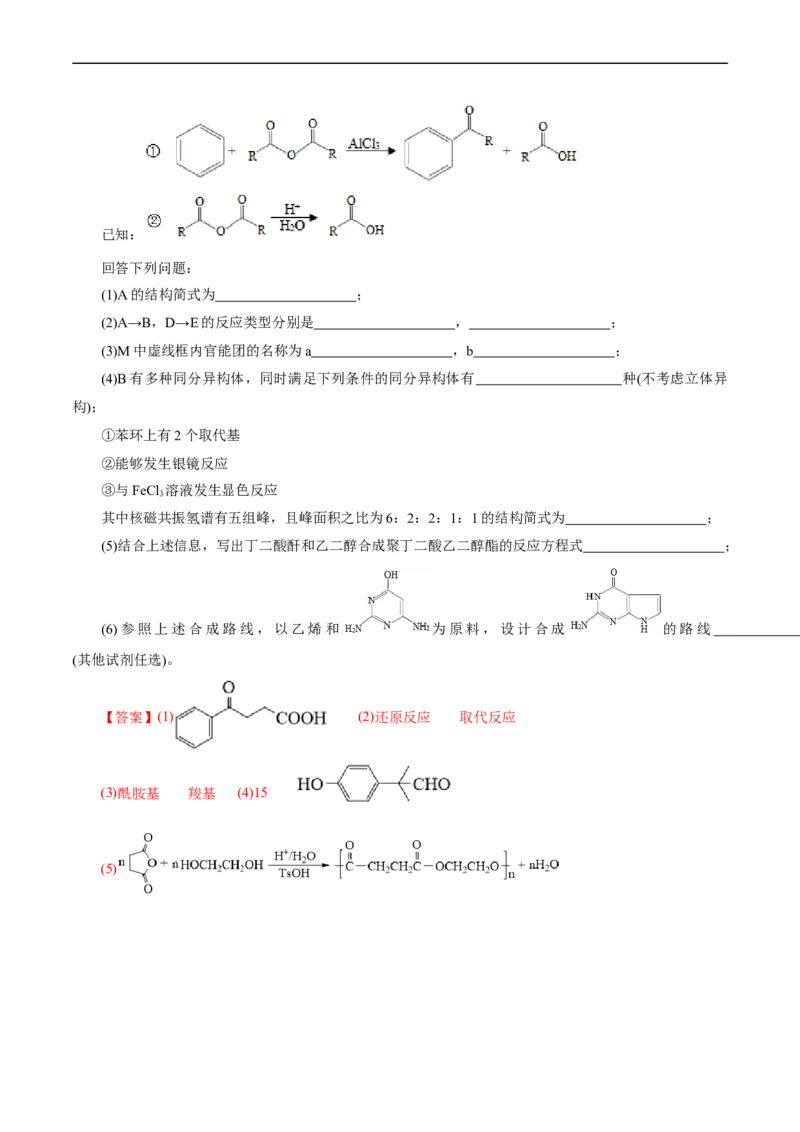
4.(2022•河北省选择性考试,18)舍曲林(Sertraline)是一种选择性 羟色胺再摄取抑制剂,用于治疗抑
郁症,其合成路线之一如下:
已知:
(ⅰ)手性碳原子是指连有四个不同原子或原子团的碳原子
(ⅱ)
(ⅲ)
回答下列问题:(1)①的反应类型为_______。
(2)B的化学名称为_______。
(3)写出一种能同时满足下列条件的D的芳香族同分异构体的结构简式_______。
(a)红外光谱显示有 键;(b)核磁共振氢谱有两组峰,峰面积比为1∶1。
(4)合成路线中,涉及手性碳原子生成的反应路线为_______、_______(填反应路线序号)。
(5)H→I的化学方程式为_______,反应还可生成与I互为同分异构体的两种副产物,其中任意一种的结
构简式为_______(不考虑立体异构)。
(6)W是一种姜黄素类似物,以香兰素( )和环己烯( )为原料,设计合成W的
路线_______(无机及两个碳以下的有机试剂任选)。
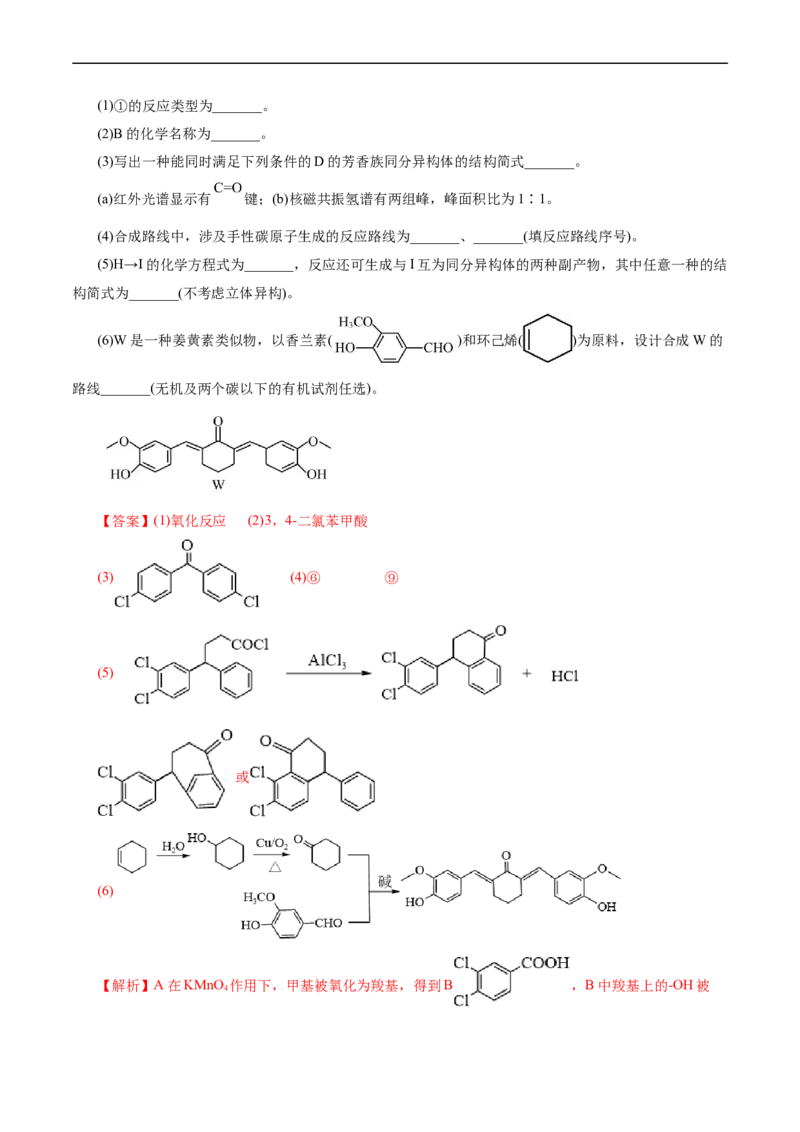
【答案】(1)氧化反应 (2)3,4-二氯苯甲酸
(3) (4)⑥ ⑨
(5)
或
(6)
【解析】A在KMnO 作用下,甲基被氧化为羧基,得到B ,B中羧基上的-OH被
4SOCl 中的Cl取代得到C,C中的Cl原子与苯环上的H原子在AlCl 环境发生消去反应得到D,D中羰基
2 3
在 和乙酸酐共同作用下生成碳碳双键得到E,E在一定条件下脱去酯基生成F,F中的碳碳
双键加氢得到G,G与SOCl 反应得到H ,H脱去HCl得到I
2
,I中的羰基发生已知(ⅱ)的反应得到目标产物舍曲林。(1)①是 中的甲基被KMnO 氧化为羧基,
4
反应类型是氧化反应。(2)据分析,B的结构简式是 ,名称是3,4-二氯苯甲酸。(3)从D
的结构简式可知,其分子式为C HClO,能满足核磁共振氢谱两组峰,且峰面积比为1:1的结构应是高
13 8 2
度对称结构,又含有C=O,则该芳香族同分异构体的结构简式为: 。(4)手性碳原
子指连接四个不同原子或原子团的碳,题给合成路线中涉及手性碳原子的物质是G(
)、H( )、I( )和Sertraline(),则涉及手性碳原子生成的反应路线是G和Sertraline的生成,即路线⑥和⑨。(5)据
分析,H→I是H中的碳基上的Cl与苯环消去HCl,形成一个环,化学方程式为:
;当该碳基上的Cl与苯环上的其它氢原
子消去,则得到I的同分异构体,有 和 。(6)根据题给信息
(ⅲ),目标物资W可由2个 与1个 合成,故设计合成路线如下:
。
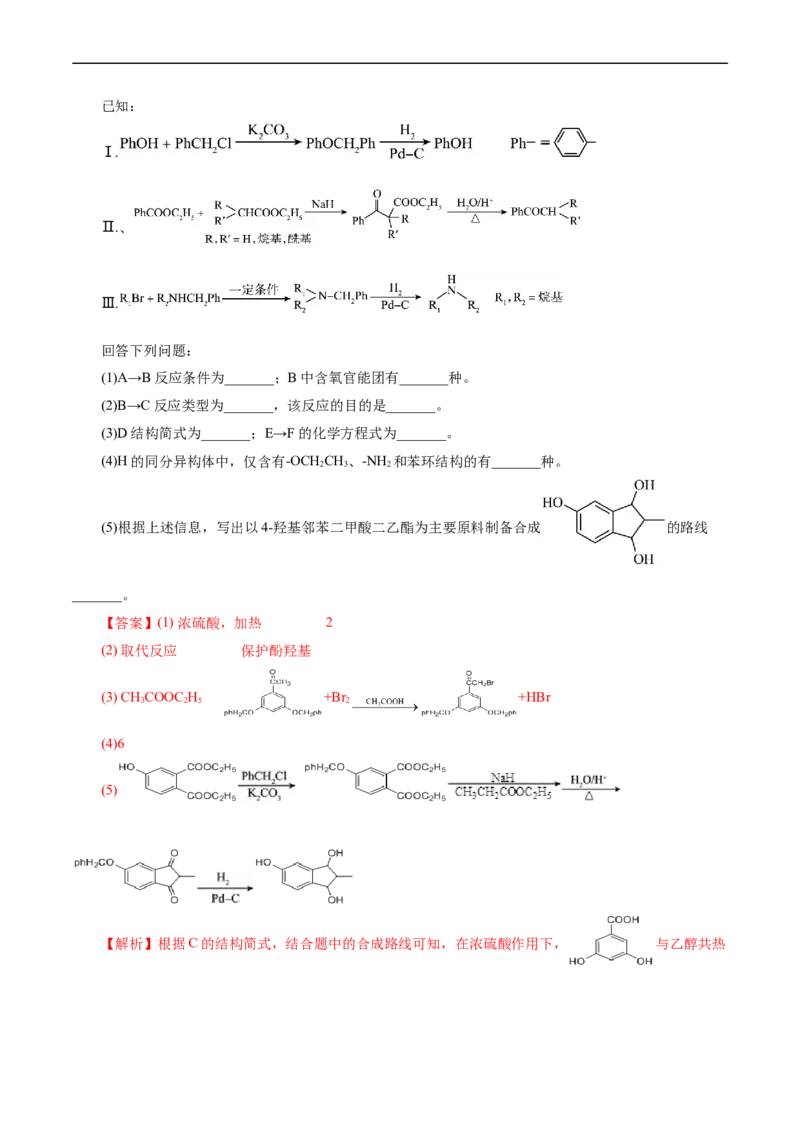
5.(2022•山东卷,19)(12分)支气管扩张药物特布他林(H)的一种合成路线如下:已知:
Ⅰ.
Ⅱ.、
Ⅲ.
回答下列问题:
(1)A→B反应条件为_______;B中含氧官能团有_______种。
(2)B→C反应类型为_______,该反应的目的是_______。
(3)D结构简式为_______;E→F的化学方程式为_______。
(4)H的同分异构体中,仅含有-OCH CH、-NH 和苯环结构的有_______种。
2 3 2
(5)根据上述信息,写出以4-羟基邻苯二甲酸二乙酯为主要原料制备合成 的路线
_______。
【答案】(1) 浓硫酸,加热 2
(2) 取代反应 保护酚羟基
(3) CH COOC H +Br +HBr
3 2 5 2
(4)6
(5)
【解析】根据C的结构简式,结合题中的合成路线可知,在浓硫酸作用下, 与乙醇共热发生酯化反应生成 ,则A为 、B为 ;在碳酸钾作用下
与phCHCl发生取代反应生成 , 与
2
CHCOOC H 发生信息Ⅱ反应生成 ,则D为CHCOOC H、E为
3 2 5 3 2 5
;在乙酸作用下 与溴发生取代反应生成 ,
则F为 ;一定条件下 与(CH)CNHCH ph发生取代反应
3 3 2
,则G为 ; 在Pd—C做催化剂作用下与
氢气反应生成H。(1)A→B的反应为在浓硫酸作用下, 与乙醇共热发生酯化反应生成 和
水;B的结构简式为为 ,含氧官能团为羟基、酯基,共有2种;(2)由分析可知,B→C的反
应为在碳酸钾作用下 与phCHCl发生取代反应生成 和氯化氢,由B和
2
H都含有酚羟基可知,B→C的目的是保护酚羟基;(3)由分析可知,D的结构简式为CHCOOC H;E→F
3 2 5的反应为在乙酸作用下 与溴发生取代反应生成 和溴化氢,反应
的化学方程式为 +Br +HBr;(4)H的同分异构体仅
2
含有—OCH CH 和—NH 可知,同分异构体的结构可以视作 、 、
2 3 2
分子中苯环上的氢原子被—NH 取代所得结构,所得结构分别有1、3、2,共有6种;(5)由
2
题给信息可知,以4—羟基邻苯二甲酸二乙酯制备 的合成步骤为在碳酸钾作用下
与phCHCl发生取代反应生成发生取代反应生成 ,
2
发生信息Ⅱ反应生成 , 在Pd—C做催化剂
作用下与氢气反应生成 ,合成路线为。
6.(15分) (2022•湖南选择性考试,19)物质J是一种具有生物活性的化合物。该化合物的合成路线如
下:
已知:① +[Ph CHR']Br-
3 2
②
回答下列问题:
(1)A中官能团的名称为_______、_______;
(2)F→G、G→H的反应类型分别是_______、_______;
(3)B的结构简式为_______;
(4)C→D反应方程式为_______;
(5) 是一种重要的化工原料,其同分异构体中能够发生银镜反应的有_______种(考虑立
体异构),其中核磁共振氢谱有3组峰,且峰面积之比为4:1:1的结构简式为_______;
(6)Ⅰ中的手性碳原子个数为_______(连四个不同的原子或原子团的碳原子称为手性碳原子);(7)参照上述合成路线,以 和 为原料,设计合成 的路线
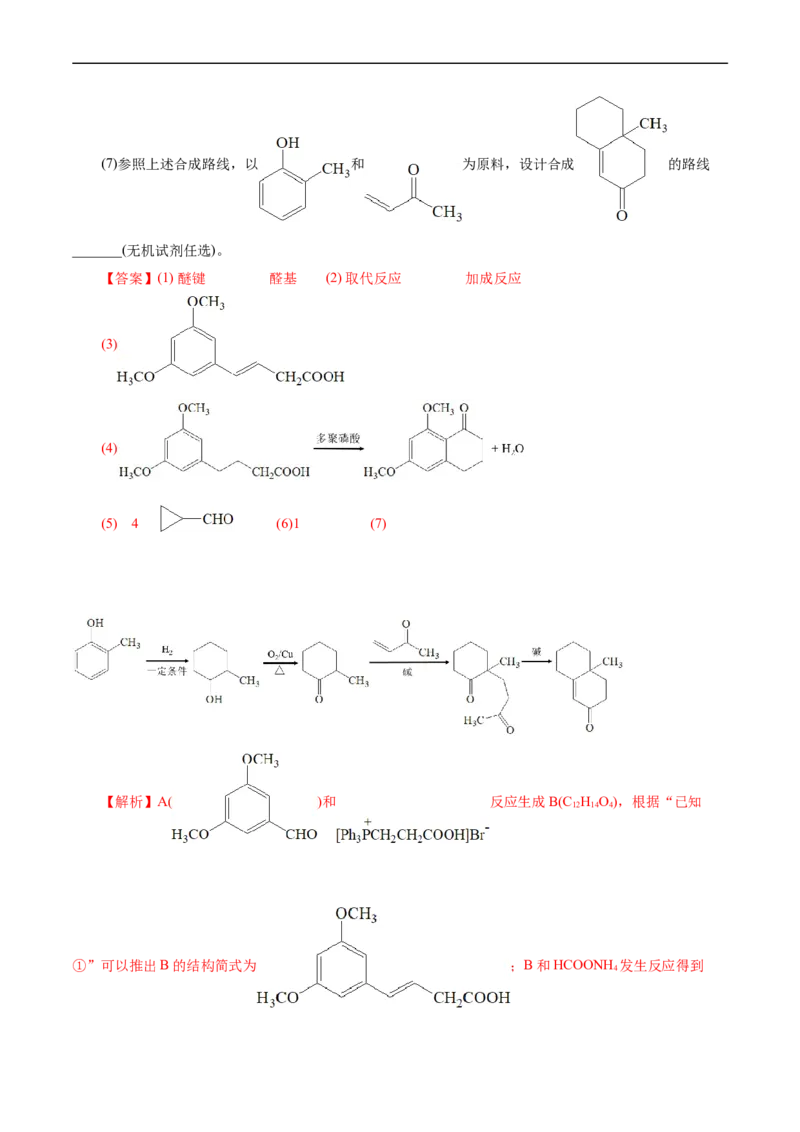
_______(无机试剂任选)。
【答案】(1) 醚键 醛基 (2) 取代反应 加成反应
(3)
(4)
(5) 4 (6)1 (7)
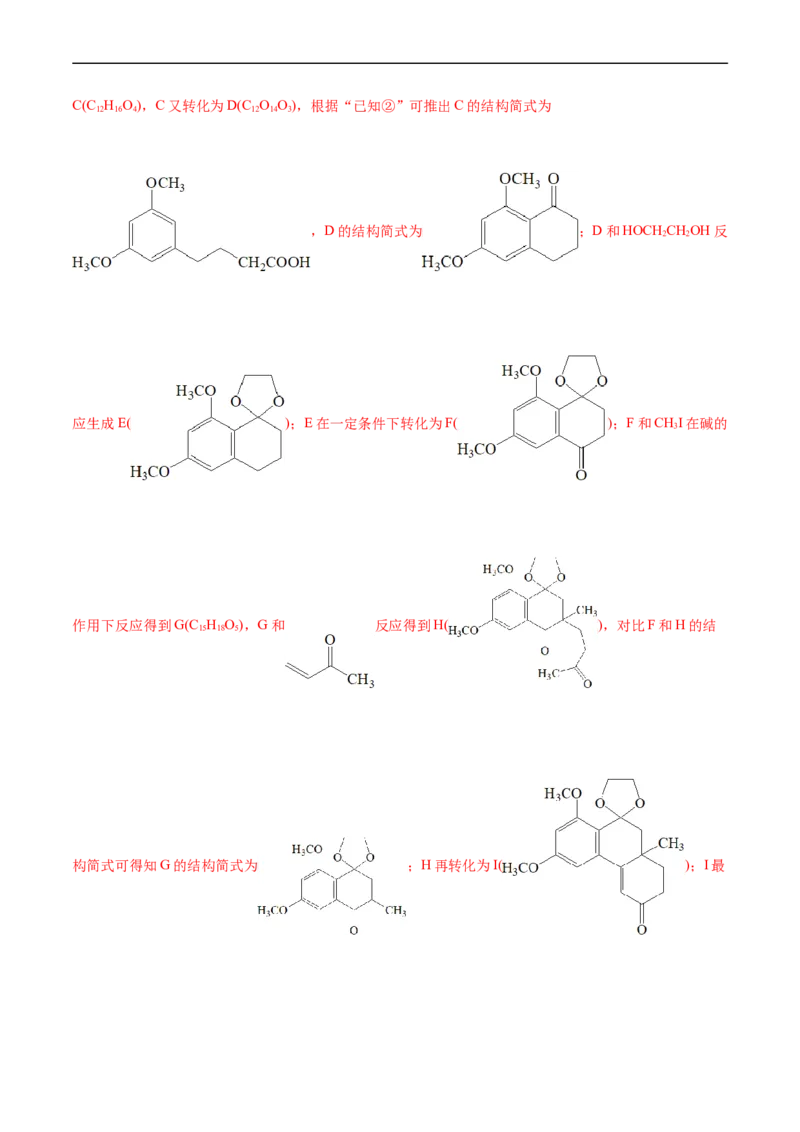
【解析】A( )和 反应生成B(C H O),根据“已知
12 14 4
①”可以推出B的结构简式为 ;B和HCOONH 发生反应得到
4C(C H O),C又转化为D(C O O),根据“已知②”可推出C的结构简式为
12 16 4 12 14 3
,D的结构简式为 ;D和HOCH CHOH反
2 2
应生成E( );E在一定条件下转化为F( );F和CHI在碱的
3
作用下反应得到G(C H O),G和 反应得到H( ),对比F和H的结
15 18 5
构简式可得知G的结构简式为 ;H再转化为I( );I最终转化为J( )。(1)A的结构简式为 ,其官能团为醚键和
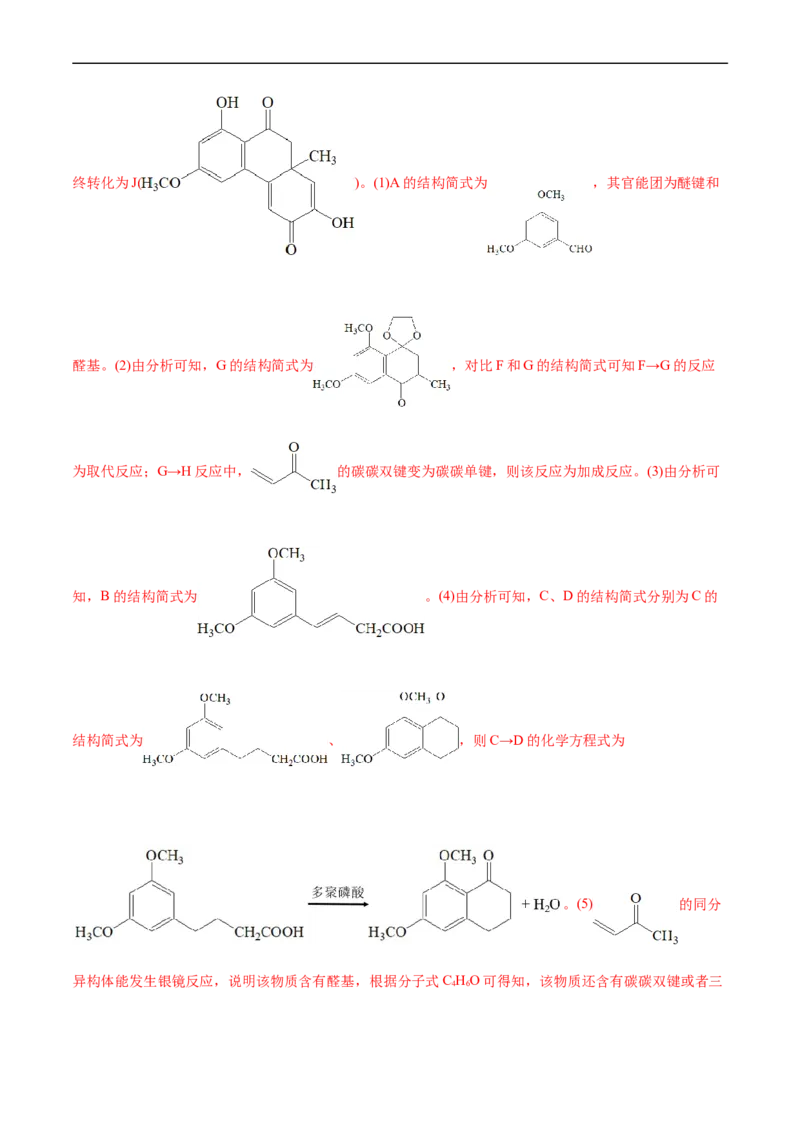
醛基。(2)由分析可知,G的结构简式为 ,对比F和G的结构简式可知F→G的反应
为取代反应;G→H反应中, 的碳碳双键变为碳碳单键,则该反应为加成反应。(3)由分析可
知,B的结构简式为 。(4)由分析可知,C、D的结构简式分别为C的
结构简式为 、 ,则C→D的化学方程式为
。(5) 的同分
异构体能发生银镜反应,说明该物质含有醛基,根据分子式C HO可得知,该物质还含有碳碳双键或者三
4 6元环,则符合条件的同分异构体有4种,它们分别是CH=CHCHCHO、 、
2 2
和 ,其中核磁共振氢谱有3组峰,且峰面积之比为4:1:1的结构简式是
。(6)连四个不同的原子或原子团的碳原子成为手性碳原子,则I中手性碳原子的个数为1,是
连有甲基的碳原子。(7)结合G→I的转化过程可知,可先将 转化为 ,再使
和 反应生成 ,并最终转化为 ;综上所述,合成路线
为: 。
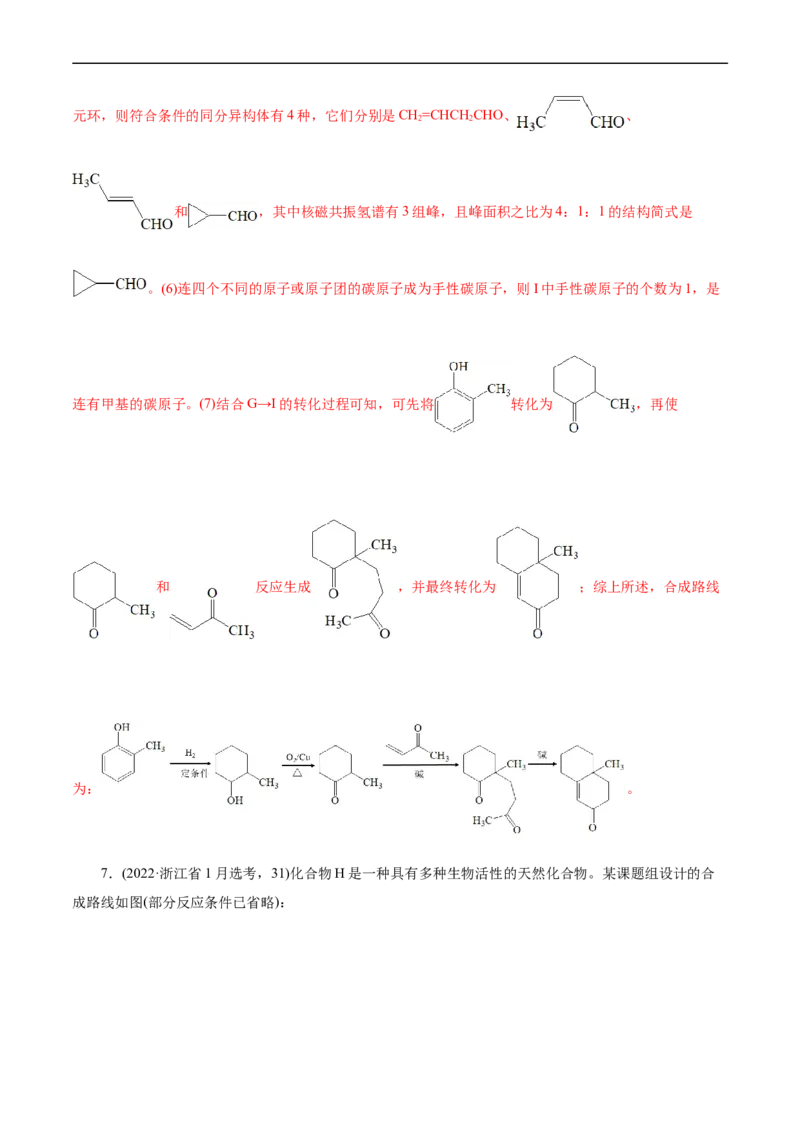
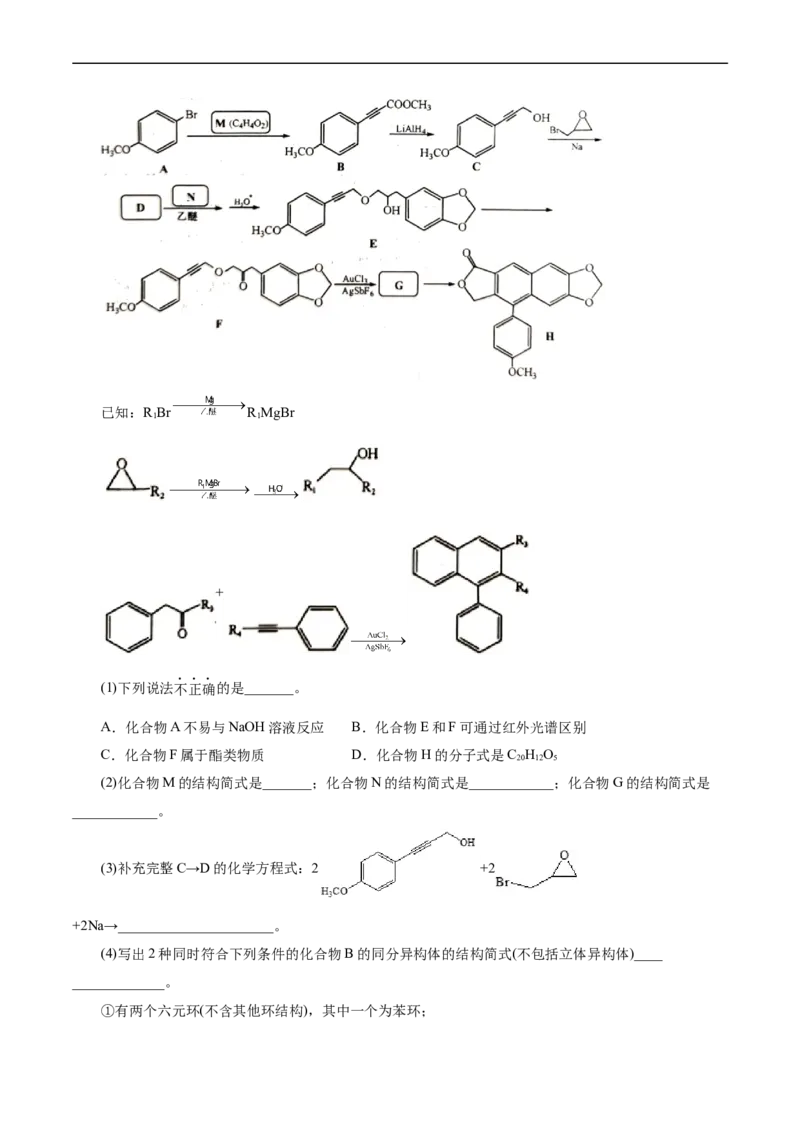
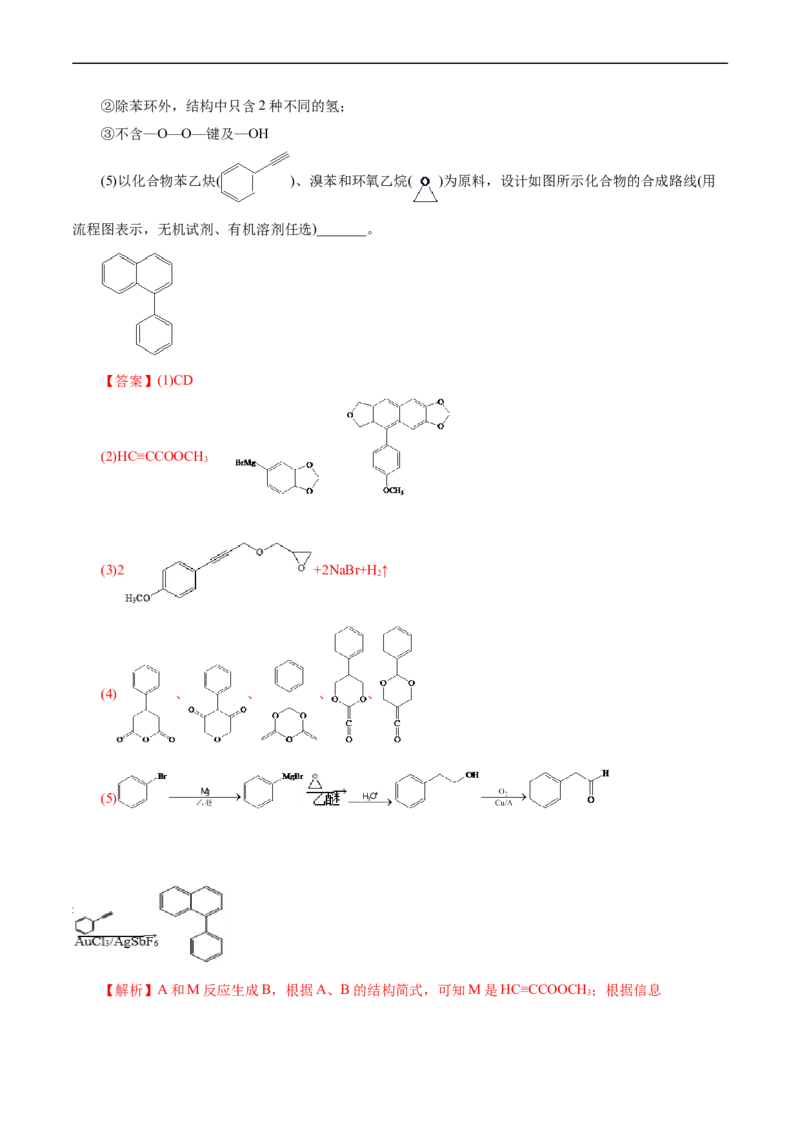
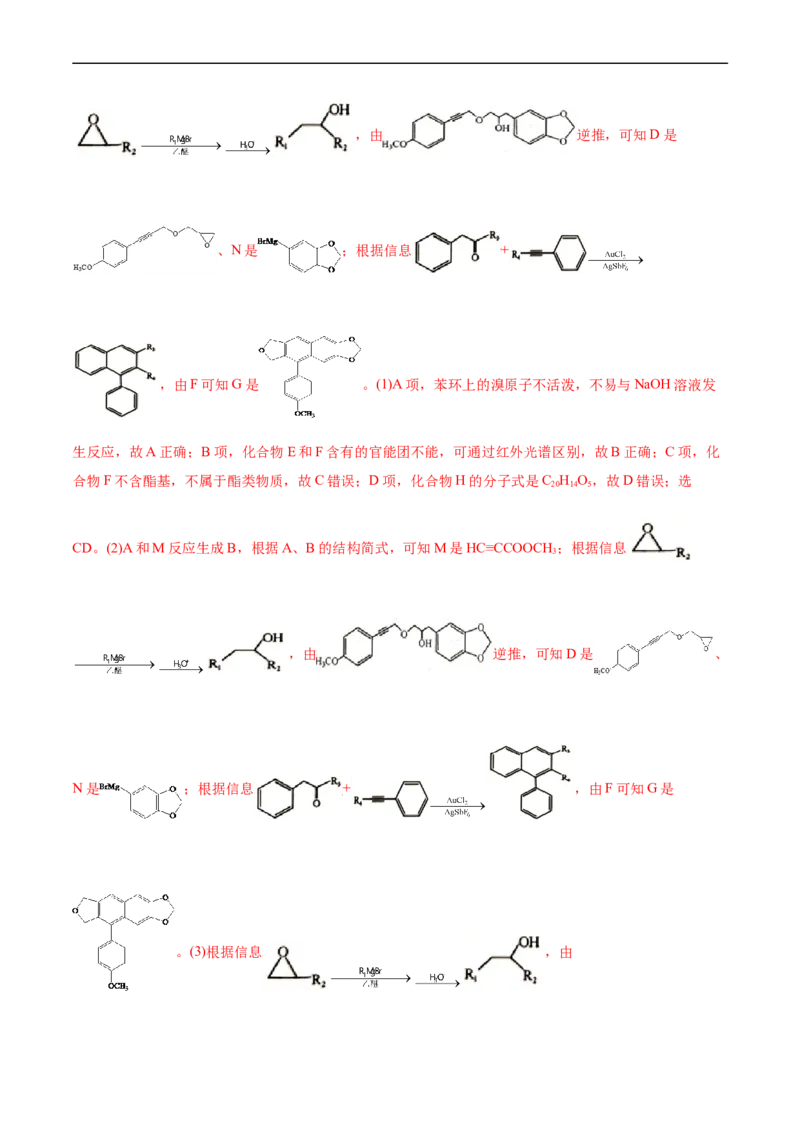
7.(2022·浙江省1月选考,31)化合物H是一种具有多种生物活性的天然化合物。某课题组设计的合
成路线如图(部分反应条件已省略):已知:R Br R MgBr
1 1
+
(1)下列说法不正确的是_______。
A.化合物A不易与NaOH溶液反应 B.化合物E和F可通过红外光谱区别
C.化合物F属于酯类物质 D.化合物H的分子式是C H O
20 12 5
(2)化合物M的结构简式是_______;化合物N的结构简式是____________;化合物G的结构简式是
____________。
(3)补充完整C→D的化学方程式:2 +2
+2Na→______________________。
(4)写出2种同时符合下列条件的化合物B的同分异构体的结构简式(不包括立体异构体)____
_____________。
①有两个六元环(不含其他环结构),其中一个为苯环;②除苯环外,结构中只含2种不同的氢;
③不含—O—O—键及—OH
(5)以化合物苯乙炔( )、溴苯和环氧乙烷( )为原料,设计如图所示化合物的合成路线(用
流程图表示,无机试剂、有机溶剂任选)_______。
【答案】(1)CD
(2)HC≡CCOOCH
3
(3)2 +2NaBr+H ↑
2
(4) 、 、 、 、
(5)
【解析】A和M反应生成B,根据A、B的结构简式,可知M是HC≡CCOOCH ;根据信息
3,由 逆推,可知D是
、N是 ;根据信息 +
,由F可知G是 。(1)A项,苯环上的溴原子不活泼,不易与NaOH溶液发
生反应,故A正确;B项,化合物E和F含有的官能团不能,可通过红外光谱区别,故B正确;C项,化
合物F不含酯基,不属于酯类物质,故C错误;D项,化合物H的分子式是C H O,故D错误;选
20 14 5
CD。(2)A和M反应生成B,根据A、B的结构简式,可知M是HC≡CCOOCH ;根据信息
3
,由 逆推,可知D是 、
N是 ;根据信息 + ,由F可知G是
。(3)根据信息 ,由逆推,可知D是 ,C→D的方程式是2
+2 +2Na→2 +2NaBr+H ↑;(4)①有两个六元环(不
2
含其他环结构),其中一个为苯环;②除苯环外,结构中只含2种不同的氢,说明结构对称;③不含—O—
O—键及—OH,符合条件的 的同分异构体有 、 、 、
、 。(5)溴苯和镁、乙醚反应生成 , 和环氧乙烷反应生成 ,
发生催化氧化生成 , 和苯乙炔反应生成 , 合成路线为
。
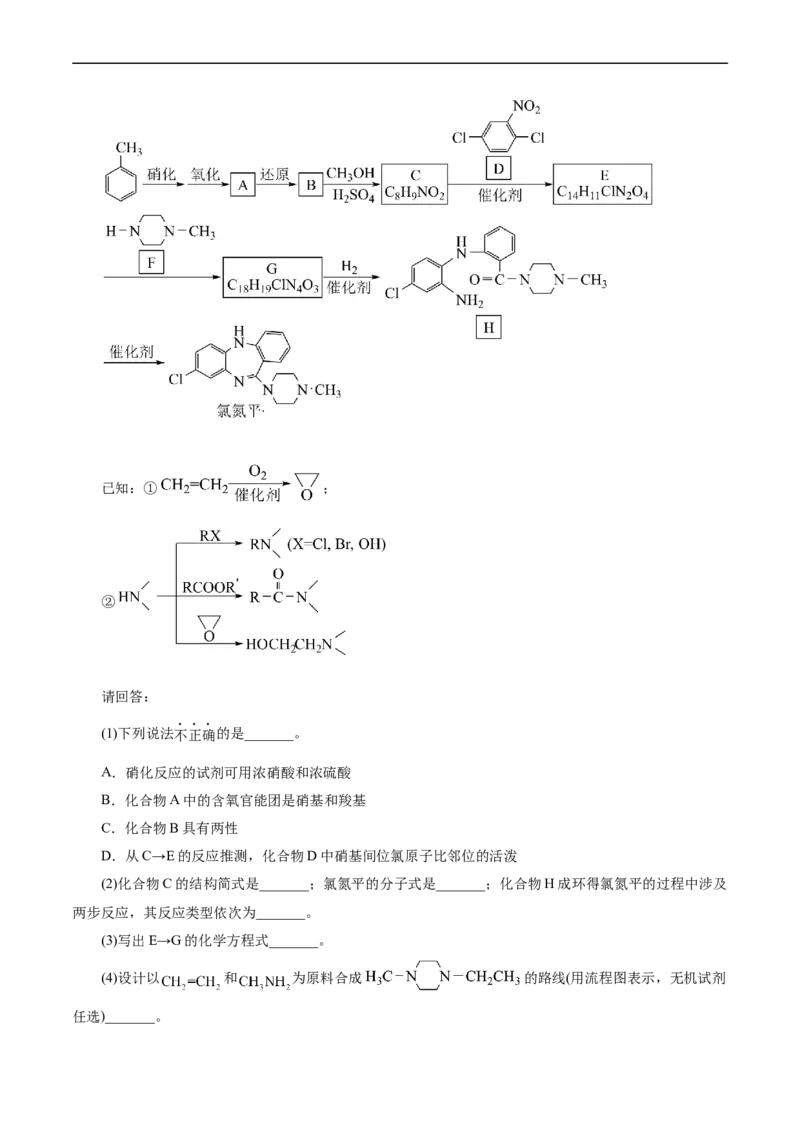
8.(2022·浙江省6月选考,31)某研究小组按下列路线合成药物氯氮平。已知:① ;
②
请回答:
(1)下列说法不正确的是_______。
A.硝化反应的试剂可用浓硝酸和浓硫酸
B.化合物A中的含氧官能团是硝基和羧基
C.化合物B具有两性
D.从C→E的反应推测,化合物D中硝基间位氯原子比邻位的活泼
(2)化合物C的结构简式是_______;氯氮平的分子式是_______;化合物H成环得氯氮平的过程中涉及
两步反应,其反应类型依次为_______。
(3)写出E→G的化学方程式_______。
(4)设计以 和 为原料合成 的路线(用流程图表示,无机试剂
任选)_______。(5)写出同时符合下列条件的化合物F的同分异构体的结构简式_______。
① 谱和IR谱检测表明:分子中共有3种不同化学环境的氢原子,有 键。
②分子中含一个环,其成环原子数 。
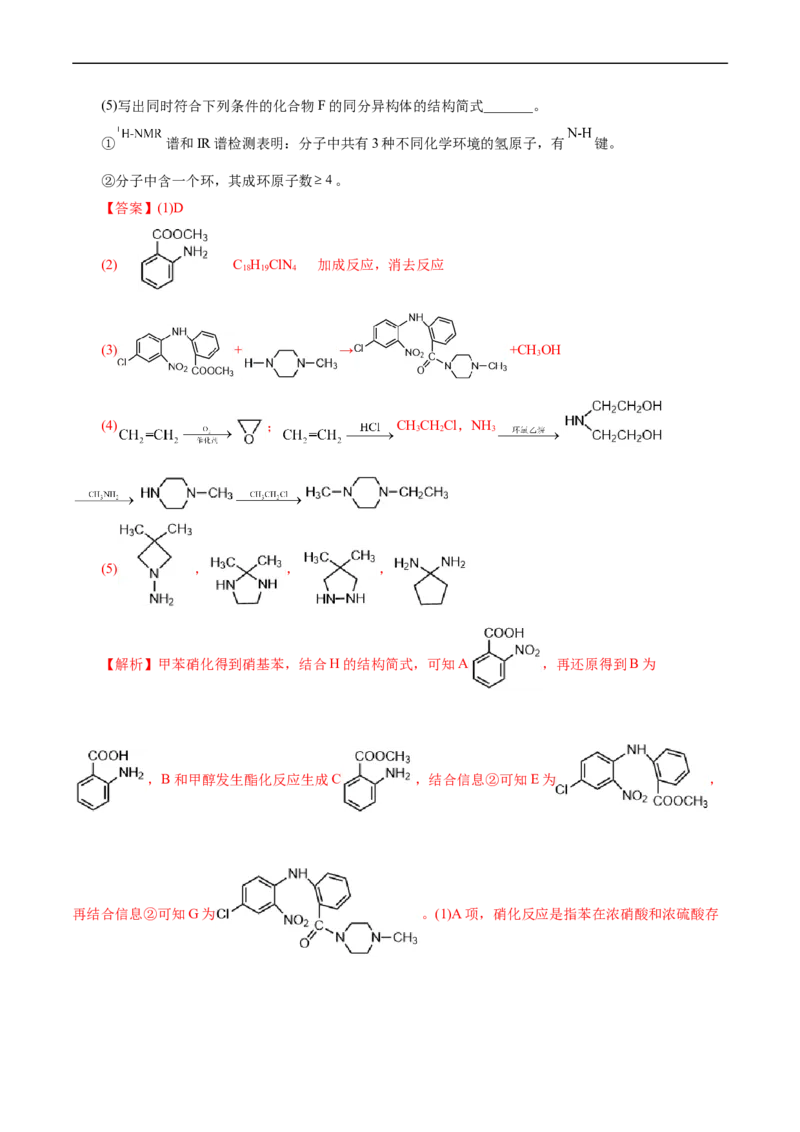
【答案】(1)D
(2) C H ClN 加成反应,消去反应
18 19 4
(3) + → +CH OH
3
(4) ; CHCHCl,NH
3 2 3
(5) , , ,
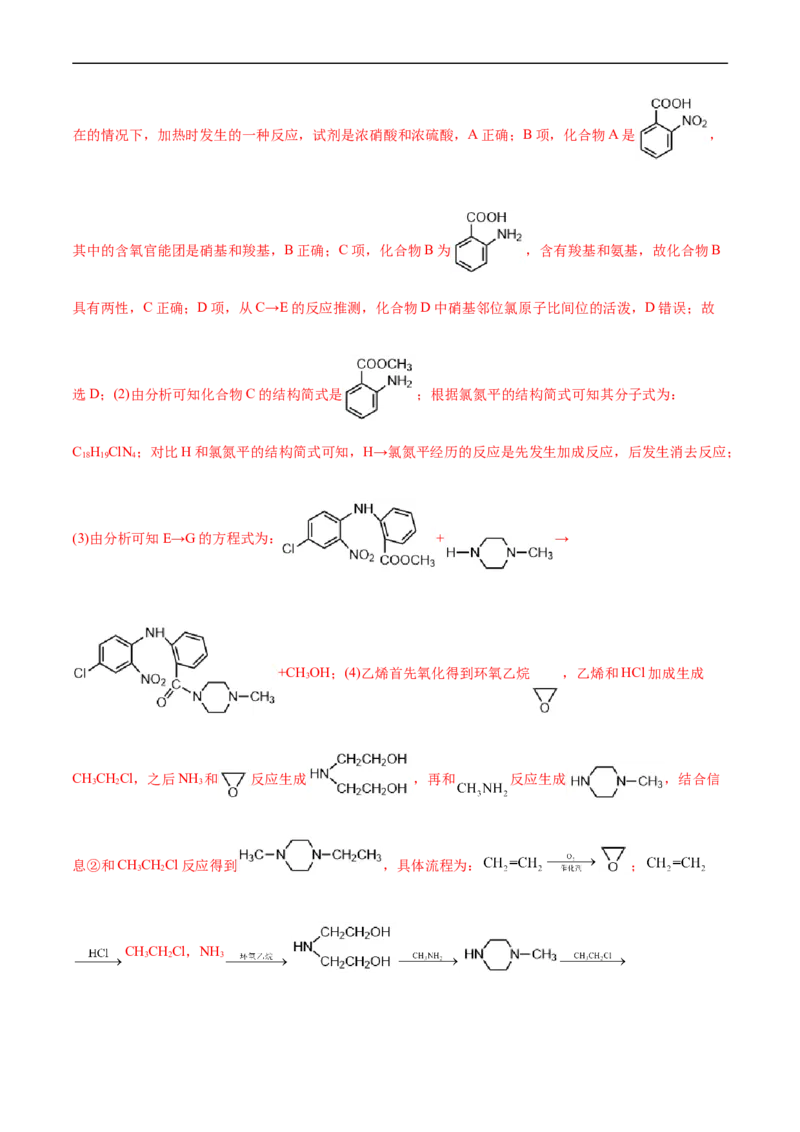
【解析】甲苯硝化得到硝基苯,结合H的结构简式,可知A ,再还原得到B为
,B和甲醇发生酯化反应生成C ,结合信息②可知E为 ,
再结合信息②可知G为 。(1)A项,硝化反应是指苯在浓硝酸和浓硫酸存在的情况下,加热时发生的一种反应,试剂是浓硝酸和浓硫酸,A正确;B项,化合物A是 ,
其中的含氧官能团是硝基和羧基,B正确;C项,化合物B为 ,含有羧基和氨基,故化合物B
具有两性,C正确;D项,从C→E的反应推测,化合物D中硝基邻位氯原子比间位的活泼,D错误;故
选D;(2)由分析可知化合物C的结构简式是 ;根据氯氮平的结构简式可知其分子式为:
C H ClN ;对比H和氯氮平的结构简式可知,H→氯氮平经历的反应是先发生加成反应,后发生消去反应;
18 19 4
(3)由分析可知E→G的方程式为: + →
+CH OH;(4)乙烯首先氧化得到环氧乙烷 ,乙烯和HCl加成生成
3
CHCHCl,之后NH 和 反应生成 ,再和 反应生成 ,结合信
3 2 3
息②和CHCHCl反应得到 ,具体流程为: ;
3 2
CHCHCl,NH
3 2 3;(5)化合物F的同分异构体,则有1个不饱和度,其有3种等效氢,含有N—H键,
且分子中含有含一个环,其成环原子数 ,则这样的结构有 , , ,
。
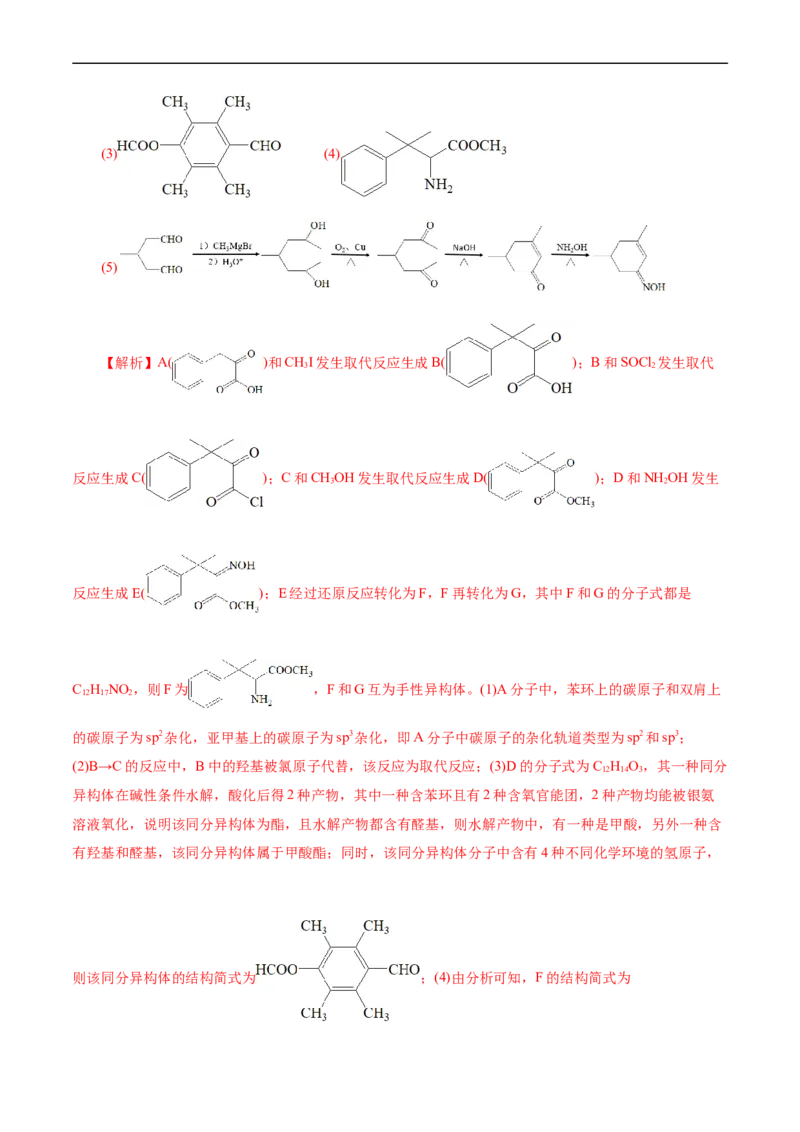
9.(15分) (2022•江苏卷,16)化合物G可用于药用多肽的结构修饰,其人工合成路线如下:
(1)A分子中碳原子的杂化轨道类型为_______。
(2)B→C的反应类型为_______。
(3)D的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:_______。
①分子中含有4种不同化学环境的氢原子;②碱性条件水解,酸化后得2种产物,其中一种含苯环且
有2种含氧官能团,2种产物均能被银氨溶液氧化。
(4)F的分子式为 ,其结构简式为_______。
(5)已知: (R和R'表示烃基或氢,R''表示烃基);
写出以 和 为原料制备 的合成路线流程图(无机试剂和有机溶剂任用,
合成路线流程图示例见本题题干)_______。
【答案】(1)sp2和sp3 (2)取代反应(3) (4)
(5)
【解析】A( )和CHI发生取代反应生成B( );B和SOCl 发生取代
3 2
反应生成C( );C和CHOH发生取代反应生成D( );D和NH OH发生
3 2
反应生成E( );E经过还原反应转化为F,F再转化为G,其中F和G的分子式都是
C H NO ,则F为 ,F和G互为手性异构体。(1)A分子中,苯环上的碳原子和双肩上
12 17 2
的碳原子为sp2杂化,亚甲基上的碳原子为sp3杂化,即A分子中碳原子的杂化轨道类型为sp2和sp3;
(2)B→C的反应中,B中的羟基被氯原子代替,该反应为取代反应;(3)D的分子式为C H O,其一种同分
12 14 3
异构体在碱性条件水解,酸化后得2种产物,其中一种含苯环且有2种含氧官能团,2种产物均能被银氨
溶液氧化,说明该同分异构体为酯,且水解产物都含有醛基,则水解产物中,有一种是甲酸,另外一种含
有羟基和醛基,该同分异构体属于甲酸酯;同时,该同分异构体分子中含有4种不同化学环境的氢原子,
则该同分异构体的结构简式为 ;(4)由分析可知,F的结构简式为;(5)根据已知的第一个反应可知, 与CHMgBr反应生成
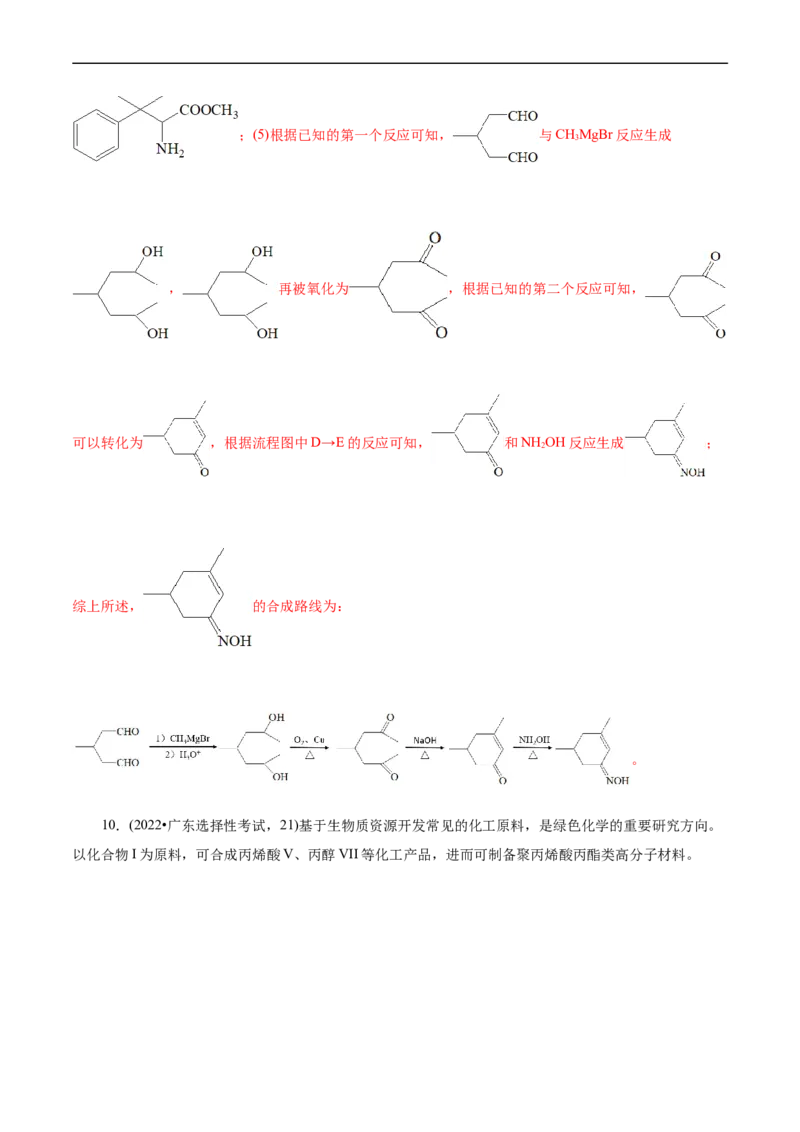
3
, 再被氧化为 ,根据已知的第二个反应可知,
可以转化为 ,根据流程图中D→E的反应可知, 和NH OH反应生成 ;
2
综上所述, 的合成路线为:
。
10.(2022•广东选择性考试,21)基于生物质资源开发常见的化工原料,是绿色化学的重要研究方向。
以化合物I为原料,可合成丙烯酸V、丙醇VII等化工产品,进而可制备聚丙烯酸丙酯类高分子材料。(1)化合物I的分子式为_______,其环上的取代基是_______(写名称)。
(2)已知化合物II也能以II′的形式存在。根据II′的结构特征,分析预测其可能的化学性质,参考①的示
例,完成下表。
序号 结构特征 可反应的试剂 反应形成的新结构 反应类型
① -CH=CH- H -CH-CH- 加成反应
2 2 2
② _______ _______ _______ 氧化反应
③ _______ _______ _______ _______
(3)化合物IV能溶于水,其原因是_______。
(4)化合物IV到化合物V的反应是原子利用率 的反应,且 与 化合物a反应得到
,则化合物a为_______。
(5)化合物VI有多种同分异构体,其中含 结构的有_______种,核磁共振氢谱图上只有一组峰
的结构简式为_______。
(6)选用含二个羧基的化合物作为唯一的含氧有机原料,参考上述信息,制备高分子化合物VIII的单体。
写出VIII的单体的合成路线_______(不用注明反应条件)。
【答案】(1) C HO 醛基
5 4 2
(2) -CHO O -COOH -COOH CHOH - COOCH 酯化反应(取代反应)
2 3 3
(3)Ⅳ中羟基能与水分子形成分子间氢键
(4)乙烯(5) 2
(6)
【解析】(1)根据化合物Ⅰ的结构简式可知,其分子式为C HO;其环上的取代基为醛基;(2)②化合
5 4 2
物Ⅱ'中含有的-CHO可以被氧化为-COOH,故答案为:-CHO;O;-COOH;
2
③化合物Ⅱ'中含有-COOH,可与含有羟基的物质(如甲醇)发生酯化反应生成酯,故答案为:-COOH;
CHOH;- COOCH ;酯化反应(取代反应);(3)化合物Ⅳ中含有羟基,能与水分子形成分子间氢键,使其能
3 3
溶于水;(4)化合物Ⅳ到化合物Ⅴ的反应是原子利用率100%的反应,且1 molⅣ与1 mola反应得到
2molV,则a的分子式为C H,为乙烯;(5)化合物Ⅵ的分子式为C HO,其同分异构体中含有 ,
2 4 3 6
则符合条件的同分异构体有 和 ,共2种,其中核磁共振氢谱中
只有一组峰的结构简式为 ;(6)根据化合物Ⅷ的结构简式可知,其单体为
,其原料中的含氧有机物只有一种含二个羧基的化合物,原料可以是, 发生题干Ⅳ→V的反应得到 ,
还原为 ,再加成得到 , 和 发生酯化
反应得到目标产物,则合成路线为
。
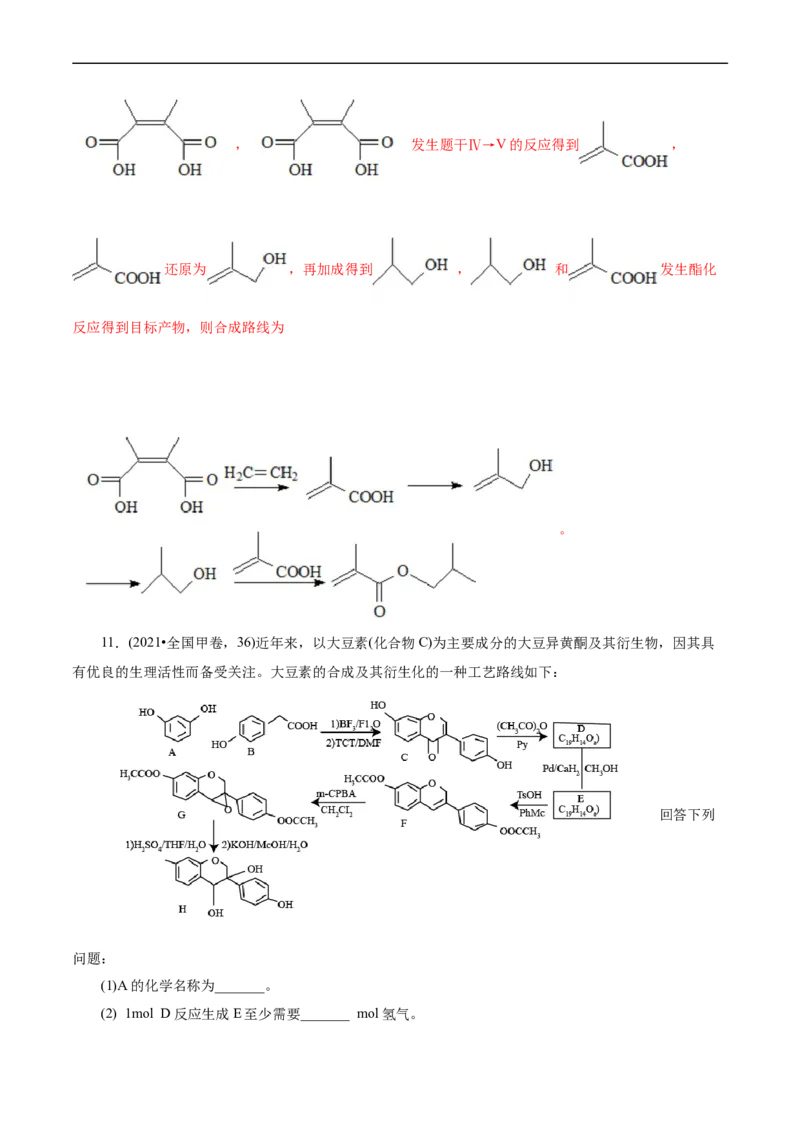
11.(2021•全国甲卷,36)近年来,以大豆素(化合物C)为主要成分的大豆异黄酮及其衍生物,因其具
有优良的生理活性而备受关注。大豆素的合成及其衍生化的一种工艺路线如下:
回答下列
问题:
(1)A的化学名称为_______。
(2) 1mol D反应生成E至少需要_______ mol氢气。(3)写出E中任意两种含氧官能团的名称_______。
(4)由E生成F的化学方程式为_______。
(5)由G生成H分两步进行:反应1)是在酸催化下水与环氧化合物的加成反应,则反应2)的反应类型
为_______。
(6)化合物B的同分异构体中能同时满足下列条件的有_______(填标号)。
a.含苯环的醛、酮
b.不含过氧键(-O-O-)
c.核磁共振氢谱显示四组峰,且峰面积比为3∶2∶2∶1
A.2个 B.3个 C.4个 D.5个
(7)根据上述路线中的相关知识,以丙烯为主要原料用不超过三步的反应设计合成下图有机物,写出合
成路线_______。
【答案】(1)间苯二酚(或1,3-苯二酚) (2)2
(3)酯基,醚键,酮基(任写两种)
(4) +H O
2
(5)取代反应 (6)C
(7)
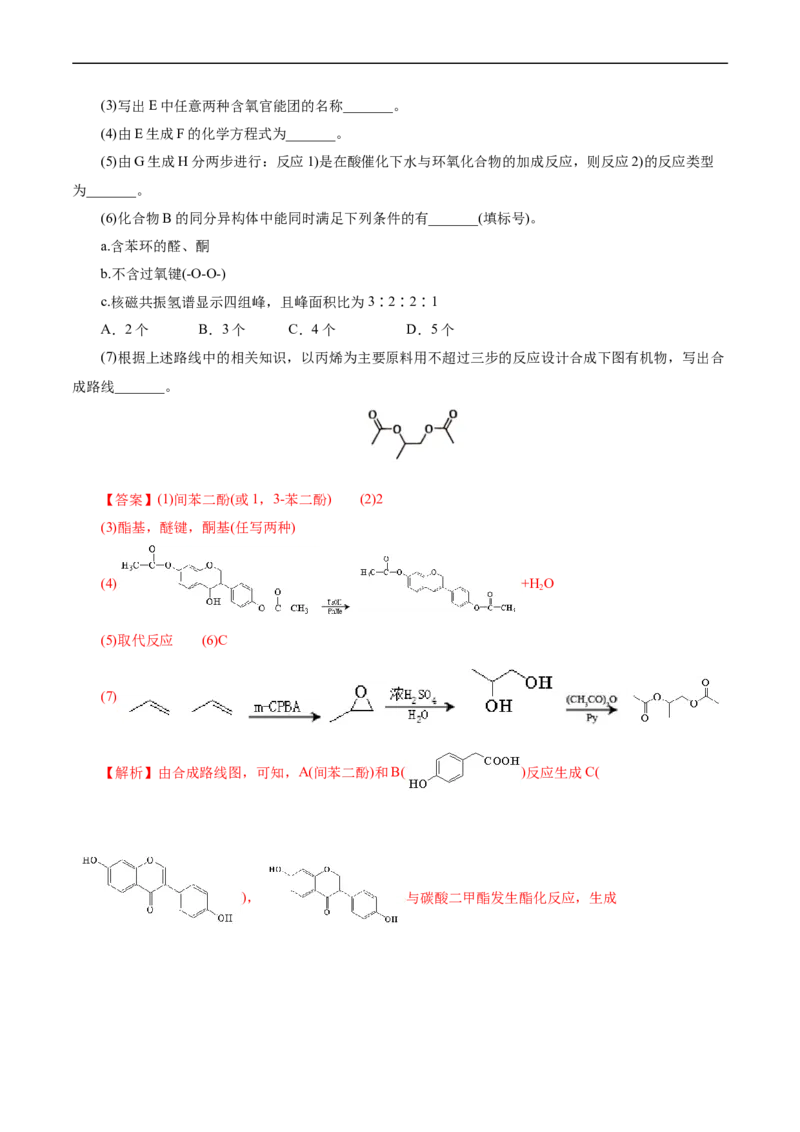
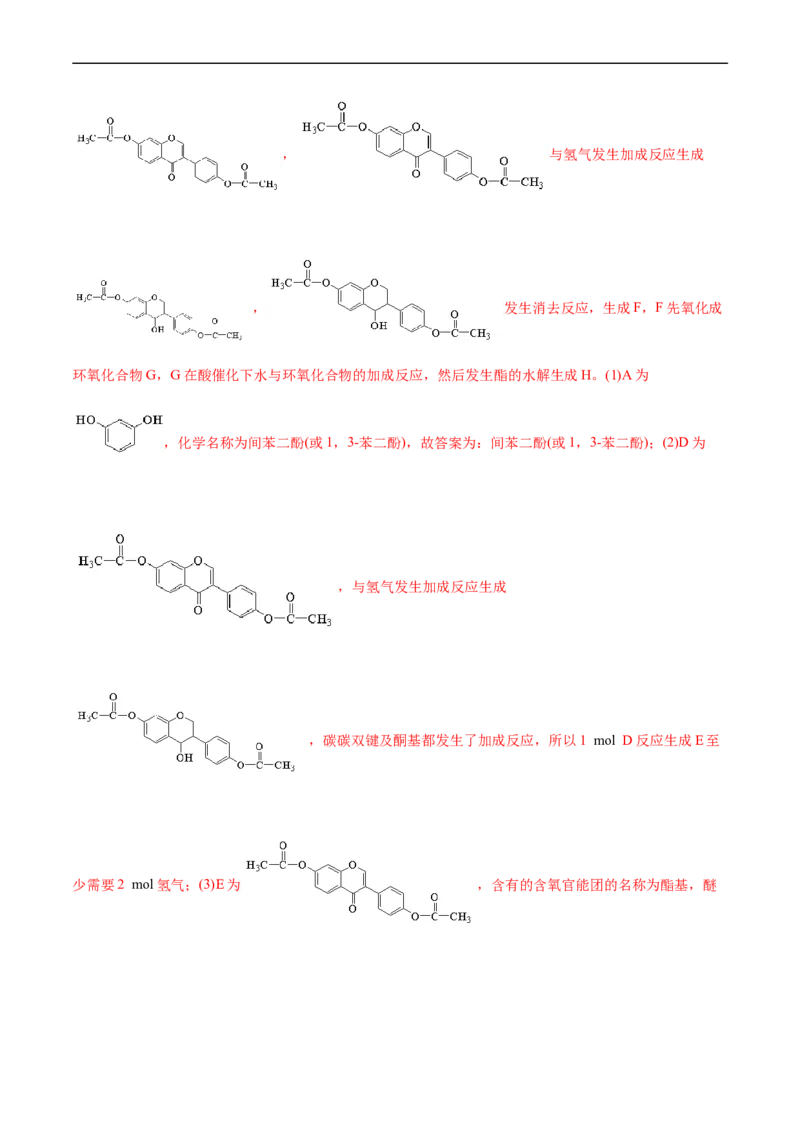
【解析】由合成路线图,可知,A(间苯二酚)和B( )反应生成C(
), 与碳酸二甲酯发生酯化反应,生成, 与氢气发生加成反应生成
, 发生消去反应,生成F,F先氧化成
环氧化合物G,G在酸催化下水与环氧化合物的加成反应,然后发生酯的水解生成H。(1)A为
,化学名称为间苯二酚(或1,3-苯二酚),故答案为:间苯二酚(或1,3-苯二酚);(2)D为
,与氢气发生加成反应生成
,碳碳双键及酮基都发生了加成反应,所以1 mol D反应生成E至
少需要2 mol氢气;(3)E为 ,含有的含氧官能团的名称为酯基,醚键,酮基(任写两种);(4)E为 ,发生消去反应,生成
,化学方程式为
+H O;(5)由G生成H分两步进行:反应1)是在酸催化下水与环氧化
2
合物的加成反应,则反应2)是将酯基水解生成羟基,反应类型为取代反应;(6)化合物B为
,同分异构体中能同时满足下列条件:.含苯环的醛、酮;b.不含过氧键( );c.核
磁共振氢谱显示四组峰,且峰面积比为3∶2∶2∶1,说明为醛或酮,而且含有甲基,根据要求可以写出:
, , , ,故
有4种,故选C; (7)以丙烯为主要原料用不超过三步的反应设计合成下图有机物,可以将丙烯在m-CPBA
的作用下生成环氧化合物,环氧化合物在酸催化下水发生加成反应,然后再与碳酸二甲酯发生酯化反应即
可,故合成路线为:。
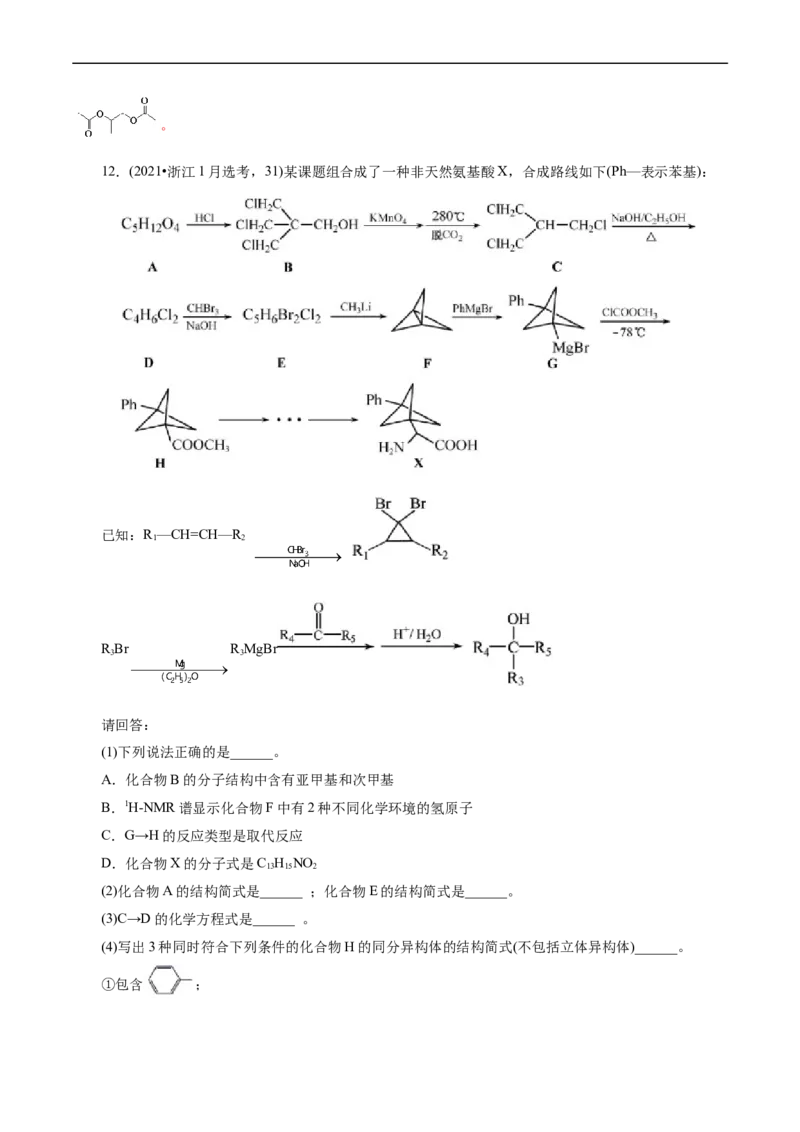
12.(2021•浙江1月选考,31)某课题组合成了一种非天然氨基酸X,合成路线如下(Ph—表示苯基):
已知:R —CH=CH—R
1 2
R Br R MgBr
3 3
请回答:
(1)下列说法正确的是______。
A.化合物B的分子结构中含有亚甲基和次甲基
B.1H-NMR谱显示化合物F中有2种不同化学环境的氢原子
C.G→H的反应类型是取代反应
D.化合物X的分子式是C H NO
13 15 2
(2)化合物A的结构简式是______ ;化合物E的结构简式是______。
(3)C→D的化学方程式是______ 。
(4)写出3种同时符合下列条件的化合物H的同分异构体的结构简式(不包括立体异构体)______。
①包含 ;②包含 (双键两端的C不再连接H)片段;
③除②中片段外只含有1个-CH-
2
(5)以化合物F、溴苯和甲醛为原料,设计下图所示化合物的合成路线(用流程图表示,无机试剂、有机
溶剂任选)______。
(也可表示为 )
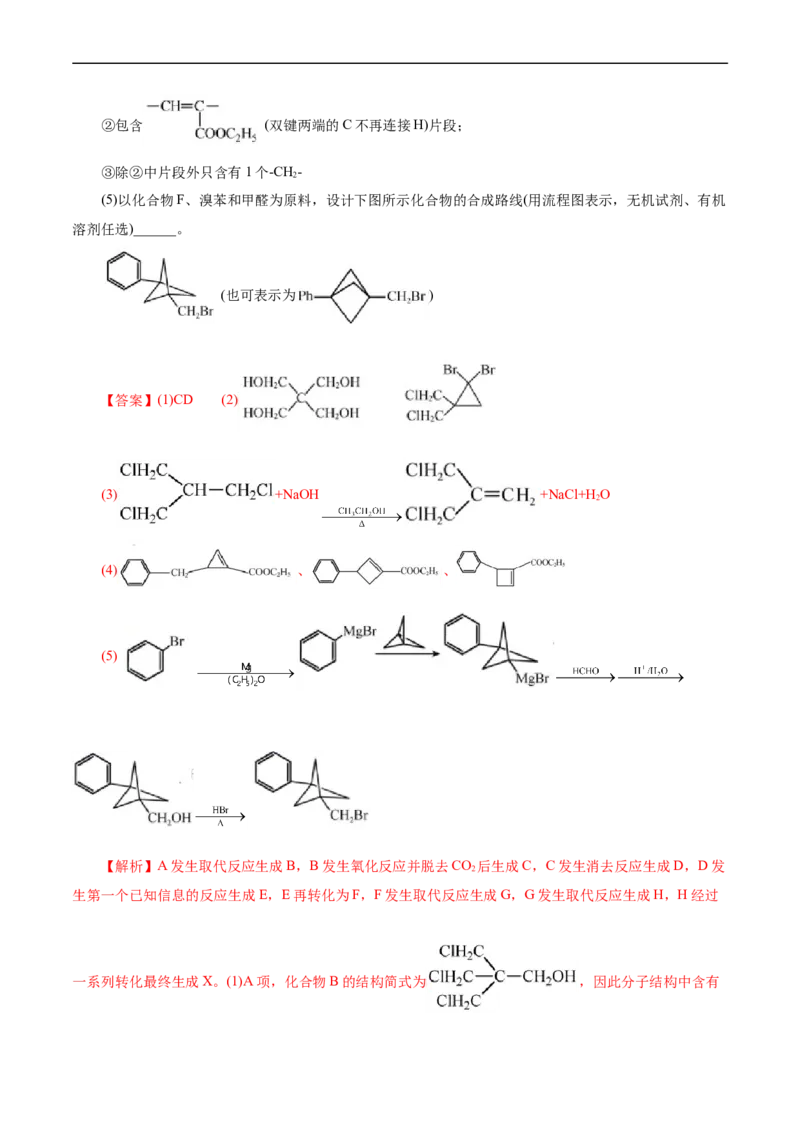
【答案】(1)CD (2)
(3) +NaOH +NaCl+HO
2
(4) 、 、
(5)
【解析】A发生取代反应生成B,B发生氧化反应并脱去CO 后生成C,C发生消去反应生成D,D发
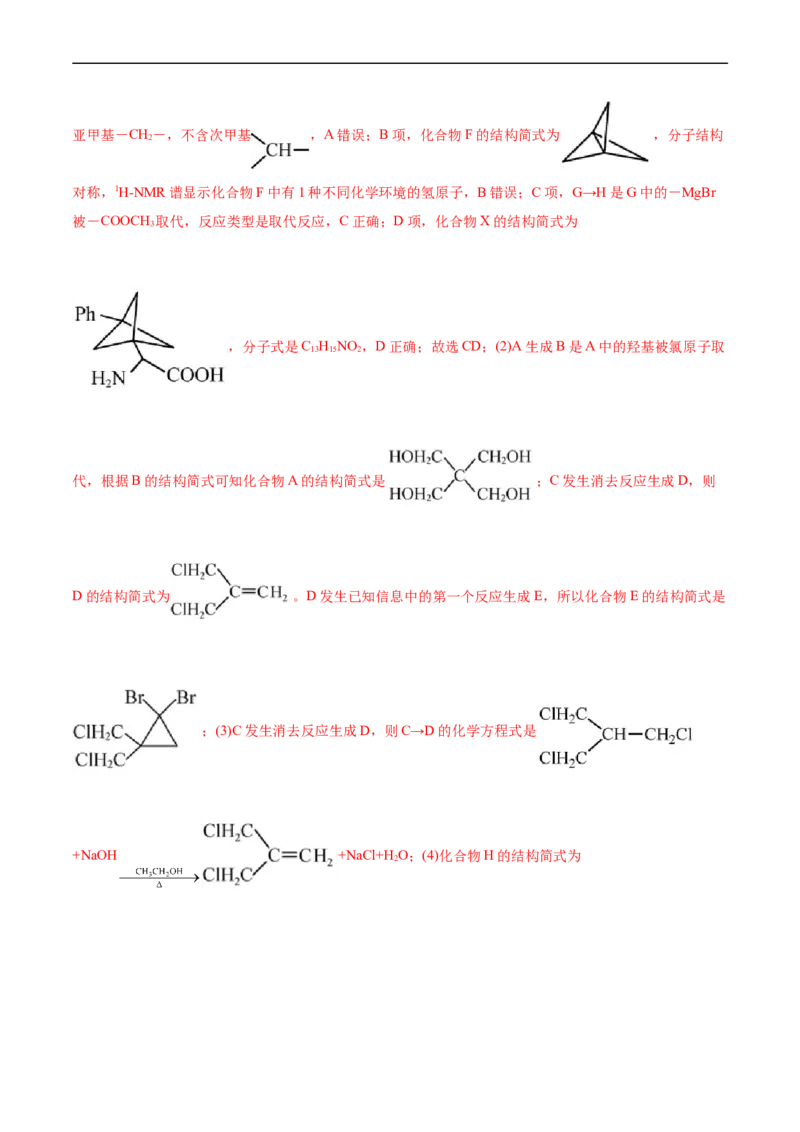
2
生第一个已知信息的反应生成E,E再转化为F,F发生取代反应生成G,G发生取代反应生成H,H经过
一系列转化最终生成X。(1)A项,化合物B的结构简式为 ,因此分子结构中含有亚甲基-CH-,不含次甲基 ,A错误;B项,化合物F的结构简式为 ,分子结构
2
对称,1H-NMR谱显示化合物F中有1种不同化学环境的氢原子,B错误;C项,G→H是G中的-MgBr
被-COOCH 取代,反应类型是取代反应,C正确;D项,化合物X的结构简式为
3
,分子式是C H NO ,D正确;故选CD;(2)A生成B是A中的羟基被氯原子取
13 15 2
代,根据B的结构简式可知化合物A的结构简式是 ;C发生消去反应生成D,则
D的结构简式为 。D发生已知信息中的第一个反应生成E,所以化合物E的结构简式是
;(3)C发生消去反应生成D,则C→D的化学方程式是
+NaOH +NaCl+HO;(4)化合物H的结构简式为
2,分子式为C H O,符合条件的同分异构体①含有苯基 ,属于芳香族
13 14 2
化合物;②含有 ,且双键两端的C不再连接H;③分子中除②中片段外中含有1
个-CH-,因此符合条件的同分异构体为 、 、
2
;
(5)根据已知第二个信息以及F转化为G反应结合逆推法可知以化合物 、溴苯和甲醛为原料
制备 的合成路线为
。
13.(2021•浙江6月选考,31)某课题组研制了一种具有较高玻璃化转变温度的聚合物P,合成路线如
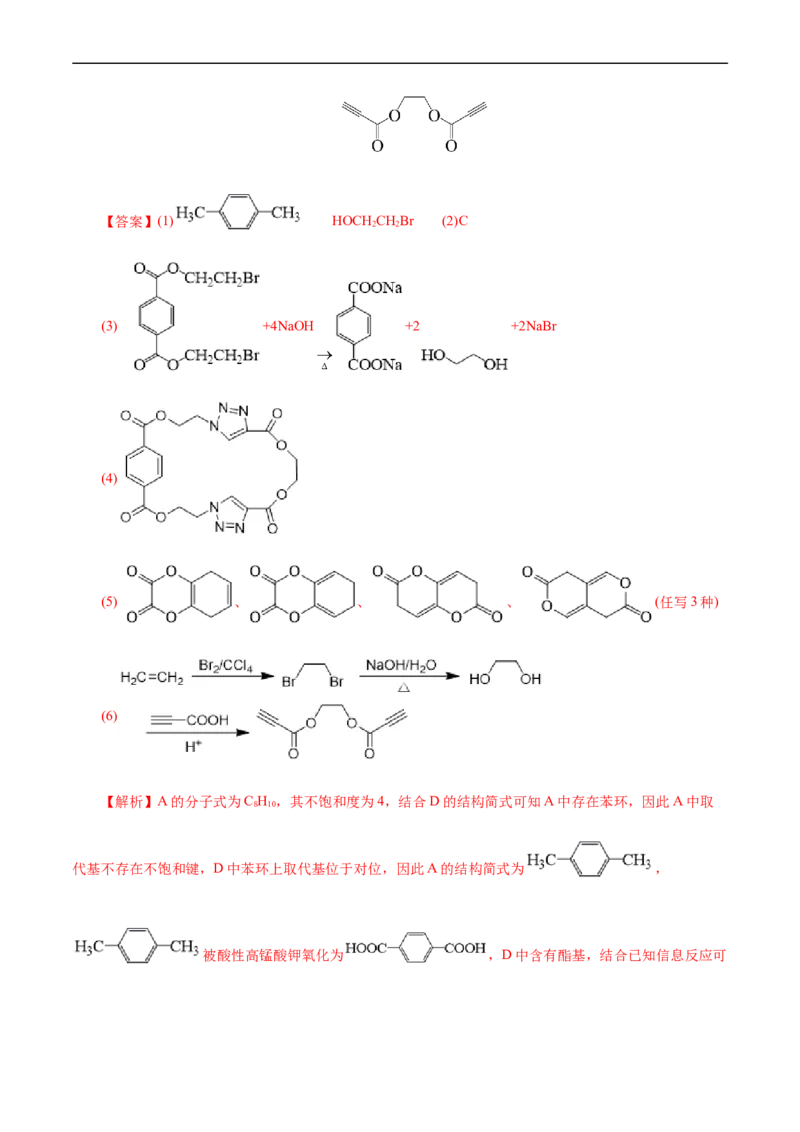
下:已知:
请回答:
(1)化合物A的结构简式是_______;化合物E的结构简式是_______。
(2)下列说法不正确的是_______。
A.化合物B分子中所有的碳原子共平面
B.化合物D的分子式为C H NO
12 12 6 4
C.化合物D和F发生缩聚反应生成P
D.聚合物P属于聚酯类物质
(3)化合物C与过量 溶液反应的化学方程式是_______。
(4)在制备聚合物P的过程中还生成了一种分子式为C H NO 的环状化合物。用键线式表示其结构
20 18 6 8
_______。
(5)写出3种同时满足下列条件的化合物F的同分异构体的结构简式(不考虑立体异构体):_______。
① 谱显示只有2种不同化学环境的氢原子
②只含有六元环
③含有 结构片段,不含 键
(6)以乙烯和丙炔酸为原料,设计如下化合物的合成路线(用流程图表示,无机试剂、有机溶剂任
选)_______。【答案】(1) HOCH CHBr (2)C
2 2
(3) +4NaOH +2 +2NaBr
(4)
(5) 、 、 、 (任写3种)
(6)
【解析】A的分子式为C H ,其不饱和度为4,结合D的结构简式可知A中存在苯环,因此A中取
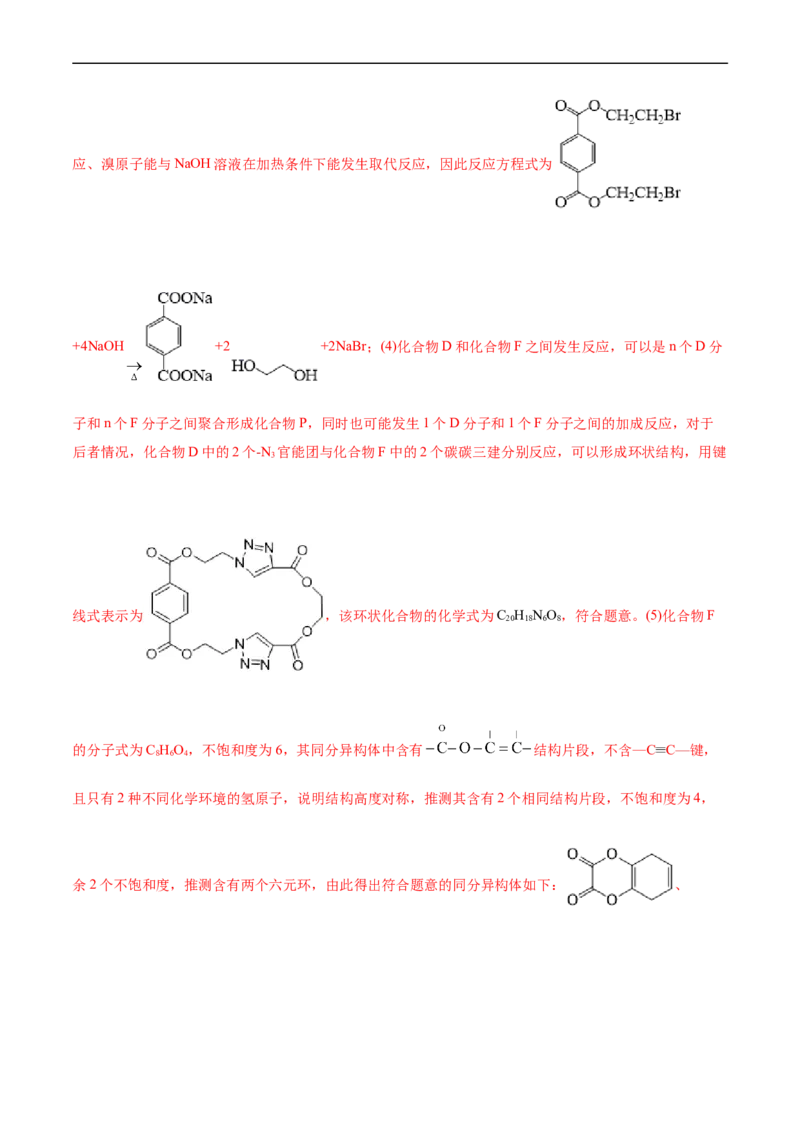
8 10
代基不存在不饱和键,D中苯环上取代基位于对位,因此A的结构简式为 ,
被酸性高锰酸钾氧化为 ,D中含有酯基,结合已知信息反应可知C的结构简式为 ,B与E在酸性条件下反应生成 ,该反应为酯化反应,
因此E的结构简式为HOCH CHBr,D和F发生已知反应得到化合物P中的五元环,则化合物F中应含有
2 2
碳碳三键,而化合物P是聚合结构,其中的基本单元来自化合物D和化合物F,所以化合物F应为
。(1) A的结构简式为 ;化合物E的结构简式为
HOCH CHBr;(2)A项,化合物B的结构简式为 ,化合物B中苯环的6个碳原
2 2
子共平面,而苯环只含有两个对位上的羧基,两个羧基的碳原子直接与苯环相连,所以这2个碳原子也应
与苯环共平面,化合物B分子中所有碳原子共平面,故A正确;B项,D的结构简式为
,由此可知化合物D的分子式为C H NO,故B正确;C项,缩
12 12 6 4
聚反应除形成缩聚物外,还有水、醇、氨或氯化氢等低分子副产物产生,化合物D和化合物F的聚合反应
不涉及低分子副产物的产生,不属于缩聚反应,故C错误;D项,聚合物P中含有4n个酯基官能团,所以
聚合物P属于聚酯类物质,故D正确;故选C。(3) 中酯基能与NaOH溶液发生水解反应、溴原子能与NaOH溶液在加热条件下能发生取代反应,因此反应方程式为
+4NaOH +2 +2NaBr;(4)化合物D和化合物F之间发生反应,可以是n个D分
子和n个F分子之间聚合形成化合物P,同时也可能发生1个D分子和1个F分子之间的加成反应,对于
后者情况,化合物D中的2个-N 官能团与化合物F中的2个碳碳三建分别反应,可以形成环状结构,用键
3
线式表示为 ,该环状化合物的化学式为C H NO,符合题意。(5)化合物F
20 18 6 8
的分子式为C HO,不饱和度为6,其同分异构体中含有 结构片段,不含—C≡C—键,
8 6 4
且只有2种不同化学环境的氢原子,说明结构高度对称,推测其含有2个相同结构片段,不饱和度为4,
余2个不饱和度,推测含有两个六元环,由此得出符合题意的同分异构体如下: 、、 、 ;(6)由逆向合成法可知,丙炔酸应与
通过酯化反应得到目标化合物,而 中的羟基又能通过 水解得到,乙
烯与Br 加成可得 ,故目标化合物的合成路线为
2
。
14.(2021•湖南选择性考试,19)叶酸拮抗剂Alimta(M)是一种多靶向性抗癌药物。以苯和丁二酸酐
为原料合成该化合物的路线如下:已知:
回答下列问题:
(1)A的结构简式为 ;
(2)A→B,D→E的反应类型分别是 , ;
(3)M中虚线框内官能团的名称为a ,b ;
(4)B有多种同分异构体,同时满足下列条件的同分异构体有 种(不考虑立体异
构);
①苯环上有2个取代基
②能够发生银镜反应
③与FeCl 溶液发生显色反应
3
其中核磁共振氢谱有五组峰,且峰面积之比为6:2:2:1:1的结构简式为 ;
(5)结合上述信息,写出丁二酸酐和乙二醇合成聚丁二酸乙二醇酯的反应方程式 ;
(6)参照上述合成路线,以乙烯和 为原料,设计合成 的路线
(其他试剂任选)。
【答案】(1) (2)还原反应 取代反应
(3)酰胺基 羧基 (4)15
(5)(6)
【解析】苯与丁二酸酐发生信息①中取代反应生成A,故A的结构简式为 ,A发生
还原反应生成B,B与乙醇发生酯化反应生成C,C系列转化生成D,D发生取代反应生成E,E与F反应
生成G可以理解为:E中C﹣Br键断裂,F中C﹣H键断裂,发生取代反应,生成HBr,并形成C﹣C键,
﹣NH 与﹣CHO之间发生加成反应,然后羟基再发生消去反应形成碳碳双键,羟基异构转化为羰基,G系
2
列转化生成M。(1)苯与丁二酸酐发生信息①中取代反应生成A,故A的结构简式为 ;
(2)A→B是 转化为 ,组成上去氧,属于氧化反应,D→E是醛基连接的
碳原子上的氢原子被溴原子替代,属于取代反应;(3)M中虚线框内官能团a为酰胺键,官能团b为羧基;
(4)B的结构简式为 ,B的同分异构体满足下列条件:②能够发生银镜反应,③与FeCl
3
溶液发生显色反应,说明含有醛基、酚羟基,①苯环上有2个取代基,其中一个为﹣OH,另外一个为
CHCHCHCHO、 中烃基失去氢原子形成的基团,前者有3种,后者有2种,2个取代基
3 2 2
有邻、间、对3种位置关系,故符合条件的同分异构体共有3×(3+2)=15种,其中核磁共振氢谱有五组峰,
且峰面积之比为6:2:2:1:1的结构简式为: ;
(5)丁二酸酐和乙二醇合成聚丁二酸乙二醇酯,可以理解为丁二酸酐水解为丁二酸后再与乙二醇发生缩聚 反 应 , 则 反 应 方 程 式 为 :
; (6) 利 用
E+F→G的转化进行设计, 与BrCHCHO反应生成 ,由D→E的转
2
化可知,CHCHO 与 DBBA(溴化剂)/CH Cl 反应生成 BrCHCHO,而乙烯与 HBr 发生加成反应生成
3 2 2 2
CHCHBr,CHCHBr碱性条件下水解生成CHCHOH,CHCHOH再发生催化氧化生成CHCHO,合成
3 2 3 2 3 2 3 2 3
路线为: 。
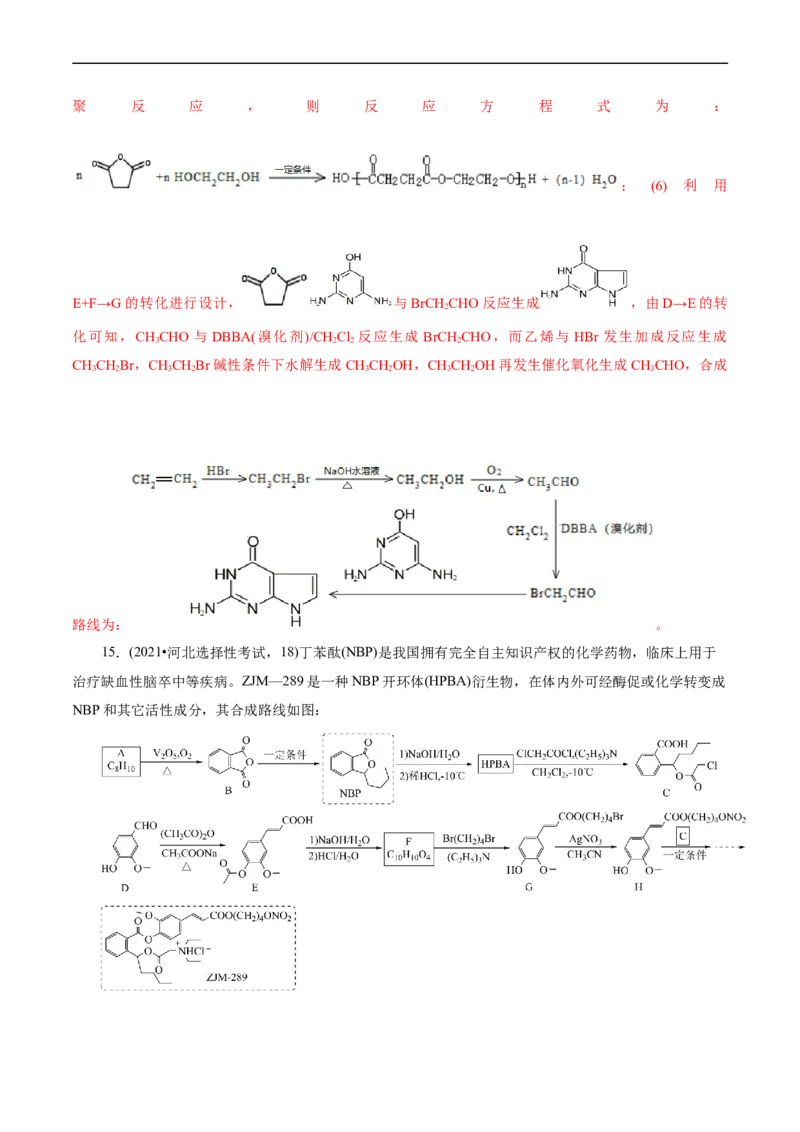
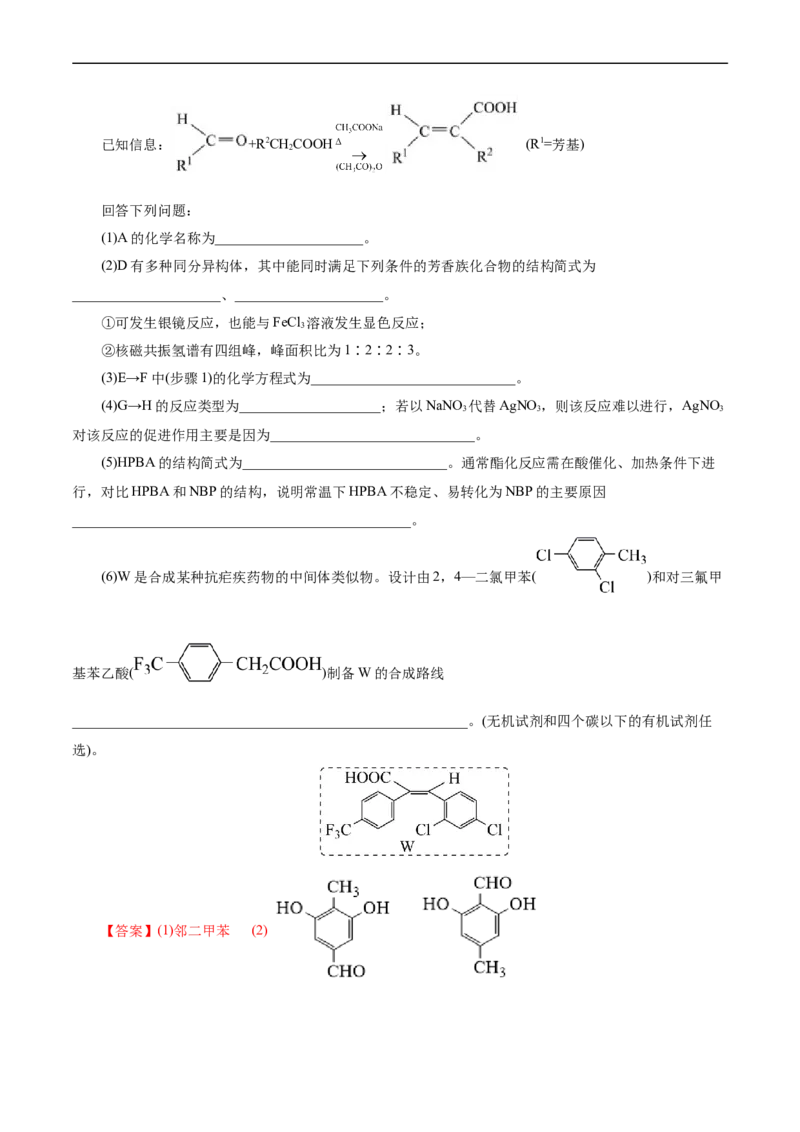
15.(2021•河北选择性考试,18)丁苯酞(NBP)是我国拥有完全自主知识产权的化学药物,临床上用于
治疗缺血性脑卒中等疾病。ZJM—289是一种NBP开环体(HPBA)衍生物,在体内外可经酶促或化学转变成
NBP和其它活性成分,其合成路线如图:已知信息: +R2CHCOOH (R1=芳基)
2
回答下列问题:
(1)A的化学名称为_____________________。
(2)D有多种同分异构体,其中能同时满足下列条件的芳香族化合物的结构简式为
_____________________、_____________________。
①可发生银镜反应,也能与FeCl 溶液发生显色反应;
3
②核磁共振氢谱有四组峰,峰面积比为1∶2∶2∶3。
(3)E→F中(步骤1)的化学方程式为_____________________________。
(4)G→H的反应类型为____________________;若以NaNO 代替AgNO,则该反应难以进行,AgNO
3 3 3
对该反应的促进作用主要是因为_____________________________。
(5)HPBA的结构简式为_____________________________。通常酯化反应需在酸催化、加热条件下进
行,对比HPBA和NBP的结构,说明常温下HPBA不稳定、易转化为NBP的主要原因
________________________________________________。
(6)W是合成某种抗疟疾药物的中间体类似物。设计由2,4—二氯甲苯( )和对三氟甲
基苯乙酸( )制备W的合成路线
________________________________________________________。(无机试剂和四个碳以下的有机试剂任
选)。
【答案】(1)邻二甲苯 (2)(3)
(4)取代反应 AgNO 反应生成的AgBr难溶于水,使平衡正向移动促进反应进行
3
(5) HPBA中烃基的空间位阻较大,使得羟基较为活泼,常温下不稳定、易转化为
NBP
(6)
【解析】(1)A的分子式为C H ,不饱和度为4,说明取代基上不含不饱和键,A与O 在VO 作催化
8 10 2 2 5
剂并加热条件下生成 ,由此可知A的结构简式为 ,其名称为邻二甲苯。(2)
的同分异构体满足:①可发生银镜反应,也能与FeCl 溶液发生显色反应,说明结构中含有醛基和酚羟基,
3
根据不饱和度可知该结构中除醛基外不含其它不饱和键,②核磁共振氢谱有四组峰,峰面积比为1:2:
2:3,说明该结构具有对称性,根据该结构中氧原子数可知该结构中含有1个醛基、2个酚羟基、1个甲基,
满足该条件的同分异构体结构简式为 和 。(3)E→F中步骤1)为
与NaOH的水溶液反应, 中酯基、羧基能与NaOH反应,反应方程式为 。(4)观察流程可知,G→H的反应为
中Br原子被AgNO 中-O-NO 取代生成 和AgBr,反应类型为
3 2
取代反应;若以NaNO 代替AgNO,则该反应难以进行,其原因是NaNO 反应生成的NaNO 易溶于水,
3 3 3 3
而AgNO 反应生成的AgBr难溶于水,使平衡正向移动促进反应进行;(5)NBP( )中酯基在碱性
3
条件下发生水解反应生成 , 经过酸化后生成HPBA( );
中烃基体积较大,对羟基的空间位阻较大使得羟基较为活泼,容易与羧基发生酯化反应生
成 ;HPBA中烃基的空间位阻较大,使得羟基较为活泼,常温下不稳定、易转化为NBP。(6)
由 和 制备 可通过题干已知信
息而得,因此需要先合成 , 可通过 氯代后水解再催化氧
化而得,因此合成路线为。
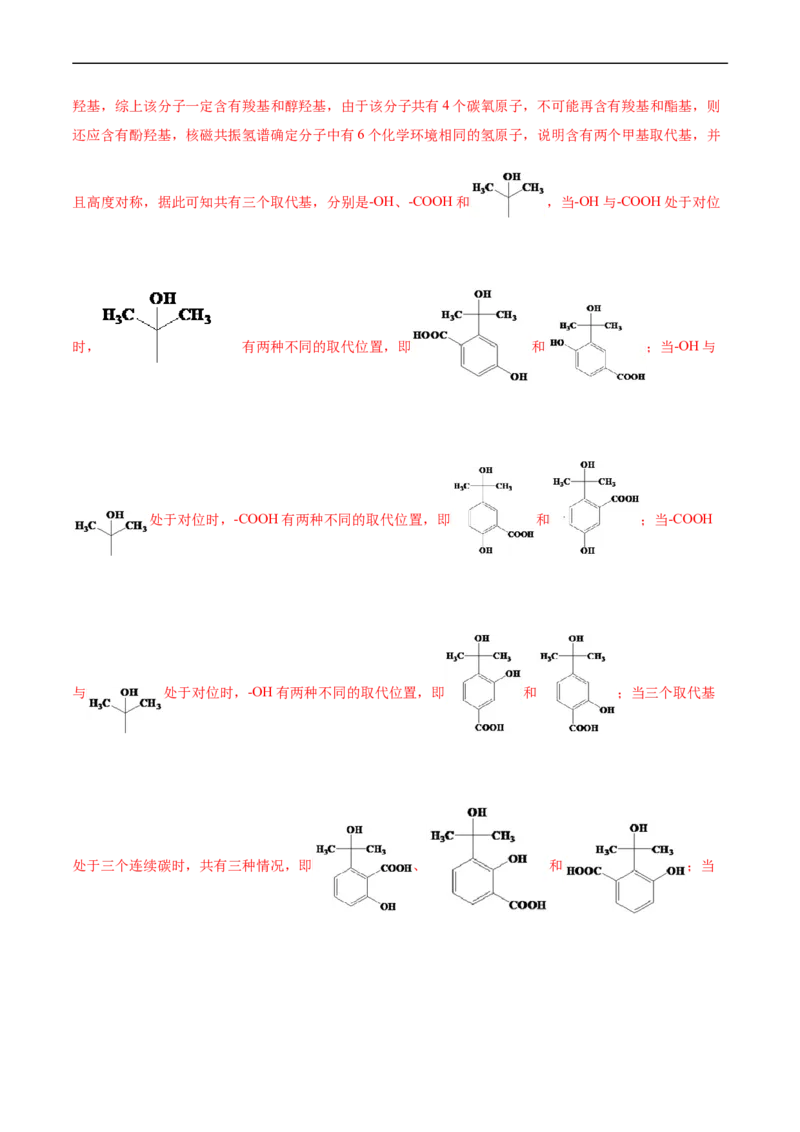
16.(2021•广东选择性考试,20)天然产物Ⅴ具有抗疟活性,某研究小组以化合物Ⅰ为原料合成Ⅴ及其
衍生物Ⅵ的路线如下(部分反应条件省略,Ph表示-C H):
6 5
已知:
(1)化合物Ⅰ中含氧官能团有_______(写名称)。
(2)反应①的方程式可表示为:I+II=III+Z,化合物Z的分子式为_______。
(3)化合物IV能发生银镜反应,其结构简式为_______。
(4)反应②③④中属于还原反应的有_______,属于加成反应的有_______。
(5)化合物Ⅵ的芳香族同分异构体中,同时满足如下条件的有_______种,写出其中任意一种的结构简
式:_______。
条件:a.能与NaHCO 反应;b. 最多能与2倍物质的量的NaOH反应;c. 能与3倍物质的量的Na发生
3
放出H 的反应;d.核磁共振氢谱确定分子中有6个化学环境相同的氢原子;e.不含手性碳原子(手性碳原子
2
是指连有4个不同的原子或原子团的饱和碳原子)。(6)根据上述信息,写出以苯酚的一种同系物及HOCH CHCl为原料合成 的路线
2 2
_______(不需注明反应条件)。
【答案】(1)(酚)羟基、醛基 (2)C H OP (3)
18 15
(4)②④ ② (5)10
(6)
【解析】(1)根据有机物Ⅰ的结构,有机物Ⅰ为对醛基苯酚,其含氧官能团为(酚)羟基、醛基;(2)反
应①的方程式可表示为:Ⅰ+Ⅱ=Ⅲ+Z,根据反应中Ⅰ、Ⅱ、Ⅲ的分子式和质量守恒定律可知,反应前与反
应后的原子个数相同,则反应后Z的分子式为C H OP;(3)已知有机物Ⅳ可以发生银镜反应,说明有机物
18 15
Ⅳ中含有醛基,又已知有机物Ⅳ可以发生反应生成 ,则有机物Ⅳ一定含有酚羟基,根据有机物Ⅳ的
分子式和 可以得出,有机物Ⅳ的结构简式为 ;(4)还原反应时物质中元素的化合价降低,
在有机反应中一般表现为加氢或者去氧,所以反应②和④为还原反应,其中反应②为加成反应;(5)化合物
Ⅳ的分子式为C H O,能与NaHCO 反应说明含有羧基,能与NaOH反应说明含有酚羟基或羧基或酯基,
10 12 4 3
最多能与2倍物质的量的NaOH反应,说明除一个羧基外还可能含有酚羟基、羧基、酯基其中的一个,能
与Na反应的挂能能团为醇羟基、酚羟基、羧基,能与3倍物质的量的发生放出的反应,说明一定含有醇羟基,综上该分子一定含有羧基和醇羟基,由于该分子共有4个碳氧原子,不可能再含有羧基和酯基,则
还应含有酚羟基,核磁共振氢谱确定分子中有6个化学环境相同的氢原子,说明含有两个甲基取代基,并
且高度对称,据此可知共有三个取代基,分别是-OH、-COOH和 ,当-OH与-COOH处于对位
时, 有两种不同的取代位置,即 和 ;当-OH与
处于对位时,-COOH有两种不同的取代位置,即 和 ;当-COOH
与 处于对位时,-OH有两种不同的取代位置,即 和 ;当三个取代基
处于三个连续碳时,共有三种情况,即 、 和 ;当三个取代基处于间位时,共有一种情况,即 ,综上分析该有机物的同分异构体共有十
种。(6)根据题给已知条件对甲苯酚与HOCH CHCl反应能得到 ,之后水解反应得到
2 2
,观察题中反应可知得到目标产物需要利用反应④,所以合成的路线为
。
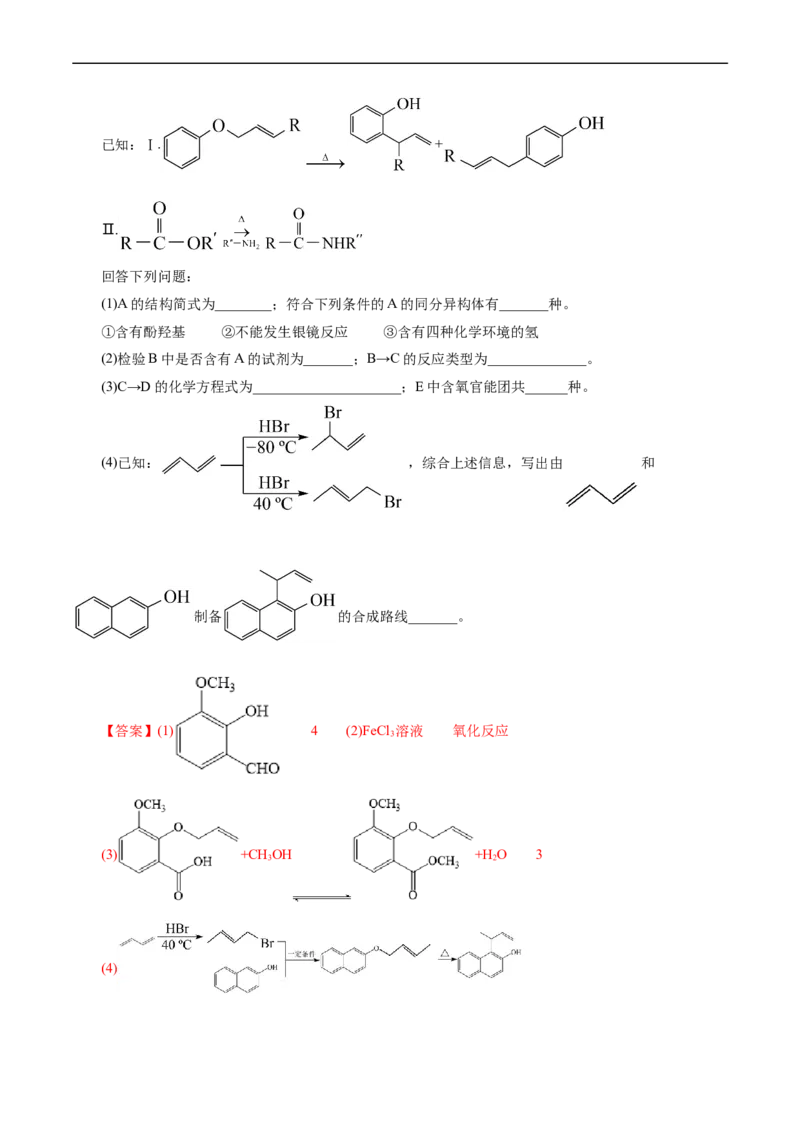
17.(2021•山东卷,19)一种利胆药物F的合成路线如图:已知:Ⅰ. +
Ⅱ.
回答下列问题:
(1)A的结构简式为________;符合下列条件的A的同分异构体有_______种。
①含有酚羟基 ②不能发生银镜反应 ③含有四种化学环境的氢
(2)检验B中是否含有A的试剂为_______;B→C的反应类型为______________。
(3)C→D的化学方程式为_____________________;E中含氧官能团共______种。
(4)已知: ,综合上述信息,写出由 和
制备 的合成路线_______。
【答案】(1) 4 (2)FeCl 溶液 氧化反应
3
(3) +CH OH +H O 3
3 2
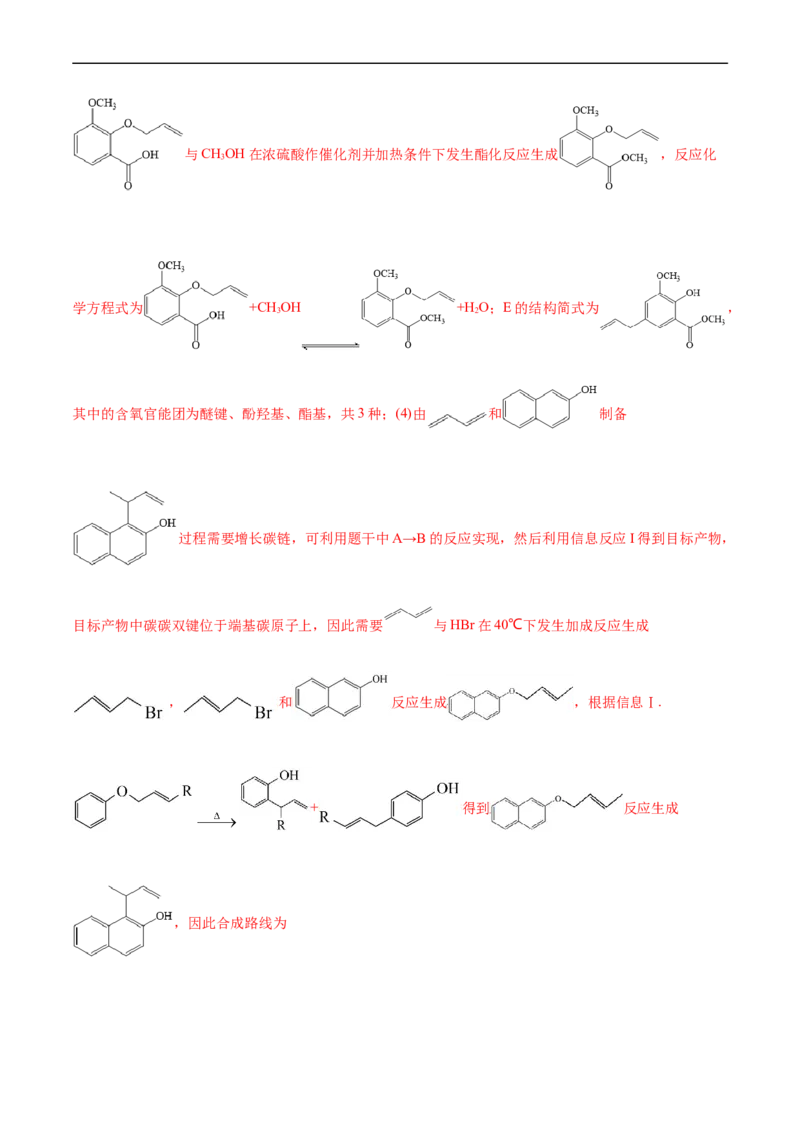
(4)【解析】由信息反应II以及F的结构简式和E的分子式可知E的结构简式为
,D发生信息反应I得到E,则D的结构简式为 ,C与CHOH
3
发生反应生成D,C相较于D少1个碳原子,说明C→D是酯化反应,因此C的结构简式为
,B→C碳链不变,而A→B碳链增长,且增长的碳原子数等于 中碳原子数,
同时B→C的反应条件为NaClO、H+,NaClO 具有氧化性,因此B→C为氧化反应,A→B为取代反应,
2 2
C HO 的不饱和度为5,说明苯环上的取代基中含有不饱和键,因此A的结构简式为 ,B的结
8 8 3
构简式为 。(1) A的结构简式为 ;A的同分异构体中满足:①含有酚羟基;
②不能发生银镜反应,说明结构中不含醛基;③含有四种化学环境的氢,说明具有对称结构,则满足条件
的结构有: 、 、 、 ,
共有4种;(2)A中含有酚羟基,B中不含酚羟基,可利用FeCl 溶液检验B中是否含有A,若含有A,则加
3
入FeCl 溶液后溶液呈紫色;由上述分析可知,B→C的反应类型为氧化反应;(3)C→D为
3与CHOH在浓硫酸作催化剂并加热条件下发生酯化反应生成 ,反应化
3
学方程式为 +CH OH +H O;E的结构简式为 ,
3 2
其中的含氧官能团为醚键、酚羟基、酯基,共3种;(4)由 和 制备
过程需要增长碳链,可利用题干中A→B的反应实现,然后利用信息反应I得到目标产物,
目标产物中碳碳双键位于端基碳原子上,因此需要 与HBr在40℃下发生加成反应生成
, 和 反应生成 ,根据信息Ⅰ.
+ 得到 反应生成
,因此合成路线为。
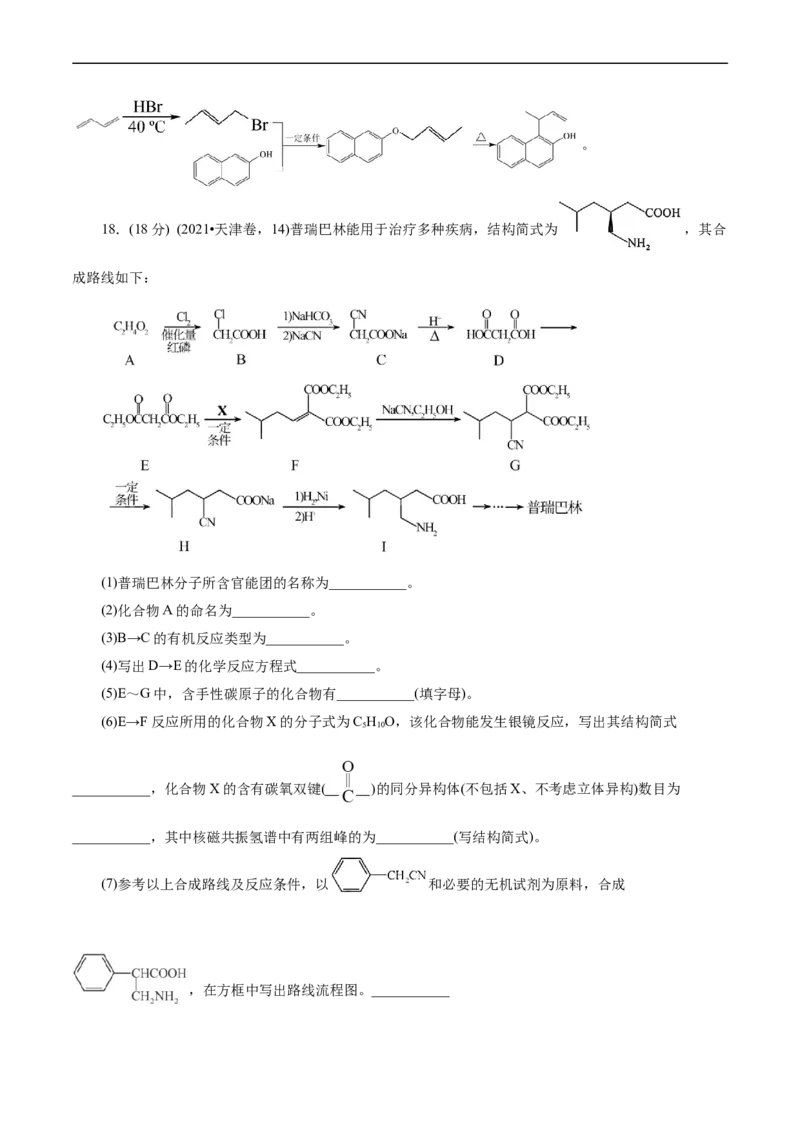
18.(18分) (2021•天津卷,14)普瑞巴林能用于治疗多种疾病,结构简式为 ,其合
成路线如下:
(1)普瑞巴林分子所含官能团的名称为___________。
(2)化合物A的命名为___________。
(3)B→C的有机反应类型为___________。
(4)写出D→E的化学反应方程式___________。
(5)E~G中,含手性碳原子的化合物有___________(填字母)。
(6)E→F反应所用的化合物X的分子式为C H O,该化合物能发生银镜反应,写出其结构简式
5 10
___________,化合物X的含有碳氧双键( )的同分异构体(不包括X、不考虑立体异构)数目为
___________,其中核磁共振氢谱中有两组峰的为___________(写结构简式)。
(7)参考以上合成路线及反应条件,以 和必要的无机试剂为原料,合成
,在方框中写出路线流程图。___________【答案】(1)羧基、氨基 (2)乙酸 (3)取代反应
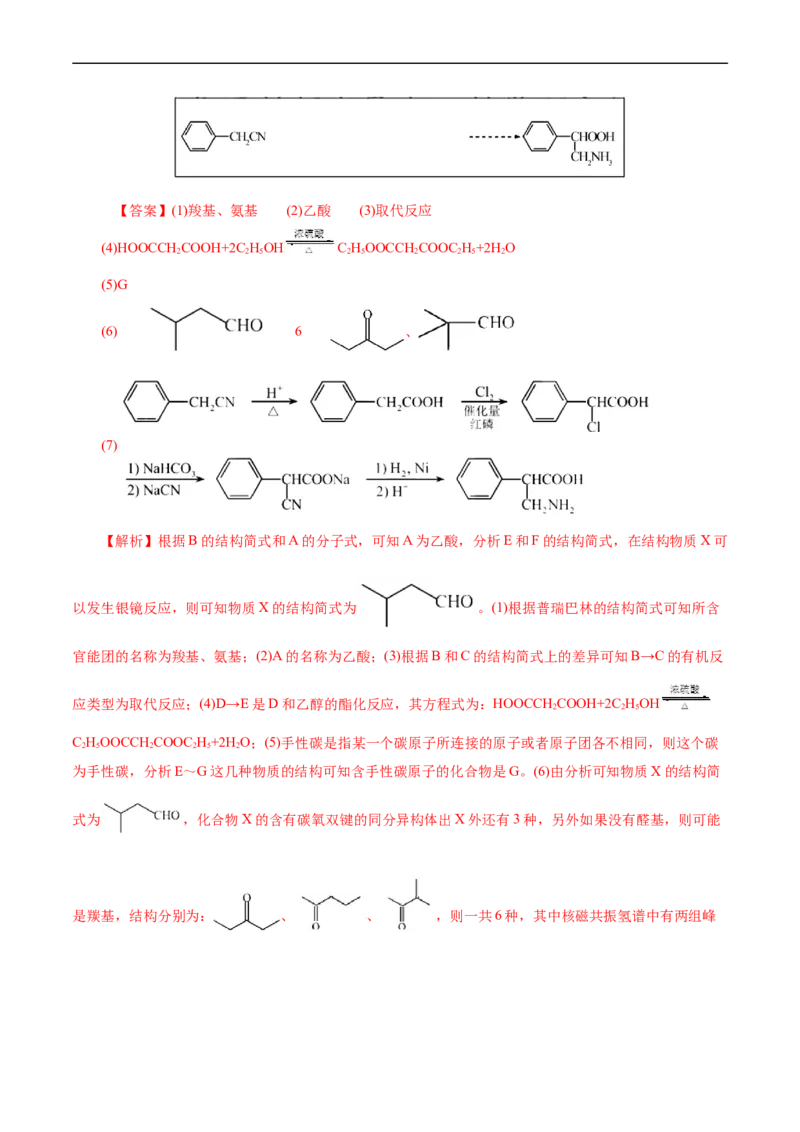
(4)HOOCCH COOH+2C HOH C HOOCCH COOC H+2H O
2 2 5 2 5 2 2 5 2
(5)G
(6) 6 、
(7)
【解析】根据B的结构简式和A的分子式,可知A为乙酸,分析E和F的结构简式,在结构物质X可
以发生银镜反应,则可知物质X的结构简式为 。(1)根据普瑞巴林的结构简式可知所含
官能团的名称为羧基、氨基;(2)A的名称为乙酸;(3)根据B和C的结构简式上的差异可知B→C的有机反
应类型为取代反应;(4)D→E是D和乙醇的酯化反应,其方程式为:HOOCCH COOH+2C HOH
2 2 5
C HOOCCH COOC H+2H O;(5)手性碳是指某一个碳原子所连接的原子或者原子团各不相同,则这个碳
2 5 2 2 5 2
为手性碳,分析E~G这几种物质的结构可知含手性碳原子的化合物是G。(6)由分析可知物质X的结构简
式为 ,化合物X的含有碳氧双键的同分异构体出X外还有3种,另外如果没有醛基,则可能
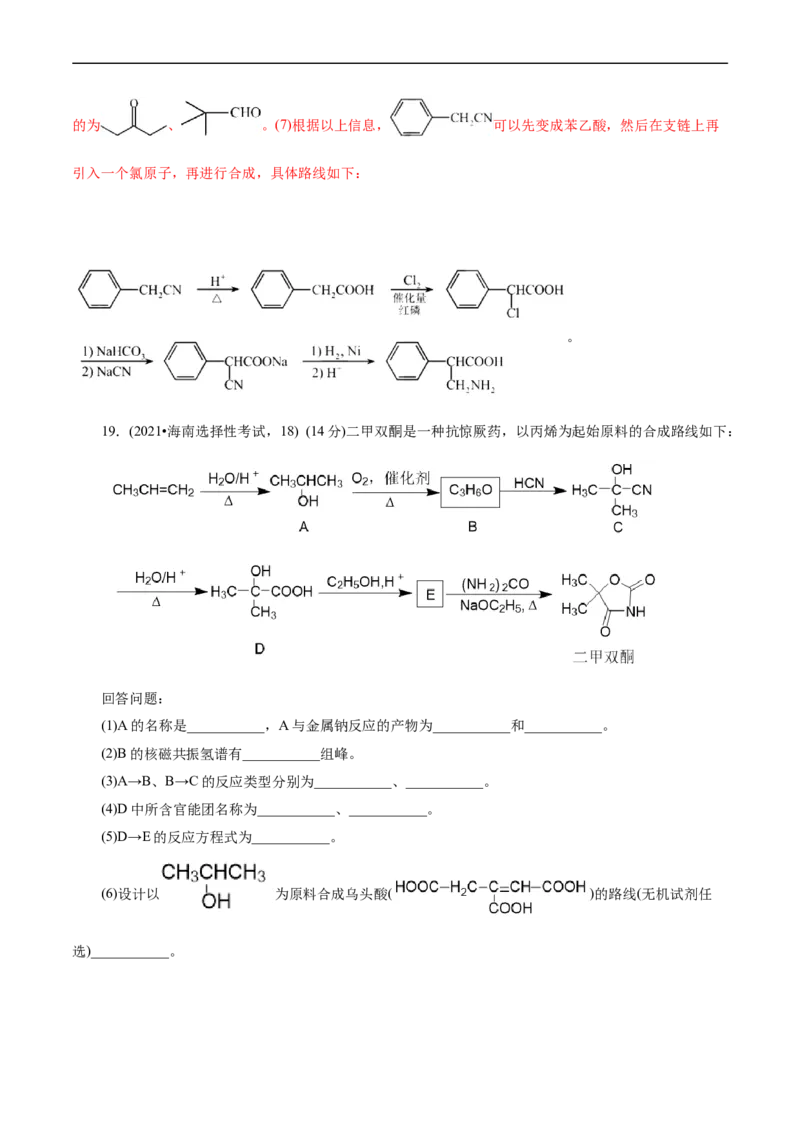
是羰基,结构分别为: 、 、 ,则一共6种,其中核磁共振氢谱中有两组峰的为 、 。(7)根据以上信息, 可以先变成苯乙酸,然后在支链上再
引入一个氯原子,再进行合成,具体路线如下:
。
19.(2021•海南选择性考试,18) (14分)二甲双酮是一种抗惊厥药,以丙烯为起始原料的合成路线如下:
回答问题:
(1)A的名称是___________,A与金属钠反应的产物为___________和___________。
(2)B的核磁共振氢谱有___________组峰。
(3)A→B、B→C的反应类型分别为___________、___________。
(4)D中所含官能团名称为___________、___________。
(5)D→E的反应方程式为___________。
(6)设计以 为原料合成乌头酸( )的路线(无机试剂任
选)___________。已知:① ②
【答案】(1)异丙醇或2-丙醇 异丙醇钠或2-丙醇钠或 氢气
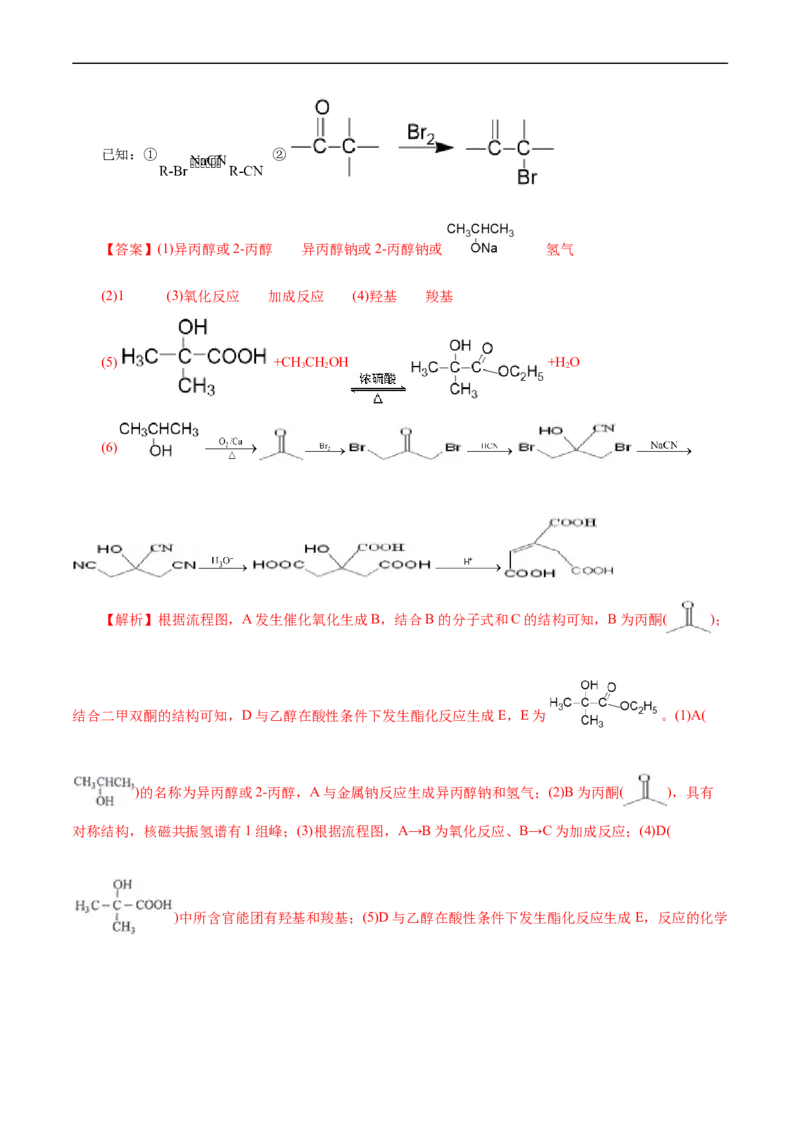
(2)1 (3)氧化反应 加成反应 (4)羟基 羧基
(5) +CH CHOH +H O
3 2 2
(6)
【解析】根据流程图,A发生催化氧化生成B,结合B的分子式和C的结构可知,B为丙酮( );
结合二甲双酮的结构可知,D与乙醇在酸性条件下发生酯化反应生成E,E为 。(1)A(
)的名称为异丙醇或2-丙醇,A与金属钠反应生成异丙醇钠和氢气;(2)B为丙酮( ),具有
对称结构,核磁共振氢谱有1组峰;(3)根据流程图,A→B为氧化反应、B→C为加成反应;(4)D(
)中所含官能团有羟基和羧基;(5)D与乙醇在酸性条件下发生酯化反应生成E,反应的化学方程式为 +CH CHOH +H O;(6)以 为
3 2 2
原料合成乌头酸( ),需要增长碳链和引入羧基,根据题干流程图中BCD的转
化关系,结合已知信息①②,需要将 氧化为丙酮后利用②引入溴原子,在利用①和题干流程图
中BCD的转化关系,即可引入三个羧基,具体合成路线为:
。