文档内容
【基础知识】原电池 化学电源
考点二 燃料电池及陌生方程式书写
【必备知识】
燃料电池(电极本身不包含活性物质,只是一个催化转化元件)
燃料作负极, 空气或 O 作正极。
2
1. 正极的电极反应式书写
①酸性介质(如HSO )或传导质子(H+)固体介质:2O+8e-+8H+===4H O
2 4 2 2
②碱性介质(如KOH):2O+8e-+4HO===8OH-
2 2
③熔融盐介质(如KCO):2O+8e-+4CO===4CO
2 3 2 2
④传导氧离子(O2-)的固体介质:2O+8e-===4O2-
2
2. 负极的电极反应式书写
(1) H
2
①酸性介质(如HSO )或传导质子(H+)固体介质:2H-4e-===4H+
2 4 2
②碱性介质(如KOH):2H+4OH--4e-===4H O
2 2
③熔融盐介质(如KCO):H-2e-+ CO===CO+HO
2 3 2 2 2
④传导氧离子(O2-)的固体介质:H-2e- + O2-===H O
2 2
(2) CH
4
①酸性介质(如HSO )或传导质子(H+)固体介质:CH-8e-+2HO===CO +8H+
2 4 4 2 2
②碱性介质(如KOH):CH-8e-+10 OH-===CO+7HO
4 2
③熔融盐介质(如KCO):CH-8e-+ 4CO===5CO +2HO
2 3 4 2 2
④传导氧离子(O2-)的固体介质:CH-8e-+4O2-===CO +2HO
4 2 2
(3)CHOH
3
①酸性介质(如HSO )或传导质子(H+)固体介质:CHOH -6e-+HO===CO +6H+
2 4 3 2 2
②碱性介质(如KOH):CHOH -6e-+8 OH-===CO+6HO
3 2
③熔融盐介质(如KCO):CHOH -6e-+ 3CO===4CO+2HO
2 3 3 2 2
④传导氧离子(O2-)的固体介质:CHOH -6e-+3O2-===CO +2HO
3 2 2
例:写出以下电极反应式
电池类型 导电介质 反应式总反应 2C H+7O+8OH-===4CO+10HO
2 6 2 2
乙烷(C H)燃料电池 碱性介质
2 6
负极反应 2C H-28e-+36OH-===4CO+24HO
2 6 2
(OH-)
正极反应 7O+14HO+28e-===28OH-
2 2
总反应 C H+5O===3CO+4HO
3 8 2 2 2
熔融碳酸盐
丙烷(C H)燃料电池 负极反应 C H-20e-+10CO===13CO+4HO
3 8 3 8 2 2
(CO)
正极反应 5O+10CO+20e-===10CO
2 2
总反应 C HOH+3O+4OH-===2CO+5HO
2 5 2 2
乙醇(C HOH)燃料电 碱性介质
2 5
负极反应 C HOH-12e-+16OH-===2CO+11HO
2 5 2
池 (OH-)
正极反应 3O+6HO+12e-===12OH-
2 2
总反应 2CO+O===2CO
2 2
固态氧化物
CO燃料电池 负极反应 2CO-4e-+2O2-===2CO
2
(O2-)
正极反应 O+4e-===2O2-
2
总反应 NH+O===N +2HO
2 4 2 2 2
肼(N H)燃料电池 碱性介质
2 4
负极反应 NH-4e-+4OH-===4H O+N
2 4 2 2
(生成氮气和水) (OH-)
正极反应 O+4e-+2HO===4OH-
2 2
总反应 4NH +3O===2N +6HO
3 2 2 2
氨气燃料电池 碱性介质
负极反应 4NH -12e-+12OH-===12H O+2N
3 2 2
(生成无污染的气体) (OH-)
正极反应 3O+12e-+6HO===12OH-
2 2
3. 电极反应式的书写方法
方法一 直接书写
方法二 间接书写
第一步,写出电池总反应式。
第二步,写出电极的正极反应式。第三步,负极反应式=总反应式-正极反应式。
【微点拨】
①若为酸性介质,先补H+,另一边补HO;若为碱性介质,先补OH—,另一边补HO
2 2
②有机物中化合价处理方法:“氧-2,氢+1,最后算碳化合价”,并且要注意溶液环境与产物之间的
反应,碱性环境下,C元素最终产物应为CO2-
3
③水溶液中不能出现O2-;碱性溶液反应物、生成物中均无H+;酸性溶液反应物、生成物中均无OH-,
中性溶液反应物中无H+ 和OH-
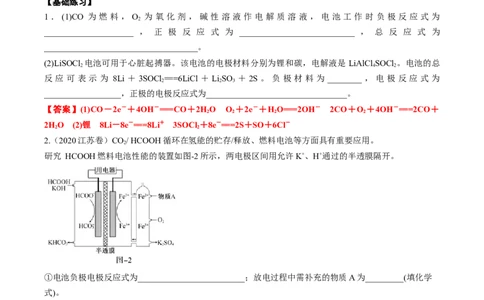
【基础练习】
1 . (1)CO 为 燃 料 , O 为 氧 化 剂 , 碱 性 溶 液 作 电 解 质 溶 液 , 电 池 工 作 时 负 极 反 应 式 为
2
_____________________ , 正 极 反 应 式 为 ___________________________ , 总 反 应 式 为
____________________________________。
(2)LiSOCl 电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是 LiAlCl SOCl 。电池的总
2 4 2
反 应 可 表 示 为 8Li + 3SOCl ===6LiCl + LiSO + 2S 。 负 极 材 料 为 ________ , 电 极 反 应 式 为
2 2 3
__________________,正极的电极反应式为_________________________________。
【答案】(1)CO-2e-+4OH-===CO+2HO O +2e-+HO===2OH- 2CO+O +4OH-===2CO+
2 2 2 2
2HO (2)锂 8Li-8e-===8Li+ 3SOCl +8e-===2S+SO+6Cl-
2 2
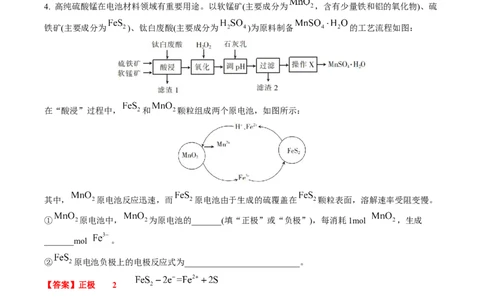
2.(2020江苏卷)CO/ HCOOH循环在氢能的贮存/释放、燃料电池等方面具有重要应用。
2
研究 HCOOH燃料电池性能的装置如图-2所示,两电极区间用允许K+、H+通过的半透膜隔开。
①电池负极电极反应式为_________________________;放电过程中需补充的物质A为_________(填化学
式)。
②图-2所示的 HCOOH燃料电池放电的本质是通过 HCOOH与O 的反应,将化学能转化为电能,其反应
2
的离子方程式为_______________。
【答案】① HSO
2 4
② 或
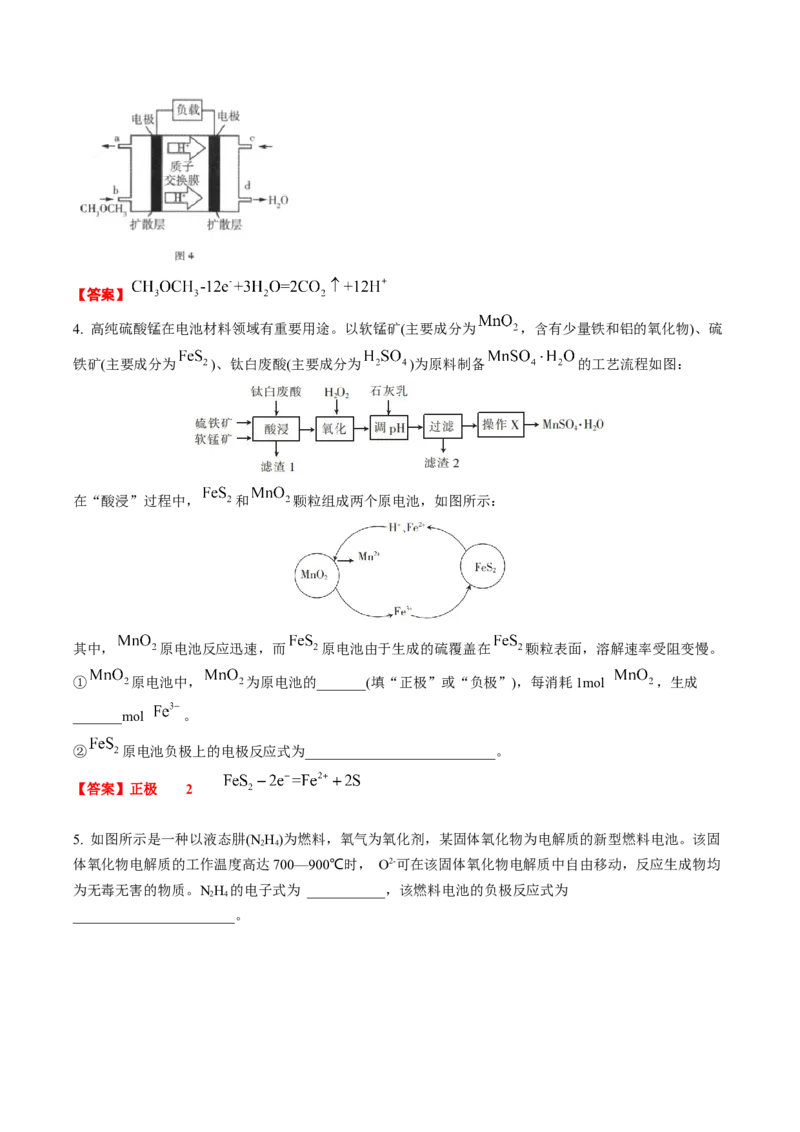
3. COS氢解反应产生的CO可合成二甲醚( ),二甲醚燃料电池的工作原理如图4所示。该电池的
负极反应式为___________。【答案】
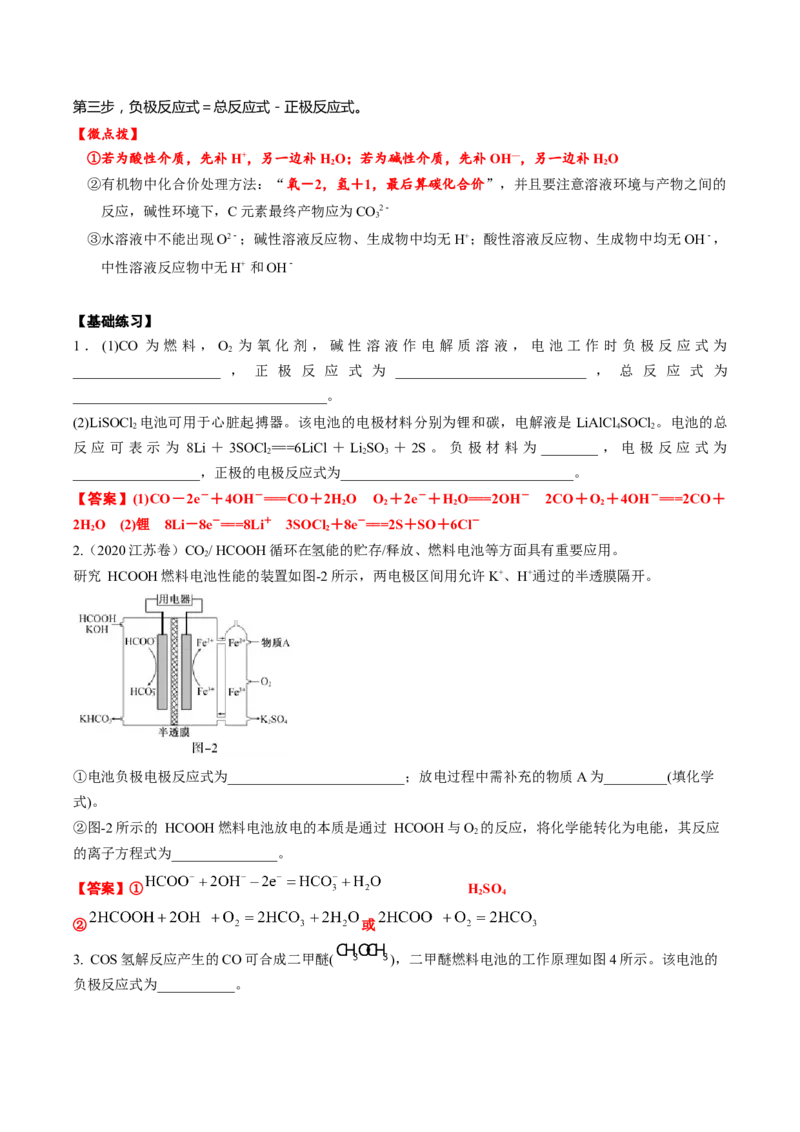
4. 高纯硫酸锰在电池材料领域有重要用途。以软锰矿(主要成分为 ,含有少量铁和铝的氧化物)、硫
铁矿(主要成分为 )、钛白废酸(主要成分为 )为原料制备 的工艺流程如图:
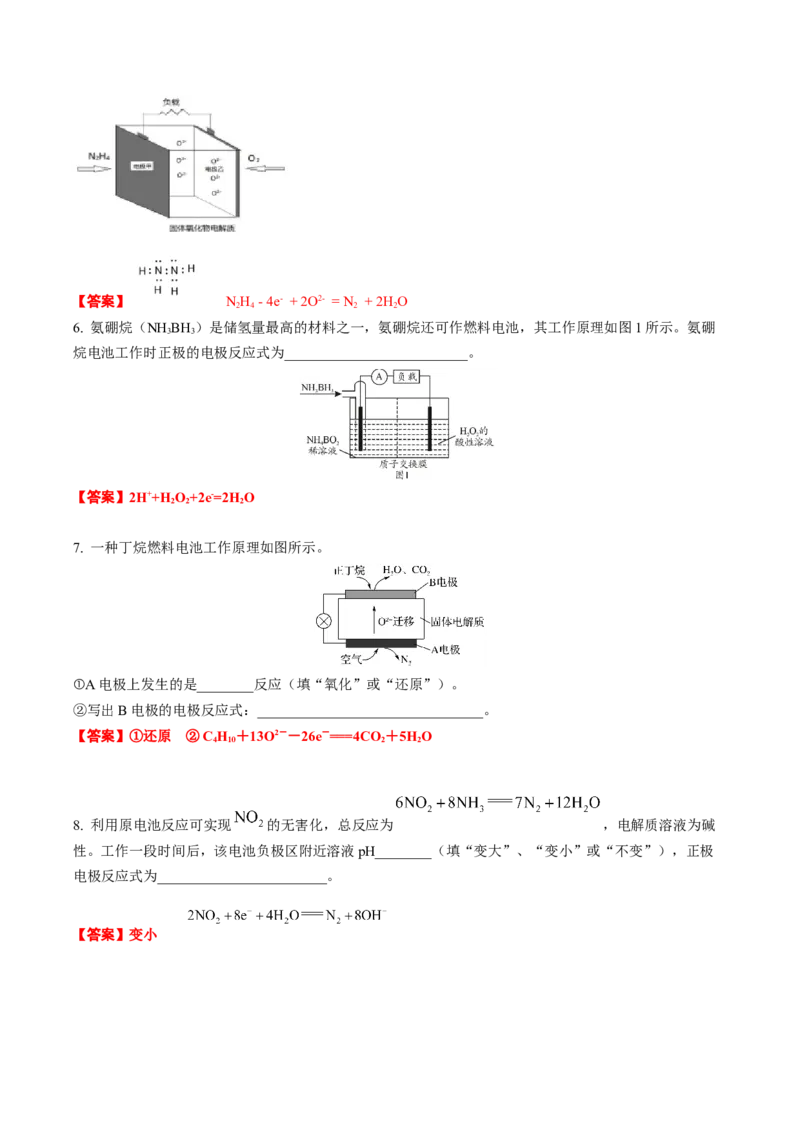
在“酸浸”过程中, 和 颗粒组成两个原电池,如图所示:
其中, 原电池反应迅速,而 原电池由于生成的硫覆盖在 颗粒表面,溶解速率受阻变慢。
① 原电池中, 为原电池的_______(填“正极”或“负极”),每消耗1mol ,生成
_______mol 。
② 原电池负极上的电极反应式为___________________________。
【答案】正极 2
5. 如图所示是一种以液态肼(N H)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。该固
2 4
体氧化物电解质的工作温度高达700—900℃时, O2-可在该固体氧化物电解质中自由移动,反应生成物均
为无毒无害的物质。NH 的电子式为 ___________,该燃料电池的负极反应式为
2 4
_______________________。【答案】 NH - 4e- + 2O2- = N + 2H O
2 4 2 2
6. 氨硼烷(NH BH)是储氢量最高的材料之一,氨硼烷还可作燃料电池,其工作原理如图1所示。氨硼
3 3
烷电池工作时正极的电极反应式为__________________________。
【答案】2H++H O+2e-=2H O
2 2 2
7. 一种丁烷燃料电池工作原理如图所示。
①A电极上发生的是________反应(填“氧化”或“还原”)。
②写出B电极的电极反应式:________________________________。
【答案】①还原 ②CH +13O2--26e-===4CO+5HO
4 10 2 2
8. 利用原电池反应可实现 的无害化,总反应为 ,电解质溶液为碱
性。工作一段时间后,该电池负极区附近溶液pH________(填“变大”、“变小”或“不变”),正极
电极反应式为________________________。
【答案】变小