文档内容
【基础知识】物质的量及计算
考点三 物质的量在化学实验中的应用
【必备知识】
一、物质的量浓度及其计算
1、物质的量浓度
(1)概念
物质的量浓度表示单位体积的溶液里所含溶质B的物质的量,也称为 B 的物质的量浓度 ,符号为c 。
B
(2)表达式:c = 。
B
(3)常用单位: 或mol·m-3,有时也用mmol·L-1。
(4)特点:对于某浓度的溶液,取出任意体积的溶液,其浓度、密度、质量分数均不变,但所含溶质的质量、
物质的量因体积不同而改变。
(5)与质量分数ω的换算公式: 。
2、溶液稀释定律(守恒观点)
(1)溶质的质量在稀释前后保持不变,即ω m =ω m 。
稀 稀 浓 浓
(2)溶质的物质的量在稀释前后保持不变,即 。
(3)溶液质量守恒(体积一般不守恒)。
3、同溶质不同物质的量浓度溶液的混合计算
(1)混合后溶液体积保持不变时,cV+cV=c ×(V +V)。
1 1 2 2 混 1 2
(2)混合后溶液体积发生改变时,cV+cV=c V ,其中V =。
1 1 2 2 混 混 混
例、按要求回答问题
(1)在标准状况下,将V L氨气溶于0.1 L水中,所得溶液的密度为ρ g·cm-3,则此氨水的物质的量浓度
为________ mol·L-1。
(2)将25 g CuSO ·5H O晶体溶于75 g水中,配成溶液,所得溶液的溶质质量分数为________。
4 2
(3)将a mL 5 mol·L-1 NaCl溶液稀释至b mL,稀释后溶液中Cl-的物质的量浓度为________。
(4)200 mL 0.3 mol·L-1 KSO 溶液和100 mL 0.2 mol·L-1 Fe (SO ) 溶液混合后不考虑混合后溶液体积的
2 4 2 4 3
变化,溶液中SO的物质的量浓度为________。
二、溶液的配制
1、仪器:玻璃棒、容量瓶、胶头滴管、烧杯、天平、量筒。
(1)托盘天平:① 物 码 ②精确度 g
(2)容量瓶: 检漏操作:
【特别提醒】容量瓶使用的四个“不能”
①不能将固体或浓溶液直接在容量瓶中溶解或稀释;②不能作为反应容器或用来长期贮存溶液;
③不能将过冷或过热的溶液转移到容量瓶中,(因为容量瓶的容积是在瓶身所标温度下确定的);
④不能配制任意体积的溶液,只能配制容量瓶上规定容积的溶液。
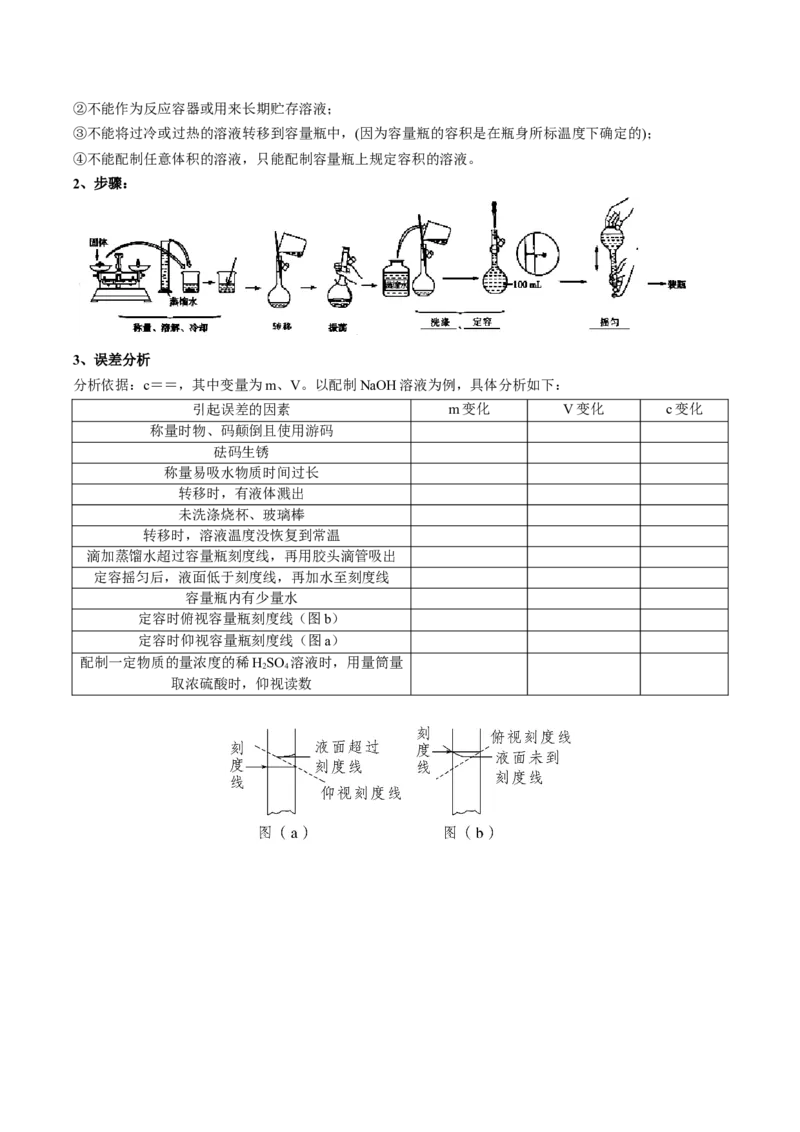
2、步骤:
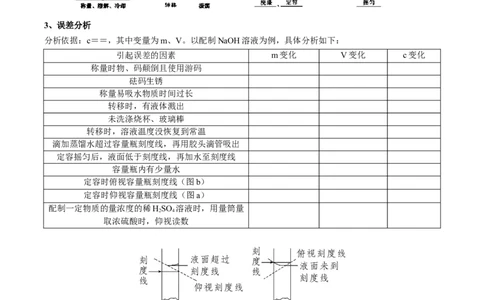
3、误差分析
分析依据:c==,其中变量为m、V。以配制NaOH溶液为例,具体分析如下:
引起误差的因素 m变化 V变化 c变化
称量时物、码颠倒且使用游码
砝码生锈
称量易吸水物质时间过长
转移时,有液体溅出
未洗涤烧杯、玻璃棒
转移时,溶液温度没恢复到常温
滴加蒸馏水超过容量瓶刻度线,再用胶头滴管吸出
定容摇匀后,液面低于刻度线,再加水至刻度线
容量瓶内有少量水
定容时俯视容量瓶刻度线(图b)
定容时仰视容量瓶刻度线(图a)
配制一定物质的量浓度的稀HSO 溶液时,用量筒量
2 4
取浓硫酸时,仰视读数例、按要求回答问题
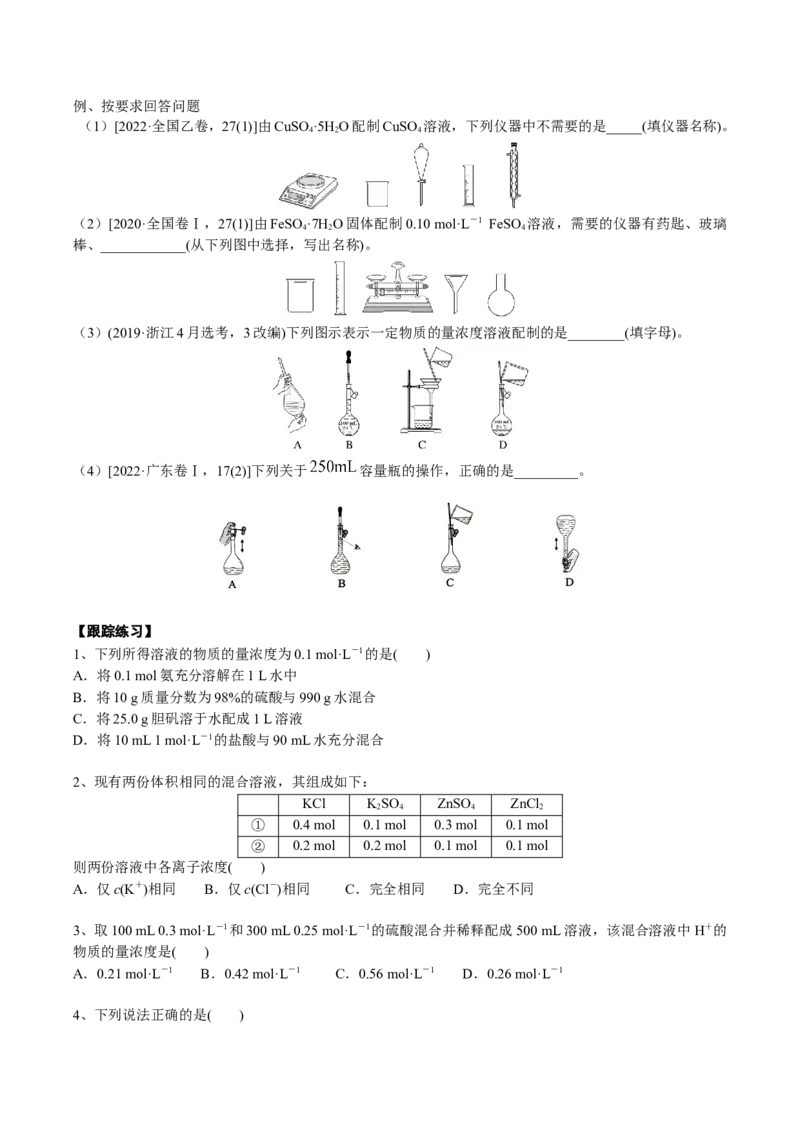
(1)[2022·全国乙卷,27(1)]由CuSO ·5H O配制CuSO 溶液,下列仪器中不需要的是_____(填仪器名称)。
4 2 4
(2)[2020·全国卷Ⅰ,27(1)]由FeSO ·7H O固体配制0.10 mol·L-1 FeSO 溶液,需要的仪器有药匙、玻璃
4 2 4
棒、____________(从下列图中选择,写出名称)。
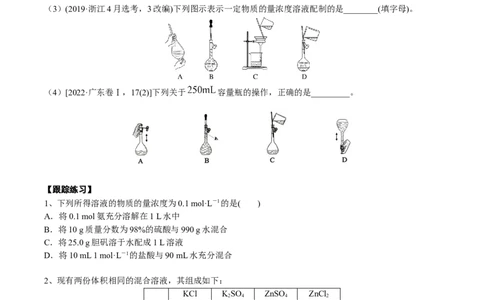
(3)(2019·浙江4月选考,3改编)下列图示表示一定物质的量浓度溶液配制的是________(填字母)。
(4)[2022·广东卷Ⅰ,17(2)]下列关于 容量瓶的操作,正确的是_________。
【跟踪练习】
1、下列所得溶液的物质的量浓度为0.1 mol·L-1的是( )
A.将0.1 mol氨充分溶解在1 L水中
B.将10 g质量分数为98%的硫酸与990 g水混合
C.将25.0 g胆矾溶于水配成1 L溶液
D.将10 mL 1 mol·L-1的盐酸与90 mL水充分混合
2、现有两份体积相同的混合溶液,其组成如下:
KCl KSO ZnSO ZnCl
2 4 4 2
① 0.4 mol 0.1 mol 0.3 mol 0.1 mol
② 0.2 mol 0.2 mol 0.1 mol 0.1 mol
则两份溶液中各离子浓度( )
A.仅c(K+)相同 B.仅c(Cl-)相同 C.完全相同 D.完全不同
3、取100 mL 0.3 mol·L-1和300 mL 0.25 mol·L-1的硫酸混合并稀释配成500 mL溶液,该混合溶液中H+的
物质的量浓度是( )
A.0.21 mol·L-1 B.0.42 mol·L-1 C.0.56 mol·L-1 D.0.26 mol·L-1
4、下列说法正确的是( )A.把100 mL 3 mol·L-1的HSO 跟100 mL H O混合,硫酸的物质的量浓度为1.5 mol·L-1
2 4 2
B.把100 g 20%的NaCl溶液跟100 g HO混合后,NaCl溶液的溶质质量分数是10%
2
C.把200 mL 3 mol·L-1的BaCl 溶液跟100 mL 3 mol·L-1的KCl溶液混合后,溶液中的c(Cl-)仍然是3
2
mol·L-1
D.把100 mL 20%的NaOH溶液跟100 mL H O混合后,NaOH溶液的溶质质量分数是10%
2
5、配制250 mL 0.5 mol·L-1的NaOH溶液,在下列仪器中:①量筒、②250 mL容量瓶、
③托盘天平和砝码、④500 mL容量瓶、⑤烧杯、⑥玻璃棒、⑦漏斗、⑧药匙、⑨胶头滴管、⑩250 mL烧
瓶,需要用到的仪器按使用先后顺序排列正确的是( )
A.⑧③⑤⑥②⑨ B.②③⑦⑤⑥
C.②⑤⑦⑥① D.④③⑦⑤⑥
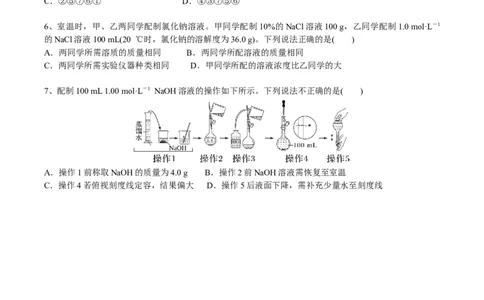
6、室温时,甲、乙两同学配制氯化钠溶液。甲同学配制10%的NaCl溶液100 g,乙同学配制1.0 mol·L-1
的NaCl溶液100 mL(20 ℃时,氯化钠的溶解度为36.0 g)。下列说法正确的是( )
A.两同学所需溶质的质量相同 B.两同学所配溶液的质量相同
C.两同学所需实验仪器种类相同 D.甲同学所配的溶液浓度比乙同学的大
7、配制100 mL 1.00 mol·L-1 NaOH溶液的操作如下所示。下列说法不正确的是( )
A.操作1前称取NaOH的质量为4.0 g B.操作2前NaOH溶液需恢复至室温
C.操作4若俯视刻度线定容,结果偏大 D.操作5后液面下降,需补充少量水至刻度线8、人体血液里 Ca2+的浓度一般采用 m g·cm-3来表示。抽取一定体积的血样,加适量的草酸铵
[(NH )C O]溶液,可析出草酸钙(CaC O)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H C O),再用
4 2 2 4 2 4 2 2 4
酸性KMnO 溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样
4
品中Ca2+的浓度。
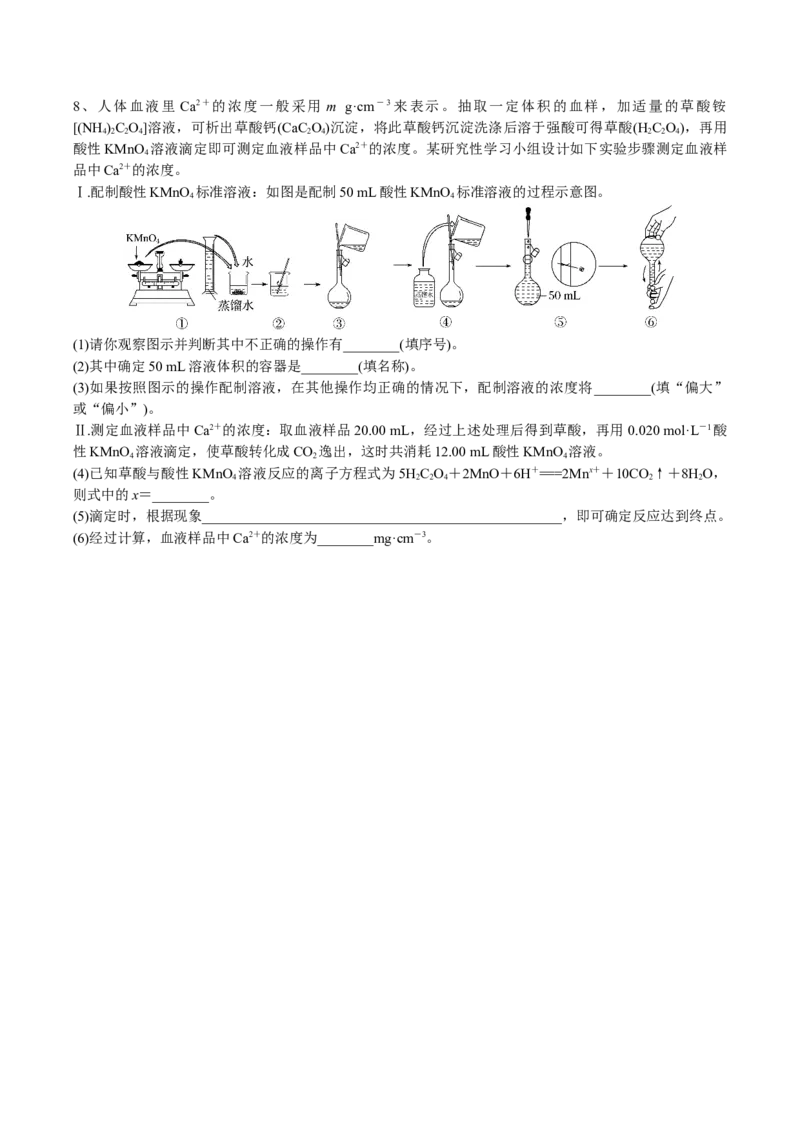
Ⅰ.配制酸性KMnO 标准溶液:如图是配制50 mL酸性KMnO 标准溶液的过程示意图。
4 4
(1)请你观察图示并判断其中不正确的操作有________(填序号)。
(2)其中确定50 mL溶液体积的容器是________(填名称)。
(3)如果按照图示的操作配制溶液,在其他操作均正确的情况下,配制溶液的浓度将________(填“偏大”
或“偏小”)。
Ⅱ.测定血液样品中Ca2+的浓度:取血液样品20.00 mL,经过上述处理后得到草酸,再用0.020 mol·L-1酸
性KMnO 溶液滴定,使草酸转化成CO 逸出,这时共消耗12.00 mL酸性KMnO 溶液。
4 2 4
(4)已知草酸与酸性KMnO 溶液反应的离子方程式为5HC O +2MnO+6H+===2Mnx++10CO↑+8HO,
4 2 2 4 2 2
则式中的x=________。
(5)滴定时,根据现象___________________________________________________,即可确定反应达到终点。
(6)经过计算,血液样品中Ca2+的浓度为________mg·cm-3。