文档内容
【基础知识】物质的量及计算
考点三 物质的量在化学实验中的应用
【必备知识】
一、物质的量浓度及其计算
1、物质的量浓度
(1)概念
物质的量浓度表示单位体积的溶液里所含溶质B的物质的量,也称为 B 的物质的量浓度 ,符号为c 。
B
(2)表达式:c =。
B
(3)常用单位: mol·L - 1 或mol·m-3,有时也用mmol·L-1。
(4)特点:对于某浓度的溶液,取出任意体积的溶液,其浓度、密度、质量分数均不变,但所含溶质的质量、
物质的量因体积不同而改变。
1000ρω
(5)与质量分数ω的换算公式:c= 。
M
2、溶液稀释定律(守恒观点)
(1)溶质的质量在稀释前后保持不变,即ω m =ω m 。
稀 稀 浓 浓
(2)溶质的物质的量在稀释前后保持不变,即c V =c V 。
稀 稀 浓 浓
(3)溶液质量守恒(体积一般不守恒)。
3、同溶质不同物质的量浓度溶液的混合计算
(1)混合后溶液体积保持不变时,cV+cV=c ×(V +V)。
1 1 2 2 混 1 2
(2)混合后溶液体积发生改变时,cV+cV=c V ,其中V =。
1 1 2 2 混 混 混
例、按要求回答问题
(1)在标准状况下,将V L氨气溶于0.1 L水中,所得溶液的密度为ρ g·cm-3,则此氨水的物质的量浓度
为________ mol·L-1。
(2)将25 g CuSO ·5H O晶体溶于75 g水中,配成溶液,所得溶液的溶质质量分数为________。
4 2
(3)将a mL 5 mol·L-1 NaCl溶液稀释至b mL,稀释后溶液中Cl-的物质的量浓度为________。
(4)200 mL 0.3 mol·L-1 KSO 溶液和100 mL 0.2 mol·L-1 Fe (SO ) 溶液混合后不考虑混合后溶液体积的
2 4 2 4 3
变化,溶液中SO的物质的量浓度为________。
【答案】 (1) (2)16% (3) mol·L-1 (4)0.4 mol·L-1
【解析】 (1)n(NH)= mol,溶液体积为×10-3 L,c= mol·L-1= mol·L-1。
3
(4)200 mL 0.3 mol·L-1 KSO 溶液中SO的物质的量为0.2 L×0.3 mol·L-1=0.06 mol,100 mL 0.2 mol·L
2 4
-1 Fe(SO ) 溶液中SO的物质的量为3×0.1 L×0.2 mol·L-1=0.06 mol,故混合液中SO的物质的量为0.06
2 4 3
mol+0.06 mol=0.12 mol,由于混合后不考虑体积的变化,混合后溶液的体积为0.3 L,混合液中SO的物
质的量浓度为=0.4 mol·L-1。
二、溶液的配制
1、仪器:玻璃棒、容量瓶、胶头滴管、烧杯、天平、量筒。
(1)托盘天平:①左物右码 ②精确度0.1g
(2)容量瓶: 检漏操作:
【特别提醒】容量瓶使用的四个“不能”
①不能将固体或浓溶液直接在容量瓶中溶解或稀释;
②不能作为反应容器或用来长期贮存溶液;
③不能将过冷或过热的溶液转移到容量瓶中,(因为容量瓶的容积是在瓶身所标温度下确定的);④不能配制任意体积的溶液,只能配制容量瓶上规定容积的溶液。
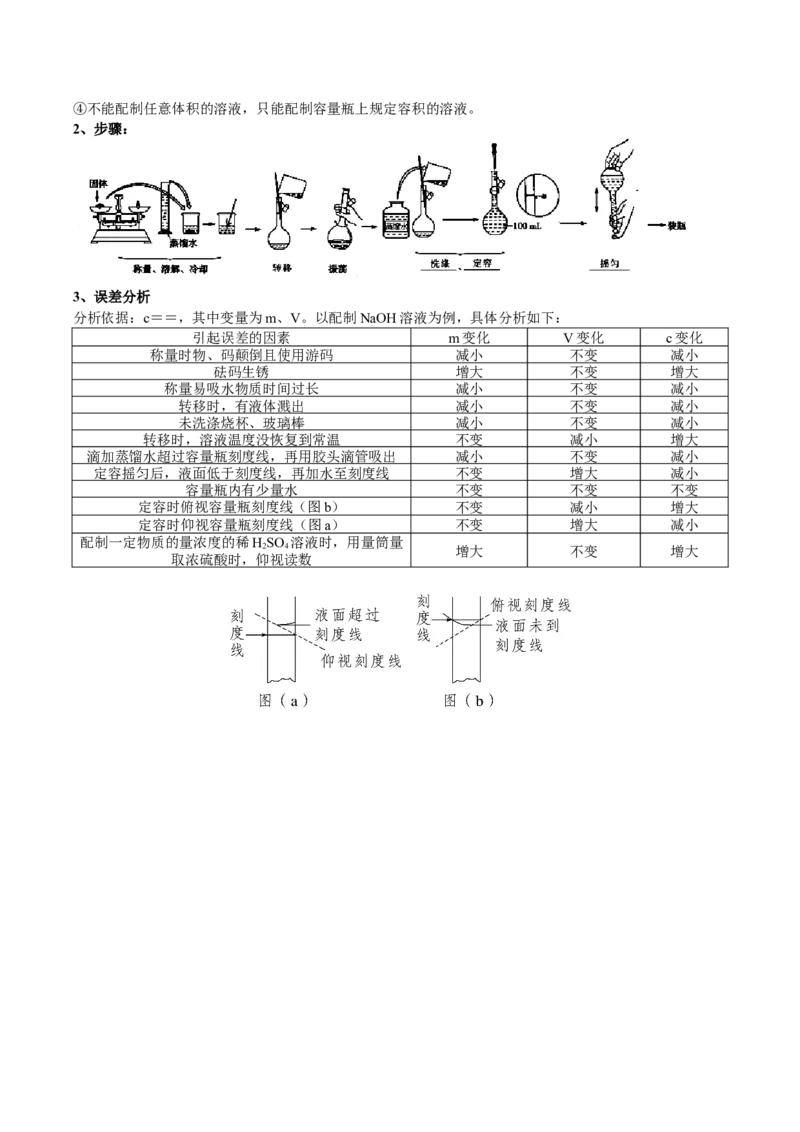
2、步骤:
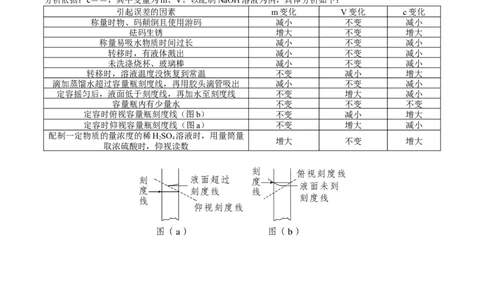
3、误差分析
分析依据:c==,其中变量为m、V。以配制NaOH溶液为例,具体分析如下:
引起误差的因素 m变化 V变化 c变化
称量时物、码颠倒且使用游码 减小 不变 减小
砝码生锈 增大 不变 增大
称量易吸水物质时间过长 减小 不变 减小
转移时,有液体溅出 减小 不变 减小
未洗涤烧杯、玻璃棒 减小 不变 减小
转移时,溶液温度没恢复到常温 不变 减小 增大
滴加蒸馏水超过容量瓶刻度线,再用胶头滴管吸出 减小 不变 减小
定容摇匀后,液面低于刻度线,再加水至刻度线 不变 增大 减小
容量瓶内有少量水 不变 不变 不变
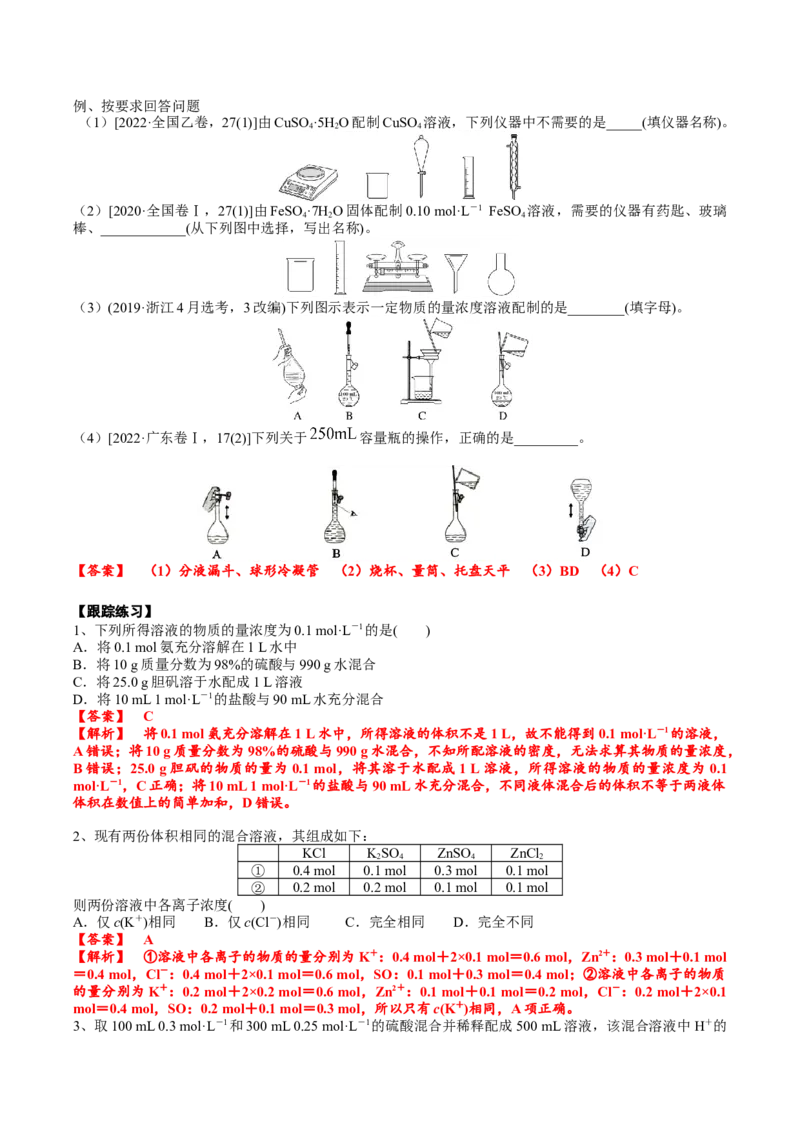
定容时俯视容量瓶刻度线(图b) 不变 减小 增大
定容时仰视容量瓶刻度线(图a) 不变 增大 减小
配制一定物质的量浓度的稀HSO 溶液时,用量筒量
2 4 增大 不变 增大
取浓硫酸时,仰视读数例、按要求回答问题
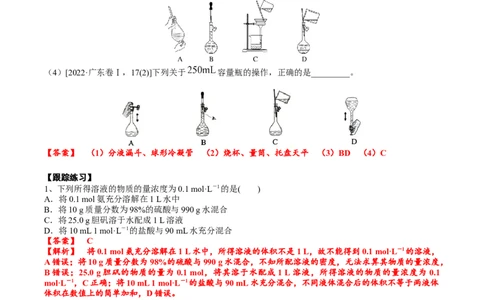
(1)[2022·全国乙卷,27(1)]由CuSO ·5H O配制CuSO 溶液,下列仪器中不需要的是_____(填仪器名称)。
4 2 4
(2)[2020·全国卷Ⅰ,27(1)]由FeSO ·7H O固体配制0.10 mol·L-1 FeSO 溶液,需要的仪器有药匙、玻璃
4 2 4
棒、____________(从下列图中选择,写出名称)。
(3)(2019·浙江4月选考,3改编)下列图示表示一定物质的量浓度溶液配制的是________(填字母)。
(4)[2022·广东卷Ⅰ,17(2)]下列关于 容量瓶的操作,正确的是_________。
【答案】 (1)分液漏斗、球形冷凝管 (2)烧杯、量筒、托盘天平 (3)BD (4)C
【跟踪练习】
1、下列所得溶液的物质的量浓度为0.1 mol·L-1的是( )
A.将0.1 mol氨充分溶解在1 L水中
B.将10 g质量分数为98%的硫酸与990 g水混合
C.将25.0 g胆矾溶于水配成1 L溶液
D.将10 mL 1 mol·L-1的盐酸与90 mL水充分混合
【答案】 C
【解析】 将0.1 mol氨充分溶解在1 L水中,所得溶液的体积不是1 L,故不能得到0.1 mol·L-1的溶液,
A错误;将10 g质量分数为98%的硫酸与990 g水混合,不知所配溶液的密度,无法求算其物质的量浓度,
B错误;25.0 g胆矾的物质的量为 0.1 mol,将其溶于水配成 1 L溶液,所得溶液的物质的量浓度为 0.1
mol·L-1,C正确;将10 mL 1 mol·L-1的盐酸与90 mL水充分混合,不同液体混合后的体积不等于两液体
体积在数值上的简单加和,D错误。
2、现有两份体积相同的混合溶液,其组成如下:
KCl KSO ZnSO ZnCl
2 4 4 2
① 0.4 mol 0.1 mol 0.3 mol 0.1 mol
② 0.2 mol 0.2 mol 0.1 mol 0.1 mol
则两份溶液中各离子浓度( )
A.仅c(K+)相同 B.仅c(Cl-)相同 C.完全相同 D.完全不同
【答案】 A
【解析】 ①溶液中各离子的物质的量分别为K+:0.4 mol+2×0.1 mol=0.6 mol,Zn2+:0.3 mol+0.1 mol
=0.4 mol,Cl-:0.4 mol+2×0.1 mol=0.6 mol,SO:0.1 mol+0.3 mol=0.4 mol;②溶液中各离子的物质
的量分别为K+:0.2 mol+2×0.2 mol=0.6 mol,Zn2+:0.1 mol+0.1 mol=0.2 mol,Cl-:0.2 mol+2×0.1
mol=0.4 mol,SO:0.2 mol+0.1 mol=0.3 mol,所以只有c(K+)相同,A项正确。
3、取100 mL 0.3 mol·L-1和300 mL 0.25 mol·L-1的硫酸混合并稀释配成500 mL溶液,该混合溶液中H+的物质的量浓度是( )
A.0.21 mol·L-1 B.0.42 mol·L-1
C.0.56 mol·L-1 D.0.26 mol·L-1
【答案】 B
【解析】 该混合溶液中H+的物质的量n(H+)=(0.1 L×0.3 mol·L-1+0.3 L×0.25 mol·L-1)×2=0.21 mol,
所以c(H+)==0.42 mol·L-1。
4、下列说法正确的是( )
A.把100 mL 3 mol·L-1的HSO 跟100 mL H O混合,硫酸的物质的量浓度为1.5 mol·L-1
2 4 2
B.把100 g 20%的NaCl溶液跟100 g HO混合后,NaCl溶液的溶质质量分数是10%
2
C.把200 mL 3 mol·L-1的BaCl 溶液跟100 mL 3 mol·L-1的KCl溶液混合后,溶液中的c(Cl-)仍然是3
2
mol·L-1
D.把100 mL 20%的NaOH溶液跟100 mL H O混合后,NaOH溶液的溶质质量分数是10%
2
【答案】 B
【解析】 把100 mL 3 mol·L-1的HSO 跟100 mL H O混合,溶液的总体积小于200 mL,硫酸的物质的
2 4 2
量浓度大于1.5 mol·L-1,A错误;与水混合前后,NaCl的质量不变,则把100 g 20%的NaCl溶液跟100 g
HO混合后,NaCl溶液的溶质质量分数为×100%=10%,B正确;3 mol·L-1的BaCl 溶液中氯离子浓度
2 2
为6 mol·L-1,3 mol·L-1的KCl溶液中氯离子浓度为3 mol·L-1,混合后氯离子浓度在3~6 mol·L-1之间,C
错误;氢氧化钠溶液的密度与水的密度不相同,不知道氢氧化钠溶液的密度,无法计算混合后溶液的总质
量,D错误。
5、配制250 mL 0.5 mol·L-1的NaOH溶液,在下列仪器中:①量筒、②250 mL容量瓶、
③托盘天平和砝码、④500 mL容量瓶、⑤烧杯、⑥玻璃棒、⑦漏斗、⑧药匙、⑨胶头滴管、⑩250 mL烧
瓶,需要用到的仪器按使用先后顺序排列正确的是( )
A.⑧③⑤⑥②⑨ B.②③⑦⑤⑥
C.②⑤⑦⑥① D.④③⑦⑤⑥
【答案】 A
【解析】 一定规格的容量瓶只能配制相应体积的溶液,故应选择 250 mL容量瓶;用药匙取用固体药品,
用托盘天平称量一定质量的药品(药品可放在烧杯中称量)后,在烧杯中溶解(可用量筒量取水),并用玻璃棒
搅拌,待溶液冷却至室温后转移到250 mL容量瓶中,转移过程中需用玻璃棒引流,用蒸馏水洗涤烧杯内
壁和玻璃棒2~3次,并将洗涤液转移到容量瓶中,当加水至液面距离刻度线1~2 cm时,改用胶头滴管滴
加至溶液凹液面恰好与刻度线相切,盖好瓶塞,摇匀。所以需要用到的仪器及先后顺序为药匙、托盘天平
和砝码、烧杯、量筒(也可不用)、玻璃棒、250 mL容量瓶、胶头滴管,即⑧③⑤(①)⑥②⑨,A项符合。
6、室温时,甲、乙两同学配制氯化钠溶液。甲同学配制10%的NaCl溶液100 g,乙同学配制1.0 mol·L-1
的NaCl溶液100 mL(20 ℃时,氯化钠的溶解度为36.0 g)。下列说法正确的是( )
A.两同学所需溶质的质量相同 B.两同学所配溶液的质量相同
C.两同学所需实验仪器种类相同 D.甲同学所配的溶液浓度比乙同学的大
【答案】 D
【解析】 配制100 g 10%的NaCl溶液需要氯化钠的质量为100 g×10%=10 g,配制100 mL
1.0 mol·L-1的NaCl溶液需要氯化钠的质量为0.1 L×1.0 mol·L-1×58.5 g·mol-1=5.85 g,二者需要氯化钠的
质量不相等,A错误;氯化钠溶液的密度大于1 g·mL-1,100 mL氯化钠溶液的质量大于100 g,B错误;配
制一定质量分数的氯化钠溶液,所需仪器有托盘天平、量筒、烧杯、玻璃棒、药匙等;配制 100 mL一定
物质的量浓度的氯化钠溶液,需要的仪器有托盘天平、烧杯、玻璃棒、药匙、100 mL容量瓶、胶头滴管
等,需要的仪器不同,C错误;配制10%的NaCl溶液100 g,其密度大于1 g·mL-1,所以100 g溶液的体
积小于100 mL,10%的NaCl溶液中氯化钠的物质的量为≈0.17 mol,其物质的量浓度大于1.7 mol·L-1,D
正确。
7、配制100 mL 1.00 mol·L-1 NaOH溶液的操作如下所示。下列说法不正确的是( )A.操作1前称取NaOH的质量为4.0 g B.操作2前NaOH溶液需恢复至室温
C.操作4若俯视刻度线定容,结果偏大 D.操作5后液面下降,需补充少量水至刻度线
【答案】 D
【解析】 操作1前称取NaOH的质量m(NaOH)=0.1 L×1.00 mol·L-1×40 g·mol-1=4.0 g,故A正确;转
移溶液之前应将溶液冷却至室温即操作2前NaOH溶液需恢复至室温,故B正确;操作4若俯视刻度线定
容,溶液体积偏小,物质的量浓度偏大,故 C正确;操作5后液面下降,液体可能在容量瓶和瓶塞之间,
不能补充水,故D错误。
8、人体血液里 Ca2+的浓度一般采用 m g·cm-3来表示。抽取一定体积的血样,加适量的草酸铵
[(NH )C O]溶液,可析出草酸钙(CaC O)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H C O),再用
4 2 2 4 2 4 2 2 4
酸性KMnO 溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样
4
品中Ca2+的浓度。
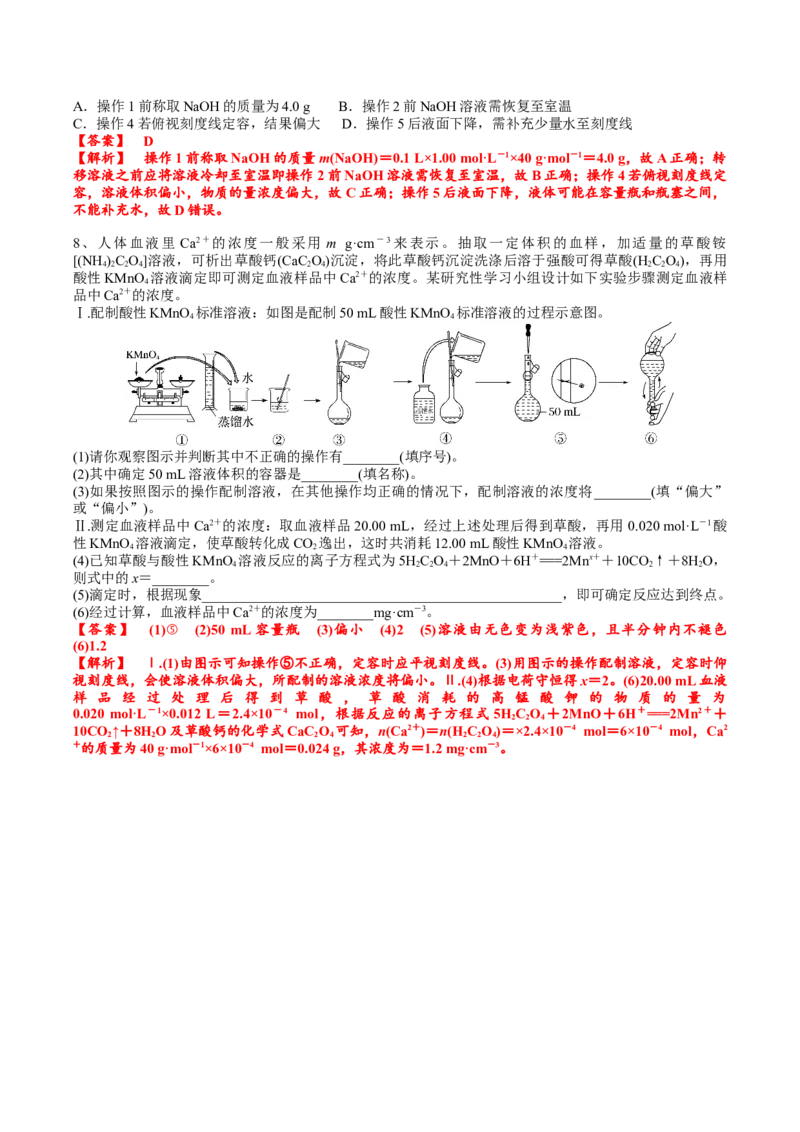
Ⅰ.配制酸性KMnO 标准溶液:如图是配制50 mL酸性KMnO 标准溶液的过程示意图。
4 4
(1)请你观察图示并判断其中不正确的操作有________(填序号)。
(2)其中确定50 mL溶液体积的容器是________(填名称)。
(3)如果按照图示的操作配制溶液,在其他操作均正确的情况下,配制溶液的浓度将________(填“偏大”
或“偏小”)。
Ⅱ.测定血液样品中Ca2+的浓度:取血液样品20.00 mL,经过上述处理后得到草酸,再用0.020 mol·L-1酸
性KMnO 溶液滴定,使草酸转化成CO 逸出,这时共消耗12.00 mL酸性KMnO 溶液。
4 2 4
(4)已知草酸与酸性KMnO 溶液反应的离子方程式为5HC O +2MnO+6H+===2Mnx++10CO↑+8HO,
4 2 2 4 2 2
则式中的x=________。
(5)滴定时,根据现象___________________________________________________,即可确定反应达到终点。
(6)经过计算,血液样品中Ca2+的浓度为________mg·cm-3。
【答案】 (1)⑤ (2)50 mL 容量瓶 (3)偏小 (4)2 (5)溶液由无色变为浅紫色,且半分钟内不褪色
(6)1.2
【解析】 Ⅰ.(1)由图示可知操作⑤不正确,定容时应平视刻度线。(3)用图示的操作配制溶液,定容时仰
视刻度线,会使溶液体积偏大,所配制的溶液浓度将偏小。Ⅱ.(4)根据电荷守恒得x=2。(6)20.00 mL血液
样 品 经 过 处 理 后 得 到 草 酸 , 草 酸 消 耗 的 高 锰 酸 钾 的 物 质 的 量 为
0.020 mol·L-1×0.012 L=2.4×10-4 mol,根据反应的离子方程式 5HCO +2MnO+6H+===2Mn2++
2 2 4
10CO ↑+8HO及草酸钙的化学式CaC O 可知,n(Ca2+)=n(H CO)=×2.4×10-4 mol=6×10-4 mol,Ca2
2 2 2 4 2 2 4
+的质量为40 g·mol-1×6×10-4 mol=0.024 g,其浓度为=1.2 mg·cm-3。