文档内容
【基础知识】离子反应
考点二 离子方程式书写
一、离子方程式书写
完成下列反应的离子方程式,注意难溶微粒、气体、难电离微粒的书写形式。
(1) 氧化镁溶于稀硫酸: 。
(2) 向AlCl 溶液中滴加过量的氨水: 。
3
(3) 向NaHSO 溶液中加入过量NaHSO 溶液: 。
3 4
(4) 向澄清石灰水中加入稀盐酸: 。
(5) NaSO 溶液与AgNO 溶液混合: 。
2 4 3
(6) 铵盐溶液与强碱溶液混合加热检测NH: 。
(7) 过氧化钠溶于水: 。
(8) 用MnO 与浓盐酸共热制Cl: 。
2 2
(9) Cl 溶于水: 。
2
(10) 铜溶于浓硝酸: 。
(11) Ba(OH) 溶液与HSO 溶液混合: 。
2 2 4
(12) Ba(OH) 溶液与(NH )SO 溶液混合: 。
2 4 2 4
(13) CuSO 溶液与Ba(OH) 溶液混合: 。
4 2
(14) 向MgSO 溶液中加入(NH )CO 溶液生成Mg(OH) ·MgCO :
4 4 2 3 2 3
(15) BaS溶液与硫酸锌溶液混合生成立德粉(ZnS·BaSO ):
4
(16) 向MnCl 溶液中加入NH HCO 生成MnCO :
2 4 3 3
(17)已知PbSO 不溶于水,但可溶于醋酸铵溶液,反应方程式如下: ,将硫化钠
4
溶液与醋酸铅溶液混合,可生成沉淀,写出反应的离子方程式:
(18) Na S O 溶液中加入稀硫酸:
2 2 3
(19) 氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于水,在潮湿空气中易水解氧化,且在氯
离子浓度较大的体系中存在CuCl+Cl-===[CuCl ]-。工业上用低品铜矿(主要含CuS、Cu S、FeO等)制备
2 2
CuCl的一种工艺流程如图所示:①滤渣Ⅱ的主要成分为MnCO ,写出除Mn2+的离子方程式:___________________________。
3
②写出反应Ⅱ中发生反应的离子方程式:_______________________________________________。
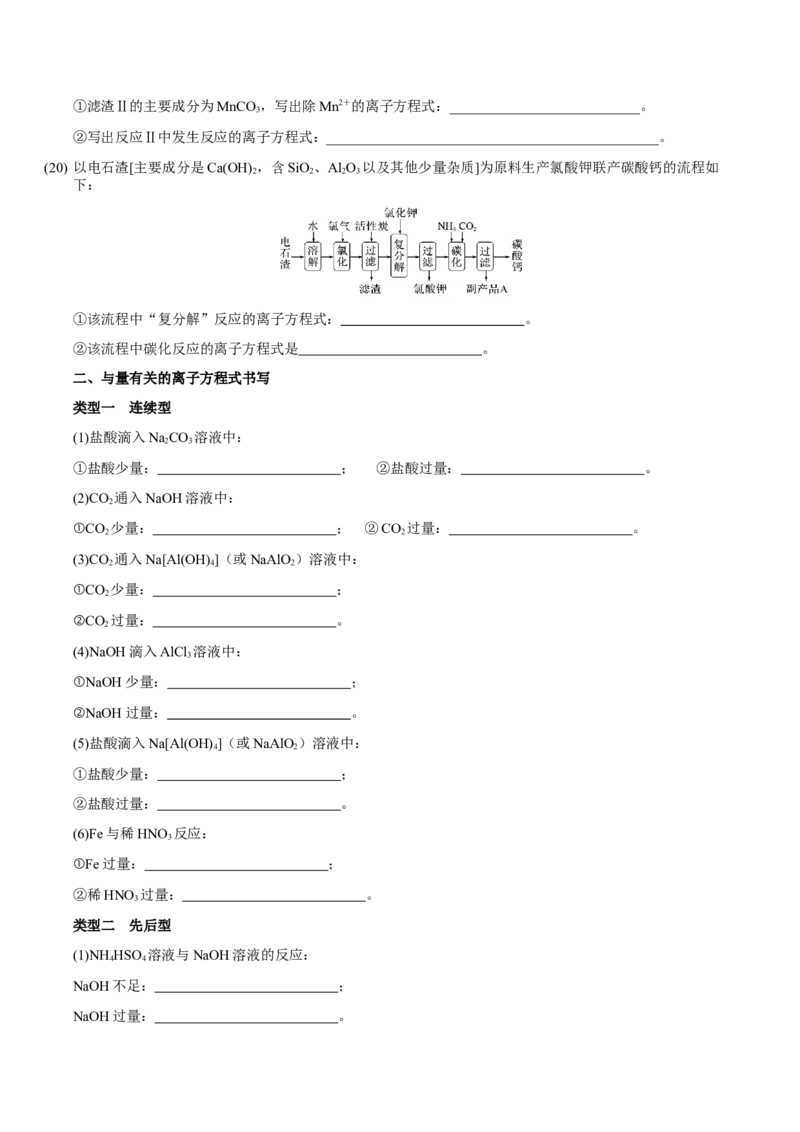
(20) 以电石渣[主要成分是Ca(OH) ,含SiO、Al O 以及其他少量杂质]为原料生产氯酸钾联产碳酸钙的流程如
2 2 2 3
下:
①该流程中“复分解”反应的离子方程式: 。
②该流程中碳化反应的离子方程式是 。
二、与量有关的离子方程式书写
类型一 连续型
(1)盐酸滴入NaCO 溶液中:
2 3
①盐酸少量: ; ②盐酸过量: 。
(2)CO 通入NaOH溶液中:
2
①CO 少量: ; ②CO 过量: 。
2 2
(3)CO 通入Na[Al(OH)](或NaAlO )溶液中:
2 4 2
①CO 少量: ;
2
②CO 过量: 。
2
(4)NaOH滴入AlCl 溶液中:
3
①NaOH少量: ;
②NaOH过量: 。
(5)盐酸滴入Na[Al(OH)](或NaAlO )溶液中:
4 2
①盐酸少量: ;
②盐酸过量: 。
(6)Fe与稀HNO 反应:
3
①Fe过量: ;
②稀HNO 过量: 。
3
类型二 先后型
(1)NH HSO 溶液与NaOH溶液的反应:
4 4
NaOH不足: ;
NaOH过量: 。(2)向含有H+、Al3+、NH的溶液中,逐滴加入NaOH溶液至过量,反应依次为
① ;② ;
③ ;④ 。
(3)向含有OH-、CO、[Al(OH) ]-(或NaAlO )的溶液中,逐滴加入稀盐酸至过量,反应依次为
4 2
① ;② ;
③ 、④ 。
(4)向FeBr 溶液中通Cl:
2 2
通入少量Cl: ;
2
通入过量Cl: 。
2
类型三 配比型
(1)Ca(HCO ) 溶液与NaOH溶液反应:
3 2
①NaOH不足: ;
②NaOH过量: 。
(2)NaHCO 溶液与Ca(OH) 溶液反应:
3 2
①NaHCO 不足: ;
3
②NaHCO 过量: 。
3
(3)Ba(OH) 溶液与NaHSO 溶液反应:
2 4
①n[Ba(OH) ]∶n(NaHSO)=1∶1,方程式为 ,此时溶液呈碱性;
2 4
②n[Ba(OH) ]∶n(NaHSO)=1∶2,方程式为 ,此时溶液呈中性,若向该溶液中
2 4
再加入Ba(OH) 溶液,反应为 。
2
(4)NH Al(SO ) 与Ba(OH) 溶液反应:
4 4 2 2
①n[NH Al(SO )]∶n[Ba(OH) ]=1∶1,方程式为 ;
4 4 2 2
②n[NH Al(SO )]∶n[Ba(OH) ]=1∶2,方程式为 。
4 4 2 2
(5)SO 与Ca(ClO)
2 2
①SO 少量:
2
②SO 过量:
2