文档内容
解密 04 离子反应
一、选择题
1.(2021·浙江宁波市期末)下列物质属于电解质且在该状态下能导电的是( )
A.熔融NaCl B.Cu C.液态HCl D.KNO
3
【答案】A
【解析】A项,熔融NaCl属于电解质且在该状态下有自由移动的离子,能导电,故A选;B项,Cu
能够导电,但属于单质,不是化合物,不属于电解质,故B不选;C项,液态HCl属于电解质且在该状态
下,没有自由移动的离子,则不导电,故C不选;D项,KNO 属于电解质且在该状态下没有自由移动的
3
离子,则不导电,故D不选;故选A。
2.(2021·大连市普兰店区第二中学高三质检)下列物质中,其水溶液能导电,但本身属于非电解质的
是( )
A.金属铁 B.SO C.酒精 D.硫酸钡晶体
2
【答案】B
【解析】A项,铁是单质,不溶于水,铁本身能导电,但不是电解质,也不是非电解质,故A错误;
B项,SO 的水溶液能导电,但SO 本身是非电解质,故B正确;C项,酒精的水溶液不能导电,酒精本身
2 2
是非电解质,故C错误;D项,硫酸钡晶体不溶于水,水溶液不导电,但硫酸钡是电解质,故D错误;故
选B。
3.(2021·浙江嘉兴市期末)下列物质属于电解质的是( )
A.CO B.HSO 溶液 C.NaSO 固体 D.C HOH(乙醇)
2 2 4 2 4 2 5
【答案】C
【解析】电解质是在水溶液里或熔融状态下能导电的化合物,非电解质是在水溶液里和熔融状态下均
不能导电的化合物。A项,CO 的水溶液虽然可以导电,但是溶液中的离子是由碳酸电离产生的,并非
2
CO 自身电离产生的,因此CO 属于非电解质,故A错误;B项,HSO 溶液是混合物,既不是电解质也不
2 2 2 4
是非电解质,故B错误;C项,NaSO 固体溶于水和熔融态均可以导电,故其是电解质,故C正确;D项,
2 4
C HOH(乙醇)在水溶液里和熔融状态下均不能导电,是非电解质,故D错误;故选C。
2 5
4.(2021·广东珠海市期末)下列说法正确的是( )
A.NaCl在熔融条件能导电
B.NaCl固体不导电,因为NaCl固体中无阴阳离子
C.NaHCO 在熔融态电离:NaHCO = Na++H++CO 2-
3 3 3
D.盐酸能导电,盐酸是电解质
【答案】A
【解析】A项,NaCl在熔融条件下能电离出自由移动的钠离子和氯离子,能导电,故A正确;B项,
NaCl固体中有钠离子和氯离子,但是不能自由移动,则NaCl固体不导电,故B错误;C项,NaHCO 在熔
3
融态电离为:NaHCO = Na++HCO-,故C错误;D项,盐酸中有自由移动的氢离子和氢氧根离子,能导电,
3 3
但盐酸是混合物,不是电解质,HCl是电解质,故D错误;故选A。
5.(2021·广东佛山市期末)下列说法正确的是( )
A.硝酸在通电的情况下,才能发生电离
B.金属钠和熔融的NaCl均能导电,其导电原理相同
C.氯气溶于水能够导电,所以氯气是电解质
D.HSO 、Ca(OH) 、AgCl均属于电解质
2 4 2
【答案】D
【解析】电解质是在水溶液或熔融状态下能导电的化合物,酸、碱、盐、金属氧化物、水等都属于电
解质,由此分析。A项,电解质的电离条件是在水溶液或熔融状态下,在通电的情况下发生的是电解,硝酸是共价化合物,在水溶液中发生电离生成氢离子和硝酸根离子,故A不符合题意;B项,金属钠中自由
电子的定向移动能导电,熔融的NaCl是自由离子的定向移动能导电,其导电原理不相同,故B不符合题
意;C项,氯气溶于水能够导电,是氯气与水反应生成了HCl和次氯酸,HCl和次氯酸是电解质;电解质
和非电解质都是化合物,而氯气是单质,既不是电解质也不是非电解质,故C不符合题意;D项,HSO
2 4
在水溶液中电离生成氢离子和硫酸根离子,Ca(OH) 在水溶液或熔融状态下电离生成钙离子和氢氧根离子,
2
AgCl在水溶液中或熔融状态下电离生成银离子和氯离子,HSO 属于酸、Ca(OH) 属于碱、AgCl属于盐,
2 4 2
均属于电解质,故D符合题意;故选D。
6.(2021·河南郑州市期末)下列厨房用品中的主要成分属于非电解质的是( )
选项 A B C D
厨房用品
主要成分 氯化钠NaCl 碳酸钠NaCO 果糖C H O 醋酸CHCOOH
2 3 6 12 6 3
【答案】C
【解析】常见电解质有酸、碱、盐、金属氧化物等化合物,如HCl、CHCOOH、NaOH、NaCl、
3
NaCO 等均属于电解质,大部分有机物为非电解质,如蔗糖、果糖、乙醇等,故选C。
2 3
7.(2021·东方市八所中学高三质检)下列叙述不正确的是( )
A.石墨有较好的导电性,不是电解质
B.CaCO 、BaSO 都难溶于水,但它们都是电解质
3 4
C.固体NaCl、固体KNO 均不能导电,所以NaCl、KNO 均是非电解质
3 3
D.酒精(即乙醇,纯净物)在水溶液和熔融状态下均不能导电,所以酒精属于非电解质
【答案】C
【解析】A项,石墨有较好的导电性,石墨为单质,不是电解质,A叙述正确;B项,CaCO 、BaSO
3 4
都难溶于水,但它们熔融状态时均能导电,都是电解质,B叙述正确;C项,固体NaCl、固体KNO 均不
3
能导电,但它们水溶液均能导电,所以NaCl、KNO 均是电解质,C叙述错误;D项,酒精(即乙醇,纯净
3
物)在水溶液和熔融状态下均不能导电,且为化合物,所以酒精属于非电解质,D叙述正确;答案选C。
8.(2021·浙江嘉兴市期末)某无色溶液由Na+、Ba2+、Al3+、AlO-、Fe3+、CO2-、SO 2-中的若干种组成。
2 3 4
取适量该溶液进行如下实验:
①加入过量盐酸,有气体生成;
②在①所得的溶液中再加入过量NH HCO 溶液,有气体生成,同时析出白色沉淀甲;
4 3
③在②所得溶液中加入过量Ba(OH) 溶液并加热,也有气体生成,并有白色沉淀乙析出。下列说法正
2
确的是( )
A.该溶液中一定含有Na+、SO 2-、CO2-
4 3
B.由①②可以得出溶液中一定含有AlO-
2
C.白色沉淀乙一定是BaSO
4
D.③中产生的气体一定是CO
2
【答案】B
【解析】该溶液为无色溶液,说明没有Fe3+;①取适量该溶液,加入过量盐酸,有气体生成,说明有
CO2-,生成CO,根据离子共存可知,溶液中没有Al3+,Ba2+;由于溶液呈电中性,必须有阳离子,所以
3 2
存在Na+;②在①所得的溶液中再加入过量NH HCO 溶液,有气体生成,HCO -与①中过量的盐酸反应生
4 3 3
成CO,同时析出白色沉淀甲,说明溶液中有AlO-,在①中AlO-与过量盐酸发生反应AlO-+4H+= Al3+
2 2 2 2+2H O,转化为Al3+,Al3+与HCO -发生双水解反应生成氢氧化铝和CO;③在②所得溶液中加入过量
2 3 2
Ba(OH) 溶液并加热,也有气体生成,并有白色沉淀乙析出,OH-与②过量的NH +在加热条件下反应生成
2 4
氨气,OH-与②过量的HCO -反应生成CO2-和水,CO2-结合钡离子生成BaCO ,则白色沉淀乙一定含有
3 3 3 3
BaCO ,可能有BaSO,不能说明一定有SO 2-。A项,该溶液中一定含有Na+、CO2-,不能确定有SO 2-,
3 4 4 3 4
故A错误;B项,由①②可以得出溶液中一定含有AlO-,故B正确;C项,白色沉淀乙一定含有BaCO ,
2 3
可能有BaSO,故C错误;D项,③中加入过量Ba(OH) 溶液,不可能生成CO,产生的气体是氨气,故
4 2 2
D错误;故选B。
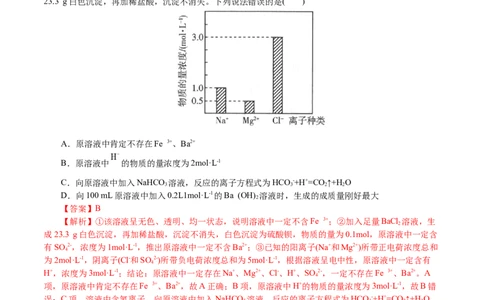
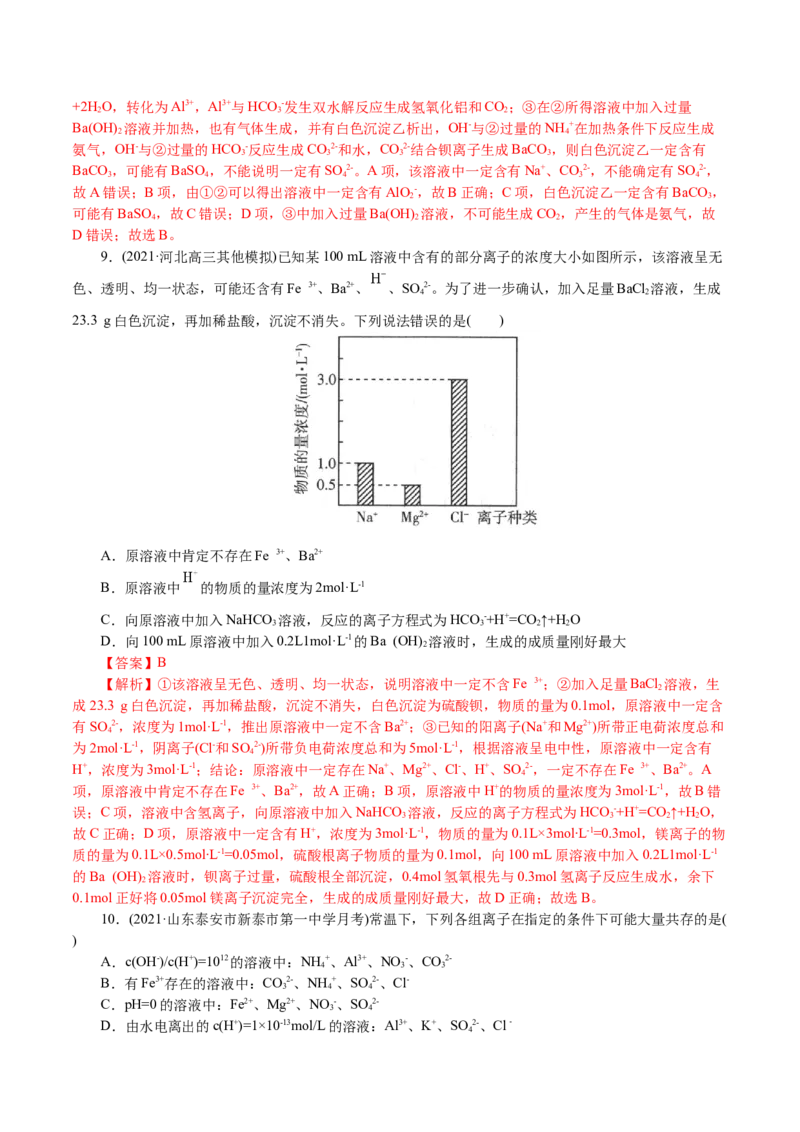
9.(2021·河北高三其他模拟)已知某100 mL溶液中含有的部分离子的浓度大小如图所示,该溶液呈无
色、透明、均一状态,可能还含有Fe 3+、Ba2+、 、SO 2-。为了进一步确认,加入足量BaCl 溶液,生成
4 2
23.3 g白色沉淀,再加稀盐酸,沉淀不消失。下列说法错误的是( )
A.原溶液中肯定不存在Fe 3+、Ba2+
B.原溶液中 的物质的量浓度为2mol·L-1
C.向原溶液中加入NaHCO 溶液,反应的离子方程式为HCO -+H+=CO ↑+H O
3 3 2 2
D.向100 mL原溶液中加入0.2L1mol·L-1的Ba (OH) 溶液时,生成的成质量刚好最大
2
【答案】B
【解析】①该溶液呈无色、透明、均一状态,说明溶液中一定不含Fe 3+;②加入足量BaCl 溶液,生
2
成23.3 g白色沉淀,再加稀盐酸,沉淀不消失,白色沉淀为硫酸钡,物质的量为0.1mol,原溶液中一定含
有SO 2-,浓度为1mol·L-1,推出原溶液中一定不含Ba2+;③已知的阳离子(Na+和Mg2+)所带正电荷浓度总和
4
为2mol·L-1,阴离子(Cl-和SO 2-)所带负电荷浓度总和为5mol·L-1,根据溶液呈电中性,原溶液中一定含有
4
H+,浓度为3mol·L-1;结论:原溶液中一定存在Na+、Mg2+、Cl-、H+、SO 2-,一定不存在Fe 3+、Ba2+。A
4
项,原溶液中肯定不存在Fe 3+、Ba2+,故A正确;B项,原溶液中H+的物质的量浓度为3mol·L-1,故B错
误;C项,溶液中含氢离子,向原溶液中加入NaHCO 溶液,反应的离子方程式为HCO -+H+=CO ↑+H O,
3 3 2 2
故C正确;D项,原溶液中一定含有H+,浓度为3mol·L-1,物质的量为0.1L×3mol∙L-1=0.3mol,镁离子的物
质的量为0.1L×0.5mol∙L-1=0.05mol,硫酸根离子物质的量为0.1mol,向100 mL原溶液中加入0.2L1mol·L-1
的Ba (OH) 溶液时,钡离子过量,硫酸根全部沉淀,0.4mol氢氧根先与0.3mol氢离子反应生成水,余下
2
0.1mol正好将0.05mol镁离子沉淀完全,生成的成质量刚好最大,故D正确;故选B。
10.(2021·山东泰安市新泰市第一中学月考)常温下,下列各组离子在指定的条件下可能大量共存的是(
)
A.c(OH-)/c(H+)=1012的溶液中:NH +、Al3+、NO -、CO2-
4 3 3
B.有Fe3+存在的溶液中:CO2-、NH +、SO 2-、Cl-
3 4 4
C.pH=0的溶液中:Fe2+、Mg2+、NO -、SO 2-
3 4
D.由水电离出的c(H+)=1×10-13mol/L的溶液:Al3+、K+、SO 2-、Cl﹣
4【答案】D
【解析】A项,OH-浓度偏高,水溶液显碱性,NH +不能大量共存,A项不符合题意;B项,Fe3+与
4
CO2-因为双水解不能大量共存,B项不符合题意;C项,pH=0是强酸性溶液,在有H+存在的情况下,
3
NO -具有强氧化性,与还原性的Fe2+不能大量共存,C项不符合题意;D项,由水电离出的氢离子浓度低
3
于10-7 mol·L-1,说明水的电离受到抑制,加酸或者加减均可抑制,所以该水溶液可能是酸性也可能是碱性,
碱性条件下,Al3+不能大量共存,酸性条件下,可以大量共存,D项符合题意;故选D。
11.(2021·四川资阳市高三一模)“过犹不及”深刻诠释了化学反应的定量关系。下列反应进行到指定程
度,继续增加画线物质的量,不会使反应发生变化的是(忽略气体溶解及与水的反应) ( )
A.在Ca(HCO ) 溶液中滴加Ca(OH) 溶液至HCO -完全反应
3 2 2 3
B.将Cl 通入FeBr 溶液至Fe2+完全氧化
2 2
C.将NH 通入CuSO 溶液至Cu2+完全沉淀
3 4
D.在KAl(SO ) 溶液中滴加Ba(OH) 溶液至沉淀物质的量最大
4 2 2
【答案】A
【解析】A项,Ca(HCO ) 溶液中滴加Ca(OH) 溶液至HCO -完全反应,反应的离子方程式为Ca2++
3 2 2 3
HCO -+OH-=CaCO ↓+H O,继续滴加Ca(OH) 溶液不再发生其他反应,即原反应不会发生变化,A符合题
3 3 2 2
意;B项,由于Fe2+的还原性比Br-强,将Cl 通入FeBr 溶液先与Fe2+反应:Cl+2Fe2+=2Cl-+2Fe3+,Fe2+完全
2 2 2
氧化后如果继续通入Cl,溶液中的Br-就会被氧化:Cl+2Br-=2Cl-+Br ,即原反应发生了变化,B不符题意;
2 2 2
C项,将NH 通入CuSO 溶液至Cu2+完全沉淀,发生反应2NH +2H O+Cu2+=Cu(OH) ↓+2NH+,若继续通入
3 4 3 2 2 4
NH ,会发生络合反应Cu(OH) +4NH=[Cu(NH)](OH) ,沉淀溶解,即原反应发生了变化,C不符题意;D
3 2 3 3 4 2
项,在KAl(SO ) 溶液中滴加Ba(OH) 溶液至沉淀物质的量最大,发生反应为2Al3++3SO2-+3Ba2++6OH-
4 2 2 4
=2Al(OH) ↓+3BaSO ↓,若继续滴加Ba(OH) 溶液,溶液中会发生反应SO 2-+2Al(OH) +Ba2++2OH-=2 AlO -
3 4 2 4 3 2
+BaSO ↓+4H O,即原反应发生了变化,D不符题意;故选A。
4 2
12.(2021·辽宁大连市·大连二十四中高三期中)下列离子方程式书写正确的是( )
A.用NaSO 溶液吸收少量Cl:3 SO2-+Cl+H O═2HSO -+2Cl﹣+ SO 2-
2 3 2 3 2 2 3 4
B.FeI 溶液中滴入过量溴水:2Fe2++2I﹣+2Br ═2Fe3++I +4Br﹣
2 2 2
C.草酸使酸性高锰酸钾溶液褪色:2 MnO- +5C O2-+16H+═2Mn2++10CO ↑+8H O
4 2 4 2 2
D.向NH HCO 溶液中滴加少量NaOH溶液:NH ++OH﹣═NH •H O
4 3 4 3 2
【答案】A
【解析】A项,用NaSO 溶液吸收少量Cl:3SO 2- +Cl +H O═2HSO ﹣+2Cl﹣+SO2-,符合得失电子守
2 3 2 3 2 2 3 4
恒、电荷守恒、元素守恒、强制弱规律,A项符合题意;B项,向FeI 溶液中滴入过量溴水,反应生成溴
2
化铁、碘单质,反应的离子方程式为:2Fe2++4I﹣+3Br ═2Fe3++2I +6Br﹣,B项不符合题意;C项,草酸是二
2 2
元弱酸,能使酸性高锰酸钾溶液褪色,草酸应该保留分子式,离子方程式为:2 MnO-
4
+5H C O+6H+═2Mn2++10CO ↑+8H O,C项不符合题意;D项,向NH HCO 中滴加少量的NaOH溶液的离
2 2 4 2 2 4 3
子反应为HCO -+OH﹣= CO2-+H O,D项不符合题意;故选A。
3 3 2
13.(2021·辽宁省实验中学东戴河分校月考)已知酸性:HCO>HClO>HCO ->Al(OH) ,氧化性:
2 3 3 3
HClO>Cl >Br >Fe3+>I 。(AlO -+H++H O=Al(OH) )下列有关离子反应或离子方程式或化学方程式的叙述中正
2 2 2 2 2 3
确的是( )
A.向含有相等物质的量的HCO -、ClO-、CO2-、AlO-溶液中,逐滴加入盐酸,反应由前到后顺序为:
3 3 2
HCO -、ClO-、CO2-、AlO-
3 3 2
B.向含有0.4molFeI 的溶液中通入0.3molCl 充分反应:4Fe2++2I-+3Cl=4Fe3++6Cl-+I
2 2 2 2
C.向NaClO溶液中通入少量二氧化碳的离子方程式:ClO-+CO +H O=HClO+HCO -
2 2 3
D.向偏铝酸钠溶液中通入少量CO 的离子方程式:AlO-+CO +H O=Al(OH) ↓+HCO-
2 2 2 2 3 3
【答案】C
【解析】A项,酸性:HCO>HClO>HCO ->Al(OH) ,则电离出氢离子的能力:HCO>HClO>HCO -
2 3 3 3 2 3 3>Al(OH) ,则结合氢离子能力:HCO -Fe3+>I ,Cl 能氧化Fe2+、I-,还原性:Fe2+HClO>HCO -,根据
2 2 2 2 2 3 3
较强酸制较弱酸原则可知向NaClO溶液中通入少量二氧化碳的离子方程式为ClO-
+CO +H O=HClO+HCO -,C正确;D项,酸性:HCO ->Al(OH) ,因此向偏铝酸钠溶液中通入少量CO 的
2 2 3 3 3 2
离子方程式为2AlO-+CO +3H O=2Al(OH) ↓+CO 2-,D错误。故选C。
2 2 2 3 3
14.(2021·大连市一〇三中学高三月考)下列各组澄清溶液中的离子能大量共存,且加入试剂后发生反
应的离子方程式书写正确的是( )
选项 离子 试剂 离子方程式
A NH +、Na+、Fe3+、S2- 少量铜粉 2Fe3++Cu=2Fe2++Cu2+
4
B NH +、Fe3+、Br-、SO 2- 过量NaS 2Fe3++S2-=2Fe2++S↓
4 4 2
C K+、Na+、ClO-、SO 2- 足量SO SO +2ClO-+H O=SO 2-+2HClO
4 2 2 2 3
D K+、Na+、CO2-、AlO- 少量HCl H++AlO -+H O=Al(OH) ↓
3 2 2 2 3
【答案】D
【解析】A项,Fe3+与S2-发生氧化还原反应,在溶液中不能大量共存,故A错误;B项,NH +、Fe3+、
4
Br-、SO 2-之间互不反应能够共存,加入过量NaS发生反应:2Fe3++3S2−=2FeS↓+S↓,故B错误;C项,
4 2
K+、Na+、ClO-、SO 2-之间互不反应能够共存,SO 过量,次氯酸根离子能够把二氧化硫氧化为硫酸根离子,
4 2
正确的离子方程式为:SO +ClO−+H O= SO 2-+Cl−+2H +,故C错误;D项,K+、Na+、CO2-、AlO-之间互不
2 2 4 3 2
反应能够共存,少量HCl与AlO-反应生成沉淀,离子方程式为:H++ AlO -+H O =Al(OH) ↓,故D正确;
2 2 2 3
故选D。
15.(2021·浙江温州市·温州中学质检)今有一混合物水溶液,只可能含有以下离子中的若干种:Na+、
Ba2+、Cl-、CO2-、SO 2-,现取200mL溶液加BaCl 溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,
3 4 2
沉淀质量为4.66g。根据上述实验,以下推断不正确的是( )
A.溶液中一定存在CO2-、SO 2-、Na+ B.溶液中c(Na+)≥0.6mol/L
3 4
C.溶液中一定没有Ba2+,可能存在Cl- D.溶液中n(SO 2-)≤0.02mol
4
【答案】D
【解析】由取200mL溶液加氯化钡溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量
为4.66g可知,溶液中存在硫酸根离子和碳酸根离子,一定不存在钡离子,由硫酸钡的质量为4.66g可得溶
液中硫酸根离子的物质的量为 =0.02mol,碳酸根离子的物质的量为 =0.04mol;
由电荷守恒可知,溶液中一定会有钠离子,综上分析可知,溶液中一定会有钠离子、硫酸根离子、碳酸根
离子,一定不存在钡离子,无法判断是否含有氯离子。A项,由分析可知,溶液中一定存在钠离子、硫酸
根离子、碳酸根离子,故A正确;B项,若溶液中不存在氯离子,由电荷守恒可知,钠离子的浓度为
=0.6mol/L,若溶液中存在氯离子,钠离子的浓度大于0.6mol/L,则溶液中
c(Na+)≥0.6mol/L,故B正确;C项,由分析可知,溶液中一定没有Ba2+,可能存在Cl-,故C正确;D项,
由分析可知,溶液中n(SO 2-)=0.02mol,故D错误;故选D。
4
16.(2021·重庆高三月考)下列离子方程式书写错误的是( )A.向明矾溶液中滴加Ba(OH) 溶液,使沉淀的物质的量最大时:2Al3++ 3 SO2-+ 3Ba2++ 6OH-=
2 4
2Al(OH) ↓+3BaSO ↓
3 4
B.向次氯酸钠溶液中通入少量二氧化碳的离子方程式:ClO-+ CO + H O =HCO-+ HClO
2 2 3
C.等物质的量MgCl 、Ba(OH) 和HCl溶液混合:Mg2++3OH-+H+ =Mg(OH) ↓+H O
2 2 2 2
D.Ca(HCO ) 溶液与澄清石灰水按溶质物质的量之比2:3混合:Ca2++ HCO -+ OH-=CaCO ↓+H O
3 2 3 3 2
【答案】C
【解析】A项,向明矾溶液中滴加Ba(OH) 溶液,以明矾的物质的量为1mol,含有2mol Al3+、3mol
2
SO 2-,Al3+恰好生成沉淀时,消耗3mol Ba(OH) ,SO 2-完全沉淀时,消耗3mol Ba(OH) ,若所加Ba(OH)
4 2 4 2 2
的物质的量大于3mol,则会有Al(OH) 溶解,因此使沉淀的物质的量最大时反应的离子方程式为:2Al3++ 3
3
SO 2-+ 3Ba2++ 6OH-= 2Al(OH) ↓+3BaSO ↓,故A正确;B项,因酸性:HCO>HClO> HCO -,则向次氯酸
4 3 4 2 3 3
钠溶液中通入少量二氧化碳的离子方程式:ClO-+ CO + H O = HCO -+ HClO,故B正确;C项,等物质的
2 2 3
量MgCl 、Ba(OH) 和HCl溶液混合时,H+先与OH-反应,剩余一半的OH-与Mg2+反应,因此反应离子方程
2 2
式为2H++4OH-+Mg2+=Mg(OH) ↓+2H O,故C错误;D项,Ca(HCO ) 溶液与澄清石灰水按溶质物质的量之
2 2 3 2
比2:3混合,OH-过量,则HCO -全部与OH-反应生成CO2-,CO2-再与Ca2+恰好反应生成CaCO ,反应离
3 3 3 3
子方程式为Ca2++ HCO -+ OH-=CaCO ↓+H O,故D正确;故选C。
3 3 2
17.(2021·商丘市第一高级中学月考)下列各组离子或分子能大量共存,当加入相应试剂后会发生化学
变化,且发生反应的离子方程式书写正确的是( )
选项 离子组 加入试剂 加入试剂后发生反应的离子方程式
2NH ++SO 2-+Ba2++2OH-=2NH·H O+
A NH +、Fe2+、SO 2- 少量Ba(OH) 溶液 4 4 3 2
4 4 2 BaSO↓
4
Mg2++2 HCO-+4OH-=2H O+Mg(OH) ↓+
B Mg2+、Cl-、HCO - 过量NaOH溶液 3 2 2
3 2CO2-
3
C K+、CO2-、NH ·H O 通入少量CO 2OH-+CO=CO 2-+HO
3 3 2 2 2 3 2
D Fe2+、Cl-、HSO - NaHSO 溶液 SO 2-+2H+=SO↑+HO
3 4 3 2 2
【答案】B
【解析】A项,含NH +、Fe2+、SO 2-溶液中加入少量Ba(OH) 溶液,由于Fe2+结合OH-的能力比
4 4 2
NH +强,故离子方程式为:Fe2++SO 2-+Ba2++2OH-=Fe(OH) ↓+BaSO↓,A不合题意;B项,含Mg2+、
4 4 2 4
Cl-、HCO -溶液中过量NaOH溶液,由于Mg(OH) 比MgCO 更难溶,故离子方程式为:Mg2++2 HCO-+
3 2 3 3
4OH-=2H O+Mg(OH) ↓+2CO2-,B符合题意;C项,含K+、CO2-、NH ·H O溶液中通入少量CO,只
2 2 3 3 3 2 2
与一水合氨反应,正确的离子反应为:2NH •H O+CO═CO 2-+2NH++H O,C不合题意;D项,含Fe2+、
3 2 2 3 4 2
Cl-、HSO -溶液中加入NaHSO 溶液,NO -在酸性条件下具有强氧化性,与HSO -发生氧化还原反应,酸性
3 4 3 3
溶液中NO -将HSO -氧化为SO 2-,D不合题意;故选B。
3 3 4
18.(2021·河北衡水市衡水中学高三质检)下列A~D四组反应中,其中I和II可用同一个离子方程式
表示的是( )
I II
A 把金属铁放入稀硫酸中 把金属铁放入稀硝酸中
B 将0.1molCl 通入含0.3molFeBr 的溶液 将0.3molCl 通入含0.1 molFeBr 的溶液
2 2 2 2
C Ca(HCO ) 溶液中加入足量的NaOH溶液 Ca(OH) 溶液中加入足量的NaHCO 溶液
3 2 2 3
D NaHSO 溶液Ba(OH) 溶液反应恰好呈中性 NaHSO 溶液Ba(OH) 溶液反应使 恰好沉淀
4 2 4 2【答案】C
【解析】A项,铁和稀硫酸发生置换反应:Fe+2H+=Fe2++H ↑,铁和稀硝酸反应生成硝酸铁、NO和水:
2
Fe+4H++NO-=Fe3++NO↑+2HO,故A不选;B项,将0.1molCl 通入含0.3molFeBr 的溶液中,由于氯气少
3 2 2 2
量,所以只能氧化Fe2+,离子方程式为:Cl+2Fe2+=2Fe3++2Cl-;将0.3molCl 通入含0.1molFeBr 的溶液中,
2 2 2
由于氯气过量,Fe2+和Br-均被氧化,离子方程式为:3Cl+2Fe2++4Br-=6Cl-+2Fe3++2Br ,故B不选;C项,
2 2
Ca(HCO ) 溶液中加入足量的NaOH溶液和Ca(OH) 溶液中加入足量的NaHCO 溶液,离子方程式均为:
3 2 2 3
Ca2++2HCO-+2OH-=CaCO ↓+ CO2-+2H O,故C选;D项,NaHSO 溶液Ba(OH) 溶液反应恰好呈中性,
3 3 3 2 4 2
NaHSO 和Ba(OH) 的物质的量之比为2:1,离子方程式为:2H+ SO 2-+2OH-+Ba2+=2H O+BaSO↓;NaHSO
4 2 4 2 4 4
溶液Ba(OH) 溶液反应使 SO 2- 恰好沉淀,NaHSO 和Ba(OH) 的物质的量之比为1:1,离子方程式为:H+
2 4 4 2
+OH-+ SO 2-+Ba2+=H O+BaSO↓,故D不选;故选C。
4 2 4
19.关于微粒在指定溶液中能否大量共存的评价正确的是( )
选项 溶液 微粒 评价
A 8% H O 水溶液 Fe3+、Mg2+、SO、Na+ 可以大量共存
2 2
NO能将SO氧化而不能大
B 室温下pH=12的水溶液 NO、Na+、SO、K+
量共存
NH Cl溶液显酸性,
C 1 mol·L-1的NH Cl溶液 Ba2+、OH-、NH ·H O 4
4 3 2 NH ·H O不能大量共存
3 2
CHCOO-能与
3
D NaHSO 水溶液 I-、K+、CHCOO-、Br- NaHSO 溶液反应,不能
4 3 4
大量共存
【答案】D
【解析】Fe3+对HO 的分解有催化作用,A错;NO只有在酸性条件下才有强氧化性,B项中的评价
2 2
错误;C项中OH-不能大量共存,原因是NH+OH-===NH·H O,C项中的评价错误;NaHSO 能完全电
3 2 4
离生成H+,故能发生反应CHCOO-+H+===CH COOH,D项正确。
3 3
20.(2021·浙江省杭州第二中学高三模拟)某溶液可能含有下列离子的某几种:Cl-、I-、SO 2-、CO2-、
4 3
Na+、NH +、Fe3+、Fe2+和Ba2+,且所含离子的浓度均相等。某同学为了确认其成分,取部分试液,设计并
4
完成了如下实验:由此可知,下列说法正确的是( )
A.原溶液中Fe3+和Fe2+可能都存在
B.溶液中至少有4种离子存在,其中Cl-一定存在,且c(Cl-)=0.2mol/L
C.SO 2-、NH +、Fe2+一定存在,CO2-、Ba2+一定不存在
4 4 3
D.若要进一步确定原溶液中是否含有Fe2+,其操作为:取少量原溶液于试管中,加入足量酸性高锰
酸钾溶液,若溶液紫红色褪去,则证明原溶液中有Fe2+
【答案】 C
【解析】加入过量NaOH溶液,加热,得到无色气体,根据所给离子可知该气体为氨气,原溶液中一
定存在NH +;沉淀灼烧得到红棕色固体为三氧化二铁,则原溶液中含有铁元素,可能为Fe3+或Fe2+,则原
4
溶液中一定没有CO2-;滤液中加入足量氯化钡溶液和盐酸溶液过滤得到4.66g沉淀为硫酸钡沉淀,硫酸钡
3的物质的量 =0.02mol,原溶液中含有0.02mol SO 2-,溶液体积为100mL,所以
4
c(SO 2-)=0.2mol/L,因为有硫酸根则一定不含Ba2+;溶液所含离子的浓度均相等,则含有0.2mol/LNH +,若
4 4
另外的阳离子为0.2mol/L的Fe3+,根据电荷守恒以及所提供的离子可知还需要0.2mol/L的Cl-和0.2mol/L的
I-,但碘离子和铁离子不共存,所以铁元素以Fe2+的形式存在,浓度为0.2mol/L,根据电荷守恒可知还应含
有0.2mol/L带一个负电荷的阴离子,可以是Cl-或I-;焰色试验是要检验钠离子,但由于加入了氢氧化钠溶
液,无法判断原溶液中是否含有钠离子,当钠离子存在时,则一定还会再多一种阴离子。A项,根据分析
可知溶液中存在Fe2+,不存在Fe3+,故A错误;B项,根据分析溶液中一定存在SO 2-、NH +、Fe2+,不一
4 4
定存在氯离子,故B错误;C项,根据分析溶液中一定存在SO 2-、NH +、Fe2+,CO2-、Ba2+一定不存在,
4 4 3
故C正确;D项,不需要进一步确认是否含有Fe2+,故D错误;故选C。
21.(2021·浙江高三期末)某溶液只可能含有下列离子中的若干种(不考虑水的电离及离子的水解),
Na+、K+、Cu2+、Al3+、Fe2+、Cl﹣、CO2-、NO -、SO 2-,且各种离子的物质的量浓度相等.化学兴趣小组同学
3 3 4
欲探究该溶液的组成,进行了如下2个实验:
①取溶液加入足量稀盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且
溶液中阴离子种类不变。
②另取溶液加入BaCl 溶液,有白色沉淀生成。
2
根据上述实验,以下推测正确的是( )
A.步骤②的白色沉淀可能为BaSO 和BaCO
4 3
B.若该溶液焰色反应呈紫色,则该溶液一定有6种离子组成
C.步骤①中可以确定Fe2+、NO -的存在,不能确定其它离子的存在
3
D.溶液中难以确定Al3+的存在与否
【答案】D
【解析】取溶液加入足量稀盐酸,有无色气体生成,该无色气体遇空气变成红棕色,说明含有具有氧
化性的NO -和具有还原性的Fe2+,另取溶液加入BaCl 溶液,有白色沉淀生成,说明原溶液中可能含有
3 2
CO2-或SO 2-,但原溶液中已经确定含有Fe2+,则不可能含有CO2-;故溶液中含有Fe2+、NO -和SO 2-,已
3 4 3 3 4
知各种离子的物质的量浓度相等,阴离子电荷比阳离子电荷多,所以还含有另外的阳离子。A项,溶液中
含有Fe2+,则不能含有CO2-,故不能含有BaCO ,A错误;B项,若该溶液焰色反应呈紫色,说明含有
3 3
K+,上述分析中有Fe2+、NO -和SO 2-,根据电荷守恒可以,4种离子已经达到电荷守恒,故只含有4种离
3 4
子,B错误;C项,步骤①中可以确定Fe2+、NO -的存在,含有Fe2+的溶液不可能含有CO2-,故步骤①可
3 3
以确定其他一些离子,C错误;D项,根据B项的分析,Al3+是否存在取决于阴离子中是否含有Cl-,而题
目中没有信息证明Cl-的存在,故难以确定Al3+的存在与否,D正确;故选D。
22.(2021·浙江衢州市高三月考)有一固体混合物,可能由KCO、NaNO 、FeCl 、KClO、AgNO 混
2 3 2 3 3 3
合而成,为检验它的成分做了如下实验:取固体加入足量的稀硝酸中,搅拌充分反应,得到无色透明溶液,
同时有黄绿色气体和白色沉淀生成(已知NaNO 不能被稀硝酸氧化)。以下判断正确的是( )
2
A.一定含有KClO、NaNO 、AgNO,不能确定是否含有FeCl
3 2 3 3
B.一定含有KClO,且在反应过程中可能被还原生成了两种还原产物
3
C.另取适量固体加水溶解,若出现白色沉淀,即可证明KCO 的存在
2 3
D.将反应产生的所有气体通入少量澄清石灰水,若未变浑浊,可证明KCO 不存在
2 3
【答案】B
【解析】已知NaNO 不能被稀硝酸氧化,所以只能是KClO 将NaNO 氧化,本身被还原为Cl,白色
2 3 2 2
沉淀为不溶于稀硝酸的AgCl,所以Cl-是KClO 被还原的另一产物,固体混合物中还应含有AgNO;因为
3 3
反应后得到无色溶液,所以不含有FeCl 。A项,由以上分析可知,固体混合物中一定含有KClO、
3 3
NaNO 、AgNO,一定不含有FeCl ,A不正确;B项,分析结果显示,固体混合物中一定含有KClO,且
2 3 3 3在反应过程中被还原为Cl、KCl两种还原产物,B正确;C项,另取适量固体加水溶解,因为KClO 被
2 3
NaNO 还原为Cl-,所以即便出现白色沉淀,也不能证明KCO 的存在,C不正确;D项,将反应产生的所
2 2 3
有气体通入少量澄清石灰水,因为Cl 与水反应生成的HCl能中和澄清石灰水中的Ca(OH) ,所以即便存在
2 2
KCO,也不产生浑浊现象,无法证明KCO 是否存在,D不正确;故选B。
2 3 2 3
23.(2021·广东茂名市高三月考)混合体系中,确认化学反应的先后顺序有利于问题的解决,下列反应
先后顺序判断正确的是( )
A.等物质的量的Fe3+、Cu2+、H+的溶液中加入Fe:Fe3+、H+、Cu2+
B.等物质的量的Ca(OH) 、NaOH的溶液中通入CO:Ca(OH) 、NaOH、CaCO 、NaCO
2 2 2 3 2 3
C.等物质的量的FeBr 、FeI 的溶液中缓慢通入Cl:Fe2+、I-、Br-
2 2 2
D.等物质的量的Al3+、H+、NH +溶液中,逐滴加入NaOH溶液:H+、Al3+、NH +、Al(OH)
4 4 3
【答案】D
【解析】A项,离子的氧化性顺序是:Fe3+>Cu2+>H+,在含等物质的量的Fe3+、Cu2+、H+的溶液中加
入Fe,Fe先和氧化性强的离子发生反应,则反应先后顺序为Fe3+、Cu2+、H+,故A错误;B项,在含等
物质的量的Ca(OH) 、NaOH的溶液中通入CO,CO 先是和Ca(OH) 发生反应生成碳酸钙沉淀和水,其次
2 2 2 2
是氢氧化钠,再是和碳酸钠之间发生反应,最后和碳酸钙发生反应,故B错误;C项,离子的还原性顺序
为I->Fe2+>Br-,在含等物质的量的FeBr 、FeI 的溶液中缓慢通入Cl,氯气具有氧化性,先和还原性强的
2 2 2
离子反应,反应先后顺序为I-、Fe2+、Br-,故C错误;D项,含等物质的量的Al3+、H+、NH +溶液中,
4
逐滴加入NaOH溶液,OH-先和H+反应生成水,再和Al3+反应生成Al(OH) 沉淀,然后和NH +反应生成一
3 4
水合氨,最后和Al(OH) 反应生成偏铝酸根离子和水,反应的先后顺序为H+、Al3+、NH +、Al(OH) ,故D
3 4 3
正确;故选D 。
24.(2021·四川省广汉中学高三月考)已知电离常数:HCNKa=5×10-10,HCOKa=4.3×10-7,
2 3 1
Ka=5.6×10-11。下列有关离子方程式的书写正确的是( )
2
A.向NaH PO (aq)中滴入少量的Ba(OH) (aq):3Ba2++6OH—+3H PO -= Ba (PO )↓+PO3-+6H O
2 4 2 2 4 3 4 2 4 2
B.在含有1mol明矾[KAl(SO)•12H O]的水溶液中,加入1mol的Ba(OH) :2Al3++3SO2-+3Ba2++6OH-
4 2 2 2 4
=2Al(OH) ↓+3BaSO ↓
3 4
C.向浓度为1.25mol/L的NaOH(aq) 1 L中通入22.4 L(标准状况测定)的CO 气体:2OH-+ CO = CO2-
2 2 3
+ H O
2
D.向KCN(aq)中通入少量的CO 气体:CO+H O+2CN-= 2HCN+CO 2-
2 2 2 3
【答案】B
【解析】A项,磷酸二氢钠溶液与少量氢氧化钡溶液反应生成磷酸氢钡、磷酸氢钠和水,反应的离子
方程式为Ba2++2OH—+2H PO -= BaHPO ↓+ HPO 2-+H O,故A错误;B项,溶液中1mol KAl(SO ) 与1mol
2 4 4 4 2 4 2
Ba(OH) 反应生成 mol Al(OH) 和1molBaSO ↓,反应的离子方程式为2Al3++3SO2-+3Ba2++6OH-
2 3 4 4
=2Al(OH) ↓+3BaSO ↓,故B正确;C项,溶液中1.25mol氢氧化钠与1mol二氧化碳反应生成0.25mol碳酸
3 4
钠和0.75mol碳酸氢钠,反应的离子方程式为5OH-+4CO = CO2-+3HCO-+H O,故C错误;D项,由电离
2 3 3 2
常数可知,电离程度为HCO>HCN>HCO -,则氰化钾溶液中通入与少量二氧化碳气体反应生成氢氰酸
2 3 3
和碳酸氢钠,反应的离子方程式为CO+H O+CN-= HCN+ HCO -,故D错误;故选B。
2 2 3
25.(2021·浙江选考模拟)某化学实验室产生的废液中的阳离子只可能含有 Na+、NH +、Ba2+、Cu2+、
4
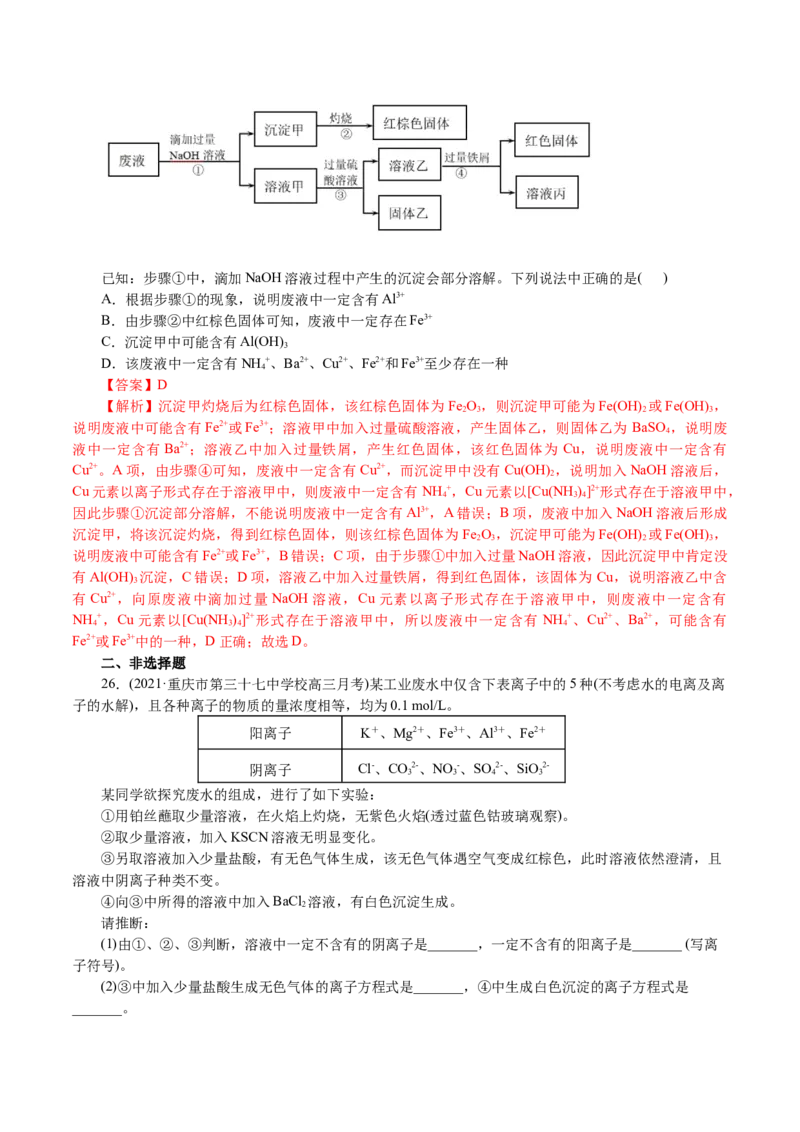
Al3+、Fe2+、Fe3+中的某几种,实验室设计了下述方案对废液进行处理,以回收金属,保护环境。已知:步骤①中,滴加NaOH溶液过程中产生的沉淀会部分溶解。下列说法中正确的是( )
A.根据步骤①的现象,说明废液中一定含有Al3+
B.由步骤②中红棕色固体可知,废液中一定存在Fe3+
C.沉淀甲中可能含有Al(OH)
3
D.该废液中一定含有NH +、Ba2+、Cu2+、Fe2+和Fe3+至少存在一种
4
【答案】D
【解析】沉淀甲灼烧后为红棕色固体,该红棕色固体为 Fe O ,则沉淀甲可能为Fe(OH) 或Fe(OH) ,
2 3 2 3
说明废液中可能含有Fe2+或Fe3+;溶液甲中加入过量硫酸溶液,产生固体乙,则固体乙为 BaSO ,说明废
4
液中一定含有Ba2+;溶液乙中加入过量铁屑,产生红色固体,该红色固体为 Cu,说明废液中一定含有
Cu2+。A项,由步骤④可知,废液中一定含有Cu2+,而沉淀甲中没有Cu(OH) ,说明加入NaOH溶液后,
2
Cu元素以离子形式存在于溶液甲中,则废液中一定含有 NH +,Cu元素以[Cu(NH )]2+形式存在于溶液甲中,
4 3 4
因此步骤①沉淀部分溶解,不能说明废液中一定含有Al3+,A错误;B项,废液中加入NaOH溶液后形成
沉淀甲,将该沉淀灼烧,得到红棕色固体,则该红棕色固体为 Fe O ,沉淀甲可能为Fe(OH) 或Fe(OH) ,
2 3 2 3
说明废液中可能含有Fe2+或Fe3+,B错误;C项,由于步骤①中加入过量NaOH溶液,因此沉淀甲中肯定没
有Al(OH) 沉淀,C错误;D项,溶液乙中加入过量铁屑,得到红色固体,该固体为 Cu,说明溶液乙中含
3
有Cu2+,向原废液中滴加过量 NaOH溶液,Cu元素以离子形式存在于溶液甲中,则废液中一定含有
NH +,Cu元素以[Cu(NH )]2+形式存在于溶液甲中,所以废液中一定含有 NH +、Cu2+、Ba2+,可能含有
4 3 4 4
Fe2+或Fe3+中的一种,D正确;故选D。
二、非选择题
26.(2021·重庆市第三十七中学校高三月考)某工业废水中仅含下表离子中的5种(不考虑水的电离及离
子的水解),且各种离子的物质的量浓度相等,均为0.1 mol/L。
阳离子 K+、Mg2+、Fe3+、Al3+、Fe2+
阴离子 Cl-、CO2-、NO -、SO 2-、SiO2-
3 3 4 3
某同学欲探究废水的组成,进行了如下实验:
①用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
②取少量溶液,加入KSCN溶液无明显变化。
③另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且
溶液中阴离子种类不变。
④向③中所得的溶液中加入BaCl 溶液,有白色沉淀生成。
2
请推断:
(1)由①、②、③判断,溶液中一定不含有的阴离子是_______,一定不含有的阳离子是_______ (写离
子符号)。
(2)③中加入少量盐酸生成无色气体的离子方程式是_______,④中生成白色沉淀的离子方程式是
_______。(3)该同学最终确定原溶液中所含阴离子是_______,阳离子是_______ (写离子符号)。
(4)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体
质量为_______ g。
【答案】(1)CO 2-、SiO2- K+、Fe3+
3 3
(2)3Fe2++NO -+4H+=3Fe3++NO↑+2HO Ba2++SO 2-=BaSO ↓
3 2 4 4
(3)Cl-、NO -、SO 2- Fe2+、Mg2+ (4)1.2g
3 4
【解析】用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察),说明没有K+。②
取少量溶液,加入KSCN溶液无明显变化,说明没有Fe3+。③另取溶液加入少量盐酸,有无色气体生成,
该无色气体遇空气变成红棕色,说明溶液中有NO -,能把其还原的只有Fe2+,此时溶液依然澄清,且溶液
3
中阴离子种类不变,说明没有CO2-和SiO2-。④向③中所得的溶液中加入BaCl 溶液,有白色沉淀生成,
3 3 2
说明一定有SO 2-。(1)由①、②、③判断,溶液中一定不含有的阳离子是K+、Fe3+,一定不含的阴离子是
4
CO2-和SiO2-。(2)③中加入少量盐酸生成无色气体的的离子方程式是3Fe2++NO -+4H+=3Fe3++NO↑+
3 3 3
2HO,④中生成白色沉淀的离子方程式是Ba2++SO 2-=BaSO ↓。(3)根据工业废水中仅含表中离子中的5种,
2 4 4
最终确定原溶液中所含阴离子是Cl-、NO -、SO 2-,阳离子是Fe2+、Mg2+。(4)原溶液中所含阳离子是Fe2+、
3 4
Mg2+,若向原溶液中加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体是MgO,
Fe O,根据题意各离子的物质的量均为0.01mol,所以m(MgO)=0.01mol×40g/mol=0.4g,m(Fe O)=
2 3 2 3
0.005mol×160g/mol=0.8g,所得固体的质量为0.4g+0.8g=1.2g。
27.(2021·辽宁朝阳市高三期中)某固体样品中含有的离子由Na+、Ca2+、Ba2+、NH 、Cl-、CO2-、
3
SO 2-中的若干种组成,取适量该固体进行如下实验:
4
实验中气体均全部逸出,回答下列问题:
(1)固体E中所含物质的化学式为_________。
(2)可用_________检验气体C,现象是_________。
(3)1.97gBaCO 在空气中高温充分灼烧得到1.69g固体,经检验没有产生有毒气体,写出高温灼烧时发
3
生反应的化学方程式_________。
(4)100mL无色溶液A中c(CO2-)=_________。
3
(5)当m>_________时,100mL无色溶液A中会含有Cl-,此时c(Cl-)=_________(用含m的代数式表
示)。
【答案】(1)CaO (2) 湿润的红色石蕊试纸 湿润的红色石蕊试纸变蓝
(3)BaCO BaO+CO↑、2BaO+O 2BaO 或2BaCO +O 2BaO+2CO
3 2 2 2 3 2 2 2
(4)0.1mol·L-1 (5)3.38【解析】固体加水溶解后得到沉淀A和无色溶液A,无色溶液A中加入过量的氯化钡溶液得到沉淀
B,沉淀B中加入稀盐酸后部分溶解,说明沉淀B为硫酸钡和碳酸钡,且n(BaSO)= =0.01mol,
4
n(BaCO)= =0.01mol;溶液B中加入足量NaOH溶液并加热后产生气体,则该气体应为NH ,
3 3
原溶液中应含有铵根,且n(NH )= =0.02mol;沉淀A经高温灼烧后会分解,应为碳酸盐沉淀,
根据题目所给离子可知推测若为碳酸钙,则n(CaCO)=0.01mol,高温分解后生成0.1molCaO,质量恰好为
3
0.56g,故沉淀A为碳酸钙符合题意。综上所述原固体样品中含有n(SO 2-)=0.01mol,
4
n(CO2-)=0.01mol+0.01mol=0.02mol,n(Ca2+)=0.01mol,n(NH +)=0.02mol,根据溶液显电中性可知,溶液还
3 4
应含有Na+,且其物质的量至少为0.02mol。(1)根据分析可知固体E为CaO;(2)气体C为NH ,可用湿润
3
的红色石蕊试纸检测,氨气为碱性气体,可用使湿润的红色石蕊试纸变蓝;(3)1.97gBaCO 的物质的量为
3
0.01mol,充分灼烧得到1.69g固体,恰好为0.01molBaO 的质量,没有产生有毒气体,根据元素守恒可知
2
应产生CO,再结合元素守恒可知化学方程式为BaCO BaO+CO↑、2BaO+O 2BaO 或2BaCO
2 3 2 2 2 3
+O 2BaO+2CO;(4)根据分析可知无色溶液A与过量氯化钡反应后生成0.01mol BaCO,所以
2 2 2 3
100mL无色溶液A中c(CO2-)= =0.1mol/L;(5)若样品中只含有:n(SO 2-)=0.01mol,
3 4
n(CO2-)=0.02mol,n(Ca2+)=0.01mol,n(NH +)=0.02mol,n(Na+)=0.02mol,此时固体的质量为
3 4
0.96g+1.2g+0.4g+0.36g+0.46g=3.38g,若固体的质量大于3.38g,说明除前述离子外,还含有氯化钠,即含
有Cl-,且c(Cl-)= = 。
28.(2021·四川遂宁市期末)某无色透明溶液中可能含有大量的K+、Ba2+、Cu2+、Mg2+、SO 2-、Cl-、
4
OH-、HCO -中的多种离子。对此混合溶液进行以下分析。
3
①取250 mL该混合溶液,加入过量盐酸,收集到标准状况下气体5.6 L;
②在操作①后的溶液中加入过量的NaOH溶液,过滤、洗涤、干燥得到白色沉淀5.8 g;
③在操作②后的溶液中加入过量的BaCl 溶液,过滤、洗涤、干燥得到白色沉淀23.3 g;
2
④在操作③后的溶液中加入过量的稀硝酸酸化的硝酸银溶液,产生大量的白色沉淀。
回答下列问题:
(1)不做实验就可确定一定不含有的离子是______。
(2)通过实验①确定一定不含有的离子是_______;通过实验②确定一定含有的离子是______;通过实
验③确定一定含有的离子是_______。
(3)写出操作②涉及的化学反应的离子方程式______ 。
(4)通过上述实验分析不能确定是否存在的离子是______;K+的物质的量浓度至少为______。
(5)在操作③的过程中判断加入的BaCl 溶液过量的操作是___________。
2
【答案】(1)Cu2+ (2)OH- Mg2+ SO 2-
4
(3)H++OH-=H O、Mg2++2OH-=Mg(OH) ↓
2 2
(4)Cl- 1.0 mol/L(5)静置片刻,取上层清液少许于另一支洁净试管,向其中继续滴加BaCl 溶液,若无白色沉淀生成,
2
说明SO 2-沉淀完全,证明BaCl 溶液过量(合理答案均可以给分)
4 2
【解析】Cu2+水溶液显蓝色,在无色透明溶液中不可能大量存在。①取250 mL该混合溶液,加入过量
盐酸,收集到标准状况下气体5.6 L,则说明溶液中含有HCO -,产生的气体为CO,根据C元素守恒可知:
3 2
n(HCO -)= =0.25 mol;由于HCO -与OH-会发生反应,因此溶液中移动不含有OH-;②在操作①
3 3
后的溶液中加入过量的NaOH溶液,过滤、洗涤、干燥得到白色沉淀5.8 g,说明含有Mg2+,沉淀为
Mg(OH) ,根据Mg元素守恒可知n(Mg2+)= =0.1 mol;③在操作②后的溶液中加入过量的BaCl 溶
2 2
液,过滤、洗涤、干燥得到白色沉淀23.3 g,说明含有SO 2-,沉淀为BaSO,根据S元素守恒可知n(
4 4
)= =0.1 mol;由于Ba2+与SO 2-会发生反应产生BaSO 而不能大量共存,说明溶液中一定不含有
4 4
Ba2+;④在操作③后的溶液中加入过量的稀硝酸酸化的硝酸银溶液,产生大量的白色沉淀,该沉淀为
AgCl,由于在①③中引入了Cl-,因此不能确定原溶液中是否含有Cl-。根据上述分析可知:溶液中一定含
有Mg2+、SO 2-、HCO -,一定不含有Cu2+、OH-、Ba2+,Cl-不能确定是否存在,根据电荷守恒计算K+是否
4 3
存在。(1)由于Cu2+水溶液显蓝色,在无色透明溶液中不可能大量存在,因此不做实验就可确定一定不含有
的离子是Cu2+;(2)通过实验①确定一定含有HCO -,由于HCO -与OH-会发生反应产生CO2-、HO,而不
3 3 3 2
能大量共存,因此通过实验①可确定该溶液中不含有的离子是OH-;通过实验②确定一定含有的离子是
Mg2+;通过实验③确定一定含有的离子是SO 2-;(3)在操作②中,加入的NaOH溶液电离产生OH-首先与盐
4
酸电离产生的H+结合形成HO,然后与溶液中的Mg2+反应产生Mg(OH) 沉淀,反应的离子方程式为:H+
2 2
+OH-=H O、Mg2++2OH-=Mg(OH) ↓;(4)由于在实验①、③使用的是氯化物,引入了Cl-,所以在操作④检
2 2
验出的Cl-可能是加入的HCl、BaCl 电离产生,也可能包括原溶液本身就含有的,因此通过上述实验分析
2
不能确定是否存在的离子是Cl-;根据上述实验,可知:n(Mg2+)=0.1 mol,n(HCO -)=0.25 mol,
3
n(SO 2-)=0.1 mol,阴离子浓度大于阳离子浓度,根据电荷守恒,溶液中还一定含有阳离子,由于Ba2+、
4
Cu2+一定不存在,则一定含有K+,若溶液中无Cl-,其值最小,n(K+)=0.1 mol×2+0.25 mol-0.1 mol×2=0.25
mol,由于溶液体积是0.25 L,则K+浓度最小值c(K+)= =1.0 mol/L;(5)若加入的BaCl 溶液过量,
2
说明溶液中无SO 2-,再加入BaCl 溶液时不会产生白色沉淀。故在操作③的过程中判断加入的BaCl 溶液
4 2 2
过量的操作是:静置片刻,取上层清液少许于另一支洁净试管,向其中继续滴加BaCl 溶液,若无白色沉
2
淀生成,说明SO 2-沉淀完全,证明BaCl 溶液过量。
4 2
29.(2021·山东威海市高三检测)某学习小组欲检测一失去标签的试剂瓶中固体物质的成分,将固体溶
于水,形成的溶液中含有Na+、NH +、Mg2+、Fe2+、SO 2-、MnO -、CO2-、SO 2-中的若干种,取一定量待测
4 3 4 3 4
液进行如下实验:
回答下列问题:
(1)该待测液中一定含有的离子是________;无法确定是否含有的离子是_______;(2)沉淀B的成分及物质的量为___________________(物质写化学式)。
(3)生成无色气体X时的离子方程式为________________。
(4)生成沉淀C时的离子反应方程式为________________。
(5)在催化剂、加热条件下气体X与气体Y可以反应转化为对环境无害的物质,该反应的化学方程式为
__________,所得氧化产物与还原产物的质量之比为_________。
【答案】(1)NH +、Fe2+、Mg2+、SO 2- 无 (2) 0.3mol Fe(OH) 、0.1mol Mg(OH)
4 4 3 2
(3)3Fe2++NO-+4H+=2H O+3Fe3++NO↑ (4)Ba2++CO +2OH-= BaCO↓ + H O
3 2 2 3 2
(5)4NH +6NO 5N+6H O 2∶3
3 2 2
【解析】待测液中加入过量的稀盐酸,无明显现象,溶液中一定没有SO 2-、CO2-,加入过量的硝酸钡
3 3
溶液,生成标准状况下2.24L的无色气体X,则溶液中含有Fe2+,发生的化学方程式是3Fe2++NO-
3
+4H+=2H O+3Fe3++NO↑ ,生成的一氧化氮的物质的量是0.1mol,则的物质的量是0.3mol,高锰酸根离子
2
具有氧化性,与亚铁离子不能共存,则溶液中不含有MnO -,一定含有SO 2-,SO 2-的物质的量是
4 4 4
=0.5mol,向滤液I中加入过量的氢氧化钠溶液,生成无色气体,则溶液中一定含有NH +,
4
NH +的物质的量是 =0.2mol,滤液I中含有铁离子,根据原子守恒生成氢氧化铁的质量是
4
0.3mol×107g/mol=32.1g,而沉淀B是37.9g,则有5.8g的氢氧化镁,其物质的量是 =0.1mol,则
溶液中一定含有0.1mol的Mg2+,依据电荷守恒:n (Na+)+ n (Mg2+)+n (Fe2+)+ n (NH +)= n (SO 2-),把数
4 4
据代入得,n (Na+)=0,则溶液中不含有钠离子。(1)有分析可知:待测液中一定含有的离子是NH +、Fe2+、
4
Mg2+、SO 2-,无法确定是否含有的离子无;(2) 有分析可知沉淀B的成分及物质的量为0.3mol Fe(OH) 、
4 3
0.1mol Mg(OH) ;(3) 生成无色气体X时的离子方程式为3Fe2++NO-+4H+=2H O+3Fe3++NO↑;(4) 滤液II中
2 3 2
含有钡离子、氢氧根离子,通入少量二氧化碳,生成沉淀C是碳酸钡,反应的离子方程式为Ba2++CO
2
+2OH-= BaCO↓ + H O;(5)一氧化氮和氨气反应生成氮气和水,化学方程式是4NH +6NO
3 2 3
5N+6H O;有方程式可知,4mol氨气被氧化生成2mol氮气,6mol一氧化氮被还原生成3mol氮气,则所
2 2
得氧化产物与还原产物的质量之比为2:3.
30.(2021·陕西西安市长安一中高三月考)环境问题是广大群众关注的热点话题之一,化工厂排放的废
水、废渣一般利用化学原理可以进行排放物达标检测与无害化处理。某皮革厂对制革工业污泥中Cr(Ⅲ)的
处理工艺流程如下:
已知:①酸浸后的溶液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:阳离子 Fe3+ Mg2+ Al3+ Cr3+
沉淀完全时的pH 3.7 11.1 5.4 9
沉淀溶解时的pH — — >8溶解 >9溶解
(1)如需配制480 mL酸浸环节所需的硫酸,需要用量筒量取18.4 mol·L-1的浓硫酸___________mL;配
制时所用玻璃仪器除量筒、烧杯和玻璃棒外,还需哪些仪器___________
(2)经氧化环节滤液Ⅰ中的Cr3+转化为Cr O2-,写出此反应的离子方程式:___________
2 7
(3)调pH=8环节,既可以将溶液中某些杂质离子转化为沉淀,同时又可以将Cr O2-转化为某种含铬元
2 7
素微粒,溶液颜色由橙色变为黄色,请结合离子反应方程式解释该颜色变化的原因___________
(4)钠离子交换树脂的反应原理为Mn++nNaR MR +nNa+,则利用钠离子交换树脂可除去滤液
n
Ⅱ中的金属阳离子有___________
(5)请写出流程中用SO 进行还原时发生反应的离子方程式:___________
2
【答案】(1)54.3 500 mL容量瓶、胶头滴管
(2)2Cr3++3HO+HO=Cr O2-+8H+
2 2 2 2 7
(3)Cr O2-+2OH- 2CrO2-+HO 或Cr O2-+HO 2CrO2-+2H+,加入碱,与H+反应,平
2 7 4 2 2 7 2 4
衡正向移动
(4)Mg2+、Ca2+ (5)2CrO 2-+3SO +12HO = 2Cr(OH)(H O) SO ↓+SO 2-+2OH-
4 2 2 2 5 4 4
【解析】含铬污泥预处理后加入硫酸酸浸,酸浸后的滤液Ⅰ中的金属离子主要是Cr3+,其次是Fe3+、
Al3+、Ca2+和Mg2+,加入HO,Cr3+被HO 氧化为Cr O2-,再加入NaOH溶液,调整pH=8,则此时
2 2 2 2 2 7
Cr O2-转化为CrO2-,且Fe3+、Al3+沉淀完全,此时滤液Ⅱ中含有金属阳离子Ca2+和Mg2+,还有CrO2-,
2 7 4 4
利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有Ca2+和Mg2+,再通入SO ,使CrO2-转化为Cr(OH)
2 4
(H O) SO 。(1)根据cV= c V 列等式,18.4×V×10-3=2×500×10-3,解得V≈54.3 mL;配制时所用玻璃仪器
2 5 4 1 1 2 2 1 1
除量筒、烧杯和玻璃棒外,还需500 mL容量瓶和胶头滴管。(2)经氧化环节滤液Ⅰ中的Cr3+被HO 氧化为
2 2
Cr O2-,此反应的离子方程式为2Cr3++3HO+HO=Cr O2-+8H+。(3) Cr O2-为橙黄色, CrO2-为黄色,
2 7 2 2 2 2 7 2 7 4
反应的离子方程式为Cr O2-+2OH- 2CrO2-+HO,调pH=8后平衡正向移动,溶液中Cr O2-浓度减
2 7 4 2 2 7
小,CrO2-浓度增大,颜色由橙黄色变为黄色的。(4)滤液Ⅱ中金属阳离子有Ca2+和Mg2+,则利用钠离子交
4
换树脂可除去滤液Ⅱ中的金属阳离子有Ca2+和Mg2+。(5)流程中用SO 进行还原时发生反应是还原CrO2-生
2 4
成Cr(OH)(HO) SO ,反应的离子方程式为2CrO2-+3SO +12HO = 2Cr(OH)(H O) SO ↓+SO 2-+2OH-。
2 5 4 4 2 2 2 5 4 4