文档内容
解密 15 实验方案的设计与评价
一、单选题
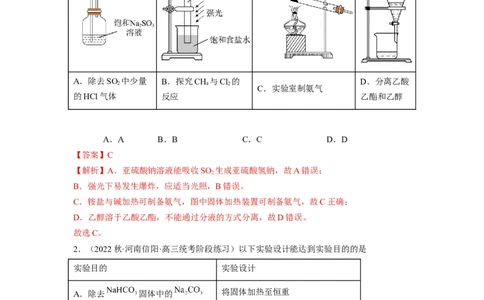
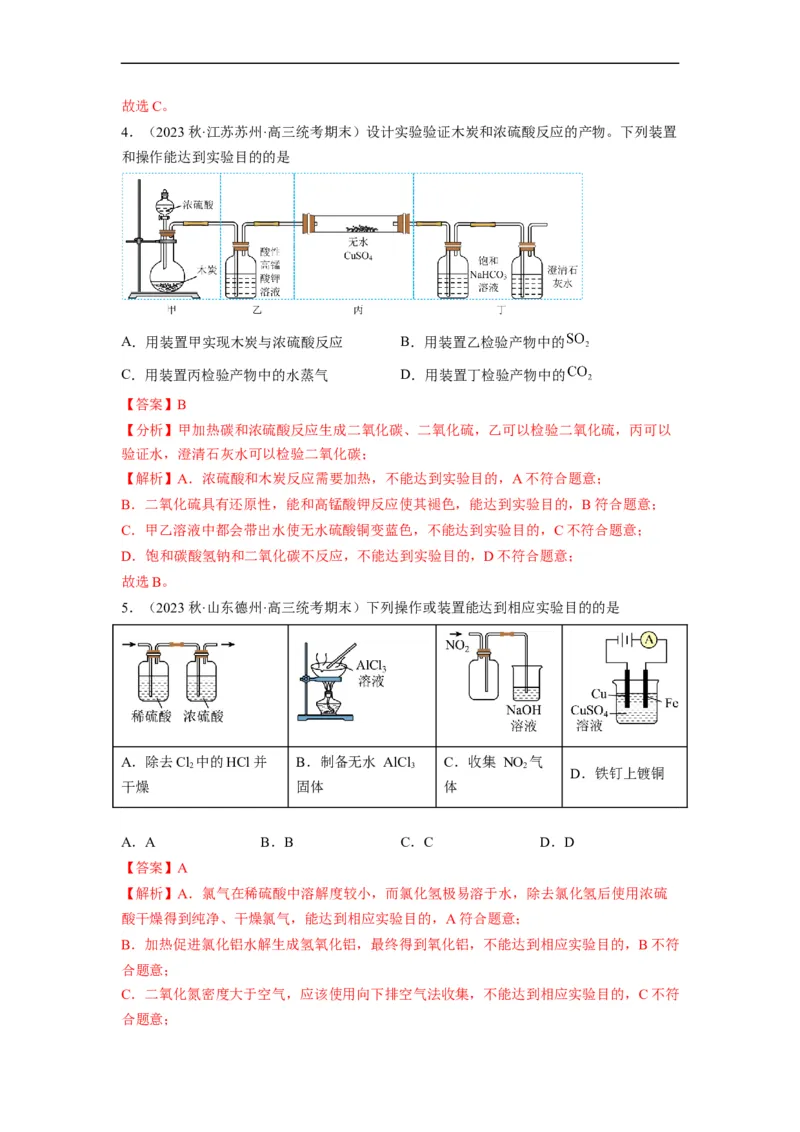
1.(2022春·山东济南·高三统考专题练习)下列实验装置及试剂的使用正确,且能达到实
验目的的是
A.除去SO 中少量 B.探究CH 与Cl 的 D.分离乙酸
2 4 2
C.实验室制氨气
的HCl气体 反应 乙酯和乙醇
A.A B.B C.C D.D
【答案】C
【解析】A.亚硫酸钠溶液能吸收SO 生成亚硫酸氢钠,故A错误;
2
B.强光下易发生爆炸,应适当光照,B错误。
C.铵盐与碱加热可制备氨气,图中固体加热装置可制备氨气,故C正确;
D.乙醇溶于乙酸乙酯,不能通过分液的方式分离,故D错误。
故选C。
2.(2022秋·河南信阳·高三统考阶段练习)以下实验设计能达到实验目的的是
实验目的 实验设计
A.除去 固体中的 将固体加热至恒重
B.制备无水 蒸发Al与稀盐酸反应后的溶液
C.检验 是否完全氧化 取样加入硫氰化钾溶液
D.鉴别NaBr和KI溶液
分别加新制氯水后,用 萃取
A.A B.B C.C D.D
【答案】D【解析】A.碳酸氢钠不稳定,受热易分解;将固体加热至恒重,只能除去NaCO 固体中
2 3
的NaHCO ,不能除去NaHCO 固体中的NaCO,故A不符合题意;
3 3 2 3
B.氯化铝水解生成氢氧化铝和盐酸,加热后氯化氢易挥发,促进水解,因此制备无水
AlCl 需在HCl气流中加热蒸发AlCl 溶液,故B不符合题意;
3 3
C.铁离子和硫氰化钾溶液反应溶液变红色,只能检验硫酸亚铁是否变质,不能检验是否
完全氧化,故C不符合题意;
D.鉴别NaBr和KI溶液,分别加新制氯水后,氯气置换溴,氯气置换碘;用CCl 萃取,
4
有机层呈橙色,说明是NaBr溶液,有机层呈紫红色,说明是KI溶液,故D符合题意。
故选D。
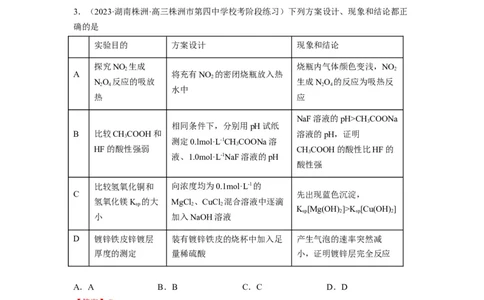
3.(2023·湖南株洲·高三株洲市第四中学校考阶段练习)下列方案设计、现象和结论都正
确的是
实验目的 方案设计 现象和结论
探究NO 生成 烧瓶内气体颜色变浅,NO
2 2
A 将充有NO 的密闭烧瓶放入热
2
NO 反应的吸放 生成NO 的反应为吸热反
2 4 2 4
水中
热 应
NaF溶液的pH>CHCOONa
3
相同条件下,分别用pH试纸
B 比较CHCOOH和 溶液的pH,证明
3
测定0.lmol·L-1CHCOONa溶
3
HF的酸性强弱 CHCOOH的酸性比HF的
3
液、1.0mol·L-1NaF溶液的pH
酸性强
比较氢氧化铜和 向浓度均为0.1mol·L-1的
C 先出现蓝色沉淀,
氢氧化镁K 的大 MgCl 、CuCl 混合溶液中逐滴
sp 2 2
K [Mg(OH) ]>K [Cu(OH) ]
sp 2 sp 2
小 加入NaOH溶液
D 镀锌铁皮锌镀层 装有镀锌铁皮的烧杯中加入足 产生气泡的速率突然减
厚度的测定 量稀硫酸 小,证明镀锌层完全反应
A.A B.B C.C D.D
【答案】C
【解析】A.NO 生成NO 是放热反应,温度升高,反应向生成红棕色气体二氧化氮的方
2 2 4
向移动,现象和结论不正确,故A错误;
B.方案设计中CHCOONa和NaF的浓度不相同,方案设计不正确,不能比较CHCOOH
3 3
和HF的酸性强弱,B错误;
C.氢氧化镁和氢氧化铜是同类型的物质,向浓度均为0.1mol·L-1的MgCl 、CuCl 混合溶液
2 2
中逐滴加入NaOH溶液,先出现蓝色沉淀,说明氢氧化铜更难溶,
K [Mg(OH) ]>K [Cu(OH) ],C正确;
sp 2 sp 2
D.锌铁都能和酸反应,方案设计不合理,锌反应的同时,可能就有铁发生反应,D错误。故选C。
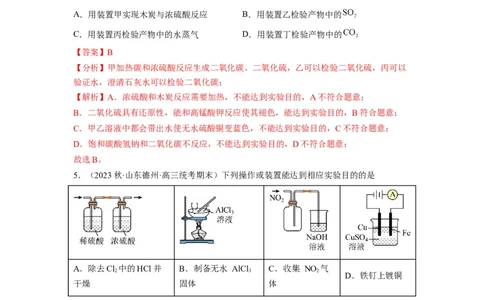
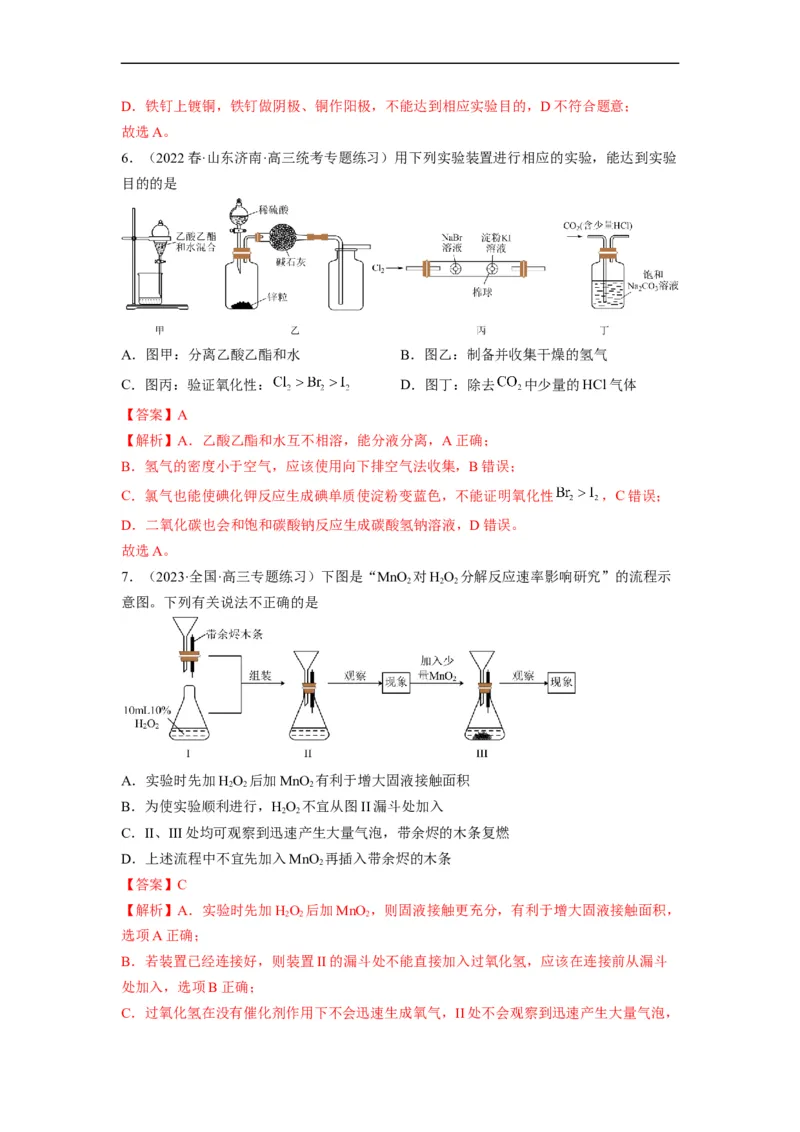
4.(2023秋·江苏苏州·高三统考期末)设计实验验证木炭和浓硫酸反应的产物。下列装置
和操作能达到实验目的的是
A.用装置甲实现木炭与浓硫酸反应 B.用装置乙检验产物中的
C.用装置丙检验产物中的水蒸气 D.用装置丁检验产物中的
【答案】B
【分析】甲加热碳和浓硫酸反应生成二氧化碳、二氧化硫,乙可以检验二氧化硫,丙可以
验证水,澄清石灰水可以检验二氧化碳;
【解析】A.浓硫酸和木炭反应需要加热,不能达到实验目的,A不符合题意;
B.二氧化硫具有还原性,能和高锰酸钾反应使其褪色,能达到实验目的,B符合题意;
C.甲乙溶液中都会带出水使无水硫酸铜变蓝色,不能达到实验目的,C不符合题意;
D.饱和碳酸氢钠和二氧化碳不反应,不能达到实验目的,D不符合题意;
故选B。
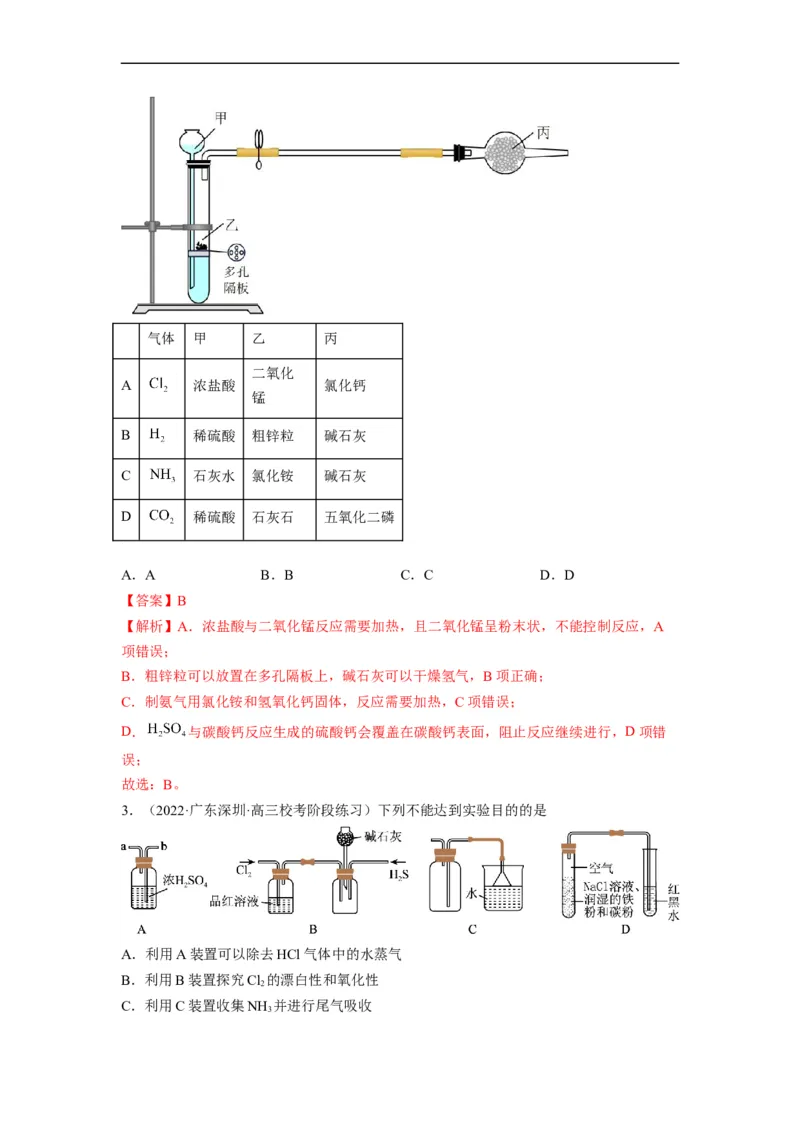
5.(2023秋·山东德州·高三统考期末)下列操作或装置能达到相应实验目的的是
A.除去Cl 中的HCl并 B.制备无水 AlCl C.收集 NO 气
2 3 2
D.铁钉上镀铜
干燥 固体 体
A.A B.B C.C D.D
【答案】A
【解析】A.氯气在稀硫酸中溶解度较小,而氯化氢极易溶于水,除去氯化氢后使用浓硫
酸干燥得到纯净、干燥氯气,能达到相应实验目的,A符合题意;
B.加热促进氯化铝水解生成氢氧化铝,最终得到氧化铝,不能达到相应实验目的,B不符
合题意;
C.二氧化氮密度大于空气,应该使用向下排空气法收集,不能达到相应实验目的,C不符
合题意;D.铁钉上镀铜,铁钉做阴极、铜作阳极,不能达到相应实验目的,D不符合题意;
故选A。
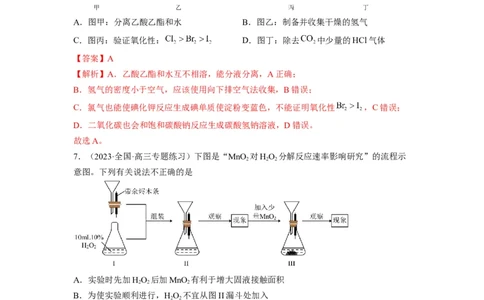
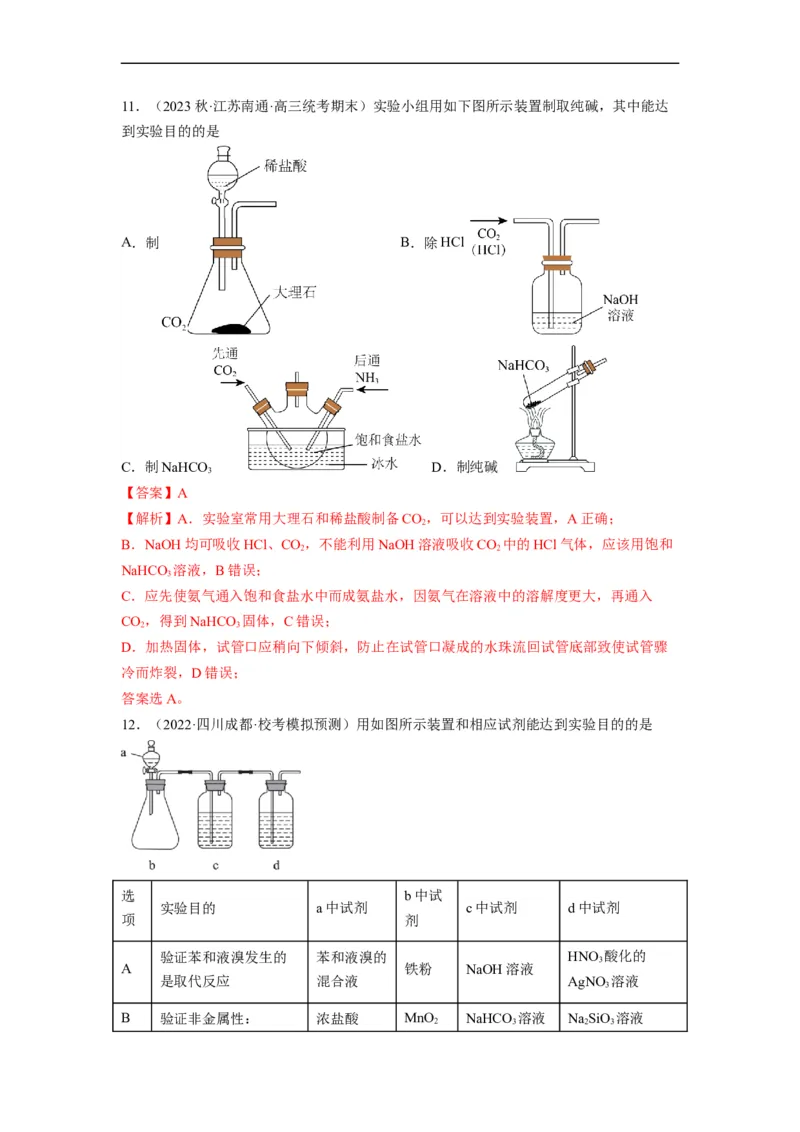
6.(2022春·山东济南·高三统考专题练习)用下列实验装置进行相应的实验,能达到实验
目的的是
A.图甲:分离乙酸乙酯和水 B.图乙:制备并收集干燥的氢气
C.图丙:验证氧化性: D.图丁:除去 中少量的HCl气体
【答案】A
【解析】A.乙酸乙酯和水互不相溶,能分液分离,A正确;
B.氢气的密度小于空气,应该使用向下排空气法收集,B错误;
C.氯气也能使碘化钾反应生成碘单质使淀粉变蓝色,不能证明氧化性 ,C错误;
D.二氧化碳也会和饱和碳酸钠反应生成碳酸氢钠溶液,D错误。
故选A。
7.(2023·全国·高三专题练习)下图是“MnO 对HO 分解反应速率影响研究”的流程示
2 2 2
意图。下列有关说法不正确的是
A.实验时先加HO 后加MnO 有利于增大固液接触面积
2 2 2
B.为使实验顺利进行,HO 不宜从图II漏斗处加入
2 2
C.II、III处均可观察到迅速产生大量气泡,带余烬的木条复燃
D.上述流程中不宜先加入MnO 再插入带余烬的木条
2
【答案】C
【解析】A.实验时先加HO 后加MnO ,则固液接触更充分,有利于增大固液接触面积,
2 2 2
选项A正确;
B.若装置已经连接好,则装置II的漏斗处不能直接加入过氧化氢,应该在连接前从漏斗
处加入,选项B正确;
C.过氧化氢在没有催化剂作用下不会迅速生成氧气,II处不会观察到迅速产生大量气泡,选项C错误;
D.上述流程中应先插入带余烬的木条,证明过氧化氢分解很慢,再加入过氧化氢证明二
氧化锰催化过氧化氢可迅速生成氧气;故不宜先加入MnO 再插入带余烬的木条,选项D
2
正确。
故选C。
8.(2022·全国·高三专题练习)用下列实验装置或操作进行相应实验,能达到实验目的的
是
A.用图甲装置干燥NH
3
B.用图乙所示装置灼烧碎海带
C.用图丙所示装置吸收多余的Cl 尾气
2
D.用图丁的装置制备Fe(OH) 胶体
3
【答案】B
【解析】A.NH 与HSO 可反应生成(NH )SO ,A错误;
3 2 4 4 2 4
B.坩埚用于固体物质的加热,碎海带可用坩埚盛放加热,B正确;
C.饱和氯化钠溶液中Cl 溶解度极低,且溶质也不与Cl 反应,无法吸收Cl,C错误;
2 2 2
D.FeCl 制备Fe(OH) 胶体应用煮沸的蒸馏水,NaOH溶液与FeCl 反应生成大量的
3 3 3
Fe(OH) 从而形成沉淀,D错误;
3
综上,本题选B。
二、填空题
9.(2023·全国·高三专题练习)为探究某绿矾样品的变质情况,化学兴趣小组的同学设计
了下列实验方案。
可供选择的试剂:硫氰化钾溶液、酸性高锰酸钾溶液、氯水、氢氧化钠溶液、氯化钡溶液,
请参与完成方案设计。
实验准备:取少量绿矾样品,用蒸馏水在烧杯中配成溶液。
(1)如何证明绿矾已经被氧化_______。
(2)如何证明绿矾已经被完全氧化_______。
(3)在使用硫酸亚铁时,如何防止 的干扰?写出相关离子方程式_______。
【答案】(1)取少量溶液,加入几滴硫氰化钾溶液,若溶液变红色,则证明绿矾样品已被氧
化(2)取少量溶液,加入几滴酸性高锰酸钾溶液,若溶液不褪色,则证明绿矾样品已被完全氧
化
(3)加入适量铁粉,
【解析】(1)绿矾被氧化后亚铁离子变为铁离子,铁离子和硫氰化钾溶液变红色,故实验
设计为:取少量溶液,加入几滴硫氰化钾溶液,若溶液变红色,则证明绿矾样品已被氧化;
(2)绿矾完全被氧化为铁离子,则不存在亚铁离子,亚铁离子能和酸性高锰酸钾溶液反应
使溶液褪色,故实验设计为:取少量溶液,加入几滴酸性高锰酸钾溶液,若溶液不褪色,
则证明绿矾样品已被完全氧化;
(3)铁离子和单质铁生成亚铁离子,加入过量铁粉,充分反应后过滤分离出铁粉,故答案
为:加入适量铁粉, 。
10.(2023·全国·高三专题练习)实验探究:补铁剂中铁元素价态检验
(1)预测补铁剂中铁元素价态
补铁剂中铁元素价态有以下3种可能
①可能为_______;
②可能为_______;
③可能既有+2价,又有+3价( 和 )。
(2)实验方案
实验操作、现象及结论
方案一:
实验操作 实验现象 实验结论
加入硫氰化钾溶液,溶液颜色无变化;加 含有 ,不含
入氯水后,溶液变为_______ _______
方案二:
实验操作 实验现象 实验结论不变红色 _______
紫红色褪去 _______
(3)实验结论分析
经过实验验证,补铁剂中铁元素价态为+2价,请写出相关反应的离子方程式:______,
_____。
【答案】(1) +2价 +3价
(2) 红色 不含 含
(3)
【分析】Fe元素常见的价态有0价、+2价和+3价,补铁剂中铁元素价态可能是+2、+3或
者二者都有,可以用硫氰化钾溶液验证 ,酸性高锰酸钾溶液验证 。
【解析】(1)Fe元素常见的价态有0价、+2价和+3价,补铁剂中铁不是单质,铁元素价
态有3种可能:①可能为+2价 ;②可能为+3价 ;③可能既有+2价,又有+3
价( 和 )。
(2)方案一:加入硫氰化钾溶液,溶液颜色无变化,说明不存在 ,加入氯水后,
Fe2+被氧化成 ,溶液变为红色,实验结论为:含有 ,不含 ;方案二:加入硫氰
化钾溶液,溶液颜色无变化,说明不存在 ;加入酸性高锰酸钾溶液,紫红色褪去,说
明其中含有 。
(3)经过实验验证,补铁剂中铁元素价态为+2价,加入氯水后,Fe2+被氧化成 ,离子
方程式为: , 和硫氰化钾溶液反应生成红色的 ,离
子方程式为: 。一、单选题
1.(2022春·湖南郴州·高三郴州一中校考期中)用如图实验装置进行有关实验,能达到实
验目的的是
A.用装置甲定量测定化学反应速率
B.用装置乙干燥
C.用装置丙分离甲醇(沸点为64.7℃)与水的混合物
D.用装置丁除去溶在 中的
【答案】D
【解析】A.生成氧气可从长颈漏斗逸出,不能测定反应速率,应改为分液漏斗,故A错
误;
B.碱石灰内含有NaOH,能与Cl 发生反应,不能干燥氯气,故B错误;
2
C.温度计应处于蒸馏烧瓶的支气管处,故C错误;
D.溴和氢氧化钠溶液反应生成可溶性的钠盐,四氯化碳不反应,四氯化碳和水不互溶,
四氯化碳密度大于水,所以水溶液在上方、四氯化碳在下方,再通过分液即可除去,故D
正确;
故选:D。
2.(2022·河北·模拟预测)用如图所示装置制备干燥的气体(甲、乙、丙表示加入的试剂)
且能随开随用、随关随停地控制反应,能实现的是气体 甲 乙 丙
二氧化
A 浓盐酸 氯化钙
锰
B 稀硫酸 粗锌粒 碱石灰
C 石灰水 氯化铵 碱石灰
D 稀硫酸 石灰石 五氧化二磷
A.A B.B C.C D.D
【答案】B
【解析】A.浓盐酸与二氧化锰反应需要加热,且二氧化锰呈粉末状,不能控制反应,A
项错误;
B.粗锌粒可以放置在多孔隔板上,碱石灰可以干燥氢气,B项正确;
C.制氨气用氯化铵和氢氧化钙固体,反应需要加热,C项错误;
D. 与碳酸钙反应生成的硫酸钙会覆盖在碳酸钙表面,阻止反应继续进行,D项错
误;
故选:B。
3.(2022·广东深圳·高三校考阶段练习)下列不能达到实验目的的是
A.利用A装置可以除去HCl气体中的水蒸气
B.利用B装置探究Cl 的漂白性和氧化性
2
C.利用C装置收集NH 并进行尾气吸收
3D.利用D装置检验该条件下Fe发生了析氢腐蚀
【答案】D
【解析】A.HCl是酸性气体,浓硫酸具有吸水性,可用浓硫酸来除去HCl气体中的水蒸
气,故A正确;
B.氯气通入品红溶液中褪色,证明其漂白性,通入硫化氢和氯气发生氧化还原反应,证
明其氧化性,故B正确;
C.氨气密度比空气小,可用向下排空气发生收集,氨气极易溶于水,可用倒扣的漏斗来
防倒吸,进行尾气处理,故C正确;
D.NaCl溶液是中性溶液,铁与氧气和水发生吸氧腐蚀,故D错误;
故选:D。
4.(2022秋·陕西商洛·高三统考期末)用下列实验装置进行相应的实验,能达到实验目的
的是
A.利用图甲验证浓硫酸具有脱水性、强氧化性,SO 具有漂白性、还原性
2
B.利用图乙制备并收集干燥的氢气
C.利用图丙制备并收集少量的NO
2
D.利用图丁制取碳酸氢钠
【答案】A
【解析】A.图甲中浓硫酸具有脱水性使蔗糖转化为碳,碳和浓硫酸生成二氧化硫气体,
可以验证浓硫酸具有脱水性、强氧化性;品红溶液、高锰酸钾溶液褪色, 可以验证SO 具
2
有漂白性、还原性,A正确;
B.氢气密度小于空气,应该用向下排空气法收集,B错误;
C.二氧化氮和水反应,不能用排水法收集,C错误;
D.氨气极易溶于水应该使用防倒吸装置,D错误;
故选A。
5.(2023·河北邢台·统考模拟预测)利用如图所示的装置(夹持装置略去)进行实验,b中的
现象能证明a中反应所得产物的是选项 发生反应 实验现象
A 乙醇和浓 反应生成乙烯 酸性 溶液褪色
B 木炭粉和浓 反应生成 溴水褪色
C 和浓盐酸反应生成 滴有酚酞的 溶液褪色
D 苯和液溴反应生成 溶液中产生浅黄色沉淀
A.A B.B C.C D.D
【答案】B
【解析】A.由于乙醇易挥发,也能使酸性 溶液褪色,因此并不能证明反应生成乙
烯,A项错误;
B.木炭粉和浓 反应,只有生成的 可使溴水褪色,B项正确;
C.浓 易挥发,因此滴有酚酞的 溶液褪色可能是 中和了 ,因此不能
证明反应生成 ,C项错误;
D.液溴易挥发,其进入 溶液中也会生成浅黄色沉淀,因此不能证明有 生成,
D项错误;
答案选B。
6.(2023·安徽合肥·统考一模)下列由实验操作和现象可得出正确结论的是
选
实验操作和现象 结论
项
使蛋白质变
A 向鸡蛋清中加入饱和 溶液,有白色沉淀产生
性
向某溶液中滴加稀硫酸,将产生的气体通入品红溶液,品红 该溶液中可能含有
B
褪色
C
向 溶液中滴入10滴溶液,生成白色沉淀,再滴加 溶液,出现黄色
沉淀
向 溶液中滴加 溶液,溶
D 具有氧化性
液褪色
A.A B.B C.C D.D
【答案】B
【解析】A.硫酸铵溶液能使蛋白质发生盐析而不是变性,A错误;
B.亚硫酸根离子和酸反应会生成使品红褪色的气体二氧化硫气体,故该溶液中可能含有
,B正确;
C.反应中银离子过量,加入碘离子会生成碘化银沉淀,不能说明 ,C
错误;
D.高锰酸钾发生还原反应为氧化剂,过氧化氢发生氧化反应体现还原性,D错误;
故选B。
7.(2023·广东·华南师大附中校联考模拟预测)用浓硫酸与乙醇共热制备乙烯时,常因温
度过高发生副反应,使制备的乙烯气体中可能存在 和 等杂质气体,某同学将上述
混合气体通入下列装置中以验证其成分,下列说法不正确的是
A.品红溶液a褪色证明气体中有
B.品红溶液b不变色且澄清石灰水变浑浊证明原乙烯气体中有
C. 的生成体现了浓硫酸的氧化性
D.酸性高锰酸钾溶液可以氧化乙烯和
【答案】B
【解析】A.二氧化硫可使品红溶液褪色,所以若品红溶液a褪色,则证明气体中有 ,
A正确;
B.因为酸性高锰酸钾可氧化乙烯气体转化为二氧化碳,所以若澄清石灰水变浑浊,只能
只能证明存在二氧化碳,不能证明原混合气体中含二氧化碳,B错误;C.乙醇与浓硫酸反应,若生成二氧化硫,则证明S元素化合价降低,即体现了浓硫酸的
氧化性,C正确;
D.乙烯和二氧化硫均具有还原性,均可被酸性高锰酸钾溶液氧化,D正确;
故选B。
8.(2023·全国·高三专题练习)实验室用如图所示装置可进行钠与二氧化碳的反应,并能
检验产物 (已知: 溶液吸收 气体产生黑色的单质Pd),下列说法错误的是
A.装置①除可制备 外,还可以制取 、 等气体
B.装置⑤中石灰水变浑浊后,再点燃装置④处的酒精灯
C.装置②、③中盛装的试剂分别为饱和 溶液、浓
D.装置⑥中产生黑色沉淀的反应为
【答案】C
【解析】A.装置①适用于固体和液体不加热反应制备气体,锌和稀硫酸反应制氢气,氧
化钙和浓氨水反应制备氨气都可以用装置①,A正确;
B.金属钠能与空气中的氧气、水蒸气等发生反应,因此需先用二氧化碳气体排除装置内
的空气,当看到装置⑤中石灰水变浑浊时,表明空气已排净,再点燃④处的酒精灯,B正
确;
C.反应产生的二氧化碳气体含有氯化氢和水蒸气,因此应先用饱和碳酸氢钠溶液除去氯
化氢,再用浓 吸收水蒸气,C错误;
D. 溶液吸收 气体, 被 还原为黑色的 , 被 氧化为 ,化
学方程式为 ,D正确;
故选C。
9.(2023·吉林·统考二模)用下列实验装置完成对应的实验(部分仪器已省略),能达到实
验目的的是
A B C D装
置
A.蒸馏海水制淡水 B.稀释浓 C.吸收 D.制取乙酸乙酯
【答案】C
【解析】A.蒸馏时温度水银部位应在蒸馏烧瓶支管口处,不能达到实验目的,故A不符
合题意;
B.浓硫酸稀释应是“酸入水”,故B不符合题意;
C.氨气不溶于四氯化碳,用该装置能吸收氨气并防止倒吸,能达到实验目的,故C符合
题意;
D.收集乙酸乙酯应该用饱和碳酸钠溶液,因此不能达到实验目的,故D不符合题意;
故选C。
10.(2022·江苏·高三统考专题练习)兴趣小组用预处理后的废弃油脂制作肥皂(高级脂肪
酸钠)并回收甘油,简单流程如下图所示。下列说法错误的是
A.步骤①中加入乙醇的目的是助溶,提高反应速率
B.步骤②中加入食盐细粒的目的是降低肥皂的溶解度
C.步骤③可借助装置M完成(夹持装置省略)
D.步骤④中包含蒸馏操作
【答案】C
【解析】A.乙醇是常用的有机溶剂,而且能够与水混溶,油脂难溶于水,步骤①中加入
乙醇的目的是增加油脂在NaOH溶液中的溶解度,使反应物充分接触发生反应。从而可提
高反应速率,A正确;
B.向混合物中加入食盐细粒,会降低高级脂肪酸钠的溶解度而结晶析出,即发生盐析现
象,B正确;
C.操作③为过滤,用到的仪器为漏斗,而不是分液漏斗,C错误;
D.甘油和水相互溶解,二者的沸点不同,用蒸馏操作分离甘油,D正确;
故合理选项是C。11.(2023秋·江苏南通·高三统考期末)实验小组用如下图所示装置制取纯碱,其中能达
到实验目的的是
A.制 B.除HCl
C.制NaHCO D.制纯碱
3
【答案】A
【解析】A.实验室常用大理石和稀盐酸制备CO,可以达到实验装置,A正确;
2
B.NaOH均可吸收HCl、CO,不能利用NaOH溶液吸收CO 中的HCl气体,应该用饱和
2 2
NaHCO 溶液,B错误;
3
C.应先使氨气通入饱和食盐水中而成氨盐水,因氨气在溶液中的溶解度更大,再通入
CO,得到NaHCO 固体,C错误;
2 3
D.加热固体,试管口应稍向下倾斜,防止在试管口凝成的水珠流回试管底部致使试管骤
冷而炸裂,D错误;
答案选A。
12.(2022·四川成都·校考模拟预测)用如图所示装置和相应试剂能达到实验目的的是
选 b中试
实验目的 a中试剂 c中试剂 d中试剂
项 剂
验证苯和液溴发生的 苯和液溴的 HNO 酸化的
3
A 铁粉 NaOH溶液
是取代反应 混合液 AgNO 溶液
3
B 验证非金属性: 浓盐酸 MnO NaHCO 溶液 NaSiO 溶液
2 3 2 3Cl>C>Si
检验X溶液中有CO 酸性 KMnO
4
C 稀硫酸 X溶液 澄清的石灰水
溶液
,无SO
制备并收集少量NO气
D 稀硝酸 铜片 水 NaOH溶液
体
A.A B.B C.C D.D
【答案】C
【解析】A.装置c中的氢氧化钠溶液会吸收溴化氢和挥发出的溴,导致装置d中硝酸酸化
的硝酸银溶液无法检验是否有溴化氢生成,故A错误;
B.浓盐酸与二氧化锰常温下不反应,挥发出的氯化氢能与碳酸氢钠溶液反应生成二氧化
碳,说明盐酸的酸性强于碳酸,但元素的非金属性与氢化物的酸性无关,所以无法比较氯
元素和碳元素的非金属性强弱,且氯化氢会优先与硅酸钠溶液反应,干扰碳元素个硅元素
的非金属性强弱的比较,故B错误;
C.向X溶液中滴入稀硫酸,反应生成的气体不能使酸性高锰酸钾溶液褪色,但能使澄清
石灰水变混浊可以说明X溶液中含有碳酸根离子,不含有亚硫酸根离子,故C正确;
D.收集一氧化氮气体应从装置c的短管通入气体,则装置c无法收集一氧化氮气体,且一
氧化氮是不成盐氧化物,不能用氢氧化钠溶液吸收尾气,故D错误;
故选C。
二、填空题
13.(2022秋·福建漳州·高三校考期中)某校探究学习小组用已部分生锈的废铁屑制作印
刷电路板的腐蚀剂,并回收铜。探究过程如图所示:
请回答下列问题:
(1)步骤①中先加入热的Na2CO3溶液除油污,操作甲的名称是________。
(2)步骤②中,除发生反应Fe+2HCl===FeCl2+H2↑外,其他可能反应的离子方程式为
_______________________________________________________。
(3)溶液C的颜色是________,溶液D中可能含有的金属阳离子有_______________。
(4)可以验证溶液B中是否含有Fe2+的一种试剂是______(填选项序号)。
a.稀硫酸 b.铁c.硫氰化钾 d.酸性高锰酸钾溶液
(5)操作乙的名称是________,步骤⑤产生金属铜的化学方程式为
_______________________________________________________________________。【答案】 过滤 Fe O+6H+===2Fe3++3HO、Fe+2Fe3+===3Fe2
2 3 2
+ 棕黄色 d Fe2+、Cu2+、Fe3+ 电解 CuCl Cu
2
+Cl↑
2
【解析】(1)加入热的碳酸钠溶液的目的是为了除去表面的油污,再经过滤得到固体。
(2)实验的的是已经部分生锈的废铁屑,所以表面会有氧化铁,应该存在氧化铁与盐酸的
反应。
(3)通入氯气以后,溶液C应该是氯化铁溶液,颜色为棕黄色。用氯化铁溶液腐蚀印刷
电路板,反应为Cu和氯化铁反应,生成氯化铜和氯化亚铁,所以溶液中可能有Fe2+、Cu2
+、Fe3+。
(4)验证是否含有Fe2+的方法是滴加酸性高锰酸钾溶液,高锰酸钾被Fe2+还原,溶液会
褪色,所以答案为d。
(5)溶液D中有氯化铁、氯化铜、氯化亚铁,要想得到单质铜和氯气应该进行电解,将
氯化铜电解为单质铜和氯气。所以反应方程式为:CuCl Cu+Cl↑。
2 2
14.(2022·全国·高三专题练习)甲、乙组同学分别做了以下探究实验。
(1)甲组探究Cl 与NaSO 溶液反应,实验装置如下。
2 2 3
①写出制取氯气的化学方程式______________。
②该装置的不足之处除无尾气吸收装置外,另一处是______________。
③Cl 与NaSO 溶液反应的离子方程式为____________。
2 2 3
④设计实验,简述实验步骤,证明洗气瓶中的NaSO 已被氧化_________。
2 3
(2)乙组探究乙酸乙酯在不同温度、不同浓度NaOH 溶液中的水解速率。取四只大小相
同的试管,在试管外壁贴上体积刻度纸,按下表进行对照实验。在两种不同温度的水浴中加
热相同时间后,记录酯层的体积来确定水解反应的速率
试管
实验试剂 试管I 试管II 试管IV
Ⅲ
乙酸乙酯/mL 1 V V V
1 2 31mol/L NaOH/ mL V4 3 0 V
5
蒸馏水/mL 0 V 5 2
6
⑤请完成上表,其中V=______,V=______,V=_______。
2 4 5
⑥实验中,可用饱和食盐水替代蒸馏水,以减小乙酸乙酯在水中的溶解度,使实验结果更准确;
但不能用饱和NaCO 溶液替代蒸馏水,其原因是____ ;实验中,试管IV比试管II中的酯层
2 3
减少更快,其原因有:温度高速率快,还可能有_________。 (乙酸乙酯沸点 为77.1℃)
【答案】 (1) MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O 没有加热装
置 Cl2+SO32-+H2O=2Cl-+SO42-+2H+ 取少量洗气瓶中的液体于干燥试管中,
加入足量盐酸(滴加稀盐酸至不再产生气体),再滴加少量的氯化钡溶液,若产生白色沉淀,
则证明已经被氧化 (2) V2=1 V4=5 V5=3 碳酸钠溶液水解显碱性,干扰
了探究NaOH溶液对水解速率的影响 水浴加热接近乙酸乙酯的沸点,温度越高,
乙酸乙酯挥发也越快,得不到正确结果
【解析】(1)①实验室利用二氧化锰和浓盐酸加热反应生成氯化锰、氯气和水,制取氯气
的化学方程式为MnO +4HCl(浓) MnCl +Cl↑+2H O;
2 2 2 2
②浓盐酸与二氧化锰制取氯气的反应需要加热,氯气有毒,应该使用尾气吸收装置,故答
案为没有加热装置;
③氯气与亚硫酸钠溶液反应生成硫酸钠和氯化氢,反应的离子方程式为:Cl+SO2-
2 3
+H O=2Cl-+SO2-+2H+;
2 4
④若洗气瓶中的NaSO 已被氧化,则洗气瓶的溶液中应该存在硫酸根离子,检验方法为:
2 3
取少量洗气瓶中的液体于干燥试管中,加入足量盐酸(滴加稀盐酸至不再产生气体),再滴
加少量的氯化钡溶液,若产生白色沉淀,则证明已经被氧化;
(2)⑤乙组探究乙酸乙酯(沸点77.1℃)在不同温度、不同浓度NaOH溶液中的水解速率,
四个试管中乙酸乙酯的体积都应该为1mL,即:V=V =V =1;试验Ⅰ和试验Ⅲ中蒸馏水的
1 2 3
体积不同,则探究的是氢氧化钠的浓度对乙酸乙酯水解的影响,还必须保证溶液总体积相
等,则氢氧化钠溶液体积应该为5mL,即:V=5;试管Ⅳ与试管Ⅰ、Ⅱ、Ⅲ的反应温度不
4
同,说明是探究温度对乙酸乙酯的水解影响,结合总体积必须相等可知,试管Ⅳ和试管Ⅱ
应该是探究温度对乙酸乙酯水解程度影响大小的,故氢氧化钠溶液体积应该为3mL,即:
V=3,即:V=1,V=5,V=3;
5 2 4 5
⑥碳酸钠溶液水解显碱性,干扰了探究NaOH溶液对水解速率的影响,所以不能用饱和
NaCO 溶液替代蒸馏水;乙酸乙酯的沸点为77.1℃,水浴温度接近乙酸乙酯的沸点,温度
2 3
越高,乙酸乙酯挥发也越快,导致试管中酯层减少速率加快,干扰了实验结果。