文档内容
解密 15 实验方案的设计与评价
一、单选题
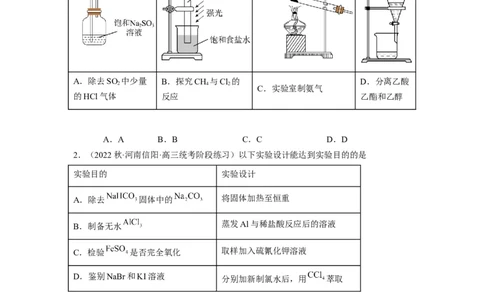
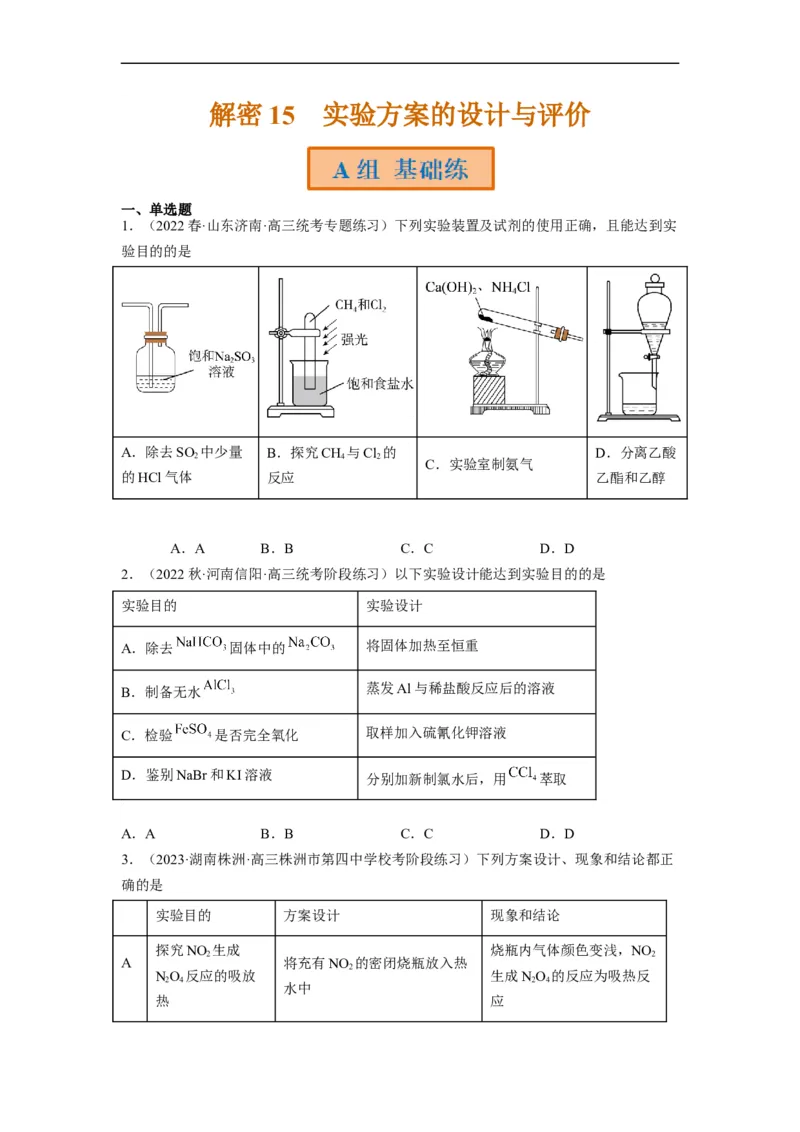
1.(2022春·山东济南·高三统考专题练习)下列实验装置及试剂的使用正确,且能达到实
验目的的是
A.除去SO 中少量 B.探究CH 与Cl 的 D.分离乙酸
2 4 2
C.实验室制氨气
的HCl气体 反应 乙酯和乙醇
A.A B.B C.C D.D
2.(2022秋·河南信阳·高三统考阶段练习)以下实验设计能达到实验目的的是
实验目的 实验设计
A.除去 固体中的 将固体加热至恒重
B.制备无水 蒸发Al与稀盐酸反应后的溶液
C.检验 是否完全氧化 取样加入硫氰化钾溶液
D.鉴别NaBr和KI溶液
分别加新制氯水后,用 萃取
A.A B.B C.C D.D
3.(2023·湖南株洲·高三株洲市第四中学校考阶段练习)下列方案设计、现象和结论都正
确的是
实验目的 方案设计 现象和结论
探究NO 生成 烧瓶内气体颜色变浅,NO
2 2
A 将充有NO 的密闭烧瓶放入热
2
NO 反应的吸放 生成NO 的反应为吸热反
2 4 2 4
水中
热 应NaF溶液的pH>CHCOONa
3
相同条件下,分别用pH试纸
B 比较CHCOOH和 溶液的pH,证明
3
测定0.lmol·L-1CHCOONa溶
3
HF的酸性强弱 CHCOOH的酸性比HF的
3
液、1.0mol·L-1NaF溶液的pH
酸性强
比较氢氧化铜和 向浓度均为0.1mol·L-1的
C 先出现蓝色沉淀,
氢氧化镁K 的大 MgCl 、CuCl 混合溶液中逐滴
sp 2 2
K [Mg(OH) ]>K [Cu(OH) ]
sp 2 sp 2
小 加入NaOH溶液
D 镀锌铁皮锌镀层 装有镀锌铁皮的烧杯中加入足 产生气泡的速率突然减
厚度的测定 量稀硫酸 小,证明镀锌层完全反应
A.A B.B C.C D.D
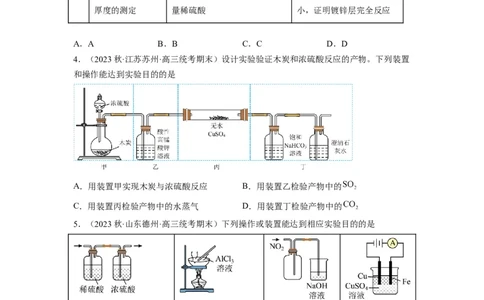
4.(2023秋·江苏苏州·高三统考期末)设计实验验证木炭和浓硫酸反应的产物。下列装置
和操作能达到实验目的的是
A.用装置甲实现木炭与浓硫酸反应 B.用装置乙检验产物中的
C.用装置丙检验产物中的水蒸气 D.用装置丁检验产物中的
5.(2023秋·山东德州·高三统考期末)下列操作或装置能达到相应实验目的的是
A.除去Cl 中的HCl并 B.制备无水 AlCl C.收集 NO 气
2 3 2
D.铁钉上镀铜
干燥 固体 体
A.A B.B C.C D.D
6.(2022春·山东济南·高三统考专题练习)用下列实验装置进行相应的实验,能达到实验
目的的是A.图甲:分离乙酸乙酯和水 B.图乙:制备并收集干燥的氢气
C.图丙:验证氧化性: D.图丁:除去 中少量的HCl气体
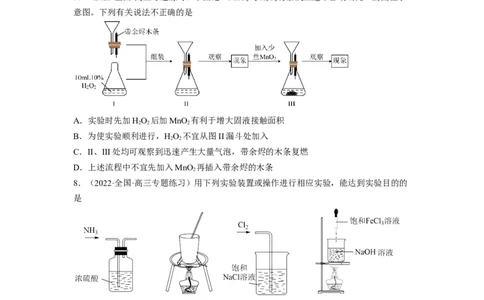
7.(2023·全国·高三专题练习)下图是“MnO 对HO 分解反应速率影响研究”的流程示
2 2 2
意图。下列有关说法不正确的是
A.实验时先加HO 后加MnO 有利于增大固液接触面积
2 2 2
B.为使实验顺利进行,HO 不宜从图II漏斗处加入
2 2
C.II、III处均可观察到迅速产生大量气泡,带余烬的木条复燃
D.上述流程中不宜先加入MnO 再插入带余烬的木条
2
8.(2022·全国·高三专题练习)用下列实验装置或操作进行相应实验,能达到实验目的的
是
A.用图甲装置干燥NH
3
B.用图乙所示装置灼烧碎海带
C.用图丙所示装置吸收多余的Cl 尾气
2
D.用图丁的装置制备Fe(OH) 胶体
3
二、填空题
9.(2023·全国·高三专题练习)为探究某绿矾样品的变质情况,化学兴趣小组的同学设计
了下列实验方案。可供选择的试剂:硫氰化钾溶液、酸性高锰酸钾溶液、氯水、氢氧化钠溶液、氯化钡溶液,
请参与完成方案设计。
实验准备:取少量绿矾样品,用蒸馏水在烧杯中配成溶液。
(1)如何证明绿矾已经被氧化_______。
(2)如何证明绿矾已经被完全氧化_______。
(3)在使用硫酸亚铁时,如何防止 的干扰?写出相关离子方程式_______。
10.(2023·全国·高三专题练习)实验探究:补铁剂中铁元素价态检验
(1)预测补铁剂中铁元素价态
补铁剂中铁元素价态有以下3种可能
①可能为_______;
②可能为_______;
③可能既有+2价,又有+3价( 和 )。
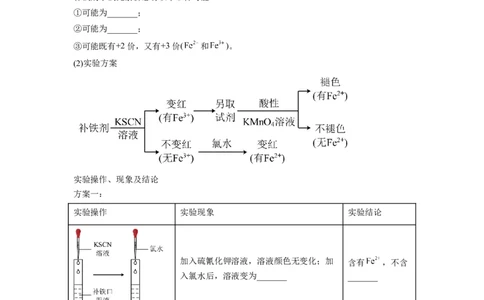
(2)实验方案
实验操作、现象及结论
方案一:
实验操作 实验现象 实验结论
加入硫氰化钾溶液,溶液颜色无变化;加 含有 ,不含
入氯水后,溶液变为_______ _______
方案二:
实验操作 实验现象 实验结论不变红色 _______
紫红色褪去 _______
(3)实验结论分析
经过实验验证,补铁剂中铁元素价态为+2价,请写出相关反应的离子方程式:______,
_____。
【
一、单选题
1.(2022春·湖南郴州·高三郴州一中校考期中)用如图实验装置进行有关实验,能达到实
验目的的是
A.用装置甲定量测定化学反应速率
B.用装置乙干燥
C.用装置丙分离甲醇(沸点为64.7℃)与水的混合物
D.用装置丁除去溶在 中的
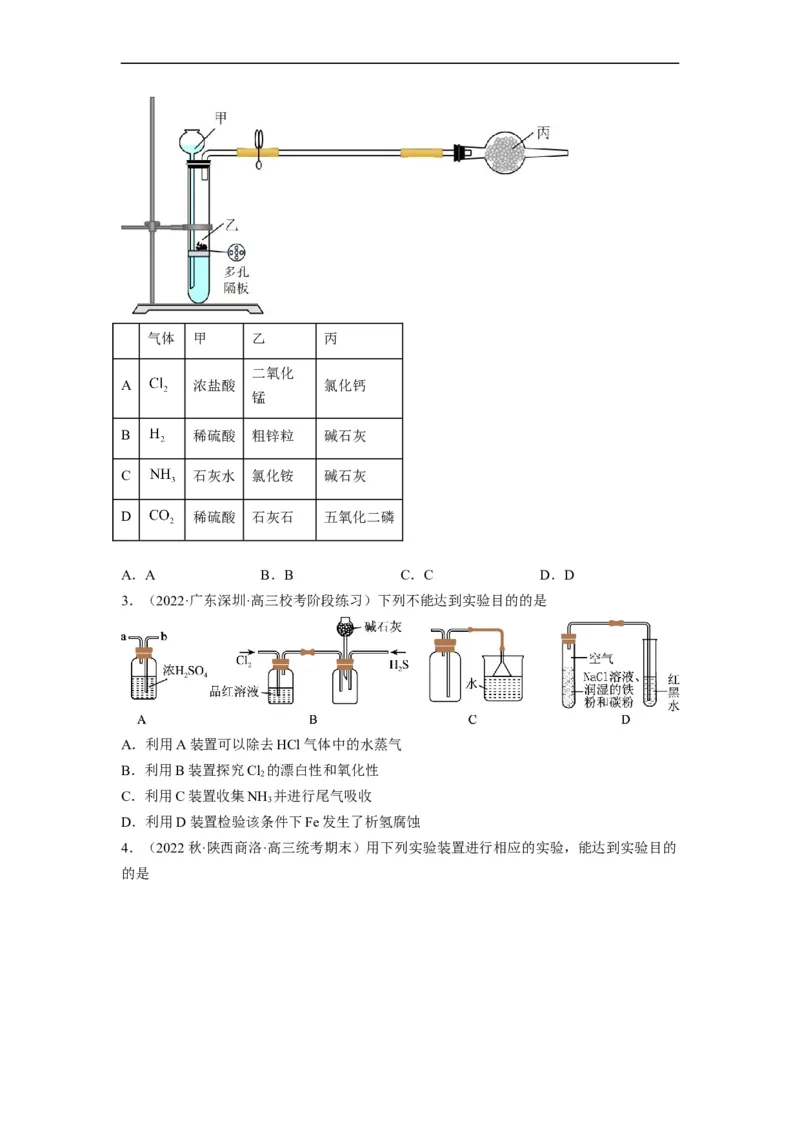
2.(2022·河北·模拟预测)用如图所示装置制备干燥的气体(甲、乙、丙表示加入的试剂)
且能随开随用、随关随停地控制反应,能实现的是气体 甲 乙 丙
二氧化
A 浓盐酸 氯化钙
锰
B 稀硫酸 粗锌粒 碱石灰
C 石灰水 氯化铵 碱石灰
D 稀硫酸 石灰石 五氧化二磷
A.A B.B C.C D.D
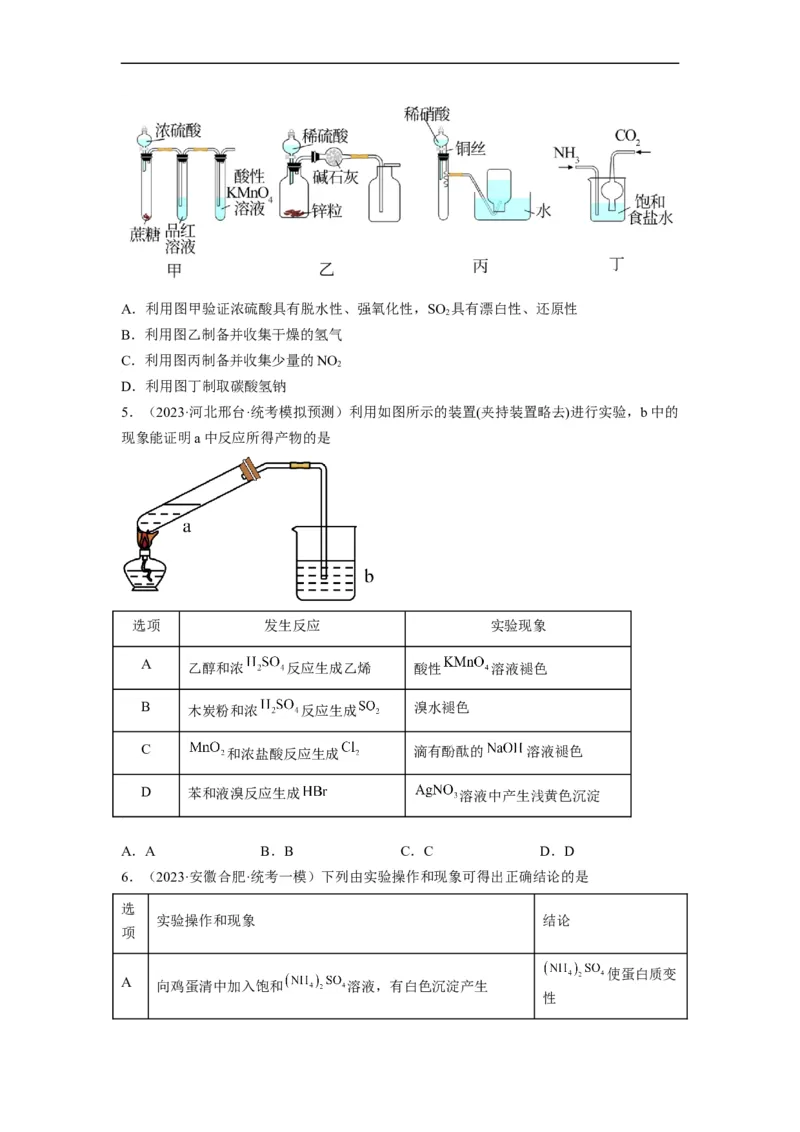
3.(2022·广东深圳·高三校考阶段练习)下列不能达到实验目的的是
A.利用A装置可以除去HCl气体中的水蒸气
B.利用B装置探究Cl 的漂白性和氧化性
2
C.利用C装置收集NH 并进行尾气吸收
3
D.利用D装置检验该条件下Fe发生了析氢腐蚀
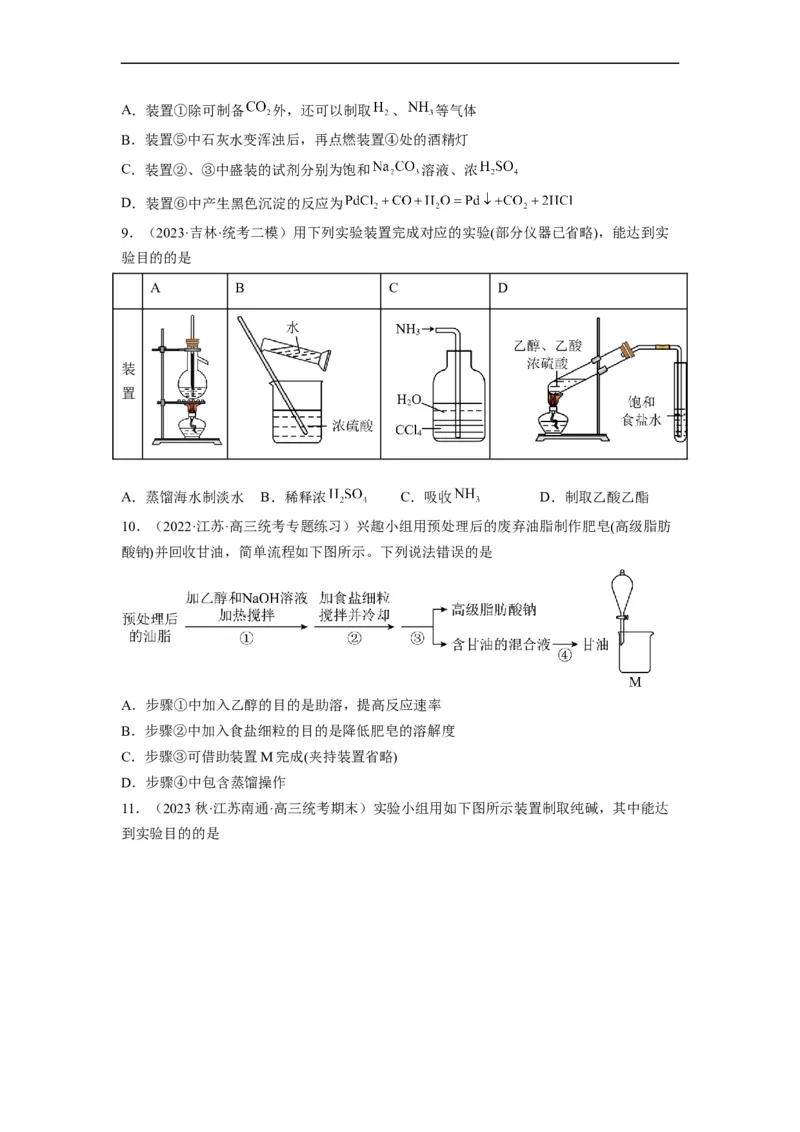
4.(2022秋·陕西商洛·高三统考期末)用下列实验装置进行相应的实验,能达到实验目的
的是A.利用图甲验证浓硫酸具有脱水性、强氧化性,SO 具有漂白性、还原性
2
B.利用图乙制备并收集干燥的氢气
C.利用图丙制备并收集少量的NO
2
D.利用图丁制取碳酸氢钠
5.(2023·河北邢台·统考模拟预测)利用如图所示的装置(夹持装置略去)进行实验,b中的
现象能证明a中反应所得产物的是
选项 发生反应 实验现象
A 乙醇和浓 反应生成乙烯 酸性 溶液褪色
B 木炭粉和浓 反应生成 溴水褪色
C 和浓盐酸反应生成 滴有酚酞的 溶液褪色
D 苯和液溴反应生成 溶液中产生浅黄色沉淀
A.A B.B C.C D.D
6.(2023·安徽合肥·统考一模)下列由实验操作和现象可得出正确结论的是
选
实验操作和现象 结论
项
使蛋白质变
A 向鸡蛋清中加入饱和 溶液,有白色沉淀产生
性向某溶液中滴加稀硫酸,将产生的气体通入品红溶液,品红 该溶液中可能含有
B
褪色
向 溶液中滴入10滴
C
溶液,生成白色沉淀,再滴加 溶液,出现黄色
沉淀
向 溶液中滴加 溶液,溶
D 具有氧化性
液褪色
A.A B.B C.C D.D
7.(2023·广东·华南师大附中校联考模拟预测)用浓硫酸与乙醇共热制备乙烯时,常因温
度过高发生副反应,使制备的乙烯气体中可能存在 和 等杂质气体,某同学将上述
混合气体通入下列装置中以验证其成分,下列说法不正确的是
A.品红溶液a褪色证明气体中有
B.品红溶液b不变色且澄清石灰水变浑浊证明原乙烯气体中有
C. 的生成体现了浓硫酸的氧化性
D.酸性高锰酸钾溶液可以氧化乙烯和
8.(2023·全国·高三专题练习)实验室用如图所示装置可进行钠与二氧化碳的反应,并能
检验产物 (已知: 溶液吸收 气体产生黑色的单质Pd),下列说法错误的是A.装置①除可制备 外,还可以制取 、 等气体
B.装置⑤中石灰水变浑浊后,再点燃装置④处的酒精灯
C.装置②、③中盛装的试剂分别为饱和 溶液、浓
D.装置⑥中产生黑色沉淀的反应为
9.(2023·吉林·统考二模)用下列实验装置完成对应的实验(部分仪器已省略),能达到实
验目的的是
A B C D
装
置
A.蒸馏海水制淡水 B.稀释浓 C.吸收 D.制取乙酸乙酯
10.(2022·江苏·高三统考专题练习)兴趣小组用预处理后的废弃油脂制作肥皂(高级脂肪
酸钠)并回收甘油,简单流程如下图所示。下列说法错误的是
A.步骤①中加入乙醇的目的是助溶,提高反应速率
B.步骤②中加入食盐细粒的目的是降低肥皂的溶解度
C.步骤③可借助装置M完成(夹持装置省略)
D.步骤④中包含蒸馏操作
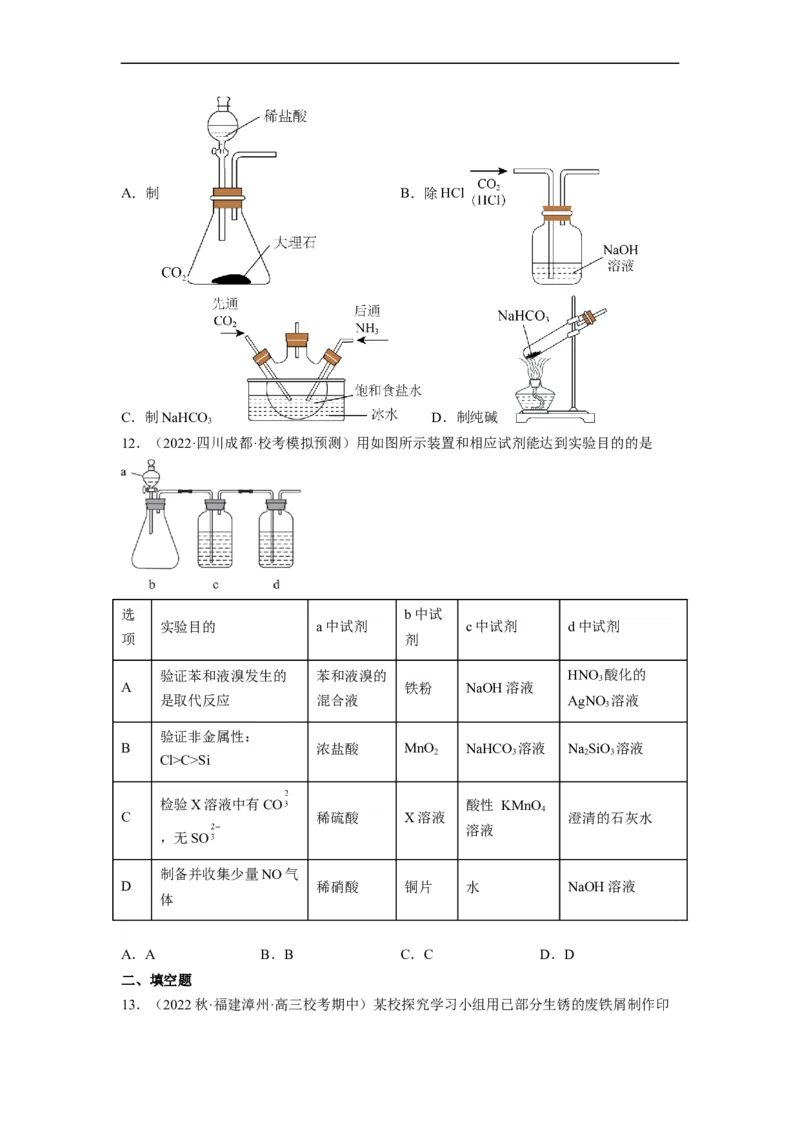
11.(2023秋·江苏南通·高三统考期末)实验小组用如下图所示装置制取纯碱,其中能达
到实验目的的是A.制 B.除HCl
C.制NaHCO D.制纯碱
3
12.(2022·四川成都·校考模拟预测)用如图所示装置和相应试剂能达到实验目的的是
选 b中试
实验目的 a中试剂 c中试剂 d中试剂
项 剂
验证苯和液溴发生的 苯和液溴的 HNO 酸化的
3
A 铁粉 NaOH溶液
是取代反应 混合液 AgNO 溶液
3
验证非金属性:
B 浓盐酸 MnO NaHCO 溶液 NaSiO 溶液
2 3 2 3
Cl>C>Si
检验X溶液中有CO 酸性 KMnO
4
C 稀硫酸 X溶液 澄清的石灰水
溶液
,无SO
制备并收集少量NO气
D 稀硝酸 铜片 水 NaOH溶液
体
A.A B.B C.C D.D
二、填空题
13.(2022秋·福建漳州·高三校考期中)某校探究学习小组用已部分生锈的废铁屑制作印刷电路板的腐蚀剂,并回收铜。探究过程如图所示:
请回答下列问题:
(1)步骤①中先加入热的Na2CO3溶液除油污,操作甲的名称是________。
(2)步骤②中,除发生反应Fe+2HCl===FeCl2+H2↑外,其他可能反应的离子方程式为
_______________________________________________________。
(3)溶液C的颜色是________,溶液D中可能含有的金属阳离子有_______________。
(4)可以验证溶液B中是否含有Fe2+的一种试剂是______(填选项序号)。
a.稀硫酸 b.铁c.硫氰化钾 d.酸性高锰酸钾溶液
(5)操作乙的名称是________,步骤⑤产生金属铜的化学方程式为
_______________________________________________________________________。
14.(2022·全国·高三专题练习)甲、乙组同学分别做了以下探究实验。
(1)甲组探究Cl 与NaSO 溶液反应,实验装置如下。
2 2 3
①写出制取氯气的化学方程式______________。
②该装置的不足之处除无尾气吸收装置外,另一处是______________。
③Cl 与NaSO 溶液反应的离子方程式为____________。
2 2 3
④设计实验,简述实验步骤,证明洗气瓶中的NaSO 已被氧化_________。
2 3
(2)乙组探究乙酸乙酯在不同温度、不同浓度NaOH 溶液中的水解速率。取四只大小相
同的试管,在试管外壁贴上体积刻度纸,按下表进行对照实验。在两种不同温度的水浴中加
热相同时间后,记录酯层的体积来确定水解反应的速率
试管
实验试剂 试管I 试管II 试管IV
Ⅲ乙酸乙酯/mL 1 V V V
1 2 3
1mol/L NaOH/ mL V4 3 0 V
5
蒸馏水/mL 0 V 5 2
6
⑤请完成上表,其中V=______,V=______,V=_______。
2 4 5
⑥实验中,可用饱和食盐水替代蒸馏水,以减小乙酸乙酯在水中的溶解度,使实验结果更准确;
但不能用饱和NaCO 溶液替代蒸馏水,其原因是____ ;实验中,试管IV比试管II中的酯层
2 3
减少更快,其原因有:温度高速率快,还可能有_________。 (乙酸乙酯沸点 为77.1℃)