文档内容
选择题标准练(三)
(选择题1~10题,每小题3分,11~15题,每小题4分,共50分)
1.生活中处处有化学。下列说法正确的是( )
A.矿泉水瓶的主要成分为无机非金属材料
B.向牛奶中加入果汁,会发生酸碱中和反应而产生沉淀
C.酿酒时加入的酒曲与面包中用到的发酵粉作用相同
D.生铁比纯铁更易生锈
2.下列化学用语的表达正确的是( )
A.基态铍原子最外层电子的电子云轮廓图:
B.CH COOH的质谱图:
3
C. 的系统命名为2,2⁃ 二甲基丁烷
D.基态N原子核外电子的轨道表示式为
3.实验安全及操作规范至关重要。下列叙述不正确的是( )
A.磷化钙、磷化铝等金属磷化物应放在干燥容器中保存,并贴上红色标签
B.启普发生器是简易制气装置,但实验室制备乙炔时不可使用启普发生器
C.在实验室做有机实验时若突发有机溶剂着火,则应迅速用大量水灭火
D.用滴定管量取20.00 mL酸性高锰酸钾溶液时应选用酸式滴定管
4.N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.标准状况下,11.2 L CH Cl中所含C—H数目为1.5N
3 A
B.1 mol重水比1 mol水多2N 个质子
A
C.0.1 mol24Mg2+中含有的电子数为1.2N
A
D.1 mol CaH 和1 mol CaO 晶体中所含离子数目均为3N
2 2 A
5.两种试剂相互滴加时,滴加的顺序不同,产生的现象可能不同。下列试剂相互滴加时,滴加的顺序不同
但产生的现象相同的是( )
A.H PO 溶液与澄清石灰水
3 4B.Na S溶液与FeCl 溶液
2 3
C.Na[Al(OH) ]溶液与盐酸
4
D.NaHCO 溶液与NaHSO 溶液
3 4
6.“香城”咸宁因满城桂花而闻名,每到金秋时节,有风香十里,无风十里香。芳樟醇是桂花致香原因之
一,其结构如图,下列有关芳樟醇的说法不正确的是( )
A.分子式为C H O
10 18
B.不存在顺反异构
C.能发生取代、加聚、氧化、消去反应
D.与Br 的CCl 溶液反应可能得到2种加成产物(不考虑立体异构)
2 4
7.下列反应方程式书写正确的是( )
A.铅酸蓄电池充电时阴极的电极反应式:PbO +2e-+4H++SO2- ===PbSO +2H O
2 4 4 2
B.密闭容器中,1 g H (g)与足量的I (g)混合反应后生成HI(g),放出a kJ热量(a>0):H (g)+I (g) 2HI(g)
2 2 2 2
ΔH<-2a kJ·mol-1
C.Cu
O溶于稀硝酸得到蓝色溶液:3Cu++NO-
+4H+===3Cu2++NO↑+2H O
2 3 2
D.Al O 溶于(NH ) SO 溶液:Al O +6N H+ ===2Al3++6NH ↑+3H O
2 3 4 2 4 2 3 4 3 2
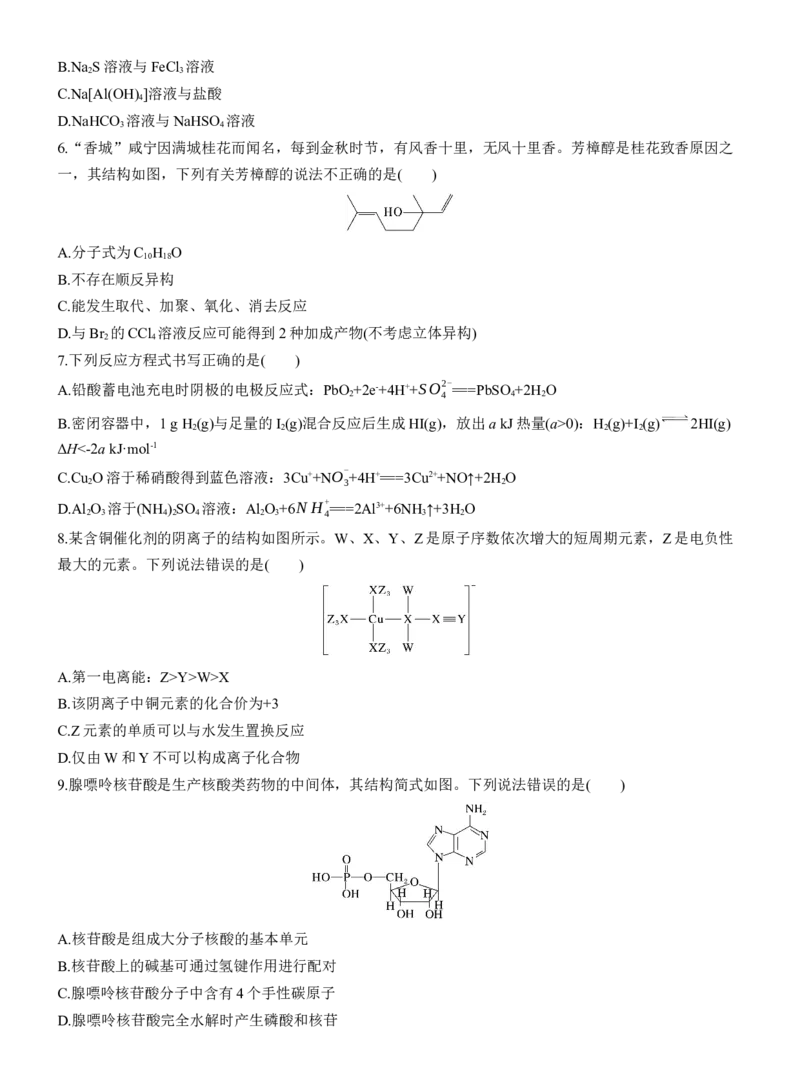
8.某含铜催化剂的阴离子的结构如图所示。W、X、Y、Z是原子序数依次增大的短周期元素,Z是电负性
最大的元素。下列说法错误的是( )
A.第一电离能:Z>Y>W>X
B.该阴离子中铜元素的化合价为+3
C.Z元素的单质可以与水发生置换反应
D.仅由W和Y不可以构成离子化合物
9.腺嘌呤核苷酸是生产核酸类药物的中间体,其结构简式如图。下列说法错误的是( )
A.核苷酸是组成大分子核酸的基本单元
B.核苷酸上的碱基可通过氢键作用进行配对
C.腺嘌呤核苷酸分子中含有4个手性碳原子
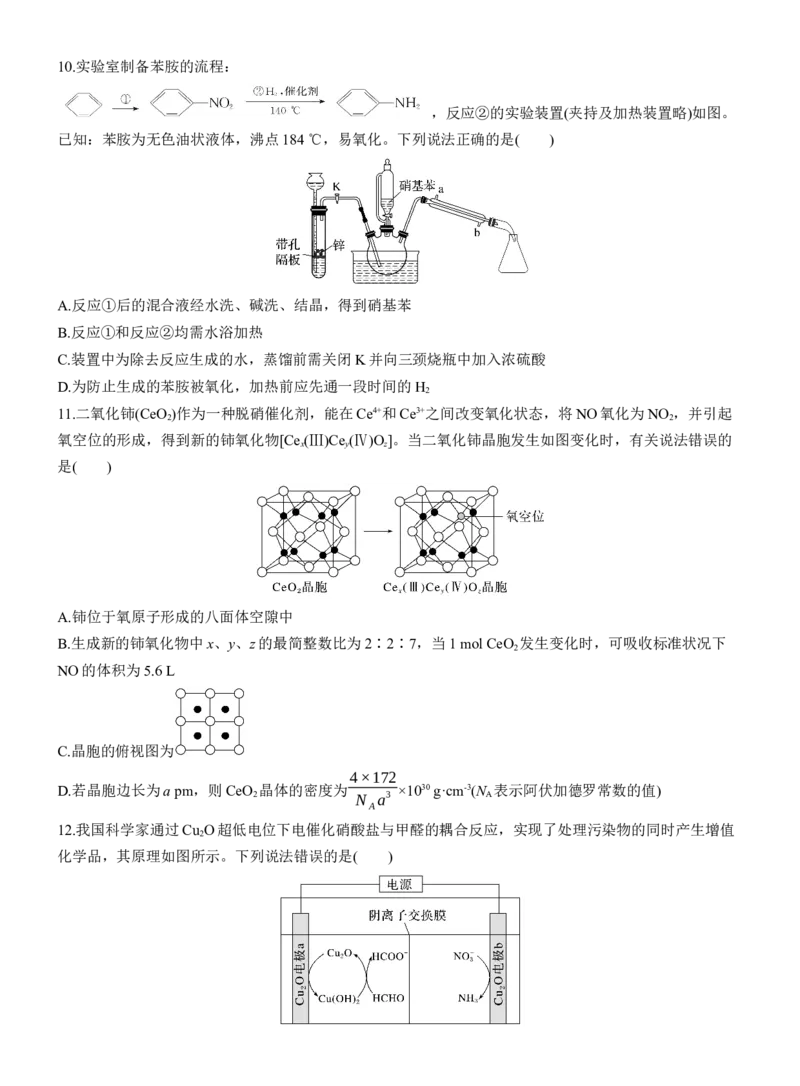
D.腺嘌呤核苷酸完全水解时产生磷酸和核苷10.实验室制备苯胺的流程:
,反应②的实验装置(夹持及加热装置略)如图。
已知:苯胺为无色油状液体,沸点184 ℃,易氧化。下列说法正确的是( )
A.反应①后的混合液经水洗、碱洗、结晶,得到硝基苯
B.反应①和反应②均需水浴加热
C.装置中为除去反应生成的水,蒸馏前需关闭K并向三颈烧瓶中加入浓硫酸
D.为防止生成的苯胺被氧化,加热前应先通一段时间的H
2
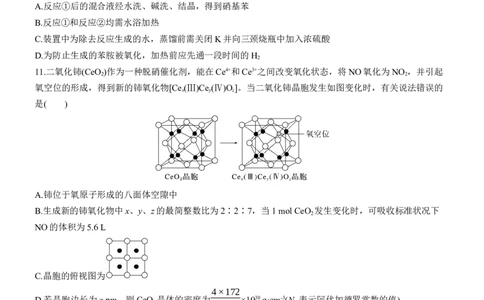
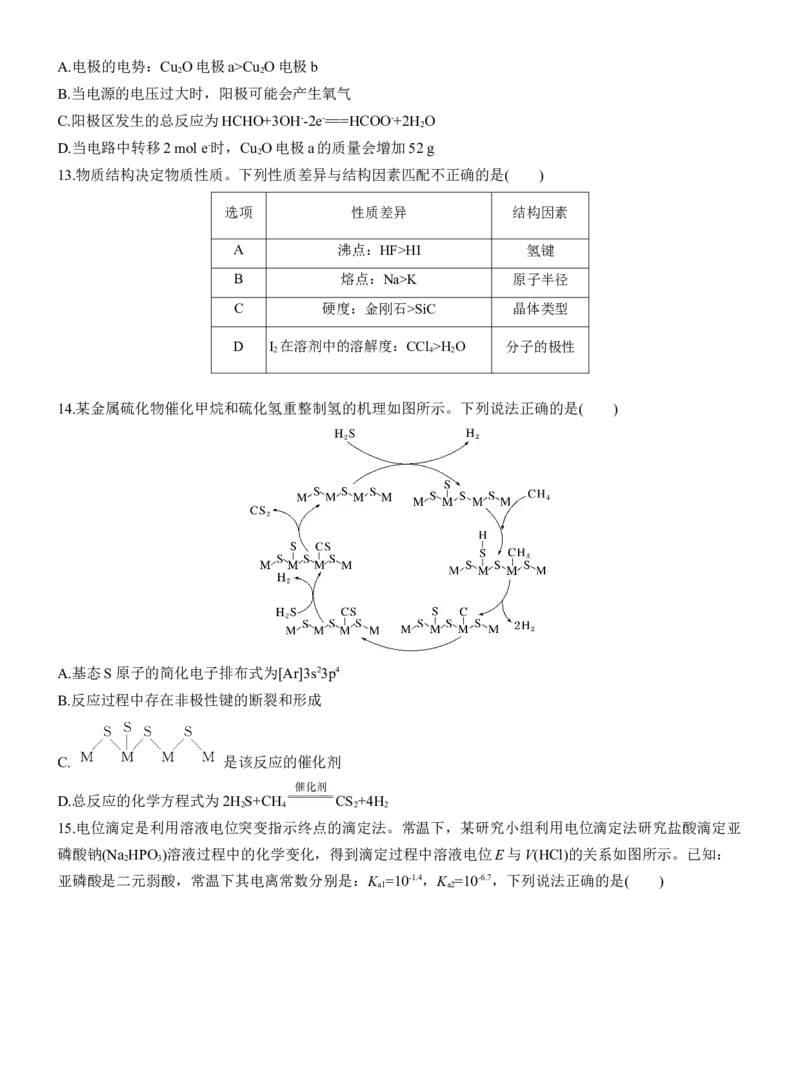
11.二氧化铈(CeO )作为一种脱硝催化剂,能在Ce4+和Ce3+之间改变氧化状态,将NO氧化为NO ,并引起
2 2
氧空位的形成,得到新的铈氧化物[Ce(Ⅲ)Ce(Ⅳ)O]。当二氧化铈晶胞发生如图变化时,有关说法错误的
x y z
是( )
A.铈位于氧原子形成的八面体空隙中
B.生成新的铈氧化物中x、y、z的最简整数比为2∶2∶7,当1 mol CeO 发生变化时,可吸收标准状况下
2
NO的体积为5.6 L
C.晶胞的俯视图为
4×172
D.若晶胞边长为a pm,则CeO 晶体的密度为 ×1030 g·cm-3(N 表示阿伏加德罗常数的值)
2 N a3 A
A
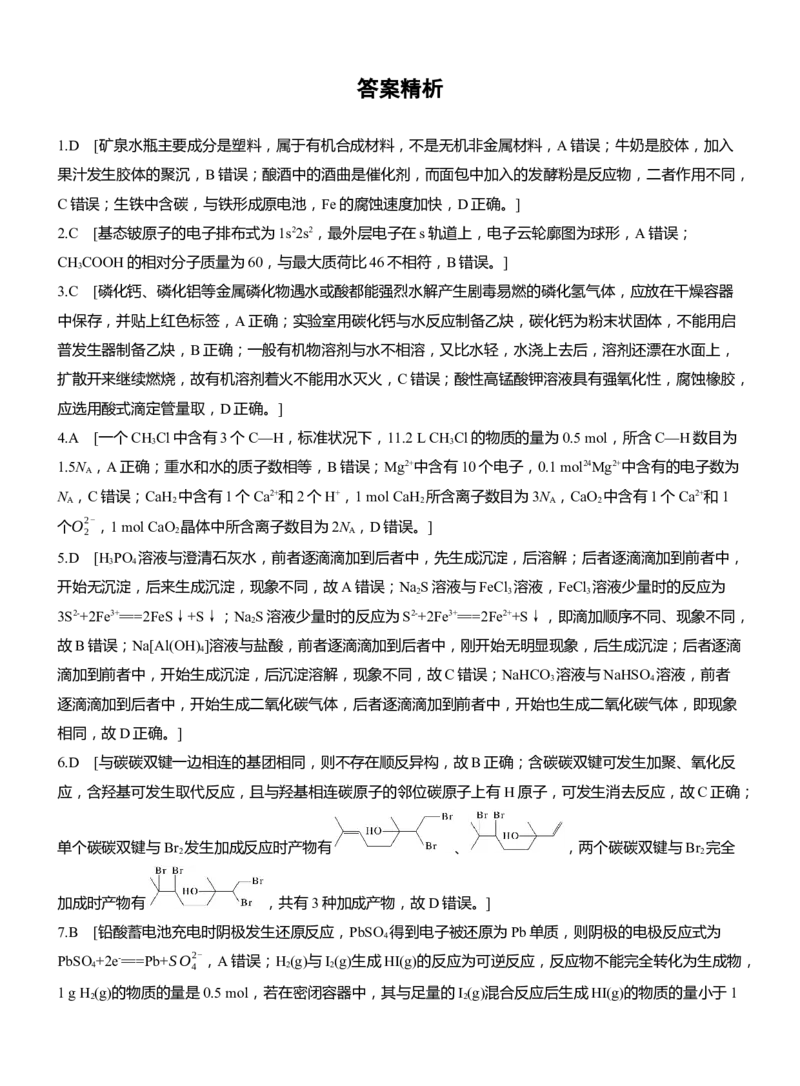
12.我国科学家通过Cu O超低电位下电催化硝酸盐与甲醛的耦合反应,实现了处理污染物的同时产生增值
2
化学品,其原理如图所示。下列说法错误的是( )A.电极的电势:Cu O电极a>Cu O电极b
2 2
B.当电源的电压过大时,阳极可能会产生氧气
C.阳极区发生的总反应为HCHO+3OH--2e-===HCOO-+2H O
2
D.当电路中转移2 mol e-时,Cu O电极a的质量会增加52 g
2
13.物质结构决定物质性质。下列性质差异与结构因素匹配不正确的是( )
选项 性质差异 结构因素
A 沸点:HF>HI 氢键
B 熔点:Na>K 原子半径
C 硬度:金刚石>SiC 晶体类型
D I 在溶剂中的溶解度:CCl >H O 分子的极性
2 4 2
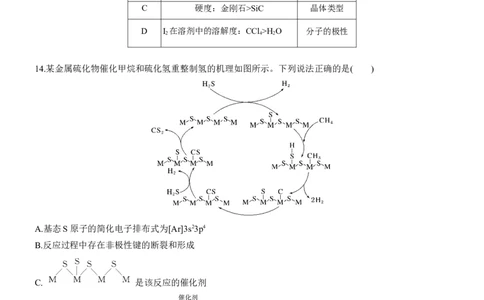
14.某金属硫化物催化甲烷和硫化氢重整制氢的机理如图所示。下列说法正确的是( )
A.基态S原子的简化电子排布式为[Ar]3s23p4
B.反应过程中存在非极性键的断裂和形成
C. 是该反应的催化剂
D.总反应的化学方程式为2H S+CH CS +4H
2 4 2 2
15.电位滴定是利用溶液电位突变指示终点的滴定法。常温下,某研究小组利用电位滴定法研究盐酸滴定亚
磷酸钠(Na HPO )溶液过程中的化学变化,得到滴定过程中溶液电位E与V(HCl)的关系如图所示。已知:
2 3
亚磷酸是二元弱酸,常温下其电离常数分别是:K =10-1.4,K =10-6.7,下列说法正确的是( )
a1 a2A.水的电离程度:a>b>d>c
B.b点对应溶液的pH>7
C.第二滴定终点时发生反应的平衡常数为K=108.1
D.c点对应溶液中一定存在:c(H+)-c(OH-)0),则若1 mol H (g)完全与I (g)生成HI(g),反应放出的热量大于2a kJ,反应放出
2 2
的热量越多,则该反应的反应热就越小,所以该反应的热化学方程式为H (g)+I (g) 2HI(g) ΔH<-2a
2 2
kJ·mol-1,B正确;Al O 是两性氧化物,只能与强酸、强碱反应,(NH ) SO 是强酸弱碱盐,水解使溶液显
2 3 4 2 4
酸性,但由于盐水解程度是微弱的,因此盐溶液酸性比较弱,与Al O 不能发生反应,所以Al O 难溶于
2 3 2 3
(NH ) SO 溶液,D错误。]
4 2 4
8.D [分析可知,W为H元素、X为C元素、Y为N元素、Z为F元素;同周期主族元素随原子序数增大
第一电离能呈增大趋势,但第ⅡA、ⅤA族第一电离能大于同周期相邻元素,则第一电离能:
F>N>H>C,故A正确;与Cu形成配位键的4个基团均为-1价基团,整个阴离子表现-1价,则Cu元素表
现+3价,故B正确;Z为F元素,单质F 与水反应生成HF和O ,发生置换反应,故C正确;仅由H和N
2 2
可以构成离子化合物NH H,故D错误。]
4
9.D [核苷酸通过磷酯键形成核酸,因此核苷酸是组成大分子核酸的基本单元,故A正确;DNA分子呈双
螺旋结构,两条链上的碱基通过氢键作用,实现碱基互补配对,故B正确;腺嘌呤核苷酸中的手性碳原子
如图所示 (标*),腺嘌呤核苷酸分子中含有4个手性碳原子,故C正确;腺嘌呤核
苷酸完全水解时产生磷酸、五碳糖和腺嘌呤,故D错误。]
10.D [反应①后的混合液中含有硝基苯和未反应完的苯,经水洗、碱洗、分液后再蒸馏,得到硝基苯,A
错误;反应②的实验温度控制在140 ℃,大于100 ℃,不能用水浴加热,B错误;苯胺还原性强,易被氧
化,有碱性,与酸反应生成盐,而浓硫酸具有酸性和强氧化性,苯胺能与浓硫酸反应,则不能选用浓硫酸,
三颈烧瓶内的反应结束后,关闭K,先在三颈烧瓶中加入生石灰后蒸馏,C错误;加热前应先通一段时间
的H ,可将装置内空气排出,避免苯胺被氧化,D正确。]
2
11.A [铈位于氧原子形成的立方体空隙中,A错误;当1 mol CeO 发生变化时,有0.5 mol Ce元素的化合
2
价由+4价变为+3价,N元素化合价由+2价NO变为+4价NO ,根据化合价升降总数相等,可知关系式为
2
0.5mol
2CeO ~NO,可吸收的NO的物质的量为n(NO)= =0.25 mol,因此可吸收标准状况下NO的体积为
2 2
1 1
0.25 mol×22.4 L·mol-1=5.6 L,B正确;根据晶胞结构可知:在CeO 晶胞中含有Ce原子数为8× +6× =4;
2 8 2
含有的O原子数为8,因此一个晶胞中含有4个CeO ,由于晶胞边长为a pm,则该晶体的密度为
2
4×(140+16×2) 4×172
g·cm-3= ×1030 g·cm-3,D正确。]
N (a×10-10 ) 3 N a3
A A
12.D [如图所示,电极b上硝酸根离子还原为氨气,发生还原反应,b为阴极,a电极Cu O氧化为
2
Cu(OH) ,发生氧化反应,a为阳极,故电极的电势:Cu O电极a>Cu O电极b,A正确;当电源的电压过
2 2 2
大时,阳极区氢氧根离子可能会放电,会产生氧气,B正确;阳极上a电极Cu O氧化为Cu(OH) ,生成的
2 2Cu(OH) 与甲醛反应生成甲酸根离子(碱性环境)和Cu O,故阳极区发生的总反应为HCHO+3OH--2e-
2 2
===HCOO-+2H O,C正确;当电路中转移2 mol e-时,Cu O先转化为Cu(OH) ,Cu(OH) 与甲醛反应又生
2 2 2 2
成Cu O,则电极a的质量不变,D错误。]
2
13.C [分子晶体的沸点由分子间作用力决定,HF能形成分子间氢键,因此HF的沸点比HI高,故A正确;
Na、K均为第ⅠA族元素,K的原子半径更大,金属键强度小于Na,因此熔点Na>K,故B正确;金刚石
和SiC都是共价晶体,金刚石中的C—C比SiC中的Si—C短,前者键能更大,因此金刚石硬度比SiC大,
故C错误;I 为非极性分子,CCl 为非极性分子,H O为极性分子,根据相似相溶原理,碘单质在四氯化
2 4 2
碳中的溶解度比在水中的溶解度大,故D正确。]
14.D [S的原子序数为16,基态S原子的简化电子排布式为[Ne]3s23p4,故A错误;反应过程中生成了氢
气,即存在非极性键的形成,但不存在非极性键的断裂,故B错误;由环式机理图可知
先消耗,后生成,所以是该反应的催化剂,故C错误;由转化机理图可知,某金属硫
化物催化甲烷和硫化氢重整制氢的总反应的化学方程式为2H S+CH CS +4H ,故D正确。]
2 4 2 2
15.D [滴定过程中先发生的反应:Na HPO +HCl===NaH PO +NaCl,所以第一次达到滴定终点时溶液的主
2 3 2 3
要成分为NaH PO 和NaCl,后发生的反应:NaH PO +HCl===H PO +NaCl,所以第二次达到滴定终点时溶
2 3 2 3 3 3
液的主要成分为H PO 和NaCl,据此分析。盐酸对水的电离起抑制作用,越加盐酸抑制作用越大,水的电
3 3
离程度越小,所以水的电离程度:a>b>c>d,故A错误; b点是第一次达到滴定终点时,溶液的主要成分
K 10-14
为NaH PO 和NaCl,其中H
PO-
的电离常数K =10-6.7,水解常数K =
w
= =10-12.6,可见电离程度大
2 3 2 3 a2 h2 K 10-1.4
a1
于水解程度,溶液显酸性,对应溶液的pH<7,故B错误;第二滴定终点时发生反应H
PO-
+H+ H PO
2 3 3 3
1 1
的平衡常数为K= =
=101.4,故C错误;c点溶液中存在电荷守恒2c(HPO2-
)+c(H
PO-
)+c(OH-)
K 10-1.4 3 2 3
a1
+c(Cl-)=c(Na+)+c(H+),所以有c(H+)-c(OH-)=2c(HPO2-
)+c(H
PO-
)+c(Cl-)-c(Na+),此时c(Cl-)