文档内容
重难点 05 氧化还原反应的概念、规律、配平及计算
►命题趋势►解题策略►真题回眸►限时检测
考向一 是否为氧化还原反应的判断
考向二 氧化还原反应的相关概念
氧化还原反应的概念、规律、配平及计算 考向三 氧化还原反应的性质规律
考向四 氧化还原反应的配平
考向五 氧化还原反应的计算
氧化还原反应是高考的必考内容,从考查内容上看:
(1)借助STSE型试题判断指定反应是否是氧化还原反应、氧化还原反应中电子的转移数目在 N 题
A
目中是命题的热点;
(2)物质氧化性、还原性的强弱常与离子方程式正误判断融合考查;
(3)在工艺流程题中常常涉及陌生氧化还原方程式的书写。
预测2024年高考仍可能在选择题中结合生产、生活,考查氧化还原反应的判断、氧化还原反应的概
念及相互关系、简单计算等,应予以关注。
【策略1】理顺氧化还原反应的基本概念及相互关系
概括为“升失氧、降得还,剂性一致、其他相反”。
【策略2】掌握氧化还原反应电子转移的表示方法
(1)双线桥法:①标变价、②画箭头(反应物指向生成物)、③算数目、④说变化。
。
(2)单线桥法:箭头由失电子原子指向得电子原子,线桥上只标电子转移的数目,不标“得”“失”字
样。。
【策略3】掌握氧化还原反应的基本规律
元素处于最高价,只有氧化性(如KMnO 中的Mn);
4
价态律 元素处于最低价,只有还原性(如S2-、I-);
元素处于中间价态,既有氧化性,又有还原性(如Fe2+、S、Cl 等)
2
氧化性:氧化剂>氧化产物;
还原性:还原剂>还原产物。
强弱律
在适宜的条件下,用氧化性(还原性)较强的物质可制备氧化性(还原性)较弱的物质,用
于比较物质的氧化性或还原性的强弱;
①同时含有几种还原剂时将按照还原性由强到弱的顺序依次反应。如:在 FeBr 溶液
2
中通入少量Cl 时,因为还原性:Fe2+>Br-,所以Fe2+先与Cl 反应。
2 2
②同时含有几种氧化剂时将按照氧化性由强到弱的顺序依次反应。如:在含有 Fe3+、
Cu2+、H+的溶液中加入铁粉,因为氧化性:Fe3+>Cu2+>H+,所以铁粉先与Fe3+反
优先律
应,然后再依次与Cu2+、H+反应。
③常见的强弱顺序
氧化性:MnO(H+)>Cl >Br >Fe3+>I >稀HSO >S,
2 2 2 2 4
还原性:Mn2+6.7
C.加入 生成 ,说明
D.“沉铬”过程中,增大溶液的pH,沉铬率提高
12.(2023·江西·校联考模拟预测)高铁酸钠(Na FeO)是一种绿色净水剂。
2 4
①实验室制备原理是 ;
②在酸性介质中高铁酸钠不稳定,发生反应: ,在碱性介质中能稳定
存在;
③已知氧化剂的电势是衡量其氧化性强度的主要参数,电势越高,对应条件下氧化剂的氧化性越强,酸性
条件下,电势:FeO >Cl。
2
下列叙述错误的是
A.配制NaFeO 溶液时添加少量NaOH溶液
2 4
B.由反应①知,氧化性:NaClO>Na FeO
2 4C.由反应②知,产生11.2LO 时转移2mol电子
2
D.向NaFeO 溶液中滴加浓盐酸产生的气体不只一种
2 4
13.(2022·浙江·校联考二模)关于反应 ,下列说法
不正确的是
A. 既是氧化剂又是还原剂
B. 发生还原反应
C.若有 加反应,被 还原的 为
D.反应若生成 ,转移 电子
14.(2023·河南·校联考一模)化石燃料燃烧会产生大气污染物 、 等,科学家实验探究用硫酸铈
循环法吸收 ,其转化原理如图所示,下列说法正确的是
A.检验 可以选用盐酸酸化的 溶液
B.反应①的离子方程式为
C.反应②中氧化剂与氧化产物的物质的量之比为1:2
D.理论上每吸收标准状况下 ,一定消耗
15.(2022·云南保山·统考一模)4.35g铜镁合金完全溶于一定浓度的硝酸,产生4480mL的 和
1120mL的NO气体(标准状况下),反应后的溶液中加入足量氢氧化钠溶液,生成的沉淀最大质量为
A.20.60g B.10.30g C.15.50g D.31.00g
16.(2023上·北京·高三校考模拟)完成下列问题。
(1)将 通入0.5mol/L 溶液中,一段时间后,试管中液面与空气接触部分出现红棕色气体。写出
与 反应的离子方程式 。
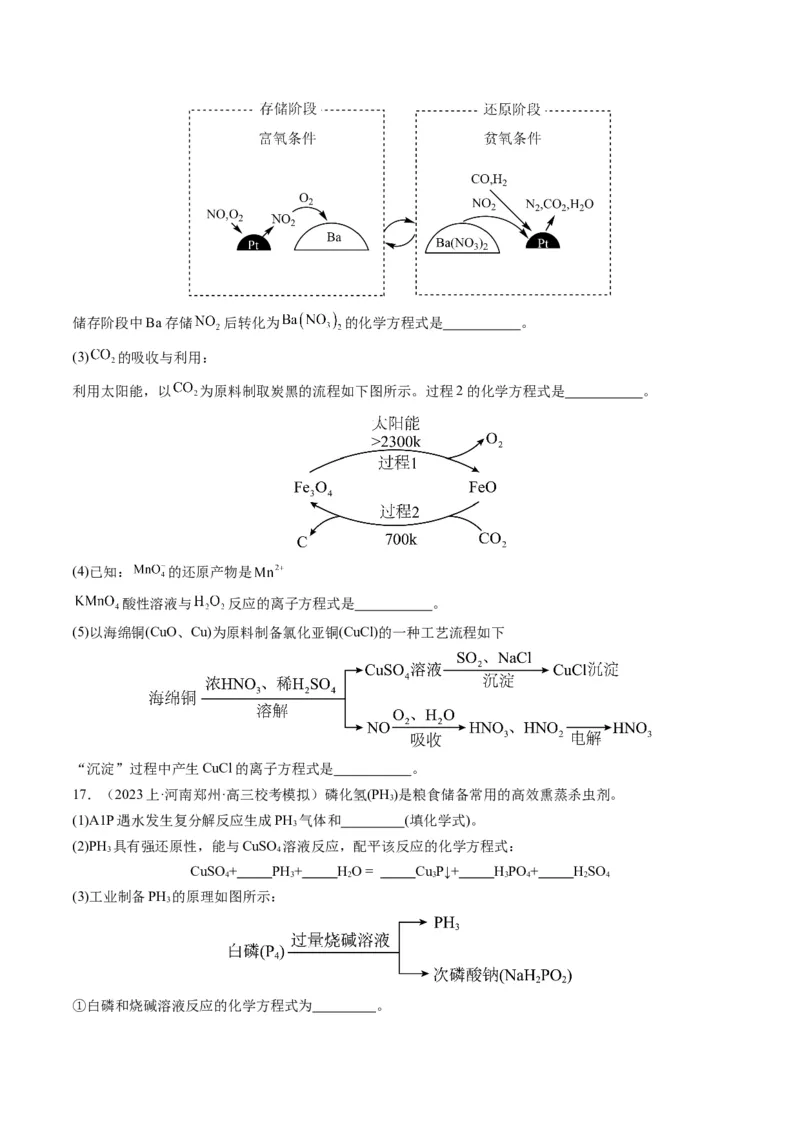
(2)NSR( 的储存和还原在不同时段交替进行)技术可有效降低稀燃柴油和汽油发动机尾气中 的排放,
其工作原理如下图。储存阶段中Ba存储 后转化为 的化学方程式是 。
(3) 的吸收与利用:
利用太阳能,以 为原料制取炭黑的流程如下图所示。过程2的化学方程式是 。
(4)已知: 的还原产物是
酸性溶液与 反应的离子方程式是 。
(5)以海绵铜(CuO、Cu)为原料制备氯化亚铜(CuCl)的一种工艺流程如下
“沉淀”过程中产生CuCl的离子方程式是 。
17.(2023上·河南郑州·高三校考模拟)磷化氢(PH )是粮食储备常用的高效熏蒸杀虫剂。
3
(1)A1P遇水发生复分解反应生成PH 气体和 (填化学式)。
3
(2)PH 具有强还原性,能与CuSO 溶液反应,配平该反应的化学方程式:
3 4
CuSO + PH + HO = Cu P↓+ HPO + HSO
4 3 2 3 3 4 2 4
(3)工业制备PH 的原理如图所示:
3
①白磷和烧碱溶液反应的化学方程式为 。②从分类来看,NaH PO 属于 。
2 2
A.正盐 B.酸式盐 C.强电解质 D.弱电解质
③NaH PO 可将溶液中的Ag+还原为银,从而用于化学镀银。已知利用此原理进行化学镀银时氧化剂与还
2 2
原剂的物质的量之比为4∶1,则氧化产物为 (填化学式)。
18.(2023上·山西吕梁·高三校考模拟)氧化还原反应在工业生产、环保及科研中有广泛的应用。请根据
以下信息,结合所掌握的化学知识,回答下列问题:
Ⅰ.可以用智利硝石提取硝酸钠后的母液为原料,加入亚硫酸氢钠制取琪,相关反应如下:
___ ___ ___ ___ ____ (未配平)
(1)配平上述化学方程式,用单线桥标出电子转移的方向和数目。
Ⅱ.钒性能优良,用途广泛,有金属“维生素”之称。
(2) 能与盐酸反应生成 和一种黄绿色气体,该黄绿色气体能与 溶液反应而被吸收,则
、 、 的还原性由强到弱的顺序是 。
(3) 在碳高温还原时,在氮气气氛下氮化还原制备VN,还生成一种具有还原性的气体,则该反应的化
学方程式为 。