文档内容
西工大附中 2022-2023 学年上学期 1 月期末
高三化学
一、选择题;本题共16小题,每小题3分,共48分
1.用于飞机制造业的材料需要满足密度低强度大的特点,具有该性质的材料是 (
)
A.钠钾合金 B.镁铝合金 C.纯铝 D.黄铜
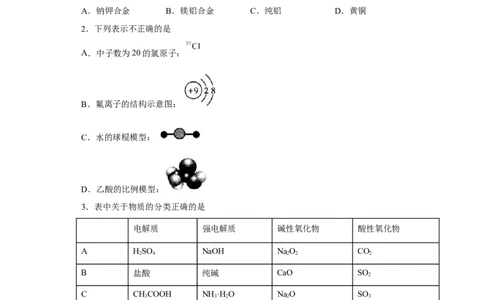
2.下列表示不正确的是
A.中子数为20的氯原子:
B.氟离子的结构示意图:
C.水的球棍模型:
D.乙酸的比例模型:
3.表中关于物质的分类正确的是
电解质 强电解质 碱性氧化物 酸性氧化物
A HSO NaOH NaO CO
2 4 2 2 2
B 盐酸 纯碱 CaO SO
2
C CHCOOH NH ·H O NaO SO
3 3 2 2 3
D NaHSO Ba(OH) Fe O PO
4 2 2 3 2 5
A.A B.B C.C D.D
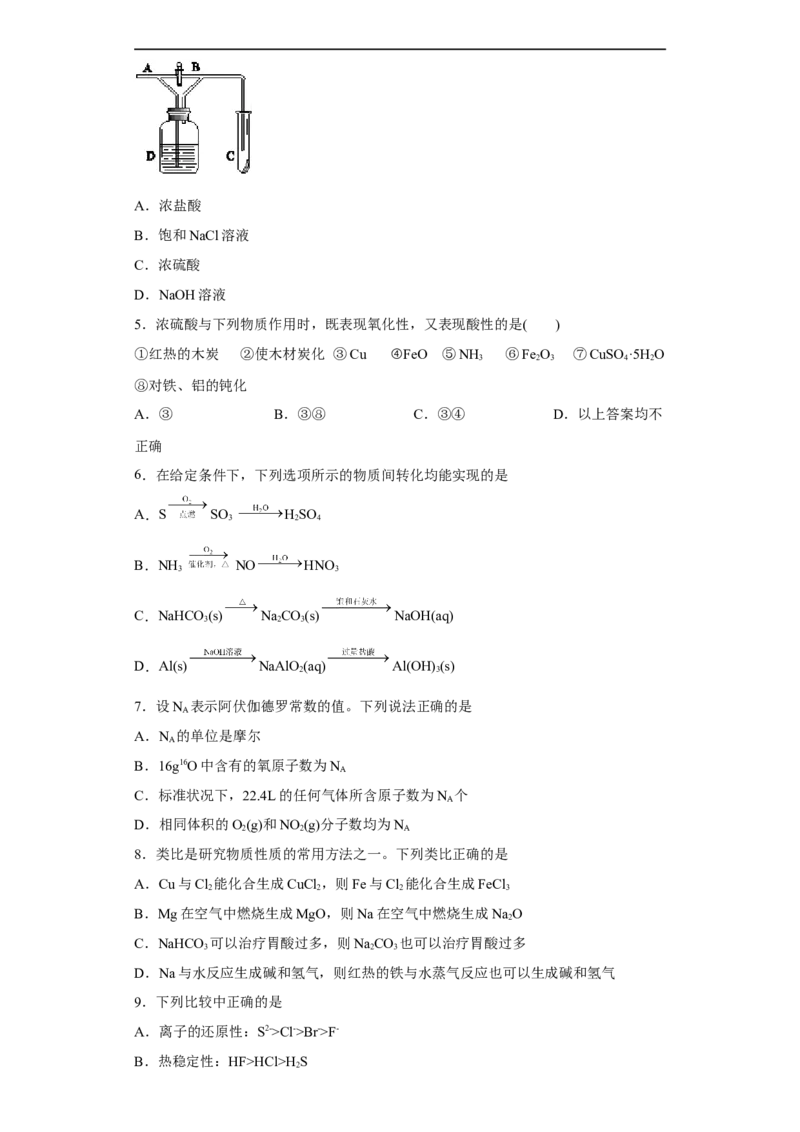
4.如图,A处通入Cl,关闭B阀时,C中的湿润红色布条看不到明显变化;打开B阀后,C
2
中的湿润红色布条逐渐褪色。则D瓶中盛放的是A.浓盐酸
B.饱和NaCl溶液
C.浓硫酸
D.NaOH溶液
5.浓硫酸与下列物质作用时,既表现氧化性,又表现酸性的是( )
①红热的木炭 ②使木材炭化 ③Cu ④FeO ⑤NH ⑥Fe O ⑦CuSO ·5H O
3 2 3 4 2
⑧对铁、铝的钝化
A.③ B.③⑧ C.③④ D.以上答案均不
正确
6.在给定条件下,下列选项所示的物质间转化均能实现的是
A.S SO HSO
3 2 4
B.NH NO HNO
3 3
C.NaHCO (s) NaCO(s) NaOH(aq)
3 2 3
D.Al(s) NaAlO (aq) Al(OH) (s)
2 3
7.设N 表示阿伏伽德罗常数的值。下列说法正确的是
A
A.N 的单位是摩尔
A
B.16g16O中含有的氧原子数为N
A
C.标准状况下,22.4L的任何气体所含原子数为N 个
A
D.相同体积的O(g)和NO (g)分子数均为N
2 2 A
8.类比是研究物质性质的常用方法之一。下列类比正确的是
A.Cu与Cl 能化合生成CuCl ,则Fe与Cl 能化合生成FeCl
2 2 2 3
B.Mg在空气中燃烧生成MgO,则Na在空气中燃烧生成NaO
2
C.NaHCO 可以治疗胃酸过多,则NaCO 也可以治疗胃酸过多
3 2 3
D.Na与水反应生成碱和氢气,则红热的铁与水蒸气反应也可以生成碱和氢气
9.下列比较中正确的是
A.离子的还原性:S2->Cl->Br->F-
B.热稳定性:HF>HCl>H S
2C.酸性:HClO>HSO >H PO
2 4 3 4
D.碱性:Al(OH) >Mg(OH) >Ca(OH)
3 2 2
10.能正确表示下列变化的离子方程式是
A.NH Al(SO ) 溶液与过量Ba(OH) 溶液反应:
4 4 2 2
B.SO 通入酸性KMnO 溶液中:
2 4
C.0.1 mol·L-1 AgNO 溶液中加入过量浓氨水:
3
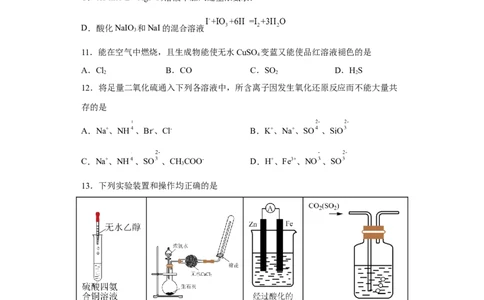
D.酸化NaIO 和NaI的混合溶液
3
11.能在空气中燃烧,且生成物能使无水CuSO 变蓝又能使品红溶液褪色的是
4
A.Cl B.CO C.SO D.HS
2 2 2
12.将足量二氧化硫通入下列各溶液中,所含离子因发生氧化还原反应而不能大量共
存的是
A.Na+、NH 、Br-、Cl- B.K+、Na+、SO 、SiO
C.Na+、NH 、SO 、CHCOO- D.H+、Fe3+、NO 、SO
3
13.下列实验装置和操作均正确的是
A.析出
C.牺牲阳极
[Cu(NH )]SO B.制取并收集氨气 D.除去CO 中少量SO
3 4 4 法保护铁 2 2
晶体
A.A B.B C.C D.D
14.已知硫代硫酸钠可作为脱氯剂,25.0 mL 0.100 mol·L-1的NaSO 溶液恰好把224
2 2 3
mL(标准状况下)Cl 转化为Cl-,则SO 将转化为
2 2A.S2- B.S C.SO D.SO
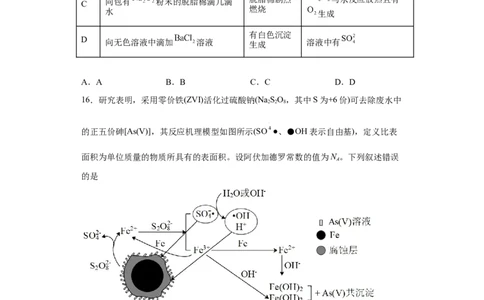
15.下列实验操作、现象及实验结论都正确的是
选
实验操作 现象 实验结论
项
将湿润的有色布条放入充满氯气的
A 布条褪色 氯气具有漂白性
集气瓶中
产生白色沉
B 向 溶液中通入适量 白色沉淀为
淀
向包有 粉末的脱脂棉滴几滴 脱脂棉剧烈 与水反应放热且有
C
水 燃烧 生成
有白色沉淀
D 向无色溶液中滴加 溶液 生成 溶液中有
A.A B.B C.C D.D
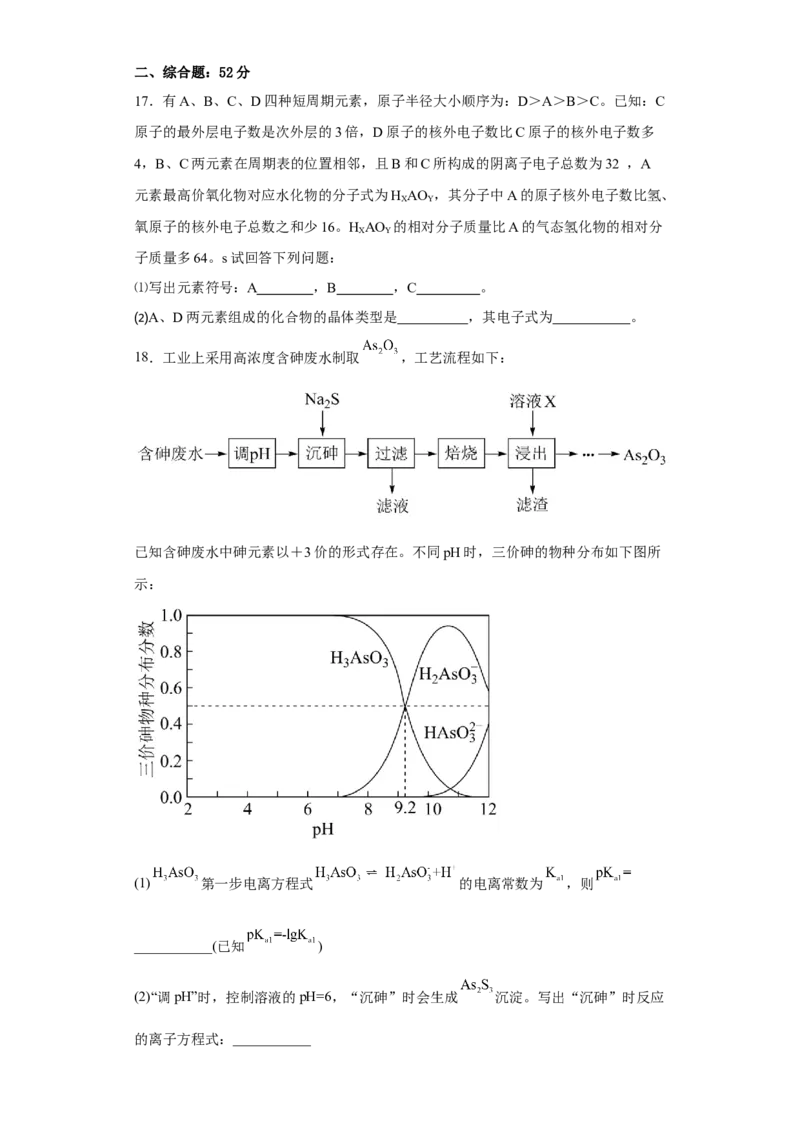
16.研究表明,采用零价铁(ZVI)活化过硫酸钠(Na SO,其中S为+6价)可去除废水中
2 2 8
的正五价砷[As(V)],其反应机理模型如图所示(SO ●、●OH表示自由基),定义比表
面积为单位质量的物质所具有的表面积。设阿伏加德罗常数的值为N 。下列叙述错误
A
的是
A.过硫酸钠中-2价氧与-1价氧的个数比为3:1
B.若56 g Fe参加反应,被还原的SO 小于1.5N 个
2 A
C.碱性条件下硫酸根自由基发生反应的方程式为SO ●+OH-=SO +●OH
D.pH越小,越有利于去除废水中的正五价砷二、综合题:52分
17.有A、B、C、D四种短周期元素,原子半径大小顺序为:D>A>B>C。已知:C
原子的最外层电子数是次外层的3倍,D原子的核外电子数比C原子的核外电子数多
4,B、C两元素在周期表的位置相邻,且B和C所构成的阴离子电子总数为32 ,A
元素最高价氧化物对应水化物的分子式为H AO ,其分子中A的原子核外电子数比氢、
X Y
氧原子的核外电子总数之和少16。H AO 的相对分子质量比A的气态氢化物的相对分
X Y
子质量多64。s试回答下列问题:
⑴写出元素符号:A ,B ,C 。
⑵A、D两元素组成的化合物的晶体类型是 ,其电子式为 。
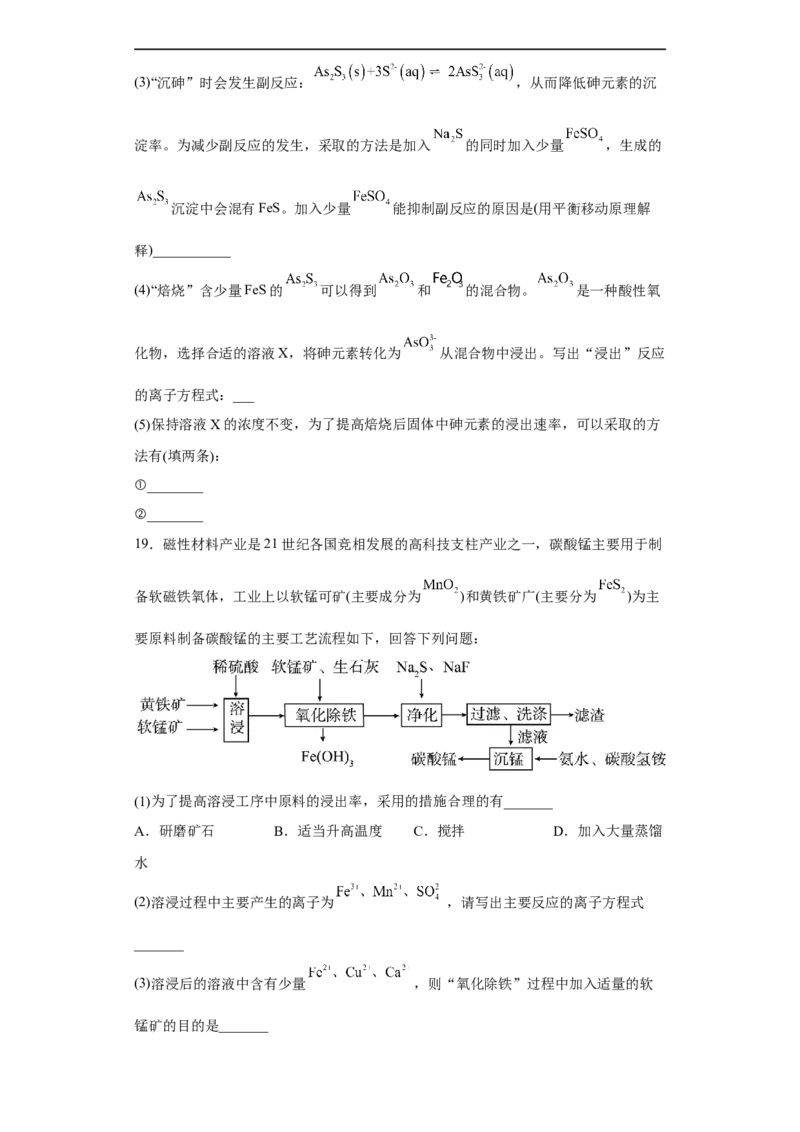
18.工业上采用高浓度含砷废水制取 ,工艺流程如下:
已知含砷废水中砷元素以+3价的形式存在。不同pH时,三价砷的物种分布如下图所
示:
(1) 第一步电离方程式 的电离常数为 ,则
___________(已知 )
(2)“调pH”时,控制溶液的pH=6,“沉砷”时会生成 沉淀。写出“沉砷”时反应
的离子方程式:___________(3)“沉砷”时会发生副反应: ,从而降低砷元素的沉
淀率。为减少副反应的发生,采取的方法是加入 的同时加入少量 ,生成的
沉淀中会混有FeS。加入少量 能抑制副反应的原因是(用平衡移动原理解
释)___________
(4)“焙烧”含少量FeS的 可以得到 和 的混合物。 是一种酸性氧
化物,选择合适的溶液X,将砷元素转化为 从混合物中浸出。写出“浸出”反应
的离子方程式:___
(5)保持溶液X的浓度不变,为了提高焙烧后固体中砷元素的浸出速率,可以采取的方
法有(填两条):
①________
②________
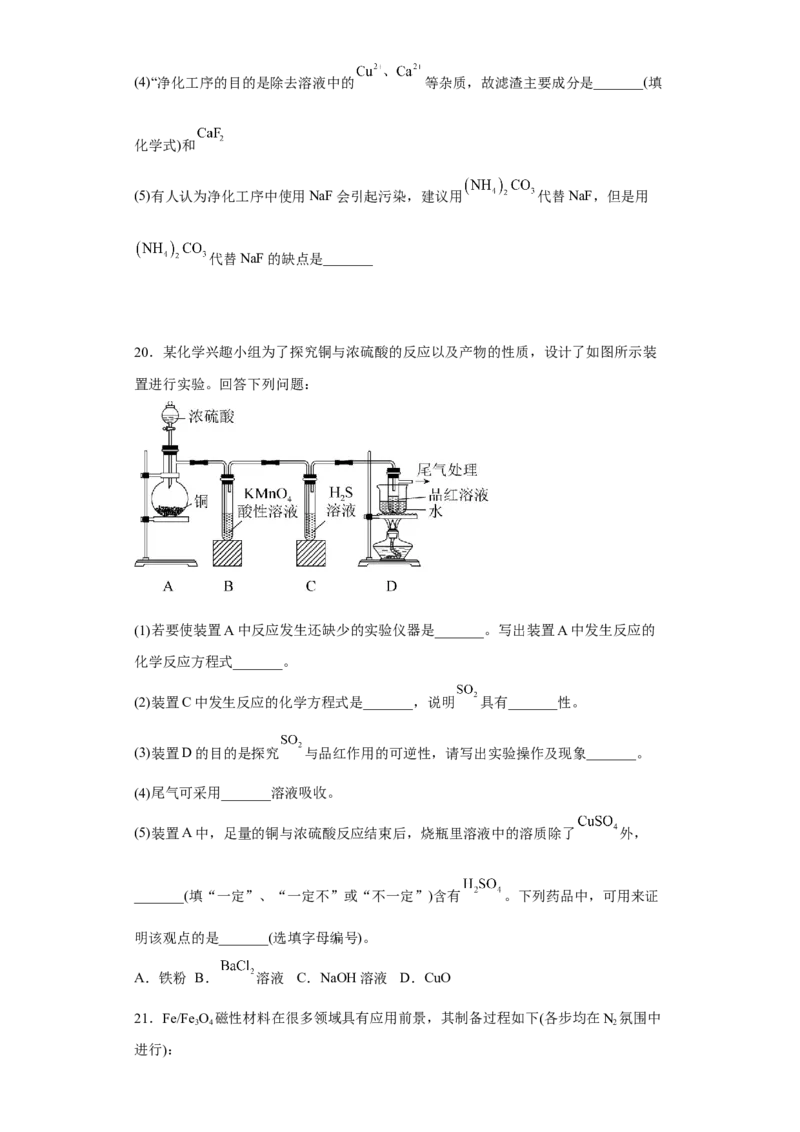
19.磁性材料产业是21世纪各国竞相发展的高科技支柱产业之一,碳酸锰主要用于制
备软磁铁氧体,工业上以软锰可矿(主要成分为 )和黄铁矿广(主要分为 )为主
要原料制备碳酸锰的主要工艺流程如下,回答下列问题:
(1)为了提高溶浸工序中原料的浸出率,采用的措施合理的有_______
A.研磨矿石 B.适当升高温度 C.搅拌 D.加入大量蒸馏
水
(2)溶浸过程中主要产生的离子为 ,请写出主要反应的离子方程式
_______
(3)溶浸后的溶液中含有少量 ,则“氧化除铁”过程中加入适量的软
锰矿的目的是_______(4)“净化工序的目的是除去溶液中的 等杂质,故滤渣主要成分是_______(填
化学式)和
(5)有人认为净化工序中使用NaF会引起污染,建议用 代替NaF,但是用
代替NaF的缺点是_______
20.某化学兴趣小组为了探究铜与浓硫酸的反应以及产物的性质,设计了如图所示装
置进行实验。回答下列问题:
(1)若要使装置A中反应发生还缺少的实验仪器是_______。写出装置A中发生反应的
化学反应方程式_______。
(2)装置C中发生反应的化学方程式是_______,说明 具有_______性。
(3)装置D的目的是探究 与品红作用的可逆性,请写出实验操作及现象_______。
(4)尾气可采用_______溶液吸收。
(5)装置A中,足量的铜与浓硫酸反应结束后,烧瓶里溶液中的溶质除了 外,
_______(填“一定”、“一定不”或“不一定”)含有 。下列药品中,可用来证
明该观点的是_______(选填字母编号)。
A.铁粉 B. 溶液 C.NaOH溶液 D.CuO
21.Fe/Fe O 磁性材料在很多领域具有应用前景,其制备过程如下(各步均在N 氛围中
3 4 2
进行):①称取9.95g FeCl ·4H O(M =199),配成50mL溶液,转移至恒压滴液漏斗中。
2 2 r
②向三颈烧瓶中加入100mL14mol· L-1KOH溶液。
③持续磁力搅拌,将FeCl 溶液以2mL·min-1的速度全部滴入三颈烧瓶中,100°C 下回
2
流3h。
④冷却后过滤,依次用热水和乙醇洗涤所得黑色沉淀,在40°C干燥。
⑤管式炉内焙烧2h,得产品3.24g。
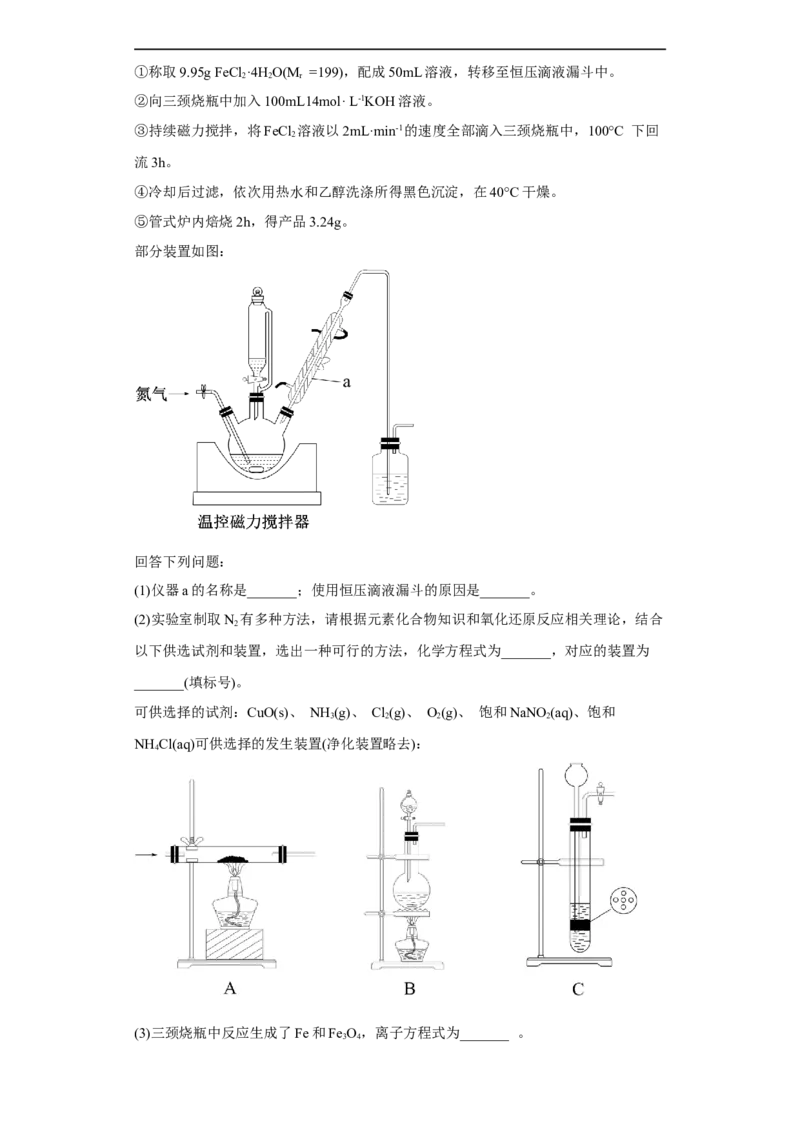
部分装置如图:
回答下列问题:
(1)仪器a的名称是_______;使用恒压滴液漏斗的原因是_______。
(2)实验室制取N 有多种方法,请根据元素化合物知识和氧化还原反应相关理论,结合
2
以下供选试剂和装置,选出一种可行的方法,化学方程式为_______,对应的装置为
_______(填标号)。
可供选择的试剂:CuO(s)、 NH (g)、 Cl(g)、 O(g)、 饱和NaNO (aq)、饱和
3 2 2 2
NH Cl(aq)可供选择的发生装置(净化装置略去):
4
(3)三颈烧瓶中反应生成了Fe和Fe O,离子方程式为_______ 。
3 4(4)为保证产品性能,需使其粒径适中、结晶度良好,可采取的措施有_______。
A.采用适宜的滴液速度
B.用盐酸代替KOH溶液,抑制Fe2+水解
C.在空气氛围中制备
D.选择适宜的焙烧温度
(5)步骤④中判断沉淀是否已经用水洗涤干净,应选择的试剂为_______;
(6)该实验所得磁性材料的产率为_______ (保留 3位有效数字)。参考答案
1.B 2.C 3.D 4.D 5.C 6.C 7.B 8.A 9.B 10.B 11.D 12.D 13.C 14.
D 15.C16.D
17.⑴Cl、N、O⑵离子晶体,
18.(1)9.2
(2)
(3) 与 结合生成FeS沉淀,使副反应的平衡左移
(4)
(5) 升高温度 充分研磨焙烧后的固体、加快搅拌速率等
19.(1)ABC
(2)
(3)使亚铁离子转化为铁离子
(4)CuS
(5)会使Mn2+沉淀进入滤渣,降低MnCO 的产率
3
20.(1) 酒精灯 Cu+2H SO (浓) CuSO +SO↑+2H O
2 4 4 2 2
(2) SO +2H S=3S↓+2H O 氧化
2 2 2
(3)将SO 气体通入品红溶液中,看到品红溶液褪色,待品红溶液褪色后,关闭分液漏斗,
2
点燃酒精灯加热烧杯,品红溶液又会恢复红色
(4)NaOH
(5) 一定 AD
21.(1) 球形冷凝管 保持气压平衡,使液体顺利流下
(2) 2NH +3CuO 3Cu+N +3H O A
3 2 2(3)4Fe2++8OH-=Fe↓+Fe O↓+4H O
3 4 2
(4)AD
(5)稀硝酸、硝酸银溶液
(6)90.0%