文档内容
题型 18 化学反应原理综合
目录
.....................................................................................................................................1
【考向一】热化学方程式及反应热的计算......................................................................................................1
【考向二】有关反应速率、转化率、速率常数的计算..................................................................................5
【考向三】分压平衡常数(Kp)计算...................................................................................................................9
【考向四】平衡图像曲线受温度、压强影响的原因分析............................................................................12
【考向五】平衡图像中最佳反应条件选择的原因分析................................................................................17
【考向六】平衡图像中转化率、产率变化的原因分析................................................................................19
【考向七】电解质溶液中有关电离(水解)平衡常数的计算..........................................................................22
【考向八】溶度积( Ksp)的相关计算..............................................................................................................27
【考向九】电极方程式书写............................................................................................................................31
...................................................................................................................................35
【考向一】热化学方程式及反应热的计算
【典例1】(2023上·上海奉贤)回答下列问题。
(1)①C(s)+O (g)=CO (g) =-437.3kJ/mol
2 2
②H (g)+ O (g)=H O(g) =-285.8 kJ/mol
2 2 2
③CO(g)+ O (g)=CO (g) =-283.0 kJ/mol
2 2
固态碳和水蒸气反应生成CO和H 的热化学方程式为 。
2
(2)根据键能数据估算CH (g)+4F (g)=CF (g)+4HF(g)的反应热 为 。
4 2 4
化学键 C-H C-F H-F F-F键能kJ/mol 414 489 565 155
(3)标准状况下,3.36L仅由C、H元素组成的某气体质量4.5g完全燃烧生成CO (g)和H O(l)时,放出
2 2
233.97kJ的热量。该气体的分子式为 ,热值为 kJ/g,该气体燃烧热的热化学方程式
为 。
【答案】(1)
(2)
(3) 51.99
【解析】(1)根据盖斯定律:①-②-③,得反应: ;
(2)焓变=反应物总键能-生成物总键能,则
;
(3)该气体物质的量: ,其摩尔质量: ,仅由C、H两种元素组
成,分子式为C H ;4.5g可燃物燃烧放出热量233.97kJ,则1g该物质燃烧放出热量:51.99kJ/g;
2 6
C H 气体燃烧放出热量233.97kJ,其热燃烧热的化学方程式:
2 6
;
1.书写热化学方程式的“五环节”
一写方程式 写出配平的化学方程式
二标状态 用s、l、g、aq标明物质的聚集状态
三定条件 确定反应的温度和压强并在ΔH后注明(101kPa、25℃时可不标注)
四标ΔH 在方程式后写出ΔH,并根据信息注明ΔH的“+”或“-”
五标数值 根据化学计量系数写出ΔH的值
2.利用盖斯定律书写热化学方程式的步骤和方法
** 错误
的表达 对比分析目标热化学方程式和已知热化学方程式,调整已知热化学方程式的化学计量
式 **对 系数与目标热化学方程式的化学计量系数一致
(1)步 比:
骤 ** 错误
的表达
根据目标热化学方程式中的反应物和生成物加减所调整的热化学方程式
式 **叠
加:** 错误
的表达
按照“叠加”步骤中的调整方法,焓变也随之作相应变化
式 **计
算:
** 错误
为了将热化学方程式相加得到目标热化学方程式,可将热化学方程式颠倒过来,反
的表达
应热的数值不变,但符号相反。这样,就不用再做减法运算了,实践证明,方程式
式 **
相减时往往容易出错
倒:
** 错误
(2)方 的表达 为了将热化学方程式相加得到目标热化学方程式,可将方程式乘以某个倍数,反应
法 式 ** 热也要相乘
乘:
** 错误
的表达 上面的两个步骤做好了,只要将热化学方程式相加即可得目标热化学方程式,反应
式 ** 热也要相加
加:
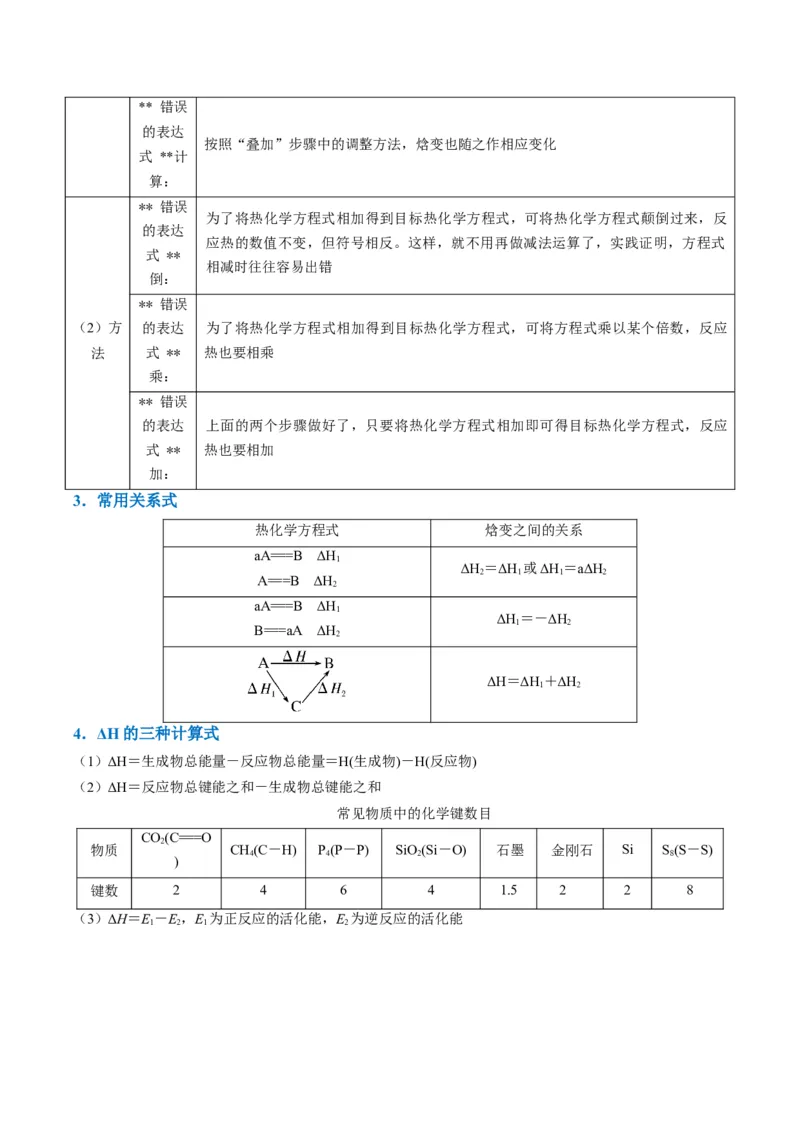
3.常用关系式
热化学方程式 焓变之间的关系
aA===B ΔH
1
ΔH=ΔH 或ΔH=aΔH
2 1 1 2
A===B ΔH
2
aA===B ΔH
1
ΔH=-ΔH
1 2
B===aA ΔH
2
ΔH=ΔH+ΔH
1 2
4.ΔH的三种计算式
(1)ΔH=生成物总能量-反应物总能量=H(生成物)-H(反应物)
(2)ΔH=反应物总键能之和-生成物总键能之和
常见物质中的化学键数目
CO(C===O
2
物质 CH(C-H) P(P-P) SiO(Si-O) 石墨 金刚石 Si S(S-S)
4 4 2 8
)
键数 2 4 6 4 1.5 2 2 8
(3)ΔH=E-E,E 为正反应的活化能,E 为逆反应的活化能
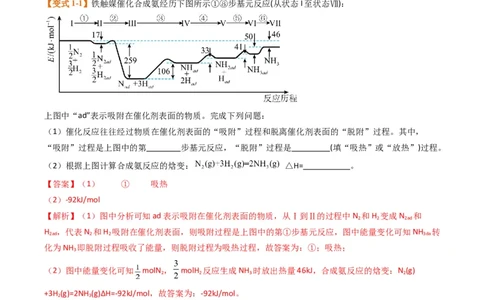
1 2 1 2【变式1-1】铁触媒催化合成氨经历下图所示①⑧步基元反应(从状态I至状态Ⅶ):
上图中“ad”表示吸附在催化剂表面的物质。完成下列问题:
(1)催化反应往往经过物质在催化剂表面的“吸附”过程和脱离催化剂表面的“脱附”过程。其中,
“吸附”过程是上图中的第 步基元反应,“脱附”过程是 (填“吸热”或“放热”)过程。
(2)根据上图计算合成氨反应的焓变: △H= 。
【答案】(1) ① 吸热
(2)-92kJ/mol
【解析】(1)图中分析可知ad表示吸附在催化剂表面的物质,从Ⅰ到Ⅱ的过程中N 和H 变成N 和
2 2 2ad
H ,代表N 和H 吸附在催化剂表面,则吸附过程是上图中的第①步基元反应,图中能量变化可知NH 转
2ad 2 2 3da
化为NH 即脱附过程吸收了能量,则脱附过程为吸热过程,故答案为:①;吸热;
3
(2)图中能量变化可知 molN , molH 反应生成NH 时放出热量46kJ,合成氨反应的焓变:N (g)
2 2 3 2
+3H (g)=2NH (g)ΔH=-92kJ/mol,故答案为:-92kJ/mol。
2 3
【变式1-2】(2023上·河南濮阳·高二濮阳一高校考)磷及其化合物应用广泛,磷元素有白磷、红磷、黑磷
等单质。
(1)一定条件下,红磷在氯气中燃烧的产物有两种( 和 ),反应过程中的能量变化关系如图所
示。回答下列问题:写出固态红磷在一定量的 中完全燃烧生成气态物质( )的热化学方程式:
。( 用图中字母表示)
(2)白磷( )在 中燃烧有如下转化关系。
其中 (用含 和 的代数式表示)。
(3)已知: (s,白磷) (s,黑磷) ;
(s,白磷) (s,红磷) ;
由此推知,其中最稳定的磷单质是 (填“白磷”、“黑磷”或“红磷”)。
【答案】(1) (或
)
(2)
(3)黑磷
【解析】(1)由题给图像知2P(s)+3Cl (g)=2PCl (g) ΔH=−(c−b)kJ⋅mol−1或P(s)+ Cl (g)=PCl (g)ΔH=−
2 3 2 3
kJ⋅mol-1
(2)根据盖斯定律, ,故
(3)能量越低越稳定,白磷→红磷、白磷→黑鳞均为放热,由盖斯定律:P(s,红磷)=P(s,黑磷) △H=-21.7
kJ⋅mol−1,红磷→黑鳞为放热反应,故黑鳞能量最低最稳定。
【考向二】有关反应速率、转化率、速率常数的计算
【典例2】(2023·江苏南通·统考二模)在催化剂作用下,以 、 为原料合成 ,其主要反应有:
反应1 kJ·mol反应2 kJ·mol
将体积比为1∶1的 、 混合气体按一定流速通过催化反应管,测得 、 的转化率随温度变
化的关系如图所示。
已知 的选择性
下列说法正确的是
A.图中曲线①表示 转化率随温度的变化
B.720~800℃范围内,随温度的升高,出口处 及 的量均增大
C.720~800℃范围内,随温度的升高, 的选择性不断增大
D.其他条件不变,加入 或选用高效催化剂,均能提高平衡时 产率
【答案】B
【分析】将体积比为1∶1的 、 混合气体按一定流速通过催化反应管,其主要反应有:
、 ,则 的转化率应
该大于 的转化率,图中曲线①表示 转化率随温度的变化,曲线②表示 的转化率,以此解答。
【解析】A.由分析可知,图中曲线①表示 转化率随温度的变化,故A错误;
B.720~800℃范围内,随温度的升高, 、 的转化率都增大,则生成 、 的物质的量增大,
出口处 及 的量均增大,故B正确;
C.720~800℃范围内,随温度的升高, 、 的转化率都增大,但 的转化率程度大于 ,说
明反应2正向进行的程度增大大于反应1, 的选择性不断减小,故C错误;
D.催化剂虽然不能改变平衡转化率,但是催化剂有选择性,可以提升目标产物的产率;CaO会吸收水和
二氧化碳,但是无法判断平衡如何移动,因此不能判断平衡时C H 的产率如何变化,故D错误;
2 4
故选B。
1.有关化学反应速率计算公式的理解
对于反应mA(g)+nB(g)===cC(g)+dD(g)Δc(A) Δn(A)
=
(1)计算公式:v(A)=
Δt V⋅Δt
(2)同一反应用不同的物质表示反应速率时,数值可能不同,但意义相同。不同物质表示的反应速率,
存在如下关系:v(A)∶v(B)∶v(C)∶v(D)=m∶n∶c∶d
(3)注意事项
①浓度变化只适用于气体和溶液中的溶质,不适用于固体和纯液体
②化学反应速率是某段时间内的平均反应速率,而不是瞬时速率,且计算时取正值
2.化学平衡计算中常用公式
对于可逆反应:对以下反应:mA(g)+nB(g) pC(g)+qD(g),令A、B起始物质的量(mol)分别为a、
b,达到平衡后,A的消耗量为mx mol,容器容积为V L
mA(g) + nB(g) pC(g)+qD(g)
起始/mol a b 0 0
变化/mol mx nx px qx
平衡/mol a-mx b-nx px qx
平衡常数:K== (固体和纯液体的浓度为常数,不计入化学平衡常数表达式中)
反应物(A)的转化率:α(A)=×100%=×100%=×100%
3.化学反应速率常数及应用
(1)速率常数含义:反应速率常数(k)是指在给定温度下,反应物浓度皆为1 mol·L-1时的反应速率。在相
同的浓度条件下,可用反应速率常数大小来比较化学反应的反应速率
(2)速率常数的影响因素:与浓度无关,但受温度、催化剂、固体表面性质等因素的影响,但温度对化
学反应速率的影响是显著的,速率常数是温度的函数,同一反应,温度不同,速率常数将有不同的值,
一般温度越高,反应速率常数越大。通常反应速率常数越大,反应进行得越快。不同反应有不同的速率
常数
(3)速率方程
①定义:一定温度下,化学反应速率与反应物浓度以其计量数为指数的幂的乘积成正比
②表达式:对于反应:aA(g)+bB(g) gG(g)+hH(g),则v =k ·ca(A)·cb(B)(其中k 为正反应的反应
正 正 正
速率常数),v =k ·cg(G)·ch(H)(其中k 为逆反应的反应速率常数)
逆 逆 逆
如:反应:2NO (g) 2NO(g)+O(g),v =k ·c2(NO ),v =k ·c2(NO)·c(O )。
2 2 正 正 2 逆 逆 2
(4)速率常数与化学平衡常数之间的关系
①K与k 、k 的关系
正 逆
对于反应:aA(g)+bB(g) pC(g)+qD(g),
则:v =k ·ca(A)·cb(B) (k 为正反应速率常数)
正 正 正
v =k ·cp(C)·cq(D) (k 为逆反应速率常数)
逆 逆 逆
k
正=
cp(C)⋅cq(D)
=K K=
k
正
反应达到平衡时v 正 =v 逆 ,此时:k 正 ·ca(A)·cb(B)=k 逆 ·cp(C)·cq(D)⇒ k 逆 ca(A)⋅cb(B) ,即: k 逆
②K 与k 、k 的关系
p 正 逆
以2NO NO 为例,v =k ·p2(NO ),v =k ·p(NO)
2 2 4 正 正 2 逆 逆 2 4反应达到平衡时v =v ,此时:k ·p2(NO )=k ·p(N O)⇒==K ,即:K =
正 逆 正 2 逆 2 4 p p
【变式2-1】(2023上·江苏盐城·高三校联考)一定条件下合成乙烯:6H (g)+2CO (g) CH =CH (g)
2 2 2 2
+4H O(g)。已知温度对CO 的平衡转化率和催化剂催化效率的影响如图所示,下列说法不正确的是
2 2
A.生成乙烯的速率:v(M)一定小于v(N)
B.当温度高于250℃,升高温度,平衡向逆反应方向移动,催化剂的催化效率降低
C.平衡常数:K >K
M N
D.若投料比n(H ):n(CO )=3:1,则图中M点乙烯的体积分数为7.7%。
2 2
【答案】A
【分析】0~250℃,催化效率随着温度的升高而增大,高于250℃时,催化效率随着温度的升高而降低,说
明温度过高会影响催化剂的活性,使催化效率降低;同时升高温度,CO 平衡转化率减小,说明该反应是
2
放热反应。
【解析】A.M点的温度低于N点的温度,但M点的催化效率高于N点的,所以生成乙烯的速率:v(M)不
一定小于v(N),A错误;
B.当温度高于250℃,升高温度,CO 平衡转化率减小,说明平衡向逆反应方向移动,同时温度过高影响
2
催化剂的活性,导致催化剂的催化效率降低,B正确;
C.该反应是放热反应,升高温度,平衡逆向移动,平衡常数减小,则K >K ,C正确;
M N
D.若投料比n(H )∶n(CO )=3∶1,图中M点转化率为50%,建立三段式:
2 2
,
相同条件下,物质的量之比等于体积之比,则M点乙烯的体积分数为 ,
D正确;
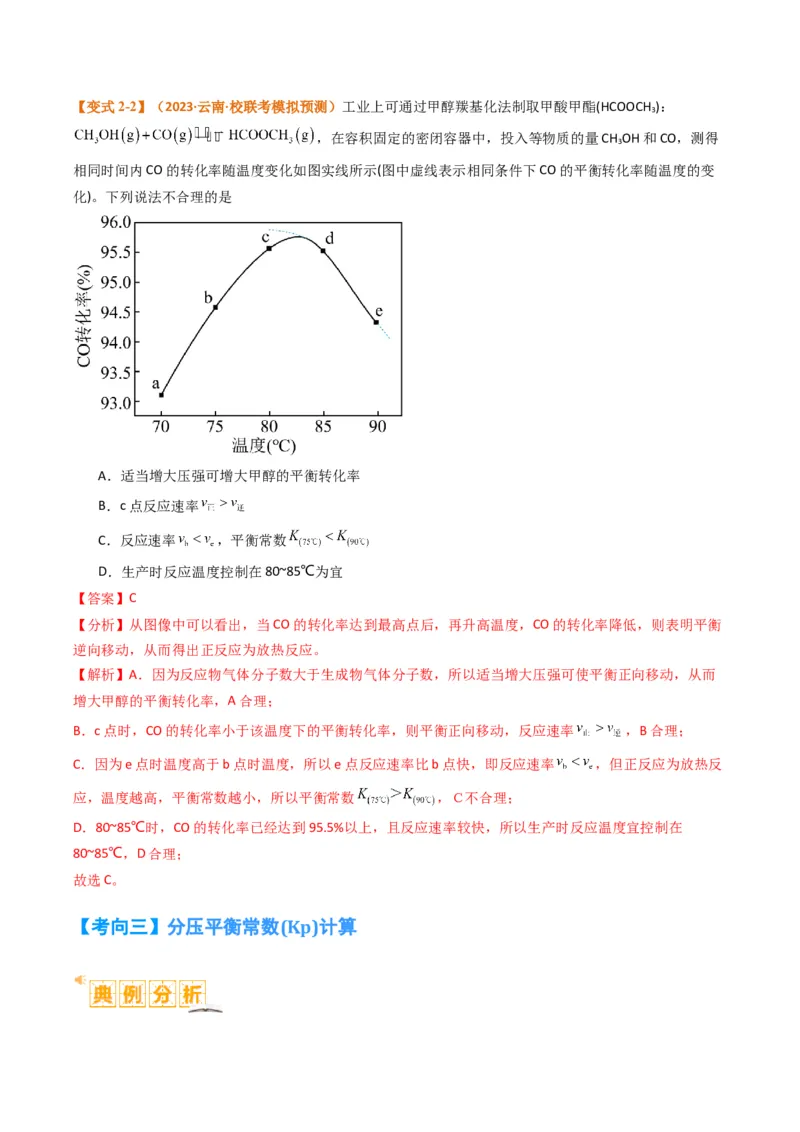
故选A。【变式2-2】(2023·云南·校联考模拟预测)工业上可通过甲醇羰基化法制取甲酸甲酯(HCOOCH ):
3
,在容积固定的密闭容器中,投入等物质的量CH OH和CO,测得
3
相同时间内CO的转化率随温度变化如图实线所示(图中虚线表示相同条件下CO的平衡转化率随温度的变
化)。下列说法不合理的是
A.适当增大压强可增大甲醇的平衡转化率
B.c点反应速率
C.反应速率 ,平衡常数
D.生产时反应温度控制在80~85℃为宜
【答案】C
【分析】从图像中可以看出,当CO的转化率达到最高点后,再升高温度,CO的转化率降低,则表明平衡
逆向移动,从而得出正反应为放热反应。
【解析】A.因为反应物气体分子数大于生成物气体分子数,所以适当增大压强可使平衡正向移动,从而
增大甲醇的平衡转化率,A合理;
B.c点时,CO的转化率小于该温度下的平衡转化率,则平衡正向移动,反应速率 ,B合理;
C.因为e点时温度高于b点时温度,所以e点反应速率比b点快,即反应速率 ,但正反应为放热反
应,温度越高,平衡常数越小,所以平衡常数 ,C不合理;
D.80~85℃时,CO的转化率已经达到95.5%以上,且反应速率较快,所以生产时反应温度宜控制在
80~85℃,D合理;
故选C。
【考向三】分压平衡常数(Kp)计算【典例3】(2023·全国·高三专题练习)用测压法在刚性密闭容器中研究T ℃时4NO(g) N (g)+2NO (g)
2 2
的分解反应,现将一定量的NO充入该密闭容器中,测得体系的总压强随时间的变化如下表所示:
反应时间/min 0 10 20 30 40
压强/MPa 15.00 14.02 13.20 12.50 12.50
(1)20 min时,NO的转化率α= %
(2)T ℃时,4NO(g) N (g)+2NO (g)反应的平衡常数K== (K 为以分压表示的平衡常数)
2 2 p p
【答案】(1)48
(2)0.1
【分析】在一定条件下 ,压强之比等于物质的量之比,因此可以直接用压强代替物质的量计算;
【解析】(1)20 min时,15-x=13.2,x=1.8,NO的转化率为α= ×100%=48%;
(2)平衡时,15-x=12.5,x=2.5,NO、N 、NO 的压强分别为5、2.5、5,代入公式K= =
2 2 p
=0.1。
1.分压平衡常数(K )
p
(1)气体的分压p(B):相同温度下,当某组分气体B单独存在且具有与混合气体总体积相同的体积时,
该气体B所具有的压强,称为气体B的分压强,简称气体B的分压。符号为p(B),单位为Pa或kPa或
MPa
(2)分压定律
①分压定律:混合气体的总压等于相同温度下各组分气体的分压之和
p(A)+p(B)+p(C)+p(D)+…=p
②气体的分压之比等于其物质的量之比:=
③某气体的分压p(B)与总压之比等于其物质的量分数:==x(B)
则:气体的分压=气体总压×体积分数=总压×物质的量分数
(3)分压平衡常数K (只受温度影响)
p
一定温度下,气相反应:mA(g)+nB(g) pC(g)+qD(g)达平衡时,气态生成物分压幂之积与气态反应
物分压
幂之积的比值为一个常数,称为该反应的压强平衡常数,用符号K 表示,K 的表达式如下:
p ppp (C)⋅pq (D)
Kp=
pm (A)⋅pn (B)
其中p(A)、p(B)、p(C)、p(D)分别为A、B、C、D各气体的分压
,
2.K 计算的两种方法:
p
方法1.根据“某气体的分压=气体总压强×该气体的体积分数(或物质的量分数)”计算压强平衡常数
第一步 根据“三段式”法计算平衡体系中各物质的物质的量或物质的量浓度
第二步 计算各气体组分的物质的量分数或体积分数。
根据分压计算公式求出各气体物质的分压,某气体的分压=气体总压强×该气体的体积分
第三步
(或物质的量分数)
根据平衡常数计算公式代入计算。例如,N(g)+3H(g) 2NH (g),压强平衡常数表达
2 2 3
第四步
式为K =
p
方法2.直接根据分压强计算压强平衡常数
N(g) + 3H(g) 2NH (g)
2 2 3
p(始): p 3p 0
0 0
Δp: p 3p 2p
p(平): p-p 3p-3p 2p
0 0
(2p) 2
(p。−p)×(3p。−3p) 3
K =
p
【变式3-1】(2023·全国·高三专题练习)活性炭还原NO 的反应为2NO (g)+2C(s) N (g)+2CO (g),在
2 2 2 2
恒温条件下,1 mol NO 和足量活性炭发生该反应,测得平衡时NO 和CO 的物质的量浓度与平衡总压的关
2 2 2
系如图所示:
计算C点时该反应的压强平衡常数K= (K 是用平衡分压代替平衡浓度计算,分压=总压×物质的
p p
量分数)
【答案】4MPa【解析】设C点时NO 的浓度为cmol·L-1,则CO 的浓度也为cmol·L-1,则
2 2
p(NO )=20MPa× =8MPa;
2
p(N )=20MPa× =4MPa;
2
p(CO )=20MPa× =8MPa;
2
Kp= = =4MPa。
【变式3-2】(2023·全国·高三专题练习)在容积恒为2 L的密闭容器中充入2 mol CH OH(g)和2 mol CO(g),
3
在一定温度下发生反应CH OH(g)+CO(g) HCOOCH (g),测得容器内的压强随时间的变化如下表所示
3 3
t/min 0 2 4 6 8 10 12 14
p/kPa P - 0.8P - - 0.7P 0.7P 0.7P
0 0 0 0 0
在此条件,0~4 min的v(CH OH)= kPa·min-1,该反应的平衡常数K= (kPa)-1 (以分压
3 p
表示,分压=总压×物质的量分数)
【答案】 0.05P
0
【解析】在此条件,0~4 min的v(CH OH)= =0.05P kPa·min-1;
3 0
设平衡时CH OH反应了x mol,列出三段式:
3
反应后总物质的量为(4-x)mol,T、V一定时,n和p成正比,所以 = ,解得x=1.2,则反应后总物
质的量为2.8 mol,CH OH的物质的量分数为 = = ,CO的物质的量分数为 = = ,
3
HCOOCH 的物质的量分数为 = = ,则K= = (kPa)-1=
3 p
(kPa)-1。【考向四】平衡图像曲线受温度、压强影响的原因分析
【典例4】(2023·全国·高三专题练习)对于 ,且压强 。下列图像中
曲线变化错误的是
A. B.
C. D.
【答案】C
【解析】A. 是放热反应,温度越高,反应速率越快,越快到达平衡,平衡后,温
度高时平衡向逆反应移动,A的转化率减小,A项正确;
B.是放热反应,同一压强下,温度越高,平衡逆反应移动,C的百分含量越低;该反应也是气体体积系数
减小的反应,同一温度下,压强越大,平衡向着正反应方向移动,C的百分含量越大,若压强 ,则图
像符合,B项正确;
C.平衡常数的大小只与温度有关, 是放热反应,温度升高,平衡常数减小,所以500℃的平衡常数比
400℃的小,C项错误;
D.其他条件不变时,温度越高,正逆反应速率变大,由于反应是放热反应,逆反应速率升高的程度比正
反应大,D项正确;
故答案选C。
1.影响化学平衡的因素
(1)若其他条件不变,改变下列条件对化学平衡的影响
改变的条件(其他条件不变) 化学平衡移动的方向
增大反应物浓度或减小生成物浓度 向正反应方向移动
浓度
减小反应物浓度或增大生成物浓度 向逆反应方向移动
压强(对有气体 反应前后气体体积改变 增大压强 向气体分子总数减小的方向移动减小压强 向气体分子总数增大的方向移动
参加的反应)
反应前后气体体积不变 改变压强 平衡不移动
升高温度 向吸热反应方向移动
温度
降低温度 向放热反应方向移动
催化剂 同等程度改变v 、v ,平衡不移动
正 逆
(2)“惰性气体”对化学平衡移动的影响
①恒温、恒容下:加入惰性气体
⃗引起
体系总压增大,但体积不变,各反应物、生成物的浓度均未改
变,故反应速率不变,V 、V 也不变,化学平衡也不发生移动
正 逆
②恒温、恒压下:加入惰性气体
⃗引起
体积增大
⃗引起
各反应物浓度减少
⃗引起
反应速率减小,V
、
正
V 均减小,等效于降压,故化学平衡向气体总体积增大的方向移动
逆
2.掌握三类平衡移动图像:反应mA(g)+nB(g) pC(g)+qD(g),m+n>p+q,且ΔH>0
(1)速率—时间图【注意断点】
t 时增大反应物的浓度,正反应速率瞬间增大,然后逐渐减小,而逆反应速率逐渐增大;t 时升高温度,
1 2
对任何反应,正反应和逆反应速率均增大,吸热反应的正反应速率增大较快;t 时减小压强,容器容积
3
增大,浓度变小,正反应速率和逆反应速率均减小;t 时使用催化剂,正反应速率和逆反应速率均瞬间
4
增大
(2)转化率(或含量)—时间图【先拐先平】
甲表示压强对反应物转化率的影响,对于气体反应物化学计量数之和大于气体生成物化学计量数之和的
反应,压强越大,反应物的转化率越大;乙表示温度对反应物转化率的影响,对于吸热反应,温度越高,
反应物的转化率越大;丙表示催化剂对反应物转化率的影响,催化剂只能改变化学反应速率,不能改变
反应物的转化率
(3恒压(温)线【定一议二】分析时可沿横轴作一条平行于纵轴的虚线,即:为等压线或等温线,然后分析另一条件变化对该反应的
影响
【答题模板及剖析】
恒压线(恒温线)
答题策略 叙特点(反应特点或容器特点)→变条件→定方向→得结论(或结果)
该反应的正反应是气体分子数减小(或增大)的反应,当温度一定时,增大压强,平衡正向
答题模板
移动,因此×××(得结论)
乙烯气相水合反应的热化学方程式为C H(g)+HO(g)===C HOH(g) ΔH=-45.5 kJ·mol-1,
2 4 2 2 5
下图是乙烯气相水合法制乙醇中乙烯的平衡转化率与温度、压强的关系[其中
n(H O)∶n(C H)=1∶1]。图中压强(p 、p 、p 、p)的大小顺序为__________,理由是
2 2 4 1 2 3 4
______________
经典例题
标注答案 p<p<p<p,反应正方向是分子数减少的反应,相同温度下,压强升高乙烯转化率提高
1 2 3 4
【变式4-1】(2023上·重庆北碚)在某一恒温、恒容的密闭容器中通入1molN 和3molH 发生反应:3H (g)
2 2 2
+N (g) 2NH (g)ΔH<0。t 时刻反应达到平衡,在t 时刻改变某一条件,其反应过程如图所示。下列说法
2 3 1 2
正确的是
A.Ⅰ、Ⅱ两过程达到平衡时,平衡常数:K <K
Ⅰ Ⅱ
B.Ⅰ、Ⅱ两过程达到平衡时,NH 的体积分数:Ⅰ<Ⅱ
3
C.该反应正反应的活化能大于逆反应的活化能D.t 时刻改变的条件可以是向密闭容器中加H 和N 的混合气
2 2 2
【答案】B
【分析】该反应的正反应为气体分子数减小的放热反应,t 时刻改变某一条件,v 瞬时不变,说明改变的
2 正
条件不可能是压强、温度和催化剂,v 后逐渐增大直至达到新平衡,说明平衡逆向移动,t 时刻改变的条
正 2
件是向容器中加入一定量的NH 。
3
【解析】A.平衡常数与温度有关,t 时刻改变的条件不可能是改变温度,温度不变,化学平衡常数不变,
2
则平衡常数:K =K ,A项错误;
Ⅰ Ⅱ
B.t 时刻改变的条件是向容器中加入一定量的NH ,平衡逆向移动,根据勒夏特列原理,Ⅰ、Ⅱ两过程达
2 3
到平衡时,NH 的体积分数:Ⅰ<Ⅱ,B项正确;
3
C.根据∆H=正反应的活化能-逆反应的活化能<0,则正反应的活化能小于逆反应的活化能,C项错误;
D.t 时刻改变的条件若是向密闭容器中加H 和N 的混合气,则v 瞬时增大,后逐渐减小直至达到新平衡,
2 2 2 正
与图不吻合,D项错误;
答案选B。
【变式4-2】(2022上·山东烟台·高三统考期中)某密闭容器中充入等物质的量的A和B,一定温度下发生
反应 ,达到平衡后,在不同的时间段内反应物的浓度随时间的变化如甲图所示,正
逆反应速率随时间的变化如乙图所示。下列说法错误的是
A.前20minB的平均反应速率为
B.30~40min间该反应使用了催化剂
C.化学方程式中的 ,正反应为放热反应
D.30min、40min时分别改变的条件是减小压强、升高温度
【答案】B
【解析】A. ,前20minB的平均反应速率为 = ,故A正确;
B.30min时C和A、B的浓度都下降了,而催化剂只会改变反应速率,不会瞬间改变反应物的浓度,故B
错误;
C.由图可知,A、B的浓度变化相同,故A、B的化学计量数相同,则x=1;40min时正逆反应速率都增大,
则改变的条件为升高温度,而条件改变后C浓度减小、A、B浓度增大,说明平衡发生了逆向移动,则正反
应为放热反应,故C正确;
D.40min时改变的条件为升高温度;30min时,C和A、B的浓度都下降了,反应速率也减小,但是平衡不移动,该反应前后气体分子不变,则改变的条件为减小压强,故D正确;
故选B。
【考向五】平衡图像中最佳反应条件选择的原因分析
【典例5】(2023·海南·模拟预测)工业合成甲醇的反应为 。
反应相同时间,实验测得甲醇的产率与压强,温度的关系分别如图1,图2所示。下列叙述正确的是
A.合成甲醇时压强越大越好 B.增大压强,正反应速率增大,逆反应速率减小
C.合成甲醇的最佳温度为520K D.520K之前升高温度单位时间内甲醇的产率减小
【答案】C
【解析】A.虽然增大压强能加快反应速率、使平衡正向移动而提高甲醇的产率,但压强越大,对材料的
强度和设备的制造要求也越高,需要的动力也越大,这将会大大增加生产投资,并可能降低综合经济效益,
故合成甲醇时不是压强越大越好,A项错误;
B.增大压强,正、逆反应速率都增大,B项错误;
C.根据图2可知,520K时甲醇的产率最大,合成甲醇的最佳温度为520K,C项正确;
D.图示曲线为反应相同时间,520K之前反应未达到平衡状态,升高温度,反应速率加快,单位时间内甲
醇的产率增大,D项错误;
答案选C。
化工生产适宜条件选择的一般原则
1.既不能过快,又不能太慢
2.既要注意外界条件对速率和平衡影响的一致性,又要注意二者影响的矛盾性
3.增加易得廉价原料,提高难得高价原料的利用率,从而降低生产成本
4.如设备承受高温、高压能力等
5.注意催化剂的活性对温度的限制【变式5-1】(2023·全国·高三专题练习)已知萃取剂A、B中pH对钴离子、锰离子萃取率的影响如图所示,
为了除去Mn2+,应选择萃取剂 (填“A”或“B”)。
【答案】B
【解析】由图可知萃取剂A对于钴离子和锰离子在相同pH时萃取率相差不是很大(大致相差20%左右),
而萃取剂B对于钴离子和锰离子在pH=5时相差最大(此时Mn2+的萃取率达到60%,而Co2+此时仅为
20%),故选择的条件为:pH=5,选取萃取剂B,
故答案为:B。
【变式5-2】(2023·北京顺义·统考二模)工业上可用“氨催化氧化法”生产NO,以氨气、氧气为原料,
在Pt-Rh合金催化剂存在下生成NO和副产物N ,两个竞争反应化学方程式如下:
2
Ⅰ.4NH (g)+5O (g) 4NO(g)+6H O(g)
3 2 2
Ⅱ.4NH (g)+3O (g) 2N (g)+6H O(g)
3 2 2 2
现将1molNH 、1.45molO 充入1L恒容密闭容器中,在上述催化剂作用下反应,相同时间内有关生成物物
3 2
质的量随温度变化曲线如图所示:
已知:有效转化率= ×100%
下列说法不正确的是
A.400℃时,主要发生反应Ⅱ
B.由图分析工业上用氨催化氧化制备HNO ,最佳温度约为840℃
3
C.520℃时,NH 的有效转化率约为66.7%
3D.840℃后,NO的物质的量下降,可能是反应I平衡逆向移动所致
【答案】C
【解析】A.400℃时,氮气的物质的量最大,说明主要发生反应Ⅱ,A正确;
B.840℃时一氧化氮的产率最高副产物氮气产率最低,则工业用氨催化氧化制备HNO ,选择的最佳温度是
3
840℃,B正确;
C.由图知520C时,生成氮气和一氧化氮的物质的量均为0.2mol,则反应Ⅱ消耗的氨气的物质的量为
0.4mol,反应Ⅰ消耗的氨气的物质的量为0.2mol,NH 的有效转化率为 ,C
3
错误;
D.840℃后,NO的物质的量下降,可能是反应Ⅰ为放热反应,升温,反应Ⅰ平衡逆向移动所致,D正确;
故选C。
【考向六】平衡图像中转化率、产率变化的原因分析
【典例6】(2023·江苏盐城·统考三模)焦炉煤气(主要成分:CH 、CO 、H 、CO)在炭催化下,使CH 与CO
4 2 2 4 2
重整生成H 和CO。其主要反应为
2
反应I:
反应II:
反应III:
反应IV:
在1×105Pa、将焦炉煤气以一定流速通过装有炭催化剂的反应管,CH 、CO、H 的相对体积和CO 的转化率
4 2 2
随温度变化的曲线如图所示。相对体积 、
相对体积
下列说法不正确的是
A.温度低于900℃,反应I基本不发生
B.850℃~900℃时,主要发生反应Ⅳ
C.增大焦炉煤气流速一定能提高CO的相对体积
D.工业生产上需要研发低温下CH 转化率高的催化剂
4
【答案】C
【解析】A.从图中可以看出,温度低于900℃时,CH 的相对体积基本上是100%,所以反应I基本不发生,
4
A正确;
B.850℃~900℃时,H 、CO的体积分数都增大,且增大的幅度相近,而CH 的相对体积略有减小,可能
2 4
是CO 转化率增大的原因,所以反应I进行的幅度很小,反应Ⅱ、Ⅲ基本不发生,主要发生反应Ⅳ,B正确;
2
C.从图中可以看出,4个反应均为生成CO的反应,且都为吸热反应,所以若想提高CO的相对体积,应选
择升高温度,与增大焦炉煤气的流速无关,C不正确;
D.图中信息显示,温度低于900℃,CH 的相对体积基本上是100%,则反应I基本不发生,所以工业生产
4
上需要研发低温下CH 转化率高的催化剂,D正确;
4
故选C。
答题要领
转化率问题首先看是否是平衡转化率,若为非平衡状态的转化率,则侧重分析温度、压强、浓度对反应快
慢、催化剂对反应快慢及选择性(主副反应)的影响;若为平衡转化率,则侧重分析温度、压强、浓度对化
学平衡的影响,有时也涉及温度对催化活性的影响
【变式6-1】(2023上·广东)氨的催化氧化是工业制硝酸的基础,其反应机理如图1;在1L密闭容器中充
入1molNH 和2molO ,测得有关产物的物质的量与温度的关系如图2。
3 2
下列说法错误的是A.加入Pt—Rh合金的目的是提高反应的速率
B.氨的催化氧化最佳温度应控制在840℃左右
C.520℃时,NH 的转化率为40%
3
D.840℃以上,发生了反应:2NO(g) O (g)+N (g) ΔH>0
2 2
【答案】C
⇌
【解析】A.Pt—Rh合金作催化剂可以降低活化能,加快反应速率,选项A正确;
B.根据图示可知840℃氨的催化氧化生成NO最多,选项B正确;
C.520 ℃时,生成0.2 mol NO和0.2 mol N ,根据氮原子守恒可知有0.6 mol NH 转化,即转化率为60%,
2 3
选项C错误;
D.840 ℃以上,N 的产率上升、NO的产率下降,说明发生了反应2NO(g) O (g)+N (g),升高温度氮气产率
2 2 2
增加,说明该反应的正反应是吸热反应,ΔH>0,选项D正确。
⇌
答案选C。
【变式6-2】(2023·广东·惠州一中校联考三模)向一恒容密闭容器中加入 和一定量的 ,发
生反应: 。 的平衡转化率按不同投料比 随温度的
变化曲线如图所示。下列说法不正确的是
A.平衡时 的浓度:
B.b、c两点的正反应速率:
C.此反应在任意温度下都可自发进行
D.当容器内气体的平均相对分子质量不变时,反应达平衡状态
【答案】C
【解析】A. 越大,甲烷的转化率越小,相同温度下x 甲烷的转化率大于x ,则x <x ,a、c
1 2 1 2
甲烷的转化率相同,则平衡时平衡时 的浓度: ,故A正确;
B.据A的解析x <x ,b甲烷的转化率大于c,b、c都处于平衡态,则 ,故B正确;
1 2
C.a、b投料比相同,升高温度,甲烷的转化率增大,说明升高温度平衡正向移动,正向 ,正向体
积增大则 , 时T较大,故该反应高温自发,故C错误;
D.都是气体参加的反应,正向体积增大,则平均相对分子量是个变值,平均相对分子量不变时各组分含量不再变化,达到平衡,故D正确;
故答案为:C。
【考向七】电解质溶液中有关电离(水解)平衡常数的计算
【典例7】(2024上·山东菏泽·高三山东省鄄城县第一中学校考)常温下,二元弱酸 的 ,
,用 固体调整0.01 的 溶液的 (设体积不发生改变)。下列说法正确的是
是
A.0.01 溶液中 的电离度约为10%
B. 溶液:
C. 溶液:
D.当溶液的 时:
【答案】B
【解析】A.0.01 溶液: , 溶液的电离度 约为1%,A项错误;
B. 溶液: 的水解常数 , 溶液中 ,B
项正确;
C. 溶液中质子守恒式: ,C项错误;
D.电荷守恒式 ,因 ,故
,D项错误。
1.电离常数与水解常数的关系
(1)电离常数表达式
c(H+)⋅c(A−)
Ka=
①一元弱酸(HA): HA H++A- c(HA)
c(H+)⋅c(HA−)
Ka=
②二元弱酸(H 2 A):H 2 A H++HA- 1 c(H 2 A)c(H+)⋅c(A2−
)
Ka=
HA— H++A2- 2 c(HA—)
c(B+)⋅c(OH−)
K =
③一元弱碱(BOH):BOH B++OH- b c(BOH)
(2)电离常数(K )与电离度(α)的关系——以一元弱酸HA为例
电离
25 ℃,c mol·L-1的弱酸HA,设电离度为α
HA H+ + A-
起始浓度/mol·L-1 c 0 0
变化浓度/mol·L-1 c ·α c ·α c ·α
酸 酸 酸
平衡浓度/mol·L-1 c -c ·α c ·α c ·α
酸 酸 酸 酸
电离平衡常数K==,由于α很小,可认为1-α≈1
a
√K ⋅c
则K=c ·α2,α= (越稀越电离),则:c(H+)=c ·α= a 酸
a 酸 酸
(3)电离常数与水解常数的关系
①对于一元弱酸HA,K 与K 的关系:K =
a h h
如:CHCOONa:CHCOO-+HO CHCOOH+OH-
3 3 2 3
c(CH COOH)⋅c(OH—) c(CH COOH)⋅c(OH—)⋅c(H+) K K
K = 3 = 3 = w = w
h c(CH COO—) c(CH COO—)⋅c(H+) c(CH COO—)⋅c(H+) K (CH COOH)
3 3 3 a 3
c(CH COOH)
3
K K
K = w K = w
h1 K h2 K
②对于二元弱酸H B,K (H B)、K (H B)与K (HB-)、K (B2-)的关系: a2; a1
2 al 2 a2 2 h h
B2-+HO HB-+OH-,K (B2-)===
2 h1
HB-+HO HB+OH-,K (HB-)===
2 2 h2
③强酸弱碱盐:K =
h
如:NH Cl:NH ++HO NH ·H O+H+
4 4 2 3 2
c(NH⋅H O)⋅c(H+) c(NH⋅H O)⋅c(H+)⋅c(OH—) K K
K = 3 2 = 3 2 = w = w
h c(NH ) c(NH )⋅c(OH—) c(NH )⋅c(OH—) K (NH⋅H O)
4+ 4+ 4+ b 3 2
c(NH⋅H O)
3 2
Kwn
Ksp
(4)水解常数(K )与溶度积常数(K )的关系——强酸多元弱碱盐:K =
h sp h
如:AlCl:Al3++3HO Al(OH) +3H+
3 2 3
c3 (H+) c3 (H+)⋅c3 (OH−) Kw3
K = = =
h c(Al3+) c(Al3+)⋅c3 (OH−) Ksp
2.计算电离常数的常见类型
(1)起点时刻:巧用三段式
例1.HR是一元酸。室温时,用0.250 mol·L-1 NaOH溶液滴定25.0 mL HR溶液时,溶液的pH变化情况
如图所示。其中,b点表示两种物质恰好完全反应。计算的电离常数K= 5×10 - 6
a方法探究:此题根据纵坐标所给的数据,起点时刻pH=3,HR中和一半时的pH=
4.7,可以优先考虑起点时刻计算电离常数,常用方法:三段式
解析:根据题意,b点时酸碱恰好完全反应,则c(HR)=0.250 mol·L-1×0.02 L÷0.025 L
=0.2 mol·L-1,即0.2 mol·L-1的HR溶液的pH=3
HR H++ R—
起始:0.2 0 0
转化:10-3 10-3 10-3
平衡:0.2-10-3 10-3 10-3
c(H+)⋅c(R−)
c(HR)
HR的电离常数K= ==5×10-6
a
(2)遇中性时刻:电荷守恒配合物料守恒两步搞定
例2.在25℃下,amol·L-1的氨水与0.01mol·L-1的盐酸以体积比3:4混合,此时溶液中c(NH)=c(Cl-),
9
4×10—
3a-0.04
则溶液显中性(填“酸”、“碱”或“中”);用含a的代数式表示NH ·H O的电离常数K=
3 2 b
方法探究:中性时刻采取电荷守恒和物料守恒,解题时建议用物质的量守恒去写,因为在反应过程
中体积已经发生了变化
解析:根据电荷守恒得c(H+)+c(NH)=c(Cl-)+c(OH-),因为c(NH)=c(Cl-),所以c(H+)=c(OH-),故
溶液显中性。
电荷守恒得:n(H+)+n(NH)=n(Cl-)+n(OH-),则:n(NH)=n(Cl-)=0.01×4=0.04 mol
物料守恒得:3a=n(NH)+n(NH ·H O),则:n(NH ·H O)=(3a—0.04) mol
3 2 3 2
0.04 7
c(NH )×c(OH−) ×10— 9
4
+ 4+3 4×10—
= =
c(NH⋅H O) 3a-0.04 3a-0.04
3 2
K =
4+3
b
(3)恰好完全反应时刻:水解三段式法或利用水解常数和电离常数的关系
例3、25 ℃时,0.1 mol·L-1的HCOONa溶液的pH=10,则HCOOH的电离常数K = 1 0 - 7
a
方法探究:方法** 错误的表达式 **、直接列水解三段式求解
方法** 错误的表达式 **、先求出水解常数,再利用水解常数和电离常数的关系进行计算
方法** 错误的表达式 **、先求出水解常数,再利用
方法** 错误的表达式 **、直接列水解三段式求
水解常数和电离常数的关系进行计算
解
利用左边的三段式,先求出HCOO—的水解常数
HCOO—+H O HCOOH+OH-
2 c(HCOOH)⋅c(OH−) 10−4 ⋅10−4
=10−7
起始: 0.1 0 0
K =
c(HCOO−)
=
0.1−10−4
h
转化: 10-4 10-4 10-4
K 10−14
平衡: 0.1-10-4 10-4 10-4 w = =10−7
K 10−7
K= h
ac(H+)⋅c(R−) 10−10 ⋅(0.1−10−4
)
=10−7
c(HR) 10−4
K= =
a
【变式7-1】(2023上·河北邯郸·高三磁县第一中学校考)25℃时,用氢氧化钠溶液调节醋酸溶液的 ,
实验测得溶液中 、 的分布系数 与 的关系如图所示。其中
。下列说法错误的是
A.25℃, 的电离常数
B.曲线2代表
C.溶液中始终存在
D.
【答案】C
【解析】A.由图可知,当 时, ,解得
, , ,故 ,A正确;
B.随着 的增加, 浓度减小, 浓度增大,由图可知曲线1代表 ,曲
线2代表 ,B正确;
C.根据电荷守恒可知,溶液中始终存在 ,C错误;D. ,D正确;
故选C。
【变式7-2】(2023上·河南郑州·高三统考)常温下,用浓度为 的 标准溶液滴定浓度
均为 的 和 的混合溶液,滴定过程中溶液的 随 的变化
曲线如图所示。下列说法错误的是
A.b点:
B.c点:
C.水的电离程度:
D.常温下 的水解平衡常数约为
【答案】A
【分析】盐酸是强酸、醋酸是弱酸,用氢氧化钠滴定 和 的混合溶液,氢氧化钠先和盐酸反
应,当 =1时,溶质为氯化钠和醋酸。
【解析】A.b点 =1.5,溶质为NaCl、CH COONa、CH COOH,物质的量比为2:1:1,溶液呈酸性,
3 3
CH COONa 水解小于CH COOH电离,所以 ,故A错误;
3 3
B.c点 =1.5,溶质为等物质的量的NaCl、CH COONa,根据物料守恒
3
,故B正确;
C.c点溶质为NaCl、CH COONa,CH COONa水解促进水电离,c点之前 越小,剩余的酸越多,对电离的
3 3
抑制作用越大,所以水的电离程度: ,故C正确;
D.a点 =1,溶质是浓度均为0.01mol/L的NaCl、CH COOH,醋酸电离使溶液呈酸性,pH=3.38,则Ka=
3
,常温下 的水解平衡常数约为 ,故D正确;
选A。【考向八】溶度积( Ksp)的相关计算
【典例8】(2023上·贵州·高三清华中学校联考)常温下,向 溶液中逐滴加入等浓
度的氨水。反应过程中, 或 与加入氨水体积的关系如图所示。下列说法正确
的是
A.a点溶液中:
B.已知 ,则b点溶液的pH约为8
C.从b到c的过程中,水的电离程度增大
D.m点溶液中:
【答案】D
【解析】A.a点溶液为 溶液,Ag+部分水解,所以 ,故A错误;
B.b点溶液中Ag+刚好完全生成 ,此时 , ,已知 ,所
以 ,则 ,b点溶液的pH约为10,故B错误;
C.b到c的过程为 ,生成OH-,抑制水的电离,故C错误;
D.根据电荷守恒, ,m点溶液中 的
浓度为0.01mol/L,溶液呈碱性,所以 ,即
,故D正确;
故答案选D。类型一、由溶度积求饱和溶液溶质的物质的量浓度——比较溶解度的大小
计算技巧
1:1型 x=√K
sp
√K
1:2型或2:1型 x= 3 sp
饱和溶液时的物质的量浓度与K sp 的关系 4
√K
1:3型或3:1型 x= 4 sp
27
类型二、已知溶度积、溶液中某离子的浓度,求溶液中的另一种离子的浓度
某温度下AgCl的K =a,在0.1 mol·L-1的NaCl溶液中加入过量的AgCl固体,达到平衡后c(Ag
sp
计算技巧 Ksp
0.1
+)= =10a mol·L-1
类型三、判断沉淀的生成或沉淀是否完全
①把离子浓度数据代入K 表达式得Q,若Q>K ,则有沉淀生成;若Q105,则认为沉淀完全转化)
技巧 已知常温下,ZnS和CuS的K 分别为1.6×10-24和6.4×10-36,判断常温下反应:
sp
ZnS(s)+Cu2+(aq)===CuS(s)+Zn2+(aq)能否进行
该反应的平衡常数K=====2.5×1011>105,故反应能完全转化
Kwn
Ksp
类型六、 溶度积常数(K )与水解常数(K )的关系——强酸多元弱碱盐:K =
sp h h
K
c3 (H+) c3 (H+)×c3 (OH−) 3
计算技巧 K= = = w
Fe3++3HO Fe(OH) +3H+(aq),平衡常数
c(Fe3+) c(Fe3+)×c3 (OH−) K
sp
2 3类型七、溶度积与溶解度的相互计算
①由饱和溶液的物质的量浓度c(mol·L-1)
⃗转化
饱和溶液的溶解度S(g)
以AgCl(s) Ag+(aq)+Cl-(aq)为例,饱和溶液的物质的浓度c=1.34×10-5mol·L-1
即:1L溶液中含有1.34×10-5 mol的AgCl溶质,也就是(1.34×10-5×143.5)g=1.92×10-3g
即:1L溶液中溶解的AgCl为1.92×10-3g,由于溶液极稀,其溶液近似等于水的密度,ρ=
1g/cm3
即:1000g溶液中溶解了1.92×10-3g的AgCl,100g水中溶解了1.92×10-4g的AgCl
即:AgCl的溶解度S(AgCl)=1.92×10-4g
计算
技巧 ②饱和溶液的溶解度S(g) ⃗转化 由饱和溶液的物质的量浓度c(mol/L) ⃗转化 K
SP
20℃时,S(AgCl)=1.5×10-4g,即:100g水中溶解了AgCl的质量为1.5×10-4g,由于溶液极稀,
其溶液近似等于水的密度,ρ=1g/cm3,也即是:0.1L水中溶解了AgCl的质量为1.5×10-4g,也
1.5×10-4g
=1.05×10-6mol
即是:0.1L溶液中溶解了AgCl的质量为1.5×10-4g,此时n(AgCl)=143.5g/mol ,
n 1.05×10—6mol
c(AgCl)= =
V 0.1L ,c(AgCl)=1.05×10-5 mol·L-1,K =c(Ag+)·c(Cl-)=1.05×10-5×1.05×10-5=
SP
1.1×10-10
【变式8-1】(2024上·山东菏泽·高三山东省鄄城县第一中学校考) 在不同温度下的沉淀溶解平衡
曲线如图所示( )。下列说法不正确的是
A.温度为 时, B. 的溶解度:
C. 的溶解过程吸收能量 D.将Z溶液升温可以得到Y溶液
【答案】D
【解析】A.由Y点可知, ,A项正确;B.X、Z、W是同一温度下的饱和溶液, 相同,等体积的溶液中溶解的 的物质的量的关系为
, 的溶解度的关系为 ,B项正确;
C.温度升高 变大,说明 的溶解是吸热的,C项正确;
D.将Z溶液升温,虽溶解度增大,但没加入 ,故得不到Y溶液,D项错误;
故选D。
【变式8-2】(2023上·河北沧州·高三泊头市第一中学校联考)一定温度下, 和 的沉淀溶解平
衡曲线如图所示。
或
下列说法正确的是
A. ,
B.a点能生成 沉淀,不能生成 沉淀
C.b点时,
D.向 、 均为 的混合溶液中滴加 溶液,先产生 沉淀
【答案】D
【解析】A. 的溶度积常数表达式为 ,对该等式求负对数可得:
,因此 。题
图中 的沉淀溶解平衡曲线斜率约为1,因此 ;同理可求得 ,A项错误;
B.过a点做横轴垂线并反向延长,该垂线分别与 和 的沉淀溶解平衡曲线相交,a点纵坐标小
于垂线与 的沉淀溶解平衡曲线交点的纵坐标,该点的 大于相应的 饱和溶液中的 ,
因此能生成 沉淀,同理分析可知不能生成 沉淀,B项错误;
C.由点 计算可得到 的溶度积常数 ,由点
可得到 的溶度积常数 ,因此,C项错误;
D.向 、 均为 的混合溶液中滴加 溶液,开始沉淀时所需要的 分别为
和 ,说明此时沉淀 需要的 更低,在这种情况下,先产生 沉
淀,D项正确;
答案选D。
【考向九】电极方程式书写
【典例9】(2023上·上海黄浦·高三格致中学校考期中)我国科学家研发出一种新系统,通过钠离子电池
“溶解”水中的二氧化碳,以触发电化学反应,可有效减少碳的排放,其工作原理如图所示。其中钠超离
子导体,除了明显的结构稳定性外它们还表现出异常高的离子电导率。
(1)b极区是 极,系统工作时,b极区 参与的电极总反应式为 。
(2)工作是b极区可能会有少量固体析出,分析原因 。
【答案】(1) 正极
(2)负极产生的钠离子并移动到正极,遇到碳酸氢根离子,形成碳酸氢钠饱和溶液后析出碳酸氢钠固体
【解析】(1)由图可知,加入金属钠的为负极,即a极区为负极,则b极区是正极,系统工作时,b极区
CO 参与反应会生成H 和 ,电极总反应式为; ;
2 2
(2)工作时b极区可能会有少量固体析出,原因是负极产生的钠离子移到正极,遇到碳酸氢根离子,形
成碳酸氢钠饱和溶液后析出碳酸氢钠固体。
一、原电池中电极反应式的书写
1、先确定原电池的正负极,列出正负极上的反应物质,并标出相同数目电子的得失。
2、注意负极反应生成的阳离子与电解质溶液中的阴离子是否共存。若不共存,则该电解质溶液中的阴离子应写入负极反应式:若正极上的反应物质是O ,且电解质溶液为中性或碱性,则水必须写入正极反应式
2
中,且O 生成OH-,若电解质溶液为酸性,则H+必须写入正极反应式中,O 生成水。
2 2
3、正负极反应式相加得到电池反应的总反应式。若已知电池反应的总反应式,可先写出较易书写的电极
反应式,然后在电子守恒的基础上,总反应式减去较易写出的书写电极反应式,即得到较难写出的书写电
极反应式。
二、电解池中电极反应式的书写
1、首先看阳极材料,如果阳极是活泼电极(金属活动顺序表Ag以前),则应是阳极失电子,阳极不断溶
解,溶液中的阴离子不能失电子。
2、如果阳极是惰性电极(Pt、Au、石墨),则应是电解质溶液中的离子放电,应根据离子的放电顺序进
行书写电极反应式。
阳极(惰性电极)发生氧化反应,阴离子失去电子被氧化的顺序为:S2->SO >I->Br->C1->OH->水电离
的OH->含氧酸根离子>F-。
阴极发生还原反应,阳离子得到电子被还原的顺序为:Ag+>Hg2+>Fe3+>Cu2+>(酸电离出的H+)>Pb2+>
Sn2+>Fe2+>Zn2+>(水电离出的H+)>Al3+>Mg2+>Na+>Ca2+>K+。
注:在水溶液中A13+、Mg2+、Na+、Ca2+、K+这些活泼金属阳离子不被还原,这些活泼金属的冶炼往往采用
电解无水熔融态盐或氧化物而制得。
三、燃料电池电极反应式的书写
电极:惰性电极。
燃料包含:H ;烃如:CH ;醇如:C H OH等。
2 4 2 5
电解质包含:①酸性电解质溶液如:H SO 溶液:②碱性电解质溶液如:NaOH溶液:③熔融氧化物如:
2 4
Al O ;④熔融碳酸盐如:K CO 等。
2 3 2 3
第一步:写出电池总反应式
燃料电池的总反应与燃料的燃烧反应一致,若产物能和电解质反应则总反应为加合后的反应。
如氢氧燃料电池的总反应为:2H +O =2H O:甲烷燃料电池(电解质溶液为NaOH溶液)的反应为:
2 2 2
①CH +2O =CO +2H O
4 2 2 2
②CO +2NaOH=Na CO +H O
2 2 3 2
①式+②式得燃料电池总反应为:CH +2O +2NaOH=Na CO +3H O
4 2 2 3 2
第二步:写出电池的正极反应式
根据燃料电池的特点,一般在正极上发生还原反应的物质都是O ,随着电解质溶液的不同,其电极反应有
2
所不同,其实,我们只要熟记以下四种情况:
(1)酸性电解质溶液环境下电极反应式:O +4H++4e-=2H O
2 2
(2)碱性电解质溶液环境下电极反应式:O +2H O+4e-=40H-
2 2
(3)固体电解质(高温下能传导O2-)环境下电极反应式:O +4e-=2O2-
2
(4)熔融碳酸盐(如:熔融K CO )环境下电极反应式:O +2CO +4e-=2CO 。
2 3 2 2
第三步:根据电池总反应式和正极反应式写出电池的负极反应式
电池的总反应和正、负极反应之间有如下关系:电池的总反应式=电池正极反应式+电池负极反应式故根据第一、二步写出的反应,有:电池的总反应式-电池正极反应式=电池负极反应式,注意在将两个反
应式相减时,要约去正极的反应物O 。
2
四、可充电电池电极反应式的书写及应用
(一)可充电电池试题必备知识
1.对可充电电池充电和放电两过程认识:放电是原电池反应,充电是电解池反应。要能根据题给总反应式
写出原电池总反应式和电解池总反应式。
2.对可充电电池电极极性和材料的判断:判断电池放电时电极极性和材料,可先标出放电(原电池)总反
应式电子转移的方向和数目,失去电子的一极为负极,该物质即为负极材料:得到电子的一极为正极,该
物质即为正极材料。若判断电池充电时电极极性和材料,方法同前,失去电子的一极为阳极,该物质即为
阳极材料;得到电子的一极为阴极,该物质即为阴极材料。
3.可充电电池电极反应式的书写方法:
书写可充电电池电极反应式,一般都是先书写放电的电极反应式。书写放电的电
极反应式时,一般要遵守三步:第一,先标出原电池总反应式电子转移的方向和
数目,指出参与负极和正极反应的物质;第二,写出一个比较容易书写的电极反
应式(书写时一定要注意电极产物是否与电解质溶液共存);第三,在电子守恒
的基础上,总反应式减去写出的电极反应式即得另一电极反应式。
充电的电极反应与放电的电极反应过程相反,充电的阳极反应为放电止极反应的逆过程,充电的阴极反应
为放电负极反应的逆过程。
对可充电电池某电极是发生氧化还是还原反应及某元素被氧化还是被还原的判断:可根据电极反应式进行
分析,放电(原电池)的负极及充电(电解池)的阳极均失去电子,发生了氧化反应,其变价元素被氧化;
放电(原电池)的正极及充电(电解池)的阴极均得到电子,发生了还原反应,其变价元素被还原。
5.对溶液中离子的移动方向判断:放电时,阴离子移向负极,阳离子移向正极;充电时,阴离子移向阳极
阳离子移向阴极。
6.可充电电池充电时与电源的连接:可充电电池用完后充电时,原电池的负极与外电源的负极相连,原电
池的正极与外电源的正极相连。
7.有关电化学的计算:有关电化学的计算都必须利用电子守恒,要注意各电极转移的电子数均相等。这类
计算通常有计算电极的增重或较少量、溶液的PH、溶液的离子浓度、电子转移的数目等。
五、特殊情况电极反应式的书写
在书写电极反应式时,一定要注意一些特殊情况。
1、注意溶液中的离子浓度的改变会引起离子放电顺序的改变溶液中的离子浓度改变,有时可导致离子放
电顺序的改变。
2、注意电解质溶液的改变会引起电极正负的改变在原电池中,一般较活泼金属作负极,但当电解质溶液
发生改变时,较活泼金属就不一定作负极了。
【变式9-1】Ⅰ.与MnO —Zn电池类似,K FeO —Zn也可以组成碱性电池,K FeO 在电池中作为正极材料,
2 2 4 2 4
其电极反应式为 ,该电池总反应的离子方程式为 。【答案】 Fe +3e—+4H O=Fe(OH) +5OH— 2Fe +3Zn+8H O=2Fe(OH) ↓+3Zn(OH) ↓+4OH—
2 3 2 3 2
【解析】由题意可知,高铁酸钾是原电池的正极,水分子作用下高铁酸根离子在正极得到电子发生还原反
应生成氢氧化铁和氢氧根离子,电极反应式为Fe +3e—+4H O=Fe(OH) ↓+5OH—,锌是负极,碱性条件下
2 3
锌失去电子发生氧化反应生成氢氧化锌,电极反应式为Zn—2e—+2OH—=Zn(OH) ,则总反应为2Fe
2
+3Zn+8H O=2Fe(OH) ↓+3Zn(OH) ↓+4OH—,故答案为:Fe +3e—+4H O=Fe(OH) +5OH—;2Fe
2 3 2 2 3
+3Zn+8H O=2Fe(OH) ↓+3Zn(OH) ↓+4OH—。
2 3 2
Ⅱ.以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH) ,该电
2
池反应的化学方程式是 。
【答案】
【解析】利用题中信息可知放电时NiO(OH)作正极,发生还原反应放电时NiO(OH)转化为Ni(OH) ,,则Al
2
作负极,因电解质溶液为NaOH,则放电时Al极发生氧化反应生成NaAlO ,电池总反应式:
2
。
【变式9-2】2019年诺贝尔化学奖颁给在锂离子电池发展方面作出突出贡献的三位科学家,颁奖词中说:
他们创造了一个可再充电的世界。下面是最近研发的Ca-LiFePO 可充电电池的工作示意图,锂离子导体膜
4
只允许Li+通过,电池反应为:xCa2++2LiFePO xCa+2Li FePO +2xLi+。
4 1-x 4
负极反应: ;正极反应: ;阳极反应: ;阴极反应: 。
【答案】 Ca-2e-=Ca2+ Li FePO +xLi++xe-=LiFePO LiFePO -xe-=xLi++Li FePO Ca2++
1-x 4 4 4 1-x 4
2e-=Ca
【分析】根据电池反应知,放电时Ca发生失电子的氧化反应生成Ca2+,Li FePO 发生得电子的还原反应生
1-x 4
成LiFePO ;充电时Ca2+发生得电子的还原反应生成Ca,LiFePO 发生失电子的氧化反应生成Li FePO 。
4 4 1-x 4
【解析】根据电池反应知,放电为原电池原理,总反应为xCa+2Li FePO +2xLi+= xCa2++2LiFePO ,Ca元素
1-x 4 4的化合价由0价升至+2价,钙电极为负极,负极反应为Ca-2e-=Ca2+,Li FePO /LiFePO 电极为正极,正极
1-x 4 4
上Li FePO 发生得电子的还原反应生成LiFePO ,正极反应为Li FePO +xLi++xe-=LiFePO ;充电为电解池原
1-x 4 4 1-x 4 4
理,电解总反应为xCa2++2LiFePO xCa+2Li FePO +2xLi+,钙电极为阴极,阴极反应为Ca2++2e-=Ca,
4 1-x 4
Li FePO /LiFePO 电极为阳极,阳极反应为LiFePO -xe-=xLi++Li FePO ;答案为:Ca-2e-=Ca2+;Li FePO +
1-x 4 4 4 1-x 4 1-x 4
xLi++xe-=LiFePO ;LiFePO -xe-=xLi++Li FePO ;Ca2++2e-=Ca。
4 4 1-x 4
1.(2023·全国卷)一定温度下,AgCl和Ag CrO 的沉淀溶解平衡曲线如图所示。
2 4
下列说法正确的是
A.a点条件下能生成Ag CrO 沉淀,也能生成AgCl沉淀
2 4
B.b点时,c(Cl-)=c(CrO ),K (AgCl)=K (Ag CrO )
sp sp 2 4
C.Ag CrO +2Cl- 2AgCl+CrO 的平衡常数K=107.9
2 4
D.向NaCl、Na CrO 均为0.1mol·L-1的混合溶液中滴加AgNO 溶液,先产生Ag CrO 沉淀
2 4 3 2 4
【答案】C
【分析】根据图像,由(1.7,5)可得到Ag CrO 的溶度积K (Ag CrO )=c2(Ag+)·c(CrO )=(1×10-5)2×1×10-1.7=10-
2 4 sp 2 4
11.7,由(4.8,5)可得到AgCl的溶度积K (AgCl)=c(Ag+)·c(Cl)=1×10-5×1×10-4.8=10-9.8,据此数据计算各选项结果。
sp
【解析】A.假设a点坐标为(4,6.5),此时分别计算反应的浓度熵Q得,Q(AgCl)=10-10.5,Q(Ag CrO )=10-
2 4
17,二者的浓度熵均小于其对应的溶度积K ,二者不会生成沉淀,A错误;
spB.K 为难溶物的溶度积,是一种平衡常数,平衡常数只与温度有关,与浓度无关,根据分析可知,二者
sp
的溶度积不相同,B错误;
C.该反应的平衡常数表达式为K= ,将表达式转化为与两种难溶物的溶度积有关的式子得K=
= = = =1×107.9,C正确;
D.向NaCl、Na CrO 均为0.1mol·L-1的混合溶液中滴加AgNO ,开始沉淀时所需要的c(Ag+)分别为10-8.8和10-
2 4 3
5.35,说明此时沉淀Cl-需要的银离子浓度更低,在这种情况下,先沉淀的是AgCl,D错误;
故答案选C。
2.(2023·全国卷)室温钠-硫电池被认为是一种成本低、比能量高的能源存储系统。一种室温钠-硫电池的
结构如图所示。将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂有硫黄粉末的炭化纤维素纸作为另一
电极。工作时,在硫电极发生反应: S +e-→ S , S +e-→S ,2Na++ S +2(1- )e-→Na S
8 2 x
下列叙述错误的是
A.充电时Na+从钠电极向硫电极迁移
B.放电时外电路电子流动的方向是a→b
C.放电时正极反应为:2Na++ S +2e-→Na S
8 2 x
D.炭化纤维素纸的作用是增强硫电极导电性能
【答案】A
【分析】由题意可知放电时硫电极得电子,硫电极为原电池正极,钠电极为原电池负极。
【解析】A.充电时为电解池装置,阳离子移向阴极,即钠电极,故充电时,Na+由硫电极迁移至钠电极,
A错误;
B.放电时Na在a电极失去电子,失去的电子经外电路流向b电极,硫黄粉在b电极上得电子与a电极释
放出的Na+结合得到Na S,电子在外电路的流向为a→b,B正确;
2 x
C.由题给的的一系列方程式相加可以得到放电时正极的反应式为2Na++ S +2e-→Na S,C正确;
8 2 x
D.炭化纤维素纸中含有大量的炭,炭具有良好的导电性,可以增强硫电极的导电性能,D正确;
故答案选A。3.(2023·全国卷)下图为 和 在水中达沉淀溶解平衡时的 关系图(
; 可认为 离子沉淀完全)。下列叙述正确的是
A.由 点可求得
B. 时 的溶解度为
C.浓度均为 的 和 可通过分步沉淀进行分离
D. 混合溶液中 时二者不会同时沉淀
【答案】C
【解析】A.由点a(2,2.5)可知,此时pH=2,pOH=12,则 = = =
,故A错误;
B.由点(5,6)可知,此时pH=5,pOH=9,则 = = = , 时
的溶解度为 =10-3 ,故B错误;
C.由图可知,当铁离子完全沉淀时,铝离子尚未开始沉淀,可通过调节溶液pH的方法分步沉淀 和
,故C正确;
D.由图可知, 沉淀完全时, ,pM 5,此时pH约为4.7,在此pH下 刚开始
沉淀的浓度为 ,而题中 > ,则 会同时沉淀,故D错误;
答案选C。
4.(2023·全国卷)向 饱和溶液(有足量 固体)中滴加氨水,发生反应
和 , 与 的关系如下图所示(其
中M代表 、 、 或 )。下列说法错误的是
A.曲线I可视为 溶解度随 浓度变化曲线
B. 的溶度积常数
C.反应 的平衡常数K的值为
D. 时,溶液中
【答案】A
【分析】氯化银饱和溶液中银离子和氯离子的浓度相等,向饱和溶液中滴加氨水,溶液中银离子浓度减小,
氯离子浓度增大、一氨合银离子增大,继续滴加氨水,一氨合银离子增大的幅度小于二氨合银离子,则曲
线I、Ⅱ、Ⅲ、Ⅳ分别表示二氨合银离子、一氨合银离子、银离子、氯离子与氨气浓度对数变化的曲线。
【解析】A.氨的浓度较小时AgCl(s) Ag+(aq)+Cl-(aq),浓度较大时AgCl(s)+2NH (aq)
3
+Cl-(aq),氯化银的溶解度曲线应与氯离子的曲线吻合,应该为曲线Ⅳ,故A错误;
B.由图可知,c(NH )=10-1mol/L时,c(Cl-)=10-2.35mol/L,c(Ag+)=10-7.40mol/L,则氯化银的溶度积为10-2.35×10-
3
7.40=10-9.75,故B正确;
C.由图可知,氨分子浓度对数为-1时,溶液中二氨合银离子和一氨合银离子的浓度分别为10-2.35mol/L和
10-5.16mol/L,则 的平衡常数K=
= = ,故C正确;
D.由分析可知,曲线I、Ⅱ、Ⅲ、Ⅳ分别表示二氨合银离子、一氨合银离子、银离子、氯离子与氨气浓度
对数变化的曲线,则 时,溶液中 ,故D正
确;
故选A。
5.(2023·天津卷)已知 ,如图下表是几种不同有机酸的 大小,由此产生的推断,正确的
是有机酸
pKa 2.66 2.86 2.86 4.74
A.对键合电子吸引力: B.酸性:
C. D.碱性:
【答案】C
【解析】A.电负性:F>Cl>Br,电负性越大,对键合电子吸引力越强,则对键合电子吸引力:F>Cl>Br,故
A错误;
B.由于电负性:F>I,F的电负性较大,C-F的共用电子对偏向F,通过传导作用,导致羧基中O-H键的极
性最大,酸性增强,则酸性: ,故B错误;
C.F的电负性最大,C-F的共用电子对偏向F,通过传导作用,导致羧基中O-H键的极性最大,酸性增强,
氟原子个数越多,酸性越大,所以酸性: ,则 ,故
C正确;
D.由表格数据可知, ,则酸性: ,酸性越弱,对应酸
根水解程度越大,碱性越强,则碱性: ,故D错误;
故选C。
6.(2023·天津卷)在浓度为 的 溶液中,如下说法正确的是
A.溶液中浓度最大的离子是
B.
C.
D.磷酸第二步电离平衡的平衡常数表达式为
【答案】B
【解析】A. 在水溶液中完全电离生成Na+和 , 又发生电离和水解,则溶液中浓度
最大的离子是Na+,故A错误;
B.根据NaH PO 溶液中的物料守恒可得:c(Na+)=c( )+c(PO )+c(HPO )+c(H PO )=0.1mol/L,故B正确;
2 4 3 4
C.根据NaH PO 溶液中的电荷守恒可得:c(Na+)+c(H+)=c(OH-)+c(H PO )+2c(HPO )+3c(PO ),故C错误;
2 4 2
D.磷酸第二步电离方程式为: ,电离平衡的平衡常数表达式为 ,
故D错误;
故选B。故选:B。7.(2023·全国卷)硫酸亚铁在工农业生产中有许多用途,如可用作农药防治小麦黑穗病,制造磁性氧化
铁、铁催化剂等。回答下列问题:
(1)在 气氛中, 的脱水热分解过程如图所示:
根据上述实验结果,可知 , 。
(2)已知下列热化学方程式:
则 的 。
(3)将 置入抽空的刚性容器中,升高温度发生分解反应:
(Ⅰ)。平衡时 的关系如下图所示。 时,该反应的平
衡总压 、平衡常数 。 随反应温度升高而 (填“增大”
“减小”或“不变”)。
(4)提高温度,上述容器中进一步发生反应 (Ⅱ),平衡时 (用表示)。在 时, ,则 ,
(列出计算式)。
【答案】(1) 4 1
(2)(a+c-2b)
(3) 3 增大
(4) 46.26
【解析】(1)由图中信息可知,当失重比为19.4%时, 转化为 ,则
,解之得 =4;当失重比为38.8%时, 转化为 ,则
,解之得y=1。
(2)①
②
③
根据盖斯定律可知,①+③-② 2可得 ,则
(a+c-2b) 。
(3)将 置入抽空的刚性容器中,升高温度发生分解反应:
(Ⅰ)。由平衡时 的关系图可知, 时, ,
则 ,因此,该反应的平衡总压 3 、平衡常数 。由
图中信息可知, 随着温度升高而增大,因此, 随反应温度升高而增大。
(4)提高温度,上述容器中进一步发生反应 (Ⅱ),在同温同压下,不同气体
的物质的量之比等于其分压之比,由于仅发生反应(Ⅰ)时 ,则 ,因此,平衡
时 。在 时, ,则 、 ,
联立方程组消去 ,可得 ,代入相关数据可求出 46.26 ,则
, 。
8.(2023·全国卷)甲烷选择性氧化制备甲醇是一种原子利用率高的方法。回答下列问题:
(1)已知下列反应的热化学方程式:
①②
反应③ 的 ,平衡常数 (用 表
示)。
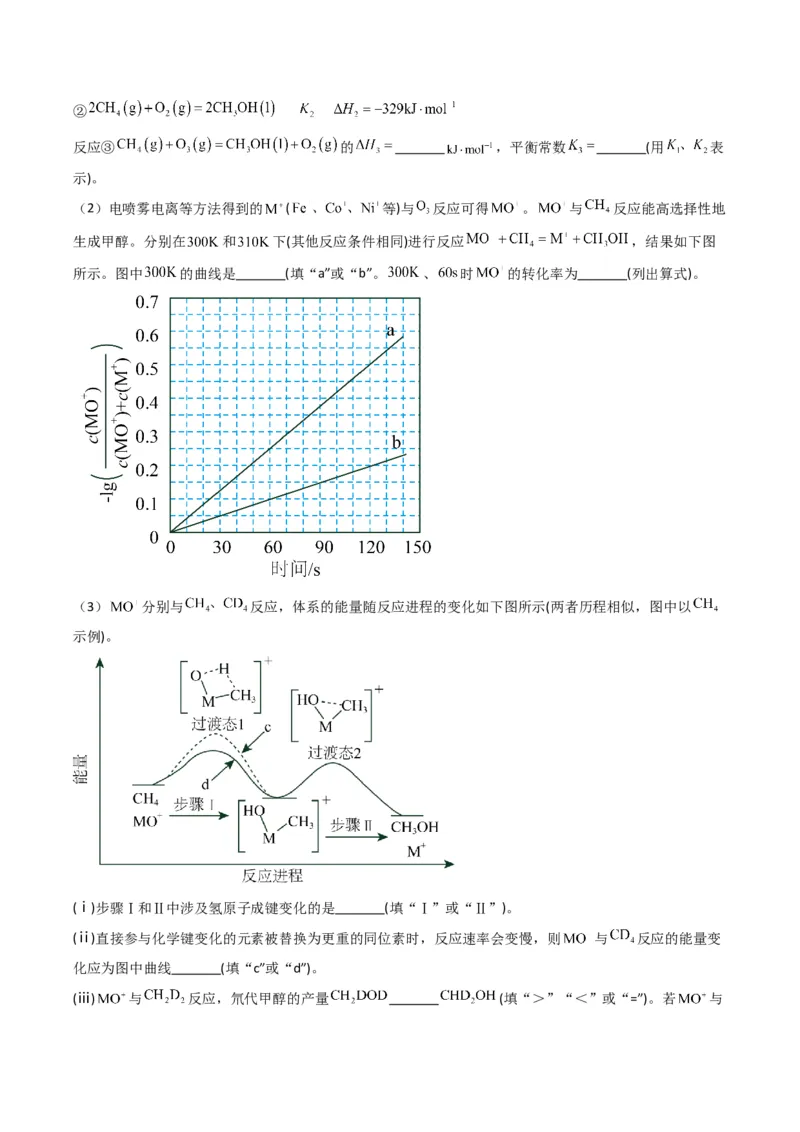
(2)电喷雾电离等方法得到的 ( 等)与 反应可得 。 与 反应能高选择性地
生成甲醇。分别在 和 下(其他反应条件相同)进行反应 ,结果如下图
所示。图中 的曲线是 (填“a”或“b”。 、 时 的转化率为 (列出算式)。
(3) 分别与 反应,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以
示例)。
(ⅰ)步骤Ⅰ和Ⅱ中涉及氢原子成键变化的是 (填“Ⅰ”或“Ⅱ”)。
(ⅱ)直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢,则 与 反应的能量变
化应为图中曲线 (填“c”或“d”)。
(ⅲ) 与 反应,氘代甲醇的产量 (填“>”“<”或“=”)。若 与反应,生成的氘代甲醇有 种。
【答案】(1) 或
(2) b
(3) Ⅰ c <
2
【解析】(1)根据盖斯定律可知,反应③= (反应②-①),所以对应
;根据平衡常数表达式与热化学方程式之
间的关系可知,对应化学平衡常数 或 ,故答案为: ; 或 ;
(2)根据图示信息可知,纵坐标表示-lg( ),即与MO+的微粒分布系数成反比,与M+的微
粒分布系数成正比。则同一时间内,b曲线生成M+的物质的量浓度比a曲线的小,证明化学反应速率慢,
又因同一条件下降低温度化学反应速率减慢,所以曲线b表示的是300 K条件下的反应;
根据上述分析结合图像可知, 、 时-lg( )=0.1,则 =10-0.1,利用数
学关系式可求出 ,根据反应 可知,生成的M+即为转
化的 ,则 的转化率为 ;故答案为:b;
;
(3)(ⅰ)步骤Ⅰ涉及的是碳氢键的断裂和氢氧键的形成,步骤Ⅱ中涉及碳氧键形成,所以符合题意的是步
骤Ⅰ;
(ⅱ)直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢,则此时正反应活化能会增大,
根据图示可知, 与 反应的能量变化应为图中曲线c;
(ⅲ) 与 反应时,因直接参与化学键变化的元素被替换为更重的同位素时,步骤Ⅰ的活化能增大,
反应速率会变慢,则CH DOD更难获得,故产率: < ;根据反应机理可知,若 与
2
反应,生成的氘代甲醇可能为 或 共2种,故答案为:<;2。
1.(2024上·甘肃酒泉)氨是最重要的化学品之一,我国目前氨的生产能力位居世界首位。回答下列问题:能量转换关系
(1)根据如图数据判断H—H的键能为 。
(2)合成氨反应,根据上述反应机理,使用催化剂,该反应的 (填“增大”“减小”或
“不变”),写出(ⅱ)步的热化学方程式: ;计算反应 的
。
(3)用 催化还原 还可以消除氮氧化物的污染。
写出 被 还原生成 的热化学方程式: 。
【答案】(1)
(2) 不变
(3)
【解析】(1)根据如图所示, ,吸收的能量为654kJ数据判断H—H的键能为
;
(2)使用催化剂,只改变反应历程,降低活化能,不改变反应的焓变,所以 不变;第(ⅱ)步的热化
学方程式为: ;根据如图所示数据,反应 的
;
(3)根据已知反应, 被 还原生成 的化学方程式为:
, ,热化学方程式为:
。
2.(2023下·湖北武汉·高三华中师大一附中校联考)一定温度下,向容器相同的恒容密闭容器中充入
1mol M和W的混合物气体和4mol N,发生如下反应反应Ⅰ.
反应Ⅱ.
实验测得起始充入的 与M和W的平衡转化率的关系如图所示。下列说法正确的是
A.曲线 表示起始充入的 与M的平衡转化率的关系
B.x>1
C.若M和W的转化率均处于b点状态时,反应Ⅰ和Ⅱ均存在
D.若缩小容器的容积,达到新平衡后P的体积分数与原平衡相等
【答案】B
【解析】A.W只是Ⅱ的反应物, 增大,W的平衡转化率增大, 表示起始充入的 与W的平
衡转化率的关系,A项错误;
B.根据2个反应方程式可知,当x=1时,即M和W等物质的量,M的平衡转化率大于W,当x>1时,M
的平衡转化率才可能等于W,B项正确;
C.对于反应Ⅰ: ,对于反应Ⅱ: ,C项错误;
D.缩小容器体积,反应Ⅱ正向进行,M减小,Q增多,反应Ⅰ逆向进行,P的体积分数改变,D项错误;
故选B。
3.Binoist等进行了H S热分解实验:2H S(g) 2H (g)+S (g),开始时,当1 mol H S与23.75 mol Ar混合,
2 2 2 2 2
在101 kPa及不同温度下反应达平衡时H 、H S及S (g)的体积分数如图所示,该反应在Q点对应温度下的平
2 2 2
衡常数K= kPa(K 为以分压表示的平衡常数,分压=总压×物质的量分数,结果保留小数点后两
p p
位)【答案】1.01
【解析】设S (g)的生成量为a mol,则有
2
Q点:1-2a=2a,a=0.25
p(H S)= ×101 kPa=2.02 kPa=p(H ),p(S )= ×101 kPa=1.01 kPa,K=
2 2 2
=1.01 kPa。
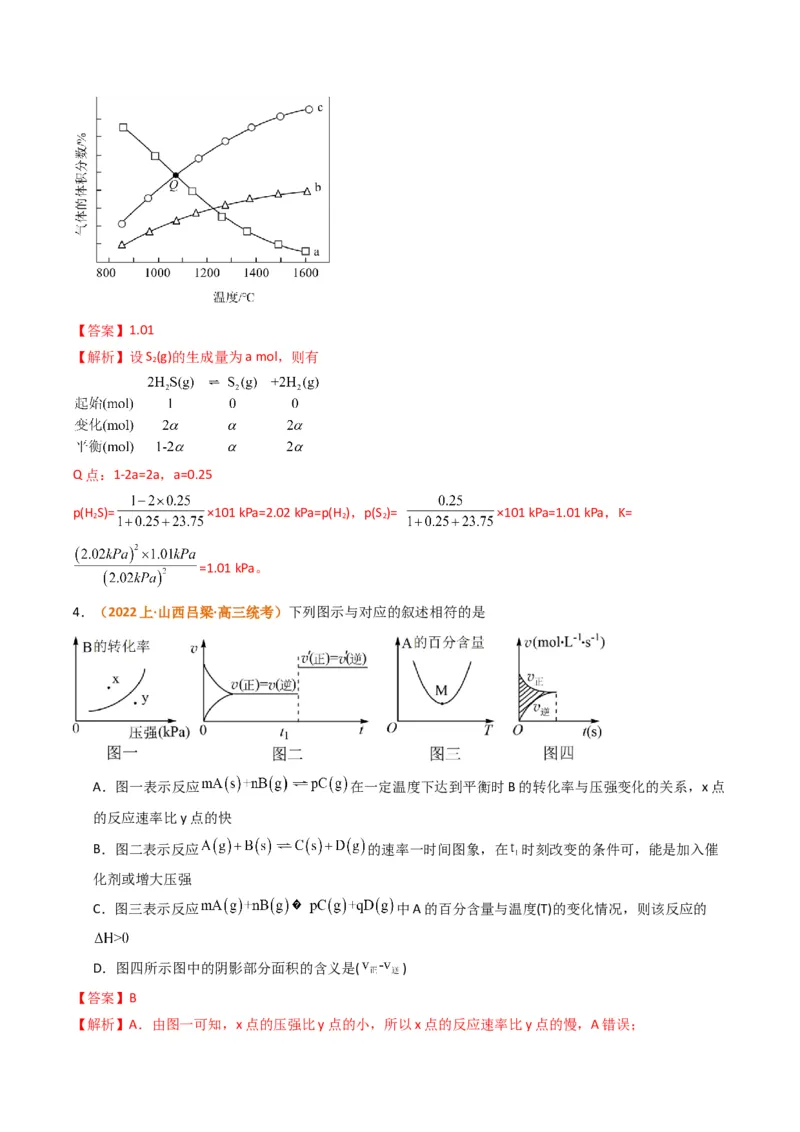
4.(2022上·山西吕梁·高三统考)下列图示与对应的叙述相符的是
A.图一表示反应 在一定温度下达到平衡时B的转化率与压强变化的关系,x点
的反应速率比y点的快
B.图二表示反应 的速率一时间图象,在 时刻改变的条件可,能是加入催
化剂或增大压强
C.图三表示反应 中A的百分含量与温度(T)的变化情况,则该反应的
D.图四所示图中的阴影部分面积的含义是( )
【答案】B
【解析】A.由图一可知,x点的压强比y点的小,所以x点的反应速率比y点的慢,A错误;B.由图二可知,在 时刻正、逆反应速率都增大且增大的程度相同,所以改变的条件可能是加入催化剂或
增大压强,B正确;
C.由图三可知,在M点之前,反应未达平衡,在M点之后,随着温度的不断升高,A的百分含量不断增
大,则平衡逆向移动,所以该反应的 ,C错误;
D.图四表示速率-时间关系曲线,图中的阴影部分面积的含义是 ,D错误。
答案选B。
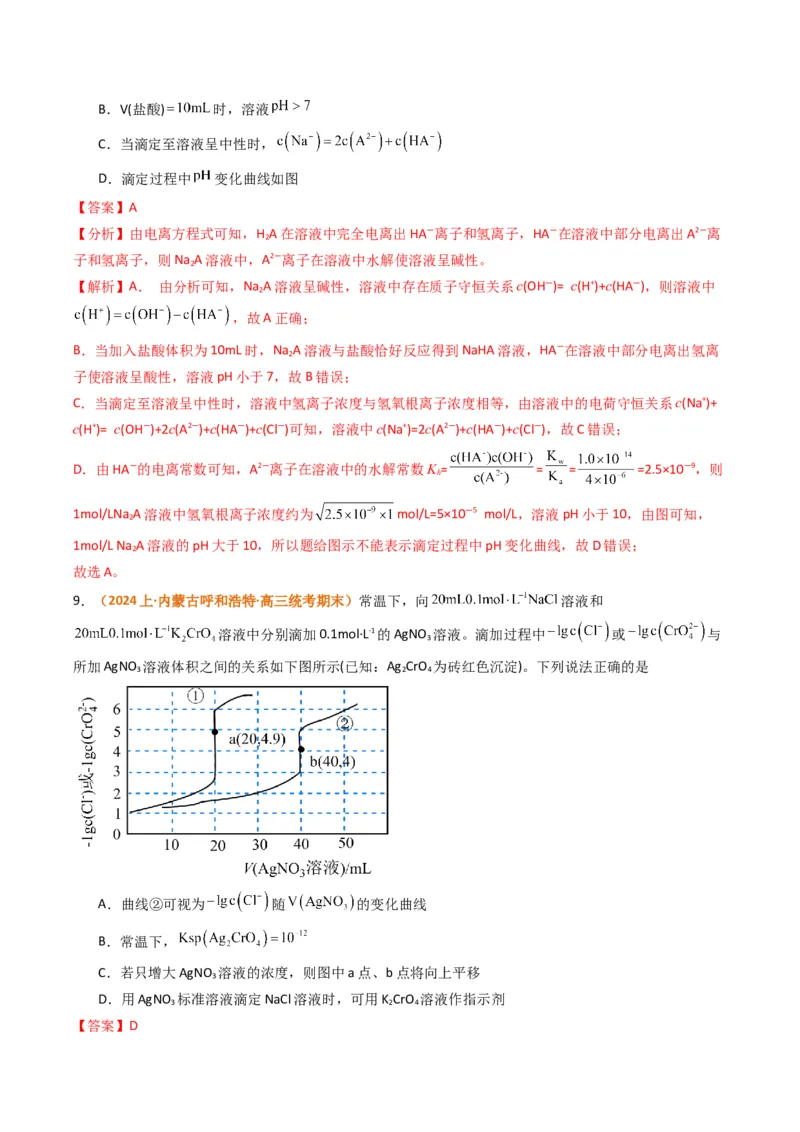
5.(2024上·江苏南通·高三校联考)二氧化碳的资源化利用对实现“双碳”有着重要意义。二氧化碳加氢
制甲烷过程中的主要反应为
在密闭容器中, 、 时, 平衡转化率、在催化剂作用下反应相同
时间所测得的 实际转化率随温度的变化如题图所示。 的选择性可表示为 。下列
说法正确的是
A.反应
B. 的选择性一定随着温度的升高而增加
C.用该催化剂催化二氧化碳反应的最佳温度约为 的原因是此温度下 的平衡转化率接近
100%
D. 时,提高 的值或增大压强,均能使 平衡转化率达到X点的值
【答案】D
【解析】A.① ,
② ,
根据盖斯定律:①-②计算反应 的焓变
,A错误;
B.生成CH 的反应是放热反应,升高温度时平衡逆向移动,CH 的物质的量减小,温度达到550°C后CO
4 4 2平衡转化率增大,则CH 的选择性降低,B错误;
4
C.由图可知,400℃时CO 实际转化率最大,由图可知,用该催化剂催化二氧化碳反应的最佳温度范围约
2
为350~400°C,C错误;
D.生成CH 的反应是气体体积减小的反应,增大压强、增大氢气的浓度均能使平衡正向移动,有利于提高
4
CO 平衡转化率,即温度一定时提高 的值或增大压强,均能使CO 平衡转化率达到X点的值,D
2 2
正确;
答案选D。
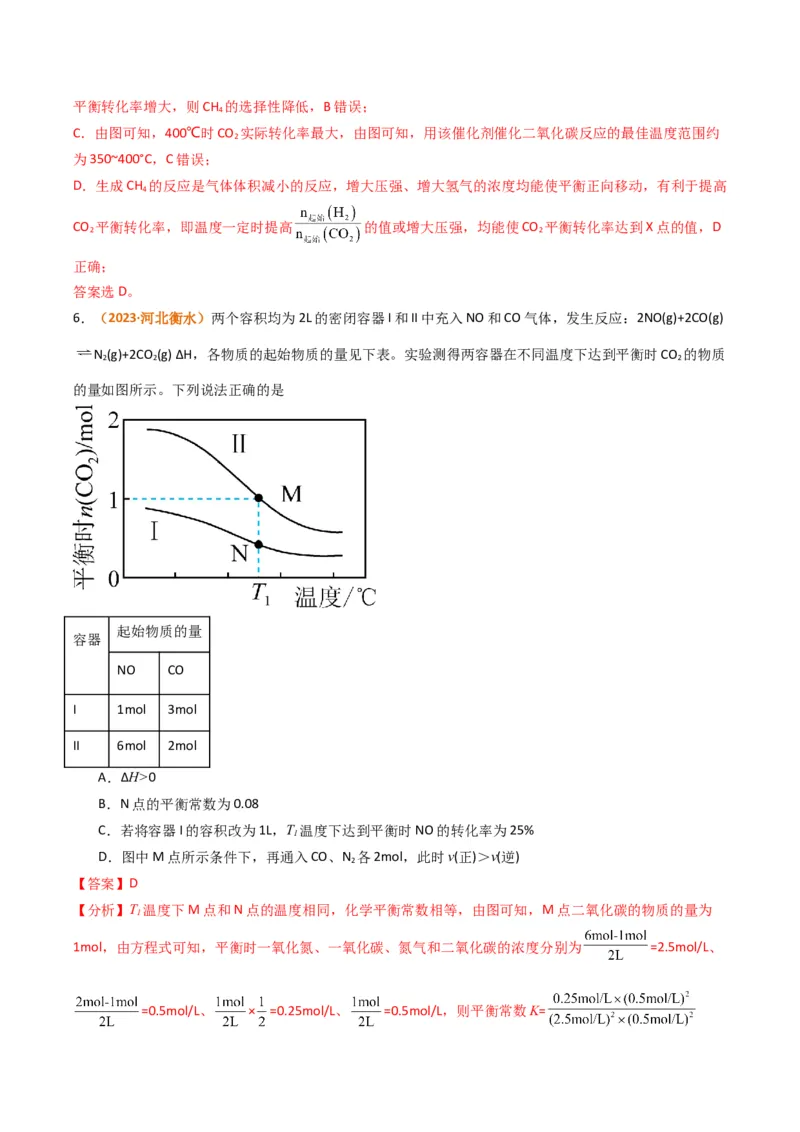
6.(2023·河北衡水)两个容积均为2L的密闭容器I和II中充入NO和CO气体,发生反应:2NO(g)+2CO(g)
N (g)+2CO (g) ΔH,各物质的起始物质的量见下表。实验测得两容器在不同温度下达到平衡时CO 的物质
2 2 2
的量如图所示。下列说法正确的是
起始物质的量
容器
NO CO
I 1mol 3mol
II 6mol 2mol
A.ΔH>0
B.N点的平衡常数为0.08
C.若将容器I的容积改为1L,T 温度下达到平衡时NO的转化率为25%
1
D.图中M点所示条件下,再通入CO、N 各2mol,此时v(正)>v(逆)
2
【答案】D
【分析】T 温度下M点和N点的温度相同,化学平衡常数相等,由图可知,M点二氧化碳的物质的量为
1
1mol,由方程式可知,平衡时一氧化氮、一氧化碳、氮气和二氧化碳的浓度分别为 =2.5mol/L、
=0.5mol/L、 × =0.25mol/L、 =0.5mol/L,则平衡常数K==0.04。
【解析】A.由图可知,温度升高,平衡时二氧化碳的物质的量减小,说明升高温度,平衡向逆反应方向
移动,该反应为放热反应,反应ΔH<0,故A错误;
B.由分析可知,N点的平衡常数为0.04,故B错误;
C.化学平衡常数是温度函数,温度不变,化学平衡常数不变,设T 温度下达到平衡时NO的转化率为
1
25%,由方程式可知,平衡时一氧化氮、一氧化碳、氮气和二氧化碳的浓度分别为
=0.75mol/L、 =2.75mol/L、 × =0.125mol/L、 =0.25mol/L,平衡常数
K= ≈0.0018≠0.04,故C错误;
D.若图中M点所示条件下,再通入一氧化碳和氮气各2mol,此时一氧化氮、一氧化碳、氮气和二氧化碳
的浓度分别为2.5mol/L、1.5mol/L、1.25mol/L、0.5mol/L,浓度熵Q=
c
≈0.022<0.04,则平衡向逆反应方向移动,反应速率v(正)>v(逆),故D正确;
故选D。
7.(2023·上海金山)在体积均为1.0L的恒容密闭容器甲、乙中,起始投料量如表,在不同温度下发生反
应:CO (g)+C(s) 2CO(g)。CO的平衡浓度随温度的变化如图所示。下列说法正确的是
2
容
n(CO )/mol n(C)/mol n(CO)/mol
2
器
甲 0.1 0.3 0
乙 0 0 0.4
A.曲线Ⅰ对应的是甲容器
B.a、b两点所处状态的压强大小关系:9p>14p
a b
C.c点:CO的体积分数>
D.900K时,若起始向容器乙中加入CO、CO 、C各1mol,则v(正)>v(逆)
2【答案】C
【解析】A.固体物质不应平衡移动,乙投入0.4mol一氧化碳相当于投入0.2mol二氧化碳,所以乙相当于
两个甲容器加压,无论平衡如何移动,乙中一氧化碳浓度一定大于甲,故图中曲线Ⅰ对应的是乙容器,A
错误;
B.甲容器b处
乙容器a处
若a、b两点所处温度相同,压强比等于物质的量之比,p:p =(0.12+0.16):(0.02+0.16)=14:9,即
a b
9p=14p ,由于b点温度更高,故a、b两点所处状态的压强大小关系:9p<14p ,B错误;
a b a b
C.a点一氧化碳体积分数为 ;c点相当于减压,平衡正向移动,一氧化碳体积分数变大,故
CO的体积分数> ,正确;
D.a点1100K时的K= ,降温则一氧化碳浓度减小,K值减小,900K时K值小于0.213;若起
始向容器乙中加入CO、CO 、C各1mol,则Q= ,平衡逆向移动,v(正)