文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(福建专用)
黄金卷04
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5 Fe-56 Co-59 Cu-64
第Ⅰ卷
一、单项选择题:共10题,每题4分,共40分。每题只有一个选项最符合题意。
1.中华文化源远流长,化学与文化传承密不可分。下列说法错误的是
A.青铜器“四羊方尊”的主要成分为金属材料
B.制作宣纸的材料,其主要成分是天然有机高分子材料
C.用皮影戏生动讲述航天故事,制作皮影的兽皮是合成高分子材料
D.陶瓷是以黏土为主要原料,经高温烧结而成,它的主要成分为无机非金属材料
【答案】C
【详解】A.青铜是合金,属于金属材料,故A正确;
B.制作宣纸材料的主要成分是纤维素,属于天然有机高分子,故B正确;
C.兽皮的主要成分是蛋白质,属于天然有机高分子材料,不是合成高分子材料,故C错误;
D.陶瓷的主要成分是硅酸盐,属于传统无机非金属材料,故D正确;
故选C。
2.已知异丙烯苯可发生如下转化,下列说法正确的是
A.高聚物M的链节为
B.异丙烯苯与足量氢气完全加成所得产物的一氯代物有5种
C.可用酸性 溶液鉴别异丙烯苯和异丙苯D.异丙烯苯分子中最多有17个原子共平面
【答案】D
【分析】异丙烯苯在催化剂作用下生成高聚物M,链节为 ;异丙烯苯与氢气在一定条件下生
成异丙苯。
【详解】A.高聚物M的链节为 ,A错误;
B.异丙烯苯与足量氢气完全加成所得产物为 ,分子中含有6种化学环境的氢原子,故一氯
代物有6种,B错误;
C.异丙烯苯和异丙苯均与酸性 溶液反应,故不能用酸性 鉴别二者,C错误;
D.苯环和碳碳双键分别确定一个平面,通过旋转双键碳与苯环之间的碳碳单键,可以使两个平面重合,
此时,异丙烯苯分子中最多有17个原子共平面,D正确;
故选D。
3.设 为阿伏加德罗常数的值,下列说法正确的是
A. 中 杂化的碳原子数目为1
B. 溶液中所含 数目为
C.标准状况下, 中含有的电子数目为
D.常温下,将 投入足量浓硝酸中,反应转移电子数目为
【答案】A
试卷第2页,共3页【详解】A.CHCHO中甲基中碳原子采用sp3杂化,醛基上碳原子采用sp2杂化, (为
3
1mol)中 杂化的碳原子数目为1 ,A正确;
B. 溶液中铜元素以四氨合铜离子存在,不存在单独的 ,B错误;
C.标准状况下HF为液体,故无法计算中含有的电子数目,C错误;
D.常温下Fe遇到浓硝酸将发生钝化,将投入足量浓硝酸中,无法计算反应转移电子数目,D错误;
故选B。
4.下列有关离子方程式错误的是
A.硫酸铜溶液加入饱和氯化钠:
B.向 溶液中通入少量的SO :
2
C. 溶液滴入FeCl 溶液中:
2
D.Cl 溶于水:
2
【答案】B
【详解】A.硫酸铜溶液加入饱和氯化钠,氯离子与铜离子形成 络离子,溶液中存在
,A正确;
B.向 溶液中通入少量的SO ,发生氧化还原反应生成硫酸钙,B错误;
2
C. 溶液滴入FeCl 溶液中,生成 沉淀,C正确;
2
D.Cl 溶于水生成盐酸和次氯酸,次氯酸为弱酸不拆,D正确;
2
故选B。
5.含氰废水中氰化物的主要形态是HCN和CN-,CN-具有较强的配位能力,能与Cu+形成一种无限长链离
子,其片段为 ;CN-结合H+能力弱于CO 。氰化物浓度较低时,可在碱性条件
下用HO 或Cl 将其转化为N;浓度较高时,可加入HCN、Fe和KCO 溶液反应生成K[Fe(CN) ]溶液。
2 2 2 2 2 3 4 6
下列物质性质与用途具有对应关系的是A.N 的化学性质稳定,可用于金属焊接保护
2
B.HO 具有还原性,可用于处理含氰废水
2 2
C.FeCl 溶液显酸性,可用于刻蚀覆铜板
3
D.NaHCO 受热易分解,可用于治疗胃酸过多
3
【答案】A
【详解】A.N 的化学性质稳定,可用于金属焊接保护,A正确;
2
B.HO 可将氰化物转化为氮气,氰化物中N元素化合价升高,作还原剂,则HO 在该反应中表现氧化性,
2 2 2 2
B错误;
C.FeCl 能与Cu生成可溶性氯化铜,表现出较强氧化性,可用于蚀刻印刷电路板,与FeCl 溶液显酸性无
3 3
关,C错误;
D.NaHCO 性质不稳定,受热易发生分解反应生成CO,CO 能使面团松软多孔,可用作食品膨松剂;能
3 2 2
治理胃酸过多是因为能与胃酸中的盐酸反应,D错误;
答案选A。
6.前四周期元素X、Y、Z、M原子序数依次增大,由这四种元素形成的一种常见的血红色配离子的结构
如图所示,该离子中X、Y、Z都满足8电子结构。下列说法错误的是
A.电负性:Y>Z>X>M B.该配离子中M的配位数为6
C. 离子中X为sp杂化 D.该配离子中所有键角都为180°
【答案】D
【分析】血红色配离子为 ,X、Y、Z、M原子序数依次增大,该离子中X、Y、Z都满足8
电子结构,则X为C元素、Y为N元素、Z为S元素;M为Fe元素。
【详解】A. 元素非金属性越强电负性越大,电负性:N>S>C>Fe,故A正确;
B. 该配离子中Fe3+与N原子形成6个配位键,配位数为6,故B正确;
C.SCN-离子中C原子形成4个共价键,无孤电子对,有2个σ键,价电子对数为2,采用sp杂化,故C正
确;
D.该配离子的空间构型为正八面体,6个配位键的夹角都为90°,故D错误;
试卷第4页,共3页选D。
7.根据下列实验操作和现象所得到的结论正确的是
选
实验操作和现象 结论
项
A 向 溶液中通入 气体,有沉淀生成 酸性:
的溶解性符合“相似相
B 向5 mL碘水中加入1 mL 振荡,静置,上层无色,下层紫色
溶”规律
C 向滴有酚酞的氨水中加入 固体,溶液的红色变浅 溶液呈酸性
将石油分馏的产品石蜡加热,产生的气体通入酸性高锰酸钾溶液中,
D 石油中含有烯烃
溶液紫红色逐渐褪去
A.A B.B C.C D.D
【答案】B
【详解】A.ClO-具有强氧化性能将SO 氧化成SO ,因此本实验不能比较HClO、HSO 酸性强弱,故A
2 2 3
错误;
B.碘单质、四氯化碳均为非极性分子,四氯化碳的密度大于水,下层呈紫色,应是碘的四氯化碳溶液,
说明碘单质溶于四氯化碳,符合“相似相溶”规律,故B正确;
C.氨水中存在NH ·H O NH +OH-,加入醋酸铵,c(NH )增大,抑制NH ·H O电离,c(OH-)减小,不
3 2 3 2
能说明醋酸铵溶液呈酸性,NH ·H O、CHCOOH的电离平衡常数相同,因此NH 、CHCOO-水解常数相
3 2 3 3
同,即醋酸铵溶液显中性,故C错误;
D.产生的气体通入酸性高锰酸钾溶液中,溶液紫红色逐渐褪去,说明气体中含有不饱和烃,故D错误;
答案为B。
8.以浓差电池(因电解质溶液浓度不同而形成的电池)为电源,以石墨为电极将 转化为高纯 的装置
如图。下列说法错误的是A.电解过程中,丙池溶液的 会减小
B.转移 时乙室电解质溶液质量减少
C.停止工作后若要使电池恢复原状态, 连接的是电源负极
D.N极电极反应式为:
【答案】B
【分析】由题意知,右池为电解NH 生成H 的装置,左池为浓差电池,右池电极M区NH 失电子被氧化
3 2 3
为N,故电极M为阳极,发生电极反应:2NH -6e-+6OH-=N ↑+6H O,则N为阴极,发生电极反应:
2 3 2 2
2HO+2e- =H ↑+2OH-,所以左池Cu(1)为正极,正极发生反应:Cu2++2e=Cu,Cu (2)为负极,负极发
2 2
生反应:Cu-2e-=Cu2+。
【详解】A.电极M为阳极,发生电极反应:2NH -6e-+6OH-=N ↑+6H O,消耗了OH-,碱性减弱,pH减
3 2 2
小,A正确;
B.转移2mol电子时,Cu(1)极析出1mol铜,即64g,同时有1mol即96g硫酸根从乙室到甲室,乙室电
解质溶液质量共减少64g+96g=160g,B错误;
C.恢复原浓差Cu(2)电极需发生还原反应,Cu2+放电析出铜单质,所以和电源负极相连,C正确;
D.N 为阴极,电极反应式为:2HO+2e- =H ↑+2OH-,D正确;
2 2
故选B。
9.一定温度、某催化剂条件下,物质A在某有机溶剂中同时发生以下两个反应:
① ;② 。反应①的速率可表示为 ,反应
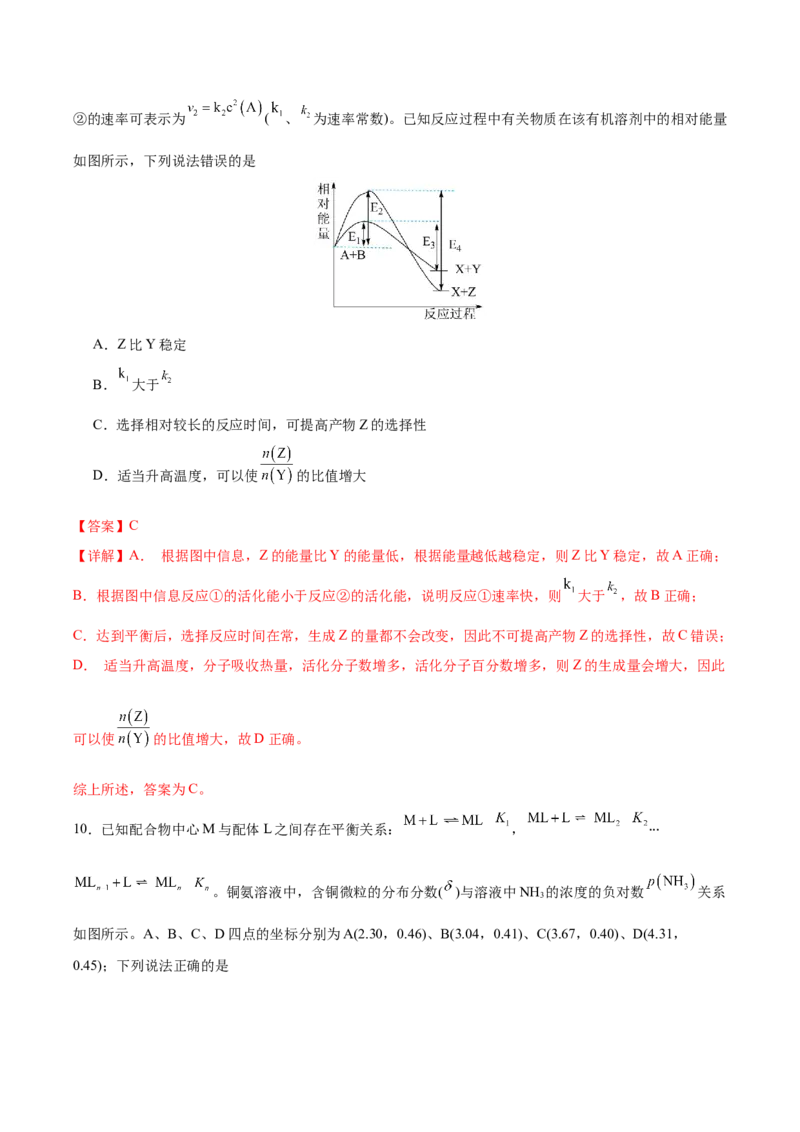
试卷第6页,共3页②的速率可表示为 ( 、 为速率常数)。已知反应过程中有关物质在该有机溶剂中的相对能量
如图所示,下列说法错误的是
A.Z比Y稳定
B. 大于
C.选择相对较长的反应时间,可提高产物Z的选择性
D.适当升高温度,可以使 的比值增大
【答案】C
【详解】A. 根据图中信息,Z的能量比Y的能量低,根据能量越低越稳定,则Z比Y稳定,故A正确;
B.根据图中信息反应①的活化能小于反应②的活化能,说明反应①速率快,则 大于 ,故B正确;
C.达到平衡后,选择反应时间在常,生成Z的量都不会改变,因此不可提高产物Z的选择性,故C错误;
D. 适当升高温度,分子吸收热量,活化分子数增多,活化分子百分数增多,则Z的生成量会增大,因此
可以使 的比值增大,故D正确。
综上所述,答案为C。
10.已知配合物中心M与配体L之间存在平衡关系: , ∙∙∙
。铜氨溶液中,含铜微粒的分布分数( )与溶液中NH 的浓度的负对数 关系
3
如图所示。A、B、C、D四点的坐标分别为A(2.30,0.46)、B(3.04,0.41)、C(3.67,0.40)、D(4.31,
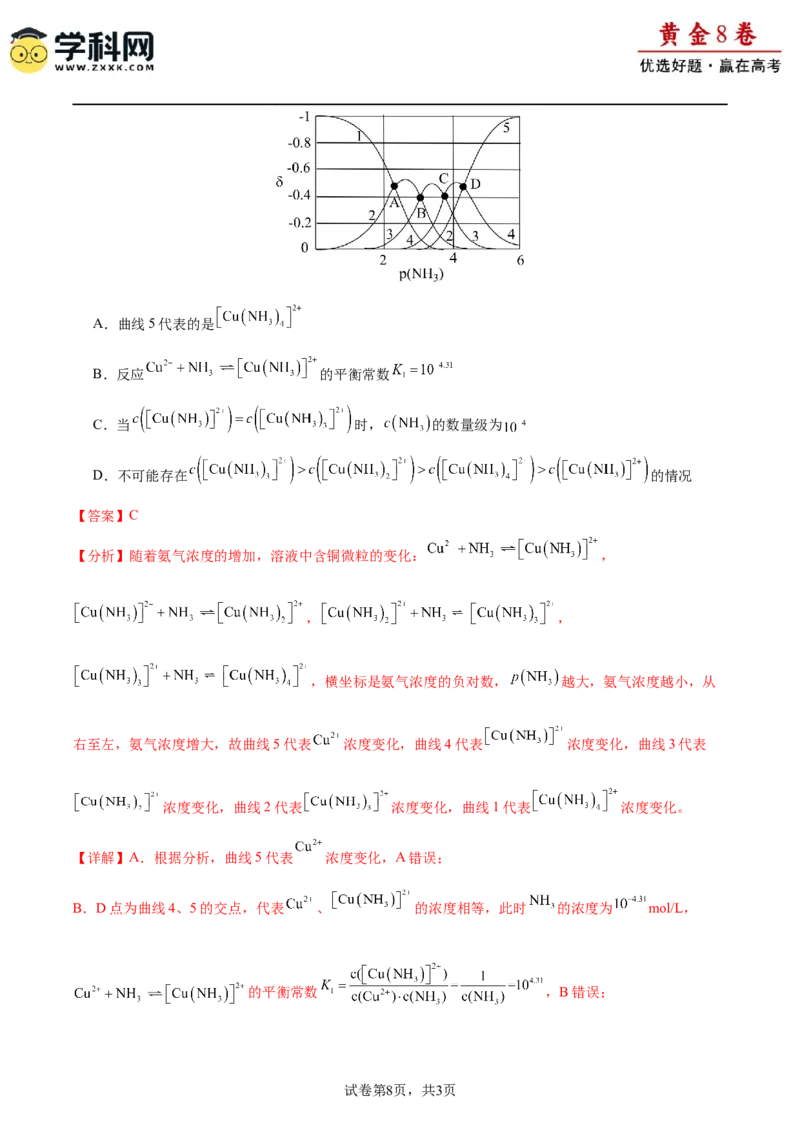
0.45);下列说法正确的是A.曲线5代表的是
B.反应 的平衡常数
C.当 时, 的数量级为
D.不可能存在 的情况
【答案】C
【分析】随着氨气浓度的增加,溶液中含铜微粒的变化: ,
, ,
,横坐标是氨气浓度的负对数, 越大,氨气浓度越小,从
右至左,氨气浓度增大,故曲线5代表 浓度变化,曲线4代表 浓度变化,曲线3代表
浓度变化,曲线2代表 浓度变化,曲线1代表 浓度变化。
【详解】A.根据分析,曲线5代表 浓度变化,A错误;
B.D点为曲线4、5的交点,代表 、 的浓度相等,此时 的浓度为 mol/L,
的平衡常数 ,B错误;
试卷第8页,共3页C.当 时,是曲线4和曲线2的交点,横坐标 数值大于3小于
4,故 的数量级为 ,C正确;
D.曲线1、3交点右侧附近对应的位置,存在
的情况,D错误;
故选C。
第Ⅱ卷
二、非选择题:共4题,共60分。
11.(15分)从某冶锌工厂的工业废料[除ZnO和少量Fe O 外,还含有铟(In)、铋(Bi)、锗(Ge)的氧化物]中回
2 3
收几种金属的单质或化合物的工业流程如图:
已知:该工艺条件下, , 。
请回答下列问题:
(1)下列措施更有利于完成“酸浸l”目的,提高“酸浸l”浸取率的是 (填选项字母)。
a.适当升高温度 b.酸浸过程中不断搅拌
c.将硫酸浓度增大到70% d.加大废料的用量
(2)“酸浸2”时铋的氧化物( )发生反应的离子方程式为 。
(3)“沉锗”的反应原理为 ,该操作中需调节pH为2.5,不能过高或过低,
原因是 。
(4)①配离子[Zn(NH )(H O) ]3+的空间结构只有1种,由此推知[Zn(NH )]2+的空间结构是 。
3 2 2 2 3 4
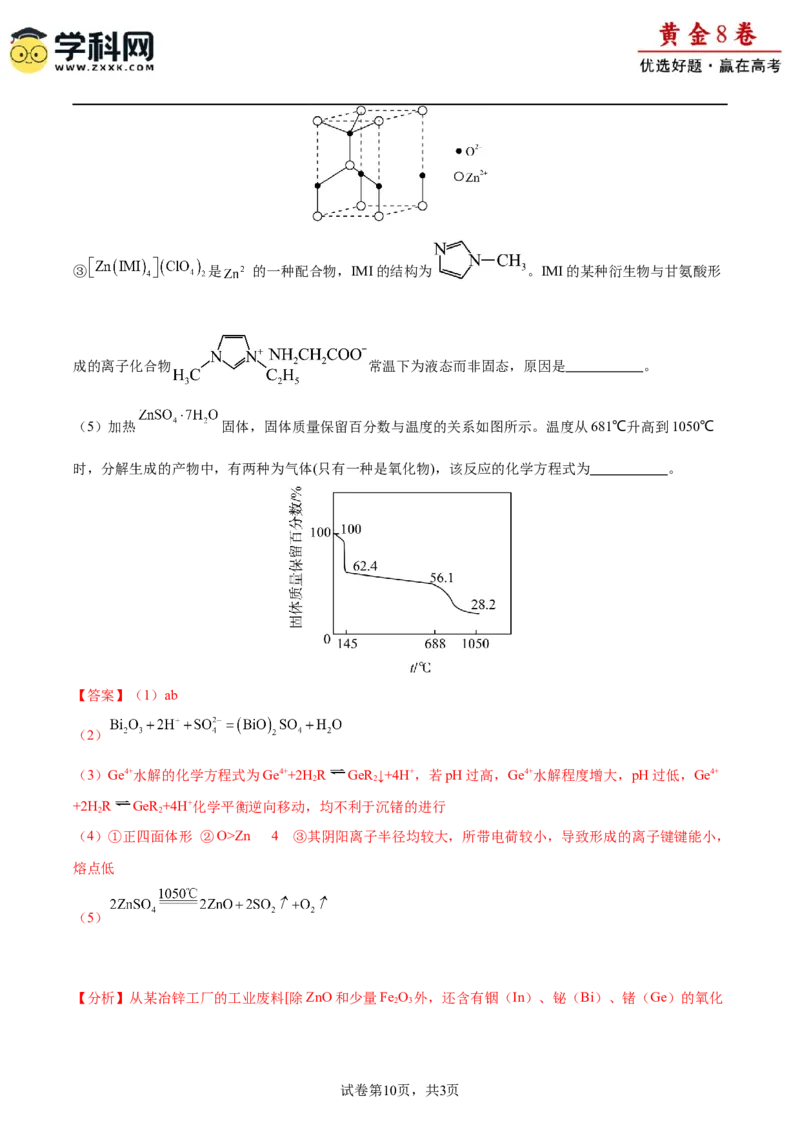
②氧化锌有多种晶体结构,其中一种晶胞结构与六方硫化锌的晶胞结构相同,其晶胞如图所示。Zn、O两
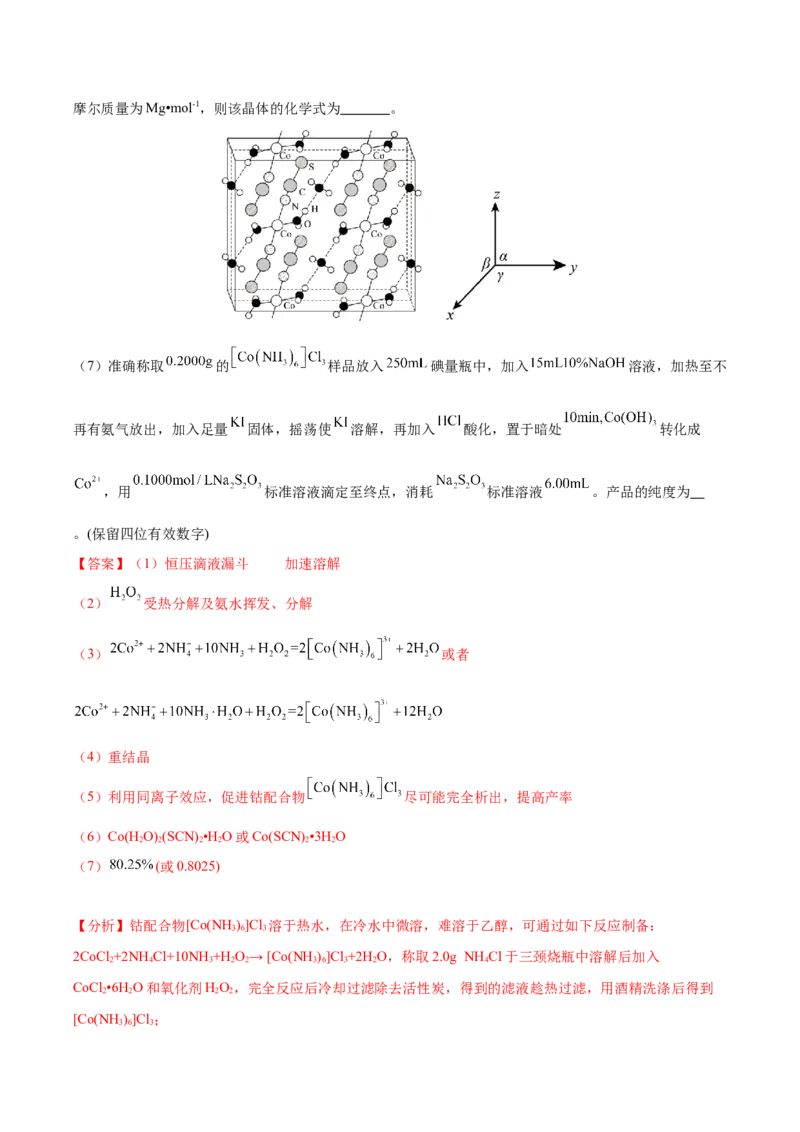
种元素的电负性大小顺序为 ,晶体中锌离子的配位数为 。③ 是 的一种配合物,IMI的结构为 。IMI的某种衍生物与甘氨酸形
成的离子化合物 常温下为液态而非固态,原因是 。
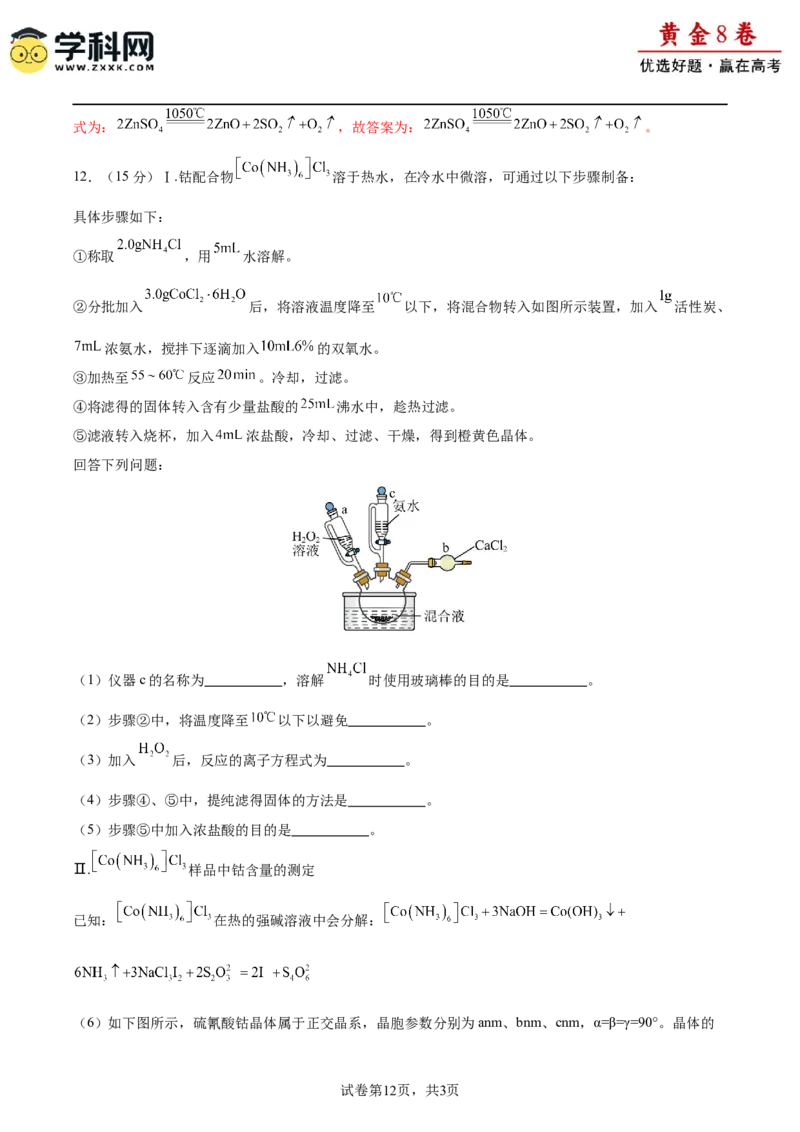
(5)加热 固体,固体质量保留百分数与温度的关系如图所示。温度从681℃升高到1050℃
时,分解生成的产物中,有两种为气体(只有一种是氧化物),该反应的化学方程式为 。
【答案】(1)ab
(2)
(3)Ge4+水解的化学方程式为Ge4++2H R GeR ↓+4H+,若pH过高,Ge4+水解程度增大,pH过低,Ge4+
2 2
+2H R GeR +4H+化学平衡逆向移动,均不利于沉锗的进行
2 2
(4)①正四面体形 ②O>Zn 4 ③其阴阳离子半径均较大,所带电荷较小,导致形成的离子键键能小,
熔点低
(5)
【分析】从某冶锌工厂的工业废料[除ZnO和少量Fe O 外,还含有铟(In)、铋(Bi)、锗(Ge)的氧化
2 3
试卷第10页,共3页物]中回收几种金属的单质或化合物,工业废料加入稀硫酸,氧化锌、氧化铁和硫酸反应,过滤后浸液1中
含有硫酸锌和硫酸铁,调节pH使铁离子沉淀,溶液浓缩结晶得到硫酸锌的晶体;浸渣加入70%硫酸,得
到铋渣和浸液2,浸液2加入P2O4煤油进行萃取,有机相中加入盐酸进行反萃取,得到水相,再经过一系
列处理德奥海绵铟,水相加入单宁酸进行沉锗,过滤得到滤渣,然后焙烧、氯化蒸馏得到GeCl ,据此解
4
答。
【详解】(1)a.适当升高温度可提高反应速率,提高“酸浸1”浸取率,a正确;
b.酸浸过程中不断搅拌可增大接触面积,提高反应速率,提高“酸浸1”浸取率,b正确;
c.将硫酸浓度增大到70%会浸出铟、锗,不可取,c错误;
d加大废料的用量不会提高“酸浸1”浸取率,d错误,
故答案为:ab;
(2)“酸浸2”时铋的氧化物(BiO)发生反应的离子方程式为BiO+2H++ =(BiO)SO ↓+H O,
2 3 2 3 2 4 2
故答案为:BiO+2H++ =(BiO)SO ↓+H O;
2 3 2 4 2
(3)“沉锗”的反应原理为Ge4++2H R GeR ↓+4H+,该操作中需调节pH为2.5,原因为pH高于2.5时
2 2
Ge4+水解程度增强,pH低于2.5时酸性太强,平衡逆移沉锗率下降,故答案为:Ge4+水解的化学方程式为
Ge4++2H R GeR ↓+4H+,若pH过高,Ge4+水解程度增大,pH过低,Ge4++2H R GeR +4H+化学平衡逆
2 2 2 2
向移动,均不利于沉锗的进行;
(4)①配离子[Zn(NH )(H O) ]3+的空间结构只有1种,说明[Zn(NH )(H O) ]3+的空间结构为四面体,由此
3 2 2 2 3 2 2 2
推知[Zn(NH )]2+的空间结构是正四面体。
3 4
②Zn、O电负性排序为Zn