文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(福建专用)
黄金卷04
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5 Fe-56 Co-59 Cu-64
第Ⅰ卷
一、单项选择题:共10题,每题4分,共40分。每题只有一个选项最符合题意。
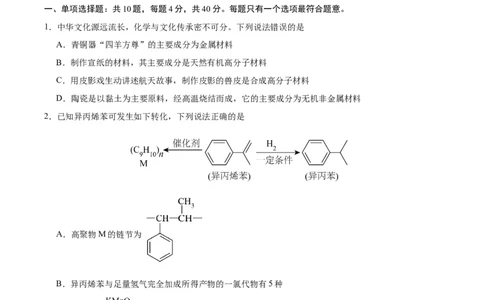
1.中华文化源远流长,化学与文化传承密不可分。下列说法错误的是
A.青铜器“四羊方尊”的主要成分为金属材料
B.制作宣纸的材料,其主要成分是天然有机高分子材料
C.用皮影戏生动讲述航天故事,制作皮影的兽皮是合成高分子材料
D.陶瓷是以黏土为主要原料,经高温烧结而成,它的主要成分为无机非金属材料
2.已知异丙烯苯可发生如下转化,下列说法正确的是
A.高聚物M的链节为
B.异丙烯苯与足量氢气完全加成所得产物的一氯代物有5种
C.可用酸性 溶液鉴别异丙烯苯和异丙苯
D.异丙烯苯分子中最多有17个原子共平面
3.设 为阿伏加德罗常数的值,下列说法正确的是
A. 中 杂化的碳原子数目为1
B. 溶液中所含 数目为C.标准状况下, 中含有的电子数目为
D.常温下,将 投入足量浓硝酸中,反应转移电子数目为
4.下列有关离子方程式错误的是
A.硫酸铜溶液加入饱和氯化钠:
B.向 溶液中通入少量的SO :
2
C. 溶液滴入FeCl 溶液中:
2
D.Cl 溶于水:
2
5.含氰废水中氰化物的主要形态是HCN和CN-,CN-具有较强的配位能力,能与Cu+形成一种无限长链离
子,其片段为 ;CN-结合H+能力弱于CO 。氰化物浓度较低时,可在碱性条件
下用HO 或Cl 将其转化为N;浓度较高时,可加入HCN、Fe和KCO 溶液反应生成K[Fe(CN) ]溶液。
2 2 2 2 2 3 4 6
下列物质性质与用途具有对应关系的是
A.N 的化学性质稳定,可用于金属焊接保护
2
B.HO 具有还原性,可用于处理含氰废水
2 2
C.FeCl 溶液显酸性,可用于刻蚀覆铜板
3
D.NaHCO 受热易分解,可用于治疗胃酸过多
3
6.前四周期元素X、Y、Z、M原子序数依次增大,由这四种元素形成的一种常见的血红色配离子的结构
如图所示,该离子中X、Y、Z都满足8电子结构。下列说法错误的是
A.电负性:Y>Z>X>M B.该配离子中M的配位数为6
C. 离子中X为sp杂化 D.该配离子中所有键角都为180°
7.根据下列实验操作和现象所得到的结论正确的是
试卷第2页,共3页选项 实验操作和现象 结论
A 向 溶液中通入 气体,有沉淀生成 酸性:
的溶解性符合“相似相
B 向5 mL碘水中加入1 mL 振荡,静置,上层无色,下层紫色
溶”规律
C 向滴有酚酞的氨水中加入 固体,溶液的红色变浅 溶液呈酸性
将石油分馏的产品石蜡加热,产生的气体通入酸性高锰酸钾溶液
D 石油中含有烯烃
中,溶液紫红色逐渐褪去
A.A B.B C.C D.D
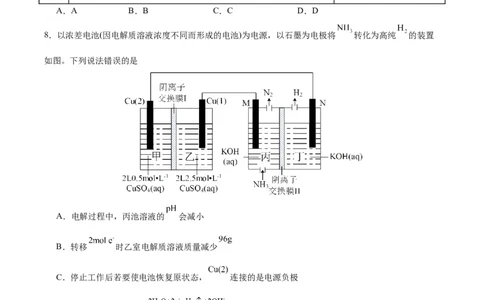
8.以浓差电池(因电解质溶液浓度不同而形成的电池)为电源,以石墨为电极将 转化为高纯 的装置
如图。下列说法错误的是
A.电解过程中,丙池溶液的 会减小
B.转移 时乙室电解质溶液质量减少
C.停止工作后若要使电池恢复原状态, 连接的是电源负极
D.N极电极反应式为:
9.一定温度、某催化剂条件下,物质A在某有机溶剂中同时发生以下两个反应:
① ;② 。反应①的速率可表示为 ,反应
②的速率可表示为 ( 、 为速率常数)。已知反应过程中有关物质在该有机溶剂中的相对能量
如图所示,下列说法错误的是A.Z比Y稳定
B. 大于
C.选择相对较长的反应时间,可提高产物Z的选择性
D.适当升高温度,可以使 的比值增大
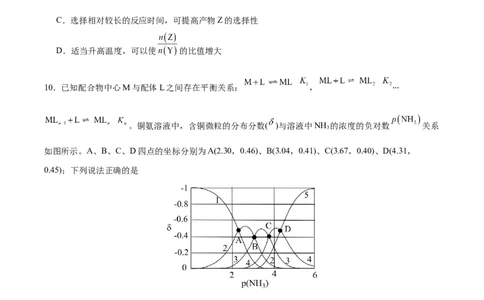
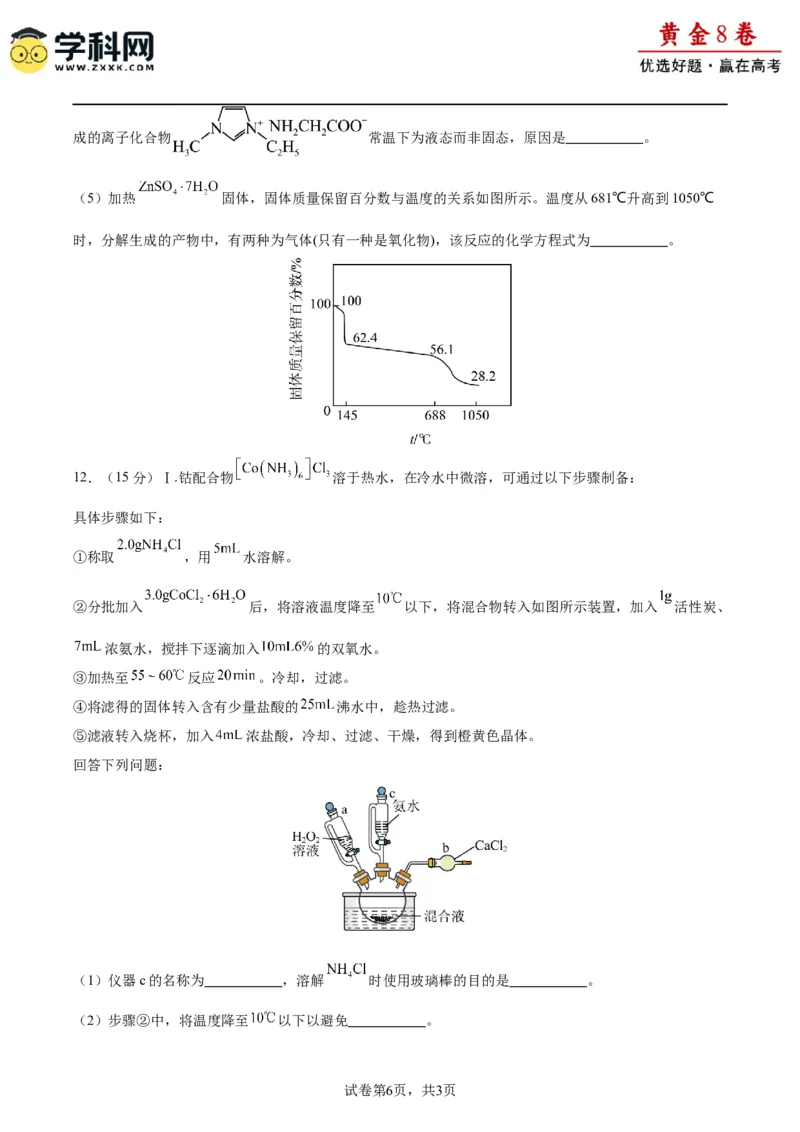
10.已知配合物中心M与配体L之间存在平衡关系: , ∙∙∙
。铜氨溶液中,含铜微粒的分布分数( )与溶液中NH 的浓度的负对数 关系
3
如图所示。A、B、C、D四点的坐标分别为A(2.30,0.46)、B(3.04,0.41)、C(3.67,0.40)、D(4.31,
0.45);下列说法正确的是
A.曲线5代表的是
B.反应 的平衡常数
C.当 时, 的数量级为
D.不可能存在 的情况
试卷第4页,共3页第Ⅱ卷
二、非选择题:共4题,共60分。
11.(15分)从某冶锌工厂的工业废料[除ZnO和少量Fe O 外,还含有铟(In)、铋(Bi)、锗(Ge)的氧化物]中回
2 3
收几种金属的单质或化合物的工业流程如图:
已知:该工艺条件下, , 。
请回答下列问题:
(1)下列措施更有利于完成“酸浸l”目的,提高“酸浸l”浸取率的是 (填选项字母)。
a.适当升高温度 b.酸浸过程中不断搅拌
c.将硫酸浓度增大到70% d.加大废料的用量
(2)“酸浸2”时铋的氧化物( )发生反应的离子方程式为 。
(3)“沉锗”的反应原理为 ,该操作中需调节pH为2.5,不能过高或过低,
原因是 。
(4)①配离子[Zn(NH )(H O) ]3+的空间结构只有1种,由此推知[Zn(NH )]2+的空间结构是 。
3 2 2 2 3 4
②氧化锌有多种晶体结构,其中一种晶胞结构与六方硫化锌的晶胞结构相同,其晶胞如图所示。Zn、O两
种元素的电负性大小顺序为 ,晶体中锌离子的配位数为 。
③ 是 的一种配合物,IMI的结构为 。IMI的某种衍生物与甘氨酸形成的离子化合物 常温下为液态而非固态,原因是 。
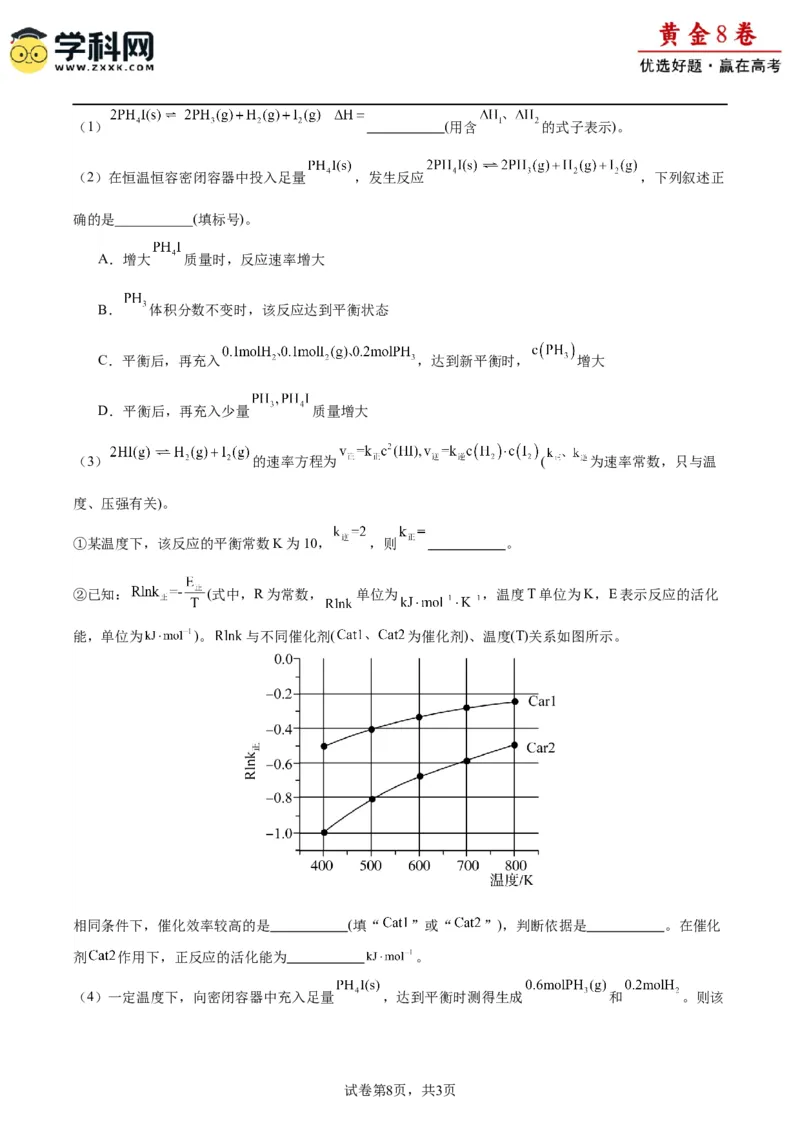
(5)加热 固体,固体质量保留百分数与温度的关系如图所示。温度从681℃升高到1050℃
时,分解生成的产物中,有两种为气体(只有一种是氧化物),该反应的化学方程式为 。
12.(15分)Ⅰ.钴配合物 溶于热水,在冷水中微溶,可通过以下步骤制备:
具体步骤如下:
①称取 ,用 水溶解。
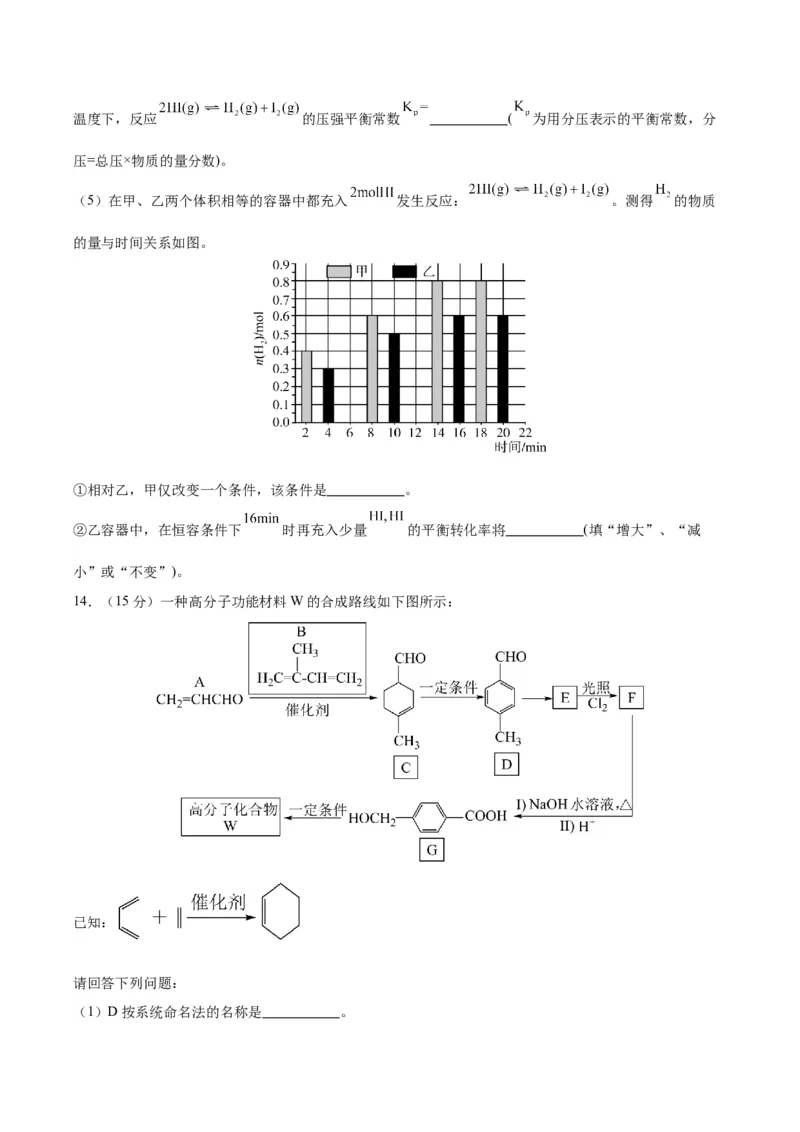
②分批加入 后,将溶液温度降至 以下,将混合物转入如图所示装置,加入 活性炭、
浓氨水,搅拌下逐滴加入 的双氧水。
③加热至 反应 。冷却,过滤。
④将滤得的固体转入含有少量盐酸的 沸水中,趁热过滤。
⑤滤液转入烧杯,加入 浓盐酸,冷却、过滤、干燥,得到橙黄色晶体。
回答下列问题:
(1)仪器c的名称为 ,溶解 时使用玻璃棒的目的是 。
(2)步骤②中,将温度降至 以下以避免 。
试卷第6页,共3页(3)加入 后,反应的离子方程式为 。
(4)步骤④、⑤中,提纯滤得固体的方法是 。
(5)步骤⑤中加入浓盐酸的目的是 。
Ⅱ. 样品中钴含量的测定
已知: 在热的强碱溶液中会分解:
(6)如下图所示,硫氰酸钴晶体属于正交晶系,晶胞参数分别为anm、bnm、cnm,α=β=γ=90°。晶体的
摩尔质量为Mg•mol-1,则该晶体的化学式为 。
(7)准确称取 的 样品放入 碘量瓶中,加入 溶液,加热至不
再有氨气放出,加入足量 固体,摇荡使 溶解,再加入 酸化,置于暗处 转化成
,用 标准溶液滴定至终点,消耗 标准溶液 。产品的纯度为
。(保留四位有效数字)
13.(15分)已知: 是一种重要的化工品,在一定温度下可发生分解反应:
①
②
回答下列问题:(1) (用含 的式子表示)。
(2)在恒温恒容密闭容器中投入足量 ,发生反应 ,下列叙述正
确的是___________(填标号)。
A.增大 质量时,反应速率增大
B. 体积分数不变时,该反应达到平衡状态
C.平衡后,再充入 ,达到新平衡时, 增大
D.平衡后,再充入少量 质量增大
(3) 的速率方程为 ( 为速率常数,只与温
度、压强有关)。
①某温度下,该反应的平衡常数K为10, ,则 。
②已知: (式中,R为常数, 单位为 ,温度T单位为K,E表示反应的活化
能,单位为 )。 与不同催化剂( 为催化剂)、温度(T)关系如图所示。
相同条件下,催化效率较高的是 (填“ ”或“ ”),判断依据是 。在催化
剂 作用下,正反应的活化能为 。
(4)一定温度下,向密闭容器中充入足量 ,达到平衡时测得生成 和 。则该
试卷第8页,共3页温度下,反应 的压强平衡常数 ( 为用分压表示的平衡常数,分
压=总压×物质的量分数)。
(5)在甲、乙两个体积相等的容器中都充入 发生反应: 。测得 的物质
的量与时间关系如图。
①相对乙,甲仅改变一个条件,该条件是 。
②乙容器中,在恒容条件下 时再充入少量 的平衡转化率将 (填“增大”、“减
小”或“不变”)。
14.(15分)一种高分子功能材料W的合成路线如下图所示:
已知:
请回答下列问题:
(1)D按系统命名法的名称是 。(2)C中官能团名称是 ;D→E的反应类型为 。
(3)已知E的分子式为 , 的结构简式为 。
(4)G→W的化学反应方程式为 。
(5)M是G的同分异构体,同时满足下列条件的结构有 种(不考虑立体异构)。
①遇氯化铁溶液能发生显色反应;
②能与 反应产生气体。
其中核磁共振氢谱上有5组峰且峰的面积比为1:2:2:2:1的结构简式为 。
(6)设计以2,3-二氯丁烷( )、丙烯醛( )为原料合成苯甲醛的合成路线
(无机试剂任选)。
试卷第10页,共3页