文档内容
表示物质转化的化学用语
离子方程式正误判断的三个关键
化学式拆写
“四原则”
易溶强电解质拆,弱电解质、难溶物不拆
微溶物清拆浊不拆
单质、氧化物不拆
浓硫酸不拆,浓盐酸、浓硝酸拆
反应产物
“三分析”
分析量不同时的产物
分析是否漏掉同步反应
分析变价元素的产物
方程式遵循
“三守恒”
原子守恒
电荷守恒
得失电子守恒
1.(2024·新课标卷,10)对于下列过程中发生的化学反应,相应离子方程式正确的是( )
A.试管壁上的银镜用稀硝酸清洗:Ag+2H++NO-
===Ag++NO ↑+H O
3 2 2
B.工业废水中的Pb2+用FeS去除:Pb2++S2-===PbS↓
C.海水提溴过程中将溴吹入SO 吸收塔:Br +SO +2H O===2Br-+SO2- +4H+
2 2 2 2 4
D.用草酸标准溶液测定高锰酸钾溶液的浓度:2MnO- +5C O2- +16H+===2Mn2++10CO ↑+8H O
4 2 4 2 2
答案 C解析
银与稀硝酸反应生成硝酸银、一氧化氮和水,该反应的离子方程式为3Ag+4H++NO-
===3Ag+
3
+NO↑+2H O,A错误;FeS为难溶物,在离子方程式中不拆分,反应的离子方程式为Pb2+
2
+FeS===PbS+Fe2+,B错误;SO 具有还原性,海水提溴过程中将溴吹入SO 吸收塔时,Br 被还原为Br-,
2 2 2
该反应的离子方程式为Br +SO +2H
O===2Br-+SO2-
+4H+,C正确;H C O 属于弱酸,在书写离子方程式
2 2 2 4 2 2 4
时不能拆分,反应的离子方程式为2MnO-
+5H C O +6H+===2Mn2++10CO ↑+8H O,D错误。
4 2 2 4 2 2
2.(2024·湖南,6)下列过程中,对应的反应方程式错误的是( )
《天工开物》记载用炉甘石(ZnCO )
3
A
2ZnCO +C 2Zn+3CO↑
火法炼锌 3
B CaH 用作野外生氢剂 CaH +2H O===Ca(OH) +2H ↑
2 2 2 2 2
C 饱和Na CO 溶液浸泡锅炉水垢 CaSO
(s)+CO2-
(aq) CaCO
(s)+SO2-
(aq)
2 3 4 3 3 4
绿矾(FeSO ·7H O)处理酸性工业废
4 2
D 6Fe2++Cr O2- +14H+===6Fe3++2Cr3++7H O
水中的Cr O2- 2 7 2
2 7
答案 A
解析 火法炼锌过程中C作还原剂,ZnCO 在高温条件下分解为ZnO、CO ,CO 与C在高温条件下生成
3 2 2
还原性气体CO,CO还原ZnO生成Zn,因此总反应为ZnCO +2C Zn+3CO↑,故A项错误;CaH 为
3 2
活泼金属氢化物,因此能与H O发生归中反应生成碱和氢气,反应的化学方程式为
2
CaH +2H O===Ca(OH) +2H ↑,故B项正确;锅炉水垢的主要成分为CaSO 、MgCO 等,由于溶解性:
2 2 2 2 4 3
CaSO >CaCO ,因此向锅炉水垢中加入饱和Na CO 溶液,根据难溶物转化原则可知CaSO 转化为
4 3 2 3 4
CaCO ,反应的化学方程式为CaSO
(s)+CO2-
(aq) CaCO
(s)+SO2-
(aq),故C正确;Cr
O2-
具有强氧化
3 4 3 3 4 2 7
性,加入具有还原性的Fe2+,二者发生氧化还原反应生成Fe3+、Cr3+,Cr元素化合价由+6价降低至+3价,
Fe元素化合价由+2价升高至+3价,则反应的离子方程式为6Fe2++Cr
O2-
+14H+===6Fe3++2Cr3++7H O,故D
2 7 2
正确。
3.(2024·湖北,7)过量SO 与以下0.1 mol·L-1的溶液反应,下列总反应方程式错误的是( )
2
溶液
现象
化学方程式
A
Na S
2
产生淡黄色沉淀3SO +2Na S===3S↓+2Na SO
2 2 2 3
B
FeCl
3
溶液由棕黄色变浅绿色
2FeCl +SO +2H O===2FeCl +H SO +2HCl
3 2 2 2 2 4
C
CuCl
2
溶液褪色,产生白色沉淀
SO +2CuCl +2H O===2CuCl↓+H SO +2HCl
2 2 2 2 4
D
Na CO
2 3
(含酚酞)
溶液由红色变无色
2SO +Na CO +H O===CO +2NaHSO
2 2 3 2 2 3
答案 A
解析 过量 SO 与0.1 mol·L-1的Na S溶液反应,产生的淡黄色沉淀是S,同时生成NaHSO ,总反应化学
2 2 3
方程式为5SO +2Na S+2H O===3S↓+4NaHSO ,A错误;Na CO 水解使溶液显碱性,其水溶液能使酚酞
2 2 2 3 2 3
变红;过量SO 与0.1 mol·L-1的Na CO 溶液反应,生成CO 、NaHSO ,NaHSO 溶液显酸性,滴有酚酞的
2 2 3 2 3 3
溶液由红色变无色,总反应的化学方程式为2SO +Na CO +H O===CO +2NaHSO ,D正确。
2 2 3 2 2 3
4.(2023·湖南,5)下列有关电极方程式或离子方程式错误的是( )
A.碱性锌锰电池的正极反应:MnO +H O+e-===MnO(OH)+OH-
2 2
B.铅酸蓄电池充电时的阳极反应:Pb2++2H O-2e-===PbO +4H+
2 2
C.K [Fe(CN) ]溶液滴入FeCl 溶液中:K++Fe2++[Fe(CN) ]3-===KFe[Fe(CN) ]↓
3 6 2 6 6
D.TiCl 加入水中:TiCl +(x+2)H O===TiO ·xH O↓+4H++4Cl-
4 4 2 2 2
答案 B
解析 碱性锌锰电池放电时正极得到电子生成MnO(OH),电极反应为MnO +H O+e-===MnO(OH)+OH-,A
2 2
正确;铅酸蓄电池在充电时阳极失电子,发生反应:PbSO -2e-+2H O===PbO
+4H++SO2-
,B错误;
4 2 2 4
K [Fe(CN) ]溶液与Fe2+反应生成蓝色沉淀,反应的离子方程式为K++Fe2++[Fe(CN) ]3-===KFe[Fe(CN) ]↓,C
3 6 6 6
正确;TiCl 容易发生水解,反应的离子方程式为TiCl +(x+2)H O===TiO ·xH O↓+4H++4Cl-,D正确。
4 4 2 2 2
5.(2022·湖南,11改编)下列离子方程式正确的是( )
A.Cl 通入冷的NaOH溶液:3Cl
+6OH-===5Cl-+ClO-
+3H O
2 2 3 2
B.用醋酸和淀粉⁃KI溶液检验加碘盐中的IO- :IO-
+5I-+6H+===3I +3H O
3 3 2 2
C.FeSO 溶液中加入H O 产生沉淀:2Fe2++H O +4H O===2Fe(OH) ↓+4H+
4 2 2 2 2 2 3
D.NaHCO 溶液与少量的Ba(OH)
溶液混合:HCO-
+Ba2++OH-===BaCO ↓+H O
3 2 3 3 2答案 C
解析 Cl 通入冷的NaOH溶液中发生反应生成氯化钠和次氯酸钠,离子方程式为Cl +2OH-===Cl-+ClO-
2 2
+H
O,A不正确;用醋酸和淀粉⁃KI溶液检验加碘盐中的IO- 的原理是IO-
在酸性条件下与I-发生归中反应
2 3 3
生成I ,淀粉遇I 变蓝,由于醋酸是弱酸,在离子方程式中不能拆,B不正确;H O 具有较强的氧化性,
2 2 2 2
FeSO 溶液中加入H O 产生的沉淀是氢氧化铁,该反应的离子方程式为2Fe2+
4 2 2
+H O +4H O===2Fe(OH) ↓+4H+,C正确;NaHCO 溶液与少量的Ba(OH) 溶液混合发生反应生成碳酸钡沉
2 2 2 3 3 2
淀、碳酸钠和水,该反应的离子方程式为2HCO-
+Ba2++2OH-===BaCO
↓+CO2-
+2H O,D不正确。
3 3 3 2
题型突破练 [分值:50 分]
(选择题1~10题,每小题3分,11~14题,每小题5分,共50分)
1.下列离子方程式正确的是( )
A.将少量SO 通入Ca(ClO) 溶液中:SO +Ca2++ClO-+H O===CaSO ↓+Cl-+2H+
2 2 2 2 4
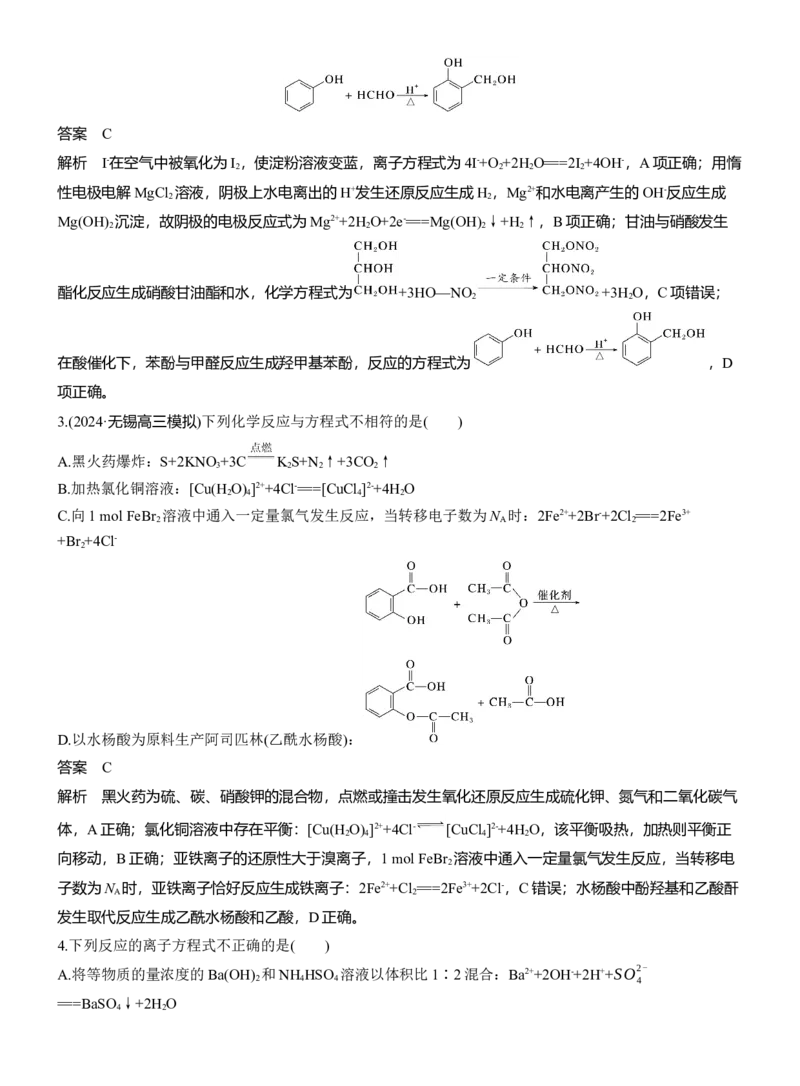
B.向乙二醇溶液中加入足量酸性高锰酸钾溶液:
O-
4
5 +8Mn +24H+===5 +8Mn2++22H O
2
C.向饱和Na CO 溶液中通入过量CO :CO2- +CO +H O===2HCO-
2 3 2 3 2 2 3
D.向Fe(NO )
溶液中加入过量HI溶液:Fe3++12H++3NO-
+10I-===Fe2++5I +6H O+3NO↑
3 3 3 2 2
答案 D
解析 少量二氧化硫与次氯酸钙溶液反应生成硫酸钙沉淀、氯化钙和次氯酸,反应的离子方程式为
SO +Ca2++3ClO-+H O===CaSO ↓+Cl-+2HClO,故A错误;乙二醇溶液与足量酸性高锰酸钾溶液反应生成
2 2 4
O-
4
硫酸钾、硫酸锰、二氧化碳和水,反应的离子方程式为 +2Mn +6H+===2Mn2++2CO ↑+6H O,
2 2
故B错误;饱和碳酸钠溶液与过量二氧化碳反应生成碳酸氢钠沉淀,反应的离子方程式为2Na++CO2-
3
+CO +H O===2NaHCO ↓,故C错误;硝酸铁溶液与过量氢碘酸反应生成碘化亚铁、碘、一氧化氮和水,
2 2 3
反应的离子方程式为Fe3++12H++3NO-
+10I-===Fe2++5I +6H O+3NO↑,故D正确。
3 2 2
2. (2024·宁波市十校高三联考)下列指定反应与方程式不相符的是( )
A.淀粉碘化钾溶液在空气中变蓝:4I-+O +2H O===2I +4OH-
2 2 2
B.用惰性电极电解MgCl 溶液,阴极的电极反应式:Mg2++2H O+2e-===Mg(OH) ↓+H ↑
2 2 2 2
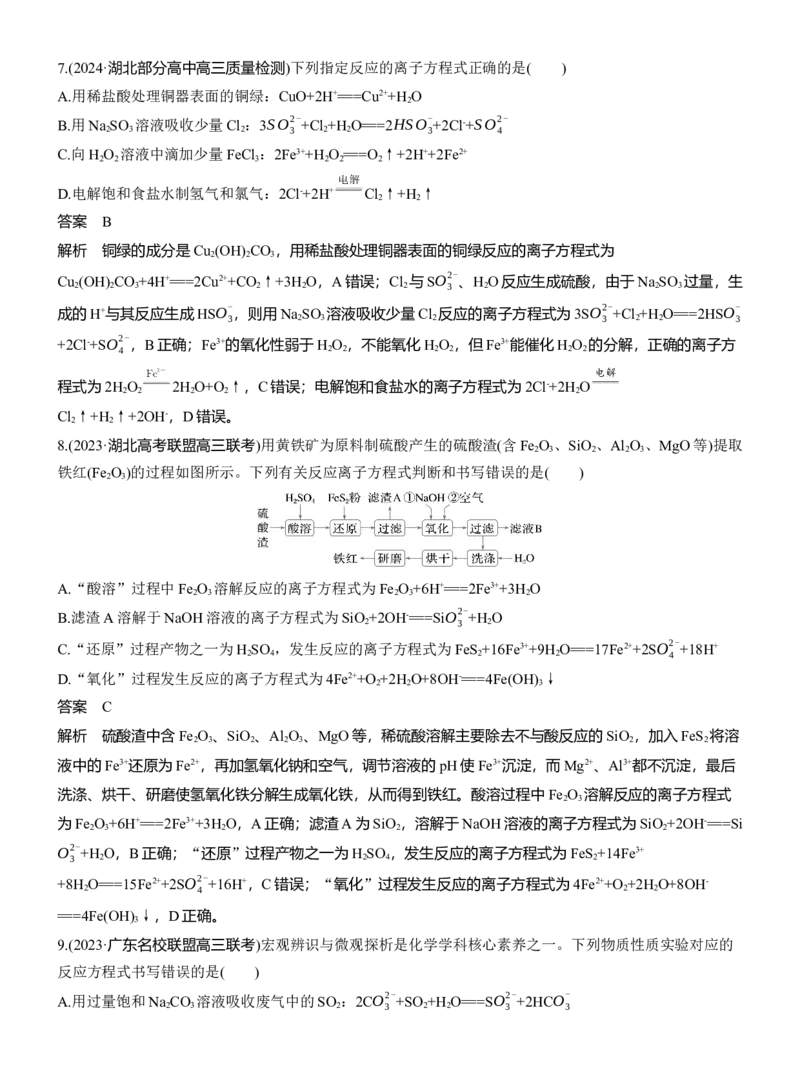
C.甘油与硝酸发生酯化反应: +3HNO
3
D.在酸催化下,苯酚与甲醛反应生成羟甲基苯酚:答案 C
解析 I-在空气中被氧化为I ,使淀粉溶液变蓝,离子方程式为4I-+O +2H O===2I +4OH-,A项正确;用惰
2 2 2 2
性电极电解MgCl 溶液,阴极上水电离出的H+发生还原反应生成H ,Mg2+和水电离产生的OH-反应生成
2 2
Mg(OH) 沉淀,故阴极的电极反应式为Mg2++2H O+2e-===Mg(OH) ↓+H ↑,B项正确;甘油与硝酸发生
2 2 2 2
酯化反应生成硝酸甘油酯和水,化学方程式为 +3HO—NO +3H O,C项错误;
2 2
在酸催化下,苯酚与甲醛反应生成羟甲基苯酚,反应的方程式为 ,D
项正确。
3.(2024·无锡高三模拟)下列化学反应与方程式不相符的是( )
A.黑火药爆炸:S+2KNO +3C K S+N ↑+3CO ↑
3 2 2 2
B.加热氯化铜溶液:[Cu(H O) ]2++4Cl-===[CuCl ]2-+4H O
2 4 4 2
C.向1 mol FeBr 溶液中通入一定量氯气发生反应,当转移电子数为N 时:2Fe2++2Br-+2Cl ===2Fe3+
2 A 2
+Br +4Cl-
2
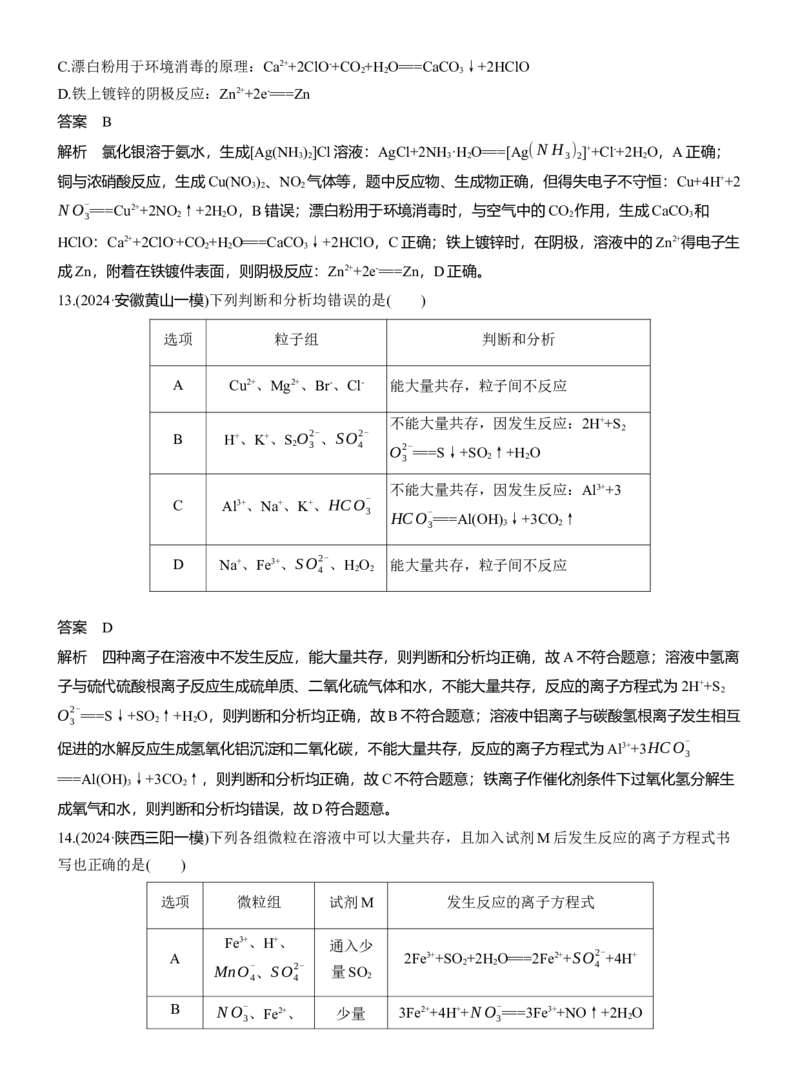
D.以水杨酸为原料生产阿司匹林(乙酰水杨酸):
答案 C
解析 黑火药为硫、碳、硝酸钾的混合物,点燃或撞击发生氧化还原反应生成硫化钾、氮气和二氧化碳气
体,A正确;氯化铜溶液中存在平衡:[Cu(H O) ]2++4Cl- [CuCl ]2-+4H O,该平衡吸热,加热则平衡正
2 4 4 2
向移动,B正确;亚铁离子的还原性大于溴离子,1 mol FeBr 溶液中通入一定量氯气发生反应,当转移电
2
子数为N 时,亚铁离子恰好反应生成铁离子:2Fe2++Cl ===2Fe3++2Cl-,C错误;水杨酸中酚羟基和乙酸酐
A 2
发生取代反应生成乙酰水杨酸和乙酸,D正确。
4.下列反应的离子方程式不正确的是( )
A.将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H++SO2-
2 4 4 4
===BaSO ↓+2H O
4 2B.用Na S O 溶液吸收水中的Cl :4Cl +S O2- +5H O===10H++2SO2- +8Cl-
2 2 3 2 2 2 3 2 4
C.CuSO 溶液中滴加过量的浓氨水:Cu2++2NH ·H O===2N H+ +Cu(OH) ↓
4 3 2 4 2
D.向酸性重铬酸钾溶液中加少量乙醇溶液:2Cr O2- +3C H OH+16H+===4Cr3++3CH COOH+11H O
2 7 2 5 3 2
答案 C
解析 将Ba(OH) 和NH HSO 溶液按物质的量为1∶2混合,发生反应产生BaSO 沉淀、(NH ) SO 和
2 4 4 4 4 2 4
H
O,反应的离子方程式为Ba2++2OH-+2H++SO2-
===BaSO ↓+2H O,故A正确;向硫酸铜溶液中滴加浓
2 4 4 2
氨水,一开始生成蓝色氢氧化铜沉淀,继续滴加氨水,沉淀溶解,得到含配离子[Cu(NH ) ]2+的深蓝色溶液,
3 4
故C错误;酸性重铬酸钾具有强氧化性,乙醇具有还原性,乙醇被重铬酸根离子氧化,离子方程式为2Cr
2
O2- +3C H OH+16H+===4Cr3++3CH COOH+11H O,故D正确。
7 2 5 3 2
5.(2024·江苏扬州中学高三模拟)ⅤA族元素及其化合物应用广泛。肼(N H )的燃烧热为624 kJ·mol-1,是常
2 4
用的火箭燃料。P元素可形成多种含氧酸,其中次磷酸(H PO )为一元弱酸,H PO 为三元中强酸。雌黄
3 2 3 4
(As S )和SnCl 在盐酸中反应转化为雄黄(As S )和SnCl (沸点:114 ℃)并放出H S气体。下列化学反应表示
2 3 2 4 4 4 2
正确的是( )
A.NO 制HNO 的离子方程式:3NO +H O===2HNO +NO
2 3 2 2 3
B.次磷酸与足量NaOH溶液反应:H PO +3NaOH===Na PO +3H O
3 2 3 2 2
C.肼燃烧的热化学方程式:N H (l)+O (g)===N (g)+2H O(g) ΔH=-624 kJ·mol-1
2 4 2 2 2
D.雌黄制备雄黄的化学方程式:2As S +2SnCl +4HCl===As S +2SnCl +2H S↑
2 3 2 4 4 4 2
答案 D
解析 NO 制HNO 的离子方程式:3NO +H
O===2H++2NO-
+NO,故A错误;次磷酸是一元弱酸,次磷酸
2 3 2 2 3
与足量NaOH溶液反应生成NaH PO ,化学方程式为H PO +NaOH===NaH PO +H O,故B错误;1 mol肼
2 2 3 2 2 2 2
完全燃烧生成氮气和液态水时放出624 kJ热量,热化学方程式:N H (l)+O (g)===N (g)+2H O(l) ΔH=-624
2 4 2 2 2
kJ·mol-1 ,故C错误。
6.(2024·湖北高三模拟)化学用语可以表达化学过程。下列化学用语的表达错误的是( )
A.用离子方程式表示铜在氨水中被腐蚀:2Cu+O +8NH ·H O===2[Cu(NH ) ]2++4OH-+6H O
2 3 2 3 4 2
B.用电子式表示水分子的形成过程:
C.牙膏中添加氟化物能预防龋齿的原因:Ca (PO ) OH(s)+F-(aq) Ca (PO ) F(s)+OH-(aq)
5 4 3 5 4 3
D.用化学方程式表示钢铁表面进行“烤蓝”处理:3Fe+4H O(g) Fe O +4H
2 3 4 2
答案 B
解析 铜在氨水环境中被空气中的氧气氧化为四氨合铜离子,A正确; 水为共价化合物,用电子式表示水
分子的形成过程为 ,B错误;牙膏中添加氟化物能将Ca 5 (PO 4 ) 3 OH转化为更难溶
的Ca (PO ) F,从而保护牙齿,C正确;钢铁表面进行“烤蓝”处理是在铁的表面形成一层致密的氧化膜,
5 4 3
反应为铁和水蒸气在高温条件下生成四氧化三铁和氢气,D正确。7.(2024·湖北部分高中高三质量检测)下列指定反应的离子方程式正确的是( )
A.用稀盐酸处理铜器表面的铜绿:CuO+2H+===Cu2++H O
2
B.用Na SO 溶液吸收少量Cl :3SO2- +Cl +H O===2HSO- +2Cl-+SO2-
2 3 2 3 2 2 3 4
C.向H O 溶液中滴加少量FeCl :2Fe3++H O ===O ↑+2H++2Fe2+
2 2 3 2 2 2
D.电解饱和食盐水制氢气和氯气:2Cl-+2H+ Cl ↑+H ↑
2 2
答案 B
解析 铜绿的成分是Cu (OH) CO ,用稀盐酸处理铜器表面的铜绿反应的离子方程式为
2 2 3
Cu (OH) CO +4H+===2Cu2++CO ↑+3H O,A错误;Cl
与SO2-
、H O反应生成硫酸,由于Na SO 过量,生
2 2 3 2 2 2 3 2 2 3
成的H+与其反应生成HSO-
,则用Na SO 溶液吸收少量Cl
反应的离子方程式为3SO2-
+Cl +H
O===2HSO-
3 2 3 2 3 2 2 3
+2Cl-+SO2- ,B正确;Fe3+的氧化性弱于H O ,不能氧化H O ,但Fe3+能催化H O 的分解,正确的离子方
4 2 2 2 2 2 2
程式为2H O 2H O+O ↑,C错误;电解饱和食盐水的离子方程式为2Cl-+2H O
2 2 2 2 2
Cl ↑+H ↑+2OH-,D错误。
2 2
8.(2023·湖北高考联盟高三联考)用黄铁矿为原料制硫酸产生的硫酸渣(含Fe O 、SiO 、Al O 、MgO等)提取
2 3 2 2 3
铁红(Fe O )的过程如图所示。下列有关反应离子方程式判断和书写错误的是( )
2 3
A.“酸溶”过程中Fe O 溶解反应的离子方程式为Fe O +6H+===2Fe3++3H O
2 3 2 3 2
B.滤渣A溶解于NaOH溶液的离子方程式为SiO +2OH-===SiO2- +H O
2 3 2
C.“还原”过程产物之一为H SO ,发生反应的离子方程式为FeS +16Fe3++9H O===17Fe2++2SO2- +18H+
2 4 2 2 4
D.“氧化”过程发生反应的离子方程式为4Fe2++O +2H O+8OH-===4Fe(OH) ↓
2 2 3
答案 C
解析 硫酸渣中含Fe O 、SiO 、Al O 、MgO等,稀硫酸溶解主要除去不与酸反应的SiO ,加入FeS 将溶
2 3 2 2 3 2 2
液中的Fe3+还原为Fe2+,再加氢氧化钠和空气,调节溶液的pH使Fe3+沉淀,而Mg2+、Al3+都不沉淀,最后
洗涤、烘干、研磨使氢氧化铁分解生成氧化铁,从而得到铁红。酸溶过程中Fe O 溶解反应的离子方程式
2 3
为Fe O +6H+===2Fe3++3H O,A正确;滤渣A为SiO ,溶解于NaOH溶液的离子方程式为SiO +2OH-===Si
2 3 2 2 2
O2- +H O,B正确;“还原”过程产物之一为H SO ,发生反应的离子方程式为FeS +14Fe3+
3 2 2 4 2
+8H O===15Fe2++2SO2- +16H+,C错误;“氧化”过程发生反应的离子方程式为4Fe2++O +2H O+8OH-
2 4 2 2
===4Fe(OH) ↓,D正确。
3
9.(2023·广东名校联盟高三联考)宏观辨识与微观探析是化学学科核心素养之一。下列物质性质实验对应的
反应方程式书写错误的是( )
A.用过量饱和Na CO 溶液吸收废气中的SO :2CO2- +SO +H O===SO2- +2HCO-
2 3 2 3 2 2 3 3B.用白醋除铁锈:Fe O ·xH O+6H+===(3+x)H O+2Fe3+
2 3 2 2
C.苯酚钠溶液通入CO 后变浑浊: +CO +H O―→ +NaHCO
2 2 2 3
D.将KI溶液滴入稀硫酸酸化的KIO
溶液中:5I-+IO-
+6H+===3I +3H O
3 3 2 2
答案 B
解析 白醋除铁锈:Fe O ·xH O+6CH COOH===(3+x)H O+6CH COO-+2Fe3+,B错误。
2 3 2 3 2 3
10.(2024·贵州部分学校模拟)下列离子方程式或化学方程式正确的是( )
CH COOH+CH
A.在浓硫酸、加热条件下,CH CH 18OH和CH COOH制备乙酸乙酯: 3 3CH 18OH
3 2 3 2
CH COOCH CH +H 18O
3 2 3 2
B.用亚硫酸钠溶液吸收少量氯气:SO2-
+Cl +H
O===SO2-
+2H++2Cl-
3 2 2 4
C.向溴的四氯化碳溶液中通入乙烯:Br +CH ==CH —→CH CHBr
2 2 2 3 2
D.在NaHSO 溶液中滴加少量NaClO溶液:2HSO- +ClO-===SO2- +Cl-+SO ↑+H O
3 3 4 2 2
答案 D
解析 在浓硫酸、加热条件下,CH CH 18OH和CH COOH制备乙酸乙酯,酸脱羟基、醇脱氢,反应的化
3 2 3
学方程式为CH COOH+CH CH 18OH CH CO18OCH CH +H O,A错误;用亚硫酸钠溶液吸收少量氯
3 3 2 3 2 3 2
气,反应的离子方程式为3SO2-
+Cl +H
O===SO2- +2HSO-
+2Cl-,B错误;向溴的四氯化碳溶液中通入乙烯:
3 2 2 4 3
Br +CH ==CH —→CH BrCH Br,C错误;在NaHSO 溶液中滴加少量NaClO溶液,次氯酸根离子将亚硫
2 2 2 2 2 3
酸氢根离子氧化成硫酸根离子,离子方程式为2HSO- +ClO-===SO2-
+Cl-+SO ↑+H O,D正确。
3 4 2 2
11.下列离子方程式,能正确解释沉淀产生原因的是( )
A.向FeCl 溶液中加入氨水,产生红褐色沉淀:Fe3++3OH-===Fe(OH) ↓
3 3
O2-
B.向甲醛中加入足量新制Cu(OH) ,加热,产生砖红色沉淀:HCHO+4Cu(OH) +2OH- C 3
2 2
+2Cu O↓+6H O
2 2
C.向饱和Na CO 溶液中通入CO ,产生白色沉淀:Na++CO2- +CO +H O===NaHCO ↓
2 3 2 3 2 2 3
D.向Ba(NO ) 溶液中通入SO ,产生白色沉淀:Ba2++SO +H O===BaSO ↓+2H+
3 2 2 2 2 3
答案 B
解析 向FeCl 溶液中加入氨水,产生红褐色沉淀,一水合氨是弱电解质,不能拆写成离子:Fe3+
3
+3NH ·H O===Fe(OH) ↓+3N H+ ,A错误;向饱和Na CO 溶液中通入CO ,产生白色沉淀:2Na++CO2-
3 2 3 4 2 3 2 3
+CO +H O===2NaHCO ↓,C错误;向Ba(NO ) 溶液中通入SO ,发生氧化还原反应,产生硫酸钡白色
2 2 3 3 2 2
沉淀:3Ba2++2NO-
+3SO +2H O===3BaSO ↓+4H++2NO↑,D错误。
3 2 2 4
12.(2024·安徽淮北高三质量检测)下列离子方程式错误的是( )
A.氯化银溶于氨水:AgCl+2NH ·H O===[Ag(NH ) ]++Cl-+2H O
3 2 3 2 2
B.铜与浓硝酸反应:3Cu+8H++2NO-
===3Cu2++2NO ↑+4H O
3 2 2C.漂白粉用于环境消毒的原理:Ca2++2ClO-+CO +H O===CaCO ↓+2HClO
2 2 3
D.铁上镀锌的阴极反应:Zn2++2e-===Zn
答案 B
解析 氯化银溶于氨水,生成[Ag(NH ) ]Cl溶液:AgCl+2NH ·H O===[Ag(N H ) ]++Cl-+2H O,A正确;
3 2 3 2 3 2 2
铜与浓硝酸反应,生成Cu(NO ) 、NO 气体等,题中反应物、生成物正确,但得失电子不守恒:Cu+4H++2
3 2 2
NO- ===Cu2++2NO ↑+2H O,B错误;漂白粉用于环境消毒时,与空气中的CO 作用,生成CaCO 和
3 2 2 2 3
HClO:Ca2++2ClO-+CO +H O===CaCO ↓+2HClO,C正确;铁上镀锌时,在阴极,溶液中的Zn2+得电子生
2 2 3
成Zn,附着在铁镀件表面,则阴极反应:Zn2++2e-===Zn,D正确。
13.(2024·安徽黄山一模)下列判断和分析均错误的是( )
选项 粒子组 判断和分析
A Cu2+、Mg2+、Br-、Cl- 能大量共存,粒子间不反应
不能大量共存,因发生反应:2H++S
2
B H+、K+、S O2-、SO2-
2 3 4 O2- ===S↓+SO ↑+H O
3 2 2
不能大量共存,因发生反应:Al3++3
C
Al3+、Na+、K+、HCO-
3 HCO- ===Al(OH) ↓+3CO ↑
3 3 2
D
Na+、Fe3+、SO2-、H
O 能大量共存,粒子间不反应
4 2 2
答案 D
解析 四种离子在溶液中不发生反应,能大量共存,则判断和分析均正确,故A不符合题意;溶液中氢离
子与硫代硫酸根离子反应生成硫单质、二氧化硫气体和水,不能大量共存,反应的离子方程式为2H++S
2
O2- ===S↓+SO ↑+H O,则判断和分析均正确,故B不符合题意;溶液中铝离子与碳酸氢根离子发生相互
3 2 2
促进的水解反应生成氢氧化铝沉淀和二氧化碳,不能大量共存,反应的离子方程式为Al3++3HCO-
3
===Al(OH) ↓+3CO ↑,则判断和分析均正确,故C不符合题意;铁离子作催化剂条件下过氧化氢分解生
3 2
成氧气和水,则判断和分析均错误,故D符合题意。
14.(2024·陕西三阳一模)下列各组微粒在溶液中可以大量共存,且加入试剂M后发生反应的离子方程式书
写也正确的是( )
选项 微粒组 试剂M 发生反应的离子方程式
Fe3+、H+、 通入少
A 2Fe3++SO +2H O===2Fe2++SO2- +4H+
MnO- 、SO2- 量SO 2 2 4
4 4 2
B NO- 、Fe2+、 少量 3Fe2++4H++NO- ===3Fe3++NO↑+2H O
3 3 2SO2-
、Na+ 硫酸
4
Cl-、Na+、 过量醋
C 2H++SiO2- ===H SiO ↓
SiO2- 、K+ 酸溶液 3 2 3
3
K+、
适量
D [Al(OH) 4 ]-、 HNO 3 H++[Al(OH) 4 ]- ===Al(OH) 3 ↓+H 2 O
SO2- 、HCO- 溶液
4 3
答案 B
解析
Fe3+、H+、MnO- 、SO2-
在溶液中能大量共存,但通入少量SO
后,发生的是MnO-
与SO 的氧化
4 4 2 4 2
还原反应,而不是Fe3+与SO
的氧化还原反应,A不正确;NO- 、Fe2+、SO2-
、Na+在溶液中能大量共存,
2 3 4
加入H SO
后,溶液呈酸性,NO-
的氧化能力增强,能将Fe2+氧化为Fe3+,从而发生反应:3Fe2++4H++
2 4 3
NO- ===3Fe3++NO↑+2H O,B正确;Cl-、Na+、SiO2- 、K+在溶液中能大量共存,加入过量醋酸溶液,
3 2 3
SiO2-
转化为H SiO ,但醋酸为弱酸,不能拆写成H+和CH COO-,应以化学式表示,离子方程式为
3 2 3 3
2CH COOH+SiO2- ===H SiO ↓+2CH COO-,C不正确;K+、[Al(OH) ]-、SO2- 、HCO- 在溶液中不能大量
3 3 2 3 3 4 4 3
共存,因为[Al(OH)
]-、HCO-
能发生反应:[Al(OH)
]-+HCO-
===Al(OH)
↓+CO2-
+H O,D不正确。
4 3 4 3 3 3 2