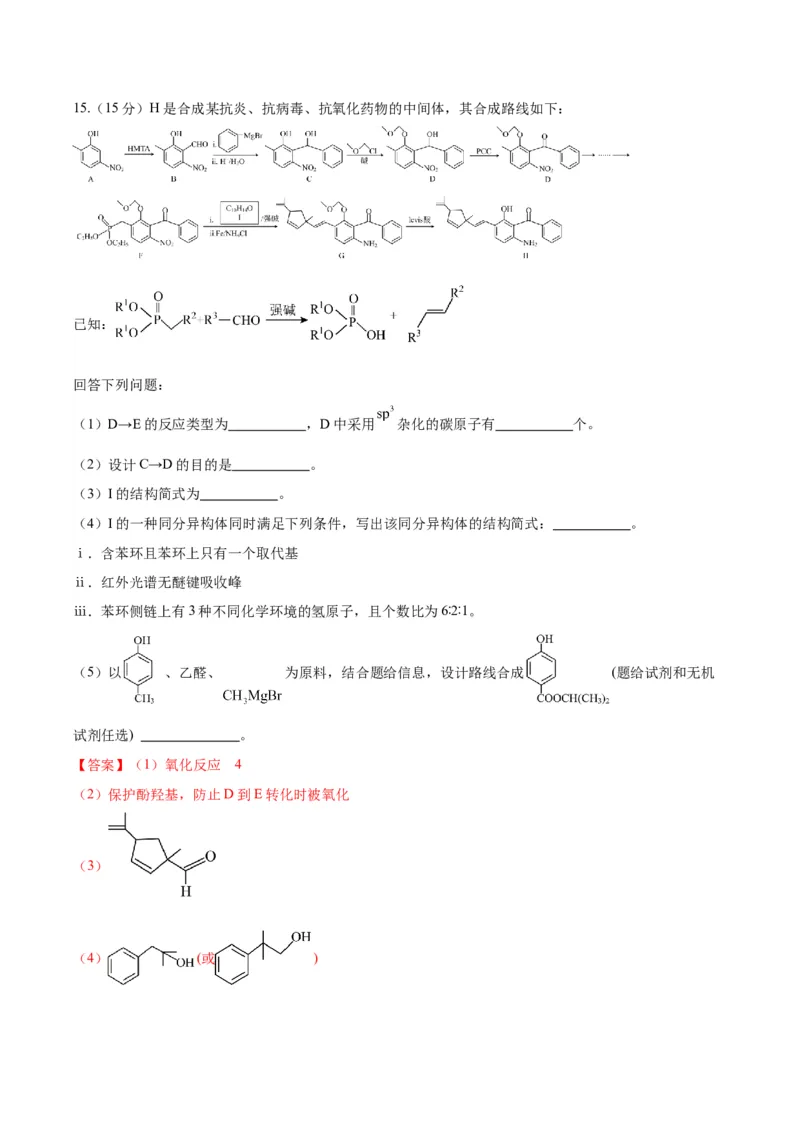
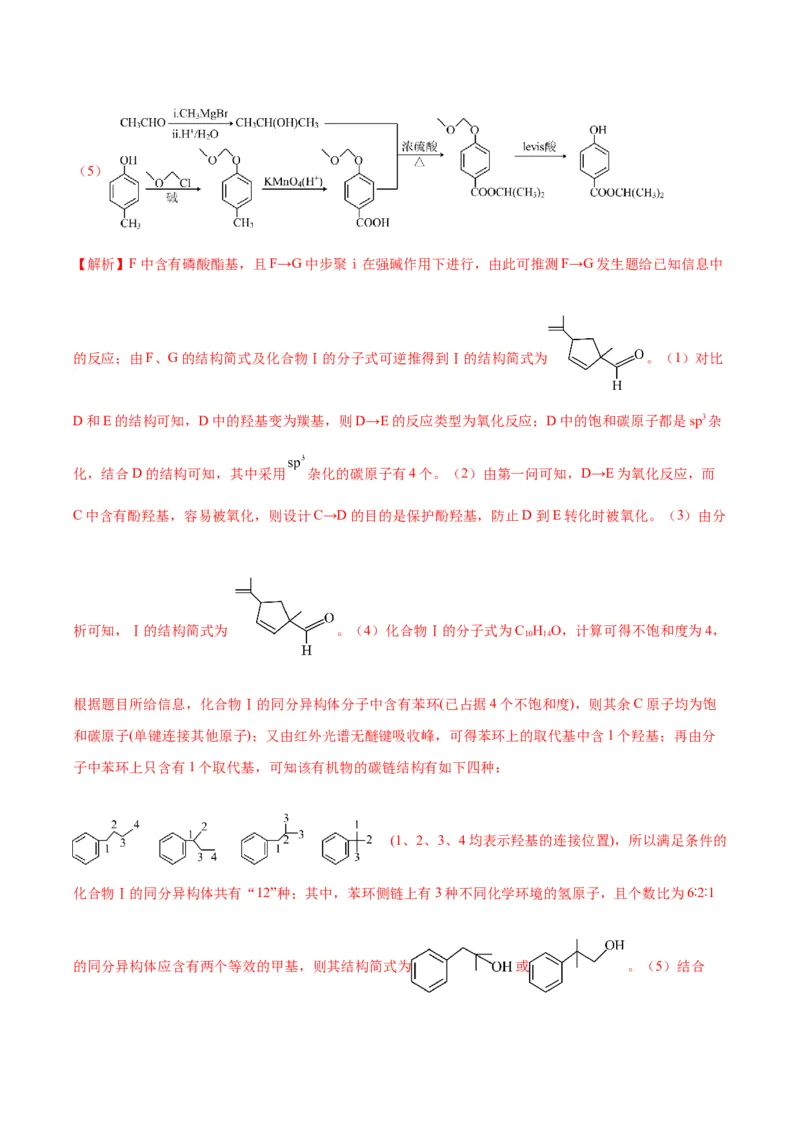
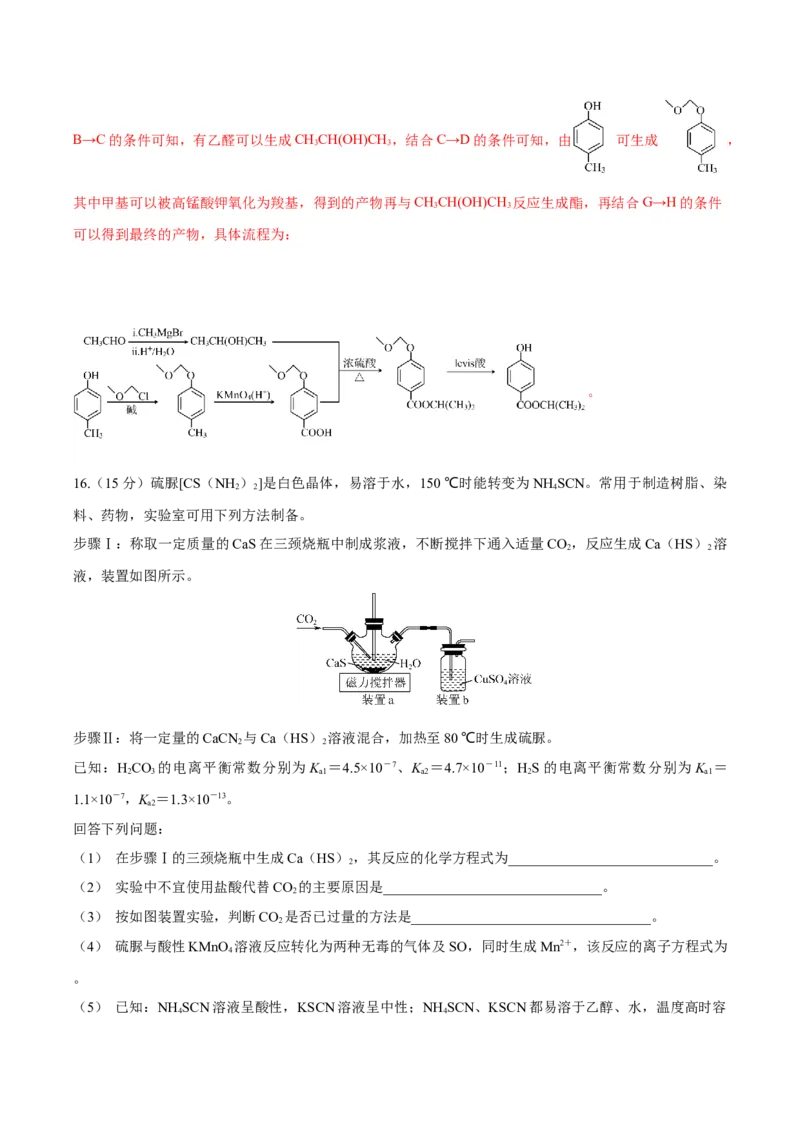
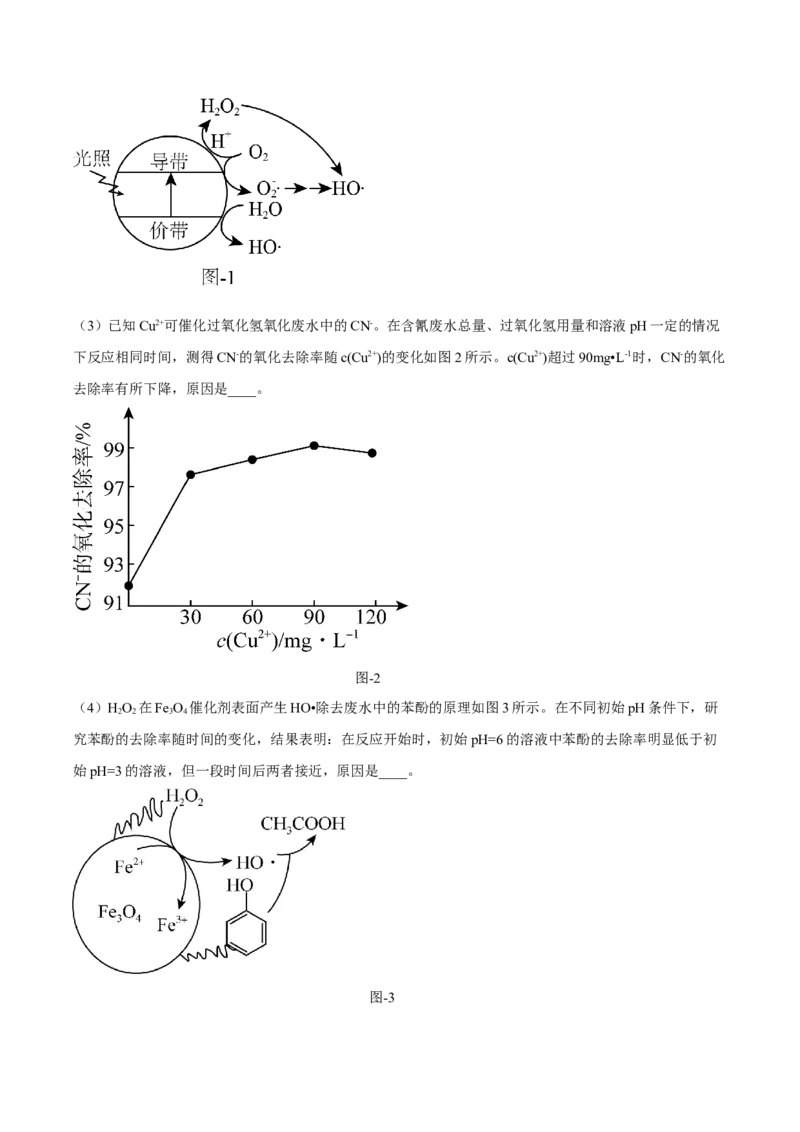
文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(江苏专用)
黄金卷08
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64 Ce 140
第Ⅰ卷
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1. 化学与生产、生活和社会发展密切相关,下列叙述正确的是
A.华为5G手机麒麟9000芯片(HUAWEIKirin)主要成分是二氧化硅
B.“酒曲”的酿酒工艺,是利用了催化剂使平衡正向移动的原理
C.免洗洗手液的有效成分之一活性银离子能使病毒蛋白质变性
D.葛洪所著《抱朴子》中“丹砂(HgS)烧之成水银,积变又还原成丹砂”,二者为可逆反应
【答案】C
【解析】硅是良好的半导体材料,芯片主要成分是硅,A项错误;“酒曲”酿酒工艺中,酒曲为催化剂,
能加快反应速率,但不影响化学平衡,不能使平衡发生移动,B项错误;银离子是重金属离子,重金属离
子能使蛋白质发生变性,C项正确;“丹砂(HgS)在加热下生成汞,汞在常温下可转变为丹砂(HgS)” 二者
反应条件不同、不互为可逆反应,D项错误。
2.下列化学用语表述错误的是 ( )
A.HClO的电子式
B.中子数为10的氧原子:18
O
8
C.NH 分子的VSEPR模型:
3
D.基态N原子的价层电子排布图:
【答案】C
【解析】HClO中O原子分别与H、Cl原子间以共价键结合,因此HClO的电子式为 ,A正确;中子数为10、质子数为8的O原子,其质量数为10+8=18,该原子表示为 O,B正确;根据VSEPR模型计算,NH
18 3
8
分子中N原子上有1个孤电子对,每个N原子还连接3个H原子,因此NH 的VSEPR模型为四面体形,C错误;
3
基态N原子的价层电子排布为2s22p3,其价层电子排布图为 ,D正确。
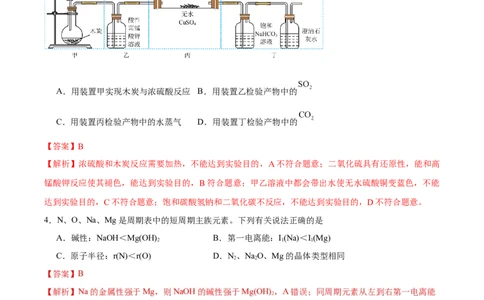
3. 设计实验验证木炭和浓硫酸反应的产物。下列装置和操作能达到实验目的的是
A.用装置甲实现木炭与浓硫酸反应 B.用装置乙检验产物中的
C.用装置丙检验产物中的水蒸气 D.用装置丁检验产物中的
【答案】B
【解析】浓硫酸和木炭反应需要加热,不能达到实验目的,A不符合题意;二氧化硫具有还原性,能和高
锰酸钾反应使其褪色,能达到实验目的,B符合题意;甲乙溶液中都会带出水使无水硫酸铜变蓝色,不能
达到实验目的,C不符合题意;饱和碳酸氢钠和二氧化碳不反应,不能达到实验目的,D不符合题意。
4.N、O、Na、Mg是周期表中的短周期主族元素。下列有关说法正确的是
A.碱性:NaOH<Mg(OH) B.第一电离能:I(Na)<I(Mg)
2 1 1
C.原子半径:r(N)<r(O) D.N、NaO、Mg的晶体类型相同
2 2
【答案】B
【解析】Na的金属性强于Mg,则NaOH的碱性强于Mg(OH) ,A错误;同周期元素从左到右第一电离能
2
呈增大的趋势,且镁3s轨道全满,较为稳定,第一电离能较大,B正确;同周期元素,从左到右原子半径
逐渐减小,则原子半径N>O,C错误;氮气是分子晶体,NaO为离子晶体,Mg为金属晶体,晶体类型不
2
同,D错误。
阅读下列材料,回答5~7题:
氧、硫、铁可形成多种用途广泛的物质。HO 具有较强的氧化性。亚硫酰氯(SOCl )遇水发生水解反应
2 2 2
生成HSO 与HCl。Fe O 可用作锂离子电池的电极材料,电池工作时有Li+嵌入其中生成LiFe O。FeS 可
2 3 3 4 3 4 2
用于生产HSO ,其一种晶胞结构如图1所示。工业上可电解HSO 与(NH )SO 混合溶液制备过二硫酸
2 4 2 4 4 2 4铵[(NH )SO],其结构如图2所示。
4 2 2 8
图1 图2
5.下列说法正确的是( )
A.SOCl 中硫原子带正电,氯原子带负电
2
B.SO中硫原子的轨道杂化类型是sp2
C.该FeS 晶胞中含S的数目为14
2
D.该FeS 晶体中每个Fe2+周围距离最近且相等的S数目为8
2
【答案】A
【解析】A项,O和Cl的电负性大于S,则S带正电,Cl带负电,正确;B项,SO中S的孤电子对数为=
1,价层电子对数为1+3=4,则S为sp3杂化,错误;C项,S位于8个顶点和6个面心,共有8×+6×=
4,错误;D项,与顶点S最近的Fe2+共有6个,错误
6.下列化学反应表示正确的是( )
A.FeS 在足量空气中煅烧:4FeS+15O=====2Fe O+8SO
2 2 2 2 3 3
B.H O 氧化酸性废水中的Fe2+: 2Fe2++HO===2Fe3++2OH-
2 2 2 2
C. HSO 与氨水中和:HSO (aq)+2NH ·H O(aq)===(NH )SO (aq)+2HO(l);ΔH=-
2 4 2 4 3 2 4 2 4 2
114.6 kJ·mol-1
D.电解法制备(NH )SO 时的阳极反应:2SO-2e-===S O
4 2 2 8 2
【答案】D
【解析】A项,应生成SO ,错误;B项,酸性条件下,不能生成OH-,错误;C项,氨水为弱碱,酸碱
2
中和放出的部分热量用于氨水的电离,即放出的热量小于57.3 kJ×2=114.6 kJ,错误;D项,SO中S为+6
价,SO中S的平均价态为+7,S的化合价升高,失去电子,正确。
2
7.对下列物质性质的解释不合理的是( )
A. H O的热稳定性强于HS,HO分子间存在氢键
2 2 2
B. SO 易液化,SO 是极性分子,分子间作用力较大
2 2
C.(NH )SO 具有较强的氧化性,(NH )SO 中含过氧键(OO)
4 2 2 8 4 2 2 8
D.Fe O 晶体中可嵌入Li+形成LiFe O,Fe3+可转化为Fe2+
3 4 3 4
【答案】A【解析】A项,O的非金属性强于S,则O与H之间的作用力强于S与H,则HO的热稳定性强于HS,
2 2
HO分子间氢键影响熔沸点物理性质,与物质的稳定性无关,错误;B项,SO 是极性分子,极性越强,
2 2
分子间作用力越大,正确;C项,过氧键具有强氧化性,如HO、NaO 均含有过氧根,正确;D项,
2 2 2 2
Fe O 中含有+2、+3价的Fe,当嵌入Li+时,由于O原子的数目不变,负电荷总量不变,则正电荷总量
3 4
也不变,所以有部分Fe3+会转化为Fe2+,正确。
8.硫及其化合物的转化具有重要应用。下列说法不正确的是
A.硫酸型酸雨产生的途径:
B.工业制备硫酸过程中的物质转化:
C.钙基固硫过程中发生的总反应:
D.实验室制备少量 的原理: (固体) (浓)
【答案】C
【解析】硫酸型酸雨产生的途径: ,A正确;工业制硫酸过程中的物质
转化为:FeS 和O 反应生成SO ,SO 发生催化氧化反应生成SO ,SO 和HO反应生成HSO ,B正确;
2 2 2 2 3 3 2 2 4
钙基固硫过程中发生的总反应: ,C错误;实验室制备少量 的原
理: (固体) (浓) ,D正确。
9.化合物Z是一种镇痛消炎药的中间体,可通过如下路线合成。下列说法正确的是
A.化合物X易溶于水 B.1mol Y最多可与1mol NaOH反应
C.X+Y→Z的反应类型为取代反应 D.化合物Z分子中含有手性碳原子
【答案】D
【解析】X中不含亲水基,所以不易溶于水,A错误;Y中酯基水解、氯原子水解都能与NaOH 以1:1反应,所以1molY最多消耗2molNaOH,B错误;Y中羰基和X发生加成反应生成Z,该反应为加成反应,
C错误;Z中连接醇羟基的碳原子为手性碳原子,D正确。
10.活性Fe O 催化反应 ,进而可制得甲酸。反应机理如图所示。
3 4-x
下列说法正确的是
A.该反应的△H>0
B.该反应的平衡常数
C.反应前后,碳原子的杂化方式和化合价均没有发生变化
D.题图所示的反应机理中,步骤Ⅰ可理解为带部分负电荷的氢与HCO 中带部分正电荷的碳结合,带
部分正电荷的氢与带部分负电荷的羟基氧结合生成水,HCO 转化为的HCOO-
【答案】D
【解析】该反应为自发反应,则△H