文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(江苏专用)
黄金卷08
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64 Ce 140
第Ⅰ卷
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1. 化学与生产、生活和社会发展密切相关,下列叙述正确的是
A.华为5G手机麒麟9000芯片(HUAWEIKirin)主要成分是二氧化硅
B.“酒曲”的酿酒工艺,是利用了催化剂使平衡正向移动的原理
C.免洗洗手液的有效成分之一活性银离子能使病毒蛋白质变性
D.葛洪所著《抱朴子》中“丹砂(HgS)烧之成水银,积变又还原成丹砂”,二者为可逆反应
2.下列化学用语表述错误的是 ( )
A.HClO的电子式
B.中子数为10的氧原子:18
O
8
C.NH 分子的VSEPR模型:
3
D.基态N原子的价层电子排布图:
3. 设计实验验证木炭和浓硫酸反应的产物。下列装置和操作能达到实验目的的是
A.用装置甲实现木炭与浓硫酸反应 B.用装置乙检验产物中的
C.用装置丙检验产物中的水蒸气 D.用装置丁检验产物中的
4.N、O、Na、Mg是周期表中的短周期主族元素。下列有关说法正确的是
A.碱性:NaOH<Mg(OH) B.第一电离能:I(Na)<I(Mg)
2 1 1
C.原子半径:r(N)<r(O) D.N、NaO、Mg的晶体类型相同
2 2阅读下列材料,回答5~7题:
氧、硫、铁可形成多种用途广泛的物质。HO 具有较强的氧化性。亚硫酰氯(SOCl )遇水发生水解反应
2 2 2
生成HSO 与HCl。Fe O 可用作锂离子电池的电极材料,电池工作时有Li+嵌入其中生成LiFe O。FeS 可
2 3 3 4 3 4 2
用于生产HSO ,其一种晶胞结构如图1所示。工业上可电解HSO 与(NH )SO 混合溶液制备过二硫酸
2 4 2 4 4 2 4
铵[(NH )SO],其结构如图2所示。
4 2 2 8
图1 图2
5.下列说法正确的是( )
A.SOCl 中硫原子带正电,氯原子带负电
2
B.SO中硫原子的轨道杂化类型是sp2
C.该FeS 晶胞中含S的数目为14
2
D.该FeS 晶体中每个Fe2+周围距离最近且相等的S数目为8
2
6.下列化学反应表示正确的是( )A.FeS 在足量空气中煅烧:4FeS+15O=====2Fe O+8SO
2 2 2 2 3 3
B.H O 氧化酸性废水中的Fe2+: 2Fe2++HO===2Fe3++2OH-
2 2 2 2
C. HSO 与氨水中和:HSO (aq)+2NH ·H O(aq)===(NH )SO (aq)+2HO(l);ΔH=-
2 4 2 4 3 2 4 2 4 2
114.6 kJ·mol-1
D.电解法制备(NH ) SO 时的阳极反应:2SO-2e-===S O7.对下列物质性质的解释不
4 2 2 8 2
合理的是( )
A. H O的热稳定性强于HS,HO分子间存在氢键
2 2 2
B. SO 易液化,SO 是极性分子,分子间作用力较大
2 2
C.(NH )SO 具有较强的氧化性,(NH )SO 中含过氧键(OO)
4 2 2 8 4 2 2 8
D.Fe O 晶体中可嵌入Li+形成LiFe O,Fe3+可转化为Fe2+
3 4 3 4
8.硫及其化合物的转化具有重要应用。下列说法不正确的是
A.硫酸型酸雨产生的途径:
B.工业制备硫酸过程中的物质转化:
C.钙基固硫过程中发生的总反应:
D.实验室制备少量 的原理: (固体) (浓)
9.化合物Z是一种镇痛消炎药的中间体,可通过如下路线合成。下列说法正确的是A.化合物X易溶于水 B.1mol Y最多可与1mol NaOH反应
C.X+Y→Z的反应类型为取代反应 D.化合物Z分子中含有手性碳原子
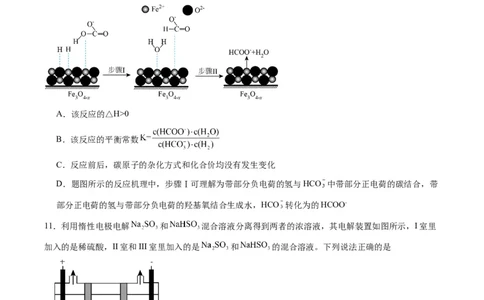
10.活性Fe O 催化反应 ,进而可制得甲酸。反应机理如图所示。
3 4-x
下列说法正确的是
A.该反应的△H>0
B.该反应的平衡常数
C.反应前后,碳原子的杂化方式和化合价均没有发生变化
D.题图所示的反应机理中,步骤Ⅰ可理解为带部分负电荷的氢与HCO 中带部分正电荷的碳结合,带
部分正电荷的氢与带部分负电荷的羟基氧结合生成水,HCO 转化为的HCOO-
11.利用惰性电极电解 和 混合溶液分离得到两者的浓溶液,其电解装置如图所示,I室里
加入的是稀硫酸,II室和III室里加入的是 和 的混合溶液。下列说法正确的是
A.阳极上发生的电极反应:
B.交换膜 是阴离子交换膜
C.电解一段时间后,II室得到的 溶液
D.电解时每转移 电子,理论上阴极区可获得 气体12.室温下,用 溶液制备 的过程如图所示。已知: ,
, , , 。
下列说法正确的是
A.0.1 溶液中:
B. 溶液中:
C.制备 的离子方程式为:
D. 时,应控制
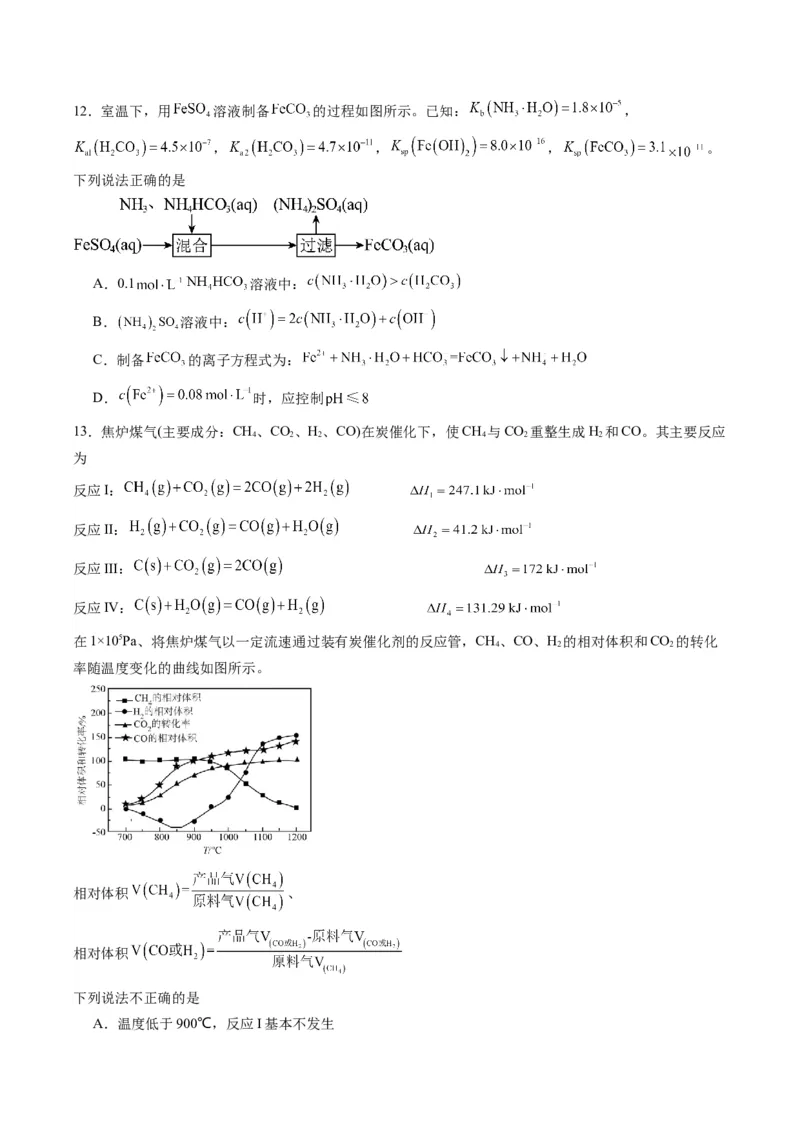
13.焦炉煤气(主要成分:CH、CO、H、CO)在炭催化下,使CH 与CO 重整生成H 和CO。其主要反应
4 2 2 4 2 2
为
反应I:
反应II:
反应III:
反应IV:
在1×105Pa、将焦炉煤气以一定流速通过装有炭催化剂的反应管,CH、CO、H 的相对体积和CO 的转化
4 2 2
率随温度变化的曲线如图所示。
相对体积 、
相对体积
下列说法不正确的是
A.温度低于900℃,反应I基本不发生B.850℃~900℃时,主要发生反应Ⅳ
C.增大焦炉煤气流速一定能提高CO的相对体积
D.工业生产上需要研发低温下CH 转化率高的催化剂
4
第Ⅱ卷
二、非选择题:共4题,共61分。
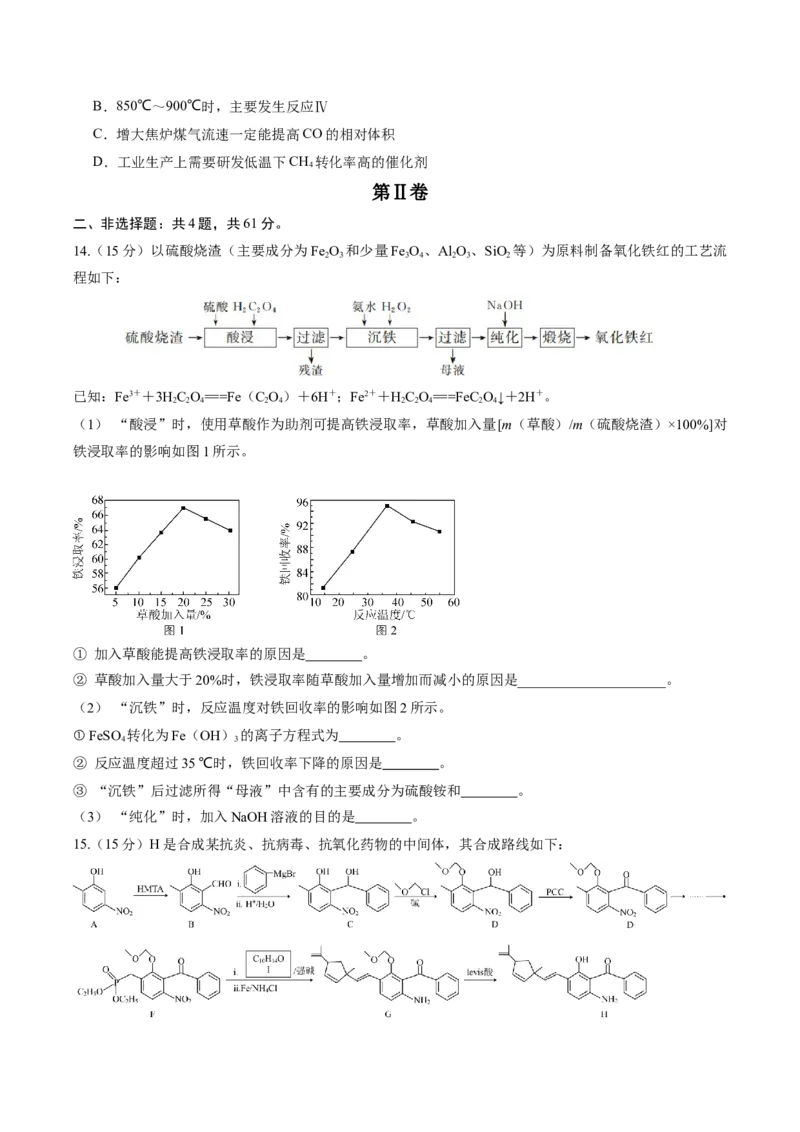
14.(15分)以硫酸烧渣(主要成分为Fe O 和少量Fe O 、Al O 、SiO 等)为原料制备氧化铁红的工艺流
2 3 3 4 2 3 2
程如下:
已知:Fe3++3HC O===Fe(C O)+6H+;Fe2++HC O===FeC O↓+2H+。
2 2 4 2 4 2 2 4 2 4
(1) “酸浸”时,使用草酸作为助剂可提高铁浸取率,草酸加入量[m(草酸)/m(硫酸烧渣)×100%]对
铁浸取率的影响如图1所示。
① 加入草酸能提高铁浸取率的原因是 。
② 草酸加入量大于20%时,铁浸取率随草酸加入量增加而减小的原因是_____________________。
(2) “沉铁”时,反应温度对铁回收率的影响如图2所示。
① FeSO 转化为Fe(OH) 的离子方程式为 。
4 3
② 反应温度超过35 ℃时,铁回收率下降的原因是 。
③ “沉铁”后过滤所得“母液”中含有的主要成分为硫酸铵和 。
(3) “纯化”时,加入NaOH溶液的目的是 。
15.(15分)H是合成某抗炎、抗病毒、抗氧化药物的中间体,其合成路线如下:已知:
回答下列问题:
(1)D→E的反应类型为 ,D中采用 杂化的碳原子有 个。
(2)设计C→D的目的是 。
(3)I的结构简式为 。
(4)I的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式: 。
ⅰ.含苯环且苯环上只有一个取代基
ⅱ.红外光谱无醚键吸收峰
ⅲ.苯环侧链上有3种不同化学环境的氢原子,且个数比为6∶2∶1。
(5)以 、乙醛、 为原料,结合题给信息,设计路线合成 (题给试剂和无机
试剂任选) 。
16.(15分)硫脲[CS(NH ) ]是白色晶体,易溶于水,150 ℃时能转变为NH SCN。常用于制造树脂、染
2 2 4
料、药物,实验室可用下列方法制备。
步骤Ⅰ:称取一定质量的CaS在三颈烧瓶中制成浆液,不断搅拌下通入适量CO ,反应生成Ca(HS) 溶
2 2
液,装置如图所示。
步骤Ⅱ:将一定量的CaCN 与Ca(HS) 溶液混合,加热至80 ℃时生成硫脲。
2 2
已知:HCO 的电离平衡常数分别为K =4.5×10-7、K =4.7×10-11;HS的电离平衡常数分别为K =
2 3 a1 a2 2 a1
1.1×10-7,K =1.3×10-13。
a2
回答下列问题:
(1) 在步骤Ⅰ的三颈烧瓶中生成Ca(HS),其反应的化学方程式为_____________________________。
2
(2) 实验中不宜使用盐酸代替CO 的主要原因是_______________________________。
2
(3) 按如图装置实验,判断CO 是否已过量的方法是__________________________________。
2
(4) 硫脲与酸性KMnO 溶液反应转化为两种无毒的气体及SO,同时生成Mn2+,该反应的离子方程式为
4
。
(5) 已知:NH SCN溶液呈酸性,KSCN溶液呈中性;NH SCN、KSCN都易溶于乙醇、水,温度高时容
4 4
易分解和氧化;常温下KSCN的溶解度为217 g。利用硫脲制备KSCN的方法是:取一定量硫脲 ,将加热后的产物溶
于一定比例的无水乙醇和水中形成溶液, 干燥,得到
KSCN晶体。(实验中可选用试剂:KOH、无水乙醇。实验中须使用的实验仪器有pH计)。
17.(16分)HO、O、O 在水中可形成具有超强氧化能力的羟基自由基(HO•),可有效去除废水中的
2 2 2 3
HPO 、CN-、苯酚等物质。
2
(1)弱碱性条件下HO•将HPO 氧化成PO ,该反应的离子方程式为____。
2
(2)光催化氧化技术也可生成HO•降解有机污染物,其原理如图1,光照时,价带失去电子产生有强氧化
性的空穴,价带上生成HO•的电极反应式为____。图中HO•还有另外的产生途径,描述其产生过程____。
(3)已知Cu2+可催化过氧化氢氧化废水中的CN-。在含氰废水总量、过氧化氢用量和溶液pH一定的情况
下反应相同时间,测得CN-的氧化去除率随c(Cu2+)的变化如图2所示。c(Cu2+)超过90mg•L-1时,CN-的氧化
去除率有所下降,原因是____。
图-2
(4)HO 在Fe O 催化剂表面产生HO•除去废水中的苯酚的原理如图3所示。在不同初始pH条件下,研
2 2 3 4
究苯酚的去除率随时间的变化,结果表明:在反应开始时,初始pH=6的溶液中苯酚的去除率明显低于初
始pH=3的溶液,但一段时间后两者接近,原因是____。
图-3
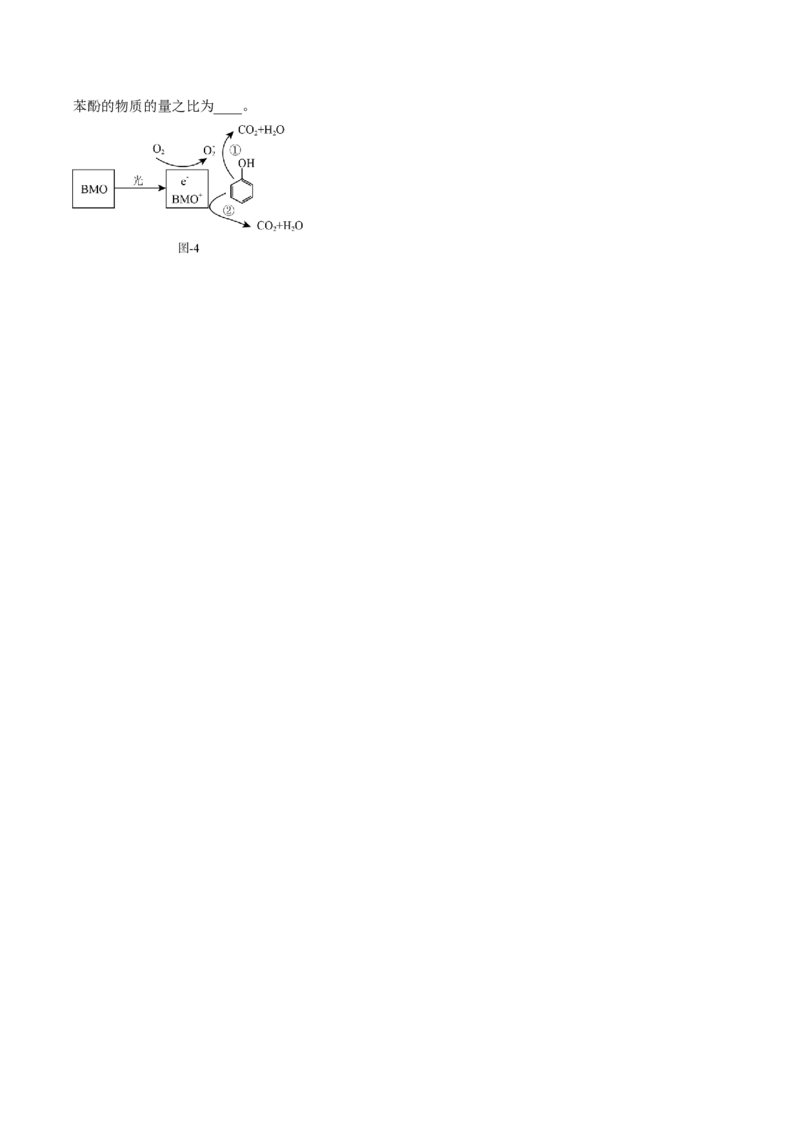
(5)BMO(Bi MoO )是一种高效光催化剂,可用于光催化降解苯酚,原理如图4所示。①和②中被降解的
2 6苯酚的物质的量之比为____。