文档内容
化学键
课题 化学键 单元 4 学科 化学 年级 九 年
级
宏观辨识与微观探析:从宏观上学习离子化合物的特点,从微
观上辨析什么是离子化合物的区别与相似点,体会微观粒子的变化
对宏观物质的性质的影响。
证据推理与模型认知:通过物质分类的基本模型,理解元素的
原子构成的物质的不同之处,通过结合理论与实际感a 知化学学习
【教学目标与
的魅力,为后续的化学知识的学习奠定坚实的方法基础。
核心素养】
科学探究与创新意识:熟悉离子化合物的电子式书写规律,熟
练掌握用电子式表示离子化合物的形成过程的能力,体会化学研究
过程中的科学方法。
科学精神与社会责任:通过对元素的原子构成的物质的不同的
学习和理解,掌握更高效的学习方法,建立高效学习的科学精神。
【重点难点】 1.学习和理解离子化合物的概念。
2.熟悉并掌握电子式的书写方法。
3.学习和理解共价化合物的概念。
4.辨析极性键、非极性键、化学键、分子间作用力的概念。
【教学过程】
教学环节 教师活动 学生活动 设计意图
【第一课时】
导入新课 教师:从元素周期表可以看出,到目前 认 真 倾 图 文 并
为止,已经发现的元素有一百多种。然而, 听老师的描 茂,能够较快
由这一百多种元素的原子构成的物质已超过 述,适当时 地让学生进入
1亿中。那么,元素的原子之间通过什么作 候 做 好 笔 本 节 课 堂 学
用形成如此丰富的物质呢? 记。 习。
在 老 师 简 单 的 思
教师提问:在化学反应的原子组合中, 的带领下, 维训练能够让
原子结合成物质时的相互作用发生了什么变 对问题进行 学生不害怕对
化? 思考。引出 本节课知识点
本 节 课 内 学习,感悟本
容。 节 课 的 知 识
点。
1 / 14教师:引出本节课学习内容
讲授新课 教师利用多媒体设备向学生投影出下面 老 师 和 通 过 讨
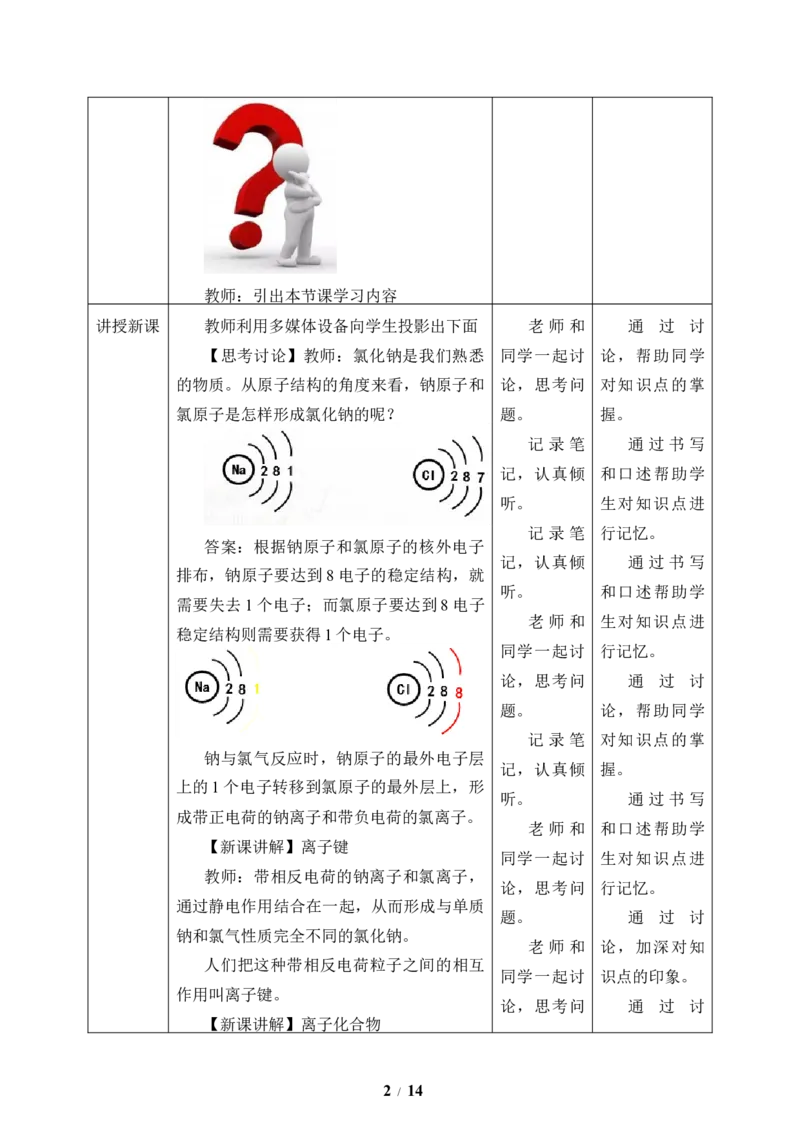
【思考讨论】教师:氯化钠是我们熟悉 同学一起讨 论,帮助同学
的物质。从原子结构的角度来看,钠原子和 论,思考问 对知识点的掌
氯原子是怎样形成氯化钠的呢? 题。 握。
记 录 笔 通 过 书 写
记,认真倾 和口述帮助学
听。 生对知识点进
记 录 笔 行记忆。
答案:根据钠原子和氯原子的核外电子
记,认真倾 通 过 书 写
排布,钠原子要达到8电子的稳定结构,就
听。 和口述帮助学
需要失去1个电子;而氯原子要达到8电子
老 师 和 生对知识点进
稳定结构则需要获得1个电子。
同学一起讨 行记忆。
论,思考问 通 过 讨
题。 论,帮助同学
记 录 笔 对知识点的掌
钠与氯气反应时,钠原子的最外电子层
记,认真倾 握。
上的1个电子转移到氯原子的最外层上,形
听。 通 过 书 写
成带正电荷的钠离子和带负电荷的氯离子。
老 师 和 和口述帮助学
【新课讲解】离子键
同学一起讨 生对知识点进
教师:带相反电荷的钠离子和氯离子,
论,思考问 行记忆。
通过静电作用结合在一起,从而形成与单质
题。 通 过 讨
钠和氯气性质完全不同的氯化钠。
老 师 和 论,加深对知
人们把这种带相反电荷粒子之间的相互
同学一起讨 识点的印象。
作用叫离子键。
论,思考问 通 过 讨
【新课讲解】离子化合物
2 / 14教师:按像氯化钠这样,由离子键构成 题。 论,加深对知
的化合物叫做离子化合物。 认 真 倾 识点的印象。
注:通常,活泼金属与活泼非金属形成 听,在课本 通 过 知 识
离子化合物 的相应位置 点的学习和练
做好笔记。 习题的思考,
记 录 笔 归纳出电子式
【思考讨论】教师:氯化钾、氯化镁、
记,认真倾 的书写步骤。
氯化钙、硫酸锌、氢氧化钠是离子化合物
听。 通 过 书 写
吗?
老 师 和 和口述帮助学
答案:氯化钾的化学式是 KCl,其中K
同学一起讨 生对知识点进
是活泼金属,Cl是活泼非金属,因此氯化钾
论,思考问 行记忆。
是离子化合物;
题。 通 过 讨
氯化镁的化学式是 MgCl ,其中 Mg 是
2
学 生 自 论,加深对知
活泼金属,Cl是活泼非金属,因此氯化镁是
行思考,完 识点的印象。
离子化合物;
成 课 堂 练 通 过 对 习
氯化钙的化学式是CaCl ,其中Ca是活
2
习。 题的解答,加
泼金属,Cl是活泼非金属,因此氯化钙是离
深对知识点的
子化合物;
巩固。
硫酸锌的化学式是 ZnSO ,其中 Zn 和
4
SO42-之间是离子键,因此硫酸锌是离子化
合物;
氢氧化钠的化学式是NaOH,其中Na和
OH-之间是离子键,因此氢氧化钠是离子化
合物。
注:一般来说,化合物中只要含有离子
键就是离子化合物。
【新课讲解】电子式
教师:为方便起见,我们在元素符号周
围用“·”或“×”表示原子的最外层电子(价
电子)。这种式子叫做电子式。
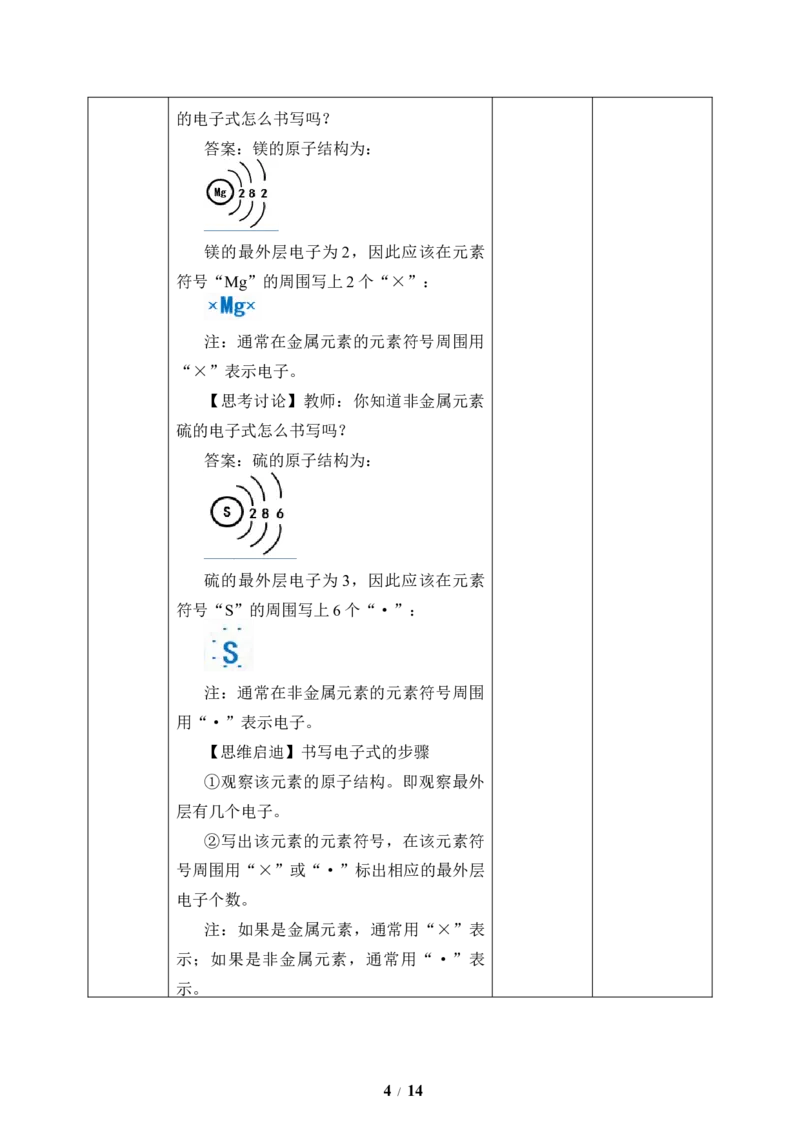
【思考讨论】教师:你知道金属元素镁
3 / 14的电子式怎么书写吗?
答案:镁的原子结构为:
镁的最外层电子为2,因此应该在元素
符号“Mg”的周围写上2个“×”:
注:通常在金属元素的元素符号周围用
“×”表示电子。
【思考讨论】教师:你知道非金属元素
硫的电子式怎么书写吗?
答案:硫的原子结构为:
硫的最外层电子为3,因此应该在元素
符号“S”的周围写上6个“·”:
注:通常在非金属元素的元素符号周围
用“·”表示电子。
【思维启迪】书写电子式的步骤
①观察该元素的原子结构。即观察最外
层有几个电子。
②写出该元素的元素符号,在该元素符
号周围用“×”或“·”标出相应的最外层
电子个数。
注:如果是金属元素,通常用“×”表
示;如果是非金属元素,通常用“·”表
示。
4 / 14【新课讲解】离子化合物的形成表示
教师:离子化合物的形成,可以用电子
式表示,如氯化钠的形成过程可以表示为:
【新课讲解】书写原则
(1)原子、离子都要标出最外层电
子,离子必须标明电荷
(2)阴离子要用方括号括起来
(3)相同的原子可以合并谢,相同的
粒子要单个写(箭头左边相同的微粒可以合
并,箭头右边相同的微粒不可以合并)
(4)不能把“—>”写成“=”
【思考讨论】教师:你能用电子式写出
离子化合物氯化镁的形成过程吗?
【课堂达标】
1.填写下列空格:
带相反电荷的钠离子和氯离子,通过
________结合在一起,从而形成与单质钠和
氯气性质完全不同的氯化钠。
人们把这种带相反电荷粒子之间的相互
作用叫______。像氯化钠这样,由离子键构
成的化合物叫做___________。
解析:带相反电荷的钠离子和氯离子,
通过静电作用结合在一起,从而形成与单质
钠和氯气性质完全不同的氯化钠。
人们把这种带相反电荷粒子之间的相互
作用叫离子键。像氯化钠这样,由离子键构
5 / 14成的化合物叫做离子化合物。
2.写出下列(非)金属元素的电子
式:
①S_______;
②K_______;
③H_______。
解析:首先思考元素的原子结构,例如
“S”的最外层电子数为6,因此在“S”周
围应该有 6 个电子,非金属元素的电子用
“·”表示。所以“S”的电子式如上所
示;“K”的最外层电子数为 1,因此在
“K”周围应该有1个电子,金属元素的电
子用“×”表示。所以“K”的电子式如上
所示;“H”的最外层电子数为 1,因此在
“H”周围应该有1个电子,非金属元素的
电子用“·”表示。所以“H”的电子式如
上所示。
3.写出下列物质的电子式:
①KCl_________________;
②MgCl _________________;
2
③NaCl_________________。
解析:钾失去1个电子形成钾离子,氯
原子得到1个电子形成氯离子,其电子式如
上所示;镁失去2个电子形成镁离子,氯原
子得到1个电子形成氯离子,其电子式如上
所示;钠失去1个电子形成钠离子,氯原子
得到1个电子形成氯离子,其电子式如上所
示。
4.下列物质属于离子化合物的是(
)
A.CO
2
6 / 14B.H SO
2 4
C.SO
2
D.NaF
解析:选项A中,CO 分子只含有共价
2
键,是共价化合物,故 A 错误;选项 B
中,H SO 中只含有共价键,是共价化合
2 4
物,故B错误;选项C中,SO 分子只含有
2
共价键,是共价化合物,故C错误;选项D
中,NaF 分子只含有离子键,是离子化合
物,故D正确。因此选D。
课堂小结 离子键和离子化合物:带相反电荷的钠 学 生 和 通 过 对 课
离子和氯离子,通过静电作用结合在一起, 老师一起快 堂学习知识的
从而形成与单质钠和氯气性质完全不同的氯 速回顾本次 总结,帮助同
化钠。人们把这种带相反电荷粒子之间的相 课的学习内 学 们 加 深 印
互作用叫离子键。像氯化钠这样,由离子键 容。 象。
构成的化合物叫做离子化合物。
电子式:为方便起见,我们在元素符号
周围用“·”或“×”表示原子的最外层电
子(价电子)。这种式子叫做电子式。
用电子式表示离子化合物的形成过程注
意事项:
(1)原子、离子都要标出最外层电
子,离子必须标明电荷
(2)阴离子要用方括号括起来
(3)相同的原子可以合并谢,相同的
粒子要单个写(箭头左边相同的微粒可以合
并,箭头右边相同的微粒不可以合并)
(4)不能把“—>”写成“=”
7 / 14板书 学 生 在 方 便 学 生
笔记本上对 课后回顾。
板书进行誊
写。
【第二课时】
导入新课 教师:为什么 2 个氢原子结合成氢分 认 真 倾 图 文 并
子,2 个氯原子结合成氯分子,而不是 3 听老师的描 茂,能够较快
个,4个呢? 述,适当时 地让学生进入
候 做 好 笔 本 节 课 堂 学
记。 习。
在 老 师 简 单 的 思
的带领下, 维训练能够让
教师提问:为什么1个氢原子和1个氯 对问题进行 学生不害怕对
思考。引出 本节课知识点
原子结合成氯化氢分子,氯原子和氢原子的
个数比是1:1,而不是以其他个数比相结合 本 节 课 内 学习,感悟本
容。 节 课 的 知 识
呢?
点。
教师:引出本节课学习内容
讲授新课 教师利用多媒体设备向学生投影出下面 老 师 和 通 过 讨
【思考讨论】教师:氯分子是如何形成 同学一起讨 论,帮助同学
的呢? 论,思考问 对知识点的掌
答案:氯原子的最外层有7个电子,要 题。 握。
达到 8 电子稳定结构,都需要获得 1 个电 记 录 笔 通 过 书 写
子,所以氯原子之间难以发生电子的得失。 记,认真倾 和口述帮助学
如果2个氯原子各提供1个电子,形成共用 听。 生对知识点进
电子对,2个氯原子就形成了 8电子稳定结 记 录 笔 行记忆。
构: 记,认真倾 通 过 书 写
听。 和口述帮助学
记 录 笔 生对知识点进
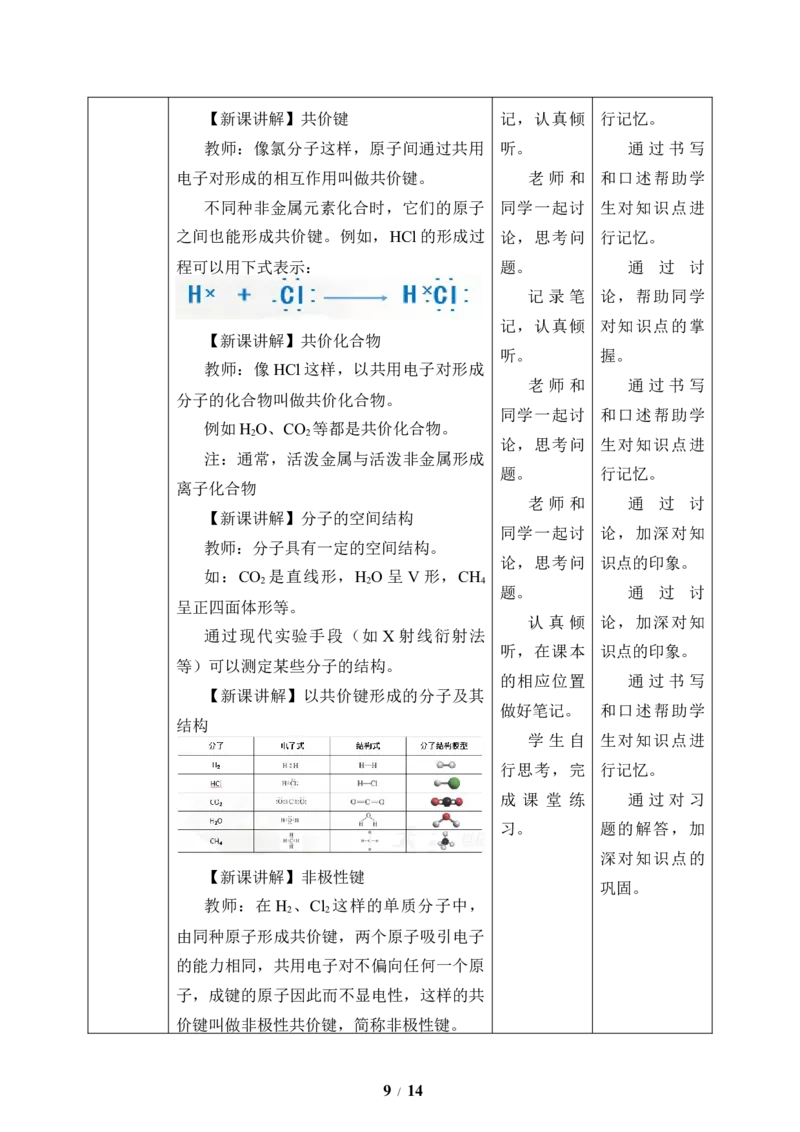
8 / 14【新课讲解】共价键 记,认真倾 行记忆。
教师:像氯分子这样,原子间通过共用 听。 通 过 书 写
电子对形成的相互作用叫做共价键。 老 师 和 和口述帮助学
不同种非金属元素化合时,它们的原子 同学一起讨 生对知识点进
之间也能形成共价键。例如,HCl的形成过 论,思考问 行记忆。
程可以用下式表示: 题。 通 过 讨
记 录 笔 论,帮助同学
记,认真倾 对知识点的掌
【新课讲解】共价化合物
听。 握。
教师:像HCl这样,以共用电子对形成
老 师 和 通 过 书 写
分子的化合物叫做共价化合物。
同学一起讨 和口述帮助学
例如H O、CO 等都是共价化合物。
2 2
论,思考问 生对知识点进
注:通常,活泼金属与活泼非金属形成
题。 行记忆。
离子化合物
老 师 和 通 过 讨
【新课讲解】分子的空间结构
同学一起讨 论,加深对知
教师:分子具有一定的空间结构。
论,思考问 识点的印象。
如:CO 是直线形,H O 呈 V 形,CH
2 2 4
题。 通 过 讨
呈正四面体形等。
认 真 倾 论,加深对知
通过现代实验手段(如 X 射线衍射法
听,在课本 识点的印象。
等)可以测定某些分子的结构。
的相应位置 通 过 书 写
【新课讲解】以共价键形成的分子及其
做好笔记。 和口述帮助学
结构
学 生 自 生对知识点进
行思考,完 行记忆。
成 课 堂 练 通 过 对 习
习。 题的解答,加
深对知识点的
【新课讲解】非极性键
巩固。
教师:在 H 、Cl 这样的单质分子中,
2 2
由同种原子形成共价键,两个原子吸引电子
的能力相同,共用电子对不偏向任何一个原
子,成键的原子因此而不显电性,这样的共
价键叫做非极性共价键,简称非极性键。
9 / 14【思考讨论】教师:在化合物分子中,
不同种原子形成共价键时有什么特点呢?
答案:因为原子吸引电子的能力不同,
共用电子对偏向吸引电子能力强的一方,所
以吸引电子能力强的原子一方显负电性,吸
引电子能力弱的原子一方显正电性。
例如,HCl分子中,Cl吸引电子的能力
比H强,共用电子对偏向Cl一方,Cl一方
相对显负电性,H一方则相对显正电性。
【新课讲解】极性键
教师:像HCl这样,共用电子对偏移的
共价键叫做极性共价键,简称极性键。
H O、CO 中的共价键也是极性键。
2 2
注:共价键分为极性键和非极性键。
【新课讲解】化学键
教师:原子结合成分子时存在相互作
用。
这种作用存在于分子内相邻原子之间,
也存在于非直接相邻的原子之间,而相邻原
子之间的相互作用比较强烈。我们把这种相
邻的原子之间强烈的相互作用叫做化学键。
【思考讨论】教师:化学键的形成与什
么有关?
答案:化学键的形成与原子结构有关,
它主要通过原子的价电子间的转移或共用来
实现。一般的化学物质主要由离子键或共价
键结合而成。
【思考讨论】教师:化学反应是反应物
中原子重新组合成产物分子的一种过程吗?
10 / 14答案:表面上看,化学反应是反应物中
原子重新组合成产物分子的一种过程,其
实,化学反应过程中,包含着反应物分子内
化学键的断裂和产物分子中化学键的形成。
其中包含两个步骤:①H 和Cl 中的化
2 2
学键(旧化学键)断裂,生成H和Cl;②H
和Cl结合成HCl,形成了H和Cl之间的化
学键H—Cl(新化学键)。
研究证实,化学反应的过程,本质上就
是旧化学键断裂和新化学键形成的过程。
【新课讲解】分子间作用力
教师:分子内相邻的原子之间存在着化
学键。分子间还存在一种把分子聚集在一起
的作用力,即分子间作用力。
荷兰物理学家范德华最早研究分子间作
用力,所以最初也将分子间作用力称为范德
华力。范德华力比化学键弱得多,对物质的
熔点、沸点等有影响。
NH 、Cl 、CO 等气体在降低温度、增
3 2 2
大压强时能凝结成液态或固态,就是由于存
在范德华力。
分子间形成的氢键也是一种分子间作用
力,它比化学键弱,但比范德华力强。氢键
会使物质的熔点和沸点升高,这是因为固体
熔化或液体汽化时必须破坏分子间的氢键,
消耗较多能量。
【课堂达标】
11 / 141.填空
原子间通过共用电子对形成的相互作用
叫做________。
共用电子对不偏向任何一个原子,成键
的原子因此而_________,这样的共价键叫
做非极性共价键,简称_________。
共用电子对偏移的共价键叫做极性共价
键,简称_________。
解析:原子间通过共用电子对形成的相
互作用叫做共价键;共用电子对不偏向任何
一个原子,成键的原子因此而不显电性,这
样的共价键叫做非极性共价键,简称非极性
键;共用电子对偏移的共价键叫做极性共价
键,简称极性键。
2.写出下列物质的电子式:
①Cl _______________
2
②H O_______________
2
③CH _______________
4
解析:首先思考元素的原子结构,例如
“Cl”的最外层电子数为7,因此在“Cl”
周围应该有7个电子,非金属元素的电子用
“·”表示。所以两个“Cl”结合成的
“Cl ”的电子式如上所示;“H”的最外层
2
电子数为1,“O”的最外层电子数为6,两
个“H”都失掉一个电子,正好可以使
“O”周围的电子数达到8个,金属元素的
电子用“×”表示。所以“H O”的电子式
2
如上所示; “H”的最外层电子数为
1,“C”的最外层电子数为4,四个“H”
都失掉一个电子,正好可以使“C”周围的
电子数达到8个。所以“CH ”的电子式如
4
12 / 14上所示。
3.下列变化过程中,共价键被破坏的
是( )
A.烧碱固体溶于水
B.氯化氢气体溶于水
C.CO 气体变成干冰
2
D.碘溶于酒精
解析:选项A中,氢氧化钠是离子化合
物,溶于水电离出阴阳离子,破坏的是离子
键,故 A 错误;选项 B 中,氯化氢溶于
水,电离出阴阳离子,破坏的是共价键,故
B 正确;选项 C 和 D 中,CO 气体变成干
2
冰、碘溶于酒家中都是物理变化,破坏的是
分子间作用力,故D错误。因此选B。
4.下列物质中,含有极性共价键的是
( )
A.单质碘
B.氯化镁
C.溴化钾
D.水
解析:选项A中,非金属单质分子含有
非极性共价键,A项错误;选项B中,氯化
镁只含有离子键,B项错误;选项C中,溴
化钾中只含有离子键,C 项错误;选项 D
中,水所含化学键为不同非金属原子之间形
成的,为极性共价键,D 项正确。因此选
D。
课堂小结 共价键和共价化合物:像氯分子这样, 学 生 和 通 过 对 课
原子间通过共用电子对形成的相互作用叫做 老师一起快 堂学习知识的
共价键。不同种非金属元素化合时,它们的 速回顾本次 总结,帮助同
原子之间也能形成共价键。例如HCl。 课的学习内 学 们 加 深 印
13 / 14像HCl这样,以共用电子对形成分子的 容。 象。
化合物叫做共价化合物。
分子的空间结构:分子具有一定的空间
结构。如:CO 是直线形,H O 呈 V 形,
2 2
CH 呈正四面体形等。通过现代实验手段
4
(如X射线衍射法等)可以测定某些分子的
结构。
极性键和非极性键:像 HCl这样,共用
电子对偏移的共价键叫做极性共价键,简称
极性键。
在 H 、Cl 这样的单质分子中,由同种
2 2
原子形成共价键,两个原子吸引电子的能力
相同,共用电子对不偏向任何一个原子,成
键的原子因此而不显电性,这样的共价键叫
做非极性共价键,简称非极性键。
化学反应的实质:化学反应的过程,本
质上就是旧化学键断裂和新化学键形成的过
程。
板书 学 生 在 方 便 学 生
笔记本上对 课后回顾。
板书进行誊
写。
14 / 14