文档内容
氯及其化合物
课题 氯及其化合物 单元 2 学科 化学 年级
知识与技能
1学习氯的物理性质。掌握氯与非金属、金属的反应。掌握氯与
水的反应。
2掌握氯与碱的反应。掌握实验室制氯气的方法。学习氯离子的
检验方法。
过程与方法
【 教 学 目
1引导学生自主学习,引导学生学习氯的物理性质,掌握氯与非
标】
金属、金属、水的反应。
2引导学生自主学习,引导学生学习氯与碱的反应,掌握实验室
制氯气的方法,学习氯离子的检验方法。
情感、态度与价值观
1培养学生严谨求实、勇于探索的化学态度.
2对知识进行分类的方法是简单易行的科学方法.
【 教 学 重 1学习氯的物理性质。掌握氯的化学性质。
点】 2掌握氯与碱的反应。掌握实验室制氯气的方法。
【 教 学 难 1掌握氯的化学性质。
点】 2掌握氯与碱的反应。
3掌握实验室制氯气的方法。
【教学过程】
【第一课时】
教学环节 教师活动 学生活动 设计意图
导入新课 教师:氯是一种重要的“成盐物质”。 老师引 图 文 并
教师:在自然界中除了以 NaCl、MgCl 、 导 学 生 思 茂,能够较
2
CaCl 等形式大量存在于海水中,还存在于陆地 考。 快地让学生
2
的盐湖和盐矿中。(展示图片) 在老师 进入本节课
的带领下, 堂学习。
对氯的相关 简 单 的
内容进行了 思维训练能
教师:氯的单质氯气是一种重要的化工原
解。 够让学生不
料。大量用于制造盐酸、有机溶剂、农药、染
害怕对本节
料和药品等。(展示图片)
课知识点学
习,感悟本
节课的知识
1/17点。
教师提问:氯有哪些性质呢?
教师:引出本节课学习内容
讲授新课 教师利用多媒体设备向学生投影出下面 了解氯 增 长 见
思维启迪:18世纪70年代,瑞典化学家舍 气的发现历 识,对学习
勒将软锰矿与浓盐酸混合加热,产生了一种黄 程。 氯气有更宽
绿色、有刺激性气味的气体。受当时流行学说 老师和 广的了解。
的影响,舍勒未能确认这种气体。直到 1810 同学一起讨 通 过 讨
年,英国化学家戴维才确认这种气体是一种新 论,思考问 论,帮助同
元素组成的单质——氯气。(展示照片) 题。 学对知识点
了解氯 的掌握。
气的发现历 增 长 见
程。 识,拓宽学
总结氯 生知识面。
气的物理性 加 深 对
质。 知识点的印
思考讨论:教师:从氯气的发现到氯被确
老师和 象。
认为一种新的元素,时间长达三十多年,其间
同学一起讨 通 过 讨
经历了数位科学家的不懈探索。你从这一史实
论,思考问 论,帮助同
中得到什么启示?
题。 学对知识点
记录笔 的掌握。
记,在书中 通 过 老
相应部位进 师口述和实
教师:启示1:科学研究需要由正确的理论 行誊写,养 验展示,帮
做指导,错误的理论只会浪费时间和精力。 成良好的学 助同学们掌
教师:启示2:科学研究需要以大量事实为 习习惯。 握知识点,
依据,只有大量事实才能推翻错误理论,建立 观察实 并加深对知
正确的理论或推动科学理论的发展。 验现象。 识 点 的 印
2/17教师:启示3:科学研究需要有热爱科学的 老师和 象。
思想和奉献科学的精神。 同学一起讨 通 过 老
思维启迪:氯气的命名 论,思考问 师口述和实
1810年,英国化学家戴维以大量事实为依 题。 验展示,帮
据,确认黄绿色气体是一种新元素组成的单 记录笔 助同学们掌
质,并将这种元素命名为chlorine。这一名称来 记,在书中 握知识点,
自希腊文,有“绿色”的意思。中文译名曾为 相应部位进 并加深对知
“绿气”,后改为“氯气”。 行誊写,养 识 点 的 印
新课讲解:氯气的性质 成良好的学 象。
①形态:气体 习习惯。 增 长 见
②颜色:黄绿色 同学们 识,对学习
③熔点:-101℃ 在老师的引 氯气有更宽
④沸点:-34.6℃ 导 下 , 讨 广的了解。
⑤密度:3.214g/L(0℃) 论。 加 深 对
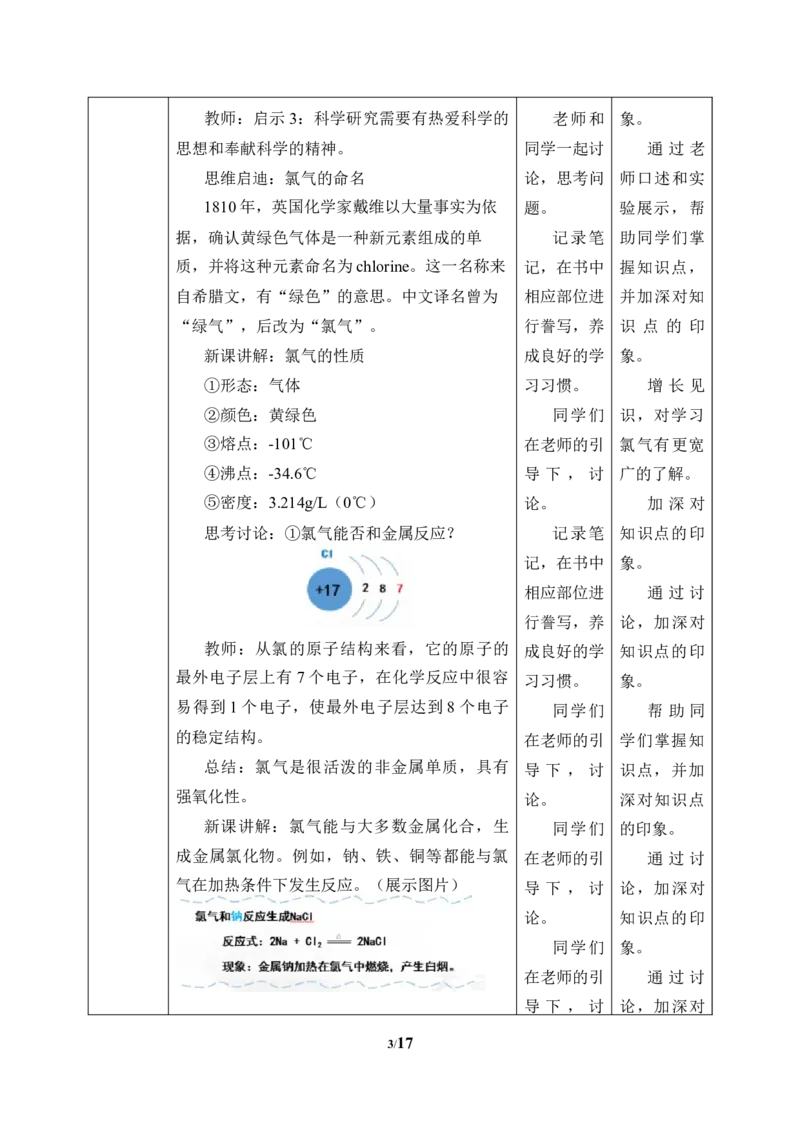
思考讨论:①氯气能否和金属反应? 记录笔 知识点的印
记,在书中 象。
相应部位进 通 过 讨
行誊写,养 论,加深对
教师:从氯的原子结构来看,它的原子的 成良好的学 知识点的印
最外电子层上有 7个电子,在化学反应中很容
习习惯。 象。
易得到1个电子,使最外电子层达到 8个电子
同学们 帮 助 同
的稳定结构。 在老师的引 学们掌握知
总结:氯气是很活泼的非金属单质,具有 导 下 , 讨 识点,并加
强氧化性。 论。 深对知识点
新课讲解:氯气能与大多数金属化合,生 同学们 的印象。
成金属氯化物。例如,钠、铁、铜等都能与氯 在老师的引 通 过 讨
气在加热条件下发生反应。(展示图片) 导 下 , 讨 论,加深对
论。 知识点的印
同学们 象。
在老师的引 通 过 讨
导 下 , 讨 论,加深对
3/17论。 知识点的印
学生自 象。
行思考,完 通 过 讨
成 课 堂 练 论,加深对
习。 知识点的印
象。
通 过 对
思考讨论:②氯气能否和非金属反应?
习 题 的 解
教师:在空气中点燃氢气,然后将导管缓
答,加深对
慢伸入盛满氯气的集气瓶中,观察现象。
知识点的巩
(注:氯气有毒,人吸入少量氯气会使鼻
固。
和喉头的黏膜受到刺激,引起咳嗽和胸部疼
痛,吸入大量氯气会中毒致死。)
现象:可以观察到纯净的H 在Cl 中安静的
2 2
燃烧,发出苍白色火焰。反应生成的气体是
HCl,它在空气中与水蒸气结合,呈现雾状。
反应式:H +Cl ——2HCl
2 2
(注:HCl气体溶于水,就成为我们常用的
盐酸)
思考讨论:我们以前学过的燃烧反应,都
是物质在氧气中的燃烧。现在又观察到了 H 在
2
Cl 中的燃烧。你对燃烧的条件及其本质有什么
2
新的认识?
教师:启示1:燃烧不一定要有氧气参与。
任何发光、发热的剧烈化学反应,都是燃烧。
教师:启示2:Cl 和O 相似,既能和金属
2 2
反应,也能和非金属反应,是一种活泼的非金
属单质。具有强氧化性。
4/17教师:启示3:任何可燃物的燃烧都要经历
氧化分解、着火、燃烧等阶段。
新课讲解:氯气与金属、非金属单质的反
应
①与金属钠加热生成NaCl
②与金属铁加热生成FeCl
3
③与金属铜加热生成CuCl
2
④与氢气加热生成HCl
思考讨论:目前,很多自来水厂用氯气来
杀菌、消毒,我们偶尔闻到的自来水散发出的
刺激性气味就是余氯的气味。为什么可以用氯
气杀菌、消毒呢?
教师:在25℃时,1体积的水可以溶解约2
体积的氯气,氯气的水溶液称为氯水。常温
下,溶于水中的部分氯气会与水发生反应,生
成盐酸和次氯酸。Cl +H O——HCl+HClO
2 2
总结:氯气可以杀菌、消毒,正是因为氯
气与水反应产生的次氯酸。次氯酸具有强氧化
性,因此,次氯酸能杀死水中的病菌,起到消
毒的作用。
概念辨析:氯和氯水
液氯是氯气加压降温液化后的产物。是单
纯的氯气,是纯净物。
5/17氯水是氯气溶于水以后的混合物。里面含
有氯化氢、次氯酸、还有没有反应只是溶解的
氯气。
思维启迪:新的自来水消毒剂
氯气是一种有毒气体,但控制氯气的用
量,使水中余氯的含量达到国家引用标准,氯
气可以用于自来水的杀菌、消毒。使用氯气对
自来水消毒时可能产生一些负面影响,因此,
人们已经开始使用一些新型自来水消毒剂。
思考讨论:使用氯气对自来水消毒时,氯
气会与水中的有机物发生反应,生成的有机氯
化物可能对人体有害。所以,国家规定了饮用
水中余氯含量的标准;而且已经开始使用新的
自来水消毒剂,如二氧化氯、臭氧等。你能得
到什么启示吗?
教师:启示1:科学是把双刃剑,有利也有
弊。
教师:启示2:只要弄清楚了化学反应的本
质,就能通过控制氯气的用量达到理想的效
果。
教师:启示3:根据化学反应的本质,我们
可以寻找氯气的替代品来解决现实生活中的问
题。
思考讨论:
(1)取干燥的和湿润的有色纸条(或布
条)各一条,分别放入两个盛有干燥氯气的集
气瓶中,盖上玻璃片,观察现象。
6/17教师:现象如图所示。
总结:干燥的氯气不具有漂白性,不能使
有色纸条褪色,氯气和水反应生成盐酸和次氯
酸,次氯酸有漂白性,可使有色纸条褪色。
思考讨论:
(2)将有色鲜花放入盛有干燥氯气的集气
瓶中,盖上玻璃片,观察现象。
教师:干燥的氯气使有色鲜花变色了。
新课讲解:次氯酸
教师:次氯酸的强氧化性还能使某些染料
和有机色素褪色,因此,次氯酸可用作棉、麻
和纸张的漂白剂。次氯酸是很弱的酸,只存在
于水溶液中。次氯酸不稳定,在光照下容易分
解放出氯气。
课堂达标:
1.填写下列氯气的物理性质
金 属 钠 : 颜 色 ________ ; 形 态
7/17__________;气味________;__________毒、
__________溶于水
解析:氯气是黄绿色气体,气味大,有
毒,且易溶于水并和水反应产生次氯酸。
2.下列描述中正确的是( )
A.液氯和氯水是同一种物质
B.氯气是黄绿色气体
C.氯气与水反应,氯是氧化剂,水是还原
剂
D.氯原子的最外电子层上只有1个电子
解析:液氯、氯水都是液体,但前者是纯
氯,后者是氯与水的混合物,A错误;氯气是
黄绿色气体,B正确;氯与水的反应是氯分子
中氯原子间发生的自身氧化还原,即歧化反
应,水虽然是反应物,却未参加氧化还原,C
错误;氯原子最外电子层有 7个电子,容易得
电子,D错误。故选B。
3.下列反应式书写正确的是( )
A . 氯 气 和 水 反 应 : 2Cl +H O— —
2 2
HCl+HClO
B.氯气和铁反应:Fe+Cl ——FeCl
2 2
C.氯气和钠反应:2Na+Cl ——2NaCl
2
D.氯气和铜反应:2Cu+3Cl ——2CuCl 解
2 3
析:氯气和水反应产生次氯酸的反应式应为:
Cl +H O——HCl+HClO;A错误;氯气和铁反
2 2
应产生氯化铁:2Fe+3Cl ——2FeCl ,B错误;
2 3
C 正确;氯气和铜反应产生氯化铜:Cu+Cl
2
——CuCl ,D错误。故选C。
2
4.湿润的有色纸条放入盛有干燥氯气的集
气瓶中会褪色是因为物质( )
A.HCl
8/17B.HClO
C.Cl
2
D.H O
2
解析:氯气和水反应生成盐酸和次氯酸,
次氯酸有漂白性,可使有色纸条褪色。
课堂小结 氯气的物理性质:黄绿色气体,气味大, 学生和 通 过 对
有毒 老师一起快 课堂学习知
易溶于水,熔点:-101℃,沸点:-34.6℃ 速回顾本次 识的总结,
氯的化学性质: 课的学习内 帮助同学们
能与金属反应:与金属钠加热生成 NaCl, 容。 加深印象。
与金属铁加热生成 FeCl ,与金属铜加热生成
3
CuCl ;
2
能与非金属反应:与氢气加热生成HCl;能
与水反应:与水反应生成次氯酸。
板书 学生在 方 便 学
笔记本上对 生 课 后 回
板书进行誊 顾。
写。
【第二课时】
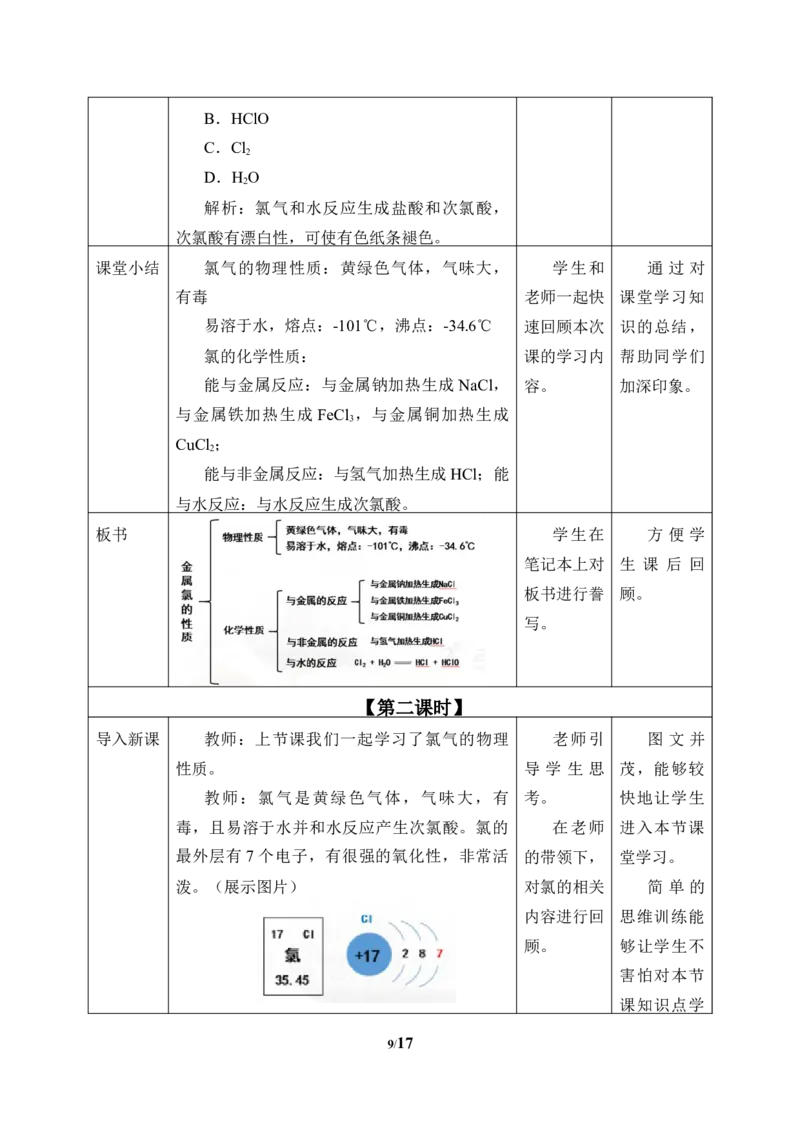
导入新课 教师:上节课我们一起学习了氯气的物理 老师引 图 文 并
性质。 导 学 生 思 茂,能够较
教师:氯气是黄绿色气体,气味大,有 考。 快地让学生
毒,且易溶于水并和水反应产生次氯酸。氯的 在老师 进入本节课
最外层有7个电子,有很强的氧化性,非常活 的带领下, 堂学习。
泼。(展示图片) 对氯的相关 简 单 的
内容进行回 思维训练能
顾。 够让学生不
害怕对本节
课知识点学
9/17教师:上节课我们一起学习了氯的化学性 习,感悟本
质。(展示图片) 节课的知识
氯能与金属反应:与金属钠加热生成 点。
NaCl;与金属铁加热生成FeCl ;与金属铜加热
3
生成CuCl 。
2
氯能与水反应:氯气与水反应产生的次氯
酸具有强氧化性,因此,次氯酸能杀死水中的
病菌,起到消毒的作用。
氯能与非金属反应与氢气加热生成HCl。
教师提问:氯可以与金属、非金属、水反
应,它的化学性质非常活泼。那么氯能不能和
碱反应呢?(展示图片)
教师:引出本节课学习内容
讲授新课 教师利用多媒体设备向学生投影出下面 通过提 通 过 讨
思考讨论:教师:常温下,将 Cl 通入 示与讨论, 论,帮助同
2
NaOH溶液中,可以得到以 NaClO为有效成分 书写相关反 学对知识点
的漂白液。你能书写出正确的反应式吗? 应式。 的掌握。
答案: 记录笔 拓 展 同
Cl +2NaOH——NaCl+NaClO+H O 记,认真倾 学 的 知 识
2 2
思考讨论:教师:常温下,将Cl 通入石灰 听。 面。
2
乳中,就能得到Ca(ClO) 为有效成分的漂白 老师和 通 过 讨
2
粉。你能书写出正确的反应式吗? 同学一起讨 论,帮助同
答案: 论,思考问 学对知识点
2Cl +2Ca(OH) ——Ca(ClO) +CaCl +2H O 题。 的掌握。
2 2 2 2 2
思维启迪:最初,人们直接用氯水作漂白 记录笔 拓 展 同
剂,但因氯气的溶解度不大,而且生成的次氯 记,认真倾 学 的 知 识
酸不稳定,难以保存,使用起来很不方便,效 听。 面。
10/17果也不理想。在Cl 与水反应原理的基础上,人 老师和 加 深 对
2
们制得了次氯酸钠、次氯酸钙等具有漂白作用 同学一起讨 知识点的印
的次氯酸盐。 论,思考问 象。
思考讨论:教师:为什么要用次氯酸盐取 题。 通 过 老
代次氯酸做漂白剂?(展示图片) 记录笔 师口述和实
记,在书中 验展示,帮
相应部位进 助同学们掌
行誊写,养 握知识点,
答案:HClO不稳定,难以保存。NaClO虽
成良好的学 并加深对知
然会分解,但它的水溶液在低温存放三年才分
习习惯。 识 点 的 印
解一半,比HClO稳定得多。
老师和 象。
思维启迪:漂粉精、漂白液、漂白粉既可
同学一起讨 通 过 讨
作漂白棉、麻、纸张的漂白剂,又可用作游泳
论,思考问 论,加深对
池等场所的消毒剂。(展示图片)
题。 知识点的印
思考讨论:教师:你知道舍勒是怎么发现
记录笔 象。
氯气的吗?(展示图片)
记,在书中 加 深 对
相应部位进 知识点的印
行誊写,养 象。
答案:舍勒发现氯气的方法至今还是实验 成良好的学 通 过 讨
室中制取氯气的主要方法之一。即利用浓盐酸 习习惯。 论,加深对
与二氧化锰反应来制取氯。 同学们 知识点的印
新课讲解:制取氯气 在老师的引 象。
教师:浓盐酸与二氧化锰制取氯气的反应 导 下 , 讨 通 过 老
式: 论。 师口述和实
MnO +4HCl(浓)——MnCl +Cl +2H O 同学们 验展示,帮
2 2 2 2
在老师的引 助同学们掌
导 下 , 讨 握知识点,
论。 并加深对知
记录笔 识 点 的 印
记,在书中 象。
相应部位进 帮 助 同
11/17行誊写,养 学们掌握知
成良好的学 识点,并加
习习惯。 深对知识点
同学们 的印象。
在老师的引 通 过 讨
导 下 , 讨 论,加深对
论。 知识点的印
学生自 象。
行思考,完 通 过 对
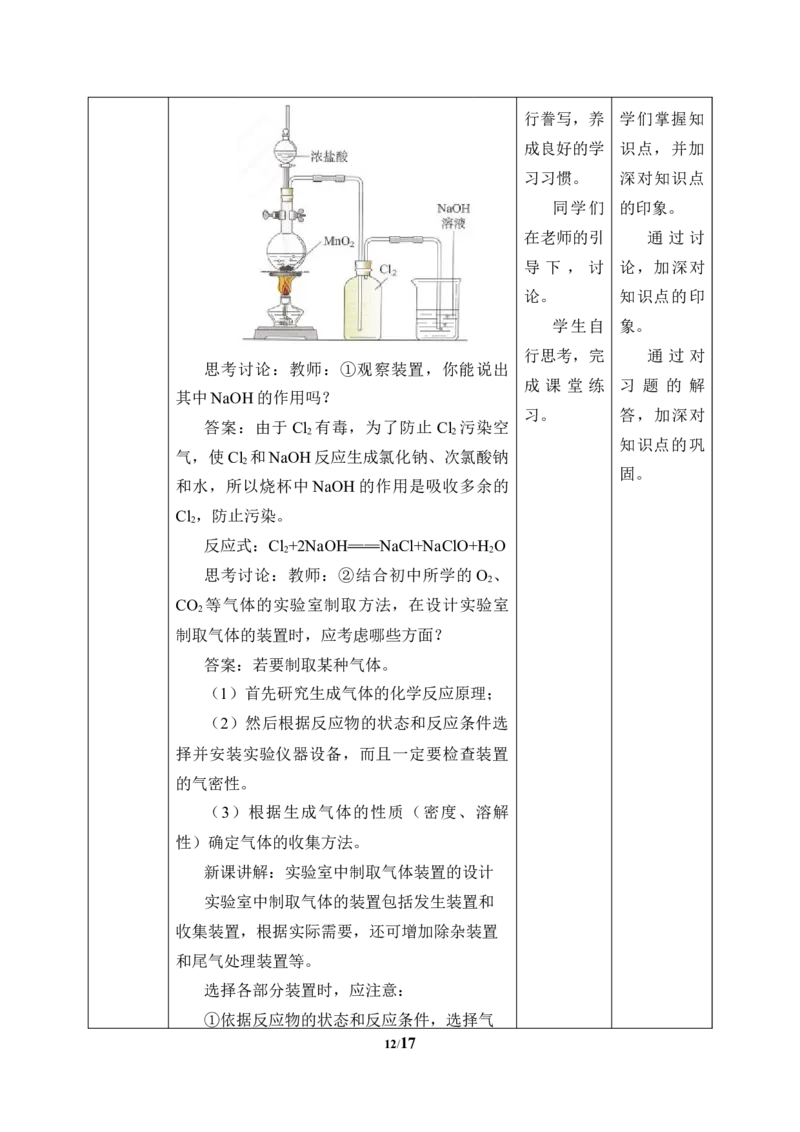
思考讨论:教师:①观察装置,你能说出
成 课 堂 练 习 题 的 解
其中NaOH的作用吗?
习。 答,加深对
答案:由于 Cl 有毒,为了防止 Cl 污染空
2 2
知识点的巩
气,使Cl 和NaOH反应生成氯化钠、次氯酸钠
2
固。
和水,所以烧杯中 NaOH的作用是吸收多余的
Cl ,防止污染。
2
反应式:Cl +2NaOH——NaCl+NaClO+H O
2 2
思考讨论:教师:②结合初中所学的 O 、
2
CO 等气体的实验室制取方法,在设计实验室
2
制取气体的装置时,应考虑哪些方面?
答案:若要制取某种气体。
(1)首先研究生成气体的化学反应原理;
(2)然后根据反应物的状态和反应条件选
择并安装实验仪器设备,而且一定要检查装置
的气密性。
(3)根据生成气体的性质(密度、溶解
性)确定气体的收集方法。
新课讲解:实验室中制取气体装置的设计
实验室中制取气体的装置包括发生装置和
收集装置,根据实际需要,还可增加除杂装置
和尾气处理装置等。
选择各部分装置时,应注意:
①依据反应物的状态和反应条件,选择气
12/17体的发生装置;
②依据气体及其所含杂志的性质,选择除
杂装置;
③依据气体的密度、气体在水中的溶解
性,以及是否与水反应,选择收集装置;
④依据气体的性质,选择尾气处理装置。
装置的连接顺序一般为:
发生装置→除杂装置→收集装置→尾气处
理装置
思考讨论:氯的性质很活泼,能与很多金
属反应生成盐,其中大多数盐能溶于水并电离
出氯离子。有没有什么办法能检验物质中是否
存在氯离子呢?
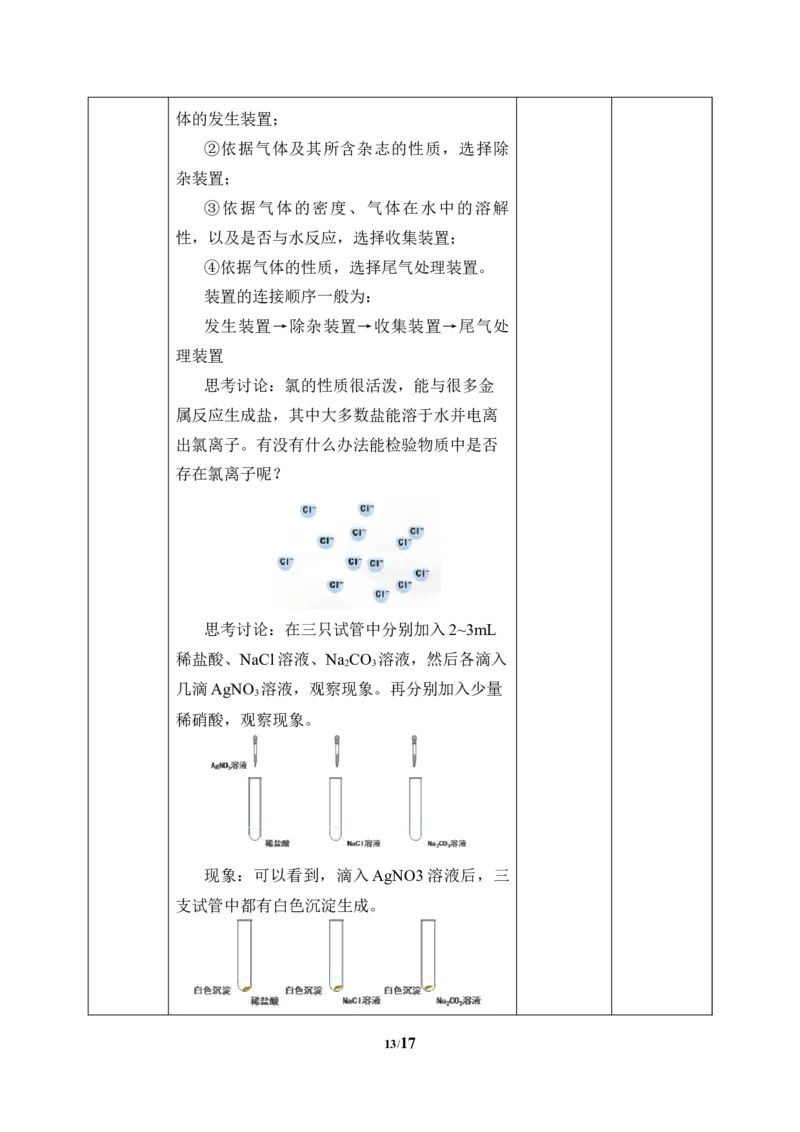
思考讨论:在三只试管中分别加入2~3mL
稀盐酸、NaCl溶液、Na CO 溶液,然后各滴入
2 3
几滴AgNO 溶液,观察现象。再分别加入少量
3
稀硝酸,观察现象。
现象:可以看到,滴入AgNO3溶液后,三
支试管中都有白色沉淀生成。
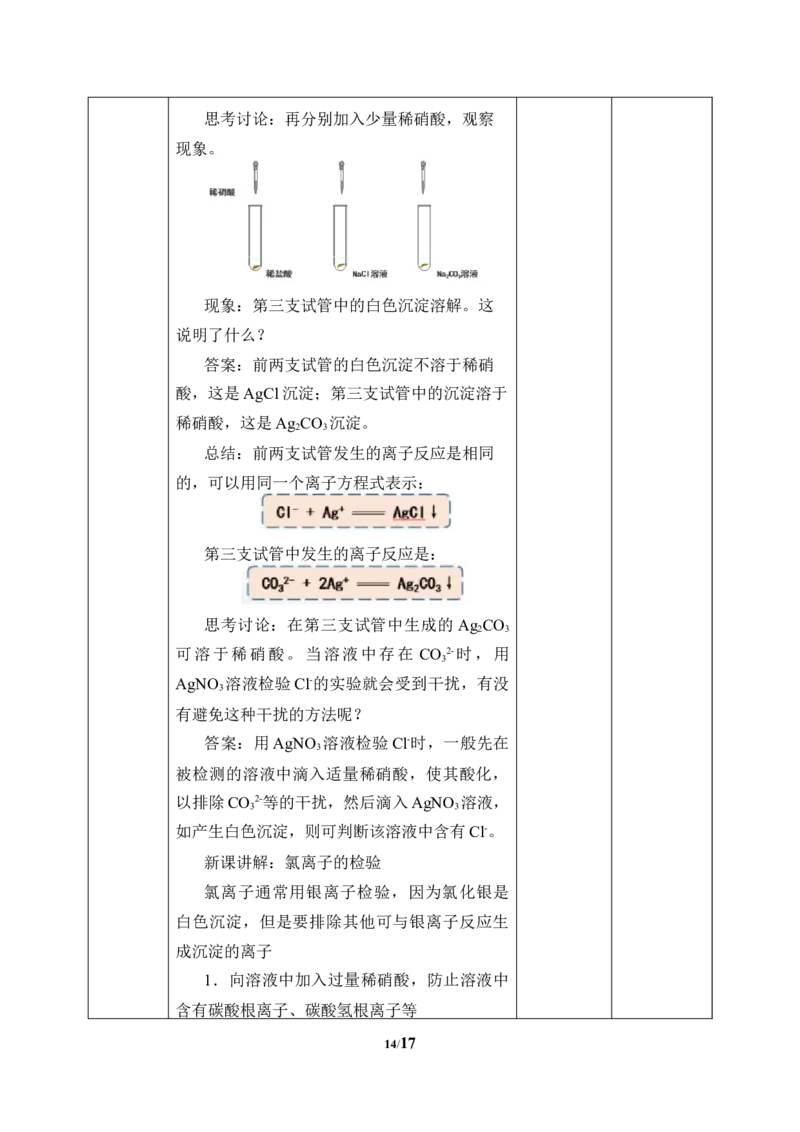
13/17思考讨论:再分别加入少量稀硝酸,观察
现象。
现象:第三支试管中的白色沉淀溶解。这
说明了什么?
答案:前两支试管的白色沉淀不溶于稀硝
酸,这是AgCl沉淀;第三支试管中的沉淀溶于
稀硝酸,这是Ag CO 沉淀。
2 3
总结:前两支试管发生的离子反应是相同
的,可以用同一个离子方程式表示:
第三支试管中发生的离子反应是:
思考讨论:在第三支试管中生成的 Ag CO
2 3
可溶于稀硝酸。当溶液中存在 CO 2-时,用
3
AgNO 溶液检验Cl-的实验就会受到干扰,有没
3
有避免这种干扰的方法呢?
答案:用AgNO 溶液检验Cl-时,一般先在
3
被检测的溶液中滴入适量稀硝酸,使其酸化,
以排除CO 2-等的干扰,然后滴入AgNO 溶液,
3 3
如产生白色沉淀,则可判断该溶液中含有Cl-。
新课讲解:氯离子的检验
氯离子通常用银离子检验,因为氯化银是
白色沉淀,但是要排除其他可与银离子反应生
成沉淀的离子
1.向溶液中加入过量稀硝酸,防止溶液中
含有碳酸根离子、碳酸氢根离子等
14/172.向1中的溶液加入少量硝酸银溶液,若
有白色沉淀生成,则证明原溶液中有氯离子
课堂达标:
1.下列生活中的物质与其有效成分的化学
式、用途的对应关系中不正确的是( )
解析:食盐中有效成分是氯化钠,化学式
为NaCl,可做调味品,A正确;小苏打中有效
成分是NaHCO ,可做发酵粉,B错误;复方氢
3
氧化铝片中有效成分是 Al(OH) ,可做抗酸
3
药,C正确;漂白粉中有效成分是 Ca(ClO)
,可做消毒剂,D正确。因此选B。
2
2.下列关于制取气体的装置描述中正确的
是( )
A.依据反应物的状态和反应条件,选择除
杂装置
B.依据气体及其所含杂志的性质,选择气
体的发生装置
C.依据气体的性质,选择尾气处理装置
D.装置的连接顺序一般为:发生装置→收
集装置→除杂装置→尾气处理装置
解析:依据反应物的状态和反应条件,选
择气体的发生装置,A错误;依据气体及其所
含杂志的性质,选择除杂装置,B错误;依据
气体的性质,选择尾气处理装置,C正确;装
置的连接顺序一般为:发生装置→除杂装置→
收集装置→尾气处理装置,D 错误。因此选
C。
3.下列反应式书写正确的是( )
A.实验室制氯气:MnO +4HCl(稀)——
2
15/17MnCl +Cl +2H O
2 2 2
B.制取漂白粉有效成分:
Cl +2Ca ( OH ) — — Ca ( ClO )
2 2
+CaCl +H2O
2 2
C.制取漂白液有效成分:Cl +2NaOH——
2
NaCl+NaClO+H O
2
D.碳酸银和氯化钠的离子反应式:Cl-
+Ag+——AgCl
解析:实验室制氯气通常用二氧化锰和浓
盐 酸 , 反 应 式 为 MnO +4HCl ( 浓 ) — —
2
MnCl +Cl +2H O;A错误;漂白粉的有效成分
2 2 2
是Ca(ClO) ,通过将氯气通入石灰乳得到,
2
反应式为:2Cl +2Ca(OH) ——Ca(ClO)
2 2
+CaCl +2H O,B 错误;C 正确;碳酸银和氯
2 2 2
化钠反应会生成氯化银沉淀,因此需要打沉淀
符号,即:Cl-+Ag+——AgCl↓,D 错误。因
此选C。
4.下列有关氯气及其化合物的说法不正确
的是( )
A.氯气能与大多数金属化合,其一般将变
价金属氧化至最高价
B.干燥的氯气能使鲜花褪色
C.除去氯气中少量氯化氢可使气体通过饱
和食盐水
D.因为氯气有毒,所以可用于杀菌、消
毒、漂白
解析:氯气是强氧化剂,与变价金属氧化
为高价化合物,A正确;根据氯气无漂白性,
遇到水生成次氯酸,次氯酸具有漂白性,B正
确;氯气不溶于饱和食盐水,而氯化氢能溶于
饱和食盐水,C正确;氯气的杀菌,消毒,漂
16/17白作用是由于遇水生成了次氯酸,D错误。因
此选D。
课堂小结 氯气的物理性质:黄绿色气体,气味大, 学生和 通 过 对
有毒 老师一起快 课堂学习知
易溶于水,熔点:-101℃,沸点:-34.6℃ 速回顾本次 识的总结,
氯的化学性质: 课的学习内 帮助同学们
能与金属反应:与金属钠加热生成 NaCl, 容。 加深印象。
与金属铁加热生成 FeCl ,与金属铜加热生成
3
CuCl ;
2
能与非金属反应:与氢气加热生成HCl;
能与水反应:与水反应生成次氯酸。
能与碱的反应:生成次氯酸钙、次氯酸
钠,用于制作漂粉精、漂白液、漂白粉。
氯气的实验室制法:MnO +4HCl(浓)
2
——MnCl +Cl +2H O
2 2 2
氯离子的检验:对于可溶性氯化物中的氯
离子,可以用AgNO 溶液和稀硝酸进行检验。
3
板书 学生在 方 便 学
笔记本上对 生 课 后 回
板书进行誊 顾。
写。
17/17