文档内容
氧化还原反应
【第一课时】
知识与技能 1.学会用化合价的变化和电子转移的观点判断氧
化还原反应;
教 2.初步掌握根据化合价的变化和电子转移的观点
分析氧化还原反应的方法;
学 3.理解氧化还原反应的本质就是发生了电子转
移。
目
过程与方法 1.复习巩固初中四种基本反应类型以及从得氧、
失氧角度划分氧化反应和还原反应,进一步了解化学
标
反应的多种分类方法,并由此得出划分的依据不同而
有不同的使用范围的。
2.培养学生思考及分析,解决问题的能力。
情感态度与 1.理解氧化跟还原的相互依存和对立统一的辩证
价值观 关系。
重点 用化合价升降和电子转移的观点理解氧化还原反应;
难点 理解氧化还原反应的本质就是发生了电子转移。
知 氧化还原反应
识 一、氧化还原反应
结 1.氧化反应( oxidation reaction):元素化合价升高的
构 反应
与 还原反应( reduction reaction):元素化合价降低的
板 反应
书 氧化还原反应:凡有元素化合价升降的化学反应就是
设 2.氧化还原反应的判断依据-----有元素化合价变化
计 失电子总数=化合价升高总数==得电子总数==化合价降低
总数。
3.氧化还原反应的实质------电子的转移(电子的得失或
共用电子对的偏移
口诀:化合价升高,失电子,被氧化;
化合价降低,得电子,被还原
教学过程 教学方法、
手段、师生活动
[复习]化学反应可以从不同的角度进行分类,其目的在于 通过回忆旧知识发
了解各类反应的本质。回忆一下,我们初中学过哪些基本反应类 现问题,引起学生思
型?并举例说明。 考,将学生的注意力
[小结] 引入课堂。并遵循由
四种基本类型的反应 旧入新、由浅入深的
反应 课堂教学规律。
举例 表示式
类型
化合
C+O ==(点燃)==CO A+B==AB
反应 2 2
分解 CaCO ==(高温)==CaO+CO ↑ AB==A+B
3 2
1 / 8反应 学生板书方程式 1.
置换 C + 2CuO== ( 高 温 ) ==2Cu + A+BC==AC+Cu+O ==2CuO 化合反
2
反应 CO ↑ B 应
2
复 分 解 CaCO +2HCl====CaCl +H O+CO AB + CD==AD 2.CuO+H 2 ==H 2 O+Cu
3 2 2 2
置换反应
反应 ↑ +CB
3 .
[引]初中阶段我们学习过许多化学反应,根据反应物和生
Fe+CuSO =FeSO +Cu
成物的类别以及反应前后物质的种类的多少可以把他们分为四个 4 4
置换反应
基本反应类型,但是有一些反应,比如 Fe O + 3CO ==2Fe
2 3
4 .
+3CO ,经过分析,它不属于四个基本反应类型的任何一个,说
2
NaCl+AgNO ==AgCl
明上述分类方法不能包括所有反应,所以我们需要制定一个新的 3
↓+NaNO 复分解反应
分类方法,这节课我们就来共同探讨解决一下这个问题 3
[板书]第三节 氧化还原反应 5 . CaCO 3 ==CaO
[过]化学学习和日常生活中,我们认识了许多化学反应, +CO ↑分解反应
2
现在请你写出屏幕上几个反应的化学方程式,并讨论并交流这类
化学反应的分类标准。
写出下列化学反应
1.铜和氧气的反应
2.氧化铜与氢气的反应
3.铁与硫酸铜溶液的反应
4.氯化钠溶液与硝酸银溶液的反应
5.碳酸钙的分解反应
[问]反应2Cu +O ==2CuO 除属化合反应外还属于什么反
2
应类型?
(氧化反应)
[问]什么叫氧化反应?
(物质跟氧发生的化学反应称为氧化反应)
[问]请判断下列反应中H 发生了什么反应?
2
CuO+H ==H O+Cu
2 2
(H 夺取了CuO中的氧并与氧结合生成了H O,发生
2 2
了氧化反应)
[问]那么CuO发生了什么反应?
(CuO失去了氧,发生的是还原反应)
[讲]在这个反应中,氧化铜失去氧变成单质铜,发生了还
原反应;碳得到了氧变成了二氧化碳,发生了氧化反应。也就是
说,氧化反应和还原反应是同时发生的,这样的反应称为氧化还
原反应。
[思考与交流]请分析下列 3个氧化还原反应中各种元素的
化合价在反应前后有无变化,讨论氧化还原反应与元素化合价的
升降有什么关系。
1.2CuO+C===2Cu+CO ↑
2
2.H O+C==H +CO
2 2
3.CuO+H ===Cu+H O
2 2
(在反应1中,铜元素化合价降低,碳元素化合价升高;在 通过及时到位的练
反应2中,氢元素化合价降低,碳元素化合价升高;在反应3中 习更好的巩固氧化还
铜元素化合价降低,氢元素化合价升高,) 原反应的判断依据和
[讲]由此可知,有元素化合价升高的反应是氧化反应,有 应用。
元素化合价降低的反应是还原反应,氧化与还原这两个对立的过
程相互依存而统一于一个氧化还原反应之中,同时发生而且不可
2 / 8以分离。总的来说,在化学反应中,物质的某些元素的化合价在
反应前后发生了变化就是氧化还原反应。
[板书]一、氧化还原反应
1.氧化反应( oxidation reaction):元素化合价升高的反
应
还原反应( reduction reaction):元素化合价降低的反
应
氧化还原反应:凡有元素化合价升降的化学反应就是氧
化还原反应。
2.氧化还原反应的判断依据-----有元素化合价变化
[过]为什么氧化还原反应前后元素的化合价发生变化?其
本质原因是什么呢?
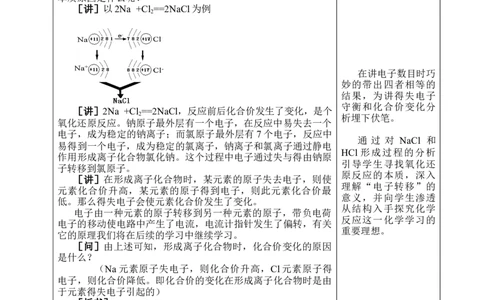
[讲]以2Na +Cl ==2NaCl为例
2
在讲电子数目时巧
妙的带出四者相等的
结果,为讲得失电子
守衡和化合价变化分
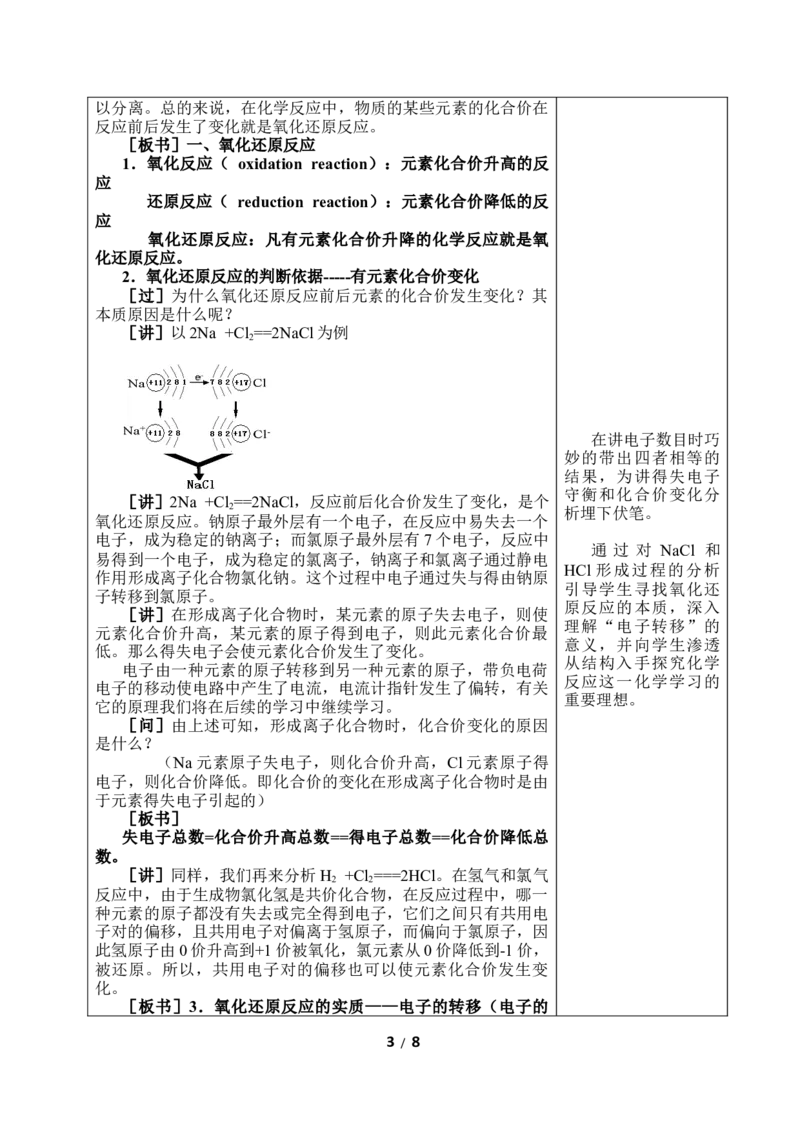
[讲]2Na +Cl ==2NaCl,反应前后化合价发生了变化,是个
2 析埋下伏笔。
氧化还原反应。钠原子最外层有一个电子,在反应中易失去一个
电子,成为稳定的钠离子;而氯原子最外层有7个电子,反应中
通 过 对 NaCl 和
易得到一个电子,成为稳定的氯离子,钠离子和氯离子通过静电
HCl 形成过程的分析
作用形成离子化合物氯化钠。这个过程中电子通过失与得由钠原
引导学生寻找氧化还
子转移到氯原子。
原反应的本质,深入
[讲]在形成离子化合物时,某元素的原子失去电子,则使
理解“电子转移”的
元素化合价升高,某元素的原子得到电子,则此元素化合价最
意义,并向学生渗透
低。那么得失电子会使元素化合价发生了变化。
从结构入手探究化学
电子由一种元素的原子转移到另一种元素的原子,带负电荷
反应这一化学学习的
电子的移动使电路中产生了电流,电流计指针发生了偏转,有关
重要理想。
它的原理我们将在后续的学习中继续学习。
[问]由上述可知,形成离子化合物时,化合价变化的原因
是什么?
(Na元素原子失电子,则化合价升高,Cl元素原子得
电子,则化合价降低。即化合价的变化在形成离子化合物时是由
于元素得失电子引起的)
[板书]
失电子总数=化合价升高总数==得电子总数==化合价降低总
数。
[讲]同样,我们再来分析H +Cl ===2HCl。在氢气和氯气
2 2
反应中,由于生成物氯化氢是共价化合物,在反应过程中,哪一
种元素的原子都没有失去或完全得到电子,它们之间只有共用电
子对的偏移,且共用电子对偏离于氢原子,而偏向于氯原子,因
此氢原子由0价升高到+1价被氧化,氯元素从0价降低到-1价,
被还原。所以,共用电子对的偏移也可以使元素化合价发生变
化。
[板书]3.氧化还原反应的实质——电子的转移(电子的
3 / 8得失或共用电子对的偏移
[总结]让学生总结本节课所学主要内容。
得氧失氧 化合价升降 电子转移观
观点 观点 点
氧化 得到氧的 化合价升高 失去电子的
反应 反应 的反应 反应
还原 失去氧的 化合价降低 得到电子的
反应 反应 的反应 反应
氧化 得氧失氧 化合价升降 得失电子同
还 原 的 同时发生 同时发生(且升 时发生(且得
关系 降总数相等) 失电子总数相
等)
氧化 有氧得失 有化合价升 有电子转移
还 原 反 的反应 降的反应 的反应
应
[板书]口诀:化合价升高,失电子,被氧化;
化合价降低,得电子,被还原
教学回顾:
氧化还原反应
【第二课时】
知识与 1.掌握四种基本反应类型和氧化还原反应间的关系,理解氧化剂和
技能 还原剂的概念;
教 2.了解氧化还原反应在日常生活、生产中的应用。
过程与 1.通过氧化还原反应概念的教学,培养学生准确描述概念、深刻理
学 方法 解概念、比较辨析概念的能力;
2.通过对氧化还原反应概念认识的过程,体会科学探究的基本方
目
法,提高科学探究能力。
情感 1.通过氧化还原反应概念的演变,培养学生用发展的观点、科学的
标
态度 态度、探索的精神学习化学;
价值观 2.通过创设问题情景,引导学生积极思维,激发学生学习化学的兴
趣和求知欲望。
重 点 氧化还原反应的本质
难 点 氧化还原反应的概念的应用
4 / 84.氧化还原反应与四种基本反应类型的关系
二、氧化剂和还原剂
1.氧化剂和还原剂(反应物)
氧化剂:得电子(或电子对偏向)的物质——氧化性
知 还原剂:失电子(或电子对偏离)的物质——还原性
识 氧化产物:氧化后的生成物
结 还原产物:还原后的生成物。
构
与
板 氧化剂 + 还原剂 == 还原产物 + 氧化产物
书
设
计
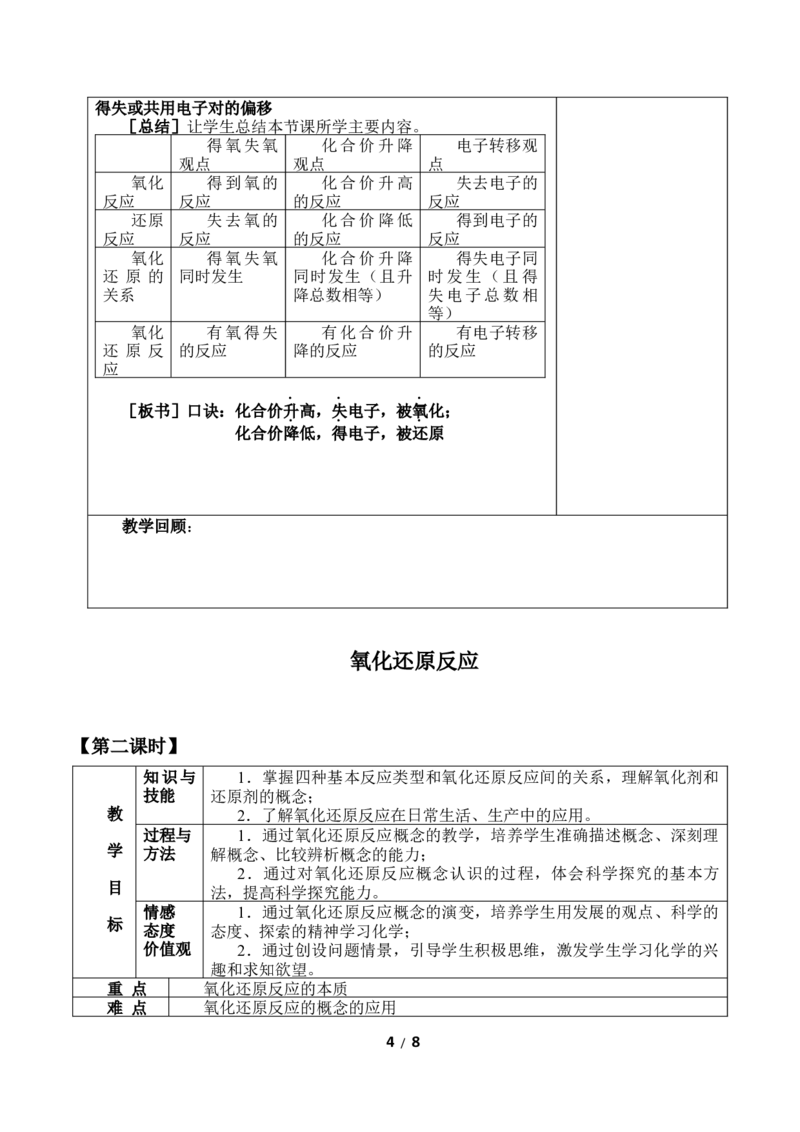
2.氧化还原反应中电子转移的
表示方法
(1)双线桥法---表示电子得失
结果
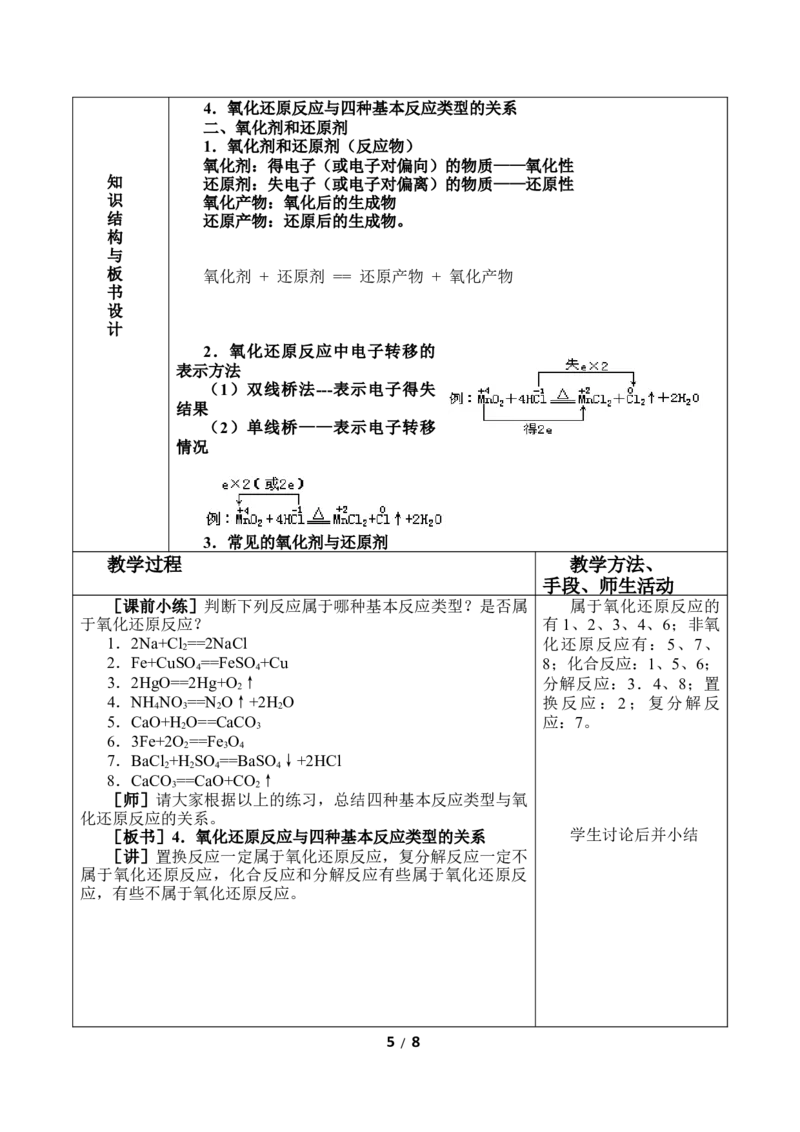
(2)单线桥——表示电子转移
情况
3.常见的氧化剂与还原剂
教学过程 教学方法、
手段、师生活动
[课前小练]判断下列反应属于哪种基本反应类型?是否属 属于氧化还原反应的
于氧化还原反应? 有1、2、3、4、6;非氧
1.2Na+Cl ==2NaCl 化还原反应有:5、7、
2
2.Fe+CuSO ==FeSO +Cu 8;化合反应:1、5、6;
4 4
3.2HgO==2Hg+O ↑ 分解反应:3.4、8;置
2
4.NH NO ==N O↑+2H O 换反应:2;复分解反
4 3 2 2
5.CaO+H O==CaCO 应:7。
2 3
6.3Fe+2O ==Fe O
2 3 4
7.BaCl +H SO ==BaSO ↓+2HCl
2 2 4 4
8.CaCO ==CaO+CO ↑
3 2
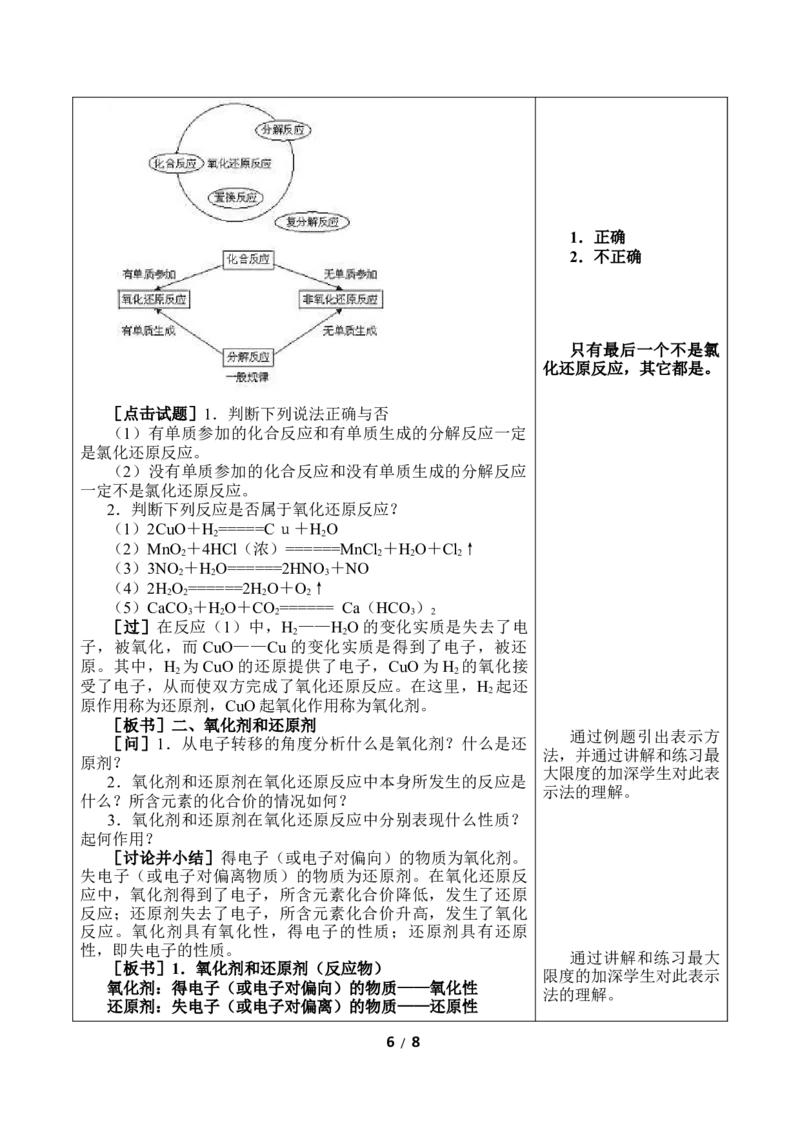
[师]请大家根据以上的练习,总结四种基本反应类型与氧
化还原反应的关系。
[板书]4.氧化还原反应与四种基本反应类型的关系 学生讨论后并小结
[讲]置换反应一定属于氧化还原反应,复分解反应一定不
属于氧化还原反应,化合反应和分解反应有些属于氧化还原反
应,有些不属于氧化还原反应。
5 / 81.正确
2.不正确
只有最后一个不是氯
化还原反应,其它都是。
[点击试题]1.判断下列说法正确与否
(1)有单质参加的化合反应和有单质生成的分解反应一定
是氯化还原反应。
(2)没有单质参加的化合反应和没有单质生成的分解反应
一定不是氯化还原反应。
2.判断下列反应是否属于氧化还原反应?
(1)2CuO+H =====Cu+H O
2 2
(2)MnO +4HCl(浓)======MnCl +H O+Cl ↑
2 2 2 2
(3)3NO +H O======2HNO +NO
2 2 3
(4)2H O ======2H O+O ↑
2 2 2 2
(5)CaCO +H O+CO ====== Ca(HCO )
3 2 2 3 2
[过]在反应(1)中,H ——H O的变化实质是失去了电
2 2
子,被氧化,而 CuO——Cu 的变化实质是得到了电子,被还
原。其中,H 为CuO的还原提供了电子,CuO为H 的氧化接
2 2
受了电子,从而使双方完成了氧化还原反应。在这里,H 起还
2
原作用称为还原剂,CuO起氧化作用称为氧化剂。
[板书]二、氧化剂和还原剂
通过例题引出表示方
[问]1.从电子转移的角度分析什么是氧化剂?什么是还
法,并通过讲解和练习最
原剂?
大限度的加深学生对此表
2.氧化剂和还原剂在氧化还原反应中本身所发生的反应是
示法的理解。
什么?所含元素的化合价的情况如何?
3.氧化剂和还原剂在氧化还原反应中分别表现什么性质?
起何作用?
[讨论并小结]得电子(或电子对偏向)的物质为氧化剂。
失电子(或电子对偏离物质)的物质为还原剂。在氧化还原反
应中,氧化剂得到了电子,所含元素化合价降低,发生了还原
反应;还原剂失去了电子,所含元素化合价升高,发生了氧化
反应。氧化剂具有氧化性,得电子的性质;还原剂具有还原
性,即失电子的性质。
通过讲解和练习最大
[板书]1.氧化剂和还原剂(反应物)
限度的加深学生对此表示
氧化剂:得电子(或电子对偏向)的物质——氧化性
法的理解。
还原剂:失电子(或电子对偏离)的物质——还原性
6 / 8[讲]在氧化还原反应中,氧化剂得电子具有氧化性,起氧
化作用,本身被还原后的生成物叫还原产物。还原剂失电子具
有还原性,起还原作用,本身被氧化,氧化后的生成物叫氧化
产物。
[板书]氧化产物:氧化后的生成物。
还原产物:还原后的生成物。
[总结]氧化还原反应中各概念间的关系为
[板书]
氧化剂+还原剂==还原产物+氧化产物
[过]氧化还原反应的实质是电子的转移,下面我们学习如
何在方程式上简单地表示反应中电子的转移情况。
[板书]2.氧化还原反应中电子转移的表示方法
(1) 双线桥法---表示电子得失结果
[小结]步骤:
1.先标化合价,双线桥从左指向右连接不同价态的同种元
素。
2.线上标明电子得失数。
[点击试题]用双线桥表示下列氧化还原反应,并指出氧化
剂和还原剂。
(1)3H +Fe O ==3H O+2Fe
2 2 3 2
(2)2KClO ==2KCl+3O
3 2
(3)2H S+SO =3S+2H O
2 2 2
[板书](2)单线桥——表示电子转移情况
[小结]步骤:重点:
(1)单箭号(在反应物之间);
(2)箭号起点为被氧化(失电子)元素,终点为被还原
(得电子)元素;
(3)只标转移电子总数,不标得与失(氧化剂得电总数等
于还原剂失电子总数)。
[过]下面根据我们已有的经验,总结一下常见的氧化剂和
还原剂。
[板书]3.常见的氧化剂与还原剂
[小结]
7 / 81.常见的氧化剂
(1)活泼的非金属单质:O 、Cl 、Br 。
2 2 2
(2)含高价金属阳离子的化合物:FeCl 。
3
(3)含某些较高化合价元素的化合物:浓H SO 、HNO 、
2 4 3
KMnO 、MnO 。
4 2
2.常见的还原剂:
(1)活泼或较活泼的金属:K、Ca、Na、Al、Mg、Zn(按
金属活动性顺序,还原性递减)。
(2)含低价金属阳离子的化合物:Fe2+。
(3)某些非金属单质:C、H 。
2
(4)含有较低化合价元素的化合物:HCl、H S、HI、KI。
2
[结束语]氧化还原反应是和工农业生产、科学技术、日常
生活密切相关的重要反应。它对我们人类既有贡献又有害处,
比如我们酿酒、燃料燃烧都是利用氧还反应,但是铁生锈,易
燃物自然等等也同样是氧还反应。我们在学习了化学之后就可
以充分去避免氧还反应的危害,最大限度的利用它来为人类服
务。
教学回顾:
8 / 8