文档内容
元素及其化合物框图推断(上)同步练习
(答题时间:40分钟)
一、选择题
1. X、Y是中学化学中两种常见元素的单质,甲、乙是两种常见的化合物,这些单质和
化合物之间存在如图关系。下列分析不正确的是( )
A. 若甲为CO,则乙可能是金属氧化物
2
B. 若甲为Al O,则X可能是单质Fe
2 3
C. 若甲为液态水,则X可能是非金属单质
D. 若甲为氨气,则乙可能是一种盐
2. 中学常见元素组成几种物质,其转化关系如图所示:
下列推断一定错误的是( )
A. 若M为Cu S,则X可能是Cu O
2 2
B. 若M为FeCO,则X可能是Fe O
3 3 4
C. 若Y为SO ,则X可能是Al O
2 2 3
D. 若X为Fe O,则M可能是Fe C
3 4 3
3. 有A、B、C、D四瓶无色溶液,它们都是中学化学中常见的无机试剂。B、C、D是
三种阴离子各不相同的盐溶液。现进行如下实验:
①A有刺激性气味,用蘸有浓盐酸的玻璃棒接近A时产生白烟;
②将A分别加入其他三种溶液中,只有C中有沉淀产生;继续加入过量A时,C中沉
淀完全溶解;
③将B分别加入C、D中,均有白色沉淀生成,再加入稀硝酸,沉淀均不溶解。
根据上述实验信息判断下列说法错误的是( )
A. B为BaCl 溶液
2
B. C为AgNO 溶液
3
C. D不可能是Al (SO ) 溶液
2 4 3
D. A为氨水,D可能为MgSO 溶液
4
第1页二、填空题
4. A是自然界存在最广泛的ⅡA族元素,常以化合物F存在. 从单质A起始发生的一系
列化学反应可由下图表示:
请回答下列问题:
(1)A与水反应的化学方程式为________________________________,E与水反应的
化学方程式为________________________________;
(2)F 的化学式为________,G 和 D 的电子式分别为________________和
_____________;
(3)D与H反应可能生成的盐有__________________(填化学式);
(4)实际生产中,可由F为原料制备单质A,简述一种制备方法____________。
5. 已知A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,它
们之间有如下反应关系。
(1)若A是一种红色金属单质,B是一种常见的挥发性酸,反应时生成的C是无色气
体,反应的离子方程式为___________,若反应放出1. 12 L气体(标准状况下),则被还
原的B物质的量为___________mol。
(2)若实验室中利用固体A和B的反应制备气体C,C是一种无色、刺激性气味、密
度比空气小、碱性的气体,试写出此反应的化学方程式________________;实验室检验C
的方法为_______________。
(3)若B是黄绿色有毒气体,上述关系经常用于实验室尾气处理,则反应的离子方
程式为________________。若用湿润的淀粉碘化钾试纸靠近盛满B的试管口,看到的现象
为______________。
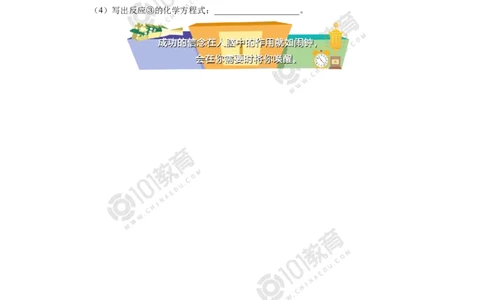
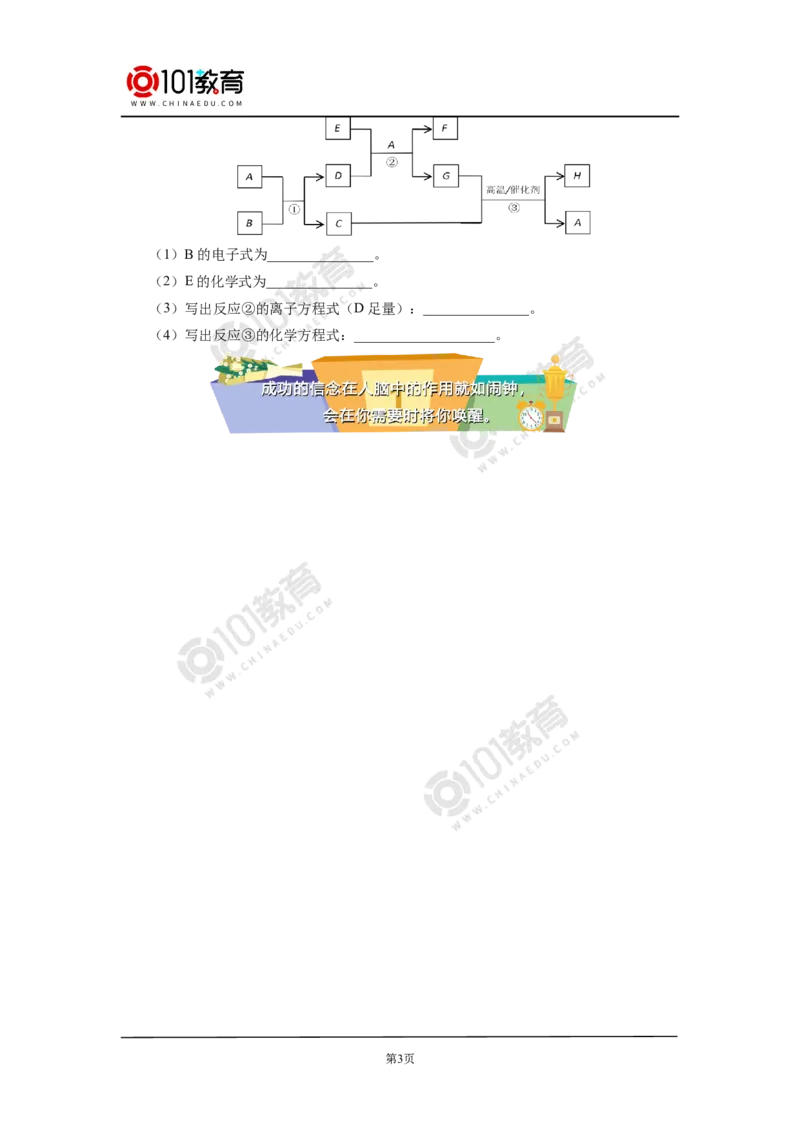
6. A为日常生活中常见的化合物,B为淡黄色固体,C、G、H均为气体,其中C、H为
单质,G能使红色石蕊试剂变蓝,E是一种由两种元素组成的具有耐高温、硬度大的耐热
冲击材料,其摩尔质量为 41 g/moL。
第2页(1)B的电子式为_______________。
(2)E的化学式为_______________。
(3)写出反应②的离子方程式(D足量):_______________。
(4)写出反应③的化学方程式:____________________。
第3页元素及其化合物框图推断(上)同步练习参考答案
1.【答案】B
【解析】若甲为CO ,则乙可能是MgO,发生的反应为2Mg+CO C+2MgO,A
2 2
项正确;若甲为Al O ,则X不可能是单质Fe,Fe不能置换Al,B项错误;若甲为液态水,
2 3
则X可能是非金属单质F ,发生的反应为2F +2HO=4HF+O ,C项正确;若甲为氨气,
2 2 2 2
则可能发生的反应为3Cl+8NH =6NH Cl+N,D项正确。
2 3 4 2
2.【答案】C
【解析】本题考查无机化合物推断,意在考查考生的推理能力。A项,若M为Cu S,
2
在空气中灼烧可能生成Cu O和SO ,Cu O与硝酸发生氧化还原反应生成NO,正确。B项,
2 2 2
若M为FeCO ,在空气中灼烧,铁元素化合价升高,X为Fe O ,Y为CO ,正确。C项,
3 3 4 2
若Y为SO ,X为Al O ,Al O 与稀硝酸不能发生氧化还原反应,不生成NO,错误。D项,
2 2 3 2 3
若M为Fe C,Fe C在空气中灼烧生成Fe O 和CO,正确。
3 3 3 4 2
3.【答案】D
【解析】本题考查简单的无机推断,意在考查考生在解决简单化学问题的过程中,运
用科学的方法,初步了解化学变化规律,并对化学现象提出科学合理解释的能力。根据实
验①可以确定A是氨水,根据实验②可以确定C是AgNO 溶液,根据实验③:将B分别加
3
入C、D中,均有白色沉淀生成,再加入稀硝酸,沉淀均不溶解,可知 B中含有氯离子和
2− 2−
钡离子,D中含有SO 或SO ,但是根据实验②可知D不可能是Al (SO ) 溶液或
4 3 2 4 3
MgSO 溶液。
4
4.【答案】(1)Ca+2HO=Ca(OH)+H↑ NaH+HO=NaOH+H↑
2 2 2 2 2
(2)CaCO
3
(3)NaCO、NaHCO
2 3 3
(4)CaCO 高温加热分解生成CaO,CaO经电解生成单质Ca
3
【解析】由题干信息可推知,A是钙,F是CaCO ,其他易推出,B是H ,C是Ca
3 2
(OH) ,E是NaH,D是CO ,G是CaO,H是NaOH,(3)小题CO 和NaOH溶液可
2 2 2
能发生反应有:CO+2NaOH=NaCO+HO,CO+HO+NaCO=2NaHCO .
2 2 3 2 2 2 2 3 3
5.【答案】(1)2NO -+ 3Cu + 8H+=2NO↑+ 4HO + 3 Cu 2+ 0.052
3 2
(2)NH Cl+ Ca(OH) CaCl +2NH↑+2H O
4 2 2 3 2
把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气
(3)Cl+2OH-=Cl-+ClO- + H O 试纸变为蓝色
2 2
【解析】A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,
考虑E为HO;
2
(1)A是一种红色单质,B是一种常见的挥发性酸,反应时生成的C是无色气体,则
第4页A为Cu,B为稀硝酸,C为NO,D为硝酸铜,反应的离子反应为2NO -+3Cu+8H+=
3
2NO↑+4H O+3Cu2+,生成硝酸铜体现硝酸的酸性,生成NO体现硝酸的氧化性;若反应放
2
出1.12 LNO气体(标准状况下),NO的物质的量为0.05mol,则被还原的HNO 物质的量
3
为0.05mol;
(2)C是一种无色、刺激性气味、密度比空气小的气体,则C为NH ,实验室利用铵
3
盐与熟石灰反应制备氨气,该反应方程式为:2NH Cl+Ca(OH)
4 2
CaCl +2NH↑+2H O,检验方法为把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该
2 3 2
气体为氨气(或用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨
气);
(3)若B是黄绿色有毒气体,应该为氯气,实验室常用NaOH溶液吸收其尾气,则
反应的离子方程式为Cl+2OH-=Cl-+ClO- + H O ;若用湿润的淀粉碘化钾试纸靠近盛满B
2 2
的试管口,氯气能氧化I-生成碘单质,则看到的现象为试纸变为蓝色。
6.【答案】 AlN AlN+OH- +H O=AlO-+NH ↑
2 2 3
4NH +3O 2N↑ +6H O
3 2 2 2
【解析】B是淡黄色固体,B与化合物A反应产生单质气体C和化合物D,则B是
NaO,C是O,G能使红色石蕊试剂变蓝,则G是NH ,NH 与O 在高温下发生反应:
2 2 2 3 3 2
4NH +3O 2N↑ +6H O,可知A是HO,H是N;D是NaOH;E是一种由两种元
3 2 2 2 2 2
素组成的具有耐高温、硬度大的耐热冲击材料,其摩尔质量为 41 g/moL,由于其中一种元
素是N元素,N相对原子质量是14,则另一种元素相对原子质量是42-14=27,则另外一
种元素是Al元素,E是AlN,NaOH、HO、AlN发生反应,产生NH 和NaAlO ;则F是
2 3 2
NaAlO
2
第5页元素及其化合物框图推断(下)同步练习
(答题时间:40分钟)
一、选择题
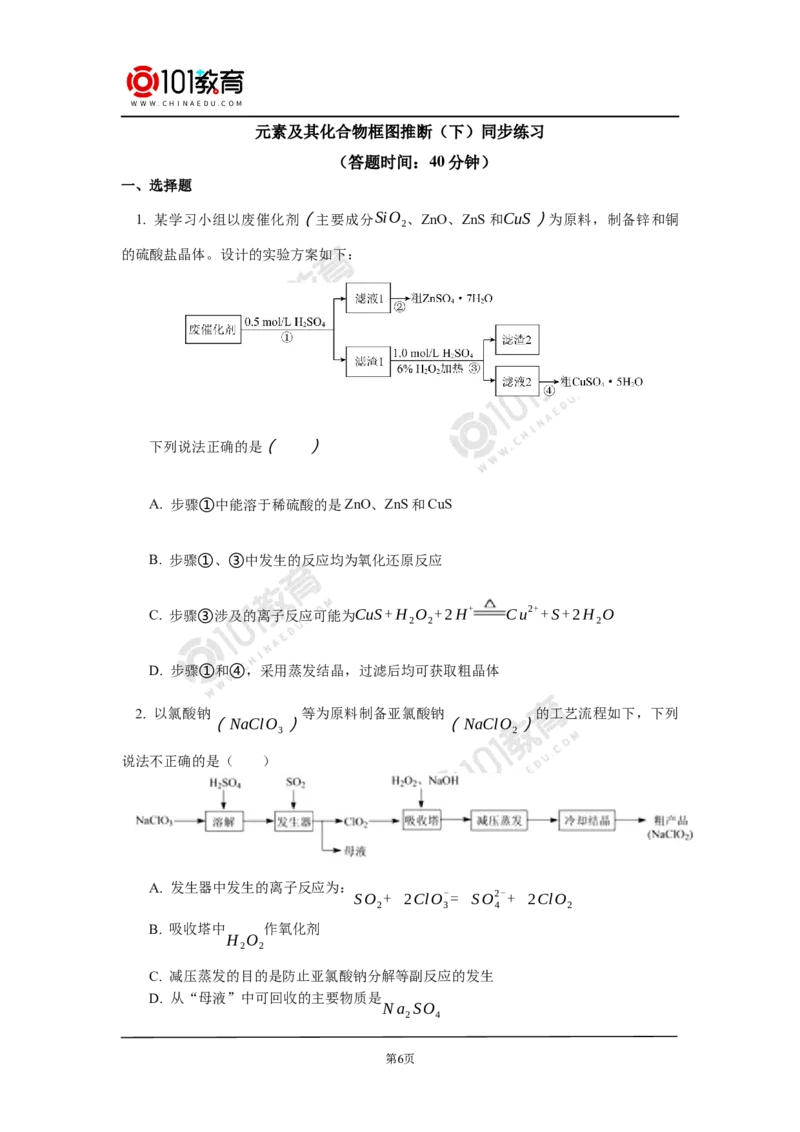
1. 某学习小组以废催化剂(主要成分SiO 、ZnO、ZnS和CuS)为原料,制备锌和铜
2
的硫酸盐晶体。设计的实验方案如下:
下列说法正确的是( )
A. 步骤①中能溶于稀硫酸的是ZnO、ZnS和CuS
B. 步骤①、③中发生的反应均为氧化还原反应
C. 步骤③涉及的离子反应可能为CuS+H O +2H+ Cu2++S+2H O
2 2 2
D. 步骤①和④,采用蒸发结晶,过滤后均可获取粗晶体
2. 以氯酸钠 等为原料制备亚氯酸钠 的工艺流程如下,下列
(NaClO ) (NaClO )
3 2
说法不正确的是( )
A. 发生器中发生的离子反应为:
SO + 2ClO-= SO2-+ 2ClO
2 3 4 2
B. 吸收塔中 作氧化剂
H O
2 2
C. 减压蒸发的目的是防止亚氯酸钠分解等副反应的发生
D. 从“母液”中可回收的主要物质是
Na SO
2 4
第6页3. 以重晶石(BaSO )为原料,可按如下工艺生产立德粉(ZnS⋅BaSO ):
4 4
下列说法不正确的是( )
A. 在回转炉中重晶石被过量焦炭还原为可溶性硫化钡,该过程的化学方程式为
高温
BaSO +4C ̲(cid:14) BaS+4CO↑
4 ̲(cid:14)
B. 回转炉尾气中含有有毒气体,生产上可通过水蒸气变换反应将其转化为 和一
CO
2
高温
种清洁能源气体,该反应的化学方程式为CO+H O ̲(cid:14) CO +H
2 ̲(cid:14) 2 2
C. 在潮湿空气中长期放置的“还原料”,会逸出臭鸡蛋气味的气体,且水溶性变差.
其原因是“还原料”表面生成了难溶于水的
BaSO
4
D. 沉 淀 器 中 发 生 的 离 子 反 应 方 程 式 为 :
S2-+Ba2++Zn2++SO2- ̲(cid:14) ZnS⋅BaSO ↓
4 ̲(cid:14) 4
4. 将燃煤排放的含有 的烟气通入海水 主要含 、 、 、 、 、
SO ( Na+ K+ Ca2+ M g2+ Cl-
2
、A. 、 、 等离子 进行脱硫的工艺流程如图所示,下列说法中正确
SO2- Br- CO2- HCO- )
4 3 3
的是
( )
A. 天然海水显酸性
B. 氧化过程中可能发生的离子反应为
2SO +2H O+O =4H++2SO2-
2 2 2 4
C. 排入大海的溶液与天然海水相比,只有 数量发生了变化
SO2-
4
第7页D. 若将氧化后的液体进行蒸发结晶,得到的晶体中 含量最高
CaSO
4
5. 锂离子电池被人们广泛使用,利用废旧锂离子电池的正极材料 主要含 回
( LiCoO )
2
收制备 的工艺流程如下:
Co O
3 4
已知:①浸出液A中含有大量的Co2+、Li+及少量Fe3+、Al3+、Cu2+等离子;
②CoC O ⋅2H O微溶于水,它的溶解度随温度的升高而逐渐增大。
2 4 2
下列叙述错误的是( )
A. 过 程 ①中 LiCoO 转 化 为 Co2+的 离 子 反 应 为 :
2
2LiCoO +H O +6H+=2Co2++2Li2++O ↑+4H O
2 2 2 2 2
B. 过程②中加入NaOH溶液调节pH的目的是将Fe3+、Al3+、Cu2+形成沉淀与Co2+、
分离
Li+
C. 过程 中用 代替 溶液,析出 ,效果
③ H C O (N H )C O CoC O ⋅2H O
2 2 4 4 2 2 4 2 4 2
更佳
D. 过程 中反应的化学方程式为:
④
6. 由 硫 铁 矿 烧 渣 (主 要 成 分 : Fe O 、 Fe O 和 FeO)得 到 绿 矾
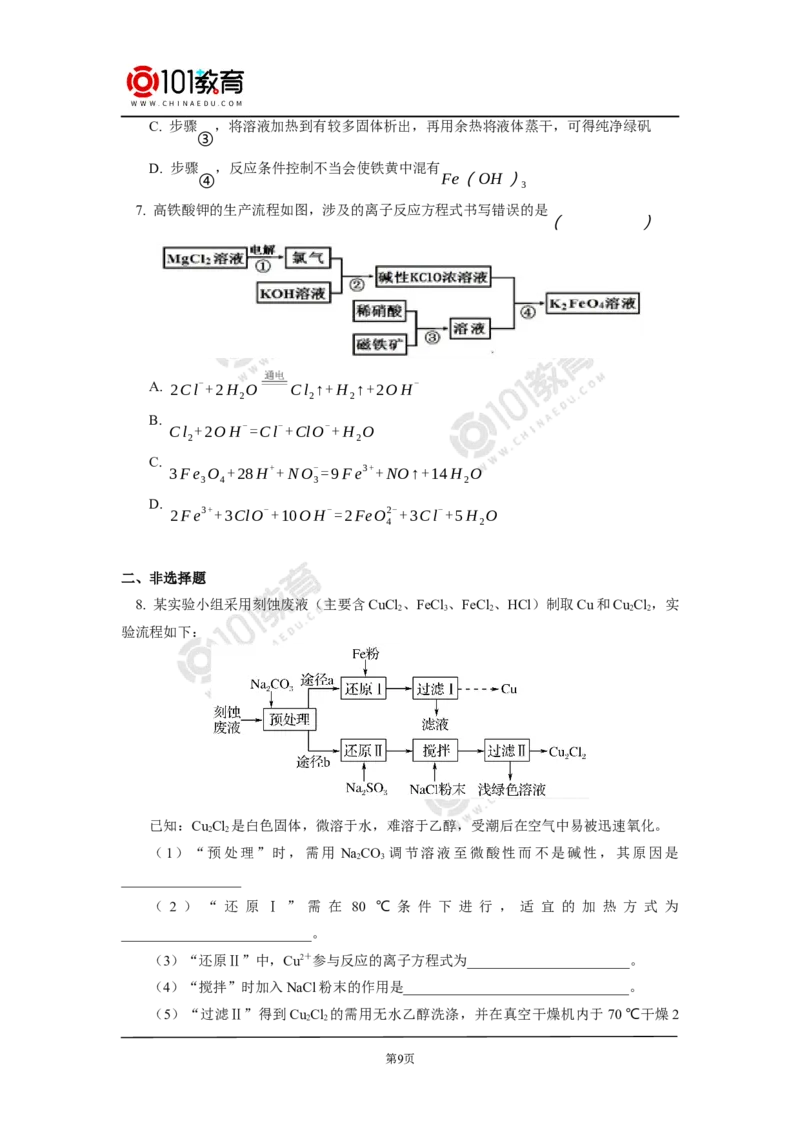
3 4 2 3
(FeSO ⋅7H O),再通过绿矾制备铁黄[FeO(OH)]的流程如下:烧渣
4 2
⃯(cid:2)
溶液 绿矾 铁黄
③
已知:FeS 和铁黄均难溶于水下列说法不正确的是
2
A. 步骤 ,最好用硫酸来溶解烧渣
①
B. 步骤 ,涉及的离子反应为
② FeS +14Fe3++8H O=15Fe2++2SO2-+16H+
2 2 4
第8页C. 步骤 ,将溶液加热到有较多固体析出,再用余热将液体蒸干,可得纯净绿矾
③
D. 步骤 ,反应条件控制不当会使铁黄中混有
④ Fe(OH)
3
7. 高铁酸钾的生产流程如图,涉及的离子反应方程式书写错误的是
( )
A. 2Cl-+2H O Cl ↑+H ↑+2OH-
2 2 2
B.
Cl +2OH-=Cl-+ClO-+H O
2 2
C.
3Fe O +28H++NO-=9Fe3++NO↑+14H O
3 4 3 2
D.
2Fe3++3ClO-+10OH-=2FeO2-+3Cl-+5H O
4 2
二、非选择题
8. 某实验小组采用刻蚀废液(主要含CuCl 、FeCl 、FeCl 、HCl)制取Cu和Cu Cl ,实
2 3 2 2 2
验流程如下:
已知:Cu Cl 是白色固体,微溶于水,难溶于乙醇,受潮后在空气中易被迅速氧化。
2 2
(1)“预处理”时,需用 NaCO 调节溶液至微酸性而不是碱性,其原因是
2 3
_________________
( 2 ) “ 还 原 Ⅰ ” 需 在 80 ℃ 条 件 下 进 行 , 适 宜 的 加 热 方 式 为
___________________________。
(3)“还原Ⅱ”中,Cu2+参与反应的离子方程式为_______________________。
(4)“搅拌”时加入NaCl粉末的作用是________________________________。
(5)“过滤Ⅱ”得到Cu Cl 的需用无水乙醇洗涤,并在真空干燥机内于70 ℃干燥2
2 2
第9页小时,冷却,密封包装。于70 ℃真空干燥的目的是___________________________。
(6)①请设计从“过滤Ⅰ”所得滤渣中获取Cu的实验方案:
_____________________________________________________________________
(实验中可供选择的试剂:稀硫酸、稀硝酸、蒸馏水)。
② 现 欲 测 定 途 径 a 、 b 回 收 铜 元 素 的 回 收 率 比 , 请 补 充 实 验 方 案 :
_____________________________________________________________________,分别按途
径a、b制取Cu和Cu Cl ,测得Cu的质量为m g,Cu Cl 的质量为m g,则途径a、b铜
2 2 1 2 2 2
素的回收率比为________(铜元素回收率=产品中铜元素质量/废液中铜元素的质量
×100%)。
第10页元素及其化合物框图推断(下)同步练习参考答案
1. 【答案】C
【解析】A.ZnO、ZnS可与硫酸反应,CuS不溶于硫酸,故A错误;
B. ①中发生ZnO+H SO =ZnSO +H O、ZnS+H SO =ZnSO +H S↑,不是
2 4 4 2 2 4 4 2
氧化还原反应,故B错误; C.③中发生CuS+H O +H SO CuSO +S+2H O,
2 2 2 4 4 2
离子反应为CuS+H O +2H+ Cu2++S+2H O,故C正确; D.步骤④为结晶得到含
2 2 2
结晶水的晶体,应采用蒸发浓缩、冷却结晶法获得晶体,故D错误。故选C。
2. 【答案】B
【解析】A.NaClO 在酸性条件下与二氧化硫发生氧化还原反应生成ClO ,方程式为
3 2
2NaClO +SO =2ClO +Na SO , 离 子 反 应 为 :
3 2 2 2 4
SO + 2ClO-= SO2-+ 2ClO 故 A 正确; B.吸收塔中发生的反应方程式为:
2 3 4 2
H O +2ClO +2NaOH=2NaClO +2H O+O ,从化合价分析,H O 做还原剂,故
2 2 2 2 2 2 2 2
B错误;C.减压蒸发在较低温度下可进行,防止常压蒸发温度过高,亚氯酸钠容易分解,
故C正确;D.根据元素守恒,母液中含有Na SO ,故D正确。故选B。
2 4
3. 【答案】C
【解析】A. 根据题目信息可知重晶石与焦炭发生氧化还原反应,产生硫化钡和 CO,
高温
对应的化学方程式为:BaSO + 4C ̲(cid:14) BaS + 4CO↑,故A不选; B.由于回转炉
4 ̲(cid:14)
产生了CO气体,利用水蒸气与其反应可以得到二氧化碳和氢气,对应的化学方程式为:
高温
CO+H O ̲(cid:14) CO +H ,故B不选;C.在潮湿空气中长期放置的“还原料”,
2 ̲(cid:14) 2 2
会逸出臭鸡蛋气味的气体,且水溶性变差.其原因是“还原料”表面生成了难溶于水的碳
酸钡和硫化氢气体,故C选; D.沉淀器中硫化钡与硫酸锌反应产生硫酸钡沉淀和硫化锌,
对应的离子反应方程式为:S2-+Ba2++Zn2++SO2- ̲(cid:14) ZnS⋅BaSO ↓,故D不选。
4 ̲(cid:14) 4
4.【答案】B
【解析】A.
天然海水中有CO2- 、HCO-
,它们水解使海水呈弱碱性,故A错误;B.
3 3
氧化过程中可能发生的离子反应为:2SO +2H O+O =4H++2SO2- ,故B正确;C.
2 2 2 4
第11页由于氧化过程中生成了硫酸,排入大海的溶液与天然海水相比,除了SO2-
数量发生了变化,
4
碳酸根、碳酸氢根离子数量也发生变化,故C错误;D. 海水中氯化钠含量最高,若将氧化
后的液体进行蒸发结晶,得到的晶体中氯化钠含量最高,故D错误。故选B。
5. 【答案】C
【解析】A. 酸性溶液中,在过氧化氢的还原作用下LiCoO 转化为Co2+,离子反应的
2
方程式为:2LiCoO +H O +6H+=2Co2++2Li++O ↑+4H O,故A正确;B. 加碱
2 2 2 2 2
调节pH的目的是将Fe3+ 、Al3+ 、Cu2+ 金属离子几乎被完全沉淀而Co2+
离子损失率较小,
便于分离,故B正确;C. 溶液中存在硫酸根,H C O 代替(N H )C O 时若发生复
2 2 4 4 2 2 4
分解反应会产生硫酸,而不能得到CoC O ·2H O,故 C错误;D. 过程④中,在空气
2 4 2
中加热CoC O ·2H O转化为Co O 的反应为晶体被空气中氧气氧化得到Co O ,反应
2 4 2 3 4 3 4
Δ
的化学方程式为:3CoC O ·2H O+2O =Co O +6CO +6H O,故D正确。故选
2 4 2 2 3 4 2 2
C。
6. 【答案】C
【解析】A.因绿矾的酸根离子为硫酸根离子,则步骤①,最好用硫酸来溶解烧渣,故
A
正确;B.步骤②发生FeS +7Fe (SO )+8H O=15FeSO +8H SO ,离子
2 2 4 3 2 4 2 4
反应为FeS +14Fe3++8H O=15Fe2++2SO2-+16H+ ,故B正确; C.步骤③为蒸发
2 2 4
浓缩、冷却结晶析出绿矾,若蒸干时绿矾受热失去结晶水,故 C错误; D.步骤④,反应
条件控制不当,绿矾与氨水、空气可发生氧化还原反应生成Fe(OH),故D正确。故
3
选C。
7. 【答案】A
【解析】A.氯化镁溶液电解:MgCl +2H O Cl ↑+H ↑+Mg (OH)↓,
2 2 2 2 2
离 子 反 应 方 程 式 : M g2+ +2Cl-+2H O Cl ↑+H ↑+Mg (OH)↓,
2 2 2 2
是难溶物,不可拆,故 A 错误; B.氯气和氢氧化钾溶液反应:
Mg (OH)
2
第12页,离子反应方程式: ,
Cl +2KOH=KCl+KClO+H O Cl +2OH-=Cl-+ClO-+H O
2 2 2 2
故 B 正 确 ; C. 磁 铁 矿 和 稀 硝 酸 反 应 : 稀
3Fe O +28HNO (
3 4 3
, 离 子 反 应 方 程 式 :
)=9Fe(NO )+NO↑+14H O
3 3 2
,故 C 正确; D.碱性 KClO 溶液与
3Fe O +28H++NO-=9Fe3++NO↑+14H O
3 4 3 2
溶 液 反 应 :
Fe(NO )
3 3
,离子反
3KClO+2Fe(NO )+10KOH=2K FeO +3KCl+5H O+ 6KNO
3 3 2 4 2 3
应方程式: ,故D正确。故选A。
2Fe3++3ClO-+10OH-=2FeO2-+3Cl-+5H O
4 2
二、非选择题
8. 【答案】(1) 防止Cu2+形成沉淀 (2)水浴加热 (3)2Cu2++SO+2Cl-+
HO===Cu Cl↓+SO+2H+
2 2 2
(4)Cu Cl 微溶于水,增大Cl-浓度,有利于Cu Cl 析出(沉淀)
2 2 2 2
(5)加快乙醇和水的挥发,防止Cu Cl 被空气氧化
2 2
(6)① 将稀硫酸加到滤渣中,搅拌,充分反应至无气体产生为止,过滤并用蒸馏水
洗涤2~3次,低温烘干 ②取两份相同体积的预处理后的水样
【解析】(1)若溶液呈碱性,则生成Cu(OH) 沉淀。(3)利用SO还原Cu2+,生
2
成Cu Cl 沉淀。(4)加入NaCl,增大c(Cl-),由题给信息“Cu Cl 微溶于水”,有利
2 2 2 2
于Cu Cl 析出。(5)由题给信息“Cu Cl 受潮后在空气中易被迅速氧化”,70 ℃真空干燥
2 2 2 2
有利于加快乙醇和水的挥发,防止Cu Cl 被空气氧化。
2 2
第13页