文档内容
专题(一)物质的量
重难点 题型 分值
重点 1. 以物质的量为中心的有关计算 选择和填空 10-12分
2. 物质的量浓度及计算。
难点 以物质的量为中心的有关计算
核心知识点一:
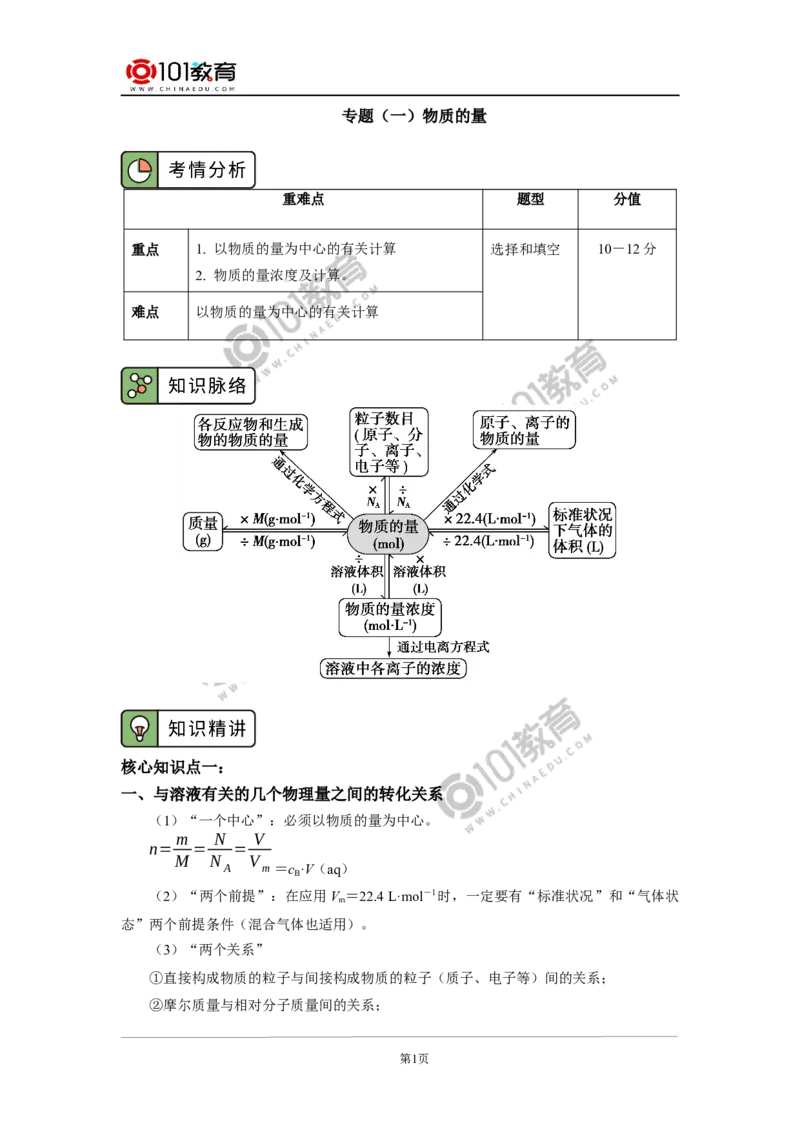
一、与溶液有关的几个物理量之间的转化关系
(1)“一个中心”:必须以物质的量为中心。
m N V
n= = =
M N V
A m=c ·V(aq)
B
(2)“两个前提”:在应用V =22.4 L·mol-1时,一定要有“标准状况”和“气体状
m
态”两个前提条件(混合气体也适用)。
(3)“两个关系”
①直接构成物质的粒子与间接构成物质的粒子(质子、电子等)间的关系;
②摩尔质量与相对分子质量间的关系;
第1页二、阿伏加德罗定律及其推论
(1)阿伏加德罗定律:同温同压下,相同体积的任何气体,含有相同数目的分子(或
气体的物质的量相同)。
m m
M V
(2)阿伏加德罗定律的推论(可通过pV=nRT及n= 、ρ= 导出)
相同条件 结论
公式 语言叙述
n V
T、p相同 1 = 1 同温、同压下,气体的体积与其物质的量成正比
n V
2 2
p n
T、V相同 1 = 1 同温、同体积下,气体的压强与其物质的量成正比
p n
2 2
ρ M
T、p相同 1 = 1 同温、同压下,气体的密度与其摩尔质量(或相对
ρ M
2 2
分子质量)成正比
T、P、V相同 同温、同压同体积下,气体的质量与其摩尔质量(或
相对分子质量)成正比
核心知识点二:
一、与物质的量浓度有关的计算
1. 溶液组成的两种表示方法
(1)物质的量浓度(c )
B
概念 以单位体积溶液里所含溶质B的物质的量来表示溶液组成的物理量,表达式为c
B
n
B
=V ,单位是 mol·L - 1
注意事项 ①从一定物质的量浓度溶液中取出任意体积的溶液,其浓度相同、所含溶质的物
质的量不同;
②溶质的浓度和离子的浓度不一定相同,要依据化学式进行分析计算。如:0.5
mol·L-1AlCl 溶液中,c(Cl-)=0.5 mol·L-1×3=1.5 mol·L-1
3
(2)溶质的质量分数(w)
①概念:用溶质的质量与溶液质量的比值来表示溶液组成的物理量,一般用百分数表
示。
m(溶质)
m(溶液)
②表达式:w= ×100%。
2. 物质的量浓度计算的要素
第2页(1)正确判断溶液的溶质
⃗
与水发生反应生成新 如Na、NaO、NaO水NaOH;
2 2 2
⃗ ⃗
的物质 SO水HSO ;NO水HNO
3 2 4 2 3
特殊物质 如NH 溶于水后溶质为NH ·H O,但计算浓度时仍以NH 作为溶质
3 3 2 3
含结晶水的物质 CuSO ·5H O―→CuSO ;
4 2 4
NaCO·10H O―→NaCO
2 3 2 2 3
(2)准确计算溶液的体积
n
V
c= 中的V是溶液的体积,不是溶剂的体积,也不是溶质和溶剂的体积之和,不能
m
ρ
用水的体积代替溶液的体积,应根据V= 计算。
二、物质的量浓度计算的三种常见题型
1. 物质与所含离子间物质的量浓度的换算
2. 溶液的稀释和混合规律
(1)溶液的稀释
①溶质的物质的量在稀释前后保持不变,即cV=cV。
1 1 2 2
②溶液质量守恒,m(稀)=m(浓)+m(水)(体积一般不守恒)。
[提醒] 1 L 1 mol·L-1的氨水中,NH 的物质的量并不是1 mol,而是指溶液中NH 、
3 3
NH ·H O、NH三者的物质的量之和为1 mol。
3 2
(2)溶液的混合规律
注意:同种溶质的溶液混合后浓度计算的关键点
有关溶液稀释及混合的计算,应抓住稀释前后溶质的物质的量不变列方程式:c ·V
前 前
=c ·V 或cV +cV =c ·V ,混合后溶液的体积不等于混合前两溶液的体积和,而是要
后 后 1 1 2 2 混 混
m
混
ρ
根据密度计算,即V = 混 。
混
3. 物质的量浓度与质量分数的关系
如图所示,体积为 V L,密度为ρ g·cm-3的溶液,含有溶质的摩尔质量为M g·mol-
1,溶质的质量分数为w,则物质的量浓度c与质量分数w的关系是:
第3页m(溶质)
n(溶质) M m(溶质) 1000ρwV 1000ρw cM
c= = = = = ⇒w=
V V MV MV M 1000ρ
核心知识点一:
1. N 为阿伏加德罗常数的值。下列叙述正确的是( )
A
A. 含有N个氦原子的氦气在标准状况下的体积为11.2L
A
B. 25℃,1.01×105Pa,64gSO 中含有的原子数为3N
2 A
C. 11.2LCl 含有的分子数为0.5N
2 A
D. 标准状况下,11.2LCCl 含有的分子数为0.5N
4 A
【答案】B
【解析】①氦气为单原子分子,A项错误②质量、物质的量和粒子数不受温度和压强
影响,B项正确;③未指明是否在标准状况,C项错误;④标准状况下,CCl 为液体,D项
4
错误。
【考点】以物质的量为中心的计算
2. 同温同压下,相同体积的甲、乙两种气体的质量比是17:14。若乙气体是CO,则甲气
体可能是( )
A. Cl B. HCl C. NH D. HS
2 3 2
【答案】D
【解析】M =17×27÷14=34(g/mol)
甲
【考点】阿伏伽德罗定律的应用
同温同压下,等质量的二氧化碳和氮气相比较,下列叙述中正确的是( )
A. 密度比为7∶11
B. 密度比为11∶7
C. 体积比为11∶7
D. 物质的量之比为1∶1
【答案】B
【解析】M M =7∶14。
(氮气)/ (二氧化碳)
【考点】阿伏伽德罗定律的应用
第4页核心知识点二:
在标准状况下,将V L氨气溶于0.1 L水中,所得溶液的密度为ρ g·cm-3,则此氨水
的物质的量浓度为____________ mol·L-1。
1000Vρ
【答案】
17V+2240
V
22.4
【解析】n(NH )= mol,
3
V
×17+100
22.4
ρ
溶液体积:V= ×10-3 L
V
22.4
c=
V
×17+100
22.4
×10−3
ρ mol·L-1
1000Vρ
=
17V+2240
mol·L-1。
【考点】有关物质的量浓度的计算
一定量的H 在Cl 中充分燃烧,所得混合物用100mL3mol/L的NaOH溶液(密度为
2 2
1.12g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.05mol。
(1)原NaOH溶液的质量分数为__________%(小数点后保留1位数字)。
(2)所得溶液中Cl-的物质的量为_________mol。
(3)所用Cl 和参加反应的H 的物质的量之比为n(Cl) ∶ n(H) =
2 2 2 2
________。
【答案】(1)10.7 (2)0.25 (3)3:2
1000ρw
M
【解析】(1)根据 可知,NaOH溶液的质量分数为
3×40
×100%≈10.7%
1000×1.12
。
(2)用NaOH溶液吸收一定量的H 与Cl 充分反应后所得混合气体,所得溶液中含有
2 2
NaClO,说明H 与Cl 充分反应后Cl 有剩余,用NaOH溶液吸收后所得溶液中的溶质为
2 2 2
NaCl、NaClO,根据钠元素守恒可知n(NaOH)=n(NaCl)+n(NaClO)=0.1L×3mol/L
=0.3mol,故溶液中n(NaCl)=0.3mol-0.05mol=0.25mol,溶液中n(Cl-)=n
第5页(NaCl)=0.25mol。
(3)n(NaClO)=0.05mol,则Cl 与NaOH反应生成的NaCl的物质的量为
2
0.05mol,则HCl与NaOH反应生成的NaCl的物质的量为0.25mol-0.05mol=0.2mol,故n
(HCl)=0.2mol,n(H)=0.1mol,根据氯原子和钠原子守恒知2n(Cl)=n(NaCl)
2 2
+n(NaClO)=n(NaOH)=0.3mol,所以n(Cl)=0.15mol,因此所用Cl 和参加反应
2 2
的H 的物质的量之比为n(Cl)∶n(H)=0.15∶0.1=3:2。
2 2 2
【考点】有关物质的量浓度的计算
(答题时间:25分钟)
一、选择题
1. 下列说法正确的是( )
A. 1 mol H 所占体积约为22.4 L
2
B. 22 g CO 中含有的分子数约为6.02×1023
2
C. 100 mL 0.5 mol·L-1 NaOH溶液中含溶质的质量为0.05 g
D. 标准状况下,11.2 L O 和H 的混合气体所含分子数约为3.01×1023
2 2
2. 设N 为阿伏加德罗常数,如果 a g 某气态双原子分子的分子数为p,则b g该气体
A
在标准状况下的体积V(L)是( )
22.4ap 22.4ab 22.4N b 22.4pb
A
bN pN aN
A. A B. A C.
a
D. A
3. 现有V L 0.5 mol·L-1的盐酸,欲将其浓度扩大一倍,以下方法中最宜采用的是(
)
A. 加热浓缩到原来体积的一半
B. 加入5 mol·L-1的盐酸0.125V L
C. 加入10 mol·L-1的盐酸0.1V L,再稀释至1.5V L
D. 标况下通入11.2 L氯化氢气体
4. CO和CO 的混合气体18 g,完全燃烧后测得CO 体积为11.2 L(标准状况),则
2 2
(1)混合气体中CO的质量是________g。
(2)混合气体中CO 在标准状况下的体积是________L。
2
(3)混合气体在标准状况下的密度是________g·L-1。
(4)混合气体的平均摩尔质量是________g·mol-1。
5. (1)已知标准状况下,气体A的密度为2.857 g·L-1,则气体A的相对分子质量为
________,可能是________气体。
(2)标准状况下,1.92 g 某气体的体积为 672 mL,则此气体的相对分子质量为
第6页________。
(3)在一定条件下,m g NHHCO 完全分解生成NH 、CO、HO(g),按要求填空。
4 3 3 2 2
①若所得混合气体对H 的相对密度为d,则混合气体的物质的量为____________。
2
NH HCO 的摩尔质量为________________(用含m、d的代数式表示)。
4 3
②若所得混合气体的密度折合成标准状况为ρ g·L-1,则混合气体的平均摩尔质量为
________________(用含ρ的代数式表示)。
③若在该条件下,所得NH 、CO 、HO(g)的体积分数分别为a%、b%、c%,则混
3 2 2
合气体的平均相对分子质量为________________________(用含a、b、c的代数式表示)。
6. (1)在100 g物质的量浓度为c mol·L-1,密度为ρ g·cm-3的硫酸中加入一定量的水
稀释成 mol·L-1的硫酸,则加入水的体积________(填“=”“>”或“<”,下同)
100 mL。
(2)若把(1)中的HSO 改成氨水,应加入水的体积______ 100 mL。
2 4
(3)若把(1)(2)中的物质的量的浓度均改为溶质的质量分数,则加入水的体积
________ 100 mL。
第7页1. 【答案】D
【解析】温度、压强会影响气体摩尔体积,未说明温度和压强,气体摩尔体积不一定是
22g
22.4 L·mol-1,故A项错误;22 g二氧化碳的物质的量为
44g⋅mol−1
=0.5 mol,二氧化
碳分子数目为0.5 mol×6.02×1023 mol-1=3.01×1023,故B项错误;氢氧化钠的物质的量为0.1
L×0.5 mol·L-1=0.05 mol,NaOH的质量为0.05 mol×40 g·mol-1=2 g,故C项错误;混合气
11.2L
体总物质的量为
22.4L⋅mol−1
=0.5 mol,分子总数目为 0.5 mol×6.02×1023 mol-1=
3.01×1023,故D项正确。
2. 【答案】D
p
N
【解析】 a g双原子分子的物质的量= A mol,
aN
ag
A
=
p p
mol
N
双原子分子的摩尔质量= A g·mol-1,
所以b g气体在标准状况下的体积为
bg
aN 22.4pb
A g⋅mol−1
aN
p
×22.4 L·mol-1= A L。
3. 【答案】C
【解析】加热蒸发,HCl挥发,溶液浓度降低,故A错误;溶液的体积不具有加和性,
故B错误;混合后溶液中的 HCl的物质的量为 0.5 mol·L-1×V L+10 mol·L-1×0.1V L=
1.5Vmol
1.5VL
1.5V mol,所以混合后HCl的浓度为 =1 mol·L-1,故C正确;通入氯化氢气体,
溶液的体积发生变化,无法求出浓度,故D错误。
4. 【答案】(1)7 (2)5.6 (3)1.61 (4)36
【解析】CO燃烧发生反应:2CO+O2CO ,CO的体积与生成CO 的体积相等,燃烧
2 2 2
后CO 的总体积为11.2 L,故18 g CO和CO 的混合气体的总体积为11.2 L,在标准状况下,
2 2
18 g CO和CO 的混合气体的物质的量为0.5 mol,设CO的物质的量为x mol,CO 的物质
2 2
的量为y mol,
28 44 18
{ x y
+ = ¿¿¿¿
则 ,解得x=0.25,y=0.25。
(1)混合气体中CO的质量=28 g·mol-1×0.25 mol=7 g。
(2)原混合气体中,CO 的体积为0.25 mol×22.4 L·mol-1=5.6 L。
2
第8页18g
11.2L
(3)原混合气体的密度= ≈1.61 g·L-1。
M¯
(4) =ρ·22.4 L·mol-1=1.61 g·L-1×22.4 L·mol-1≈36 g·mol-1。
m
2d
5. 【答案】(1)64 SO (2)64 (3)① mol 6d g·mol-1 ②22.4ρ g·mol-1
2
③17a%+44b%+18c%
【解析】(1)M=ρ×22.4 g·mol-1≈64 g·mol-1。
1.92g
0.672L
(2)M=
22.4L⋅mol−1
=64 g·mol-1。
(3)因为NH HCO (s)NH (g)+CO(g)+HO(g)
4 3 3 2 2
m
2d
①M(混)=2d⇒n(混)= mol,
⇒M(NH HCO )=2d×3 g·mol-1=6d g·mol-1。
4 3
M¯
② (混)=22.4ρ g·mol-1。
③n(NH )∶n(CO)∶n(HO)=a%∶b%∶c%,
3 2 2
M¯
(混)=17a%+44b%+18c%。
6. 【答案】(1)< (2)> (3)=
100 100+V
c
水
⋅
ρ ρ' 2
【解析】(1) ·c=
200 {ρ'
¿
ρ
V = -100
水
由于ρ′<ρ,所以V <100 mL。
水
(2)由于ρ′>ρ,所以V >100 mL。
水
溶质质量
溶液质量
(3)根据质量分数= ×100%知,溶质不变,质量分数减半,则溶液质量加
倍,所以均应加入100 mL水。
第9页