文档内容
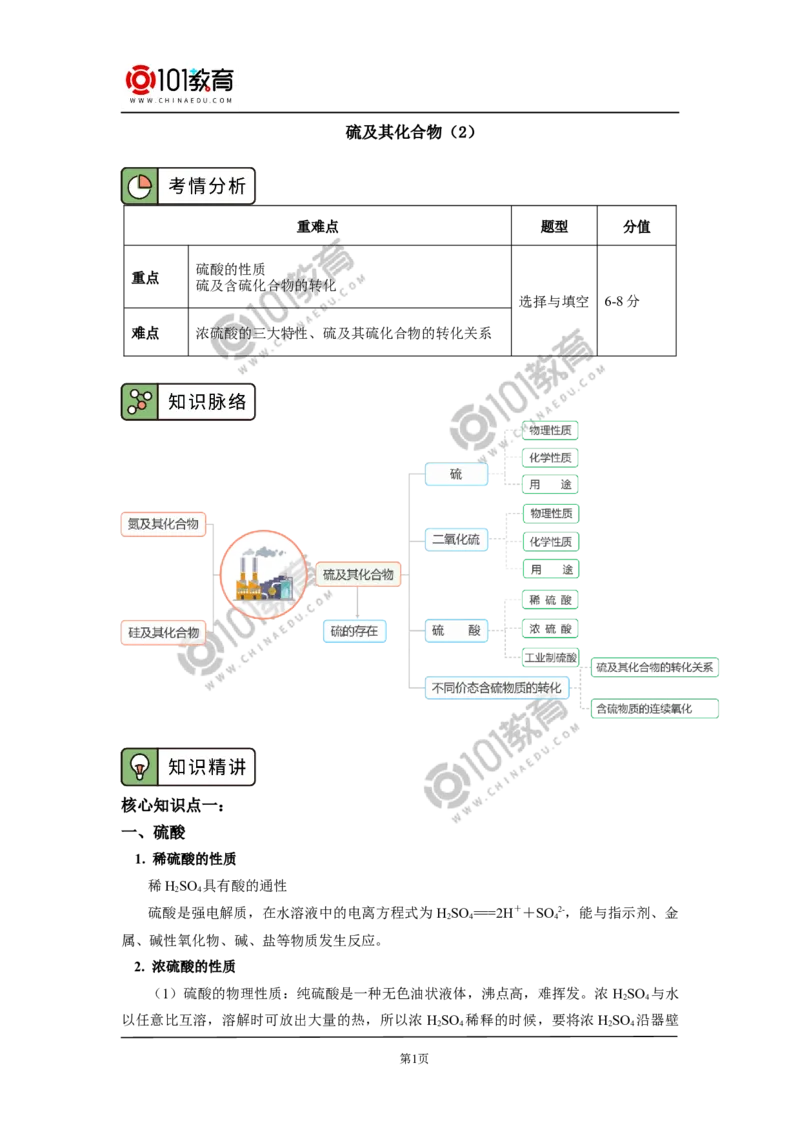
硫及其化合物(2)
重难点 题型 分值
硫酸的性质
重点
硫及含硫化合物的转化
选择与填空 6-8分
难点 浓硫酸的三大特性、硫及其硫化合物的转化关系
核心知识点一:
一、硫酸
1. 稀硫酸的性质
稀HSO 具有酸的通性
2 4
硫酸是强电解质,在水溶液中的电离方程式为 HSO ===2H++SO 2-,能与指示剂、金
2 4 4
属、碱性氧化物、碱、盐等物质发生反应。
2. 浓硫酸的性质
(1)硫酸的物理性质:纯硫酸是一种无色油状液体,沸点高,难挥发。浓 HSO 与水
2 4
以任意比互溶,溶解时可放出大量的热,所以浓 HSO 稀释的时候,要将浓HSO 沿器壁
2 4 2 4
第1页慢慢注入水中,并用玻璃棒不断搅拌。
(2)浓HSO 的三大特性
2 4
①吸水性:可作为干燥剂,但由于氧化性和酸性的存在,因此不能够干燥还原性气体
如HS和碱性气体NH 。通常使用装置为洗气瓶。
2 3
②脱水性:蔗糖中加入浓硫酸或用蘸有浓硫酸的玻璃棒在纸张上写字,都会发现有黑
色的碳生成。
说明:蔗糖黑面包实验中,我们闻到的刺鼻性气味就是脱水后的碳与浓硫酸反应的结
果。
③强氧化性:
与金属反应:
Cu+2HSO (浓) CuSO +SO ↑+2HO、C+2HSO (浓) CO↑+2SO ↑
2 4 4 2 2 2 4 2 2
+2HO。
2
钝化常温下,铁、铝遇浓HSO 钝化,可用铝槽车运浓HSO 。
2 4 2 4
但是在加热条件下铁、铝可以与浓硫酸反应:2Fe + 6H SO (浓) Fe (SO ) +
2 4 2 4 3
3SO ↑+ 6H O;2Al + 6H SO (浓) Al (SO ) + 3SO ↑+ 6H O;
2 2 2 4 2 4 3 2 2
与非金属反应:热的浓硫酸还能氧化碳、硫等非金属单质。
C + 2H SO (浓) CO + 2SO ↑+ 2H O;
2 4 2 2 2
S + 2H SO (浓) 3SO + 2H O
2 4 2 2
浓硫酸还能与还原性较强的物质反应,如HS、HI等。
2
HS + H SO (浓)= S↓+ 3SO + 2H O;
2 2 4 2 2
2HI + H SO (浓)= I + SO ↑ + 2H O。
2 4 2 2 2
3. 硫酸根的检验
取被检测溶液于试管中,向试管中加足量盐酸溶液,无现象,再向溶液中加入氯化钡
溶液,观察有无白色沉淀。
注:①盐酸酸化的作用是排除其他离子干扰,一般指碳酸根
②硫酸钡是不溶于稀强酸的沉淀,所以可以用作医用的钡餐实验,而碳酸钡不能
使用,否则溶解在胃酸中,产生有毒的重金属钡离子,破坏胃蛋白而中毒!
4. 工业制硫酸
核心知识点二:
第2页二、不同价态含硫物质的转化
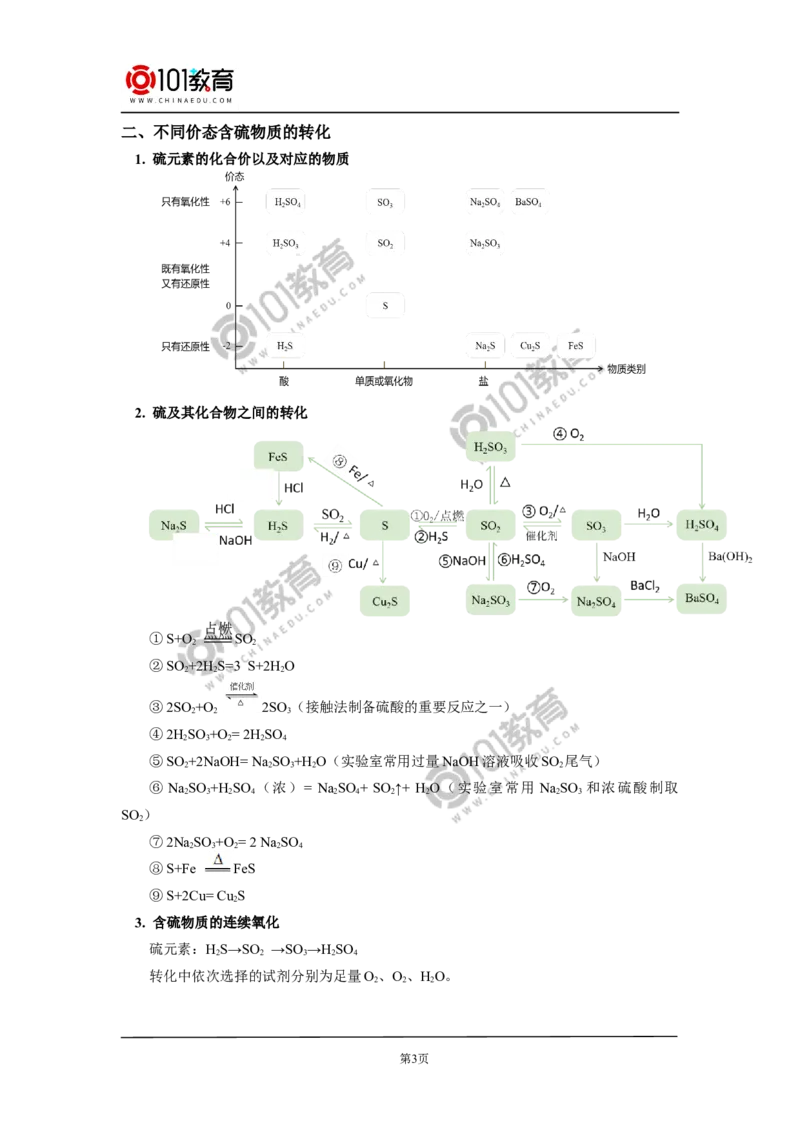
1. 硫元素的化合价以及对应的物质
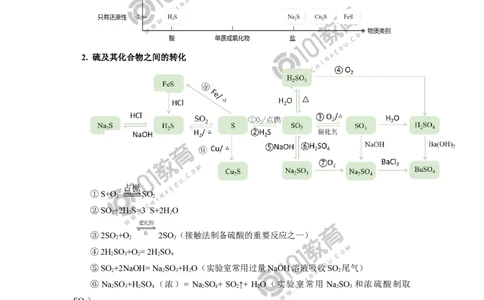
2. 硫及其化合物之间的转化
点燃
①S+O SO
2 2
②SO +2H S=3 S+2HO
2 2 2
③2SO +O 2SO (接触法制备硫酸的重要反应之一)
2 2 3
④2HSO +O = 2H SO
2 3 2 2 4
⑤SO +2NaOH= Na SO +H O(实验室常用过量NaOH溶液吸收SO 尾气)
2 2 3 2 2
⑥ NaSO +H SO (浓)= Na SO + SO ↑+ H O(实验室常用 NaSO 和浓硫酸制取
2 3 2 4 2 4 2 2 2 3
SO )
2
⑦2NaSO +O = 2 Na SO
2 3 2 2 4
⑧S+Fe FeS
⑨S+2Cu= Cu S
2
3. 含硫物质的连续氧化
硫元素:HS→SO →SO →HSO
2 2 3 2 4
转化中依次选择的试剂分别为足量O、O、HO。
2 2 2
第3页核心知识点一:
下列关于浓硫酸的叙述中正确的是( )
A. 浓硫酸具有吸水性,因而能使蔗糖碳化
B. 浓硫酸是在常温下可迅速与铜片反应放出二氧化硫气体
C. 浓硫酸是一种干燥剂,能干燥氨气、氢气等气体
D. 浓硫酸在常温下能够使铁、铝等金属钝化
【答案】D
【解析】浓硫酸具有脱水性,能使蔗糖脱水而炭化;浓硫酸在加热条件下才与铜片发
生反应放出二氧化硫气体;浓硫酸是一种干燥剂,但不能用于干燥像氨(碱性)、硫化氢
(还原性)等气体;浓硫酸具有强氧化性,在常温下能够使铁、铝等金属钝化。
常见的还原性气体有HS、HBr、HI等,这些气体不能被浓硫酸干燥,而 H 、CO、
2 2
NO、SO 则可以。
2
【考点】浓硫酸的性质
含硫煤燃烧会产生大气污染物,为防治该污染,某工厂设计了新的治污方法,同时可
得到化工产品,该工艺流程如图所示,下列叙述不正确的是( )
A. 该过程中可得到化工产品HSO
2 4
B. 该工艺流程是除去煤燃烧时产生的SO
2
C. 该过程中化合价发生改变的元素为Fe和S
D. 图中涉及的反应之一为Fe (SO )+SO+2H O=2FeSO + 2H SO
2 4 3 2 2 4 2 4
【答案】C
【解析】根据工艺流程图可知,该工艺中Fe (SO ) ;溶液吸收SO 生成FeSO ;和
2 4 3 2 4
HSO ,该反应的化学方程式为Fe (SO ) +SO+2H O=2FeSO +2H SO 。该工艺不仅吸收
2 4 2 4 3 2 2 4 2 4
第4页了二氧化硫,还得到了化工产品硫酸,A、D正确;根据上述分析可知该工艺流程是除去
煤燃烧时产生的SO ,B正确;该过程中化合价发生变化的元素有氧、铁、硫,C错误。
2
【考点】硫及其化合物
核心知识点二:
如图:A为单质,B为一种具有还原性的二元含氧酸,C为溶液,且溶液中仅有一种
溶质,D为气体,E、F为白色沉淀。物质间转化过程中需要加入的试剂未完全写出。回答
下列问题:
(1)在空格处写出相应物质的化学式:A为_______________;D为_______________;
E为_______________。
(2)③中所加的试剂应该具有_____________性(“氧化”或“还原”),可能为
______________或_____________。
(3)写出B→E的离子方程式:___________________________________。
写出C → F的离子方程式:______________________________________。
【答案】(1)S SO BaSO (2)氧化 O H O(合理即可)
2 3 2 2 2
(3)HSO + Ba2+ + 2OH-= BaSO↓+ 2 H O Ba2+ SO 2- = BaSO↓
2 3 3 2 + 4 4
【解析】
【考点】含硫物质的转化
在下列物质转化中,A是一种正盐,D的相对分子质量比C的相对分子质量大16,E
是酸;当X无论是强酸还是强碱时,都有如下的转化关系:
第5页当X时强酸时,A、B、C、D、E均含同一种元素;当X是强碱时, A 、B、C、D、
E均含另一种元素。
请回答下列问题:
(1)A是___________,Y是___________,Z是____________。
(2)当X是强酸时,E是__________,写出B生成C的化学方程式:_____________。
(3)当X是强碱时,写出B生成C的化学方程式:_______________________。
【答案】(1)(NH )S O H O
4 2 2 2
点燃
(2)HSO 2H S + 3O 2SO + 2H O
2 4 2 2 2 2
(3)4NH + 5O 4NO + 6H O
3 2 2
【解析】
且M(D)-M(C)=16,可知Y为O ,连续氧化后与Z生成酸E,则A中含有N
r r 2
或S元素,又因为A为正盐,则A为(NH )S。
4 2
当X为强酸时: 。
当X为强碱时: 。
(答题时间:25分钟)
一、选择题
1. 某同学设想用如图所示装置来验证浓硫酸的某些性质,其中不能达到实验目的的是(
)
选项 A B C D
实验
吸水性 脱水性 溶解放热 强氧化性
目的
实验
装置
2. 下列事实与浓硫酸表现出的性质(括号中)对应关系正确的是( )
A. 在空气中敞口久置的浓硫酸,溶液质量增大(难挥发性)
B. 在加热条件下铜与浓硫酸反应(强氧化性、酸性)
第6页C. 蔗糖与浓硫酸反应中有海绵状的炭生成(吸水性)
D. 浓硫酸与少量胆矾晶体混合,晶体由蓝色变成白色(脱水性)
3. 用20 mL 18.4 mol·L-1浓HSO 与金属铜共热一段时间后,冷却,过滤,除去多余的铜,
2 4
将滤液加水稀释到100 mL,所得溶液中SO 2-浓度为3. 18 mol·L-1,则此时溶液中CuSO 的
4 4
物质的量浓度为( )
A. 0. 50 mol·L--1 B. 0. 75 mol·L-1
C. 1. 00 mol·L-1 D. 3. 18 mol·L-1
4. 下列各组物质混合后,没有明显现象的是( )
①HS和SO ;②SO 和SO ;③SO 和氯水;④SO (气)和Cl;⑤HS和Cl
2 2 2 3 2 3 2 2 2
A. ①③⑤ B. ②④
C. ②⑤ D. ③④⑤
5. 硫黄在空气中燃烧生成气体甲,甲溶于水得溶液乙,向乙溶液中滴加溴水,溴水褪色,
乙转化为丙。在丙溶液中加入NaS生成气体丁,把丁通入乙溶液中得到沉淀戊。甲、乙、
2
丙、丁、戊均含有硫元素,则它们分别是( )
A. SO 、HSO 、HSO 、HS、S
3 2 4 2 3 2
B. SO 、HSO 、HSO 、SO 、SO
2 2 3 2 4 2 3
C. SO 、HSO 、HSO 、SO 、NaSO
3 2 4 2 3 2 2 2 3
D. SO 、HSO 、HSO 、HS、S
2 2 3 2 4 2
6. 已知A是一种不溶于水的固体,在一定条件下有下列转化关系(部分产物及 HO省
2
略)
试回答:
(1)写出物质的化学式:A________,E________。
(2)写出由B和C反应生成A,由F的浓溶液生成C的化学方程式:
B+C A_____________________________________________________,
F(浓) C___________________________________________________。
(3)写出D和F的稀溶液反应的离子方程式_________________________________
__________________。
7. 某化学兴趣小组为了探究SO 的性质,按下图所示装置进行实验。
2
第7页请回答下列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是________,其中发生反应的化学方程式为
___________________;
(2)实验过程中,装置 B、C 中产生的现象分别是______________________、
______________,这些现象分别说明SO 具有的性质是________和________;装置B中发
2
生反应的离子方程式为________________________。
(3)装置 D 的目的是探究 SO 与品红作用的可逆性,请写出实验操作及现象
2
________________________________。
(4)尾气可采用________溶液吸收。
第8页1.【答案】D
【解析】盛有水的烧杯中水的量减少可以证明浓硫酸具有吸水性,故A正确;滤纸片
脱水炭化可以证明浓硫酸具有脱水性,故B正确;U形管中的水面右高左低,说明浓硫酸
溶解时放出大量的热,使锥形瓶中压强增大,故C正确;Cu与浓HSO 常温下不反应,加
2 4
热反应生成硫酸铜、二氧化硫和水,故D错误。
2.【答案】B
【解析】在空气中敞口久置的浓硫酸,会吸收空气中的水分而使溶液的质量增大,表
现的是浓硫酸的吸水性,故A错误;在加热条件下铜与浓硫酸反应生成硫酸铜、二氧化硫
和水,硫元素化合价部分变化,体现浓硫酸的强氧化性和酸性,故 B正确;蔗糖与浓硫酸
反应中有海绵状的炭生成,体现浓硫酸的脱水性,故C错误;浓硫酸与少量胆矾晶体混合,
晶体由蓝色变成白色,体现浓硫酸的吸水性,故D错误。
3.【答案】A
【解析】浓HSO 的总物质的量为0. 02 L×18. 4 mol·L-1=0. 368 mol,反应后剩余SO 2-
2 4 4
的物质的量n(SO 2-)=0. 1 L×3. 18 mol·L-1=0. 318 mol,则表现氧化性的HSO 的物质的量
4 2 4
n(HSO )=0. 368 mol-0. 318 mol=0. 05 mol。设该反应中Cu的物质的量为x mol,由得失
2 4
0.05mol
0.1L
电子守恒有等式:2x=2×0. 05,x=0. 05,故c(CuSO )= =0. 50 mol·L-1。
4
4.【答案】B
【解析】SO 和SO 中硫元素为相邻价态,不能发生氧化还原反应。SO 和Cl 都具有
2 3 3 2
氧化性,相互间不能发生反应。
5.【答案】D
【解析】题目中所述的变化过程可表示为:
由题意可推出:甲是SO ,乙是HSO ,丙是HSO ,丁是HS,戊是S。
2 2 3 2 4 2
6.【答案】(1)S SO (2)2HS+SO ===3S↓+2HO
3 2 2 2
Cu+2HSO (浓) CuSO +SO ↑+2HO
2 4 4 2 2
(3)FeS+2H+===Fe2++HS↑
2
【解析】由A+H B,A+O C知:A元素的化合价既能升高,也能降低,
2 2
故A为非金属元素,B为氢化物,C为氧化物,且B+C A,则A为硫,进一步推知
B为HS,C为SO ,D为FeS,E为SO ,F为HSO 。
2 2 3 2 4
7.【答案】(1)蒸馏烧瓶 NaSO +HSO (浓)===Na SO +SO ↑+HO (2)溶液
2 3 2 4 2 4 2 2
−
由紫红色变为无色 无色溶液中出现黄色浑浊 还原性 氧化性 5SO +2MnO4 +
2
第9页2−
2HO===2Mn2++5SO4 +4H+ (3)品红溶液褪色后,关闭分液漏斗的旋塞,点燃酒精
2
灯加热,溶液恢复为红色 (4)NaOH
【解析】(1)根据仪器的特征,该仪器是蒸馏烧瓶;亚硫酸钠和浓硫酸反应生成硫酸
钠、SO 和水,化学方程式为NaSO +HSO (浓)===Na SO +SO ↑+HO。
2 2 3 2 4 2 4 2 2
(2)酸性高锰酸钾有强氧化性,二氧化硫有还原性,所以二氧化硫能被酸性高锰酸钾
溶液氧化而褪色,同时说明二氧化硫有还原性,SO 的氧化性能将S2-氧化成S,则实验过
2
程中,装置B、C中发生的现象分别是溶液由紫红色变为无色、无色溶液中出现黄色浑浊,
这些现象分别说明SO 具有的性质是还原性和氧化性;装置B中发生反应的离子方程式为
2
− 2−
5SO +2MnO4 +2HO===2Mn2++5SO4 +4H+。(3)二氧化硫具有漂白性,能使品红溶
2 2
液褪色,但加热褪色后的品红溶液,溶液的颜色能复原,所以探究 SO 与品红作用的可逆
2
性的实验操作及现象是品红溶液褪色后,关闭分液漏斗的活塞,点燃酒精灯加热,溶液恢
复为红色(4)该实验的尾气是SO ,可用NaOH溶液吸收。
2
第10页