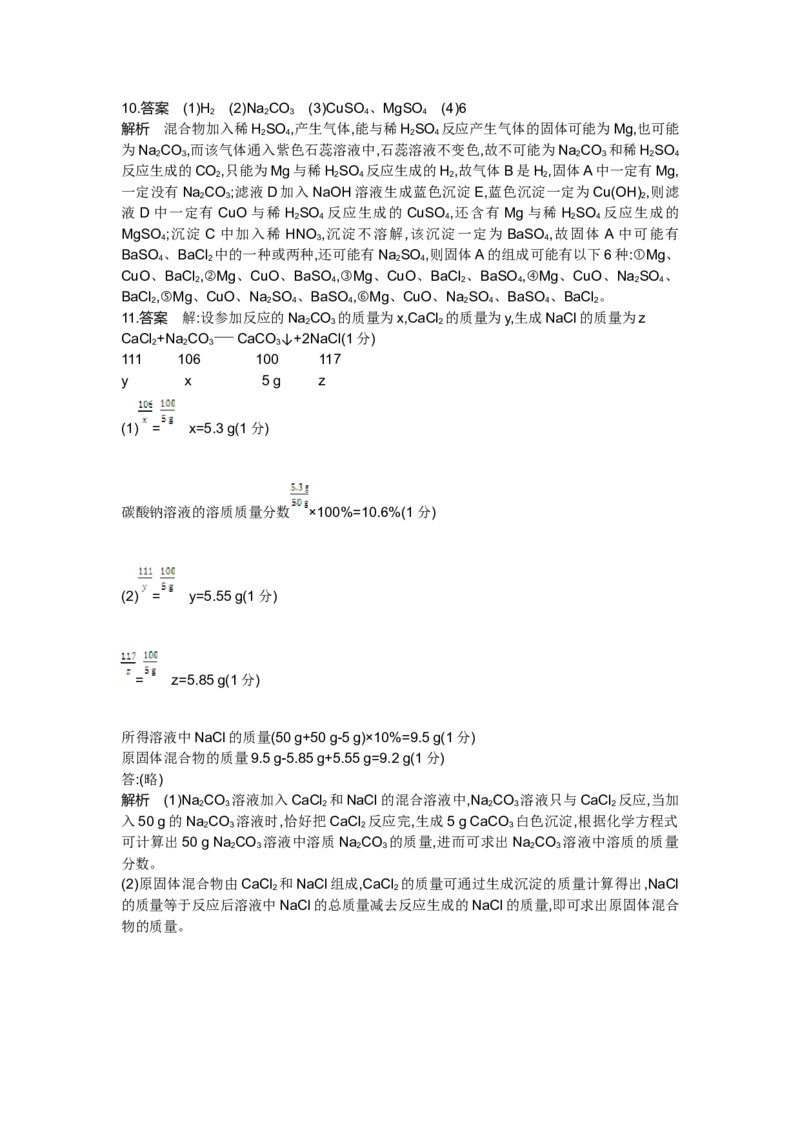文档内容
包头市 2015 年初中升学考试
化学试题(含答案全解全析)
可能用到的相对原子质量:H—1 C—12 O—16 Na—23 Mg—24 S—32 Cl—35.5
K—39 Ca—40 Fe—56
一、选择题(每题2分,共12分。每小题只有一个选项符合题意)
1.物质的下列用途主要利用其物理性质的是( )
A.白醋用于清除水壶中的水垢 B.干冰用于人工降雨
C.稀盐酸用于金属表面除锈 D.苏打水用于缓解胃酸过多
2.下列说法错误的是( )
A.同种分子构成的物质是纯净物
B.原子是化学变化中的最小粒子
C.同种元素组成的物质是单质
D.元素的化学性质与该元素原子的最外层电子数目关系最密切
3.下列有关物质的除杂、鉴别所用试剂或方法正确的是( )
A.除去铁粉中混有的锌粉,可加过量的硫酸亚铁溶液并过滤
B.用酚酞溶液可一次性鉴别稀硫酸、澄清石灰水和氯化钠溶液
C.要除去CO 气体中混有的少量HCl气体,可将其通过足量的NaOH溶液
2
D.不加任何试剂即可鉴别KCl溶液、NaOH溶液、K SO 溶液和CuSO 溶液
2 4 4
4.50克20%的KOH溶液和50克20%的H SO 溶液充分混合,混合后溶液的pH( )
2 4
A.小于7 B.等于7 C.大于7D.无法判断
5.天平两边各放质量相等的烧杯,分别盛有等质量、等质量分数的稀硫酸,此时天平平衡。将等
质量的MgCO 和Na CO 分别加入两烧杯中,充分反应后,下列说法错误的是( )
3 2 3
A.若天平不平衡,指针一定偏向加Na CO 的一边
2 3
B.若天平平衡,两烧杯中的酸一定完全反应
C.若反应后的Na CO 有剩余,天平一定平衡
2 3
D.若天平不平衡,两种碳酸盐一定都没有剩余
6.下表中,有关量的变化图像与其对应叙述相符的是( )
A B C D
t ℃时,向等质量的甲、乙、
常温下,向一定质 向一定质量的过 向等质量的铁和镁
丙三种物质中分别加水配
量的饱和石灰水 氧化氢的水溶液 中分别加入足量的
制成饱和溶液,所得溶液质
中加入氧化钙 中加入二氧化锰 稀盐酸
量最小的是丙
二、填空题(每空1分,化学方程式2分,共21分。)
7.(1)用化学符号填空
①两个铁离子
②硫酸中硫元素的化合价③ 表示的是
(2)汽油中加入适量乙醇作为汽车燃料,可适当节省石油资源,并减少污染。写出乙醇在空气中
完全燃烧的化学方程式 。
(3)在一个密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得数据如下:
物质 A B C D
反应前的质量/g 6.4 3.2 4.0 2.8
反应后的质量/g 5.2 待测 7.2 2.0
反应后待测的B的质量是 克,该反应所属的基本反应类型是 。
(4)现有铁、氧化铜、稀盐酸、氢氧化镁、氢氧化钠溶液、硫酸铜溶液六种物质,两两混合能发生
的反应有 个。
8.某化学小组向一定量AgNO 和Cu(NO ) 的混合溶液中加入Mg粉,充分反应后过滤,得到
3 3 2
滤液A和固体B。
对滤液A所含的溶质有以下几种猜想:
①Mg(NO ) 、Cu(NO ) 、AgNO ②Mg(NO ) 、Cu(NO )
3 2 3 2 3 3 2 3 2
③Mg(NO ) 、AgNO ④只有Mg(NO )
3 2 3 3 2
经过讨论,大家一致认为不合理的猜想是 (填序号),理由是
。
若猜想④成立,通过以下实验可以确定固体B的成分,请将下表填写完整。
实验步骤 现象 固体B的成分
有气泡产生
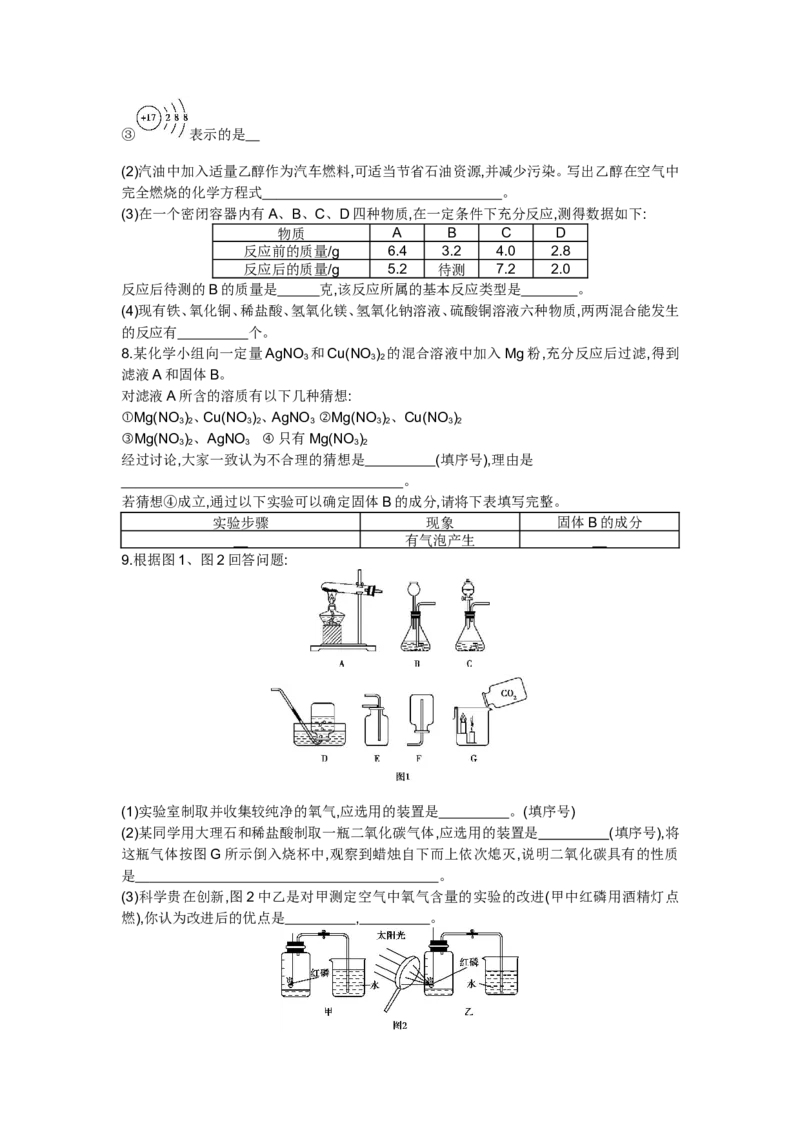
9.根据图1、图2回答问题:
(1)实验室制取并收集较纯净的氧气,应选用的装置是 。(填序号)
(2)某同学用大理石和稀盐酸制取一瓶二氧化碳气体,应选用的装置是 (填序号),将
这瓶气体按图G所示倒入烧杯中,观察到蜡烛自下而上依次熄灭,说明二氧化碳具有的性质
是 。
(3)科学贵在创新,图2中乙是对甲测定空气中氧气含量的实验的改进(甲中红磷用酒精灯点
燃),你认为改进后的优点是 , 。10.固体混合物A是由Mg、CuO、Na SO 、Na CO 、BaSO 、BaCl 中的几种混合而成,为确
2 4 2 3 4 2
定其组成,进行如图实验。(假设每步反应均恰好完全反应)
试推断:
(1)气体B是 。
(2)固体A中一定没有的物质是 。
(3)滤液D中一定含有的溶质是 。
(4)固体A的组成可能有 种。
三、计算题(共7分)
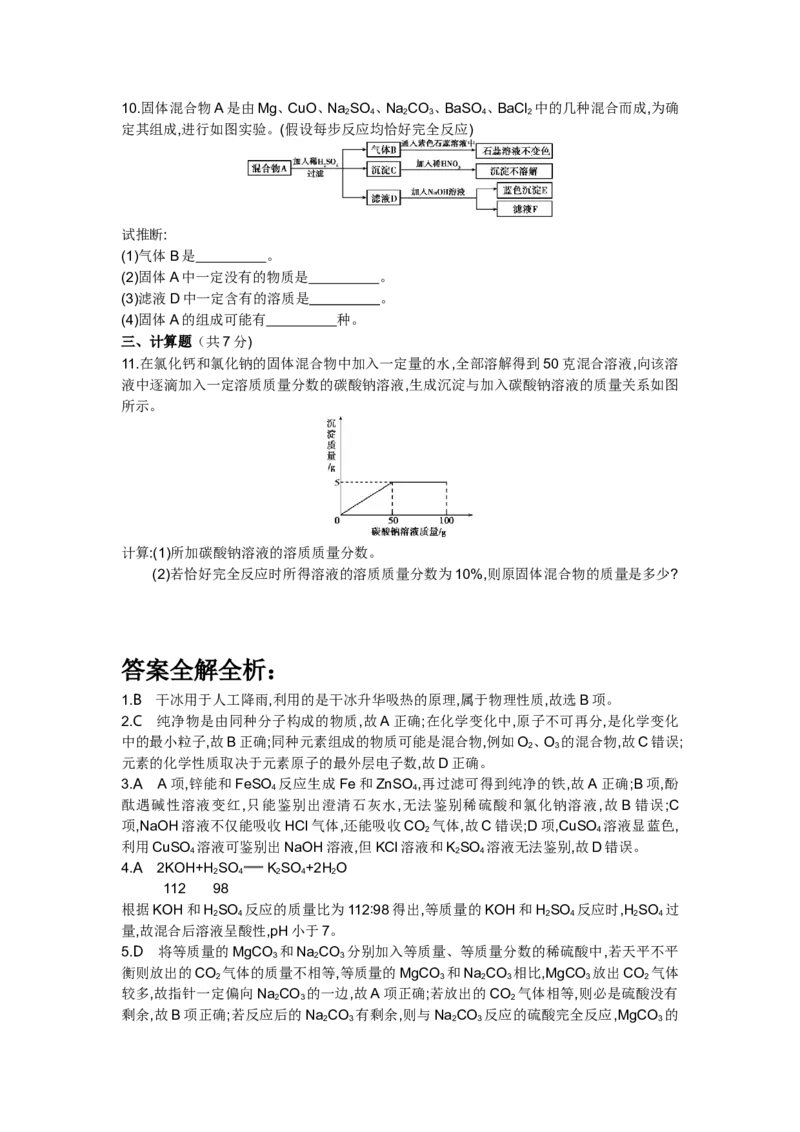
11.在氯化钙和氯化钠的固体混合物中加入一定量的水,全部溶解得到50克混合溶液,向该溶
液中逐滴加入一定溶质质量分数的碳酸钠溶液,生成沉淀与加入碳酸钠溶液的质量关系如图
所示。
计算:(1)所加碳酸钠溶液的溶质质量分数。
(2)若恰好完全反应时所得溶液的溶质质量分数为10%,则原固体混合物的质量是多少?
答案全解全析:
1.B 干冰用于人工降雨,利用的是干冰升华吸热的原理,属于物理性质,故选B项。
2.C 纯净物是由同种分子构成的物质,故A正确;在化学变化中,原子不可再分,是化学变化
中的最小粒子,故B正确;同种元素组成的物质可能是混合物,例如O 、O 的混合物,故C错误;
2 3
元素的化学性质取决于元素原子的最外层电子数,故D正确。
3.A A项,锌能和FeSO 反应生成Fe和ZnSO ,再过滤可得到纯净的铁,故A正确;B项,酚
4 4
酞遇碱性溶液变红,只能鉴别出澄清石灰水,无法鉴别稀硫酸和氯化钠溶液,故B错误;C
项,NaOH溶液不仅能吸收HCl气体,还能吸收CO 气体,故C错误;D项,CuSO 溶液显蓝色,
2 4
利用CuSO 溶液可鉴别出NaOH溶液,但KCl溶液和K SO 溶液无法鉴别,故D错误。
4 2 4
4.A 2KOH+H SO K SO +2H O
2 4 2 4 2
112 98
根据KOH和H SO 反应的质量比为112∶98得出,等质量的KOH和H SO 反应时,H SO 过
2 4 2 4 2 4
量,故混合后溶液呈酸性,pH小于7。
5.D 将等质量的MgCO 和Na CO 分别加入等质量、等质量分数的稀硫酸中,若天平不平
3 2 3
衡则放出的CO 气体的质量不相等,等质量的MgCO 和Na CO 相比,MgCO 放出CO 气体
2 3 2 3 3 2
较多,故指针一定偏向Na CO 的一边,故A项正确;若放出的CO 气体相等,则必是硫酸没有
2 3 2
剩余,故B项正确;若反应后的Na CO 有剩余,则与Na CO 反应的硫酸完全反应,MgCO 的
2 3 2 3 3相对分子质量比Na CO 小,则与Na CO 等质量的MgCO 也一定有剩余,因此放出CO 的
2 3 2 3 3 2
质量一定相等,天平一定平衡,故C项正确;当两种碳酸盐都没有剩余时,则产生CO 的质量不
2
同,此时天平不平衡,故D项错误。
6.C A项,氧化钙与水反应生成氢氧化钙,饱和溶液中的水被消耗一部分,这部分水中溶解的
溶质也随之析出,故溶液的质量减小,A项错误;B项,t ℃时甲、乙、丙三种物质的溶解度由大到
小的顺序为甲>乙>丙,故等质量的甲、乙、丙分别加水达到饱和状态时,甲所需水的质量最小,
丙所需水的质量最大,故所得溶液质量最小的应是甲,B项错误;C项,在MnO 的催化下,过氧
2
化氢分解生成水和氧气,故水的质量增大直至反应完毕,水的质量不再改变,C项正确;D项,向
等质量的铁和镁中分别加入足量的稀盐酸,镁生成盐的质量大,故D项错误。
7.答案 (1)①2Fe3+ ②H O ③Cl-
2 4
(2)C H OH+3O 2CO +3H O(不配平扣1分)
2 5 2 2 2
(3)2 化合反应 (4)6
解析 (1)铁离子的符号为Fe3+,故两个铁离子为2Fe3+;硫酸中H元素的化合价为+1,O元素
的化合价为-2,根据化合物中各元素正、负化合价的代数和为零,得S元素的化合价为+6;核外
电子数为18,核内质子数为17,则表示的为Cl-。
(2)乙醇在空气中完全燃烧,生成CO 和H O,化学方程式为C H OH+3O 2CO +3H O。
2 2 2 5 2 2 2
(3)根据表中数据得出,A的质量减小1.2 g,C的质量增大3.2 g,D的质量减小0.8 g,根据质量
守恒定律,B的质量应减小3.2 g-0.8 g-1.2 g=1.2 g,反应后B的质量=3.2 g-1.2 g=2.0 g,质量
减小的为反应物,质量增大的为生成物,故反应物有A、B和D,生成物有C,则该反应为化合反
应。
(4)铁、氧化铜、稀盐酸、氢氧化镁、氢氧化钠溶液、硫酸铜溶液六种物质,两两混合能发生的反
应有:①铁和稀盐酸;②铁和硫酸铜溶液;③氧化铜和稀盐酸;④稀盐酸和氢氧化镁;⑤稀盐酸
和氢氧化钠溶液;⑥氢氧化钠溶液和硫酸铜溶液,共6个反应。
8.答案 ③ Mg 先与 AgNO 反应,后与 Cu(NO ) 反应,当有 AgNO 剩余时,一定有
3 3 2 3
Cu(NO ) 取少量固体B于试管中,滴加稀盐酸(或稀硫酸) Ag、Cu、Mg
3 2
解析 Mg粉加入AgNO 和Cu(NO ) 的混合溶液中,Mg先和AgNO 反应,再和Cu(NO ) 反
3 3 2 3 3 2
应,若滤液中有AgNO ,则一定有Cu(NO ) 和Mg(NO ) ,则猜想③不合理;若猜想④成立,滤液
3 3 2 3 2
中只有Mg(NO ) ,则固体B中一定有Cu和Ag,可能有Mg,要想确定Mg是否存在,可取少量
3 2
固体B置于试管中,滴加稀盐酸(或稀硫酸),若有气泡产生,则B中一定有Mg,固体B的成分
为Ag、Cu、Mg。
9.答案 (1)AD(或CD)
(2)CE 既不燃烧也不支持燃烧,密度比空气大
(3)无污染,提高测定的准确性,操作简便(答对任意两点即可)
解析 (1)实验室制O ,若原料采用KMnO 或KClO 与MnO 的混合物,发生装置应选用A;若
2 4 3 2
原料采用过氧化氢溶液和MnO ,发生装置应选用C;要收集较纯净的O ,应选用排水法,故收
2 2
集装置应选用D,故答案为AD(或CD)。(2)用大理石和稀盐酸制CO ,发生装置应选用C;CO
2 2
的密度比空气大,能溶于水,收集装置应选用E;蜡烛熄灭,说明CO 既不燃烧也不支持燃烧,蜡
2
烛自下而上熄灭,说明CO 的密度比空气大。(3)图乙和图甲相比,用放大镜聚焦太阳光来点燃
2
红磷取代红磷在瓶外点燃再放入瓶中,这样做可提高测定的准确性,操作上更简单,防止生成
的P O 污染空气。
2 510.答案 (1)H (2)Na CO (3)CuSO 、MgSO (4)6
2 2 3 4 4
解析 混合物加入稀H SO ,产生气体,能与稀H SO 反应产生气体的固体可能为Mg,也可能
2 4 2 4
为Na CO ,而该气体通入紫色石蕊溶液中,石蕊溶液不变色,故不可能为Na CO 和稀H SO
2 3 2 3 2 4
反应生成的CO ,只能为Mg与稀H SO 反应生成的H ,故气体B是H ,固体A中一定有Mg,
2 2 4 2 2
一定没有Na CO ;滤液D加入NaOH溶液生成蓝色沉淀E,蓝色沉淀一定为Cu(OH) ,则滤
2 3 2
液 D 中一定有 CuO 与稀 H SO 反应生成的 CuSO ,还含有 Mg 与稀 H SO 反应生成的
2 4 4 2 4
MgSO ;沉淀 C 中加入稀 HNO ,沉淀不溶解,该沉淀一定为 BaSO ,故固体 A 中可能有
4 3 4
BaSO 、BaCl 中的一种或两种,还可能有Na SO ,则固体A的组成可能有以下6种:①Mg、
4 2 2 4
CuO、BaCl ,②Mg、CuO、BaSO ,③Mg、CuO、BaCl 、BaSO ,④Mg、CuO、Na SO 、
2 4 2 4 2 4
BaCl ,⑤Mg、CuO、Na SO 、BaSO ,⑥Mg、CuO、Na SO 、BaSO 、BaCl 。
2 2 4 4 2 4 4 2
11.答案 解:设参加反应的Na CO 的质量为x,CaCl 的质量为y,生成NaCl的质量为z
2 3 2
CaCl +Na CO CaCO ↓+2NaCl(1分)
2 2 3 3
111 106 100 117
y x 5 g z
(1) = x=5.3 g(1分)
碳酸钠溶液的溶质质量分数 ×100%=10.6%(1分)
(2) = y=5.55 g(1分)
= z=5.85 g(1分)
所得溶液中NaCl的质量(50 g+50 g-5 g)×10%=9.5 g(1分)
原固体混合物的质量9.5 g-5.85 g+5.55 g=9.2 g(1分)
答:(略)
解析 (1)Na CO 溶液加入CaCl 和NaCl的混合溶液中,Na CO 溶液只与CaCl 反应,当加
2 3 2 2 3 2
入50 g的Na CO 溶液时,恰好把CaCl 反应完,生成5 g CaCO 白色沉淀,根据化学方程式
2 3 2 3
可计算出50 g Na CO 溶液中溶质Na CO 的质量,进而可求出Na CO 溶液中溶质的质量
2 3 2 3 2 3
分数。
(2)原固体混合物由CaCl 和NaCl组成,CaCl 的质量可通过生成沉淀的质量计算得出,NaCl
2 2
的质量等于反应后溶液中NaCl的总质量减去反应生成的NaCl的质量,即可求出原固体混合
物的质量。